Дегидратационный шок при инфекционных заболеваниях
Обновлено: 18.04.2024
Этапы регидратационной терапии. Расчет регидратационной терапии
Водно-электролитная терапия, проводимая внутривенно вводимыми полиионными кристаллоидными растворами, как и оральная, осуществляется в два этапа: I — восстановление потерь жидкости и солей, отмечавшихся до начала инфузионной терапии; II — коррекция продолжающихся водно-электролитных потерь.
Приступая к I этапу регидратационной терапии, прежде всего следует определить объем жидкости, который целесообразно ввести больному. С этой целью выявляется степень обезвоживания. При I степени обезвоживания потеря жидкости не превышает 3 % массы тела, при II — потеря жидкости составляет 4—6 %, при III — 7—9 %, при IV (декомпенсированное обезвоживание) — ю % и более. Определив степень обезвоживания по клиническим и лабораторным показателям с помощью таблицы и выяснив массу тела больного (со слов пациента или путем взвешивания в отделении) можно вычислить величину потери жидкости. Важность правильной оценки степени обезвоживания заключается в том, что она определяет метод и темпы регидратационной терапии — ключевого звена в лечении больных с острыми кишечными инфекциями.
Примеры расчетов: 1) у больного обезвоживание III степени, масса тела — 80 кг. При данной степени обезвоживания потеря жидкости в среднем составляет 8 % массы тела, или 6400 мл. Это значит, что объем внутривенно вводимых жидкостей на I этапе лечения будет равен 6400 мл; 2) у больного обезвоживание IV степени, масса тела 90 кг. При данной степени обезвоживания потери жидкости составляют не менее 10 % массы тела, или 9 л. Объем вводимых внутривенно растворов на I этапе лечения срставит 9 л.
В целом при холере и нехолерных острых кишечных инфекциях сходство клинических проявлений обусловлено общими патофизиологическими механизмами — остро развивающимся изотоническим обезвоживанием, дефицитом электролитов, гемоконцентрацией, метаболическим ацидозом, гемодинамической недостаточностью с функциональной перегрузкой правых отделов сердца и легочной гипертензией, тромбогеморрагическим синдромом, гипоксией, недостаточностью внешнего дыхания и функции почек. Такое сходство определяет целесообразность синдромального подхода при проведении регидратационной терапии.
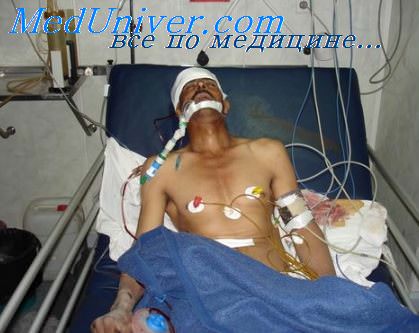
Водно-солевая терапия при холере с обезвоживанием II—IV степени должна обязательно включать I этап регидратации, при котором оптимальная скорость внутривенной инфузии составляет 70—120 мл в минуту, а объем вводимой жидкости определяется дефицитом массы тела в соответствии с указанной степенью обезвоживания.
Водно-солевая терапия при острых кишечных инфекциях нехолерной этиологии должна проводиться при тяжелом течении болезни со скоростью 70—90 мл/мин в объеме 60—120 мл/кг, а при среднетяжелом течении — со скоростью 60—80 мл/мин, в объеме 55—75 мл/кг.
Опыт показывает, что регидратация больных с острыми кишечными инфекциями, проведенная в объеме менее 60 мл/кг и со скоростью менее 50 мл/мин, наряду с более длительным сохранением симптомов обезвоживания и интоксикации не способствует восстановлению возникших изменений и у больных развиваются вторичные нарушения гомеостаза. Указанные нарушения являются фактором повторного прогрессирования обезвоживания, гемодинамических нарушений, микроциркуляторных расстройств, изменений гемостаза, развития осложнений, в том числе острой почечной и коронарной недостаточности, тромбоза мезентериальных сосудов.
Завершение I этапа регидратационной терапии происходит при восстановлении гемодинамики, прекращении рвоты и нормализации диуреза. У значительной части больных возникает необходимость в проведении II этапа регидратации. Лечение осуществляется с помощью тех же полиионных кристаллоидных растворов с учетом продолжающихся потерь жидкости с испражнениями, рвотными массами и мочой за определенный период (при больших потерях их объем определяют каждые 2 ч, при малых — каждые 4—6 ч). Скорость введения жидкости на II этапе лечения может колебаться в зависимости от объема продолжающихся потерь и обычно составляет 40—60 мл/мин. Баланс потерь и количество выделяемой жидкости каждые 2 ч фиксируются в истории болезни. Такой учет потерь жидкости (с рвотой, калом, мочой) и объема вводимых растворов является принципиально важным в лечении больных с острыми кишечными инфекциями, если проводится регидратационная терапия.
Внутривенное введение жидкости прекращается после исчезновения рвоты, отчетливой стабилизации гемодинамики и восстановления выделительной функции почек. Важным критерием для решения вопроса о прекращении внутривенных инфузий является значительное преобладание количества выделенной мочи над количеством испражнений в течение последних 4 ч.
Общий объем внутривенно вводимой жидкости в тяжелых и затяжных случаях может достигать несколько десятков литров.
Часто после I этапа лечения с помощью внутривенной инфузий II этап осуществляется методом оральной регидратации. При этом принципы лечения и объем вводимой жидкости остаются неизменными.
Безусловно, необходима коррекция метаболического ацидоза, который у части больных бывает декомпенсированным.
Коррекция метаболического ацидоза у большинства больных осуществляется полиионными кристаллоидными растворами. Наиболее эффективны растворы "Трисоль" и "Квартасоль". Когда же это не удается осуществить коррекция метаболического ацидоза проводится с помощью 4 % раствора натрия гидрокарбоната или раствора трисамина.
Дегидратационный шок – патологическое состояние, развивающееся вследствие возникновения катастрофического несоответствия объема циркулирующей крови (ОЦК) емкости сосудистого русла из-за нарастающей дегидратации и деминерализации в результате рвоты и диареи.
Дегидратационный шок является разновидностью гиповолемического шока и характеризуется выраженными изменениями водно-электролитного баланса, кислотно-основного равновесия, сердечной деятельности, сосудистого и мышечного тонуса и функции почек, а также развитием нарастающей гипоксии.
Причины развития дегидратационного шока
Этиологические факторы различных типов дегидратации

Факторы, обусловливающие возникновение гиповолемии при холере
Классический холерный токсин
активирует аденилатциклазу, обусловливающую
цАМФ-зависимое фосфорилирование белков, что увеличивает транспорт натрия и хлоридов
в просвет кишки, за которыми выходит вода
Токсин Zonula occludens
повышает проницаемость слизистой оболочки тонкой кишки за счет изменения структуры плотных межклеточных контактов
Дополнительный холерный токсин
встраивается в апикальную мембрану энтероцита и начинает выполнять транспортные функции – перенос ионов хлора, а за ними воды в просвет кишки
Эндогенные индукторы диареи
связывается с серотониновыми рецепторами нейронов интрамуральной нервной дуги, которая контролирует водно-эдектролитную интестинальную секрецию
Вазоактивный интестинальный пептид (ВИП)
взаимодействует с ВИП-рецепторами базолатеральной мембраны эпителиоцитов,
тем самым индуцируя водно-электролитную секрецию, и ингибирует интестинальную абсорбцию электролитов
стимулируют синтез цАМФ
Ig-зависимая реакция гиперчувствительности
Патогенез дегидратационного шока
Потеря изотонической жидкости и электролитов

Уменьшение объема плазмы и интерстициальной жидкости

Повышение вязкости крови


Нарушение микроциркуляции
Шок – остро развивающийся, угрожающий жизни патологический процесс, характеризующийся прогрессирующим снижением тканевой перфузии, тяжелыми нарушениями деятельности ЦНС, кровообращения, дыхания и обмена веществ.
Виды шока
Гиповолемический
Кардиогенный
Перераспределительный
- травматический шок;
- геморрагический шок;
2. Потеря плазмы:
3. Потеря жидкости:
1. Острый инфаркт миокарда (истинный кардиогенный).
2. Нарушения сердечного ритма.
3. Тромбоэмболия легочной артерии (обструкционный)
4. Тампонада сердца
1. Анафилактический шок.
2. Септический шок (инфекционно-токсический).
3. Спинальный шок (нейрогенный)
Основные симптомы шока:
- Холодная, бледная, влажная кожа.
- Симптом “белого пятна” – замедленное наполнение капилляров кожи после их сдавления (более 2 секунд).
- Тахикардия.
- Вначале возбуждение, потом заторможенность.
- Снижение систолического артериального давления менее 100 мм рт.ст.
- Уменьшение пульсового давления менее 20 мм рт.ст.
- Снижение диуреза (олиго- или анурия).
Шок любой этиологии характеризуется фазностью развития расстройств периферического кровообращения, однако, последовательность развития фаз прослеживается не всегда. Проводимая терапия зависит от вида шока и основной причины.
В детском возрасте наиболее часто оказание неотложной помощи врачом-педиатром требуется при перераспределительном шоке (инфекционно-токсическом и анафилактическом).
Инфекционно-токсический шок
Инфекционно-токсический шок может возникнуть у больных с менингококковой инфекцией, особенно часто при молниеносной форме менингококцемии, стафилококковом и грибковом сепсисах, а также при других острых инфекционных заболеваниях с тяжелым течением (дифтерия, скарлатина и другие).
Стадии инфекционно-токсического шока:
I (компенсированная) - гипертермия, сознание сохранено, возможно возбуждение или беспокойство ребенка, тахипноэ, тахикардия, АД нормальное.
На догоспитальном этапе объем неотложной помощи больным ИТШ зависит от причины и стадии шока и направлен на борьбу с жизнеугрожающими синдромами – гипертермическим, судорожным и т.д.
Неотложная помощь:
- при гипертермии - ввести 50% раствор метамизола (анальгина) в комбинации с 1% раствором дифенгидрамина (димедрола) в дозе 0,1-0,15 мл на год жизни в/мышечно;
- при выраженном психомоторном возбуждении и судорогах - ввести 0,5% раствор диазепама в разовой дозе 0,1 мл/кг массы тела (не более 2 мл на введение) в/венно или в/мышечно;
- при ИТШ, развившемся на фоне менингококкемии, ввести хлорамфеникол (левомицетина сукцинат) в дозе 30 мг/кг в/мышечно;
- при отеке головного мозга - ввести 1% раствор фуросемида (лазикса) из расчета 1-2 мг/кг в/ мышечно (только при систолическом АД не ниже 100 мм рт.ст.) или 25% р-р магния сульфата 1,0 мл на год жизни;
- при ИТШIстадии - ввести преднизолон из расчета 3-5 мг/кг в/мышечно;
- при ИТШ II стадии:
- кислородотерапия;
- обеспечить доступ к вене;
- ввести преднизолон 5-10 мг/кг массы тела в/венно, при отсутствии эффекта и невозможности транспортировки больного в течение 30-40 мин. - повторное введение преднизолона в тех же дозах;
- в/венное введение кристаллоидных (0,9% р-р натрия хлорида) и коллоидных растворов (реополиглюкин, полиглюкин, 5% альбумин) до нормализации АД (до 15 мл/кг массы тела);
- при ИТШ III стадии:
- кислородотерапия;
- обеспечить доступ к вене (желательно к двум);
- ввести преднизолон 10 мг/кг массы тела в/венно, при отсутствии эффекта - повторное введение в тех же дозах через 30-40 мин;
- ввести в/в струйно 0,9% раствор хлорида натрия в разовой дозе 20 мл/кг до появления отчетливого пульса на лучевой артерии, при отсутствии эффекта повторное болюсное введение в прежней дозе через15-20 мин.
Госпитализация - в ОИТР стационара.
Менингококковая инфекция
Менингококцемия – одна из форм генерализованной менингококковой инфекции, характеризующаяся острым началом с подъемом температуры тела до фебрильных цифр, общей интоксикацией, кожными геморрагическими высыпаниями, развитием инфекционно-токсического шока.
Клинические проявления менингококковой инфекции:
Угрожающими синдромами при генерализованных формах менингококковой инфекции являются:
- инфекционно-токсический шок развивается при сверхостром течении менингококцемии. Как правило, симптомы шока возникают одновременно либо после появления геморрагической сыпи. Однако ИТШ может возникать и без высыпаний, поэтому всем детям с инфекционным токсикозом необходимо проводить измерение АД;
- отек головного мозга с дислокацией ствола. Проявляется нарушением сознания, гипертермей, выраженными менингеальными симптомами (в терминальной стадии болезни иногда их отсутствие), судорожным синдромом и необычными изменениями со стороны гемодинамики в виде относительной брадикардии и наклонности к повышению артериального давления. В терминальной стадии отека мозга - абсолютная брадикардия и аритмия дыхания.
Неотложная помощь:
- Обеспечить проходимость верхних дыхательных путей, оксигенотерапия.
- Ввести хлорамфеникол (левомицетина сукцинат) в дозе 25-30 мг/кг в/мышечно.
- В/венное (при невозможности - в/мышечное) введение глюкокортикоидов в пересчете на преднизолон 5-10 мг/кг или дексаметазона 0,6-0,7 мг/кг массы; при отсутствии эффекта и невозможности транспортировки больного необходимо провести повторное введение гормонов в тех же дозах (при ИТШIIIстадии доза кортикостероидов может увеличиваться в 2-5 раз).
- Ввести 50% раствор метамизола (анальгина) 0,1 мл/год жизни в/мышечно + 1% р-р дифенгидрамина (димедрола) в дозе 0,1-0,15 мл на год жизни в/мышечно (или 2 % р-р супрастина – 2 мг/кг в/мышечно ) + 2% р-ра папаверина 0,1 мл/год жизни ).
- При возбуждении, судорожном синдроме - 0,5% р-р диазепама в разовой дозе 0,1 мл/кг массы тела (не более 2 мл на введение) в/венно или в/мышечно, при не купирующихся судорогах повторно в той же дозе.
- При выраженном менингеальном синдроме – в/мышечное введение 1% раствор фуросемида из расчета 1-2 мг/кг в/мышечно или 25% р-р магния сульфата 1,0 мл/год жизни в/мышечно.
Вызов реанимационной бригады на себя. Госпитализация в ОИТР ближайшего стационара. При подозрении на менингококковую инфекцию показана госпитализация.
Кишечный токсикоз с эксикозом - патологическое состояние, являющееся осложнением острых кишечных инфекций (ОКИ) вследствие воздействия на организм токсических продуктов и значительных потерь жидкости, что приводит к нарушению гемодинамики, водно-электролитного обмена, кислотно-основного резерва, развитию вторичной эндогенной интоксикации.
В патогенезе токсикоза с эксикозом ведущую роль играет дегидратация, которая приводит к дефициту объема вне- (а в тяжелых случаях и внутри-) клеточной жидкости и объема циркулирующей крови. Степень эксикоза (дегидратации) обуславливает выбор терапевтической тактики и влияет на прогноз.
Критерии инфекционно-токсического шока. Степени ИТШ
В нашем понимании, существуют следующие клинико-патогенетические критерии ИТШ:
• генерализация инфекции и выраженность интоксикационного синдрома;
• нарушения КОС и водно-электролитного обмена;
• гипоксия;
• гемодинамические расстройства;
• расстройства микроциркуляции и капилляротрофи-ческая недостаточность;
• ДВС-синдром;
• развитие "шоковых органов" и полиорганной недостаточности.
"Шоковые органы" могут обнаруживаться не только у больных с ИТШ и, следовательно, не являются эквивалентом шока. По мнению В.А.Гологорского и соавт. (1988), дисфункция органов при шоке определяется их резервами и исходной способностью противостоять метаболическим расстройствам. По данным Г.А Рябова (1994), метаболические расстройства у больных с ИТШ сводятся к: 1) гипергликемии; 2) повышению уровня свободных жирных кислот; 3) катаболизму белков с повышением синтеза мочевины; 4) повышению внутриклеточной осмолярности.
В последние годы клинико-патогенетические различия в процессах, обусловленных грамположительной и грамотрицательной флорой, вызывающих ИТШ, рядом исследователей во внимание не принимаются и рассматриваются как архаизм.
Шоковые состояния с патофизиологических позиции целесообразно разделить на 2 категории ; 1) со сниженным сердечным выбросом и нарушенной общей периферической тканевой перфузией; 2) с нормальным или повышенным сердечным выбросом и нарушенным распределением периферического кровотока.
По мнению Г.А.Рябова (1994), для шока характерна фазовость патологического процесса. По данным В.Л.Айзенберга (1993, 1995), при ИТШ у детей, страдающих острыми кишечными инфекциями, целесообразно различать две стадии: компенсированную и декомпенсированную. Первая стадия характеризуется патологической гипердинамией с увеличением сердечного индекса в значительных пределах, тахикардией и натриемией при нормальной концентрации калия, вторая — гиподинамическим вариантом нарушения кровообращения со снижением сердечного индекса, гипонатриемией и гипокалиемией.
Для ИТШ у больных с острыми кишечными инфекциями характерно развитие ДВС-синдрома. При этом четко определяется фазовость коагулопатии. В одних случаях в клинической картине доминируют проявления тромбоза, в других — развитие геморрагического синдрома. При этом тромбоз чаще регистрируется в области мезентериальных, реже в области коронарных и мозговых сосудов. Кровоизлияния выявляются чаще на коже, слизистой оболочке кишки, в паренхиме легких, веществе и оболочках головного мозга.
Помимо непосредственного действия бактериальной флоры на сердечно-сосудистую систему и клеточный метаболизм, патогенез ИТШ определяется действием эндотоксина и липополисахаридных компонентов оболочек грамотрицательных бактерий. Последние активируют систему комплемента и освобождают биологически активные амины.
Таким образом, вначале развивается гипердинамическая фаза шока, и в связи с постепенным перемещением внутрисосудистой жидкости в интерстициальное и внутриклеточное пространства возникает гиподинамическая Фаза шока. С этого момента ИТШ более сходен с гиповолемическим.
Патогенез шока представлен ниже в виде схемы. Практически важным является разграничение шока У больных с острыми кишечными инфекциями по степени тяжести.
Шок I степени (компенсированный): тяжелое состояние больного, двигательное беспокойство, периодическое возбуждение, состояние тревоги, повышенная температура тела, бледность кожных покровов, цианоз губ и ногтевых фаланг. Характерны умеренная одышка, тахикардия и нормальное АД. Диурез умеренно снижен. Рвота и жидкий стул несколько раз в сутки. В крови — метаболический ацидоз, чаще компенсированный, гипокалиемия.
Шок II степени (субкомпенсированный): тяжелое состояние больного, заторможенность. Температура тела повышенная или нормальная. Бледность кожного покрова, цианоз. Тахикардия и глухость тонов сердца.
Пульс слабого наполнения, АД 85/60—60/20 мм рт.ст. рвота и жидкий стул под себя несколько раз в сутки. Олигурия. Декомпенсированный метаболический ацидоз, гипоксемия, гипокалиемия.
Шок III степени (декомпенсированный): крайне тяжелое состояние, сознание сохранено, возможны бред и галлюцинации, при отеке головного мозга — судороги и потеря сознания. Гипотермия и тотальный ацидоз. Тоны сердца глухие, пульс нитевидный или не определяется. дД 50/0 мм рт.ст. Анурия. Стул жидкий под себя несколько раз в сутки, но может отсутствовать. Рвота чаще всего сохраняется. В крови — декомпенсированный метаболический ацидоз, гипоксемия.
Мы наблюдали 36 762 больных с острыми кишечными инфекциями, в том числе 31 555 больных (85,8 %) с пищевыми токсикоинфекциями; 3455 (9,4 %) — сальмонеллезами, 1752 больных (4,8 %) —острой дизентерией, среди них мужчин 6,9%, женщин —93,1 %. Больных в возрасте до 20 лет — 10,9 %, 21 года — 40 лет — 26,5 %, 41 года — 60 лет — 26,9 %, 61 года — 70 лет — 25,6 %, старше 71 года— 10,1 %. Тяжелое течение отмечалось у 2,9% больных, средней тяжести — у 90,6 %, легкое — у 6,5 % больных. ИТШ развился у 57 больных (0,15 %): с выраженным обезвоживанием — у 24, а без выраженного обезвоживания с токсикозом — у 33 больных.
При пищевых токсикоинфекциях ИТШ наблюдался у 32 больных (0,1 %), в том числе с выраженным обезвоживанием — у 15, без выраженного обезвоживания — у 17 больных. При сальмонеллезе ИТШ развился у 21 больного (0,6 %), в том числе с выраженным обезвоживанием — у 9, без выраженного — у 12. При острой дизентерии ИТШ наблюдался у 4 больных (0,2 %) и всегда протекал без выраженного обезвоживания. Таким образом, ИТШ чаще всего возникал у больных сальмонеллезом.
Информация на сайте подлежит консультации лечащим врачом и не заменяет очной консультации с ним.
См. подробнее в пользовательском соглашении.
Дегидратационный шок – патологическое состояние, развивающееся вследствие возникновения катастрофического несоответствия объема циркулирующей крови (ОЦК) емкости сосудистого русла из-за нарастающей дегидратации и деминерализации в результате рвоты и диареи.
Дегидратационный шок является разновидностью гиповолемического шока и характеризуется выраженными изменениями водно-электролитного баланса, кислотно-основного равновесия, сердечной деятельности, сосудистого и мышечного тонуса и функции почек, а также развитием нарастающей гипоксии.
Причины развития дегидратационного шока
Этиологические факторы различных типов дегидратации

Факторы, обусловливающие возникновение гиповолемии при холере
Классический холерный токсин
активирует аденилатциклазу, обусловливающую
цАМФ-зависимое фосфорилирование белков, что увеличивает транспорт натрия и хлоридов
в просвет кишки, за которыми выходит вода
Токсин Zonula occludens
повышает проницаемость слизистой оболочки тонкой кишки за счет изменения структуры плотных межклеточных контактов
Дополнительный холерный токсин
встраивается в апикальную мембрану энтероцита и начинает выполнять транспортные функции – перенос ионов хлора, а за ними воды в просвет кишки
Эндогенные индукторы диареи
связывается с серотониновыми рецепторами нейронов интрамуральной нервной дуги, которая контролирует водно-эдектролитную интестинальную секрецию
Вазоактивный интестинальный пептид (ВИП)
взаимодействует с ВИП-рецепторами базолатеральной мембраны эпителиоцитов,
тем самым индуцируя водно-электролитную секрецию, и ингибирует интестинальную абсорбцию электролитов
стимулируют синтез цАМФ
Ig-зависимая реакция гиперчувствительности
Патогенез дегидратационного шока
Потеря изотонической жидкости и электролитов

Уменьшение объема плазмы и интерстициальной жидкости

Повышение вязкости крови


Нарушение микроциркуляции
Читайте также:

