Деринат при опоясывающем лишае
Обновлено: 14.05.2024
Что такое герпес
Чаще всего проблемы вызывает вирус простого герпеса 1 и 2 типов. 1 тип - это герпес на губах, глазах и полости рта. 2 тип - это генитальный герпес и герпес беременных и новорожденных.
Как понять, что это именно герпес?
Возьмем к примеру самый банальный герпес на губах. Первое что чувствует человек это зуд в области губ (часто может и не заметить в течении дня). В этот же день появляется краснота и красные пятна. На следующие сутки в месте покраснения появляется пузырек и отек. Спустя 3-5 дней образуется корочка на месте лопнувших пузырьков. Через 7-9 дней все симптомы проходят. Также в стадию с пузырьками может подняться температура до 37,5—38,5°С и появиться боль.
Но для достоверного подтверждения диагноза необходим анализ крови на наличие специфической реакции организма на вирус (IgM) он будет говорить о том, что на момент сдачи крови у вас протекает острый период болезни.
При генитальном герпесе, также берут на исследование выделения из половых путей и уретры. Обязательна консультация специалиста (дерматовенеролога).
Как можно заразиться
Заражение происходит через слизистые:
- Губ
- Рта
- Носа
- Гениталии
- Глаза
- Через кожу при контакте с биологическими жидкостями (слюна, моча, сперма, слезы, выделения из носа, непосредственно жидкость из герпесного пузырька).
То есть чаще всего заражение происходит при несоблюдении гигиены и защиты при половом акте. Так же при расчесывании уже появившихся пузырьков происходит занос на новые участки кожи и слизистых.
Отдельный путь заражения от матери к плоду, на данный момент является обязательным обследование на ВПГ-1,2 у планирующих беременность и беременных женщин.
Инфекция поражает нервную систему и опасна своими последствиями для организма.
Как себя вести при герпесе
- Не трогать высыпания руками, если задели, то сразу же мыть руки.
- Использовать отдельную посуду, косметику, полотенце.
- Воздержаться от поцелуев и половых контактов.
- Наносить лечебные гели и мази ватной палочкой, а не руками.

Для достоверного подтверждения диагноза необходимо сдать анализ.
Препараты
Рассмотрим подробно группы препаратов для лечения
Данная группа препаратов воздействуют непосредственно на причину, сам вирус. Курс и схему приема назначает врач после комплексного обследования.
Переносимость препаратов достаточно хорошая, противопоказаны при беременности и кормлении грудью. Так же осторожно и под контролем врача применение у лиц с почечной и печеночной недостаточностью. Детям дозу определяет педиатр исходя из расчета по весу.
2. Препараты интерферона:
При заболевании герпесной инфекцией происходит снижение выработки собственного интерферона альфа , а это означает снижение защитных сил организма от вируса.
Противопоказаний у данной группы практически нет. Она является основным способом лечения такой уязвимой группы как беременные и кормящие женщины.
Используют для стимуляции выработки собственного интерферона и избежания усугубления течения и распространения инфекции. Переносится достаточно хорошо. Противопоказания у каждого препарата определенный возраст указанный в инструкции.
- Местные антибактериальные и противовирусные препараты:
Данные препараты применяются при герпетических поражения слизистой рта, обладают антибактериальным, противовирусным действием, а также снимают воспаление и обезболивают.
- Мазь Зовиракс и Зовиракс Дуо актив
- Виферон
- Инфагель
- Панавир
Обладают местным противовирусным действием, Зовиракс Дуо Актив в сочетании с гормоном гидрокортизоном дает быстрое снятие воспаления и соответственно боли, также не дает образоваться новым пузырькам. Но так как в составе гормональная составляющая, очень внимательно необходимо прочитать инструкцию. Только с 12 лет. Перед применением любых мазей и гелей необходимо очистить кожу от косметики и загрязнений.
- Иммуномодуляторы под контролем иммунограммы:
- Полиоксидоний
Только под контролем иммунолога.
Снимают боль, воспаление и так же при необходимости температуру.
Помогают избежать отечности.
- Витаминные комплексы:
- Витрум
- Компливит
- Селен
- Цинк
- Витамин С
Также отдельно можно выделить вакцину против герпеса. Показана она взрослым, которые болеют герпесом более 3 раз в год и высоким титром антител, пожилым лицам, ВИЧ-инфицированным. Также детям которые не переболели ветрянкой.
Лечение беременных женщин выбирается в зависимости от срока беременности, строго акушером-гинекологом и зависит от степени тяжести течения!
Герпес-является комплексной проблемой. Причиной повторяющегося или впервые возникшего герпеса является снижение иммунитета, гормональные изменения.
Главной профилактикой является поддержание работы иммунитета:
Федеральные клинические рекомендации по ведению больных генитальным герпесом- Москва 2015; Клинические рекомендации простой герпес у взрослых-2014 год;
Опоясывающий герпес или, как его еще называют, опоясывающий лишай, – одно из самых непонятных для обычного человека заболеваний вирусной природы. Его часто путают с другими видами лишая (розовый, стригущий, чешуйчатый), к которым приводят грибковые инфекции кожи, а также различные аутоиммунные процессы.
В случае опоясывающего лишая к появлению клинических симптомов и высыпаниям на коже приводит вирус герпеса 3 типа, Varicella zoster. Этот вирус также вызывает хорошо известную ветряную оспу. Выходит, что один и тот же вирус вызывает сразу два заболевания? Но как такое может быть? Давайте разбираться!
Когда организм человека встречается с вирусом Varicella zoster впервые, чаще всего развивается ветряная оспа. И обычно это происходит в детском возрасте, хотя в редких случаях заболевание может развиться и у взрослого человека. О том, что происходит, когда вирус дает о себе знать во второй раз, читайте далее. Также узнаете о том, как подобрать лекарство от опоясывающего герпеса.
Итак, мы выяснили, что опоясывающий герпес (опоясывающий лишай, герпес зостер, herpes zoster, ОГ) является вирусным заболеванием кожи и нервных тканей, которое возникает как результат реактивации вируса герпеса III типа (Human herpesvirus) подсемейства Alphaherpesviridae, семейства Herpesviridae. Встречается он примерно у 15 человек из 100 и проявляется у каждого четвертого взрослого из тех, кто ранее переболел ветряной оспой.
Важно помнить, что опоясывающий герпес у взрослых требует иного подхода к терапии: лекарства, которые педиатр рекомендует детям от ветряной оспы, не помогут. Терапию для лечения опоясывающего герпеса должен назначать врач-терапевт или врач-дерматолог после осмотра пациента и с учетом его анамнеза.
Как вирус герпеса зостер проникает в организм и как проявляется
Главные факторы, которые могут спровоцировать появление ОГ:
- возрастные изменения в организме – согласно данным статистики, это заболевание чаще всего встречается среди людей старше 50 лет;
- аутоиммунные и онкологические заболевания, в том числе сахарный диабет, лучевая и химиотерапия, состояние после тяжелых травм;
- беременность и вследствие этого повышенная нагрузка на организм;
- ВИЧ-инфекция – с ОГ сталкиваются почти 25% ВИЧ-инфицированных лиц, что в восемь раз превышает средний показатель заболеваемости пациентов среднего и старшего возраста;
- трансплантация органов, когда необходим прием иммуносупрессивных препаратов, предназначенных для искусственного угнетения иммунитета в целях предупреждения отторжения органа; i
- рецидив хронических заболеваний, затрагивающих сердечно-сосудистую систему, почки, печень и легкие;
- длительное лечение антибиотиками, цитостатиками, глюкокортикостероидами;
- частые стрессы, отсутствие достаточного отдыха, переутомление, переохлаждение или перегрев.
Опоясывающий герпес: симптомы и лечение
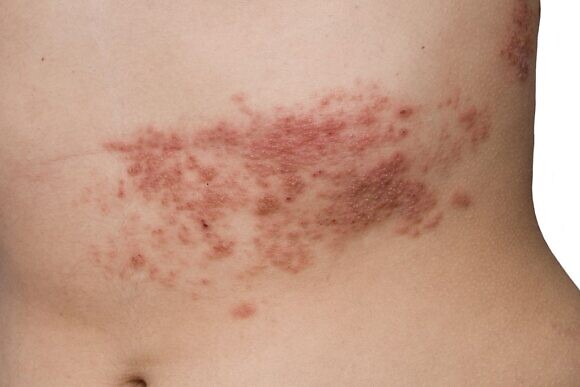
В отличие от ветряной оспы, при опоясывающем лишае не наблюдается резких вспышек заболеваемости, как в детских коллективах, также отсутствует и сезонная зависимость. Хотя некоторые ученые отмечают, что ОГ чаще встречается в теплое время года и поздней осенью. Тяжесть течения заболевания зависит от возраста. Дети, которые тоже болеют опоясывающим лишаем после перенесенной ветрянки, а также лица молодого возраста обычно переносят болезнь более благоприятно, чем пожилые люди.
Среди основных симптомов опоясывающего герпеса – кожные проявления и неврологические расстройства. Большинство инфицированных сталкивается с общеинфекционными клиническими признаками, которые проявляются в виде повышения температуры тела, головной и мышечной боли, тошноты, слабости, увеличения регионарных лимфатических узлов. Интенсивность проявления этих симптомов варьируется у каждого пациента. Продолжительность начального периода составляет примерно четыре-пять дней.
Клинические признаки ОГ могут быть похожими на плеврит, невралгию тройничного нерва и даже синдром острого живота, например, аппендицит, который требует немедленной помощи специалиста. Поэтому при общем плохом самочувствии и появлении на коже высыпаний любой природы необходимо сразу же обратиться к врачу.
В месте высыпаний перед появлением сыпи могут ощущаться легкие зуд и жжение. Потом на коже появляются розовые пятна круглой или неправильной формы, которые не склонны к слиянию, они отечные и немного приподнятые над поверхностью кожи. Затем на коже появляются везикулы с жидким серозным содержимым. Через несколько дней пузырьки подсыхают, на их месте появляются серозные корки, которые со временем отпадают и на их месте появляются пигментированные участки кожи. При правильном лечении снижается температура тела и исчезают симптомы общей интоксикации организма.
Как лечить опоясывающий герпес геморрагической, гангренозной абортивной и других форм
Кроме наиболее часто встречаемой формы опоясывающего лишая, о которой идет речь выше, также встречаются другие, которые могут выглядеть не совсем обычно и даже пугающе для неподготовленного человека. Например, при геморрагической форме везикулы заполняются кровянистым содержимым, поэтому на теле сыпь выглядит как пятна темно-коричневого цвета. Иногда везикулы не заживают бесследно, по разным причинам их дно некротизируется, после чего на коже остаются рубцы. Абортивная форма ОГ характеризуется появлением практически незаметных визуально папул (пузырьки не образуются), поэтому пациент не обращается к врачу.
При буллезной форме пузырьки на коже достаточно крупные, они могут сливаться в единый конгломерат с неровными краями. Их повреждение может приводить к инфицированию ранки, после чего может начаться гнойный процесс. В самых тяжелых случаях везикулы сливаются в обширные области, которые со временем некротизируются. В этом случае речь идет уже о гангренозной форме. Чаще эта форма развивается у пожилых людей, у лиц с язвенной болезнью и сахарным диабетом. В данном случае пациенту может быть необходима госпитализация и комплексное лечение.
Одна из главных целей лечения опоясывающего герпеса у взрослых, которые не требуют лечения в стационаре, – максимально быстрое купирование клинических симптомов заболевания (высыпаний и субъективных ощущений). Это обусловлено тем, что в зависимости от длительности цитопатического (приводящего к дегенеративным изменениям в клеточных структурах) действия вируса варицелла-зостер на клетки пораженных нервов значительно возрастает риск развития постгерпетической невралгии и других осложнений.
Возможные последствия отказа от лечения опоясывающего герпеса
ОГ приводит к многочисленным поражениям периферического и центрального отделов нервной системы. Чаще всего встречается такое осложнение, как постгерпетическая невралгия. Она проявляется в виде сильных болей, которые сохраняются или появляются через несколько недель и даже месяцев после появления первых высыпаний. Человек ощущает жгучие, резкие и приступообразные боли в области расположения сыпи. Этот симптом особенно усиливается по ночам. Особенно часто с таким осложнением болезни сталкиваются пожилые люди. Также встречаются случаи, когда вирус опоясывающего герпеса поражает брюшные мышцы и мочевой пузырь.
Кроме того, ОГ может поразить нервы, которые находятся в черепе. Подобное поражение может затронуть мозговые оболочки, что приводит к массе проблем со здоровьем. Одна из них – это поражение офтальмической ветви тройничного нерва, что неблагоприятно влияет на зрение.
Исследователи утверждают, что персистирующая, т.е. упорно протекающая и периодически вспыхивающая герпетическая инфекция может привести иммунную защиту организма к так называемой клеточной депрессии. Без поддержки в виде правильного лечения и возможности полноценно защитить себя организм может столкнуться с самыми разными осложнениями со стороны функционирования различных органов и систем.
Диагностика и правильное лечение опоясывающего герпеса у взрослых
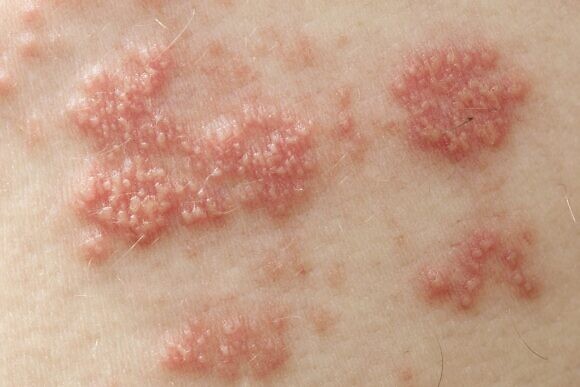
При подозрении на опоясывающий герпес необходимо обращаться к врачу-терапевту для осмотра и начала курса лечения. Также может понадобиться помочь врача-дерматолога и врача-иммунолога, а при выраженном болевом синдроме – врача-невролога.
Диагностика ОГ является преимущественно клинической, для подтверждения диагноза может потребоваться проведение лабораторных исследований. Также необходимо дифференцировать это заболевание от других похожих. Для этой цели широко применяется метод полимеразной цепной реакции (ПЦР), иммуноферментный анализ (ИФА) и иммунофлуоресцентный анализ, которые обычно не оставляют сомнений в диагнозе. Кроме того, могут потребоваться результаты общего и биохимического анализа крови, общего анализа мочи. При развитии генерализованной формы врач может дополнительно назначить анализ на ВИЧ.
Лечение ОГ чаще всего проводят амбулаторно, оно должно быть комплексным и включать как этиологические, так и патогенетические средства. Эффективность терапии во многом зависит от сроков начала лечения: чем раньше вы обратитесь к врачу и начнете лечение, тем быстрее наступит выздоровление и тем ниже будут риски развития осложнений.
Опоясывающий герпес: лечение народными средствами
Не стоит слепо доверять советам родственников и знакомых, не имеющих медицинского образования. Любые настойки, ванночки, растирания и аппликации на кожу могут принести вред, усилить зуд и расширить область появления высыпаний. Ведь во многих случаях народная медицина может не только не помочь избавиться от заболевания, но и быть небезопасной.
Опоясывающий герпес: лечение, препараты и методы терапии
В настоящее время все методы лекарственного лечения и профилактики ОГ можно объединить в три основные группы, куда входят химиотерапия (прием ациклических нуклеозидов), иммунотерапия и комбинация этих двух групп, где пациент одновременно принимает химио- и иммуномодулирующие препараты.
Также применяют витамины B1, В6 и В12, аскорбиновую кислоту, рутин и при необходимости – антигистаминные препараты. При сильном болевом симптоме пациенту показан прием НПВП и анальгетиков.
Для лечения опоясывающего герпеса на теле пациентам необходима иммунокоррекция. Поэтому в этом случае будет уместной стратегия сочетания ациклических нуклеозидов и препаратов интерферона альфа-2b, которая признана врачами обоснованной и наиболее эффективной, что отражено в клинических и методических рекомендациях.
Противовирусный препарат ВИФЕРОН в лечении опоясывающего герпеса
Одним из препаратов, применяемых для лечения герпеса, является ВИФЕРОН – противовирусный и иммуномодулирующий препарат, который обладает рядом уникальных фармакологических свойств.
ВИФЕРОН в своем составе сочетает рекомбинантный интерферон а-2b и комплекс антиоксидантов (витамины Е и С), в присутствии которых возрастает специфическая противовирусная активность главного действующего вещества, а также усиливается его иммуномодулирующее действие, что позволяет повысить эффективность собственного иммунного ответа организма на патогенные микроорганизмы. ii
Препарат в форме свечей удобен в применении и для взрослых: он не перегружает желудочно-кишечный тракт (ЖКТ), что особенно актуально для людей, страдающих гастритом и другими заболеваниями ЖКТ, а также для тех, кто принимает большое количество таблетированных препаратов (пожилые пациенты и лица с сопутствующими заболеваниями).
Для лечения герпесвирусных инфекций у взрослых применяются свечи в дозировке 1 000 000 МЕ, у беременных женщин – 500 000 МЕ с последующими поддерживающими курсами с использованием дозировки 150 000 МЕ.

ВИФЕРОН Гель в виде полоски не более 0,5 см наносят на предварительно подсушенную пораженную поверхность 3-5 раз в день в течение 5-6 дней.
Сочетание ациклических нуклеозидов с препаратом ВИФЕРОН гарантированно сокращает сроки купирования ОГ и позволяет значительно снизить риск развития осложнений за счет комбинированного противовирусного действия (нарушение размножения вируса варицелла-зостер и препятствие прямому токсическому воздействию). iii
Как применять мазь при опоясывающем герпесе
Любая противогерпетическая мазь при опоясывающем герпесе может применяться в качестве дополнения к системной терапии, но не вместо нее.
Национальное научное общество инфекционистов и Московский научно-практический центр дерматовенерологии и косметологии рекомендуют включать препарат ВИФЕРОН в комплексную терапию опоясывающего герпеса у детей и взрослых, включая беременных женщин. iv
Справочно-информационный материал
Автор статьи
Врач общей практики
iii Халдин А.А., Васильев А.Н., Д.В. Баскаков Д.В. Виферон: опыт применения в дерматологической практике // Ремедиум Приволжье. – январь-февраль 2009. – С.20-22.
iv Потекаев Н.Н., Халдин А.А., Жукова О.В., Дмитриев Г.А. Методические рекомендации. Простой герпес. Опоясывающий герпес. Цитомегаловирусная инфекция. Московский научно-практический центр дерматовенерологии и косметологии ДЗМ. – 2019. – 32 с.
Вирус герпеса третьего типа varicella zoster (VZV) вызывает два клинически обособленных заболевания - ветряную оспу и опоясывающий герпес (Баринский И.Ф. и др., 1986; Haanpaa M., 2001). Оба заболевания, прежде всего, характеризуются везикулярной сыпью. Первичная инфекция манифестирует в форме ветряной оспы (ветрянки), а реактивация латентного VZV обусловливает появление локализованных высыпаний - опоясывающего лишая (Хахалин Н.Н., 2002). Мысль о связи между ветрянкой оспой и опоясывающим лишаем впервые была высказана в 1888 венским врачом Яношом Бокеем (von Bokay J., 1909).
Эпизод ветряной оспы в детстве способствует формированию специфической клеточной и гуморальной иммунной защиты. Считается, что рецидив инфекции у таких пациентов может развиться только на фоне недостаточности иммунной защиты, вследствие снижения активности специфических натуральных киллеров, Т-киллеров и системы интерферонов (Fleming D.M. et al., 2004). После первичной инфекции излюбленным местом персистенции VZV являются ганглий тройничного нерва и спинномозговые ганглии чувствительных корешков грудного отдела спинного мозга, где VZV находится в латентном состоянии. В течение этого времени вирус не размножается и не проявляет патогенных свойств. По-видимому, время латентного состояния вируса определяется уровнем специфических антител к VZV. Снижение их количества ведет к реактивации вируса, вирусной репликации (размножению), что на клиническом уровне и проявляется в виде опоясывающего лишая (Arvin A., 2005). Данный вывод подтверждается высокой корреляцией между вероятностью возникновения опоясывающего лишая у людей пожилого возраста и возрастным ослаблением активности клеточного звена иммунитета (Gilden et al., 2000)., На это также указывают данные, свидетельствующие о более высокой заболеваемости опоясывающим герпесом среди лиц, инфицированных вирусом иммунодефицита человека (Gilson I.H. et al., 1989), однако точные механизмы, лежащие в основе перехода вируса из латентного состояния в активное неизвестны.
В случае реактивации VZV ганглии чувствительных нервов становятся местами репликации вируса, именно в них обнаруживаются наиболее выраженные дегенеративные повреждения нейронов (Zerboni L. et al., 2005; Reichelt M. et al., 2008). В результате развивается ганглионит, сопровождаемый распространением инфекции вниз по нервным аксонам к коже. Каким образом происходит транспортировка вируса в поврежденных аксонах неизвестно. Инфекция также может распространяться центрально, приводя к воспалению оболочек в области передних и задних рогов спинного мозга (Gray F. et al. 1994). Отдельные патолого-анатомические наблюдения также свидетельствуют о наличии воспалительных изменений и в контралатеральных спинномозговых ганглиях (Miller S. E. et al., 1997), отмечается снижение количества нейронов и наличие воспалительных инфильтратов в ганглиях, периферических нервах, и спинномозговых корешках (Gowrishankar K. et al., 2007). В некоторых случаях отмечается выраженные некротические изменения в спинномозговых ганглиях. Большинство изменений в периферическом нерве протекает по типу Валлериановской дегенерации, имеющей место, как в толстых, так и в тонких волокнах. (Denny-Brown et al., 1944).
Острая VZV инфекция клинически характеризуется стадией продрома и стадией везикулярных высыпаний (Arvin A., 2005).
Сыпь обычно локализуется в одном или нескольких смежных дерматомах и сопровождается развитием острой невропатической боли. У 50% больных сыпь встречается на туловище, у 20% - на голове, у 15% - на руках, и у 15% - на ногах (Arani R.B. et al., 2001).
Клинический диагноз опоясывающего лишая в типичных случаях достаточно прост. Однако иногда требуется проведение лабораторной диагностики с целью идентификации вируса. Наиболее быстрым и высокочувствительным методом является полимеразная цепная реакция.
В остром периоде болезни или после него возможно развитие осложнений, захватывающих различные системы организма. Наиболее серьезными считаются неврологические осложнения. В структуре неврологических расстройств ведущее место занимает поражение периферической нервной системы. При данном заболевании воспалительный процесс затрагивает региональные, чувствительные ганглии с развитием ганглиолитов. Наличие у больных корешковых болей, парастезий, сегментарных нарушений чувствительности отмечается практически у каждого больного (Stankus S. et al., 2000; Thyregod H. G. et al., 2007). Болевой синдром имеет выраженную вегетативную окраску в виде жгучих, приступообразных, резких болей, усиливающихся в ночное время. В головном мозге при опоясывающем герпесе могут быть обнаружены явления отека, выраженная диффузная инфильтрация подпаутинного пространства, геморрагии в белом веществе, базальных ганглиях (Sissoko D. et al., 1998). Следует заметить, что осложнения со стороны головного и спинного мозга в настоящее время встречаются редко. В случаях развития VZV-инфекции в области тройничного нерва часто наблюдаются осложнения со стороны глаз - кератит, ирит, ретинит, офтальмит. Ранее, при отсутствии специфической противогерпетической терапии, к частым осложнениям VZV-инфекции относились пневмонии, энцефалиты или гепатиты, иногда приводившие к летальному исходу.
Вместе с тем, из всех перечисленных осложнений VZV инфекции самым распространенным считается постгерпетическая невралгия (Dworkin R.H., Portenoy R.K., 1996).
Различают острую герпетическую невралгию (в течение 30 дней после начала заболевания) и постгерпетическую невралгию (Choo P. et al.,1997). К ПГН относят упорные боли в областях, затронутых герпесной инфекцией после заживления кожи (Dworkin R. et al. 2003). Наиболее хорошо установленными факторами риска для ПГН являются пожилой возраст, большая распространенность высыпаний на коже и выраженная боль перед везикулярной сыпью (Desmond R.A. et al., 2002; Fleming D.M. et al., 2004). Все эти факторы находятся во взаимосвязи, поэтому пациенты 50 лет и старше в большинстве случаев испытывают тяжелую, нестерпимую боль и значительные кожные высыпания, что гораздо чаще приводит к развитию ПГН. У пациентов со всеми этими факторами риск развития ПГН превышает 50-75 % (Gnann J., Whitley R. 2002; Jung B.F., 2004). Постгерпетическая невралгия может развиться в любом возрасте, однако для нее характерна прямая корреляция частоты встречаемости и длительности ПГН с возрастом. Более 50% всех пациентов с ПГН - старше 60 лет, 75% больных с указанной патологией приходится на возрастную группу старше 75 лет (Nurmikko T.J., 2001). Половина всех пациентов с ПГН старше 60 лет испытывает постоянную боль более 6 месяцев, в то время как в возрастной группе 30-50 лет ПГН более 6 месяцевь наблюдается у 10% больных (Whitley R. et al. 1996). В США ежегодно регистрируется 100-200 тыс. новых случаев ПГН (Nurmikko T.J., 2001). Однако, истинная распространенность ПГН не известна, не только потому, что эпидемиологические данные недостаточны, но также из-за отсутствия конценсусса по определению ПГН. Некоторые авторы относят к ПГН боли, возникающие в любой период герпесной инфекции, другие считают, что ПГН - это боль, сохраняющаяся спустя 3 месяца после заживления кожи. В первом случае определения ПГН ее распространенность составляет 8%, во втором - 4,5% (Choo P. et al. 1997). Постоянную боль в течение 1 мес после сыпи испытывают до 15% пациентов и около 4% пациентов от общего количества перенесших опоясывающий лишай отмечают сохранение боли в течение года (Lancaster T. et al. 1995).
Классическое проспективное исследование, проведенное Hope-Simpson (1975), продемонстрировало, что из 321 пациента с опоясывающим лишаем 10 % имеют выраженную боль спустя 3 месяца после острой герпетической инфекции, а 4 % - и через 12 месяцев. Подобные результаты были получены и в других проспективных исследованиях (Helgason S. et al. 1996; 2000; Scott F.T. et al., 2006), в которых также было показано, что наибольший риск пролонгации болевого синдрома после перенесенного опоясывающего лишая имеют пациенты в возрасте около 60 лет.
Постгерпетическая невралгия занимает третье место по частоте встречаемости среди различных типов невропатической боли и уступает только болям в нижней части спины и диабетической невропатии (Montero H.J. et al., 2005; Breivik H. et al, 2006; Torrance N. et al., 2006).
Локализация болевого синдрома практически всегда соответствует зоне кожных высыпаний. Интенсивность болевого синдрома как правило высокая. Кроме глубоких ноющих и стреляющих болей очень характерны поверхностные жгучие боли и наличие стимулозависимых болей - динамической гипералгезии и аллодинии (Baron R., 2004).
При клиническом осмотре в зоне болей выявляются нарушения поверхностной чувствительности. Качество боли в острый период опоясывающего лишая и при ПГН различно. Вместе с тем, несмотря на разный выбор дескрипторов из МакГилловского болевого вопросника, пациенты с опоясывающим лишаем и ПГН для описания своих болевых ощущений выбирают похожие по смыслу слова, например, горячая и жгучая боль или пронзающая и простреливающая боль (Bennett M., 2001).
Схожие проявления наблюдаются и при описании вызванной боли пациентами с опоясывающим лишаем и ПГН. И те, и другие отмечают наличие схожих типов гипералгезии и аллодинии (Haanpaa M. et al., 2000; Berry J.D., Rowbotham M.C., 2004).
У большинства пациентов боль, связанная с ПГН, уменьшается в течение первого года. Однако у части больных она может сохраняться годами и даже в течение всей оставшейся жизни, причиняя немалые страдания (Cunningham A.L., Dworkin R.H., 2000). Затяжной, тяжелый характер заболевания с длительным, выраженным болевым синдромом способствует формированию расстройств психики (Dworkin R.H., et al., 1992). У таких пациентов выявляются тревожно-депрессивные расстройства, когнитивные нарушения - снижение активного внимания, памяти, затруднения осмысления происходящего, отмечается некритичность, нетерпеливость, неряшливость, страх боли, неуверенность в завтрашнем дне, отмечается снижение социальной активности (Haythornthwaite J.A. et al., 2003). ПГН оказывает значительное отрицательное влияние на качество жизни и функциональный статус пациентов особенно пожилого возраста (Lydick E. et al., 1995). У пациентов с ПГН отмечается хроническая усталость, снижение массы тела, физической активности, нарушения сна (Morin C.M., Gibson D., Wade J., 1998).
В основе боли, связанной с ПГН, лежат воспалительные изменения или повреждения ганглиев задних корешков спинного мозга и периферических нервов в пораженных зонах тела. Такие боли относят к невропатическим болям, их выделяют в отдельную самостоятельную группу и определяют как боли, возникающие вследствие первичного повреждения соматосенсорной нервной системы (Treede R.D. et al., 2008).
Патофизиологической основой невропатических болевых синдромов являются нарушения генерации и проведения ноцицептивного сигнала в нервных волокнах, а также механизмов контроля возбудимости ноцицептивных нейронов в структурах спинного и головного мозга (Кукушкин М.Л., Хитров Н.К., 2004; Baron R. 2000).
Лечебная тактика при опоясывающем лишае включает два основных направления: противовирусная терапия и купирование невропатической боли, как в острый период заболевания, так и в стадии постгерпетической невралгии. Результаты нескольких рандомизированных контролируемых испытаний свидетельствуют о том, что раннее начало лечения простого герпеса может предотвратить развитие постгерпетической невралгии или способствовать ее скорейшему разрешению (Исаков В.А. и др., 2004; Helgason S. et al., 1996; Jackson J.L. et al., 1997 ; Volmink J. et al., 1996).
Наиболее широкое применение нашли такие специфические противогерпетические препараты, как ацикловир, фамцикловир и валацикловир, которые, являясь нуклеозидными аналогами, блокируют вирусную репликацию (Романцев М.Г., 1996; Beutner K. et al., 1995; Bruxelle J., 1995). Важно, что противовирусное лечение проявляет наивысшую активность, если назначено в течение 72 ч от начала герпетических высыпаний (Johnson R., 2001; Johnson R., Dworkin R.H., 2003). В ряде исследований доказана высокая эффективность ацикловира в уменьшении тяжести, продолжительности острой герпесной инфекции и профилактике ПГН, особенно при его раннем назначении. Оценка эффективности фамцикловира также продемонстрировала уменьшение времени до разрешения сыпи (Dworkin R.H. et al., 1998). В сравнительном исследовании ацикловира и валацикловира показана эквивалентная эффективность в сокращении продолжительности невропатической ПГН (Beutner K. et al. 1995). В другом клиническом испытании установлена терапевтическая эквивалентность фамцикловира и валацикловира для неосложненного герпеса (Tyring S. et al. 2000). Возможно также сочетанное использование противовирусной терапии и глюкокортикостероидов (Whitley R. et al. 1999). Выявлено, что такая комбинация эффективнее монотерапии противовирусными препаратами, особенно для лечения острой боли и коррекции различных аспектов качества жизни пациентов. Комбинация ацикловир+преднизолон значительно быстрее купирует острую невралгию и возвращает пациента к обычной жизнедеятельности, но существенно не влияет на течение ПГН, то есть она наиболее показана в остром периоде в старших возрастных группах для терапии острого болевого синдрома. Доказано, что хотя преднизолон является иммуносупрессором, его использование не увеличивает частоты развития ПГН и в этом смысле его действие сравнимо с влиянием плацебо, то есть данная комбинация может быть спокойно использована в старших возрастных группах. Для некупируемых тяжелых случаев ПГН некоторые исследователи рекомендуют интратекальное введение метилпреднизолона (Kost R., Straus S., 1996).
В настоящее время в США делается акцент на профилактику герпетической инфекции. С 1995 г. в США проводится всеобщая вакцинация от ветряной оспы, особенно пожилых лиц, и с 1999 г. отмечается резкое снижение заболеваемости (Hambleton S., Gershon A., 2005; Oxman M.N. et al., 2005).
При постгерпетической невралгии препаратами с доказанной эффективностью (класс А - терапия первой линии) являются: пластины с 5% лидокаином, габапентин, прегабалин, трициклические антидепрессанты, трамадол (Attal et al., 2006).
На сегодняшний день эффективность применения пластин с 5% лидокаином (Версатис, Grunenthal Gmbh) убедительно доказана при лечении ПГН. Так, в нескольких рандомизированных клинических исследованиях установлено, что применение пластин с 5% лидокаином статистически достоверно более значимо облегчает проявления болевого синдрома у пациентов с постгерпетической невралгией по сравнению с плацебо (Rowbotham M.C., 1996; Galer B.S., 1999, 2002). На основании полученных данных FDA одобрило применение данного препарата в качестве стартовой терапии у пациентов с постгерпетической невралгией. (Richard L. et al., 2004)
Версатис - это топический анальгетик, который действует непосредственно там, где болит. Он выпускается в виде мягких пластин размером 10х14 см, которые наклеиваются на неповрежденную кожу без признаков воспаления. Медленно высвобождающийся из пластины лидокаин создает более или менее значительную концентрацию лишь в поверхностных слоях кожи, где проходят тонкие волокна, обеспечивающие болевую и температурную чувствительность (Gammaitoni AR, Davis MW. 2002.). Лидокаин лишь в незначительной степени проникает в более глубокие слои кожи, где проходят кровеносные сосуды, поэтому его попадание в системный кровоток сведено к минимуму. У пациентов, использовавших пластины Версатис, не наблюдалось никаких известных системных эффектов лидокаина (влияние на деятельность ЦНС и сердечно-сосудистой системы). Таким образом, важнейшим преимуществом пластин Версатис служит отсутствие системного действия, что гарантирует безопасность лечения. Практически полное отсутствие системного эффекта позволяет назначать Версатис совместно с любыми другими препаратами для лечения нейропатической боли.
Механизм лечебного эффекта препарата Версатис не ограничивается только действием высвобождающегося из них лидокаина. Важное значение имеет также то, что пластина выполняет роль механического барьера, препятствуя раздражению участка кожи с измененной чувствительностью (аллодиния), а также оказывает не него легкое охлаждающее действие (Galer BS, Gammaitoni AR, Oleka N et al., 2004)
Пластины Версатис рекомендуется прикреплять на 12 ч в течение суток, затем следует 12-часовой перерыв. Обезболивающий эффект часто начинается в течение 30 мин после прикрепления пластины, но может проявляться и позже, нарастает в течение 4 ч и затем поддерживается в течение длительного времени, пока пластина прикреплена к коже. Более того, он может сохраняться и после ее удаления.
Для объективной оценки эффективности каждого из препаратов при лечении ПГН используется показатель NNT (number needed to treat - количество больных, которых нужно пролечить, чтобы получить у одного 50% снижение боли). Чем ниже NNT, тем более эффективен препарат при данной патологии. NNT для пластин с 5% лидокаином при лечении пациентов с ПГН составляет 2,0; для амитриптилина - 2,6; габапентина - 4,4; прегабалина - 4,6 (Wu C.L., Raja S.N., 2008); для трамадола - 3,9 (Kalso E., 2006).
Кроме того, в клинической практике очень важен показатель NNH (number needed to harm - число пациентов, которых необходимо пролечить данным препаратом, чтобы получить развитие 1 случая неблагоприятной побочной реакции, приводящей к отмене препарата). Он показывает, насколько безопасен данный препарат при его использовании. Величина NNH для трамадола, рассчитанная по результатам нескольких клинических исследований, составила 9.0, для ТЦА 14.7, для габапентина 26.1. Рассчитать показатель NNH для пластин с 5% лидокаином не представляется возможным в связи благоприятным профилем безопасности препарата, сравнимым с плацебо.
Таким образом, оценка препарата Версатис с позиций доказательной медицины делает его препаратом выбора при лечении постгерпетической невралгии, что подтверждено в соответствующих рекомендациях.
СПИСОК ЛИТЕРАТУРЫ
Одной из нозологических форм, которую вирусы простого герпеса (ВПГ) вызывают у человека, является генитальный герпес. В настоящее время эта форма ВПГ-инфекции считается наиболее распространенной среди всех инфекций, передающихся половым путем.
Одной из нозологических форм, которую вирусы простого герпеса (ВПГ) вызывают у человека, является генитальный герпес. В настоящее время эта форма ВПГ-инфекции считается наиболее распространенной среди всех инфекций, передающихся половым путем. Генитальный герпес вызывают два серотипа вируса простого герпеса: ВПГ-1 и ВПГ-2; причем наиболее часто — ВПГ-2. Согласно данным сероэпидемиологических исследований, инфицирование ВПГ-1 выявляется у 20—40%, а ВПГ-2 — у 50—70% больных генитальным герпесом [2]. Заболевание передается преимущественно при сексуальных контактах от больного генитальным герпесом. Нередко генитальным герпесом заражаются от лиц, не имеющих симптомов заболевания на момент полового контакта или не знающих о том, что они инфицированы [5]. Эта особенность ВПГ, связанная с бессимптомным вирусоносительством, является сложной задачей, от решения которой зависит не только трудоспособность и здоровье, но и личная судьба миллионов потенциальных больных. Имеются сведения о том, что от 60 до 80% новорожденных, у которых развивается неонатальный герпес, рождаются от матерей с бессимптомным носительством [6].
ВПГ-инфекция также может быть причиной нарушения репродуктивной функции, невынашивания беременности, преждевременных родов и патологии плода. Возможно участие ВПГ в развитии онкологических заболеваний гениталий, иммунодефицитных состояний, что позволяет считать герпесвирусные инфекции важной медико-социальной проблемой практического здравоохранения [2].
Лечение хронических, часто рецидивирующих форм ВПГ-инфекции, до настоящего времени представляет определенные трудности, которые объясняются особенностями взаимодействия вируса с макроорганизмом. Жизнедеятельность вирусов герпеса основывается на следующих биологических особенностях:
- все вирусы герпеса являются внутриклеточными паразитами;
- герпесвирусы пожизненно персистируют в аксоноганглиальных структурах центральной и периферической нервной системы;
- в течение жизни человек многократно реинфицируется новыми штаммами вирусов герпеса, при этом возможно одновременное сосуществование нескольких видов и штаммов вирусов [12];
- при нарушении динамического равновесия между иммунным гомеостазом и вирусами последние переходят в активную форму [9].
Согласно данным проведенных исследований только 20% инфицированных ВПГ имеют диагностированный генитальный герпес, 60% — нераспознанный симптоматический генитальный герпес (атипичную форму) и 20% — бессимптомный герпес. В настоящее время только 27% пациентов с диагнозом генитальный герпес получают противовирусную терапию, из них треть — местное лечение [2]. По данным некоторых авторов, около 95% пациентов с клиническими проявлениями генитального герпеса вообще никак не лечатся [11].
Все разнообразие методов терапии и профилактики герпесвирусных инфекций в конечном счете сводится к трем главным подходам:
- химиотерапия;
- иммунотерапия;
- комбинация этих двух методов.
Каждый врач в своей практической работе так или иначе сталкивается с необходимостью решения этой сложной задачи, требующей тонкого индивидуального подхода к каждому пациенту, страдающему ВПГ.
Различают два способа применения противовирусных химиопрепаратов: эпизодическое назначение (при обострениях герпесвирусной инфекции по мере необходимости) и супрессивная или превентивная терапия. В первом случае препарат назначается коротким курсом (5—10 дней), во втором — ежедневный прием препарата в течение нескольких месяцев, а то и лет призван помочь не столько купировать рецидив, сколько предотвратить развитие рецидивов как таковых.
Однако за последние 10 лет увеличилось число исследований, в ходе которых было показано, что изоляты вируса простого герпеса, полученные от пациенток с продолжающимися рецидивами генитального герпеса на фоне длительной супрессивной терапии (более 4 месяцев), обладают резистентностью по отношению к ацикловиру [10].
К тому же ни ацикловир, ни другие противовирусные агенты — фамцикловир, валацикловир — не предотвращают перехода вируса в латентное состояние, возникновения рецидивов после их отмены либо передачи инфекции, а также, к сожалению, не влияют на естественное течение этой инфекции, то есть не гарантируют полного излечения. Поэтому на протяжении последних двух десятилетий ученые изыскивают методы непосредственного воздействия на иммунную систему больных генитальным герпесом с целью стимуляции специфических и неспецифических ее факторов, тем самым способствуя блокаде репродукции вируса [1].
Главной мишенью применения иммуномодулирующих препаратов служат вторичные иммунодефициты, которые проявляются частыми, рецидивирующими, трудно поддающимися лечению инфекционно-воспалительными процессами разной локализации [7]. Именно к таким процессам, требующим иммунокоррекции, и относится хроническая рецидивирующая герпесвирусная инфекция (ХРГВИ), в частности ее генитальная форма. Иммуномодуляторы назначают в комплексной терапии одновременно с противовирусными средствами.
Полиоксидоний — отечественный иммуномодулятор с широким спектром фармакологического действия, не имеющий аналогов в мире [3]. Опыт применения полиоксидония начиная с 1996 года показал его высокую клиническую эффективность в комплексном лечении многих вторичных иммунодефицитных состояний, проявляющихся хроническими, рецидивирующими, вялотекущими инфекционно-воспалительными процессами различной локализации, в том числе в ходе терапии вирусных инфекций [4].
У нас также имеется определенный позитивный опыт применения полиоксидония у пациентов, резистентных к ацикловиру [9].
Мы проводили исследование открытым методом у 50 пациентов с ХРГВИ. В исследование включались пациенты (возрастной интервал от 18 до 65 лет) мужского и женского пола с достоверным диагнозом ХРГВИ. К исследованию не допускались пациенты с гиперчувствительностью к полиоксидонию и беременные женщины. Все пациенты, включенные в исследование, находились в периоде продрома или обострения не более 48 часов от момента появления высыпаний. Обязательным условием для женщин детородного возраста было соблюдение полноценной контрацепции.
На предварительном этапе были сформированы две равнозначные группы пациентов по 25 человек. Пациенты, вошедшие в изучаемые группы, отбирались методом произвольной выборки. Все пациенты предъявляли жалобы на пузырьковые или эрозивные высыпания в области гениталий, зуд, жжение. До лечения всем пациентам проводилась ПЦР-диагностика ВПГ-2 (мазок) — положительный результат получен в 98,3 %.
Возрастной состав пациентов, страдающих генитальной формой герпесвирусной инфекции, в обеих группах был приблизительно одинаковым (43,6 года в первой группе и 38,9 — во второй), в то время как в первой группе средний возраст женщин и мужчин был несколько выше по сравнению со второй группой.
Дозировка и схемы введения. Всем пациентам производилась в/м инъекция препарата утром, под контролем врача. 1-я схема: терапия проводилась в течение 45 дней: пациенты получали по 6 мг полиоксидония в день в/м в течение 5 дней и по 6 мг в/м через день в течение 10 дней. Поддерживающая терапия — по 6 мг в/м 2 раза в неделю в течение месяца. 2-я схема: 6 мг полиоксидония в/м через день в течение 10 дней (всего 5 инъекций на курс).
Обследование проводилось до приема препарата и на 12—14-й день от начала приема препарата, а также на 3—6-й день после окончания приема препарата. Обследование включало общее клиническое, иммунологическое исследования крови, исследование мочи (общее), объективное исследование. Накануне приема препарата собирался подробный анамнез пациента. В состав исследуемых включались совершеннолетние пациенты мужского и женского пола с достоверным диагнозом ХРГВИ.
Объем сопутствующей терапии: все пациенты получали стандартную сопутствующую терапию (ацикловир по 0,2 г 5 раз в день в течение 5 дней и антиоксиданты).
Критериями оценки эффективности являлись следующие параметры: первичные критерии — время достижения полного выздоровления (полная реэпитализация); вторичные критерии — длительность ремиссии и частота рецидивов в ближайшем и отдаленном периоде после терапии полиоксидонием. С целью оценки местных симптомов проводился наружный осмотр места поражения. Оценивалось состояние кожных покровов и слизистых: наличие пузырьков, язвочек, корочек, гиперемии; выяснялись жалобы пациента (зуд, жжение, общее состояние, температура, миалгия).
На фоне лечения полиоксидонием по первой схеме длительность течения рецидива и период реэпителизации сократились в среднем с 6,44 до 3,5 дня, в то время как на фоне стандартной терапии (ацикловир и антиоксиданты) те же показатели изменились с 6,44 до 5,16 дня соответственно. После курса терапии в ближайшем и отдаленном периоде длительность рецидива и быстрота наступления реэпителизации в среднем составляла 4 дня. В процессе лечения препаратом свежие высыпания ни у одного пациента не появились. 76% (19 человек) отметили уменьшение тяжести течения рецидива; остальные — 24% (6 человек) — не отметили разницы по сравнению с периодом до получения препарата. На фоне лечения полиоксидонием по второй схеме длительность течения рецидива и период реэпителизации сократились в среднем с 6,72 до 4,24 дня вместо 6,72 — 5,04 дня соответственно. После лечения полиоксидонием в ближайшем и отдаленном периоде длительность рецидива и быстрота наступления реэпителизации в среднем также составляли 4 дня. 64 % (16 человек) отметили уменьшение тяжести течения рецидива; остальные — 36% (9 человек) — не отметили никаких изменений по сравнению с периодом до получения препарата.
Частота рецидивов у пациентов, получавших полиоксидоний по первой схеме в течение 6 месяцев после лечения, уменьшилась в среднем с 6,5 до 3 раз по сравнению с показателями ближайших шести месяцев перед получением препарата. Длительность ремиссии возросла в среднем с 27 до 75 дней. Максимальная длительность ремиссии увеличилась в среднем с 45 до 180 дней (у отдельных пациентов максимальная ремиссия достигала 190–220 дней, что связано с неравномерностью возникновения рецидивов в исследуемом временном интервале). У 84% пациентов (21 человек) отмечалось ослабление клиники течения рецидива; у 16% (4 человека) после лечения клиника не изменилась. Ухудшения течения заболевания отмечено не было. Частота рецидивов у пациентов, получавших полиоксидоний по второй схеме, в течение 6 месяцев после лечения уменьшилась в среднем с 6 до 3,6 раза по сравнению с показателями ближайших шести месяцев перед получением препарата. Длительность ремиссии возросла в среднем с 33 до 62 дней. Показатель максимальной длительности ремиссии в обеих группах вырос в среднем примерно одинаково — с 45 до 180 дней. У 72% пациентов (18 человек) отмечалось ослабление клиники течения рецидива; у 28% (7 человек) после лечения клиника не изменилась. Как и в первой группе, ухудшений течения заболевания отмечено не было.
Максимальная длительность ремиссии за период наблюдения (2 года) составила 1,9 года в первой группе (у 9 пациентов — 36 %) и 1,1 года во второй группе (у 4 пациентов — 16 %).
До лечения полиоксидонием в обеих группах частота встречаемости и выраженность местных и общих клинических проявлений ХРГВИ была выше по сравнению с теми же показателями на фоне лечения полиоксидонием.
Парентеральное (в/м) введение полиоксидония в соответствии со схемами (см. выше) не вызывало аллергических реакций, не оказывало гепатонефротоксического действия и токсического действия на кроветворные органы; пациенты отмечали хорошую переносимость препарата.
По данным общеклинических и лабораторных методов исследования, побочных эффектов и осложнений при приеме полиоксидония не было.
Использование полиоксидония в комплексной терапии пациентов с генитальной формой хронической рецидивирующей герпесвирусной инфекции является эффективным способом уменьшения клинических проявлений в фазе обострения, сокращения длительности рецидивов и заметного уменьшения их частоты в отдаленном периоде.
Раннее назначение полиоксидония способствует более быстрой реэпителизации и более стойкой ремиссии.
Использование инъекционной формы полиоксидония не вызывает аллергических реакций, а также других побочных эффектов и осложнений.
При соблюдении указанного режима дозирования препарат не обладает нефро- и гепатотоксическим действием.
А. Е. Шульженко, кандидат медицинских наук ГНЦ — Институт иммунологии МЗ РФ, Москва
Если же в наличии иммунодефицит или заболевание носит острый характер, то у такого человека лечение опоясывающего лишая необходимо для того, чтобы:
уменьшить количество высыпаний;
не допустить осложнений и рецидива заболевания;
уменьшить болевой синдром;
Лечение врач назначает по результатам внешнего осмотра и анализов, а также жалоб больного.
Схема лечения опоясывающего лишая включает в себя применение противовирусных, противовоспалительных и противосудорожных препаратов, лекарств для снятия боли (анальгетиков), иммуномодулирующих средств. Необходимо также соблюдать диету и принимать витамины.
Медикаментозную терапию обычно назначают взрослым и пожилым людям с затяжным течением болезни и имеющим риск осложнений. Чем человек старше, тем хуже работает его иммунная система, тем тяжелее течение болезни.
Медикаментозное лечение заключается в использовании противовирусных средств на основе Ацикловира. Этот препарат единственный, который наиболее качественно борется с вирусом герпеса. Его вводят в виде инъекций или принимают внутрь в виде таблеток. Лечение не менее 10 дней.
Дети болеют опоясывающим лишаем редко, но если ребенок заболел, то лечение нужно начинать сразу. Наиболее эффективно лечение опоясывающего лишая у детей Ацикловиром. Чем раньше он назначен, тем меньше продолжительность рецидива, меньше болезненные ощущения. Противовирусная терапия заключается в однократном использовании иммуноглобулина, а также параллельно применяют противовирусные мази, в составе которых есть интерферон или ацикловир. Для того, чтобы уменьшить боль врач может назначить обезболивающие, нестероидные противовоспалительные лекарства, новокаиновые блокады.
Препараты для лечения опоясывающего лишая применяют чаще всего следующие:
противовирусные – Ацикловир, Валацикловир и Фамцикловир;
обезболивающие - Нурофен, Ибупрофен, Найз, Панадол;
противосудорожные – Габапентин, Прегабалин;
Если нет положительной динамики, для лечения боли врач может назначить сильные обезболивающие препараты при опоясывающем лишае, такие как Оксикодон.
Если после выздоровления человек продолжает ощущать боль, необходимо получить консультацию невропатолога.
Постгерпетическая невралгия – осложнение после опоясывающего лишая, которое из-за болезненных ощущение не дает человеку спокойно жить. Для лечения невралгии при опоясывающем лишае врач выписывает антиконвульсанты, пластыри с лидокаином, антидепрессанты, опиоидные анальгетики.
Простые анальгетики и противовоспалительные средства типа Диклофенака не эффективны.
Среди методов лечения опоясывающего лишая можно выделить народные способы, которые предполагают применение мазей, компрессов, втираний. Например, настой репейника или компрессы с отваром бессмертника.
На форумах лечение опоясывающего лишая предлагается очень разное. Но чаще Ацикловир и обезболивающие, а высыпания рекомендуют смазывать зеленкой.
Поэтому для уменьшения и лечения боли при опоясывающем лишае назначают пластыри с лидокаином, капсаициновую мазь. А такие средства, как антиконвульсанты и трициклические антидепрессанты – только по назначению невролога. Сами высыпания на коже обрабатывают растворами анилиновых красителей (водный раствор зелёнки, метиленовой синьки).
И, конечно, при лечении не нужно забывать об укреплении иммунитета: на период болезни желателен постельный режим, обильное теплое питье (в виде морсов, некрепкого чая), поливитамины, а также положительные эмоции. А в последующем – ведение здорового образа жизни, правильное питание, движение и спорт.
Отзывы о лечении опоясывающего лишая:
Читайте также:

