Диагностика микоплазменной инфекции методом ифа
Обновлено: 13.05.2024
Cреди всех видов пневмоний практическому врачу наиболее часто приходится сталкиваться с внебольничной пневмонией. По данным официальной статистики МЗ РФ, заболеваемость внебольничной пневмонией в России среди лиц старше 18 лет составляет
Cреди всех видов пневмоний практическому врачу наиболее часто приходится сталкиваться с внебольничной пневмонией. По данным официальной статистики МЗ РФ, заболеваемость внебольничной пневмонией в России среди лиц старше 18 лет составляет 3,9%. Зарубежные исследователи установили, что заболеваемость внебольничной пневмонией среди лиц молодого и среднего возраста варьирует от 1 до 11,6%, а в старшей возрастной группе достигает 25–44% [11, 13].
Наиболее распространенной причиной внебольничных пневмоний является Streptococcus pneumoniae (30–50%) [5, 11, 13]. Однако все большее значение среди этиологических факторов внебольничной пневмонии в последние годы придается так называемым атипичным микроорганизмам, прежде всего Mycoplasma pneumoniae и Chlamydophila (Chlamidia) pneumoniae, на долю которых приходится от 8 до 25% случаев заболевания [5, 9, 12].
Mycoplasma pneumoniae в структуре внебольничных пневмоний варьирует в пределах 5–50% [7, 11, 13]. Наиболее часто микоплазменная пневмония диагностируется у детей старше 5 лет и лиц молодого возраста (до 25 лет) [3, 4, 7, 10]. Каждые 3–5 лет наблюдаются эпидемиологические подъемы заболеваемости, которые длятся несколько месяцев. Вспышки заболевания характерны для изолированных и полуизолированных групп населения (военнослужащие, студенты, школьники и др., семейные вспышки) [10, 11]. Признается наличие сезонных колебаний, а именно большая распространенность инфекции в осенне-зимний период [6, 10, 13]. Источником инфекции являются как больные, так и носители. Механизм передачи инфекции — аэрогенный, путь передачи — воздушно-капельный. Инкубационный период длится 2–3 нед. Летальность при микоплазменной пневмонии составляет 1,4% [4, 11].
Mycoplasma pneumoniae занимает промежуточное положение между вирусами, бактериями и простейшими и является мембрано-ассоциированным (но может быть и внутриклеточным) анаэробом, имеет трехслойную цитоплазматическую мембрану вместо клеточной стенки, что обусловливает резистентность к различным агентам, подавляющим синтез клеточной стенки, прежде всего к пенициллину и другим β-лактамам [6, 10]. С помощью терминальной структуры микоплазма прикрепляется к клеткам хозяина (эритроцитам, клеткам реснитчатого эпителия бронхов и др.) [6]. Микоплазма также обладает механизмом мимикрии под антигенный состав клетки-хозяина, что способствует длительной персистенции возбудителя и вызывает образование аутоантител и развитие аутоиммунных процессов при микоплазменной инфекции [6, 10]. Предполагается, что именно с формированием аутоантител связано развитие нереспираторных проявлений Mycoplasma pneumoniae-инфекции.
Считается, что от 5 до 15% внебольничных пневмоний вызываются хламидиями, а в период эпидемии эти показатели могут увеличиваться до 25% [4, 5, 10]. Наиболее часто хламидийная пневмония встречается у взрослых, особенно у лиц среднего и пожилого возраста [2, 10]. Описаны эпидемиологические вспышки в изолированных и полуизолированных коллективах, случаи внутрисемейной передачи хламидийной инфекции [7, 10, 13]. Сезонной закономерности распространения этой инфекции не выявлено. Единственным известным резервуаром инфекции является человек. Механизм передачи — аэрогенный, путь передачи — воздушно-капельный. Инкубационный период составляет 2–4 нед. Летальность при хламидийных пневмониях достигает 9,8% [4, 5, 13].
Chlamydophila pneumoniae — это патогенные облигатные внутриклеточные грамотрицательные бактерии, способные к латентному существованию или персистенции в организме хозяина. Характеризуются двухфазным циклом развития, состоящим из чередования функционально и морфологически различных форм — элементарных и ретикулярных телец [2, 4, 7, 10].
Клинические проявления микоплазменнойи хламидийной пневмоний
У 30–40% пациентов, заболевших микоплазменной и/или хламидийной пневмонией, диагноз ставится лишь в конце первой недели болезни; первоначально у них чаще всего ошибочно диагностируются бронхит, трахеит или ОРЗ. Это связано с тем, что, в отличие от бактериальных пневмоний, микоплазменная и хламидийная не имеют отчетливых физикальных и рентгенологических признаков инфильтрации, а культуральная диагностика их невозможна, так как микоплазмы и хламидии являются внутриклеточными возбудителями. Поэтому диагностика микоплазменной и хламидийной пневмоний основывается в первую очередь на выявлении особенностей клинико-рентгенологических данных и подтверждается серологически или с помощью полимеразно-цепной реакции (ПЦР).
Обычно микоплазменная и хламидийная пневмонии начинаются с респираторного синдрома, проявляющегося трахеобронхитом, назофарингитом, ларингитом; протекают с субфебрильной температурой, малопродуктивным, мучительным кашлем, скудными аускультативными данными; характеризуются наличием внелегочных проявлений — кожных, суставных, гематологических, гастроэнтерологических, неврологических и других, а также нетипичными лабораторными показателями — отсутствием лейкоцитоза и нейтрофильного сдвига в периферической крови [3, 4, 7, 10, 11]. Рентгенологические изменения в легких отмечаются усилением легочного рисунка, перибронхиальной или субсегментарной инфильтрацией [5, 10, 11, 13].
Нами были обследованы 60 пациентов: 44 — с микоплазменной пневмонией и 16 — с хламидийной пневмонией. Анализ клинического материала показал, что начало заболевания при микоплазменной и хламидийной пневмониях может быть как острым, так и постепенным (табл. 1). При подостром течении пневмония начинается с поражения верхних дыхательных путей, ухудшения общего состояния и познабливания. Температура тела может быть нормальной или субфебрильной в течение 6–10 дней и лишь потом повышается до 38–39,9°С при микоплазменной и до 38–38,9°С при хламидийной пневмонии. При остром начале симптомы интоксикации появляются уже в первый день и достигают максимума к 3-му дню болезни. У пациентов с постепенным началом болезни интоксикация наиболее выражена на 7–12-й день от начала заболевания. Характерными признаками интоксикации для микоплазменной и хламидийной пневмоний являются умеренная головная боль, миалгия, общая слабость.
Одним из постоянных признаков микоплазменной и хламидийной пневмоний, по нашим данным, является кашель, который возникает одновременно с лихорадкой. У больных микоплазменной пневмонией, в отличие от хламидийной, наблюдается частый, преимущественно непродуктивный, навязчивый, мучительный, приступообразный кашель (см. табл. 1). Наряду с кашлем, у пациентов с хламидийной и микоплазменной пневмониями наблюдаются умеренные признаки поражения верхних дыхательных путей — ринит, фарингит, ларингит. Ринит чаще всего встречается у больных хламидийной пневмонией (75,0 ± 10,8%, р < 0,001) и проявляется заложенностью носа и нарушением носового дыхания, у части больных наблюдаются небольшие либо умеренные слизисто-серозные или слизисто-гнойные выделения из носа. У пациентов же с микоплазменной пневмонией чаще регистрируются явления фарингита и ларингита, проявляющиеся гиперемией ротоглотки и осиплостью голоса (77,3 ± 6,3%, р < 0,05).
Из внелегочных проявлений при микоплазменной пневмонии чаще отмечались миалгия (63,6%), макуло-папулезная сыпь (22,7%), явления желудочно-кишечного дискомфорта (25%), при хламидийной — артралгия (18,8%) и миалгия (31,3%).
Изменения в легких, характерные для уплотнения легочной ткани, при физикальном обследовании пациентов с пневмониями, вызванными атипичными возбудителями (в отличие от больных с бактериальными пневмониями), определялись не всегда. В частности, укорочение перкуторного звука у больных микоплазменной и хламидийной пневмониями наблюдалось в 68,2 и 68,8% случаев соответственно (табл. 1). Этот признак всегда выявлялся у больных с сегментарной, полисегментарной, долевой пневмонией и лишь у 1/3 пациентов с перибронхиальной инфильтрацией. У больных микоплазменной пневмонией над зоной поражения чаще выслушивались ослабленное дыхание (40,9%), сухие и влажные хрипы (47,7%), у пациентов с хламидийной пневмонией — как ослабленное (37,5%), так и бронхиальное дыхание (31,2%) и влажные хрипы (62,5%).
При рентгенографии органов грудной клетки у больных микоплазменной и хламидийной пневмониями выявлялись и типичные пневмонические инфильтрации и интерстициальные изменения. При микоплазменной пневмонии чаще наблюдается двустороннее поражение легких (40,9%) с усилением легочного рисунка (22,7%) и перибронхиальной инфильтрацией (50%), при хламидийной пневмонии — наоборот, чаще полисегментарная инфильтрация (43,7%) и реже интерстициальные изменения (31,3%).
В общем анализе крови у больных микоплазменной и хламидийной пневмониями чаще отмечается нормальное количество лейкоцитов и умеренное повышение СОЭ (в среднем 37,1 ± 1,9 мм/ч).
По нашим наблюдениям, для микоплазменной и хламидийной пневмоний характерно затяжное рецидивирующее течение.
Таким образом, согласно клинико-рентгенологическим данным и с учетом эпидемиологической ситуации, из общего числа пациентов с внебольничными пневмониями можно выделить больных с микоплазменной и/или хламидийной пневмониями. В нашем исследовании таких больных оказалось 80, из них у 60 (75%) в дальнейшем лабораторным методом была установлена микоплазменная или хламидийная этиология пневмонии.
Диагностика микоплазменной и хламидийной пневмоний
Решающая роль в выявлении микоплазменной и хламидийной инфекции отводится лабораторной диагностике.
Также в последнее время для этиологической диагностики микоплазменной и хламидийной инфекции используется ПЦР, основанная на определении ДНК возбудителя с применением метода генных зондов [3, 4, 5, 7, 10]. С помощью ПЦР возможна быстрая диагностика микоплазменной и хламидийной инфекции, но этот метод не позволяет отличить активную инфекцию от персистирующей [1, 7, 10, 11].
Таким образом, для достоверной этиологической идентификации микоплазменной и хламидийной пневмоний необходимо проведение серологических тестов в комплексе с методами, основанными на выявлении ДНК микроорганизма.
Лечение микоплазменной и хламидийной пневмоний
Рассмотренные выше микробиологические особенности Mycoplasma pneumoniae и Chlamydophila pneumoniae (главным образом внутриклеточный цикл развития) объясняют неэффективность широко используемых в клинической практике β-лактамных антибиотиков (пенициллины и цефалоспорины) и обусловливают необходимость применения антимикробных препаратов, способных проникать и накапливаться в пораженных клетках, а также блокировать внутриклеточный синтез белка. Такими свойствами обладают макролиды, фторхинолоны и тетрациклины, которые и являются средствами эрадикационной терапии при Mycoplasma pneumoniae- и Chlamydophila pneumoniae-инфекции [3, 4, 7, 10, 11].
В России макролиды представлены широким спектром препаратов (см. табл. 3). Среди них наиболее активным в отношении Mycoplasma pneumoniae признан азитромицин, имеющий ряд преимуществ перед эритромицином и кларитромицином [4, 10, 11]. В отношении Chlamydophila pneumoniae наиболее активным средством признается кларитромицин [10]. Также эффективны в отношении этих внутриклеточных патогенов и некоторые другие представители макролидов: джозамицин, спирамицин. Старый антимикробный препарат из этой группы — эритромицин — также обладает антимикоплазменной и антихламидийной активностью, но, несомненно, уступает в этом отношении вышеперечисленным антибиотикам, обладая при этом целым рядом побочных эффектов [5, 10, 11].
Значительной активностью по отношению к Mycoplasma pneumoniae и Chlamydophila pneumoniae обладают фторхинолоны — офлоксацин (заноцин, таривид, офло), ципрофлоксацин (ципробай, ципролет, цифран, сифлокс, медоциприн, цифлоксинал), в связи с чем эти антимикробные препараты рассматриваются в качестве альтернативы макролидам при данной инфекции. Высокую активность проявляют новые фторхинолоны — левофлоксацин (таваник) и моксифлоксацин (авелокс). Моксифлоксацин и левофлоксацин успешно подавляют практически любую флору, вызывающую пневмонии.
При лечении микоплазменных и хламидийных пневмоний эффективны и тетрациклины, однако антибиотики этой группы не применяются при беременности, а также печеночной недостаточности. Вероятность проявления побочных эффектов при их применении может быть выше. Из тетрациклинов активны в отношении атипичных микроорганизмов доксициклин и моноциклин (см. табл. 3).
Продолжительность антимикробной терапии неосложненных бактериальных внебольничных пневмоний составляет 5–10 дней. Для лечения микоплазменной и хламидийной пневмоний рекомендуется применять антимикробные средства не менее 2–3 нед [4, 5, 10, 11]. Сокращение сроков лечения чревато развитием рецидива инфекции [4, 10].
При нетяжелом течении микоплазменной и хламидийной пневмоний антимикробные препараты назначаются внутрь в среднетерапевтических дозах. Естественно, при тяжелых пневмониях предпочтение следует отдавать внутривенному применению антибиотика. Эритромицин фосфат назначается до 1–2 г/сут в 2–3 введения (максимально по 1 г каждые 6 ч). Спирамицин используется внутривенно по 1,5 млн МЕ 3 раза в сутки, а кларитромицин — по 250 мг 2 раза в сутки с равными интервалами. Для разведения спирамицина и кларитромицина следует применять 5%-ный раствор глюкозы.
Стоимость внутривенного лечения антибиотиками (в частности, макролидами) весьма высока, поэтому используют ступенчатую терапию, при которой лечение начинается с внутривенного применения антибиотиков, а по достижении клинического эффекта (обычно через 2–3 дня) пациент переводится на пероральную терапию тем же препаратом или другим макролидом. Ступенчатая монотерапия макролидами может проводиться эритромицином, кларитромицином, спирамицином, т. е. препаратами, которые выпускаются в двух формах: для внутривенного введения и для приема внутрь.
Несмотря на большой спектр противомикробных препаратов, эффективное лечение микоплазменных и хламидийных пневмоний представляет до настоящего времени большую проблему [2, 6, 10, 11]. Это связано с тем, что их развитие, как правило, происходит на фоне снижения антиинфекционной резистентности организма, обусловленного угнетением иммунитета [8, 9, 10, 12]. Проведенное нами исследование показателей иммунограммы у пациентов с внебольничной пневмонией микоплазменной и хламидийной этиологии выявило снижение абсолютного числа лимфоцитов, зрелых Т-лимфоцитов (CD3+), Т-хелперов (CD4+), абсолютного числа Т-супрессоров (CD8+), угнетение функциональной активности Т-системы, проявляющееся снижением плотности рецепторов к IL-2 (CD25+), способности к бласттрансформации (CD71+ — лимфоциты) и апоптозу (CD95+), а также активацию гуморального иммунитета, что проявлялось повышением числа В-лимфоцитов (CD20+), уровня IgM и ЦИК.
Микоплазмы и хламидии на разных стадиях развития располагаются как внутриклеточно, так и внеклеточно, что требует для их элиминации участия гуморальных и клеточных механизмов иммунитета [8, 9, 10, 12]. Большинство антимикробных средств действует преимущественно на внеклеточную форму возбудителей. Это приводит к персистенции возбудителей, диссеминации ее в организме, хронизации процесса, формированию осложнений. Применение лишь антимикробных средств означает лишь временное подавление возбудителей, так как на фоне такой терапии происходит сохранение и даже усугубление иммунологических расстройств, что повышает риск рецидива заболеваний [14]. Так, по результатам наших исследований, к концу курса традиционной терапии происходило усугубление Т-клеточной депрессии: снижалось относительное и абсолютное количество Т-лимфоцитов (CD3+), Т-хелперов (CD4+), Т-супрессоров (CD8+) на фоне повышения уровня IgG, ЦИК, фагоцитарного индекса и уменьшения IgA.
В связи с этим хотелось бы подчеркнуть, что терапия микоплазменной и хламидийной пневмоний должна быть комплексной и включать, помимо антимикробных средств, препараты, действие которых направлено на коррекцию иммунного ответа.
С этой целью у больных микоплазменной и хламидийной пневмониями нами применяются иммуномодуляторы (ронколейкин, ликопид, тималин, тимоген).
Включение иммуномодуляторов в комплексное лечение микоплазменных и хламидийных пневмоний позволяет добиться ярко выраженного иммунологического эффекта. Последний сочетается с выраженным клиническим воздействием, проявляющимся сокращением сроков достижения клинико-лабораторной ремиссии в среднем на 3 койко-дня, уменьшением интоксикационных симптомов через 1–3 сут после начала лечения, сокращением лихорадочного периода в 2 раза, четкой положительной рентгенологической динамикой к 12-му дню лечения у 76,7% больных; значительным уменьшением вероятности развития повторных рецидивов и хронизации процесса.
Литература
- Бочкарев Е. Г. Лабораторная диагностика хламидийной инфекции // Иммунопатология, аллергология, инфектология. — 2000. — № 4. — С. 65–72.
- Гранитов В. М. Хламидиозы. — М., 2000. — 48 с.
- Новиков Ю. К. Атипичные пневмонии // Русский медицинский журнал. — 2002. — Т. 10. — № 20. — С. 915–918.
- Ноников В. Е. Диагностика и лечение атипичных пневмоний // CONSILIUM medicum. — 2001. — T. 3. — № 12. — C. 569–574.
- Проект практических рекомендаций МЗ РФ. Внебольничная пневмония у взрослых: диагностика, лечение, профилактика. — М., 2002. — 51 с.
- Прозоровский С. В., Раковская И. В., Вульфович Ю. В. Медицинская микоплазмология. — М.: Медицина, 1995. — 285 с.
- Синопальников А. И. Атипичная пневмония // Русский медицинский журнал. — 2002. — Т. 10. — № 23. — С. 1080–1085.
- Справочник по иммунотерапии для практического врача / Под ред. А. С. Симбирцева. — СПб.: Диалог, 2002. — 480 с.
- Хаитов Р. М., Игнатьева Г. А., Сидорович И. Г. Иммунология. — М.: Медицина, 2000. — 432 с.
- Хаитов Р. Ф., Пальмова Л. Ю. Mycoplasma pneumoniae и Chlamydophila pneumoniae инфекции в пульмонологии: актуальные вопросы клиники, диагностики и лечения. — Казань, 2001. — 64 с.
- Чучалин А. Г., Синопальников А. И, Чернеховская Н. Е. Пневмония. — М.: Экономика и информатика, 2002. — 480 с.
- Boym A. Separation of leucocytes from blood und bone marrow // Scand J Clin. Lad. Jnvest. — 1968. — V. 21. — Suppl. 87. — P. 77–82.
- Guidelines for management of adult community-acquired lower respiratory tract infections. European Study in Community-acquired Pneumonia (ESOCAP) Committee // Eur Resp J. — 1998. — № 11. — Р. 986–991.
- Kawamoto M., Oshita Y., Yoshida H. et al. Two cases hypoxemic acute broncholitis due to Mycoplasma pneumoniae // Kansenshogaku Zasshi. — 2000. — V. 74. — № 3. — P. 259–263.
Г. Г. Мусалимова, кандидат медицинских наук
В. Н. Саперов, доктор медицинских наук, профессор
Т. А. Никонорова
Чувашский ГМУ, г. Чебоксары
Информацию из данного раздела нельзя использовать для самодиагностики и самолечения. В случае боли или иного обострения заболевания диагностические исследования должен назначать только лечащий врач. Для постановки диагноза и правильного назначения лечения следует обращаться к Вашему лечащему врачу.
Синонимы: микоплазменная инфекция, микоплазма, Mycoplasma
Микоплазмоз: причины появления, симптомы, диагностика и способы лечения.
Определение
Микоплазменная инфекция - острое заболевание, вызываемое грамм-отрицательными бактериями, сопровождающееся различными воспалительными поражениями респираторного, урогенитального трактов, суставов, кроветворной и нервной систем. Возбудителями являются микоплазмы из рода Mycoplasma семейства Mycoplasmataceae.
Микоплазмы неустойчивы во внешней среде, разрушаются под действием температуры, замораживания, ультрафиолета, ультразвука, а также современных моющих и дезинфицирующих средств.
Микоплазмы могут существовать не только вне, но и внутри клеток, что позволяет им ускользать от механизмов иммунной защиты организма. В отличие от бактерий, они не имеют клеточной стенки, но могут расти на специальных бесклеточных средах. Подобно вирусам, проходят через бактериальные фильтры. Самостоятельно существовать микоплазмы не могут, так как паразитируют на клетках организма-хозяина, получая из них питательные вещества.
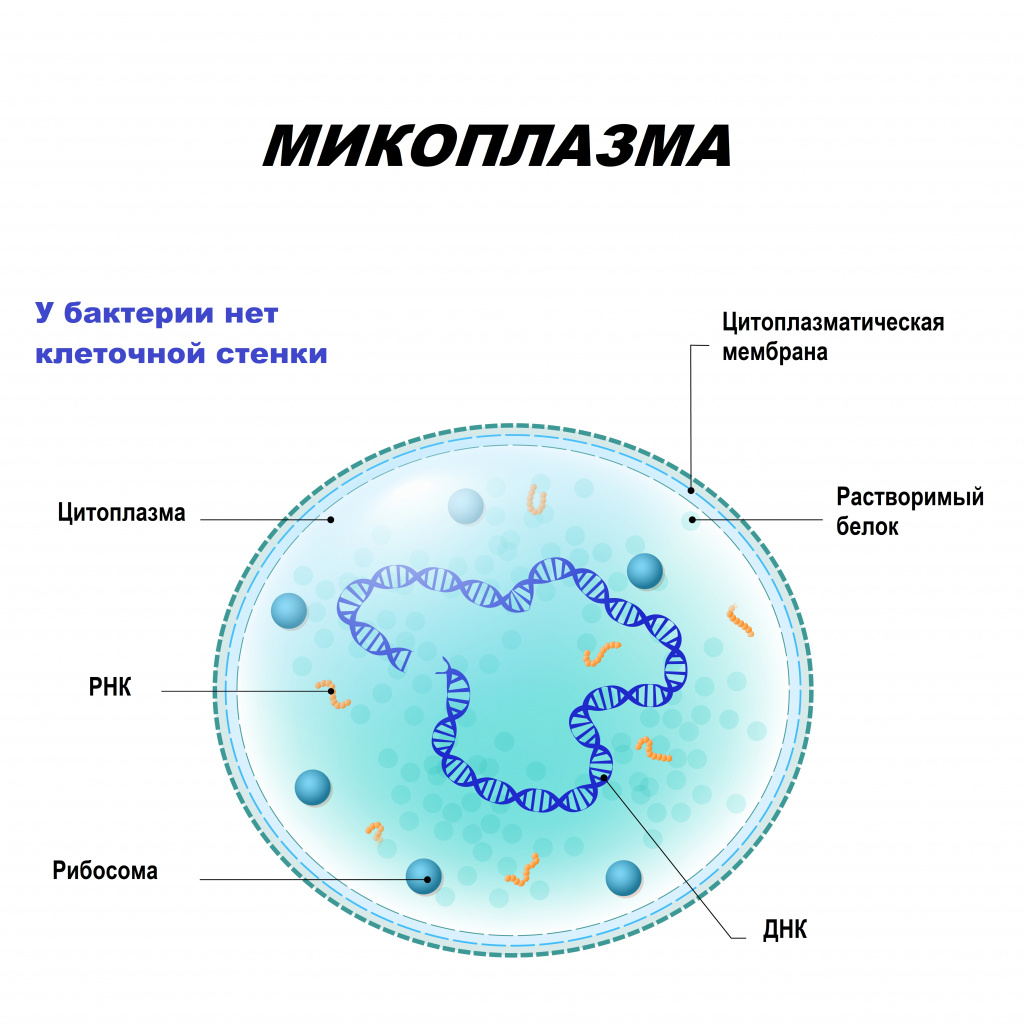
Причины появления микоплазмоза
Источником инфекции является больной человек или носитель микоплазм. Как правило, микоплазмоз протекает скрыто - примерно 40% больных не чувствуют каких-либо явных симптомов, пока стрессовая ситуация или ослабленный иммунитет не спровоцируют активизацию инфекционного процесса, часто приводя к серьезным осложнениям.
Заражение происходит воздушно-капельным путем, половым путем, вертикальным путем (от матери плоду через плаценту) или во время родов.
Респираторный микоплазмоз, вызываемый Mycoplasma pneumoniae и передающийся воздушно-капельным путем, составляет от 7% до 21% в структуре острых респираторных заболеваний, занимая 5-е место среди болезней органов дыхания.
Для передачи возбудителя требуется довольно тесный и длительный контакт, поэтому респираторный микоплазмоз особенно распространен в закрытых коллективах.
Возбудители респираторного микоплазмоза проникают в организм через дыхательные пути, фиксируются на поверхности эпителия слизистой оболочки трахеи и бронхов. Они вырабатывают токсины, которые вызывают стойкий кашель. Иммунологический ответ на этот возбудитель может провоцировать внебольничную пневмонию, тяжелые заболевания верхних дыхательных путей, острый приступ астмы.
Многочисленные исследования показали, что бактерии респираторного микоплазмоза можно выявить практически во всех органах и тканях – печени, почках, сердечной мышце, веществе мозга, перикардиальной и внутрисуставной жидкостях, крови.
Это дает возможность рассматривать микоплазменную инфекцию как генерализованный процесс с диссеминацией возбудителя и развитием полиорганных поражений.

Mycoplasma genitalium – патогенный микроорганизм, способный вызывать уретрит у лиц обоего пола, цервицит и воспалительные заболевания органов малого таза у женщин. Урогенитальный микоплазмоз распространен среди взрослых и передается половым путем.
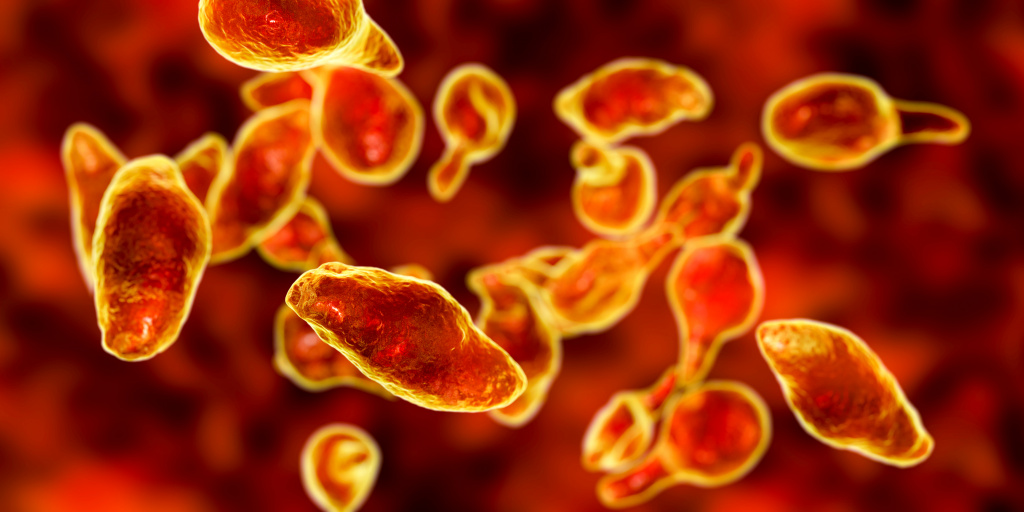
Классификация заболевания
Выделяют три основные формы заболевания: респираторный микоплазмоз, урогенитальный микоплазмоз, врожденный микоплазмоз.
Классификация по МКБ 10
А63.8 Другие уточненные заболевания, передаваемые преимущественно половым путем:
- А63.8 + N34.1 Уретрит, вызванный M. genitalium
- А63.8 + N72 Цервицит, вызванный M. genitalium
- А63.8 + N70 Сальпингоофорит, вызванный M. genitalium
- А63.8 + N71 Эндометрит, вызванный M. genitalium
- А63.8 + N45 Орхит и эпидидимит, вызванный M. genitalium
- А63.8 + N48.1 Баланопостит, вызванный M. genitalium
J20.0 Острый бронхит, вызванный M. pneumoniae
B96.0 M. рneumoniae как причина болезней, классифицированных в других рубриках.
Симптомы микоплазмоза
Для урогенитального микоплазмоза характерные клинические особенности не выявлены. Описаны микоплазменные уретриты, простатиты, вагиниты, кольпиты, цервициты, острые и хронические пиелонефриты. Чаще всего микоплазмоз протекает в виде обычной мочеполовой инфекции. Появляется зуд и жжение при мочеиспускании, болезненность в нижней части живота, а также необильные слизистые выделения с неприятным запахом.
Более тяжелым случаем является респираторный микоплазмоз, так как возможно поражение абсолютно любого отдела дыхательного тракта.
Заболевание может протекать в двух клинических формах:
- микоплазмоз верхних дыхательных путей (неосложненный респираторный микоплазмоз),
- микоплазменная пневмония.
Начало заболевания чаще постепенное, реже острое. У пациентов выявляют першение в горле, ринит, непродуктивный постоянный кашель, субфебрильную лихорадку, недомогание, чувство ломоты, головную боль, охриплость, сыпь и редко буллезное воспаление барабанной перепонки. Катаральный синдром характеризуется явлениями фарингита, трахеита или бронхита (часто с обструктивным компонентом). Нередко у детей отмечается коклюшеподобный кашель, сопровождающийся болями в груди, животе, нередко заканчивающийся рвотой.
Диагностика микоплазмоза
Основным направлением в диагностике микоплазмоза является выделение возбудителя, так как клиническая картина заболевания не позволяет достоверно установить диагноз.
Лабораторная диагностика респираторного микоплазмоза основана на прямых методах выявления микоплазм и серологических реакциях определения специфических антител.
Проводят серологическое исследование на M. pneumoniae (на специфические антитела IgM, IgG и IgA). Антитела класса IgM являются индикатором первичного инфицирования.
Индикатор текущей или имевшей место в прошлом инфекции Mycoplasma pneumoniae. Mycoplasma pneumoniae – распространённый этиологический агент атипичной пневмонии у детей и взрослых. Удельный вес микоплазмозов среди острых респираторных заболеваний, протекающих с преимущественным поражение.
ИФА или иммуноферментный анализ представляет собой лабораторное исследование крови.
Оно определяет в крови активности специфических антител (иммуноглобулинов) к определенным возбудителям инфекционных заболеваний.
При помощи такого исследования проводится диагностика микоплазмоза.
Инфекции, передающейся половым путем, возбудителем которой является микоплазма хоминис (Mycoplasma hominis).
Какие антитела к микоплазме хоминис определяются при помощи ИФА?
Для выявления факта инфицирования микоплазмой, а также определения стадии течения инфекционного процесса в организме, при помощи ИФА исследуется активность (титр) нескольких классов антител (иммуноглобулины):
- Иммуноглобулины М или IgM – указывают на острую фазу течения инфекционного процесса или недавнее инфицирование.
- Антитела IgG к микоплазме хоминис – ИФА дает возможность определить давность заражения человека.
В случае подозрения наличия микоплазма хоминис, антитела IgG и IgM позволяют врачу подобрать дальнейшую адекватную терапию.
Лечение направлено на уничтожение возбудителя (этиотропное лечение).

Антитела IgG к микоплазме хоминис ИФА
Антитела класса IgG микоплазмоза хоминис - это специфические иммуноглобулины.
Они вырабатываются в организме во время обострения болезни.
Служат маркером микоплазмоза хоминис.
Обнаружить антитела класса IgG можно с помощью иммуноферментного анализа.
Для этого делают забор венозной крови.
Микоплазма хоминис IgG - это один из классов антител микоплазмоза.
Они относятся к условно-патогенной флоре.
Паразитирует микоплазм хоминис преимущественно в клеточных мембранах.
Некоторое количество этого микроорганизма присутствует у человека в мочеполовой системе.
При увеличении их количества начинают развиваться воспалительные процессы.
Микоплазма хоминис IgG является самой распространенной инфекцией, которая передается при половом контакте.
Он может появляться в сочетании с такими заболеваниями как:
- Уреаплазмоз.
- Хламидиоз.
- Гонорея.
- Триппер.
Антитела IgG к микоплазме хоминис обнаружить можно не сразу.
В крови IgG появляется спустя две, четыре недели после незащищенного секса.
Они могут сохраняться длительное время на органах больного.
В случае обнаружения антител класса IgG можно сказать, что у человека заболевание находится в острой стадии развития или перешло в хроническое.
Интерпретация результатов определения IgM к микоплазме хоминис
Активность антител класса IgM повышается в течение 5 дней после инфицирования.
Это антитела острой фазы течения инфекционного процесса урогенитального тракта, вызванного микоплазмой.
Существует несколько вариантов результатов ИФА к этому классу иммуноглобулинов:

- Антитела IgM не выявлены – отсутствие инфицирования микоплазмой.
Или, с момента инфицирования до проведения ИФА прошло менее 5-ти дней (время, в течение которого развивается иммунный ответ организма с повышением титра иммуноглобулина М).
Также отрицательный результат может указывать на длительное течение инфекционного процесса.
При котором с момента инфицирования прошло более нескольких месяцев (период времени, в течение которого происходит снижение активности антител IgM). - Положительный ИФА на IgM – недавнее инфицирование микоплазмой хоминис или обострение хронического течения инфекционного процесса.
Для достоверной интерпретации результатов ИФА обязательно учитывается активность антител к микоплазме класса IgG.

Антитела IgGк микоплазме
хоминис рассказывает
подполковник медицинской службы,
врач Ленкин Сергей Геннадьевич
Содержание данной статьи проверено и подтверждено на соответствие медицинским
стандартам врачем дерматовенерологом, урологом, к.м.н.
Ленкиным Сергеем Геннадьевичем
| Наименование | Срок | Цена |
|---|---|---|
| Антитела к Mycoplasma hominis, IgА | 3 д. | 600.00 руб. |
| Антитела к Mycoplasma hominis, IgM | 3 д. | 600.00 руб. |
| Антитела к Mycoplasma hominis, IgG | 3 д. | 600.00 руб. |
Интерпретация результатов ИФА на IgG к микоплазме хоминис
Активность антител к микоплазме хоминис класса IgG после инфицирования повышается не сразу, а в течение нескольких месяцев.
При этом их титр сохраняется на достаточно высоком уровне длительное время (годами).

Существует несколько вариантов результата анализа на IgG:

- Отрицательный анализ – в крови IgG не определяются. Если при этом также нет антител IgM, то это означает, что в организме нет инфекции микоплазмы хоминис. В случае повышенного титра антител IgM на фоне отсутствия IgG, имеет место недавнее инфицирование микоплазмой. С момента которого прошло меньше нескольких месяцев.
- Положительный результат исследования микоплазма хоминис IgG – указывает на давнее наличие инфекционного процесса. При этом если титр антител IgM высокий, то имеет место обострение патологии. А, отсутствие иммуноглобулинов М указывает на хроническое неактивное течение микоплазмоза.
Микоплазма хоминис, IgG положительный
Если при исследовании наличия инфекционного процесса, вызванного микоплазма хоминис, IgG положительный .
Что это значит для дальнейшего течения и терапии микоплазмоза, определяет врач венеролог на основании всех результатов комплексного обследования.
В процессе лечения обязательно выполняется повторная диагностика, при помощи которой оценивается эффективность терапии.
Микоплазма хоминис IgG положительный. Что это значит?
IgG определяют с помощью иммуноферментного анализа.
IgG положительный, а антитела к IgM отрицательные, в таком случае это свидетельствует о слабом хроническом течении болезни, можно говорить о неактивном хроническом течении заболевания.
Так же это может свидетельствовать о сформировавшемся иммунитете у больного.
В том случае если IgG и IgM положительные, следует немедленно начать прием медикаментозных препаратов.
Увеличение антител микоплазмоза хоминис IgG, говорит про иммунный ответ организма на развитие воспалительных процессов.
Стоит отметить! В случае обнаружения микоплазма хоминис IgG следует исключить занятия сексом.
При незащищенных половых актах может произойти заражение полового партнера.
Может ли быть микоплазма хоминис IgG ложноположительной?
Да, такой результат можно получить.
Ложноположительный результат IgG возможен в следующих случаях:
- Если присутствуют микоплазмы других видов.
- Наличие ВИЧ инфекции.
- При аутоиммунных заболеваниях.
Кроме того, ложноположительный результат возможен в случае нарушения техники выполнения анализа.
Как убрать из крови микоплазма хоминис IgG
Антитила в крови образуются при инфицировании.
Даже после проведенного лечения, следы останутся в крови.
Это значит, что, даже после проведенного курса препаратов IgG в крови будет положительным.
Что делать если мазок отрицательный, а обнаружены микоплазма хоминис IgG
Если у Вас возникли любые сомнения в результатах тестирования, следует проконсультироваться у специалиста.
Результат IgG может говорить не об острой форме, а только о носительстве.
При наличии неприятных симптомов, следует обратиться к врачу, даже если пришел чистый мазок.
Грозит ли беременности микоплазма хоминис IgG?
Микоплазма хоминис, при наличии IgG в крови, может вызвать бесплодие.
Поэтому проводить обследование, и лечение следует во время планирования беременности.
Особую опасность микоплазмоз хоминис, антитела IgG представляет для беременных.
Разберемся в чем же его опасность для мамы и бедующего малыша?
Самой частой причиной является нарушение течения беременности.
Это может быть многоводие или неправильное прикрепление плаценты.
В процессе проникновения микоплазма хоминис в околоплодные оболочки, может произойти самопроизвольное прерывание беременности.
Если заражение произошло на поздних сроках, то возможно появление преждевременных родов.
Плод микоплазмом хоминис не поражается.
Причина этого в том, что он защищен плацентой.
Исключением может стать заражение малыша во время родов.
Происходит это в процессе прохождения ребенка по родовым путям.
Как лечить микоплазма хоминис IgG?
После лабораторного подтверждения микоплазмоза хоминис IgG это не является причиной для начала приема антибиотиков.
Следует сделать забор материала у больного, и проверить на присутствие других инфекций.
Ведь, как известно микоплазмоз хоминис IgG может сопровождать ряд других ИППП.
Проводить такие исследования необходимо.
В дальнейшем от этого будет зависеть схема антибактериального лечения.
Препараты для лечения микоплазмоза могут быть как местного воздействия, так и общего.
Для лечения применяют следующие антибиотики:
- Доксициклин.
- Азитромицин.
- Кларитромицин.
- Джозамицин.
- Ципрофлоксацин.
- Офлоксацин.
Эти препараты применяются перорально.
Внимание! Схему лечения выбирает лечащий врач.
Помимо антибактериальных препаратов местно могут назначаться противогрибковые средства.
Они помогают устранить появление грибковых заболеваний.
Назначают Флюкостат или Дифлюкан.
Для повышения работы иммунной системы назначают Циклоферон, Генферон.
В качестве местного лечения мужчинам делают инстилляции в уретру растворами антисептика мирамистина, хлоргексидина или диоксидина.
Где сдать анализ на микоплазмоз хоминис IgG?
Пройти исследования можно обратившись в частную или государственную лабораторию.
Что бы сдать анализ крови на микоплазмоз хоминис IgG можно обратиться в одну из лабораторий вашего города.
Там вам сделают забор крови для исследования.
К какому врачу обратится при микоплазме хоминис IgG?
Этот вопрос интересует многих молодых людей.
Чтобы сдать анализы для определения микоплазмы хоминис IgG следует обратиться к следующим специалистам:
- Урологу.
- Гинекологу.
- Терапевту.
- Педиатру.
Во время обращения к одному из этих специалистов вам проведут полный осмотр.
При необходимости, даст направление на исследования в лабораторию.
После получения результата специалист поможет расшифровать его, и, назначит курс лечения.
При необходимости диагностики и лечения микоплазмы, обращайтесь к автору этой статьи – венерологу, урологу в Москве с 15 летним опытом работы.
Урогенитальный микоплазмоз относится к инфекционным заболеваниям с преимущественным половым путем передачи.
Возбудителем этой инфекционно-воспалительной патологии структур урогенитального тракта мужчин и женщин является специфическая бактерия Mycoplasma genitalium и Mycoplasma hominis.
Особенностью заболевания является длительное бессимптомное течение с частым развитием осложнений.
Для выявления возбудителя проводится лабораторная диагностика микоплазмозов.

Показания для диагностики урогенитального микоплазмоза
Необходимость проведения лабораторного исследования, направленного на выявление и идентификацию возбудителя урогенитального микоплазмоза, определяется рядом случаев:
- 1. Развитие симптоматики инфекционного воспаления структур урогенитального тракта:
- жжение и боль в области уретры (мочеиспускательного канала), которые часто усиливаются во время мочеиспускания;
- диспареуния (болезненность в половых органах во время занятия сексом);
- появление слизистых необъемных выделений с неприятным запахом из уретры или влагалища у женщин.
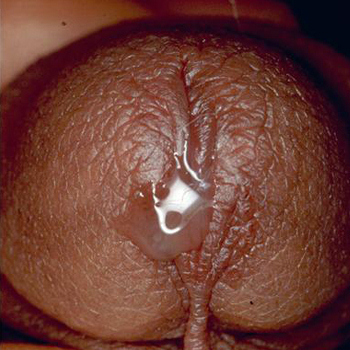
- 2. Появление признаков нарушения функциональной активности органов половой системы – эректильная дисфункция у мужчин. Нарушение менструального цикла у женщин, которые могут быть результатом развития осложнений урогенитального микоплазмоза.
- 3. Профилактическое исследование после незащищенного секса с новым половым партнером. А также в случае выявления микоплазм у постоянного полового партнера.
- 4. Комплексная диагностика причин мужского или женского бесплодия.

- 5. Диагностика урогенитального микоплазмоза проводится в ходе комплексного профилактического исследования пары на этапе планирования беременности или ее течения на ранних сроках.
Микоплазменная инфекция входит в первую десятку самых распространенных половых инфекций, поражающих как мужчин, так и женщин.

О том как проходит диагностика
урогенитального микоплазмоза
рассказывает подполковник
медицинской службы, врач
Ленкин Сергей Геннадьевич
Содержание данной статьи проверено и подтверждено на соответствие медицинским
стандартам врачем дерматовенерологом, урологом, к.м.н.
Ленкиным Сергеем Геннадьевичем
| Наименование | Срок | Цена |
|---|---|---|
| ДНК Mycoplasma hominis | 1 д. | 300.00 руб. |
| ДНК Mycoplasma genitalium | 1 д. | 300.00 руб. |
Виды лабораторной диагностики микоплазмоза
Диагностика микоплазмоза основывается на выявлении и идентификации возбудителя инфекционной патологии.
Для этого в современных лабораториях применяется несколько методов лабораторного исследования, которые включают:
- 1. Микроскопия мазка. У мужчины он берется из уретры. У женщины – из уретры, влагалища и шейки матки. Микроскопия является методом экспресс-диагностики. Она используется для постановки предварительного диагноза, так как обладает невысокой специфичностью и чувствительностью.
- 2. Культуральное бактериологическое исследование. Проводится посев биологического материала (мазок из уретры, влагалища или шейки матки, моча, сперма) на специальную питательную среду. В случае наличия возбудителя на ней вырастают колонии микроорганизмов. Их идентифицируют и определяют видовую принадлежность. Особенностью данного метода лабораторной диагностики является возможность определения чувствительности возбудителя к антибактериальным препаратам.
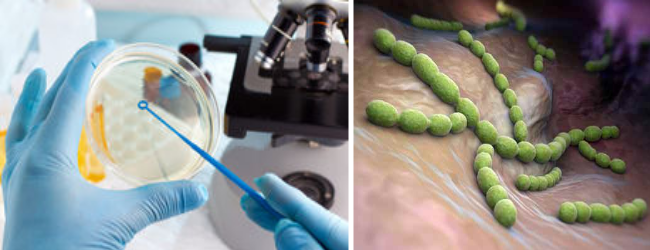
- 3. Метод амплификации нуклеотидов патогенных микроорганизмов или реакция полимеразной реакции (ПЦР). Современный метод исследования, при котором проводится выявление, накопление (множественное удваивание молекул) генетического материала возбудителя с последующей его идентификацией.
- 4. Исследование крови на определения антител к микоплазмозу. Выделяют М и G антитела к микоплазмам. Их исследуют в венозной крови пациентов.

На сегодняшний день в современных лабораториях применяется метод культурального исследования и полимеразная цепная реакция.
Интерпретация анализа на антитела в крови при микоплазмозе
Существуют 5 классов антител, которые образуются в иммунной системе в результате внедрения чужеродного агента.
Для диагностики инфекций имеют значение 3 класса – IgM, IgG и IgA.
Разберем подробнее, в какой срок, какие из антител появляются.
Время появления строго индивидуально и зависит от уровня напряженности иммунной системы.
Спустя 5-6 дней после инфицирования микоплазмой, образуются антитела класса M (IgM).
Их появление говорит об остром процессе и инфицировании в недавнем времени.
Титр данных антител нарастает и достигает максимума к 15-17 дню, затем постепенно снижается.
Антитела класса G (IgG) появляются в крови через 3-4 недели.
Этот класс иммуноглобулинов может долго присутствовать в организме.
Даже после успешного лечения, эти элементы могут оставаться в крови.
Как правило, уровень IgG сохраняется в течение нескольких лет после перенесенного заболевания.
Таким образом, обнаружение IgG говорит о наличии хронической или перенесенной инфекции либо.
Для диагностики имеет значение 4-х кратное увеличение титра IgG в двух парных сыворотках.
Определение IgA производят редко.
Они появляются в острую фазу заболевания и быстро исчезают.
Особенности посева на микоплазмоз
Культуральное исследование на микоплазмоз имеет высокую чувствительность и специфичность.
Существуют определенные трудности при выполнении этого анализа.
Микоплазма требует добавления в питательные среды определенных аминокислот, белков, стеролов и мочевины.
Для предотвращения роста транзиторной флоры, на среду наносится пенициллин.
В диагностике используют жидкие и твердые питательные среды.
Применение жидких сред основано на определение уреазной и аргиназной активности.
Первая характерна для микоплазмы уреалитикум, вторая - для микоплазмы хоминис.
По этому признаку можно их дифференцировать.
Твердые среды позволяют определить вид микроорганизма, подсчитать их количество.
Высокая контаминация микроорганизмом говорит о его виновности в развитии заболевания.
После выделения вида, производят определение чувствительности и резистентности к антибиотикам.
Сравнение точности методик ПЦР посева и ИФА на микоплазмоз
Данные два анализа получили наиболее широкую распространенность для диагностики ИППП.
Это обусловлено быстротой проведения, высокой чувствительностью и специфичностью.
ПЦР-диагностика относится к наиболее точным методам обследования, позволяет определить наличие даже одной ДНК микроорганизма.
Чувствительность и специфичность приближается к 100%.
Помните! Метод может быть неинформативен в инкубационный период заболевания.
Серологические методы обследования, в т.ч. ИФА, основаны на обнаружении антител к искомому антигену.
Данный анализ говорит только о контакте организма с инфекцией.
Выработка антител индивидуальна у каждого человека и зависит от уровня функционирования иммунной системы.
В силу различных обстоятельств, у человека могут возникнуть иммунодефицитные состояния.
По этим причинам, титр антител может оказаться незначимым даже при наличии инфекции в организме.
Таким образом, результаты ИФА на микоплазму часто требуют подтверждения ПЦР диагностикой.
Микоплазмоз – диагностика и лечение
Начало этиотропной терапии урогенитального микоплазмоза, направленной на уничтожение возбудителя, возможно только после лабораторного выявления и идентификации микоплазм.
Микоплазма является внутриклеточным микроорганизмом.
К антибиотикам, которые действуют на внутриклеточную флору, относят: макролиды, тетрациклины, фторхинолоны.
Однако выявление вида и определение чувствительности к антибактериальным препаратам обязательно.
Бесконтрольное назначение антибиотиков чревато переходом инфекции в хроническое течение.
Лабораторная диагностика проводится также для контроля эффективности лечения.

Но основании результатов исследований венеролог принимает решение о прекращении антибактериального лечения или его продолжении с использованием других препаратов.
Когда после заражения берут анализ на микоплазмоз
Срок исследования зависит от метода осуществления диагностики.
Проведение общего мазка будет информативно в период клинических проявлений.
Для микоплазмы он развивается, как правило, через 14-25 дней от момента заражения.
Проведение серологических методов обследований возможно немного ранее.
Антитела класса M появляются уже на 5-6 день от момента инфицирования.
В этом случае говорят об острой стадии заболевания и недавнем заражении.
Определение антител класса G обосновано на 3-4 неделе заболевания или в период хронического течения инфекции.
Нахождение IgG не подтверждает наличие инфекции, может свидетельствовать о перенесенном в прошлом заболевании.
Проведение ПЦР диагностики и культурального исследования рекомендуется через 3-4 недели после заражения.
После приема антибиотиков: когда можно сдать анализ на микоплазмоз
Диспансерное наблюдение после лечения микоплазмоза не отличается от других ИППП.
Показаниями для снятия с учета являются отрицательная двухкратная ПЦР диагностика либо культуральное исследование.
Еще один критерий – отсутствие клинико-лабораторных признаков воспаления в анализах.
Проводить контроль необходимо на следующих сроках:
- Спустя 14 дней после окончания исследования – общий мазок и ПЦР-диагностика
- Спустя 30 дней – повторныйПЦР-анализ
Диагностика микоплазмоза у беременных
Микоплазмоз у беременных является грозным фактором развития осложнений течения беременности и родов.
Патология опасна как для матери, так и для ребенка.
Инфекция может привести к самопроизвольному выкидышу, преждевременным родам, развитию эндометрита.
Помните! При прохождении малыша по родовым путям, во время родов, возможно заражение.
Как правило, у детей возникает респираторная форма заболевания с поражением трахеи, бронхов и легких.
Ранняя диагностика и лечение снизит риски развития осложнений.
В период подготовки к зачатию рекомендуется полное обследование на ИППП.
Проведение ПЦР или культурального исследования необхоимо.
Это наиболее достоверные методы диагностики.
В случае обнаружения микоплазмы до беременности необходимо проведения обязательной антибактериальной терапии.
В этот период доступен весь арсенал антибиотиков, действующих на данных микроорганизм.
В случае выявления у беременной микоплазмы врач-гинеколог амбулаторно либо стационарно подбирает безопасный для плода антибиотик.
Течение микоплазмоза у ВИЧ инфицированных
ВИЧ – инфекция поражает преимущественно иммунную систему человека.
На фоне иммунодефицитного состояния происходит активация условно-патогенной флоры, такой как микоплазма.
В силу невозможности ограничения чужеродного агента, происходит распространение процесса.
По этой причине у пациентов с ВИЧ все половые инфекции протекают сложнее.
Особенности ИФА крови анализа на микоплазмоз при ВИЧ
В результате дисфункции иммунной системы, возможна неправильная интерпретация результатов.
При ВИЧ-инфекции у пациента могут отсутствовать диагностически значимые титры антител.
Для более точного анализа рекомендуется проведение ПЦР теста или культуральное исследование биологического материала.
Где сдать анализ на микоплазмоз?
Диагностикой и лечением микоплазмоза занимаются врачи-специалисты в кожно-венерологических центрах.
Кроме этого, возможно обследование у врача-уролога или гинеколога.
При малейшем подозрении на наличие инфекции, обращайтесь к врачу.
Записаться на прием можно по телефону нашей клиники, или на сайте он-лайн.
Для диагностики и лечения микоплазмоза, обращайтесь к автору этой статьи – венерологу, урологу в Москве с 15 летним опытом работы.
Читайте также:

