Диагностика токсокароза у детей
Обновлено: 24.04.2024
Токсокароз (в МКБ-10 отмечен кодом B83.0) — личиночный, хронически протекающий тканевый зоонозный геогельминтоз с длительным и рецидивирующим течением, полиморфизмом клинических проявлений, с преимущественным поражением внутренних органов и органа зрения.
Эпидемиология
Инвазия токсокарами широко распространена среди животных и людей. Пораженность псовых, основных хозяев токсокар, во всем мире очень высока и достигает в отдельных регионах 90%. Рост числа собак в городах, высокая экстенсивность их инвазии токсокарами, значительная плодовитость гельминтов и устойчивость яиц во внешней среде — определяющие факторы широкого распространения этого гельминтоза.
Зараженность людей токсокарами варьирует от 2,6% в Бельгии до 80% на Карибских островах. В России, по данным эпидемиологических и серологических исследований, инвазировано до 0,5 млн человек, зараженность варьирует до 21,5%. Наблюдают ежегодный рост заболеваемости, особенно у детей в сельской местности.
Источник инвазии для человека в синантропном очаге — собаки (редко кошки), обсеменяющие почву яйцами гельминтов. Люди не могут быть источником заражения, так как в организме человека паразит не достигает половозрелой стадии и не выделяет яйца во внешнюю среду.
Существует несколько путей заражения животных:
- внутриутробное заражение щенков через плаценту инвазированной беременной суки (трансплацентарный путь);
- заглатывание собаками инвазионных яиц с обсемененной яйцами токсокар почвы (пероральный путь);
- через молоко кормящей собаки (трансмаммарный путь);
- поедание собакой тканей паратенических (резервуарных) хозяев.
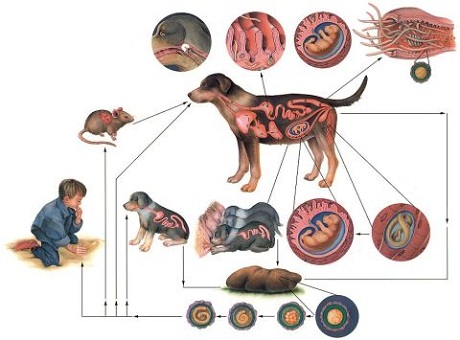
Яйца гельминтов, выделяемые собаками, созревают до инвазионной стадии в почве. Оптимальная температура — 24-30 °С, влажность воздуха — 85%, почвы — 20% и выше. При этих условиях развитие личинки в яйце происходит в течение 5-8 сут.
Человек заражается при проглатывании яиц токсокар с пищевыми продуктами и водой. К группе риска относятся: дети 1,5-5 лет, контактирующие с почвой и собаками; дети, страдающие геофагией; люди, имеющие профессиональный контакт с животными и почвой (ветеринарные работники, сотрудники питомников, цирков, зоопарков, рабочие коммунального хозяйства, продавцы овощных магазинов, работники овощных баз); умственно отсталые и психически больные со склонностью к копро- и геофагии; владельцы приусадебных участков, домашних животных.
Патогенез
В кишечнике человека из яиц выходят личинки размером 0,1-0,2 мм. Они перфорируют стенку кишки и проникают в лимфатические и кровеносные сосуды и заносятся во все органы и ткани: печень, легкие, глаза, селезенку, скелетные мышцы и головной мозг. Попав в мелкие капилляры (диаметром 0,02 мм), личинки застревают в паренхиме органа, где задерживаются, сохраняя жизнеспособность в течение многих месяцев и лет. При ослаблении защитных сил организма возможны их активизация и дальнейшая миграция по организму. Постепенно личинки инкапсулируются и погибают.
Морфологически токсокароз — эозинофильный гранулематоз как проявление аллергической реакции замедленного типа. В центре гранулемы находится очаг некроза, по периферии — большое количество эозинофилов, гистиоцитов, нейтрофилов, макрофагов, лимфоидных и эпителиоидных клеток. Многочисленные гранулемы расположены в:
- печени,
- легких,
- поджелудочной железе,
- миокарде,
- мезентериальных лимфатических узлах,
- головном мозге,
- глазах.
При миграции личинки травмируют ткани, вызывают геморрагии, некрозы, могут быть проводниками и инокуляторами патогенной микрофлоры.
Ведущую роль в патогенезе токсокароза играет сенсибилизация организма продуктами жизнедеятельности гельминта: метаболитными и соматическими антигенами с развитием реакции гиперчувствительности. Повышенная продукция специфических антител класса IgE приводит к активации тучных клеток, базофилов, нейтрофилов и высвобождению ими ряда медиаторов — гистамина, простагландинов, лейкотриенов, ответственных за аллергические реакции немедленного типа.
Активация Тh2-клеток, нарастание ИЛ-5, ИЛ-3, GM-CSF (колониестимулирующего фактора) способствуют активации эозинофилов, увеличению их количества в сосудистом русле и тканях. Эозинофилы концентрируются в местах локализации личинок токсокар, где разрушаются и высвобождают гранулы, содержащие ферменты. Эозинофильная пероксидаза повреждает эндотелий сосудов и эндокард. За счет основного базового протеина, инактивирующего гепарин, образуются тромбы.
Генерация активных радикалов кислорода и продукция катионных белков делают эозинофилы центральным повреждающим фактором при накоплении их в тканях. Сенсибилизированные Т-лимфоциты, скопившиеся вокруг личинки, выделяют лимфокины, привлекают макрофаги и другие клетки, которые включаются в процесс формирования гранулем.
Симптомы
Для токсокароза характерно длительное (до нескольких лет), рецидивирующее течение. Клинические рецидивы обусловлены периодическим высвобождением личинок паразита из гранулем и возобновлением их миграции. Различают висцеральную и глазную формы токсокароза.
Висцеральный токсокароз протекает в 2 вариантах: инаппарантном и клинически выраженном.
Висцеральный токсокароз регистрируют преимущественно у детей в возрасте 1,5-4 лет, взрослые заболевают реже и болеют легче. Мальчики инвазируются в 2 раза чаще, чем девочки, вероятно, из-за более активного контакта с почвой, пикацизма (стремления брать в рот землю).
Выделяют острую и хроническую стадии инвазии. Заболевание часто начинается остро, без продромального периода, лишь в редких случаях наблюдают короткий период легкого недомогания. Основные клинические симптомы острой стадии: рецидивирующий подъем температуры тела, лимфаденопатия, легочный синдром, увеличение печени, реже селезенки, кожные высыпания в виде крапивницы или полиморфной сыпи, отек Квинке.
Температура тела чаще субфебрильная, обычно повышается в полдень или вечером, сопровождается познабливанием, а при снижении — обильным потоотделением. Наблюдают инъекцию сосудов конъюнктивы.
Поражение бронхолегочной системы отмечено у 20-50% больных с разнообразием клинических проявлений: катаральным воспалением дыхательных путей, бронхитом, пневмонией, бронхообструктивным синдромом.
Известны редкие случаи эозинофильной пневмонии с летальным исходом; возможен стойкий бронхообструктивный синдром с исходом в бронхиальную астму.
С абдоминальным синдромом токсокароз протекает у 60% больных. У детей ухудшается аппетит, снижается масса тела, появляются боли в животе, тошнота, рвота, метеоризм, диарея. Редко развивается эозинофильный гастроэнтерит.
Типичный признак токсокароза — гепатомегалия у 40-80% больных с увеличением печени на 2-4 см, иногда до значительных размеров. Увеличение селезенки отмечено у 20-40% больных. При тяжелом течении возможен гепатит с повышением активности аминотрансфераз, реже — с признаками холестаза.
При УЗИ печени регистрируют линейные структуры повышенной эхоплотности, округлые очаги пониженной плотности, очаги кальцинации, увеличение лимфатических узлов в воротах печени, селезенки, парааортальных лимфатических узлов. При гистологическом исследовании пункционного биоптата печени обнаруживают эозинофильную инфильтрацию стромы, эозинофильные гранулемы, иногда картину острого гепатита иммунной природы. Редко обнаруживают гранулематозную тканевую реакцию, личинки токсокар. Описаны пиогенные абсцессы печени, связанные с микрофлорой вокруг паразитарных гранулем.
Увеличение лимфатических узлов отмечают у 60-70% детей, иногда значительное увеличение лимфатических узлов подчелюстной и шейной областей, ворот печени, селезенки. Пальпируемые лимфатические узлы болезненные, подвижные, без воспалительных изменений.
Поражение сердца вызвано миграцией личинок гельминта в миокард или аллергической реакцией на антигены токсокар. В остром периоде наблюдают тахикардию, глухость сердечных тонов, систолический шум, расширение границ сердца. На ЭКГ выявляют диффузные изменения миокарда, иногда нарушения ритма. Возможен миокардит токсико-аллергической природы. Описаны случаи синдрома Леффлера II — эозинофильного васкулита с пристеночным эндокардитом, развитие фибропластического эндокардита. В результате инфильтрации эндокарда и миокарда эозинофилами наступает фиброз эндокарда с рестриктивной кардиомиопатией. Поражение папиллярных мышц и хорд приводит к клапанной недостаточности. Эндокардит осложняется пристеночным тромбообразованием, тромбоэмболией.
Поражение ЦНС встречают нечасто. В острой стадии больные жалуются на головную боль, бессонницу, раздражительность. В тяжелых случаях инвазии аблюдают менингоэнцефалит, арахноидит, рецидивирующий миелит. Признаки общемозговых и очаговых поражений головного и спинного мозга: парезы, параличи, генерализованные и фокальные судороги, различные нарушения психики. Редко при патоморфологическом исследовании головного мозга выявляют васкулиты, эозинофильные гранулемы. Личинки токсокар обнаруживают в головном мозге и СМЖ.
Кожные поражения возникают у каждого четвертого больного токсокарозом как единственное проявление инвазии: узловатая эритема, мелкопапулезная сыпь, крапивница. Иногда появляются рецидивирующие болезненные образования под кожей в области поясницы и конечностей. При их биопсии выявляют инфильтрацию дермы с большим количеством эозинофилов и гигантских клеток.
Поражение мышц — редкое проявление инвазии: иногда наблюдают миалгии, усиливающиеся при физической нагрузке, ходьбе, болезненность мышц при пальпации, их уплотнение.
Реактивные артриты, васкулиты при токсокарозе редки и, вероятно, связаны с отложением иммунных комплексов в синовиальной оболочке суставов, сосудистой стенке. В клинической картине отмечают артралгию, моноартрит, тромбофлебит, васкулит, кожные поражения (пурпуру Шенлейна-Геноха).
Поражение других органов и систем: вовлечение щитовидной железы протекает с симптомами объемного образования; развиваются реактивный панкреатит, поражение почек разной степени тяжести, эозинофильный гранулематоз кишечника.
Одно из постоянных проявлений висцерального токсокароза — стойкая, длительная эозинофилия кровивплоть до эозинофильной лейкемоидной реакции. Относительная эозинофилия — 30-90%, общее число лейкоцитов — 15-20х109/л, иногда — 80-100х109/л; СОЭ повышена. При длительном течении снижен гемоглобин. В белковом спектре — гипергаммаглобулинемия, характерно повышение общего IgE.
Инаппарантный (бессимптомный) токсокароз проявляется кратковременным виражом противотоксокарозных антител в низких титрах
(1:400-1:800) без клинических проявлений инвазии. У некоторых больных при объективном обследовании обнаруживают небольшое увеличение периферических лимфатических узлов, инъекцию конъюнктив, увеличение печени на 1-2 см. В периферической крови — эозинофилия 6-18% при нормальном лейкоцитозе.
Глазная форма токсокароза редко сочетается с висцеральными поражениями и развивается преимущественно у детей старше 12 лет и взрослых. Чаще поражается сетчатая оболочка, собственно сосудистая оболочка; хрусталик с воспалением и специфическими гранулемами. Обычно страдает один глаз, но возможно и двустороннее поражение. Клинически наблюдают диффузный эндофтальмит, задний гранулематозный хориоретинит, папиллит, кератит, увеит, иридоциклит, эозинофильные абсцессы в плоской части цилиарного тела, катаракту. При тяжелом течении процесс прогрессирует до панофтальмита и отслойки сетчатки. Глазной токсокароз приводит к слепоте.
Клиническое наблюдение. Девочка, 1 год 7 мес, поступила с жалобами на сухой кашель с астматическим компонентом, общую слабость, плохой аппетит.
Анамнез: в возрасте 3 мес у ребенка появились сухой кашель с астматическим компонентом, одышка, субфебрилитет в течение месяца. Лечение отхаркивающими и отвлекающими процедурами не принесло улучшения. В анализе крови: лейкоцитоз — 26х109/л, эозинофилия — 52%, СОЭ — 48 мм/ч. Длительное лечение антигистаминными препаратами привело к исчезновению кашля и нормализации температуры тела. В анализе крови - без перемен. В 1 год и 3 мес девочка перенесла двустороннюю очаговую пневмонию. Лечение антибиотиками не привело к улучшению. При повторных исследованиях крови — эозинофилия 35-65%.
При поступлении: общее состояние средней тяжести, температура тела — 39,6 °С, питание сниженное, кожа и слизистые оболочки бледные, на животе и нижних конечностях петехиальная сыпь. Подмышечные лимфатические узлы увеличены. Печень ниже края реберной дуги на 5 см, край острый, болезненный при пальпации, селезенка пальпируется по краю реберной дуги.
Проведено лечение албендазолом в дозе 10 мг/кг массы тела в течение 5 дней, диазолином по 0,03 г 2 раза в день в течение 5 дней. После лечения температура тела снизилась до субфебрильных значений, печень уменьшилась на 2 см. Лейкоцитоз снизился до 20х109/л, эозинофилия — 37%. Через 10 дней проведен повторный курс тиабендазола в тех же дозах в течение 9 дней, одновременно — преднизолон по 10 мг/сут с постепенным снижением дозы. Температура тела нормализовалась, исчезла сыпь, печень уменьшилась до нормы. Количество эозинофилов — 5%, WBC - 13х109/л. Девочку выписали домой в удовлетворительном состоянии. Под наблюдением находилась в течение года. Печень и селезенка не увеличены. В анализе крови: WBC — 8,9х109/л, эозинофилы — 14%. Реакция с антигеном Toxocara canisотрицательная.
Диагностика
Дифференциальную диагностику токсокароза следует проводить с паразитарными инвазиями и большой группой заболеваний непаразитарной природы, сопровождаемых повышением эозинофилов в периферической крови.
Дифференциальную диагностику проводят с миграционной стадией гельминтозов человека (аскаридозом, стронгилоидозом, шистосомозами, описторхозом, клонорхозом, филяриозами); из непаразитарных заболеваний — с лимфогранулематозом, злокачественной лимфомой, синдромом Леффлера, синдромом Лефргена, болезнью Леттерера- Сиве, болезнью Франклина, эозинофильной гранулемой, узелковым периартериитом, хроническим миелолейкозом, миелофиброзом, полицитемией, семейной эозинофилией, первичным эозинофильным синдромом, болезнью Аддисона, герпетиформным дерматитом Дюринга, аденомой поджелудочной железы, гипернефромой.
Диагностика токсокароза представляет определенные трудности, поскольку клиническая симптоматика малоспецифична, а паразитологические методы для прижизненной диагностики практически не используются из-за отсутствия возможности обнаружения мигрирующих личинок и сложности их идентификации по гистологическим срезам.
Диагностику токсокароза необходимо проводить последовательно в 4 этапа:
1) определить показания к обследованию;
2) оценить эпидемиологический анамнез;
3) провести клиническое обследование больного;
4) выполнить серологическую диагностику. Показания к обследованию:
• повышенное содержание эозинофилов в периферической крови неясного генеза;
• острое заболевание органов дыхания (бронхит, пневмония, трахеит), протекающее с гиперэозинофилией;
• рецидивирующие заболевания органов дыхания, сопровождаемые гиперэозинофилией;
• синдром рецидивирующих болей в животе неясного генеза, сопровождаемый астеническим синдромом, повышенным содержанием эозинофилов в периферической крови;
• аллергические заболевания с повышенным содержанием эозинофилов в периферической крови и/или повышенным содержанием общего IgE.
Эпидемиологические факторы, свидетельствующие о возможном заражении токсокарозом:
• наличие собаки в доме или на приусадебном участке (учитывают пол собаки, возраст, наличие щенков, особенности выгула, проводимое противопаразитарное лечение);
• наличие огорода вблизи жилья;
• эпизоды геофагии у больного;
• игра ребенка в песочнице и другие контакты с землей;
• употребление в пищу немытых ягод, овощей, фруктов.
На основании клинических наблюдений в литературе предложена балльная система оценки клинических симптомов и лабораторных признаков при токсокарозе. Диагноз токсокароза считается обоснованным при сочетании симптомов и показателей, в сумме превышающих 12 баллов.
Диагностическая ценность клинико-лабораторных показателей при токсокарозе
Токсокароз у детей — это тканевой гельминтоз, который вызван паразитами рода Toxocara. Заболевание имеет полиморфную клиническую картину. Типичные признаки висцеральной формы: легочной синдром, субфебрильная лихорадка, нарушения пищеварения. При глазном токсокарозе возникают отек и гиперемия век, болезненность, экзофтальм. Диагностика гельминтоза включает серологические и гистологические анализы, методы визуализации (рентгенография грудной клетки, УЗИ органов живота, ЭКГ, ЭхоКГ). Лечение проводится этиотропными противопаразитарными препаратами, гормонами и антигистаминными средствами, пробиотиками и ферментами.
МКБ-10
Общие сведения
Токсокароз — самое распространенное на территории России паразитарное заболевание, интенсивный показатель которого составляет 380 случаев на 100 тыс. населения. Наиболее подвержены дети дошкольного возраста. Среди возрастной группы до 4 лет половых различий заболеваемости не выявлено, в категории 5-14 лет паразиты чаще поражают мальчиков, а среди подростков 14-18 лет больше заражаются девочки. Несмотря на высокую частоту встречаемости, диагностика и лечение токсокароза затруднены, что связано с полиморфностью клинической картины.

Причины
Основной фактор риска инфицирования токсокарами — несоблюдение детьми санитарно-гигиенических норм, поэтому чаще всего болезнь поражает дошкольников, которые играют в песочнице, а потом берут все грязными руками. В группу риска относят семьи, у которых есть домашние животные, жители пригородов и сельской местности. Высокий риск заражения токсокарозом и другими гельминтозами у детей, которые страдают геофагией — патологической тягой к поеданию земли и песка.
Патогенез
Инкубационный период составляет несколько дней, но не исключено латентное течение гельминтоза. Передача инфекции ребенку происходит преимущественно 3 путями: контактно-бытовым — при играх с домашними или бродячими животными, алиментарным — при поедании овощей, зелени, которые загрязнены землей с цистами токсокар, водным — при употреблении зараженной некипяченой воды. Редкий путь инфицирования — гео-оральный, который наблюдается у детей с геофагией.
Жизненный цикл возбудителя достаточно сложен, он проходит в организме животных и частично в почве. В ЖКТ человека поступают зрелые цисты, из которых образуются личинки токсокар. Через стенку кишечника они проникают в кровоток: сначала по венозной системе достигают правых отделов сердца, затем попадают в легочные сосуды, оттуда — в левую половину сердца и далее разносятся по всем внутренним органам.
Личинки могут длительное время сохраняться в тканях в латентном состоянии, а их активация происходит при снижении иммунитета. Паразиты выделяют антигены, которые провоцируют аллергические реакции немедленного и замедленного типов, образование эозинофильных гранулем. Специфические для токсокароза тканевые элементы в центре имеют зону некроза, вокруг нее расположены эозинофилы, фагоциты и лимфоидные клетки.
Классификация
В литературе по детским инфекционным болезням существует несколько вариантов систематизации токсокароза:
- по течению: типичные и атипичные (стертые, бессимптомные) варианты;
- по локализации поражения: висцеральная и глазная формы;
- по тяжести: легкое, среднетяжелое и тяжелое течение.
По длительности токсокароз у детей бывает острым (до 3 месяцев) и хроническим, который подразделяется на непрерывный и рецидивирующий вариант.
Симптомы токсокароза у детей
Висцеральная форма
Клинические признаки гельминтоза зависят от объема поглощенных цист токсокары, степени распространения личинок по организму и уровня иммунной защиты. У детей чаще встречается висцеральная форма, которая ассоциирована с одновременным проникновением большого количества гельминтов в организм. Вначале токсокароз проявляется неспецифическими признаками: повышением температуры до субфебрильных цифр, небольшим ознобом, слабостью, вялостью.
У 65% детей первично выявляются симптомы поражения легких. Пациенты жалуются на кашель, который усиливается по ночам, одышку при физических нагрузках. Возможны катаральные явления в виде насморка и заложенности носа, отхаркивания слизистой мокроты при кашле. Хронический вариант токсокароза иногда протекает под маской рецидивирующих бронхитов или персистирующей бронхиальной астмы, классическое лечение которых не дает должного эффекта.
Помимо легочного синдрома, при гельминтозе наблюдается увеличение и болезненность нескольких групп лимфатических узлов. У ребенка возможна асимметрия живота и тяжесть в правом подреберье, вызванные увеличением размеров печени. Типичным проявлением считается рецидивирующая лихорадка неясного генеза. На коже ребенка образуются зудящие волдыри, на ладонях и ступнях формируются безболезненные узелки.
Глазная форма
Глазная форма токсокароза начинается с умеренной отечности и покраснения верхнего века, которые сохраняются не более 5 дней. Симптомы повторяются на протяжении полугода с промежутками от нескольких дней до 2-3 недель. Постепенно отек становится более выраженным, заметен экзофтальм, ребенок жалуется на боли при движениях глазом. Поражение при токсокарозе чаще одностороннее.
Осложнения
Если лечение гельминтоза не проводится вовремя, происходят паразитарные и аутоиммунные повреждения внутренних органов. Зачастую у ребенка формируется тяжелая персистирующая бронхиальная астма, которая сопровождается бронхообструктивным синдромом и дыхательной недостаточностью. Нарушения вентиляции и снижение местного иммунитета — предрасполагающие факторы развития у зараженных детей затяжных пневмоний, легочных абсцессов.
Поражение органов ЖКТ проявляется панкреатитом, гепатитом, синдромом мальабсорбции и мальдигестии. Также встречаются осложнения со стороны ЦНС (парезы, параличи, нарушения чувствительности), опорно-двигательного аппарата (синовиты, артриты). При токсокарозе возможен летальный исход, если личинки паразита мигрируют в миокард и жизненно важные центры головного мозга. Смерть наступает от острой сердечной недостаточности, остановки дыхания.
Диагностика
Обследованием ребенка занимается педиатр, который при подозрении на заражение гельминтами дает направление на консультацию детского инфекциониста. При физикальном исследовании органов дыхания обращают внимание на хрипы и ослабленное дыхание, при пальпации живота врач обнаруживает гепатомегалию, при внешнем осмотре выявляется аллергическая сыпь. В план диагностики включаются:
- Рентгенография ОГК. Обзорную рентгенограмму в двух проекциях делают для исследования степени поражения легочной ткани. На снимках заметны множественные очаги инфильтрации, усиление бронхиального рисунка, могут быть признаки эмфиземы. Для детальной диагностики проводится спирометрия (школьникам), тест на бронхиальную обструкцию.
- Биопсия. Обнаружение личинок токсокары в биоптатах — наиболее достоверный способ диагностики паразитарного процесса. Детям наиболее часто делают чрескожную пункционную биопсию печени. Если на кожных покровах есть характерные узелки, их биоптаты также используют для гистологической верификации диагноза.
- Дополнительные инструментальные методы. Для оценки состояния гепатобилиарной системы, поджелудочной железы и кишечника ребенка назначается УЗИ брюшной полости. При перебоях в работе сердца показана ЭКГ и эхокардиография. При затруднениях в диагностике выполняют КТ легких, брюшных органов.
- Серологические реакции. ИФА обладает высокой чувствительностью (93,7%) и специфичностью (89,3%) при висцеральной форме токсокароза. При титре антител 1:200 или 1:400 говорят о бессимптомном носительстве, а значение 1:800 и выше указывает на активный процесс, лечение которого нужно начинать незамедлительно.
- Общеклинические анализы. В гемограмме детей с токсокарозом обнаруживают эозинофилию, лейкоцитоз, повышение СОЭ. При биохимическом исследовании крови определяют гипергаммаглобулинемию, возрастание IgE, в печеночных пробах — синдром цитолиза. Обязательно исследуют кал на яйца глист, чтобы исключить другие гельминтозы.
Лечение токсокароза у детей
Этиотропное лечение проводится противогельминтными препаратами группы бензимидазолов. Они назначаются короткими курсами в возрастных дозировках. Спустя 3 месяца выполняется иммунологический контроль терапии и при негативной динамике подбирается новый курс противопаразитарных средств. Патогенетическое и симптоматическое лечение гельминтоза предполагает прием препаратов следующих групп:
- Кортикостероиды. Рекомендованы для купирования аллергических и аутоиммунных реакций при тяжелых формах токсокароза. Уменьшают активность воспалительного процесса, предотвращают системные осложнения.
- Антигистаминные средства. Используются при кожных аллергических проявлениях — зудящих дерматозах, отеке Квинке. Быстро устраняют субъективный дискомфорт, уменьшают отечность и покраснение кожи ребенка.
- Пробиотики. Применяются для нормализации пищеварительной функции, восстановления микробиоты кишечника. При мальбасорбции обычно терапия дополняется пищеварительными ферментами. Детям, страдающим диарейным синдромом, показаны энтеросорбенты.
Прогноз и профилактика
В большинстве случаев противопаразитарное лечение эффективно уничтожает личинок гельминтов и предупреждает необратимые поражения внутренних органов. Иногда токсокароз протекает в бессимптомной форме, что коррелирует с хорошей активностью иммунной системы. Неблагоприятный прогноз устанавливают при массивной инвазии, наличии у ребенка первичного или вторичного иммунодефицита.
В отношении больного и его окружения противоэпидемические меры и изоляция не проводятся. Профилактика токсокароза предполагает обучение ребенка правилам личной гигиены, тщательное мытье овощей и зелени, использование бутилированной или кипяченой водопроводной воды. Важную роль отводят лечению бездомных животных, организации приютов, что уменьшает количество естественных резервуаров инфекции.
1. Особенности течения токсокароза у детей/ Т.В. Сорокман, И.И. Перкас// Актуальная инфектология. — 2018.
4. Токсокароз у детей/ Л.В. Глазунова, Р.Г. Артамонов, Е.Г. Бекташянц, Е.В. Куйбышева// Лечебное дело. — 2008.
Токсокароз у детей — паразитарная болезнь детей и взрослых, которая широко распространена среди жителей сёл.
Болезнь характерна для детей в возрасте до 14 лет. Прогноз благоприятный. Но бывают случаи тяжелых поражений, которые крайне редко заканчиваются смертью. Болезнь может протекать годами. Гельминтозы, согласно данным ВОЗ, занимают 4-е место по степени наносимого здоровью населения ущерба.
Что провоцирует / Причины Токсокароза у детей:
Существует больше 270 видов гельминтов, которые могут быть паразитами в человеческом теле. Ребенок или взрослый может стать случайным хозяином некоторых видов гельминтов животных, например, круглых червей токсокар. Токсокары в половозрелой стадии развития имеют длину 4-18 см. Они заселяются в тонкий кишечник. Токсокары также паразитируют в организмах животных, яйца половозрелых форм выделяются во внешнюю среду.
Токсокароз возбуждают аскаридаты, которые паразитируют на собаках и кошках (реже). Распространяют заболевания насекомые, которые живут в квартирах и домах. В основном – тараканы.
Патогенез (что происходит?) во время Токсокароза у детей:

Личинки задерживаются на некоторое время в легких ребенка, потом попадают во все органы и ткани, где и оседают. Вокруг них формируются гранулемы, окруженные капсулой, в которых они сохраняют жизнеспособность многие годы, что объясняет рецидивы (повторения) болезни.
Симптомы Токсокароза у детей:
Токсокароз у детей может проявляться множеством симптомов.
Виды токсокароза:
- системный (висцеральный)
- местный (глазной)
Болезнь имеет долгое рецидивирующее течение – до 3-4 лет. Летальный исход может быть только при попадании личинок в миокард и важные в функциональном отношении участки центральной нервной системы ребенка.
Типичные симптомы системного токсокароза у детей:
- легочный синдром
- познабливание
- рецидивирующая лихорадка
- увеличение размеров печени
- гипергаммаглобулинемия
- повышение температуры до субфебрильных значений (редко – до фебрильных)
Температура у ребенка при токсокарозе повышается в основном в периоде проявлений со стороны легких. Синдром поражения легких бывает не у всех детей, но у большей части. Он может вызвать в самом легком случае катаральные явления, а в самом тяжелом случае – астмоидные состояния. Ребенок жалуется на сухой кашель. Приступы кашля случаются ночью. Возможна тяжелая одышка.
Зафиксированы случаи тяжелых пневмоний, для которых были характерны осложнения, и исход которых был смертельным. Рентгенограмма показывает усиление легочного рисунка, множественные или единичные эозинофильные инфильтраты, картину бронхолегочной инфильтрации. Постоянным признаком токсокароза у детей считается высокая эозинофилия вплоть до лейкемоидной реакции эозинофильного типа. Абсолютное число эозинофилов может возрастать до 100х109/л. Общее число лейкоцитов повышается до 15–100x109/л.
На коже время от времени могут появляться высыпания экзематозного, эритематозного, уртикального характера. Под кожей ладоней и ступней с помощью методов пальпации находят туберкулоподобные узелки небольших размеров, в биоптатах которых периодически находят личинок токсокар. Может присоединиться вторичная стрептостафилодермия. В волосах и ногтях ребенка наблюдаются дистрофические изменения.
В большинстве случаев при токсокарозе у детей увеличены селезенка, печень, лимфатические узлы. В части случаев рассматриваемом заболевание может проходить с абдоминальным синдромом: тошнотой, рвотой, болями в животе, диареей, метеоризмом, иногда асцитом. Состав нормальной микрофлоры кишечника нарушен.
Могут быть выявлены симптомы поражения ЦНС:
- раздражительность
- нарушение сна
- расстройства поведения
- симптомы очагового поражения головного мозга (при которых могут быть парезы, конвульсии, параличи и пр.)
Согласно некоторым исследователям, существует (помимо висцеральной и местной формы) неврологическая форма токсокароза у детей.
Токсокароз глаз чаще всего поражает только одну сторону: сетчатую оболочку, сосудистую оболочку, где формируются воспалительные массы (нередко их принимают за ретинобластому или псевдоглиому) и специфические гранулемы.
Диагностика Токсокароза у детей:
При диагностике обязательно требуется подтверждение обнаружением личинок в биоптатах тканей, в частности, печени. Но на гистологических срезах идентифицировать и обнаружить мигрирующих личинок довольно трудно. Потому такое подтверждение удается далеко не во всех случаях. Эффективен такой метод диагностики как ИФА с экскреторносекреторным антигеном личинок токсокар. Титры от 1:200 до 1:400 свидетельствуют о токсокароносительстве с благоприятным течением инвазии, а титр 1:800 и выше — о болезни.
Дифференциируют токсокароз с другими гельминтозами человека, при которых проходят аллергические реакции:
Также токсокароз следует отличать от болезней, при которых есть эозинофилия:
- эозинофильный васкулит
- медикаментозная сенсибилизация
- гипернефрома
Лечение Токсокароза у детей:
Меры специфической терапии токсокароза у детей до конца не разработаны. Обычно назначают минтезол (тиабендазол), вермокс (мебендазол), дитразин цитрата (диэтилкарбамазин) и немозол (альбендазол).
Минтезол назначается дозой от 25 до 50 мг на 1 кг тела ребенка в сутки. Курс составляет от 5 до 10 дней. Могут быть побочные эффекты: тошнота, ухудшение аппетита, сонливость, головные боли, боли в животе. Они не длительны, после отмены препарата проходят почти сразу.
Вермокс следует давать ребенку по 100 мг 2 раза в сутки курсом от 2 до 4 недель, доза увеличивается постепенно до 300 мг по схеме, прописанной лечащим врачом. Могут быть побочные эффекты: тошнота, диарея, абдоминальные боли. Но они бывают в редких случаях.
Дитразина цитрат назначается больному токсокарозом ребенку в дозе 2–6 мг на 1 кг тела в сутки на протяжении 2-4 недель. Могут быть такие побочные эффекты: головокружение, головная боль, лихорадка, тошнота.
Также токсокароз лечат альбендазолом в дозе 10 мг на 1 кг тела больного, курс от 10 до 20 суток. Редко бывают такие побочные явления как при приеме дитразина цитрата. Они проходят после окончания приема препарата.
Восстановительно лечение требует приема препаратов для нормализации микрофлоры кишечника ребенка. Обязательно дают больному гепатопротекторы. Ребенка ставят на диспансерное наблюдение, длительность которого колеблется в зависимости от интенсивности заражения, длительности, реакции организма на паразита. 1 раз в месяц после окончания курса лечения проводится контроль периферической крови и ИФА. Повторные курсы проводят минимум через 3 месяца. Иногда лечение ребенка длится 3 года, а количество курсов специфической терапии достигает пяти или шести.
Повышение эффективности терапии за счет увеличения дозировки химиопрепаратов или числа курсов лечения не делается. Контроль лечения после его окончания продолжается не менее 3 лет.
Прогноз и наблюдение
Как уже отмечалось выше, прогноз при токсокарозе у детей в большинстве случаев благоприятный. Но редко могут быть поражения глаз и сердца, что более опасно. Нельзя медлить с лечением и ждать самоисцеления организма, ведь личинки могут дальше мигрировать, попадая в жизненно важные органы.
Ребенок с токсокарозом должен находиться на диспансерном наблюдении у инфекциониста, пока не нормализируется его состояние, и не придут в норму клинические анализы.
Профилактика Токсокароза у детей:
Профилактические меры заключаются в:
- сезонной дегельминтизации домашних четвероногих с применением противонематодных средств в обычной дозе, 1–2 дня
- ограничении количества бродячих собак и кошек
- недопущении загрязнения фекалиями собак детских площадок (особенно песочниц), садовых участков и огородов
- оборудовании площадок для выгула домашних животных
- неупотреблении в пищу продуктов, которые загрязнены почвой
- высаживании культур, которые препятствуют созреванию яиц нематод: бобовых, календулы, дельфиниума, бархатца и пр.
- достаточной термической обработке мяса паратенических хозяев (птицы, свинины)
- тщательном промывании клубники, черники и зелени проточной водой
- промывании и обливании горячей водой сырых овощей
К каким докторам следует обращаться если у Вас Токсокароз у детей:
Вас что-то беспокоит? Вы хотите узнать более детальную информацию о Токсокароза у детей, ее причинах, симптомах, методах лечения и профилактики, ходе течения болезни и соблюдении диеты после нее? Или же Вам необходим осмотр? Вы можете записаться на прием к доктору .
Токсокароз — паразитарное заболевание, вызываемое миграцией личинок аскарид животных семейства псовых (T. canis ). Характеризуется длительным рецидивирующим течением и полиорганными поражениями иммунологической природы. Возбудителями токсокароза могут быть также личинки других аскарид — кошки (T. mystax), коровы, буйвола, (T. vitulorum). Однако роль этих возбудителей в патологии человека практически не изучена
Половозрелые формы T. canis — крупные раздельнополые черви длиной 4 — 18 см локализуются в желудке и тонком кишечнике животных (собак). Интенсивность инвазии у собак может быть очень высокой, особенно у молодых животных. Средняя продолжительность жизни половозрелых особей составляет 4 месяца, максимальная — 6 месяцев. Самка паразита за сутки откладывает более 200 тыс. яиц. В 1 г фекалий может содержаться 10 000—15 000 яиц, так что в почву попадают миллионы яиц, обусловливая тем самым высокий риск заражения токсокарозом.
Яйца токсокар округлой формы, крупнее яиц аскариды (65—75 мкм). Наружная оболочка яйца толстая, плотная, мелкобугристая. Внутри яйца располагается темный бластомер.
Цикл развития возбудителя следующий. Выделившиеся яйца токсокар попадают в почву, где, в зависимости от влажности и температуры почвы, созревают за 5—36 суток, становясь инвазионными. Инвазионность яиц сохраняется в почве длительное время, в компосте — несколько лет.
Жизненный цикл токсокары сложный. Выделяют основной цикл и два варианта вспомогательных. Основной цикл происходит по схеме: окончательный хозяин (псовые) — почва — окончательный хозяин (псовые). Передача инвазии осуществляется геооральным путем. Вспомогательный цикл (вариант 1) идет трансплацентарно, в этом случае паразит в личиночной стадии переходит от беременной самки к плоду, в организме которого совершает полную миграцию, достигая в кишечнике щенка половозрелой стадии. Инвазированный щенок становится функционально полноценным окончательным хозяином, источником инвазии.
Вспомогательный цикл (вариант 2) осуществляется по цепи: окончательный хозяин (псовые) — почва — паратенический хозяин. Паратеническим (резервуарным) хозяином могут быть грызуны, свиньи, овцы, птицы, земляные черви. Человек также выступает в роли паратенического хозяина, но не включается в цикл передачи инвазии, являясь для паразита биологическим тупиком. Дальнейшее развитие возбудителя происходит при условии, что паратенический хозяин будет съеден собакой или другим окончательным хозяином. Механизм передачи инвазии при этом варианте — геооральный — ксенотрофный.
В зависимости от возраста хозяина реализуются разные пути миграции личинок токсокар. У молодых животных (щенков до 5 недель) почти все личинки совершают полную миграцию с достижением половозрелых форм в кишечнике и выделением яиц во внешнюю среду. В организме взрослых животных большая часть личинок мигрирует в соматические ткани, где сохраняет жизнеспособность несколько лет. В период беременности и лактации у беременных сук возобновляется миграция личинок. Мигрирующие личинки через плаценту попадают в организм плода. Личинки остаются в печени пренатально инвазированных щенков до рождения, а после рождения личинки из печени мигрируют в легкие, трахею, глотку, пищевод и попадают в желудочно-кишечный тракт, где через 3—4 недели достигают половозрелой стадии и начинают выделять во внешнюю среду яйца. Кормящие суки могут передавать щенкам инвазию также через молоко.
У человека цикл развития возбудителя, его миграция осуществляется следующим образом. Из яиц токсокар, попавших в рот, затем в желудок и тонкий кишечник выходят личинки, которые через слизистую оболочку проникают в кровеносные сосуды и через систему воротной вены мигрируют в печень, где часть из них оседает, инцистируется или окружается воспалительными инфильтратами, образуя гранулемы. Часть личинок по системе печеночных вен проходит фильтр печени, попадает в правое сердце и через легочную артерию — в капиллярную сеть легких. В легких часть личинок также задерживается, а часть, пройдя фильтр легких, по большому кругу кровообращения заносится в различные органы, оседая в них. Личинки токсокар могут локализоваться в различных органах и тканях — почках, мышцах, щитовидной железе, головном мозге и др. В тканях личинки сохраняют жизнеспособность многие годы и периодически, под влиянием различных факторов, возобновляют миграцию, обусловливая рецидивы заболевания.
Географическое распространение и эпидемиология
Токсокароз — широко распространенная инвазия, она регистрируется во многих странах. Показатели пораженности плотоядных являются высокими во всех странах мира. Средняя пораженность собак кишечным токсокарозом, обследованных на различных континентах, составляет свыше 15%, но в некоторых регионах у части животных достигает 93%. По данным сероэпидемиологических исследований, от 2 до 14% обследованных практически здоровых лиц в различных очагах токсокароза имеют положительные иммунологические реакции на токсокароз. Распространенность инвазии в различных регионах точно неизвестна, поскольку токсокароз не подлежит обязательной регистрации. Совершенно очевидно, что токсокароз имеет широкую геграфию распространения, и число больных значительно выше официально регистрируемых.
Токсокароз широко распространен и регистрируется во многих странах. Средняя пораженность кишечным токсокарозом собак, обследованных на различных континентах, составляет свыше 15%, но в некоторых регионах достигает 93%. По данным сероэпидемиологических исследований, от 2 до 14% обследованных практически здоровых лиц в различных очагах токсокароза имеют положительные иммунологические реакции на токсокароз
Основным источником инвазии для человека являются собаки, особенно щенки. Заражение происходит при непосредственном контакте с инвазированным животным, шерсть которого загрязнена инвазионными яйцами, или при попадании в рот земли, в которой были яйца токсокар. Особенно подвержены заражению дети во время игры в песке или с собакой. Наибольший риск заражения у детей, страдающих геофагией. Взрослые заражаются при бытовом контакте с инвазированными животными или в процессе профессиональной деятельности (ветеринары, собаководы, работники коммунальной службы, шоферы, землекопы и др.). У человека возможно заражение также при поедании сырого или плохо обработанного термически мяса паратенических хозяев. Описаны случаи заражения токсокарозом при употреблении в пищу печени ягненка. Не исключается возможность трансплацентарной и трансмаммарной передачи инвазии и у человека.
Патогенез и патологическая анатомия
Патогенез токсокароза сложный и определяется комплексом механизмов в системе паразит — хозяин. В период миграции личинки травмируют кровеносные сосуды и ткани, вызывая геморрагии, некроз, воспалительные изменения. Ведущая роль принадлежит иммунологическим реакциям организма в ответ на инвазию. Экскреторно-секреторные антигены личинок оказывают сенсибилизирующее действие с развитием реакций немедленного и замедленного типов. При разрушении личинок в организм человека попадают соматические антигены личинок. Аллергические реакции проявляются отеками, кожной эритемой, увеличением резистентности дыхательных путей к вдыхаемому воздуху, что клинически выражается развитием приступов удушья. В аллергических реакциях принимают участие тучные клетки, базофилы, нейтрофилы, но основную роль играют эозинофилы. Пролиферация эозинофилов регулируется Т-лимфоцитами при участии медиаторов воспалительных реакций, выделяемых сенсибилизированными лимфоцитами, нейтрофилами, базофилами. Образующиеся иммунные комплексы привлекают в очаг поражения эозинофилы. Вокруг личинок токсокар кумулируются сенсибилизированные Т-лимфоциты, привлекаются макрофаги и другие клетки — формируется паразитарная гранулома.
Патоморфологическим субстратом токсокароза является выраженное в различной степени гранулематозное поражение тканей. При интенсивной инвазии развиваются тяжелые гранулематозные поражения многих органов и систем, которые при повторных заражениях могут стать хроническими. При токсокарозе находят многочисленные гранулемы в печени, легких, поджелудочной железе, миокарде, лимфатических узлах, головном мозге и других органах.
Клиническая картина токсокароза
Наиболее характерным лабораторным показателем является повышенное содержание эозинофилов в периферической крови. Относительный уровень эозинофилии может колебаться в широких пределах, достигая в ряде случаев 70 — 80% и более. Повышается содержание лейкоцитов (от 20х109 до 30х109 на 1 л). При исследовании пунктата костного мозга выявляется гиперплазия зрелых эозинофилов. У детей нередко отмечается умеренная анемия. Некоторые исследователи отмечают прямую корреляцию между тяжестью клинических проявлений инвазии и уровнем эозинофилии и гиперлейкоцитоза периферической крови. Характерным лабораторным признаком является также ускорение СОЭ, гипергаммаглобулинемия. В случаях поражения печени наблюдается повышение билирубина, гиперферментемия.
В хронической стадии болезни острые клинические и лабораторные признаки затухают. Наиболее стабильным лабораторным показателем остается гиперэозинофилия периферической крови.
Выделяют субклиническое, легкое, среднетяжелое и тяжелое течение токсокароза. Возможна так называемая бессимптомная эозинофилия крови, когда явные клинические проявления инвазии отсутствуют, но наряду с гиперэозинофилией выявляются антитела к антигенам T.canis.
Одной из наиболее серьезных проблем, связанных с токсокарозом, является его взаимосвязь с бронхиальной астмой. При сероэпидемиологических исследованиях установлено, что у больных бронхиальной астмой нередко обнаруживаются антитела к антигенам T.canis классов Ig G и Ig E. В зависимости от остроты паразитарного процесса, его длительности и длительности клинических проявлений бронхиальной астмы преобладает тот или другой класс иммуноглобулинов. Имеются клинические наблюдения, свидетельствующие об улучшении течения бронхиальной астмы или выздоровлении после ликвидации токсокарозной инвазии.
Паразитологический диагноз устанавливается редко и только по наличию в тканях характерных гранулем и личинок и их идентификации при исследовании биопсийного и секционного материала. Это возможно при пункционной биопсии печени, легких, оперативном вмешательстве. Обычно диагноз токсокароза устанавливается на основании данных эпидемиологического анамнеза, клинической симптоматики и гематологических проявлений. Используют также иммунологические реакции, позволяющие выявлять антитела к антигенам токсокар. Обычно применяют ИФА с секреторно-экскреторным антигеном личинок токсокар второго возраста. В настоящее время в России выпускается коммерческий диагностикум. Диагностическим титром считают титр антител 1:400 и выше (в ИФА). Титр антител 1:400 свидетельствует об инвазированности, но не болезни. Титр антител 1:800 и выше свидетельствует о заболевании токсокарозом. Практика показывает, что прямая корреляция между уровнем антител и тяжестью клинических проявлений токсокароза существует не всегда. Не всегда имеется и корреляция между уровнем антител и гиперэозинофилии крови.
При постановке диагноза и определении показаний к специфической терапии следует учитывать, что токсокароз протекает циклически с рецидивами и ремиссиями, в связи с чем возможны значительные колебания клинических, гематологических и иммунологических показателей у одного и того же больного.
М. И. Алексеева и соавт. (1984) разработали алгоритм диагностики токсокароза, основанный на оценках в баллах значимости клинических симптомов и сопоставлении клинико-эпидемиологических и лабораторных показателей. Этот метод может быть перспективен при проведении массовых обследований населения.
Дифференциальный диагноз проводят с миграционной стадией других гельминтозов (аскаридоз, описторхоз), стронгилоидозом, эозинофильной гранулемой, лимфогранулематозом, эозинофильным васкулитом, метастазирующей аденомой поджелудочной железы, гипернефромой и другими заболеваниями, сопровождающимися повышенным содержанием эозинофилов в периферической крови. Следует иметь в виду, что у больных с системными лимфопролиферативными заболеваниями и серьезными нарушениями в системе иммунитета иммунологические реакции могут быть ложно положительными. В этих случаях необходим тщательный анализ клинической картины заболевания.
При интенсивной инвазии развиваются тяжелые гранулематозные поражения многих органов и систем, которые при повторных заражениях могут стать хроническими
Глазной токсокароз. Патогенез этой формы токсокароза до конца не ясен. Существует гипотеза об избирательном поражении глаз у лиц с инвазией низкой интенсивности, при которой не развивается достаточно выраженная иммунная реакция организма из-за слабого антигенного воздействия небольшого числа поступивших в организм личинок токсокар.
Эта форма токсокароза чаще наблюдается у детей и подростков, хотя описаны случаи заболевания и у взрослых.
Для токсокароза характерно одностороннее поражение глаз. Патологический процесс развивается в сетчатке, поражается хрусталик, иногда параорбитальная клетчатка. В тканях глаза формируется воспалительная реакция гранулематозного характера. Патологический процесс часто принимают за ретинобластому, проводят энуклеацию глаза. При морфологическом исследовании обнаруживают эозинофильные гранулемы, иногда — личинки токсокар.
Клинически поражение глаз протекает как хронический эндофтальмит, хориоретинит, иридоциклит, кератит, папиллит. Глазной токсокароз — одна из частых причин потери зрения.
Диагностика глазного токсокароза сложна. Количество эозинофилов обычно нормальное или незначительно повышено. Специфические антитела не выявляются или выявляются в низких титрах.
Разработано недостаточно. Применяют противонематодозные препараты — тиабендазол (минтезол), мебендазол (вермокс), медамин, диэтилкарбамазин. Эти препараты эффективны в отношении мигрирующих личинок и недостаточно эффективны в отношении тканевых форм, находящихся в гранулемах внутренних органов.
Минтезол (тиабендазол) назначают в дозах 25—50 мг/кг массы тела в сутки в три приема в течение 5—10 дней. Побочные явления возникают часто и проявляются тошнотой, головной болью, болями в животе, чувством отвращения к препарату (в настоящее время препарат в аптечную сеть России не поступает).
Вермокс (мебендазол) назначают по 200 —300 мг в сутки в течение 1—4 недель. Побочные реакции обычно не наблюдаются.
Медамин применяют в дозе 10 мг/кг массы тела в сутки повторными циклами по 10 — 14 дней.
Диэтилкарбамазин назначают в дозах 2 — 6 мг/кг массы тела в сутки в течение 2 — 4 недель. (В настоящее время препарат в России не производится, не закупается за рубежом. — Прим. ред.)
Альбендазол назначают в дозе 10 мг/кг массы тела в сутки в два приема (утро — вечер) в течение 7 — 14 дней. В процессе лечения необходим контроль анализа крови (возможность развития агранулоцитоза) и уровня аминотрансфераз (гепатотоксическое действие препарата). Небольшое повышение уровня аминотрансфераз не является показанием к отмене препарата. В случае нарастающей гиперферментемии и угрозы развития токсического гепатита требуется отмена препарата.
Критерии эффективности лечения: улучшение общего состояния, постепенная регрессия клинических симптомов, снижение уровня эозинофилии и титров специфических антител. Следует отметить, что клинический эффект лечения опережает положительную динамику гематологических и иммунологических изменений. При рецидивах клинической симптоматики, стойкой эозинофилии и положительных иммунологических реакциях проводят повторные курсы лечения.
Прогноз для жизни благоприятный, однако при массивной инвазии и тяжелых полиорганных поражениях, особенно у лиц с нарушениями иммунитета, возможен летальный исход.
Включает соблюдение личной гигиены, обучение детей санитарным навыкам.
Важным профилактическим мероприятием является своевременное обследование и дегельминтизация собак. Наиболее эффективно преимагинальное лечение щенков в возрасте 4 — 5 недель, а также беременных сук. Для лечения собак используют противонематодозные препараты. Необходимо ограничение численности безнадзорных собак, оборудование специальных площадок для выгула собак.
Следует улучшить санитарно-просветительскую работу среди населения, давать информацию о возможных источниках инвазии и путях ее передачи. Особого внимания требуют лица, по роду деятельности имеющие контакты с источниками инвазии (ветеринарные работники, собаководы, землекопы и другие).
Читайте также:

