Дифференциальная диагностика лейшманиоз кожный
Обновлено: 19.04.2024
Лепра — хроническая генерализованная гранулематозная инфекция с преимущественным поражением кожи, периферической нервной системы, глаз и некоторых внутренних органов.
Частота • В настоящее время в мире насчитывают около 2 млн больных, преимущественно в развивающихся странах • Чаще регистрируют у мужчин (2:1) • Случаи заболевания у детей до 1 года крайне редки.
Этиология. Возбудитель — кислотоустойчивая бактерия Mycobacterium leprae (палочка Хансена–Найссера).
Генетические аспекты. У лиц с гаплотипами HLA-DR2 или HLA-DR3 чаще наблюдают туберкулоидную форму, а у лиц с гаплотипом HLA-DR2-DQW1 — лепроматозную; последняя составляет 30–50% поражений в странах Индокитая и в Японии, но лишь 10% в Африке.
Эпидемиология • Заболевание малоконтагиозно, что делает невозможным выявить в каждом конкретном случае путь заражения и источник инфекции • Единственный резервуар — больной человек • Заражение происходит при непосредственных контактах, а также воздушно-капельным путём • Доказана возможность внутриутробного заражения, но дети, изолированные от больных родителей после рождения, не заболевают.
Факторы риска • Тесный бытовой контакт, например, в семьях, где есть больные • Иммунодефицитные состояния • Низкий социально-экономический статус.
Патоморфология • Туберкулоидная лепра — неказеозные гранулёмы, состоящие из лимфоцитов, эпителиоидных клеток, а также гигантских клеток; микобактерии обнаруживают редко • Лепроматозная лепра — гранулёмы организованы макрофагами, большими пенистыми клетками (клетки Вирхова), в клетках обнаруживают много микобактерий, часто окружённых сферическими массами • Пограничная лепра — состав гранулём варьирует от преобладания эпителиоидных клеток при погранично-туберкулоидной к доминированию макрофагов при пограничной лепроматозной лепре.
Классификация и клиническая картина
• Недифференцированная лепра может трансформироваться в лепроматозный или туберкулоидный тип. Характерны кожные высыпания и поражение периферических нервных стволов. Высыпания имеют вид чётко ограниченных пятен разной окраски и размеров; после короткого периода повышенной чувствительности становятся нечувствительными. Моно- и полиневриты часто сопровождают неравномерные утолщения и уплотнения нервных стволов. Встречают у пациентов с неустойчивой резистентностью. Диагноз устанавливают по факту контакта с больными лепрой в анамнезе. Кожные поражения часто самопроизвольно заживают. Однако возможно прогрессирование в более тяжёлые формы.
• Туберкулоидная лепра. Начинается с появления слабопигментированных пятен с чёткими краями и пониженной чувствительностью. Характерны разрастания грануляционной ткани в коже и слизистых, часто наблюдают один очаг, являющийся иногда единственным проявлением болезни. Зрелые туберкулоидные лепромы асимметричны, чувствительность отсутствует полностью, края приподняты над поверхностью кожи, центр лепромы атрофичен. Вокруг поражённых участков снижено количество потовых желёз и волосяных фолликулов. В патологический процесс рано вовлекаются периферические нервы. При полярной туберкулоидной форме число очагов поражений не превышает 1–3, они обычно симметричны и характеризуются выраженной анестезией. При пограничной туберкулоидной форме число очагов значительно больше, они асимметричны, анестезия выражена несколько меньше; часто наблюдают невриты локтевого, срединного, лицевого, ушного и др. нервов. Поражение лицевого нерва приводит к развитию лагофтальма, кератита и изъязвления роговицы. Атрофия мускулатуры начинается с мелких мышц кисти; позднее возможны контрактуры верхних и нижних конечностей. При бактериальных суперинфекциях наблюдают инфекционные поражения рук и посттравматические язвы на подошвах. Возможна резорбция костей, приводящая к укорочению фаланг. В клинических образцах возбудители малочисленны, их трудно обнаружить. Эту форму лепры наблюдают у лиц с нормальной резистентностью. Возможны случаи спонтанного излечения.
• Пограничная (диморфная) лепра. Кожные поражения ещё более многообразны, папулы и бляшки могут сочетаться с пятнами. Снижение чувствительности менее выражено, чем при туберкулоидной лепре. Отмечают истончение мочек ушей, гипертрофию носа и надбровных дуг. Поражения кожи более многочисленны, но не симметричны, как при лепроматозной лепре. Включает проявления как туберкулоидного, так и лепроматозного типов в различных сочетаниях. Заболевание подразделяют на погранично-туберкулоидную, собственно пограничную и погранично-лепроматозную лепру. Пограничные формы нестабильны, могут регрессировать в туберкулоидную и прогрессировать в лепроматозную формы. Эти процессы определяются эффективностью лечения и состоянием иммунного статуса пациента.
Лабораторные исследования • Обнаружение Mycobacterium leprae в соскобах слизистой оболочки носовой перегородки, поражённых участков кожи и биопсийном материале увеличенных лимфатических узлов; мазки окрашивают по Цилю–Нильсену • При сомнительных результатах — биопроба на морских свинках (чувствительны к Mycobacterium tuberculosis и резистентны к Mycobacterium leprae) • Лепроминовая проба всегда отрицательная при лепроматозной форме; её используют для дифференциального диагноза туберкулоидной формы • Анализ крови — незначительная анемия, увеличение СОЭ и гиперглобулинемия • Серодиагностика: выявление АТ к гликолипиду-1 клеточной стенки, экстрагированному фенолом; чувствительность метода — более 90% при лепроматозной форме и около 30% при туберкулоидной форме.
Дифференциальная диагностика • СКВ • Обыкновенная волчанка • Саркоидоз • Фрамбезия • Кожный лейшманиоз • Другие заболевания кожи • Периферическая невропатия • Сирингомиелия.
ЛЕЧЕНИЕ
Тактика ведения • Регулярные консультации ортопеда, хирурга, офтальмолога и терапевта • Ношение правильно подобранной обуви и использование пластырных повязок предотвращают появление язв на подошвах • Формирование контрактур верхних конечностей можно предотвратить с помощью физических упражнений и наложения повязок • При поражении глаз срочно проводят соответствующую коррекцию • При прогрессировании или развитии узловатой лепроматозной эритемы рекомендованы постельный режим, анальгетики и седативные средства • В тяжёлых случаях применяют ГК • Специфическую терапию можно проводить непрерывно.
Хирургическое лечение. Показаны реконструктивные вмешательства — трансплантации нервов и сухожилий, устранение контрактур и другие операции, улучшающие функциональные возможности и социальную адаптацию.
Лекарственная терапия
• Препараты выбора •• Дапсон 100 мг/сут и рифампицин 600 мг/сут •• При пограничной, погранично-лепроматозной и лепроматозной лепре дополнительно — этионамид 250–500 мг/сут.
• Продолжительность лекарственной терапии •• Недифференцированная и туберкулоидная лепра — дапсон 3 года, рифампицин 6 мес •• Погранично-туберкулоидная лепра — дапсон 5 лет, рифампицин 6 мес •• Пограничная лепра — дапсон 10 лет, рифампицин 2 года, клофамизин 10 лет, этионамид 10 лет •• Погранично-лепроматозная лепра и лепроматозная лепра — дапсон всю жизнь, рифампицин 2 года, этионамид всю жизнь.
Осложнения • Деформация конечностей • Укорочение фаланг пальцев вследствие травмы с вторичным инфицированием • Слепота • Артериит • Вторичный амилоидоз • Узловатая лепрозная эритема.
Течение и прогноз • Инкубационный период заболевания длится необычайно долго — в среднем 4–6 лет, нередко затягивается до 10–15 лет и более • Продромальные явления часто отсутствуют • Течение нестабильное • Прогноз благоприятный при ранней диагностике и соответствующем лечении.
Профилактика • Соблюдение элементарных санитарно-гигиенических норм • Пациента не обязательно помещать в лепрозорий.
Синонимы • Болезнь Хансена • Гансеноз • Проказа.
МКБ-10 • A30 Лепра [болезнь Гансена]
Примечание. Лепроминовая проба (реакция Мицуды) — внутрикожная аллергическая проба с лепромином с последующей оценкой местной реакции, развивающейся через 2–4 нед; используют для определения типа лепры и с целью прогнозирования
Код вставки на сайт
Лепра — хроническая генерализованная гранулематозная инфекция с преимущественным поражением кожи, периферической нервной системы, глаз и некоторых внутренних органов.
Частота • В настоящее время в мире насчитывают около 2 млн больных, преимущественно в развивающихся странах • Чаще регистрируют у мужчин (2:1) • Случаи заболевания у детей до 1 года крайне редки.
Этиология. Возбудитель — кислотоустойчивая бактерия Mycobacterium leprae (палочка Хансена–Найссера).
Генетические аспекты. У лиц с гаплотипами HLA-DR2 или HLA-DR3 чаще наблюдают туберкулоидную форму, а у лиц с гаплотипом HLA-DR2-DQW1 — лепроматозную; последняя составляет 30–50% поражений в странах Индокитая и в Японии, но лишь 10% в Африке.
Эпидемиология • Заболевание малоконтагиозно, что делает невозможным выявить в каждом конкретном случае путь заражения и источник инфекции • Единственный резервуар — больной человек • Заражение происходит при непосредственных контактах, а также воздушно-капельным путём • Доказана возможность внутриутробного заражения, но дети, изолированные от больных родителей после рождения, не заболевают.
Факторы риска • Тесный бытовой контакт, например, в семьях, где есть больные • Иммунодефицитные состояния • Низкий социально-экономический статус.
Патоморфология • Туберкулоидная лепра — неказеозные гранулёмы, состоящие из лимфоцитов, эпителиоидных клеток, а также гигантских клеток; микобактерии обнаруживают редко • Лепроматозная лепра — гранулёмы организованы макрофагами, большими пенистыми клетками (клетки Вирхова), в клетках обнаруживают много микобактерий, часто окружённых сферическими массами • Пограничная лепра — состав гранулём варьирует от преобладания эпителиоидных клеток при погранично-туберкулоидной к доминированию макрофагов при пограничной лепроматозной лепре.
Классификация и клиническая картина
• Недифференцированная лепра может трансформироваться в лепроматозный или туберкулоидный тип. Характерны кожные высыпания и поражение периферических нервных стволов. Высыпания имеют вид чётко ограниченных пятен разной окраски и размеров; после короткого периода повышенной чувствительности становятся нечувствительными. Моно- и полиневриты часто сопровождают неравномерные утолщения и уплотнения нервных стволов. Встречают у пациентов с неустойчивой резистентностью. Диагноз устанавливают по факту контакта с больными лепрой в анамнезе. Кожные поражения часто самопроизвольно заживают. Однако возможно прогрессирование в более тяжёлые формы.
• Туберкулоидная лепра. Начинается с появления слабопигментированных пятен с чёткими краями и пониженной чувствительностью. Характерны разрастания грануляционной ткани в коже и слизистых, часто наблюдают один очаг, являющийся иногда единственным проявлением болезни. Зрелые туберкулоидные лепромы асимметричны, чувствительность отсутствует полностью, края приподняты над поверхностью кожи, центр лепромы атрофичен. Вокруг поражённых участков снижено количество потовых желёз и волосяных фолликулов. В патологический процесс рано вовлекаются периферические нервы. При полярной туберкулоидной форме число очагов поражений не превышает 1–3, они обычно симметричны и характеризуются выраженной анестезией. При пограничной туберкулоидной форме число очагов значительно больше, они асимметричны, анестезия выражена несколько меньше; часто наблюдают невриты локтевого, срединного, лицевого, ушного и др. нервов. Поражение лицевого нерва приводит к развитию лагофтальма, кератита и изъязвления роговицы. Атрофия мускулатуры начинается с мелких мышц кисти; позднее возможны контрактуры верхних и нижних конечностей. При бактериальных суперинфекциях наблюдают инфекционные поражения рук и посттравматические язвы на подошвах. Возможна резорбция костей, приводящая к укорочению фаланг. В клинических образцах возбудители малочисленны, их трудно обнаружить. Эту форму лепры наблюдают у лиц с нормальной резистентностью. Возможны случаи спонтанного излечения.
• Пограничная (диморфная) лепра. Кожные поражения ещё более многообразны, папулы и бляшки могут сочетаться с пятнами. Снижение чувствительности менее выражено, чем при туберкулоидной лепре. Отмечают истончение мочек ушей, гипертрофию носа и надбровных дуг. Поражения кожи более многочисленны, но не симметричны, как при лепроматозной лепре. Включает проявления как туберкулоидного, так и лепроматозного типов в различных сочетаниях. Заболевание подразделяют на погранично-туберкулоидную, собственно пограничную и погранично-лепроматозную лепру. Пограничные формы нестабильны, могут регрессировать в туберкулоидную и прогрессировать в лепроматозную формы. Эти процессы определяются эффективностью лечения и состоянием иммунного статуса пациента.
Лабораторные исследования • Обнаружение Mycobacterium leprae в соскобах слизистой оболочки носовой перегородки, поражённых участков кожи и биопсийном материале увеличенных лимфатических узлов; мазки окрашивают по Цилю–Нильсену • При сомнительных результатах — биопроба на морских свинках (чувствительны к Mycobacterium tuberculosis и резистентны к Mycobacterium leprae) • Лепроминовая проба всегда отрицательная при лепроматозной форме; её используют для дифференциального диагноза туберкулоидной формы • Анализ крови — незначительная анемия, увеличение СОЭ и гиперглобулинемия • Серодиагностика: выявление АТ к гликолипиду-1 клеточной стенки, экстрагированному фенолом; чувствительность метода — более 90% при лепроматозной форме и около 30% при туберкулоидной форме.
Дифференциальная диагностика • СКВ • Обыкновенная волчанка • Саркоидоз • Фрамбезия • Кожный лейшманиоз • Другие заболевания кожи • Периферическая невропатия • Сирингомиелия.
ЛЕЧЕНИЕ
Тактика ведения • Регулярные консультации ортопеда, хирурга, офтальмолога и терапевта • Ношение правильно подобранной обуви и использование пластырных повязок предотвращают появление язв на подошвах • Формирование контрактур верхних конечностей можно предотвратить с помощью физических упражнений и наложения повязок • При поражении глаз срочно проводят соответствующую коррекцию • При прогрессировании или развитии узловатой лепроматозной эритемы рекомендованы постельный режим, анальгетики и седативные средства • В тяжёлых случаях применяют ГК • Специфическую терапию можно проводить непрерывно.
Хирургическое лечение. Показаны реконструктивные вмешательства — трансплантации нервов и сухожилий, устранение контрактур и другие операции, улучшающие функциональные возможности и социальную адаптацию.
Лекарственная терапия
• Препараты выбора •• Дапсон 100 мг/сут и рифампицин 600 мг/сут •• При пограничной, погранично-лепроматозной и лепроматозной лепре дополнительно — этионамид 250–500 мг/сут.
• Продолжительность лекарственной терапии •• Недифференцированная и туберкулоидная лепра — дапсон 3 года, рифампицин 6 мес •• Погранично-туберкулоидная лепра — дапсон 5 лет, рифампицин 6 мес •• Пограничная лепра — дапсон 10 лет, рифампицин 2 года, клофамизин 10 лет, этионамид 10 лет •• Погранично-лепроматозная лепра и лепроматозная лепра — дапсон всю жизнь, рифампицин 2 года, этионамид всю жизнь.
Осложнения • Деформация конечностей • Укорочение фаланг пальцев вследствие травмы с вторичным инфицированием • Слепота • Артериит • Вторичный амилоидоз • Узловатая лепрозная эритема.
Течение и прогноз • Инкубационный период заболевания длится необычайно долго — в среднем 4–6 лет, нередко затягивается до 10–15 лет и более • Продромальные явления часто отсутствуют • Течение нестабильное • Прогноз благоприятный при ранней диагностике и соответствующем лечении.
Профилактика • Соблюдение элементарных санитарно-гигиенических норм • Пациента не обязательно помещать в лепрозорий.
Синонимы • Болезнь Хансена • Гансеноз • Проказа.
МКБ-10 • A30 Лепра [болезнь Гансена]
Примечание. Лепроминовая проба (реакция Мицуды) — внутрикожная аллергическая проба с лепромином с последующей оценкой местной реакции, развивающейся через 2–4 нед; используют для определения типа лепры и с целью прогнозирования
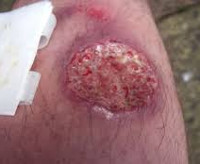
Кожный лейшманиоз – это инфекционная болезнь, вызываемая простейшими и сопровождающаяся поражением кожных покровов, реже слизистых оболочек. Характерным признаком являются язвы на месте внедрения возбудителя. Температурная реакция организма варьируется в широких пределах, другие признаки заболевания выявляются очень редко. Диагностика базируется на обнаружении возбудителя и антител к нему. Лечение проводится с помощью этиотропных препаратов и симптоматических мероприятий. В некоторых случаях необходимо хирургическое вмешательство, криодеструкция или лазеротерапия.
МКБ-10
Общие сведения
Кожный лейшманиоз (болезнь Боровского) представляет собой инфекцию, передающуюся преимущественно трансмиссивным путем. Эта болезнь известна с древности, впервые была описана английским врачом Пококом в 1745 году. Более полную клиническую характеристику нозологии дал русский хирург Боровский в 1898 году. Сам возбудитель – лейшмания – обязан своим названием английскому патологу Лейшману, который в 1903 году описал этого простейшего практически параллельно с итальянским исследователем Донованом. Патология распространена в тропических странах, сезонность связана с активностью переносчиков – с мая по ноябрь.

Причины
Возбудитель инфекции – паразит Leishmania, относящийся к простейшим. Самыми распространенными видами являются L. tropica, L. major, L. aethiopica, L. infantum, L. mexicana, L. amazonensis, L. braziliensis. Резервуарами паразитов в природе служат москиты, енотовидные собаки, ленивцы, грызуны, лисы и дикобразы. Основным способом заражения является трансмиссивный путь, реализуемый с помощью переносчиков – москитов, реже песчаных мух.
Микроорганизм нуждается в смене двух хозяев для размножения, при этом безжгутиковая фаза развития проходит в организме людей либо животных, а жгутиковая – в пищеварительном тракте самки москита. При укусе переносчик срыгивает в ранку лейшманий, которые внедряются в толщу кожи. Другие пути инфицирования (вертикальный, при гемотрансфузиях и оперативных вмешательствах) встречаются редко. Группами риска по кожному лейшманиозу являются дети, сельские жители, путешественники, ВИЧ-инфицированные лица и онкологические больные. Чаще всего заболевают молодые мужчины и пожилые женщины.
Патогенез
После проникновения в толщу дермы лейшмании поглощаются макрофагами, внутри которых могут размножаться. Для контроля репликации возбудителя в организме CD8 + Т-лимфоциты в большом количестве продуцируют фактор некроза опухоли и интерферон гамма, с помощью которых пораженные клетки кожи и макрофаги начинают индуцировать производство собственных микробицидных эффекторов, способных уничтожать лейшманий. CD8 + -лимфоциты играют значительную роль в патогенезе болезни – они активно уничтожают пораженные клетки, но не действуют на самих внутриклеточных паразитов.
Роль В-лимфоцитов изучается; ряд исследований показали возможность длительной персистенции заболевания из-за стимуляции В-лимфоцитами CD4 + -клеток и возникновения избыточной продукции как провоспалительных, так и регуляторных цитокинов. При гистологическом исследовании обнаруживаются воспалительные инфильтраты переменной интенсивности с диффузным или очаговым распределением, характеризующиеся преобладанием лимфоцитов, гистиоцитов и плазматических клеток с зонами спонгиоза, паракератоза и псевдоэпителиоматозной гиперплазии. В области поражения определяются язвы, очаговая зона некроза и хорошо организованные гранулемы.
Классификация
Кожный лейшманиоз может быть распространенным (диффузным) либо локализованным. Реже встречается кожно-слизистая форма болезни (эспундия), при которой происходит поражение слизистых оболочек рта и носоглотки. В отдельных случаях в процесс вовлекаются дыхательные пути, в частности – гортань. При этом варианте течения возникает обезображивание и деформация лица, возможна гибель от дыхательной недостаточности. Сохраняется деление болезни на городской и сельский лейшманиоз – считается, что при первом типе течение язвенного процесса медленнее, чем при втором, а заражение происходит из-за больных собак и грызунов соответственно.
Симптомы кожного лейшманиоза
Инкубационный период городской формы патологии длится от 10 суток до года, чаще – 3-5 месяцев; для сельского варианта время инкубации может сокращаться до 1-8 недель. Начало болезни постепенное, с лихорадкой до 38°C. Острый дебют характерен для маленьких детей и ВИЧ-позитивных пациентов, часто приводит к кожно-висцеральному поражению и гибели. На месте укуса москита появляется бурого цвета бугорок, который постепенно вырастает до 2-х и более сантиметров, покрывается мелкими чешуйками (лейшманиома). Затем образование продолжает свой рост и через полгода изъязвляется с появлением характерного слизисто-гнойного отделяемого. Заживление язвы завершается образованием рубца.
Сельская форма болезни протекает гораздо быстрее и агрессивнее: лейшманиомы практически сразу переходят в язвенную стадию с формированием дочерних бугорков, через 2-4 месяца дно язвы начинает напоминать рыбью икру и центробежно заживать с появлением рубцового дефекта. Лимфатические сосуды воспаляются, пальпируются в виде твердых узлов-бусин, часть из которых вскрывается. После перенесенного городского кожного варианта в редких случаях отмечается хроническое течение процесса с образованием небольших бугорков около рубца, которые не изъязвляются и могут персистировать всю жизнь человека.
Осложнения
Наиболее частыми осложнениями несвоевременно диагностированного кожного лейшманиоза являются участки гиперпигментации и рубцы на месте лейшманиом. Помимо косметического дефекта рубцовые изменения могут приводить к инвалидности (особенно при расположении на слизистых). Реже встречаются кровотечения, вызванные расплавлением сосуда на дне язвы, и вторичные гнойные процессы. При длительном течении, обширном поражении, коморбидной патологии возможно формирование хронической венозной недостаточности, лимфостаза и рецидивирующей рожи. При вовлечении надгортанника может наблюдаться ложный круп.
Диагностика
Диагноз кожной формы лейшманиоза верифицируется инфекционистом, по показаниям назначаются консультации других специалистов. Обязательным является тщательный сбор эпидемиологического анамнеза на предмет пребывания в тропических зонах. В ходе диагностического поиска применяются следующие инструментальные и лабораторные методики:
Лечение кожного лейшманиоза
Пациенты с кожными формами болезни не нуждаются в стационарном лечении. Постельный режим показан при выраженной лихорадке, болевом синдроме и гнойных осложнениях. Специальная диета не разработана, из-за возможных лекарственных побочных эффектов рекомендуется отказаться от приема алкоголя, наркотических средств и никотина, исключить на время лечения трудноперевариваемую пищу (жирное, жареное, маринады). Показана местная антисептическая обработка язв, полоскание рта и промывание носовых ходов при расположении очагов на слизистых, применение стерильных повязок с ежедневной сменой.
Специфическое антипротозойное лечение осуществляется с учетом вида возбудителя преимущественно препаратами пятивалентной сурьмы (натрия стибоглюконата). Возможно использование милтефозина, пентакарината, липосомального амфотерицина В. Системное применение этих средств сопряжено с риском развития побочных эффектов, поэтому в настоящее время ведется изучение местных медикаментов (кремы, мази) в качестве дополнения к основной терапии. Симптоматическое лечение подразумевает прием жаропонижающих, обезболивающих, дезинтоксикационных и других препаратов. При резистентности лейшманиоза проводится спленэктомия.
Местное лечение лейшманиозных кожных язв неразрывно связано с тепловым воздействием, поскольку возбудители крайне чувствительны к высоким температурам. Среди подобных методов терапии распространена радиочастотная, преимущество которой заключается в отсутствии повреждения здоровой кожи в процессе применения. Используется фотодинамическая и прямая электрическая терапия, инфракрасная стимуляция, лазеролечение. Существуют описания единичных случаев полного излечения от кожного лейшманиоза с помощью местных методик как монотерапии нозологии у ВИЧ-позитивных и иных иммуносупрессивных пациентов.
Прогноз и профилактика
Прогноз при кожном лейшманиозе при отсутствии осложнений обычно благоприятный. До 85% случаев болезни заканчиваются выздоровлением; для заболевания характерно циклическое течение и естественная реконвалесценция. Летальных случаев лейшманиоза данного вида не зафиксировано. Среди ВИЧ-инфицированных и других лиц с иммунным дефицитом даже слабопатогенные штаммы лейшманий могут вызывать висцеральную патологию. Продолжительность неосложненного сельского типа лейшманиоза кожи составляет не более 3-6 месяцев, городского – до 2 лет. Лечение продолжается в течение 20-30 дней, допускается проведение терапии сроком до двух месяцев.
Специфическая профилактика показана всем выезжающим в эндемичные зоны, рекомендуется проводить вакцинацию в зимне-осенний сезон и не позднее 3-х месяцев до планируемой поездки. Главным средством неспецифической профилактики является борьба с переносчиками: осушение подвалов и овощехранилищ, инсектицидная обработка, использование репеллентов. Важна своевременная диагностика, изоляция и лечение больных, установка в палатах противомоскитных сеток. Рекомендуется плановая вакцинация домашних собак, борьба с городскими свалками, дератизация и отстрел больных диких животных.
1. Борьба с лейшманиозом. Доклад на заседании комитета экспертов ВОЗ по борьбе с лейшманиозом/ Серия технических докладов ВОЗ №949 – 2010.
3. Cutaneous Manifestations of Human and Murine Leishmaniasis / Breanna M. Scorza, Edgar M. Carvalho, Mary E. Wilson / International Journal Molecular Sciences – 2017 - №18.
4. Diagnosis, Treatment and Clinical Features of Cutaneous Leishmaniasis in Saudi Arabia / Yousry A. Hawash, Khadiga A. Ismail, Maha M. Abdel-Wahab, Mahmoud Khalifa // The Korean Journal of Parasitology.
Лейшманиоз представляет собой протозойную инфекцию с трансмиссивным механизмом распространения, характеризующуюся поражением кожных покровов или внутренних органов внутриклеточными паразитами – лейшманиями. Лейшманиозы подразделяют на висциральные, протекающие с поражением легких, печени, селезенки, сердца, и кожные, проявляющиеся трансформирующимися в очаги изъязвления папулами. Диагностика лейшманиоза осуществляется путем выявления лейшманий в крови пациента (при висцеральной форме) или в отделяемом кожных элементов (при кожной форме).
Общие сведения
Лейшманиоз представляет собой протозойную инфекцию с трансмиссивным механизмом распространения, характеризующуюся поражением кожных покровов или внутренних органов внутриклеточными паразитами – лейшманиями.
Характеристика возбудителя
Лейшманиоз вызываются семнадцатью из более чем двадцати видов простейших паразитов рода Leishmania. Лейшмании развиваются внутри клеток хозяина (преимущественно в макрофагах и элементах ретикулоэндотелиальной системы). В течение своего жизненного цикла им необходимо сменить двух хозяев. В организме позвоночных животных лейшмании находятся в безжгутиковой форме, развиваясь в жгутиковую форму в теле членистоногого. Лейшмании отличаются резистентностью к антибиотикам, и чувствительны к препаратам пятивалентной сурьмы.
Подавляющее большинство лейшманиозов – зоонозы (резервуаром и источником инфекции являются животные), только два вида – антропонозы. Виды животных, участвующих в распространении лейшманиоза, довольно ограничены, поэтому инфекция является природно-очаговой, распространяется в пределах обитания соответствующей фауны: грызунов песчаниковых видов, псовых (лисы, собаки, шакалы), а также переносчиков – москитов. Преимущественно очаги лейшманиоза располагаются в странах Африки и Южной Америки. Большинство из них - развивающиеся, среди 69 стран, где распространен лейшманиоз, 13 являются беднейшими странами мира.
Человек является источником инфекции в случае поражения кожной формой лейшмании, при этом москиты получают возбудителя с отделяемым кожных язв. Висцеральная лейшмания в подавляющем большинстве случаев является зоонозной, москиты заражаются от больных животных. Заразность москитов отсчитывается с пятого дня попадания лейшманий в желудок насекомого и сохраняется пожизненно. Человек и животные контагиозны в течение всего срока пребывания возбудителя в организме.
Лейшманиоз передается исключительно с помощью трансмиссивного механизма, переносчики – москиты, получают инфекцию, питаясь кровью больных животных, и переносят здоровым особям и людям. Человек обладает высокой восприимчивостью к инфекции, после перенесения кожного лейшманиоза сохраняется продолжительный стойкий иммунитет, висцеральная форма такового не формирует.
Патогенез
Возбудитель проникает в толщу кожи человека при укусе москита, формируя в области входных ворот лейшманиозную гранулему. Впоследствии, при висцеральной форме инфекции гранулема рассасывается, а при кожной - прогрессирует в язву. Лейшмании разносятся по организму с током лимфы, поражая регионарные лимфатические узлы. Вдоль лимфатического сосуда паразиты могут формировать лейшманиомы – ряд последовательно располагающихся специфических язв.
В Южной Америке отмечаются формы лейшмании, протекающие с поражением слизистых оболочек ротовой полости, носоглотки и верхних дыхательных путей с грубой деформацией глубоких тканей и развитием полипозных образований. Висцеральная форма лейшманиоза развивается в результате рассеивания возбудителя по организму и попадания в печень, селезенку, костный мозг. Реже – в кишечную стенку, легкие, почки и надпочечники.
Возникающий иммунный ответ подавляет инфекцию, при этом заболевание протекает латентно, либо с маловыраженной симптоматикой. При иммунодефиците, сниженных защитных свойствах лейшманиоз прогрессирует, протекает с выраженной клиникой интоксикационного синдрома, лихорадкой. Размножение паразитов в печени способствуют замещению гепатоцитов фиброзной тканью, в селезенке отмечают атрофию пульпы с участками инфарктов и некротизации. Вследствие поражения костного мозга развивается анемия. В целом висцеральный лейшманиоз, прогрессируя, вызывает общую кахексию.
Классификация
Лейшманиозы подразделяются на висцеральные и кожные формы, каждая форма, в свою очередь, разделяется на антропонозы и зоонозы (в зависимости от резервуара инфекции). Висцеральные зоонозные лейшманиозы: детский кала-азар (средиземноморско-среднеазиатский), лихорадка дум-дум (распространена в восточной Африке), носоглоточный лейшманиоз (кожно-слизистый, лейшманиоз Нового Света).
Индийский кала-азар является висцеральным антропонозом. Кожные формы лейшманиоза представлены болезнью Боровского (городской антропонозный тип и сельский зооноз), пендинской, ашхабадской язвами, багдадским фурункулом, эфиопским кожным лейшманиозом.
Симптомы лейшманиоза
Висцеральный средиземноморско-азиатский лейшманиоз
Инкубационный период этой формы лейшманиоза составляет от 20 дней до нескольких (3-5) месяцев. Иногда (довольно редко) затягивается до года. У детей раннего возраста в этот период может отмечаться первичная папула в месте внедрения возбудителя (у взрослых встречается в редких случаях). Инфекция протекает в острой, подострой и хронической формах. Острая форма обычно отмечается у детей, характеризуется бурным течением и без должной медицинской помощи заканчивается летально.
Чаще всего встречается подострая форма заболевания. В начальном периоде отмечается постепенное нарастание общей слабости, разбитости, повышенной утомляемости. Отмечается снижение аппетита, побледнение кожи. В этом периоде при пальпации можно выявить некоторое увеличение размеров селезенки. Температура тела может подниматься до субфебрильных цифр.
Подъем температуры до высоких значений говорит о вступлении заболевания в период разгара. Лихорадка имеет неправильный или волнообразный характер, продолжается в течение нескольких дней. Приступы лихорадки могут сменяться периодами нормализации температуры или снижения до субфебрильных значений. Такое течение обычно продолжается 2-3 месяца. Лимфатические узлы увеличены, отмечается гепато- и, в особенности, спленомегалия. Печень и селезенка при пальпации умеренно болезненны. При развитии бронхоаденита отмечается кашель. При такой форме нередко присоединяется вторичная инфекция дыхательной системы и развивается пневмония.
С прогрессированием заболевания отмечается усугубление тяжести состояния больного, развивается кахексия, анемия, геморрагический синдром. На слизистых оболочках ротовой полости возникают некротизированные участки. Ввиду значительного увеличения селезенки происходит смещение сердца вправо, тоны его глухие, ритм сокращений ускорен. Отмечается склонность к падению периферического артериального давления. С прогрессированием инфекции формируется сердечная недостаточность. В терминальном периоде больные кахексичны, кожные покровы бледные и истонченные, отмечаются отеки, выражена анемия.
Хронический лейшманиоз протекает латентно, либо с незначительной симптоматикой. Антропонозный висцеральный лейшманиоз может сопровождаться (в 10% случаев) появлением на коже лейшманоидов – мелких папиллом, узелков или пятен (иногда просто участки со сниженной пигментацией), содержащих возбудителя. Лейшманоиды могут существовать годами и десятилетиями.
Кожный зоонозный лейшманиоз (болезнь Боровского)
Распространен в тропическом и субтропическом климате. Инкубационный период его составляет 10-20 дней, может сокращаться до недели и удлиняться до полутора месяцев. В области внедрения возбудителя при этой форме инфекции обычно формируется первичная лейшманиома, первоначально имеющая вид розовой гладкой папулы около 2-3 см в диаметре, в дальнейшем прогрессирующей в безболезненный или малоболезненный при надавливании фурункул. Спустя 1-2 недели в лейшманиоме формируется некротический очаг, и вскоре образуется безболезненное изъязвление с подрытыми краями, окруженное валиком инфильтрированной кожи с обильным отделяемым серозно-гнойного или геморрагического характера.
Диффузно-инфильтрирующий лейшманиоз
Отличается значительной распространенной инфильтрацией кожи. Со временем инфильтрат регрессирует, не оставляя последствий. В исключительных случаях отмечаются мелкие язвы, заживающие без заметных рубцов. Такая форма лейшманиоза достаточно редка, обычно отмечается у пожилых лиц.
Туберкулоидный кожный лейшманиоз
Наблюдается в основном у детей и молодых людей. При этой форме вокруг послеязвенных рубцов или на них появляются мелкие бугорки, могущие увеличиваться в размерах и сливаться друг с другом. Изъязвляются такие бугорки редко. Язвы при этой форме инфекции оставляют значительные рубцы.
Антропонозная форма кожного лейшманиоза
Характеризуется продолжительным инкубационным периодом, который может достигать нескольких месяцев и лет, а также медленным развитием и умеренной интенсивностью кожных поражений.
Осложнения лейшманиоза
Длительно протекающий лейшманиоз прогрессирует с развитием пневмонии, нефритов, агранулоцитоза, геморрагического диатеза, а также может осложняться гнойно-некротическими воспалениями.
Диагностика лейшманиоза
Общий анализ крови при лейшманиозе показывает признаки гипохромной анемии, нейтропении и анэозинофилии при относительном лимфоцитозе, а также пониженную концентрацию тромбоцитов. СОЭ повышена. Биохимический анализ крови может показать гипергаммаглобулинемию. Выделение возбудителя кожного лейшманиоза возможно из бугорков и язв, при висцеральном - лейшмании обнаруживаются в посеве крови на стерильность. При необходимости для выделения возбудителя производят биопсию лимфоузлов, селезенки, печени.
В качестве специфической диагностики осуществляют микроскопическое исследование, бакпосев на питательной среде NNN, биопробы на лабораторных животных. Серологическая диагностика лейшманиоза проводится с применением РСК, ИФА, РНИФ, РЛА. В периоде реконвалесценции отмечается позитивная реакция Монтенегро (кожная проба с лейшманином). Производится при эпидемиологических исследованиях.
Лечение лейшманиоза
Этиологическое лечение лейшманиоза заключается в применении препаратов пятивалентной сурьмы. При висцеральной форме их назначают внутривенно с нарастанием дозировки на 7-10 дней. В случае недостаточной эффективности терапию дополняют амфотерицином В, вводимым с 5% раствором глюкозы внутривенно медленно. На ранних стадиях кожного лейшманиоза бугорки обкалывают мономицином, сульфатом берберина или уротропином, а также назначают эти препараты в виде мазей и примочек.
Сформировавшиеся язвы являются показанием к назначению мирамистина внутримышечно. Для ускорения заживления язв эффективна лазерная терапия. Препаратами резерва при лейшманиозе являются амфотерицин В и пентамидин, их назначают в случаях рецидивирования инфекции и при резистентности лейшманий к традиционным средствам. Для повышения эффективности терапии можно добавить человеческий рекомбинантный гаммаинтерферон. В некоторых случаях бывает необходимо хирургическое удаление селезенки.
Прогноз и профилактика лейшманиоза
При легко протекающем лейшманиозе возможно самостоятельное выздоровление. Благоприятен прогноз при своевременном выявлении и должных медицинских мерах. Тяжелые формы, инфицирование лиц с ослабленными защитными свойствами, отсутствие лечения значительно ухудшают прогноз. Кожные проявления лейшманиоза оставляют косметические дефекты.
Профилактика лейшманиоза включает меры по благоустройству населенных пунктов, ликвидацию мест расселения москитов (свалок и пустырей, затопленных подвальных помещений), дезинсекцию жилых помещений. Индивидуальная профилактика заключается в использовании репеллентов, других средств защиты от укусов москитов. При обнаружении больного производят химиопрофилактику пириметамином в коллективе. Специфическая иммунная профилактика (вакцинация) производится лицам, планирующим посещение эпидемически опасных районов, а также неимунному населению очагов инфекции.
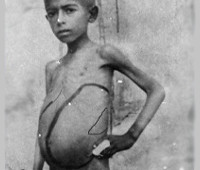
Висцеральный лейшманиоз – это хроническое инфекционное протозойное заболевание с поражением печени и селезенки, развитием анемии и кахексии. Другими симптомами являются лихорадка, увеличение лимфоузлов, кожные проявления. Диагностика включает выявление возбудителя из крови и биоптатов внутренних органов, реже путем биопроб на грызунах, поиск антител к возбудителю. Лечение состоит из курса этиотропных препаратов (преимущественно пятивалентной сурьмы) и коррекции органных дисфункций в качестве симптоматической терапии. В некоторых случаях показаны гемотрансфузии.
МКБ-10
Общие сведения
Висцеральный лейшманиоз (лихорадка дум-дум, кала-азар, черная лихорадка) принадлежит к трансмиссивным инфекциям, вызываемым простейшими. В 1903 году английский патолог Лейшман совместно с итальянским ученым Донованом описал морфологию органных поражений и выделил возбудителя. В честь исследователей инфекционный агент получил своё название Leishmania donovani. Болезнь наиболее распространена в тропических и субтропических странах, сезонный рост заболеваемости зависит от особенностей жизненного цикла переносчика и приходится на период с мая по ноябрь.

Причины
Возбудитель инфекции – простейший паразитический микроорганизм лейшмания. Источниками и резервуарами инфекции служат теплокровные дикие и домашние животные (грызуны, ленивцы, лисы, собаки), люди. Путь инфицирования преимущественно трансмиссивный, переносчики – самки москитов рода Phlebotomus. Имеются данные о единичных случаях заражения при переливаниях крови, передачи лейшманий от матери плоду, при использовании нестерильного медицинского инструментария и игл во время внутривенного введения наркотических средств.
В своем развитии лейшманиям необходимо пройти две стадии: безжгутиковую и жгутиковую в организме человека либо животного и переносчика соответственно. Амастиготы обитают внутри клеток, лишены способности к перемещению, промастиготы имеют жгутики для активных движений в пространстве. Находясь внутри самки москита, лейшмании активно размножаются в пищеварительном канале насекомого, после чего перемещаются к хоботку. Наиболее подвержены заражению дети до 5 лет, молодые мужчины, сельскохозяйственные работники, туристы, пациенты с ВИЧ-инфекцией, онкопатологиями.
Патогенез
В месте укуса переносчика формируется первичный аффект в виде гранулемы, которая состоит из макрофагов с размножающимися внутри лейшманиями, ретикулоцитов, эпителиоцитов и гигантских клеток. Через некоторое время гранулема подвергается обратному развитию, реже рубцеванию, а находящиеся в макрофагах возбудители с током лимфы и крови попадают во внутренние органы. При нормальном состоянии иммунной системы происходит разрушение пораженных клеток. В случае иммунодефицита лейшмании размножаются с увеличенной скоростью, поражают паренхиматозные органы.
Это приводит к возникновению воспалительных изменений, активному фиброзированию и увеличению размеров органов. В печеночной ткани при патогистологическом исследовании обнаруживаются участки интерлобулярного фиброза и дистрофия гепатоцитов, в лимфатических узлах – дистрофические изменения зародышевого центра и аплазия костного мозга, в селезенке – атрофия пульпы, зоны инфарктов, некроза и геморрагических инфильтратов. При длительном течении висцерального лейшманиоза возникает амилоидоз внутренних органов.
Классификация
Разделение висцерального лейшманиоза на сельский и городской виды подразумевает разные источники инфекции (домашние и дикие животные), а также тяжесть течения патологии – считается, что при городском типе болезнь протекает доброкачественнее. Выделяют острый, подострый и хронический варианты органного лейшманиоза. Наиболее благоприятным течением отличается хроническая форма, острый тип данной протозойной инфекции чаще всего встречается у детей, характеризуется бурным развитием симптомов и нередкими летальными исходами. Для подострого варианта типично наличие осложнений.
Симптомы висцерального лейшманиоза
Инкубационный период составляет от 20 дней до 1 года, чаще 3-5 месяцев. Для манифестации болезни характерно постепенное начало, появление кожной папулы бледно-розового цвета на месте внедрения возбудителя, сменяющейся участком депигментации (лейшманоид). Отмечается слабость, беспричинная усталость, снижение аппетита, похудание. В дальнейшем присоединяется лихорадка до 39-40° C, которая протекает с чередованием высокой и нормальной температуры тела на продолжении нескольких месяцев.
Наблюдается безболезненное увеличение всех групп лимфатических узлов, изменение их консистенции до плотно-эластической. Пациенты с висцеральным лейшманиозом почти всегда отмечают тяжесть и дискомфорт в подреберьях. При прогрессировании болезни наблюдается гепатоспленомегалия с появлением отеков и увеличением живота. Снижается количество выделяемой мочи. В связи с развитием гиперспленизма и поражения костного мозга возникают кровотечения. Обнаруживается одышка, язвенно-некротические поражения ротовой полости, бледность кожи, нарушения дефекации.
Осложнения
Наиболее частые осложнения (тромбогеморрагический синдром, гранулоцитопения, агранулоцитоз) связаны с поражением кроветворной системы, следствием чего является некроз миндалин, слизистой рта и десен (нома). Отечно-асцитический синдром при висцеральном лейшманиозе возникает из-за вовлечения печени, сопровождается хронической сердечной недостаточностью, нарушениями в работе ЖКТ (энтероколитом), нефритом, снижением либидо, олиго- и аменореей. Характерны случаи бактериальной пневмонии ввиду высокого стояния диафрагмы и снижения дыхательной емкости легких. К редким осложнениям относят разрывы селезенки, геморрагический шок, ДВС-синдром.
Диагностика
Определение висцеральной формы лейшманиоза требует осмотра инфекциониста, по показаниям назначаются консультации других специалистов. Важно уточнить у пациента факт пребывания в эндемичных зонах земного шара в течение предшествующих пяти лет, наличие вакцинации от лейшманиоза, род профессиональных занятий. Лабораторные и инструментальные методы верификации болезни включают в себя:
- Физикальное исследование. Во время объективного осмотра обращает на себя внимание бледность, сухость, истончение кожи, наличие язв в полости рта. Лимфоузлы плотные, увеличенные, безболезненные. При аускультации тоны сердца приглушены, выслушивается тахикардия, шумы, в легких могут определяться участки ослабленного дыхания. Пальпация живота безболезненна, размеры селезенки и печени резко увеличены. Часто обнаруживаются периферические отеки, асцит.
- Лабораторные исследования. Признаками лейшманиоза в общем анализе крови служат анемия, пойкилоцитоз, анизоцитоз, лейкопения, нейтропения, анэозинофилия, тромбоцитопения, резкое ускорение СОЭ. Биохимические параметры изменены в сторону повышения АЛТ, АСТ, СРБ, креатинина и мочевины, гипоальбуминемии. Наблюдается увеличение времени свертывания крови. В общеклиническом анализе мочи отмечается повышение плотности мочевого осадка, протеинурия, гематурия.
- Выявление инфекционных агентов. Для обнаружения лейшманий проводится микроскопия, посев биологических препаратов и крови, реже биопробы на хомячках. Серологическая диагностика (ИФА) направлена на выявление противолейшманиозных антител. Использование внутрикожной пробы Монтенегро является косвенным методом подтверждения диагноза в период реконвалесценции, применяется при эпидемиологических исследованиях в популяции.
- Инструментальные методики. Рентгенография ОГК выполняется для исключения пневмонии, туберкулезного поражения. Сонография брюшной полости визуализирует увеличение размеров печени, селезенки, признаки портальной гипертензии, наличие асцита. УЗИ и биопсию лимфатических узлов, стернальную пункцию, трепанобиопсию костного мозга, диагностическую торакоскопию и лапароскопию осуществляют по показаниям.
Туберкулез проявляется длительным субфебрилитетом, редко сухим кашлем и симптомами дисфункции вовлеченных в патологический процесс органов; часто диагноз верифицируется только лабораторно-инструментальными методиками. Схожесть клинических симптомов заболевания наблюдается с такими патологиями, как лейкоз и лимфогранулематоз, при данных патологиях диагностическими критериями становятся данные анализов крови и биопсии костного мозга. Сепсис клинически протекает схоже, но обычно имеет первичный очаг поражения (рана, гнойное образование и др.).
Лечение висцерального лейшманиоза
Пациенты с данным заболеванием госпитализируются в стационар. В обязательном порядке необходимо ограничить возможность контакта с москитами, поэтому над кроватями и в оконных проемах устанавливают противомоскитные сетки. Постельный режим показан до устойчивых нормальных цифр температуры тела в течение 3-5 дней, из-за риска разрыва селезенки при её значительном увеличении не рекомендуются резкие наклоны, повороты, поднятие тяжестей более 10 кг. Режим питания предусматривает высококалорийную, богатую белками пищу, водная нагрузка подбирается индивидуально.
Этиотропная терапия висцерального лейшманиоза должна включать препараты сурьмы (натрия стибоглюконат) либо пентамидин, милтефозин, липосомальный амфотерицин В. Некоторые исследования показали эффективность терапевтического приема производных пятивалентной сурьмы в сочетании с сульфатом паромомицина, при этом сокращается длительность курса лечения. Пациентам с осложнениями, ВИЧ-инфекцией, тяжелыми сопутствующими болезнями рекомендовано курсовое введение амфотерицина В как первой линии лечения висцерального лейшманиоза.
Выраженная анемия является показанием для эритроцитарных гемотрансфузий, реже требуется введение тромбомассы и донорских лейкоцитов. Коррекция анемии заключается в длительном приеме препаратов железа, по показаниям – колониестимулирующих факторов. Симптоматическое лечение предполагает дезинтоксикацию, прием жаропонижающих средств (аспирин – с осторожностью), антибиотиков в случае присоединения вторичных инфекций. Важной составляющей лечения является борьба с отеками, в числе прочего в план терапии включаются мочегонные средства и растворы альбумина.
Прогноз и профилактика
Прогноз при ранней диагностике благоприятный за исключением случаев болезни у ВИЧ-инфицированных пациентов – у данной категории больных даже слабопатогенные штаммы лейшманий вызывают органные поражения. Продолжительность лечения составляет 14-30 дней, наблюдение за реконвалесцентами занимает 4-6 месяцев из-за возможных рецидивов лейшманиоза. У 17% пролеченных пациентов в течение 5 лет после выздоровления могут обнаруживаться симптомы посткала-азарного дермального лейшманиоза, протоколы диагностики и лечения для которого окончательно не разработаны.
Специфическая профилактика заключается в плановом введении живой вакцины, рекомендована лицам, проживающим или планирующим длительное либо кратковременное пребывание на эндемичных территориях, туристам. Введение препарата необходимо осуществлять зимой или осенью минимум за три месяца до поездки. Неспецифические меры предотвращения висцерального лейшманиоза включают своевременное выявление, изоляцию и лечение больных, использование противомоскитных сеток, вакцинацию собак, устранение свалок, меры дезинсекции и дератизации. Борьба с москитами заключается, в том числе, в осушении болот, подвалов и овощехранилищ.
4. A Treatment outcomes of visceral leishmaniasis in Ethiopia from 2001 to 2017: a systematic review and meta-analysis / Eyob Alemayehu Gebreyohannes, Akshaya Srikanth Bhagvathula, Tadesse Melaku Abegaz// Infect Dis Poverty – 2018 - №7.

Кожный лейшманиоз Старого Света – это эндемическое протозойное трансмиссивное заболевание, вызываемое внутриклеточными паразитами рода Leishmania и передаваемое москитами, которое характеризуется образованием некротизирующихся узлов в местах укусов, заживающих с рубцеванием.
Синонимы
leishmaniosis; болезнь Боровского, кожный лейшманиоз, ашхабадская язва, пендинская язва, кокандка. Выделяют следующие клинические формы кожного лейшманиоза Старого Света: - антропонозный кожный лейшманиоз (городской, сухой или поздно-изъязвляющийся); - туберкулоидный кожный лейшманиоз – разновидность антропонозного; - зоонозный кожный лейшманиоз (сельский, влажный или остро- некротизирующийся)
Эпидемиология
Возраст: любой.
Пол: не имеет значения.
Анамнез
На открытых участках тела (лицо, шея, верхние конечности) спустя 0,5−8 месяцев (при антропонозном лейшманиозе через 2−8 месяцев, а при зоонозном в срок до 2-х месяцев) на месте укуса москита появляется бугорок (лейшманиома), трансформирующийся в дальнейшем в специфический узел (инфильтрат) буровато− или ярко−красного цвета. Узел через некоторое время изъязвляется и впоследствии заживает с образованием рубца. При туберкулоидной форме на месте рубца после перенесённого антропонозного лейшманиоза возникают мелкие бугорки буровато-красного цвета, крайне резистентные к терапии. Длительность заболевания составляет в среднем 3-4 месяца (при зоонозном), около одного года (при антропонозном) и несколько лет при туберкулоидном кожном лейшманиозе Старого Света.
Течение
постепенное начало с последующим самостоятельным разрешением высыпаний в сроки от 3-4 месяцев до нескольких лет.
Этиология
Впервые возбудителя кожного лейшманиоза Старого Света открыл в 1897 году выпускник Военно-медицинской академии военный врач П.Ф. Боровский в Ташкенте. Кожный лейшманиоз является преимущественно зоонозной инфекцией домашних и диких животных (тушканчиков, сусликов, песчанок) и реже – антропонозной, при которой первичным резервуаром инфекции является больной человек. Только около 20% видов лейшманий (наиболее часто - Leishmania tropica minor и Leishmania tropica major) являются патогенными для человека, передача возбудителя происходит при укусе разных видов москитов рода Phlebotomus. Лейшмании размножаются в пищеварительном тракте москитов и накапливаются в хоботке, откуда при укусе попадают в кожу человека.
Предрасполагающие факторы
Вероятные провоцирующие факторы:
- климато-географические (проживание (пребывание) в определенных регионах мира): Южной Европе (Испания, Португалия, юг Франции, Италия, Греция, Болгария, западная часть Турции, Мальта); Западной Азии (Абхазия, юг России, Азербайджан, Армения, Грузия, Южная Осетия, Турция, Кипр, Ирак, Иран, Афганистан); Юго-Западной Азии (Йемен, Саудовская Аравия, ОАЭ, Катар, Бахрейн, Оман, Кувейт, Сирия, Иордания, Ливан, Израиль); Южной Азии (Бангладеш, Бутан, Индия, Мальдивы, Непал, Пакистан, Шри-Ланка); Средней Азии (Туркмения, Узбекистан, Казахстан, Таджикистан, Киргизия)
- укусы москитов
- кожный лейшманиоз у членов семьи
- ношение открытой одежды
Жалобы
Болезненные высыпания, изъязвление и отёк кожи, увеличение регионарных лимфоузлов.
Дерматологический статус
процесс поражения кожи носит распространенный или ограниченный характер, элементы сыпи, как правило, не группируются, иногда могут образовывать очаги (инфильтраты) неправильных (полицикличных) очертаний
Элементы сыпи на коже
- бугорки с плоской или полушаровидной поверхностью бурого или буровато-красного цвета до 0,5 см в диаметре, мягкой консистенции, дающие при боковом освещении своеобразный блеск, иногда шелушащиеся по всей поверхности. Симптом яблочного желе (появление центрально расположенных пятнышек желтовато-коричневого цвета (цвета яблочного желе) при надавливании на бугорок прозрачным стеклом) - положительный. В дальнейшем бугорки существуют без изменений или трансформируются в специфический узел (инфильтрат);
- специфические узлы бурого, синюшно-красного или красного цвета размерами более 1 см в диаметре, плотно-эластической консистенции, возвышающиеся над поверхностью кожи (полушаровидной, конусообразной или плоской формы), малоподвижные, с гладкой или бугристой (напоминает апельсиновую кожуру) поверхностью. Узлы могут увеличиваться в размерах, превращаясь в инфильтрат, в дальнейшем некротизируются в центральной части и изъязвляются;
- болезненные язвы до 5 см в диаметре, имеющие кратерообразный (реже – неровный) край. Дно язвы, вначале гнойное или с некротическим распадом, потом – с зернистыми грануляциями (напоминающими рыбью икру). Язвы располагаются на поверхности узлов (инфильтратов), существуют несколько месяцев, впоследствии заживают с образованием мозаичных рубцов;
- корки бурого цвета на поверхности язв;
- нормо- или атрофические сплошные или мозаичные (звездчатые) рубцы перламутрово-белого или коричневатого (пигментиролванные) цвета на месте язв;
Элементы сыпи на слизистых
Придатки кожи
в месте локализации язв развивается рубцовая алопеция.
Локализация
любая − наиболее часто поражаются открытые участки тела (лицо, уши, предплечья, кисти, голени, лодыжки).
Дифференциальный диагноз
Зоонозный и антропонозный кожный лейшманиоз необходимо дифференцировать с укусами насекомых, импетиго, фурункулом, карбункулом, эктимой, сибирской язвой, гранулемой купальщиков, туберкулезом кожи, третичным сифилисом (гуммозным). Туберкулоидный кожный лейшманиоз − с туберкулезной волчанкой, проказой, саркоидозом, гранулемой лица с эозинофилией, лимфоцитарной инфильтрацией Джейсснера, доброкачественной лимфоплазией кожи, обыкновенными угрями, люпоидной розацеа, келоидными рубцами.
Сопутствующие заболевания
Диагноз
Основан на данных Анамнеза (пребывание эндемичном по кожному лейшманиозу регионе), клинической картине заболевания и положительных результатах микроскопии отделяемого с поверхности лейшманиом, иногда прибегают к гистологическому исследованию.
Патогенез
В своем жизненном цикле лейшмании проходят две стадии – промастиготы и амастиготы. В кишечнике москитов и в культуре лейшмании существуют в виде промастигот – веретенообразных, снабженных жгутиком микроорганизмов длиной 10-15 мкм (внеклеточная форма). Попадая при укусе москита в кожу, лейшмании фагоцитируются клетками ретикулоэндотелиальной системы млекопитающих и человека (клетками Лангерганса и гистиоцитами), внутри которых превращаются в безжгутиковых круглых или овальных амастигот длиной 2-4 мкм (внутриклеточная форма). Фагоцитоз оказывается незавершённым, что приводит к активации системы фагоцитирующих мононуклеаров с развитием гранулёматозного воспаления. Спустя 1-5 недель в месте укуса при зоонозном и 2-8 месяцев при антропонозном кожном лейшманиозе возникает гранулёма (лейшманиома), которая проходит ряд последовательных стадий бугорок – специфический узел (инфильтрат) − язва − рубец. Из первичных кожных очагов лейшмании могут распространяться лимфогенно, вызывая лимфангииты и лимфадениты регионарных лимфатических узлов, а также появление бугорков обсеменения на коже. Приобретенный Т-клеточный иммунитет определяет клиническое течение лейшманиоза (он протекает по Th1-типу, сопровождаясь выработкой γ-интерферона и окиси азота, которые уничтожают лейшманий в макрофагах). Гуморальный иммунитет при кожном лейшманиозе не формируется. Заболевание приводит к развитию стойкого, практически пожизненного, иммунитета, повторные заболевания наблюдаются редко.
Читайте также:

