Дифференциальная диагностика лептоспироза и пастереллеза
Обновлено: 19.04.2024
Пастереллез (геморрагическая септицемия) - острая инфекционная болезнь, характеризующаяся лихорадкой, общей интоксикацией, воспалением кожи, подкожной клетчатки, артритами, остеомиелитами. Относится к зоонозам.
Что провоцирует / Причины Пастереллеза:
Возбудитель - Pasleurella multocida - короткая овоидная палочка (длиной 0,3-1,5 мкм и шириной 0,15-0,25 мкм) грамотрицательна, неподвижная, хорошо растет на обычных питательных средах. Отмечается биполярность при окраске по Романовскому-Гимзе. Микроб не очень устойчив во внешней среде, погибает при нагревании, под влиянием ультрафиолетовых лучей, под влиянием дезинфицирующих препаратов. В земле и навозе микроб сохраняется 3-4 дня. Выделяют 4 серотипа пастереллы (А, В, D и Е); некоторые из них имеют подтипы. Возбудитель способен вырабатывать экзотоксин.
Эпидемиология. Заболевания встречаются относительно редко. До 1955 г. было описано всего 95 случаев пастереллеза человека, с 1955 по 1963 гг. наблюдался еще 21 случай, в последующие годы по 1-5 заболеваний. Источником инфекции являются многие виды животных (крупный и мелкий рогатый скот, кошки, собаки, кролики, свиньи, зайцы, крысы, птицы и др.). Чаще всего пастереллез возникает после укусов кошек и собак, а также после царапин, нанесенных кошками (бактерионосительство у кошек достигает 80%). Некоторые авторы допускают возможность алиментарного заражения и трансмиссивной передачи инфекции, однако нет конкретных доказательств, которые бы подтверждали такой механизм передачи инфекции. Случаев заражения человека от человека не наблюдалось. Однако описан случай передачи инфекции от матери плоду, что обусловило преждевременные роды, развитие сепсиса у ребенка и его гибель. У матери из эндометрия выделена культура пастереллы.
Патогенез (что происходит?) во время Пастереллеза:
Воротами инфекции являются чаще кожные покровы в месте укуса или царапины, нанесенные животным (сами животные остаются здоровыми). Допускается возможность проникновения возбудителя через слизистые оболочки. На месте поврежденной кожи развиваются воспалительные изменения. В некоторых случаях наблюдается гематогенное распространение возбудителей с формированием вторичных очагов в различных органах (легкие, мозг, суставы и др.). Септические формы могут сопровождаться развитием инфекционно-токсического шока и тромбогеморрагического синдрома.
Симптомы Пастереллеза:
Инкубационный период длится от 1 до 5 дней. В литературе описано три группы пастереллеза. В первой группе основными проявлениями были местные воспалительные изменения в области ворот инфекции (укуса или царапины кошек, собак), иногда дополнительно выявляются артриты и остеомиелиты, у больных второй группы основными проявлениями являются хронически протекающие воспалительные изменения легких. Третья группа характеризуется гематогенной диссеминацией возбудителя, поражением многих органов (менингиты, абсцессы мозга, гнойные артриты, синуситы, эндокардит, пиелонефриты, мастоидиты и пр.) и очень тяжелым течением.
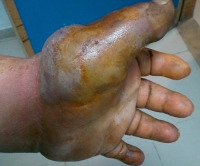
При кожной форме пастереллеза на месте внедрения возбудителя появляется вначале припухлость и покраснение кожи, болезненность при пальпации. Вскоре на этом месте образуются пустулы, заполненные мутным содержимым, после разрушения пузыря образуется струп. Воспалительный процесс может захватить и более глубокие отделы, может развиться флегмона или более ограниченные абсцессы. Иногда процесс переходит на кость, обусловливая развитие артрита или остеомиелита. Во время развития воспалительных изменений, ограниченных только кожей и подкожной клетчаткой, общее состояние больных остается удовлетворительным, температура тела остается субфебрильной, отсутствуют выраженные признаки общей интоксикации.
Хроническое течение легочных проявлений может быть обусловлено или только пастереллой, или ее сочетанием с вторичной инфекцией другими бактериальными агентами. Заболевание протекает по типу хронического бронхита, иногда с развитием бронхэктазов или в виде вяло текущей интерстициальной пневмонии. Поражение легких может развиваться и при септической форме, в этих случаях возможны абсцессы легкого, эмпиема.
Септическая форма протекает наиболее тяжело, сопровождается высокой лихорадкой, температурная кривая неправильного типа с большими суточными размахами. Появляются вторичные очаги в различных органах (эндокардит, абсцессы мозга, гнойный менингит, гнойные артриты и др.). Может развиться инфекционно-токсический шок.
Диагностика Пастереллеза:
При распознавании пастереллеза прежде всего учитывают эпидемиологические факторы. Большинство описанных случаев связано с укусами собак и особенно кошек (укусы и царапины), реже укусы других животных (описан случай пастереллеза даже после укуса льва), меньшее значение имеют контакты с другими животными. Из клинических проявлений наиболее информативным является появление выраженных воспалительных изменений в области ворот инфекции (более тяжелые формы также чаще начинаются с кожных воспалительных изменений). Для подтверждения диагноза необходимо выделение возбудителя (из отделяемого кожных язв, крови, гноя абсцессов, цереброспинальной жидкости). Серологические реакции имеют вспомогательное значение.
Лечение Пастереллеза:
Профилактика Пастереллеза:
К каким докторам следует обращаться если у Вас Пастереллез:
Вас что-то беспокоит? Вы хотите узнать более детальную информацию о Пастереллеза, ее причинах, симптомах, методах лечения и профилактики, ходе течения болезни и соблюдении диеты после нее? Или же Вам необходим осмотр? Вы можете записаться на прием к доктору .
Пастереллез – острое зоонозное инфекционное заболевание бактериального генеза. Протекает с вовлечением кожи, подкожной клетчатки, суставов и костей. Состояние проявляется высокой лихорадкой, выраженной интоксикацией, поражением внутренних органов; описаны случаи хронического течения. Диагностика патологии проводится преимущественно бактериологическими методами, в качестве вспомогательных применяются серологические методики. Лечение пастереллеза включает этиотропную антибактериальную терапию, дезинтоксикационные, жаропонижающие и другие симптоматические средства.
МКБ-10
Общие сведения
Пастереллез (геморрагическая септицемия) относится к инфекциям с контактным механизмом передачи. Впервые нозология была описана в 1878 году. Бактериальная природа возбудителя была установлена в 1880 году Луи Пастером, в честь которого и была названа данная инфекционная патология. Пастереллез распространен повсеместно, четкой сезонности у людей не имеет, заболеваемость преимущественно спорадическая. Группами риска считаются сельскохозяйственные работники, ветеринары, лица пожилого возраста, больные сахарным диабетом, циррозом печени, ХОБЛ, ВИЧ-инфекцией в стадии СПИДа, патологиями сердечно-сосудистой системы и злокачественными новообразованиями, а также пациенты, проходящие гемодиализ. Считается, что пастереллезу наиболее подвержены люди в возрасте 10-19 лет, заболевание чаще регистрируется среди женщин.

Причины
Возбудителем инфекции является бактерия Pasteurella multocida, продуцирующая экзотоксин. Пастереллы устойчивы в окружающей среде, до 2-3 недель сохраняются в воде и навозе, до 4-12 месяцев – в трупах животных и замороженном мясе. Погибают при воздействии солнечного света, кипячении, обработке дезинфицирующими средствами. Источниками инфекции становятся бактерионосители и больные сельскохозяйственные, домашние животные и птицы. Чаще всего пастереллез регистрируется у крупного рогатого скота, кур, кроликов и буйволов, при этом пастереллоносительство отмечается у 80% кошек, 70% коров, 50% овец и кроликов, 45% овец, 35% куриц в неблагополучных хозяйствах. Пастереллы выделяются с калом, мочой, носовым отделяемым, кровью, молоком животного, заражение человека обычно происходит при укусах и оцарапывании кожи кошками и собаками. Описаны воздушно-капельный и трансплацентарный пути инфицирования; предполагается возможность трансмиссивной передачи пастереллеза при укусах зараженных слепней.
Патогенез
При попадании бактерий через поврежденные кожу и слизистые образуется первичный очаг воспаления. Активное размножение пастерелл, выделение экзотоксина и продукты жизнедеятельности микробов провоцируют скопление иммунокомпетентных клеток, развитие гнойного процесса, тромбозы мелких сосудов, отек. Проникновение инфекционных агентов вглубь дермы и подлежащих тканей приводит к распространению процесса на кости и суставы, возникновению артритов и остеомиелита. Гематогенная диссеминация пастерелл наблюдается при вовлечении стенок кровеносных сосудов и проникновении возбудителей в системный кровоток. При попадании в кровь большого количества экзотоксина, продуктов распада бактерий и иммунных клеток возможно развитие инфекционно-токсического шока. Во внутренних органах пастереллы продолжают активно размножаться, нарушая структуру клеток и тканей, что приводит к критическим функциональным расстройствам.
Классификация
Пастереллез протекает остро или хронически. Обычно изменения локализуются в пределах входных ворот инфекции либо приобретают вид вялотекущего воспалительного гнойного процесса. Гематогенное распространение возбудителя возможно только при истощении защитных сил организма. В основе классификации лежит степень инвазивности патологии:
- Кожная форма. Самая распространенная разновидность болезни. Представляет собой гнойное поражение кожи на месте укуса, ослюнения либо царапины, других повреждений кожных покровов, оставленных больным животным, с тенденцией к распространению вглубь подлежащих тканей.
- Легочная форма. При аэрогенном механизме заражения может возникать первично, но чаще является следствием гематогенной диссеминации возбудителя. Клиническая картина обусловлена воспалением стенки бронхов, поражением альвеолярного дерева и соединительной ткани.
- Септическая форма. Жизнеугрожающее состояние, при котором происходит контаминация организма с массивной бактериемией. В пораженных органах развиваются дисфункциональные изменения вплоть до полного прекращения деятельности.
Симптомы пастереллеза
При недостаточном иммунном ресурсе организма возбудитель распространяется по организму с формированием висцеральных гнойных очагов. Лихорадка усиливается, приобретает волнообразный характер. Нарастают признаки интоксикации, Отмечается сильная головная боль, нарушения или изменения сознания, возможны судороги и параличи. Нередко возникает шок, сопровождающийся резким снижением артериального давления, потерей сознания, отсутствием мочевыделения, иногда – спонтанными кровотечениями.
Осложнения
Наиболее частыми осложнениями пастереллеза являются гнойные поражения кожи, мышц, подкожной клетчатки (абсцессы, флегмоны), суставов и сухожильно-связочного аппарата (бурситы, тендовагиниты, артриты), костных структур (остеомиелиты). Хронические бронхоэктазы приводят к амилоидозу внутренних органов. Возможна септикопиемия с формированием гнойных очагов в различных органах, тромбогеморрагические проявления, инфекционно-токсический шок. Описаны единичные случаи фульминантной пурпуры с высокой летальностью. В исходе гнойных артритов (особенно – поражения коленного сустава) нередко наблюдается нарушение функции, обуславливающее необходимость эндопротезирования.
Диагностика
Диагноз устанавливается инфекционистом. В зависимости от имеющейся симптоматики могут потребоваться консультации терапевта, дерматовенеролога, хирурга. При поражении респираторного тракта необходим осмотр пульмонолога, фтизиатра, при наличии жизнеугрожающих состояний – реаниматолога. Перечень диагностических мероприятий включает следующие объективные, лабораторные и инструментальные методики:
- Физикальное исследование. В очаге поражения при кожной форме обнаруживается участок гиперемии, резкая болезненность, отек кожи, пустула с мутным содержимым, струп, нередко определяется флюктуация. При поражении суставов отмечается увеличение их размеров, ограничение движений, вынужденное положение конечности. Интерстициальная пневмония при аускультации проявляется жестким дыханием, крепитацией, укорочением перкуторного звука. При бронхоэктазах наблюдается диффузное ослабление легочного дыхания с обилием влажных хрипов, уменьшающихся при откашливании.
- Лабораторные исследования. В общем анализе крови при пастереллезе выявляется лейкоцитоз с палочкоядерным сдвигом влево, увеличение СОЭ, нередко – тромбоцитопения, анемия. Изменения в биохимических показателях включают повышение АЛТ, АСТ, общего билирубина, СРБ, мочевины, креатинина, снижение общего белка, нарушения со стороны свертывающей системы. Общеклиническое исследование мочи подтверждает увеличение плотности, микрогематурию, лейкоцитурию, реже пиурию. В ликворограмме при патереллезных менингоэнцефалитах обнаруживается нейтрофильный плеоцитоз, клеточно-белковая диссоциация.
- Выявление инфекционных агентов. Основной методикой является ПЦР. Бактериологические методы посева на питательные среды используются с любым биологическим материалом, полученным от больного (отделяемое кожных язв, кровь, спинномозговая жидкость, пунктат абсцесса), включая секционный. ИФА и другие серологические методики необходимы для ретроспективной диагностики пастереллеза, поскольку требуют исследования парных сывороток с интервалом не менее 14 дней для детекции роста титра антител.
- Лучевая диагностика. При поражениях респираторного тракта назначается рентгенография грудной клетки. Часто проводится УЗИ мягких тканей, суставов, костных структур с целью своевременного обнаружения гнойных процессов. Для визуализации септикопиемических очагов в области внутренних органов используется УЗИ органов брюшной полости, почек, малого таза. МРТ и КТ головного мозга применяются при симптомах поражения ЦНС, особенно у иммунодефицитных лиц.
Дифференциальную диагностику проводят с инфекционными болезнями: сибирской язвой, кожным и висцеральным лейшманиозом, эризипелоидом. Кроме того, симптомы пастереллеза схожи с клиникой листериоза, токсоплазмоза, рожи. Генерализованные поражения возможны при туберкулезе, органных микозах и сифилисе, могут наблюдаться при туляремии, цитомегаловирусной, пневмококковой инфекции. Сепсис может быть вызван стафилококками, стрептококками, кокциеллами. В ряде случаев требуется дифференцировка с облитерирующим эндартериитом, трофическими язвами, бактериальными гнойными поражениями. Соматическими заболеваниями, сходными с пастереллезом, являются бронхоэктатическая болезнь, злокачественные новообразования ЦНС, геморрагические инсульты. Иногда необходимо исключить кожные болезни: стафилодермию, псориаз, экзему.
Лечение пастереллеза
Больным геморрагической септицемией показано стационарное лечение, особенно при принадлежности к группе риска. Постельный режим соблюдается до 3-4 дней устойчиво нормальной температуры тела. Режим питания предполагает ограничение трудноперевариваемой пищи, отказ от алкоголя. Обязательным является увеличение количества употребляемой жидкости с целью оральной дезинтоксикации. При наличии признаков артрита рекомендуется наложение бандажей, ортезов, фиксирующих повязок с использованием эластичного бинта.
Этиотропное лечение включает антибактериальные средства. Наиболее эффективными препаратами считаются пенициллины (ампициллин+сульбактам, амоксициллин+клавулановая кислота), цефалоспорины 2-го и 3-го поколения, тетрациклины, фторхинолоны, ко-тримоксазол. У пациентов, страдающих пастереллезной инфекцией вследствие контаминации диализного катетера, были зафиксированы случаи рецидива при прохождении курса монотерапии аминогликозидами, поэтому их применение в качестве единственного средства лечения сомнительно.
План лечения пастереллеза также может предполагать инфузионное введение растворов для уменьшения выраженности интоксикационного синдрома (глюкозо-солевые, сукцинат-содержащие растворы, ацесоль), прием жаропонижающих и обезболивающих препаратов. Хирургическое лечение показано при возникновении ограниченных либо разлитых гнойных процессов. Обычно производится вскрытие и дренирование гнойных очагов. При тяжелых поражениях требуется ампутация конечности.
Прогноз и профилактика
Прогноз при неосложненном варианте пастереллеза и неотягощенном преморбидном фоне благоприятный. Согласно исследованиям, около 70% случаев септического течения болезни наблюдалось у лиц старше 50 лет и лишь в 21% случаев – у больных 20-50 лет. Летальность у животных достигает 80%, у людей – 1,79%. Средняя продолжительность болезни составляет 8 дней. При наличии гнойного поражения суставов и костных структур возможна длительная реабилитация (более 1-2 месяцев), в случае ампутации конечности – инвалидизация.
Специфическая профилактика существует в виде вакцин и гипериммунной сыворотки для животных; вакцинные препараты для людей не разработаны. К мерам неспецифической профилактики относят строгий ветеринарный контроль, изоляцию больных животных, запрет на продажу молока и мяса из очагов пастереллеза. Необходимо использовать средства индивидуальной защиты (маски, щитки, перчатки) при работе с животными, проводить обработку укусов, царапин с помощью антисептических средств, тщательное мытье рук с мылом после контакта с животными.
3. Pasteurella multocida line infection: a case report and review of literature / T. C. S. Martin, J. Abdelmalek, B. Yee, S. Lavergne, M. Ritter // BMC Infecious Diseases – 2018 - №18.
Лептоспироз является природно-очаговым зоонозным инфекционным заболеванием, характеризующимся поражением печени, а также - почек и нервной системы на фоне общей интоксикации. Нередко сопровождается геморрагическим симптомом и желтухой. Возбудитель лептоспироза может проникнуть в организм через слизистые оболочки или травмированные кожные покровы. От заражения до первых клинических проявлений лептоспироза может пройти от нескольких дней до месяца. В ранней диагностике лептоспироза большую роль играет микроскопическое обнаружение лептоспир в препарате крови, результаты бакпосева зачастую носят ретроспективное значение.
Общие сведения
Лептоспироз является природно-очаговым зоонозным инфекционным заболеванием, характеризующимся поражением печени, а также - почек и нервной системы на фоне общей интоксикации. Нередко сопровождается геморрагическим симптомом и желтухой.
Характеристика возбудителя
Лептоспироз вызывает Leptospira interrogans. Это грамотрицательная аэробная подвижная спиралевидная палочка, напоминающая спирохету. В настоящее время выделено более 230 сероваров лептоспиры. Бактерии обладают умеренной устойчивостью в окружающей среде, патогенные лептоспиры погибают при воздействии солнечного света, высоких температур. В воде разные штаммы могут существовать от нескольких часов до месяца. В сухой почве жизнеспособность лептоспиры сохраняется 2 часа, в заболоченной - до 10 месяцев. Могут переносить замораживание, во влажной почве и водоемах способны пережить зиму. На пищевых продуктах лептоспиры сохраняются 1-2 дня. Погибают с течение 20 минут при воздействии однопроцентной хлороводородной кислотой и полупроцентным раствором фенола.
Основным резервуаром лептоспироза в природе являются грызуны (мыши, крысы, серые полевки) и насекомоядные млекопитающие (ежи, землеройки). Резервуаром и источником инфекции также являются сельскохозяйственные животные (свиньи, овцы, коровы, козы, лошади), пушные звери на зверофермах, собаки. Животное контагиозно на протяжении всего периода заболевания. Грызуны страдают хроническим лептоспирозом, выделяя возбудителя с мочой. Передача лептоспироза от человека крайне маловероятна.
Лептоспироз распространяется с помощью фекально-орального механизма преимущественно водным путем. Кроме того, можно отметить вероятность передачи контактным и пищевым (кормовым) путем. Человек заражается лептоспирозом через слизистые оболочки или микротравмы кожных покровов. Заражение может произойти при купании в загрязненных бактериями водоемах (и заглатывании воды), работе с сельскохозяйственными животными.
Человек обладает высокой естественной восприимчивостью к этой инфекции. После перенесения лептоспироза иммунитет стойкий и длительный, но специфичный для данного серовара бактерий и возможно повторное инфицирование лептоспирами с иной антигенной структурой.
Патогенез лептоспироза
Воротами инфекции для лептоспир являются слизистые оболочки пищеварительного тракта, носоглотки, иногда – половых органов и мочевыводящих путей, а также повреждения кожных покровов. В области внедрения возбудителя никаких патологических изменений не отмечается. Лептоспиры распространяются с током лимфы, оседая в лимфоузлах, размножаясь там, и по кровеносной системе рассеиваясь по органам и системам. Лептоспиры тропны к макроцитарным фагоцитам, склонны накапливаться в тканях печени, селезенки и почек (иногда – в легких) вызывая местное воспаление.
Симптомы лептоспироза
Инкубационный период лептоспироза колеблется в пределах от нескольких дней, до месяца, составляя в среднем 1-2 недели. Заболевание начинается остро, с резкого повышения температуры до высоких цифр, с потрясающим ознобом и выраженной симптоматикой интоксикации (интенсивные головные боли, миалгии, в особенности в икроножных и брюшных мышцах, слабость, бессонница, анорексия). При осмотре отмечается гиперемированность и отечность лица, возможно появление герпетиформной сыпи на губах и крыльях носа, содержимое везикул имеет геморрагический характер. Конъюнктива раздраженная, склеры инъецированные, умеренная гиперемия слизистой оболочки зева, ротоглотки, могут отмечаться кровоизлияния в подслизистом слое.
Кореподобные или петехиальные высыпания на туловище, конечностях появляются спустя 2-4 дня. Сыпь может сохраняться от нескольких часов до нескольких дней. Геморрагический синдром (петехии и кровоизлияния) может дополнять клинику лептоспироза уже с первых дней заболевания. Тяжелое течение может сопровождаться геморрагической сыпью в подмышечных впадинах и на локтевых сгибах, гематурией (вплоть до видимой примеси крови в моче), носовыми, маточными, желудочно-кишечными кровотечениями, кровохарканьем (вплоть до геморрагического отека легких).
Нарушения работы дыхательной системы в первые дни обычно не отмечаются, возникают при прогрессировании инфекции и в разгар заболевания при среднетяжелом и тяжелом течении чаще всего имеют патогенетическую связь с геморрагическим синдромом. Нарушения сердечной деятельности (изменения ритма, глухие сердечные тоны, падение периферического артериального давления) связывают с интоксикационным синдромом.
Кроме того, больные могут отмечать нарушения со стороны пищеварительной системы: боль в животе, тошнота и рвота, гепато- и спленомегалия, тяжесть и болезненность при пальпации в правом подреберье. Иногда развивается желтуха печеночного характера: желтеют склеры, кожные покровы окрашиваются в интенсивный шафрановый цвет, кал обесцвечивается, моча приобретает пивной оттенок. Больных может беспокоить кожный зуд.
При поражении почек больные жалуются на боль в поясничной области, отмечается олигурия (вплоть до анурии), моча приобретает темный цвет, нередко с примесью крови. Симптом Пастернацкого – положительный. Со стороны нервной системы отмечаются расстройства сна, головные боли, повышенное беспокойство, возбуждение. Могут отмечаться менингеальные симптомы (в 10-15% случаев в разгар заболевания больные демонстрируют клинику серозного менингита).
Лихорадка при лептоспирозе сохраняется до недели, после чего происходит критическое снижение температуры. Иногда возникает повторная волна лихорадки. Далее следует период реконвалесценции, в который происходит постепенное стихание симптоматики и восстановление функций органов. В случае своевременного оказания медицинской помощи и умеренной тяжести заболевания выздоровление обычно наступает через 3-4 недели. В 20-30% случаев могут отмечаться рецидивы инфекции, при которых характерна меньшая выраженность лихорадки и полиорганных нарушений, продолжительность приступов составляет обычно несколько дней. В целом рецидивирующая инфекция может длиться до 2-3 месяцев.
Осложнения лептоспироза
Самым частым осложнением болезни является почечная недостаточность. В тяжёлых случаях она способна развиться в первую же неделю, обеспечивая высокую смертность – более 60 %. Другими осложнением могут быть печёночная недостаточность, геморрагии в ткани лёгких, надпочечников, в мышцы, внутренние кровотечения.
Помимо прочего, возможно осложнения со стороны нервной системы: менингиты, менингоэнцефалиты. Осложнения со стороны органов зрения: ириты и иридоциклиты. Лептоспироз может способствовать присоединению вторичной бактериальной инфекции: вторичная пневмония, абсцессы, пролежни.
Диагностика лептоспироза
Для общего анализа крови при лептоспирозе характерна картина бактериальной инфекции – лейкоцитоз с нейтрофильным преобладанием, повышение СОЭ. Период разгара может снижаться содержание эритроцитов и концентрация эозинофилов и тромбоцитов.
В качестве анализа состояния органов и систем применим биохимический анализ крови (отмечают признаки функциональных нарушений в работе печени), анализ мочи (может обнаруживаться микрогематурия, признаки желтухи). При геморрагическом синдроме проводят исследование свертываемости - коагулограмму. При поражении почек больного лептоспирозом консультирует нефролог, проводится УЗИ почек. Менингиальные симптомы являются показанием к люмбальной пункции.
Специфическая диагностика заключается в бакпосеве крови (лептоспиры могут обнаруживаться в капле крови при микроскопии), в некоторых случаях производят выделение возбудителя и бакпосев на питательных средах. Ввиду длительного роста культуры лептоспиры посев имеет значение для ретроспективного подтверждения диагноза. Серологическая диагностика производится с помощью РНГА и HCR в парных сыворотках. Титр антител начинает нарастать в разгар заболевания, второй анализ берут в период реконвалесценции. Высокоспецифичной и чувствительной методикой диагностики лептоспироза является выявление ДНК бактерий с помощью ПЦР. Диагностика может проводиться с первых дней заболевания.
Лечение лептоспироза
Больные лептоспирозом подлежат госпитализации при вероятности развития тяжелых осложнений и с целью клинико-лабораторного контроля состояния организма в динамике. Больным показан постельный режим на весь период лихорадки и 1-2 дня после нормализации температуры. В случае появления симптомов почечной недостаточности больные также остаются в постели. Ограничения в рационе назначаются в соответствии с имеющими место функциональными нарушениями работы печени и почек.
Этиотропная терапия подразумевает использование антибиотиков. При лептоспирозе хорошо зарекомендовал себя бензилпенициллин, назначаемый внутримышечно. В качестве альтернативы возможно применение ампициллина внутривенно. Тяжело протекающий лептоспироз лечат доксициклином. В комплекс терапевтических мер включают применение специфического противолептоспирозного гетерологичного иммуноглобулина.
К мероприятиям неспецифической терапии относится дезинтоксикация, симптоматические средства, контроль состояния дыхательной и сердечно-сосудистой системы и реологических свойств крови. В случае возникновения острой печеночной недостаточности, почечной или сердечной недостаточности, отека легких прибегают к обычным мерам интенсивной терапии.
Прогноз и профилактика лептоспироза
Обычно лептоспироз имеет благоприятный прогноз, летальные случаи связаны в основном с недостаточной или несвоевременно оказанной медицинской помощью и ослабленным состоянием организма. В настоящее время смертность от лептоспироза не превышает 1-2%. Повышение этого показателя до 15-20% возможно в периоды массовых эпидемий.
Профилактика лептоспироза подразумевает в первую очередь контроль над заболеваемостью сельскохозяйственных животных, а также ограничение размножения грызунов (дератизация городских объектов, сельских хозяйств). Санитарно-гигиенические мероприятия включают контроль состояния водных источников (как мест забора воды для нужд населения, так и общественных пляжей), сельскохозяйственных угодий. Меры специфической вакцинации подразумевают введение убитой лептоспирозной вакцины лицам, работающим с животными, либо гражданам, находящимся в эпидемическом очаге в период вспышек лептоспироза.
Что такое лептоспироз? Причины возникновения, диагностику и методы лечения разберем в статье доктора Александрова Павла Андреевича, инфекциониста со стажем в 14 лет.
Над статьей доктора Александрова Павла Андреевича работали литературный редактор Маргарита Тихонова , научный редактор Сергей Федосов

Определение болезни. Причины заболевания
Лептоспироз (болезнь Васильева — Вейля, водная лихорадка, нанукаями) — острое инфекционное заболевание, вызываемое патогенными бактериями рода Leptospira, поражающими печень, почки, мышцы, лёгкие, центральную нервную системы (ЦНС), селезёнку и другие органы.
Клинически характеризуется синдромом общей инфекционной интоксикации, увеличением печени и селезёнки, распадом мышечной ткани и почечными синдромами. Летальность составляет (даже в случае своевременно начатого лечения) до 40%.
Этиология
Виды — L. interrogans (около 200 серотипов) и L. biflexa (сапрофит)
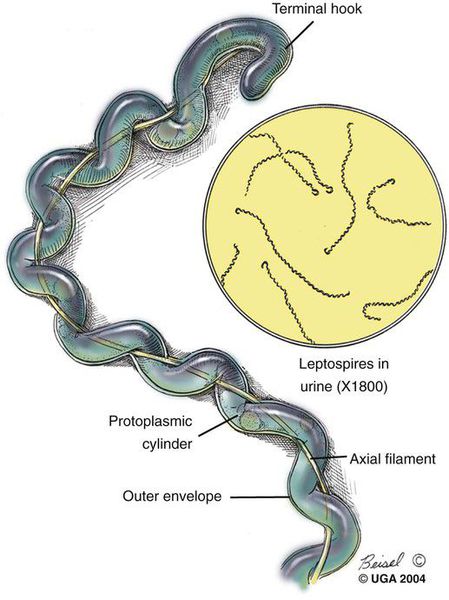
Возбудитель лептоспироза — грамм-отрицательная бактерия-спирохета, которая имеет спиралевидную форму, концы закручены в виде крючков, количество завитков зависит от длины (в среднем 20). Обладают многообразной подвижностью (тип движения — вращательно-поступательный), с которой связана их высокая инвазионная способность (внедрение в организм через клеточные и тканевые барьеры). Способны быстро перемещаться в направлении более вязкой среды.
Факторы патогенности
Бактерии рода Leptospira углеводы не ферментируют. Имеется эндотоксин, а также некоторые факторы патогенности: гиалуронидаза, фибринолизин, гемолизин и другие.
Содержит антигены: белковый соматический (определяет видовую специфичность) и поверхностный полисахаридный (определяет группы и серовары).
Выращиваются на средах, включающих сыворотку крови. Строгие аэробы, то есть существуют только в условиях кислородной среды. Являются гидрофилами: важное условие для жизни — повышенная влажность окружающей среды. Растут медленно (5-8 дней). При серебрении приобретают коричневый или чёрный цвет, по Романовскому — Гимзе окрашиваются в розовый или красноватый цвет.
Относительно неустойчивы во внешней среде, при кипячении или подсушивании погибают мгновенно, под воздействием дезинфектантов — в течении 10 минут. При низких температурах, например, в замороженном мясе сохраняются до 10 суток, летом в пресноводных водоёмах — до одного месяца, во влажной почве — до 270 суток, в молоке — до одного дня, в почках животных при разделке и охлаждении (0-4°C) — до одного месяца. [2] [3]
Жизненный цикл лептоспиры:

Эпидемиология
Зоонозное заболевание. Очень распространён (убиквитарен).
Источник инфекции — дикие грызуны и насекомоядные животные (инфекция протекает бессимптомно), лисицы, домашние животные (коровы, овцы, козы, собаки, лошади, свиньи, являющиеся антропургическими очагами, у которых инфекция может протекать в различных клинических формах, в том числе носительства), выделяющие лептоспир при мочеиспускании в природную среду. Больной человек теоретически может быть заразен.
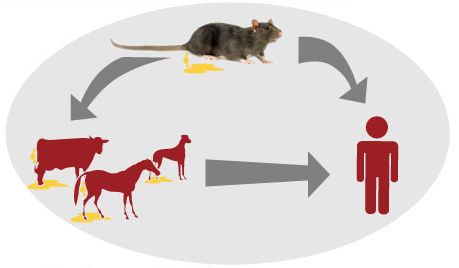
Как передаётся лептоспироз
Механизм передачи: фекально-оральный (алиментарный, водный, контактно-бытовой) и контактный (разделка мяса, купание, хождение босиком по влажной почве), иногда инфекция передаётся аспирационным путём (правильнее говорить — воздушно-пылевым). Случаи трансмиссивной передачи, т. е. через укусы кровососущих насекомых, не описаны, хотя при повреждении кожи риск заражения повышается.
Водная лихорадка имеет профессиональный характер, болеют преимущественно дератизаторы (специалисты по уничтожению грызунов), доярки, фермеры, пастухи, лесники, охотники, ветеринары, шахтёры, а также купальщики в лесных и луговых водоёмах.
Характерна летне-осенняя сезонность.
Иммунитет стойкий, типоспецифический. [1] [3]
При обнаружении схожих симптомов проконсультируйтесь у врача. Не занимайтесь самолечением - это опасно для вашего здоровья!
Симптомы лептоспироза
Инкубационный период — от 4 до 14 дней. Начало острое.
- синдром общей инфекционной интоксикации (с лихорадкой постоянного типа);
- гепатолиенальный синдром (увеличение печени и селезёнки);
- синдром рабдомиолиза (разрушение и гибель клеток скелетной мышечной ткани);
- синдром поражения почек (ведущий синдром заболевания);
- менингеальный синдром (вовлечение в патологический процесс мозговых оболочек);
- синдром нарушения пигментного обмена (желтуха) — с его появлением состояние ухудшается;
- геморрагический (в том числе с лёгочным кровотечением);
- экзантемы (кожные высыпания);
- поражения дыхательной системы (пневмония);
- поражения сердечно-сосудистой системы (миокардит).
Начало заболевания характеризуется внезапным повышением температуры тела до 39-40°C (продолжительность до 10 дней), сопровождающееся потрясающим ознобом, нарастающей головной болью, бессоницей, нарушением аппетита, тошнотой и выраженной жаждой. Появляются боли в мышцах (преимущественно в икроножных), позже присоединяется желтушность кожи и слизистых оболочек, высыпания на коже различного характера.
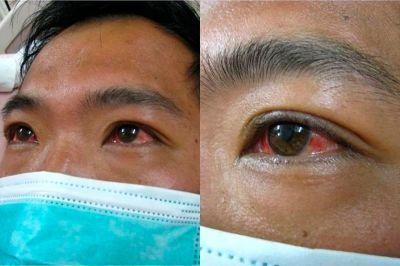
На 3-6 сутки появляются высыпания на туловище и конечностях (сыпь различного характера – пятнисто-папулёзная, мелкопятнистая, мелкоточечная, петехиальная, эритематозная с тенденцией к слиянию; после разрешения оставляет шелушение).
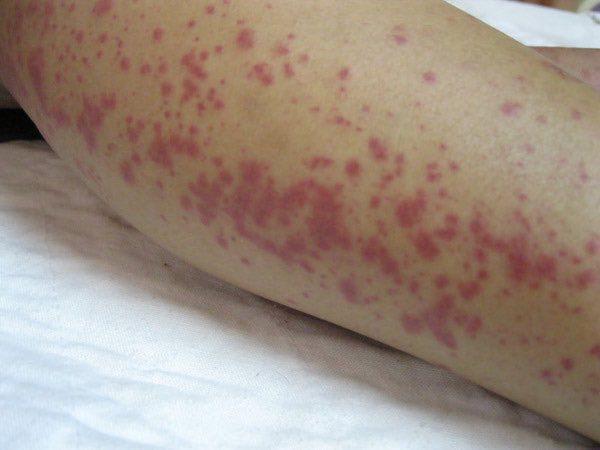
При развитии желтухи на 3-5 день появляется желтушное окрашивание кожи различной интенсивности, иктеричность (желтушность) склер, темнеет моча.
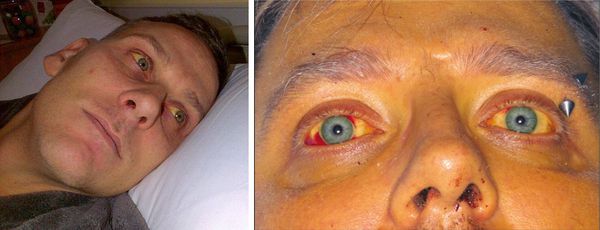
Характерным признаком является выраженная болезненность икроножных мышц, особенно при надавливании на них, а также ограничение подвижности больного из-за боли. Периферические лимфоузлы не изменяются. Со стороны сердечно-сосудистой системы наблюдается тахикардия, понижение артериального давления, глухость сердечных тонов. Возможно развитие ринофарингита и пневмонии.
К 3-4 дню увеличиваются размеры печени и селезёнки, из-за кровоизлияний появляются боли в животе. При фарингоскопии наблюдается умеренная гиперемия слизистой оболочки ротоглотки, иногда энантема (сыпь на слизистых оболочках), язык сухой, покрыт жёлто-коричневым налётом. Характерна олигоанурия (снижение количества выделяемой мочи), тёмная моча, болезненность при поколачивании по поясничной области.
Для заболевания при отсутствии адекватного лечения характеры рецидивы (через 2-7 дней нормальной температуры тела возобновление клинических проявлений) и обострения (на фоне течения заболевания усиление клинической симптоматики).
После болезни характерна длительная астения (нервно-психическая истощённость), мышечная слабость (резидуальные явления), возможно формирование хронической почечной недостаточности.
Лептоспироз при беременности
Лептоспироз у беременных протекает крайне тяжело: возникает высокий риск выкидыша, острой почечной недостаточности, ДВС-синдрома и смертельного исхода. [1] [2] [4]
Патогенез лептоспироза
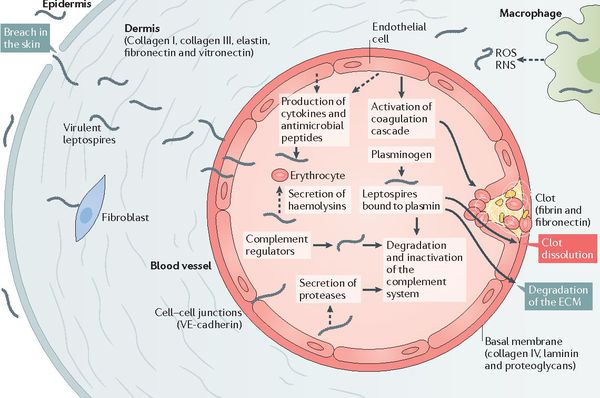
После мнимого благополучия происходит вторичный выброс лептоспир и их токсинов в кровь (при разрушении первичным звеном иммунной системы), что обуславливает начало клинических проявлений заболевания. Яды и продукты жизнедеятельности лептоспир воздействуют на стенку капилляров, что повышает их проницаемость и нарушает функционирование. Глобальный капилляротоксикоз ведёт к возникновению геморрагического синдрома (избыточной кровоточивости). Возникают кровоизлияния в надпочечники, что ведёт к острой надпочечниковой недостаточности.
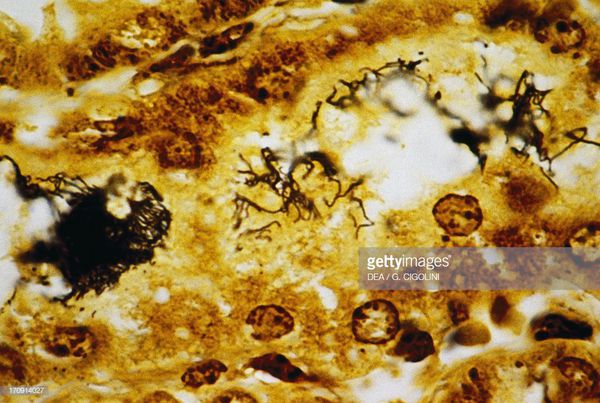
Появление желтухи обусловлено отёком, деструктивно-некротическими поражениями паренхимы (ткани печени) и распадом эритроцитов посредством гемолизинов. В почках повреждается эпителий почечных канальцев и всех структурных слоёв, что проявляется нарушением образования и экскреции мочи, доходя до стадии острой почечной недостаточности. Иногда происходит проникновение лептоспир через гематоэнцефалический барьер и развитие бактериального поражения оболочек мозга (формирование менингита). Поражаются скелетные мышцы (рабдомиолизис), особенно икроножные. Через 4-6 недель при благоприятном течении формируется иммунная защита и происходит элиминация (устранение) возбудителя. Хронизация инфекции не характерна. [2] [4]
Классификация и стадии развития лептоспироза
По степени тяжести:
- тяжелый (выраженная желтушное окрашивание кожи, тромбогеморрагический синдром, острая почечная и надпочечниковая недостаточность, менингит, часто так называемый синдром Вайля — лептоспироз с сильной лихорадкой, выраженным синдромом общей инфекционной интоксикации, снижением гемоглобина и синдромом нарушения пигментного обмена);
- средней тяжести;
- лёгкой степени тяжести.
По клинической форме:
- типичная;
- геморрагическая;
- желтушная;
- ренальная (почечная);
- менингеальная;
- смешанная.
Классификация по МКБ-10:
- А27.0 Лептоспироз желтушно-геморрагический;
- А27.8 Другие формы лептоспироза;
- А27.9 Лептоспироз неуточнённый.
По наличию осложнений:
- без осложнений;
- с осложнениями (инфекционно-токсический шок, острая почечная недостаточность, острая надпочечниковая недостаточность, ДВС-синдром и другие). [1][5]
Осложнения лептоспироза
- острая почечная недостаточность (олигоурия, анурия, рост уровня креатинина); , менингоэнцефалит, полиневрит;
- миокардит; ;
- ирит, увеит, иридоциклит (глазные осложнения);
- отит (воспаление уха);
- у детей может наблюдаться повышение артериального давления, холецистит и панкреатит;
- синдром Кавасаки (развитие миокардита, сопровождающегося водянкой желчного пузыря, экзантемой, покраснением и припухлостью ладоней и подошв с последующей десквамацией кожи). [1][2]
Диагностика лептоспироза
- клинический анализ крови (нейтрофильный лейкоцитоз со сдвигом влево, лимфопения, анэозинофилия, повышение СОЭ, анемия, тромбоцитопения);
- общий анализ мочи (анурия, протеинурия, цилиндрурия, лейкоцитурия, эритроцитурия);
- биохимический анализ крови (билирубинемия преимущественно за счёт непрямой фракции, снижение протромбинового индекса, повышение АЛТ, АСТ, КФК-ММ, ЛДГ общ, ЩФ, креатинина, СРБ);
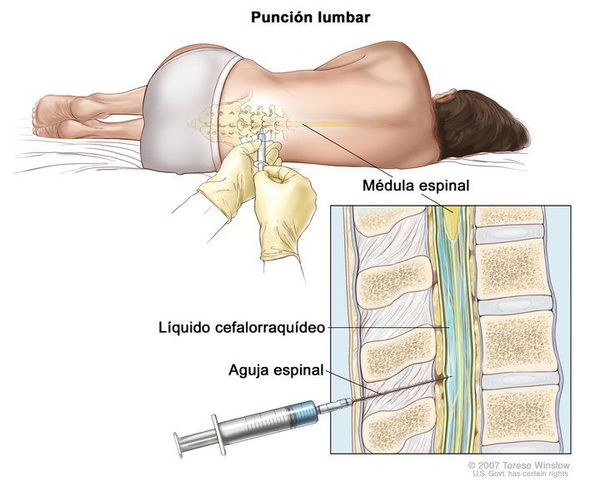
- люмбальная пункция при менингите (цитоз до 500 кл в 1 мкл, нейтрофильный плеоцитоз, повышение белка);
- бактериальный посев на листерии (материал — кровь, моча, ликвор на среды с добавлением 5 мл воды и 0,5 мл сыворотки кролика — среда Терского);
- пассажи на животных;
- серологические иммунологические реакции (РСК, РНГА, РНИФ, РМА, ИФА и другие);
- ПЦР диагностика;
- микроскопия в тёмном поле (материал — кровь, ликвор, моча);
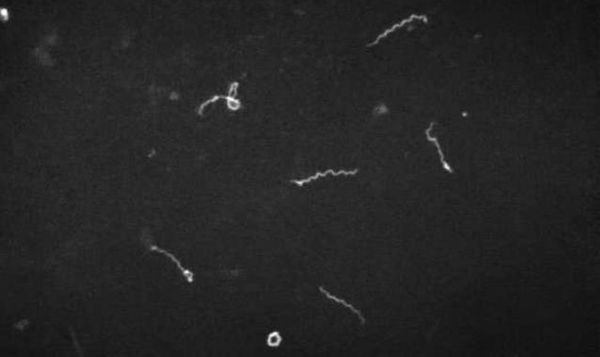
- биопсия икроножных мышц с последующим серебрением биоптата;
- ЭКГ (диффузные поражения). [2][4]
Лечение лептоспироза
Место лечения — инфекционное отделение больницы, отделение реанимации и интенсивной терапии (ОРИТ).
Режим и диета
Режим — палатный, постельный. Диета № 7 или № 2 по Певзнеру (с ограниченим Na+ и контролем жидкости).
Медикаментозное лечение
В виду выраженной аллергизации, полиорганного характера патологии незамедлительно показано введение стандартных доз глюкокортикоидов и последующая незамедлительная антибиотикотерапия (наиболее эффективна в первые трое суток заболевания). Могут быть применены препараты пенициллина, тетрациклиновая группа, фторхинолоны. Этиотропное лечение вначале должно проводиться под непрерывным контролем медицинского персонала, так как возможно развитие реакции Яриша — Герксгеймера (массивный бактериолизис и, как следствие, инфекционно-токсический шок).
При отсутствии антибиотиков возможно введение специфического гамма-глобулина на фоне десенсибилизации.
Патогенетически обосновано назначение глюкокортикостероидов, переливание плазмы, гепаринотерапия (при развитии ДВС-синдрома), сердечных гликозидов, вазопрессоров, гипербарической оксигенации, мочегонных энтеросорбентов. При ухудшении состояния больной переводится в ОРИТ, проводиться перитонеальный диализ.
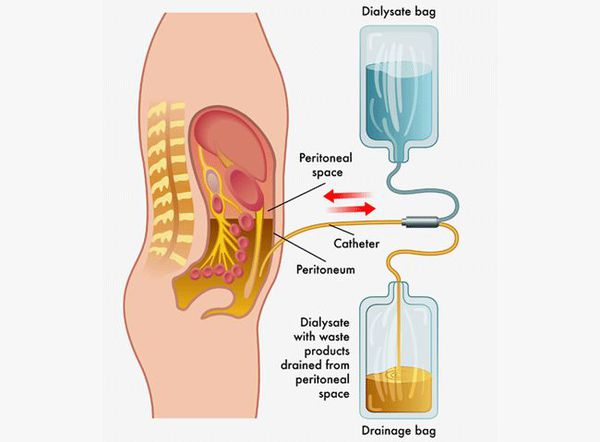
Детоксикация при лептоспирозе
Детоксикация проводится при тяжёлом течении болезни.
К детоксикации относятся:
- перитонеальный диализ — удаление токсинов, воды и электролитов через брюшину;
- гемофильтрация — метод очищения крови с помощью фильтрации через искусственные высокопроницаемые мембраны с одновременным замещением удаляемого фильтрата специальным раствором ;
- гемодиализ — кровь пациента поступает в специальный аппарат и проходит через фильтр (диализатор), затем уже очищенная кровь возвращается в организм.
Плазмаферез
Плазмаферез — это удаление части плазмы, содержащей токсины, и замещение её различными растворами, например физиологическим и раствором альбумина. При этом из организма выводятся антитела, антигены, циркулирующие иммунные комплексы, продукты распада тканей и клеток, бактерии и их токсины, медиаторы воспаления и другие вещества. При плазмаферезе пациенту в вену на руке вводится пластиковый катетер, который соединяется системой трубок с плазмофильтром. Внутри плазмофильтра располагаются разные фильтры, насосы, мембраны и центрифуги. После включения программы происходит автоматический забор крови внутрь аппарата, где она разделяется на фракции и очищается, а затем возвращается обратно в организм.
Специфическая сыворотка против лептоспироза
В первые дни болезни могут применяться специфические гамма-глобулины и плазма с высоким содержанием противолептоспирозных антител, однако этот метод слабо распространён.
Выписка из стационара осуществляется после нормализации температуры тела, клинического состояния и лабораторных показателей. За реконвалесцентами осуществляется динамическое наблюдение в течении шести месяцев с периодическими (раз в два месяца) осмотрами врачом-инфекционистом и лабораторным обследованием. [1] [3]
Прогноз. Профилактика
Прогноз при своевременно начатой терапии в случаях средней и лёгкой степени тяжести относительно благоприятный, при развитии тяжёлого течения заболевания и осложнений возможен летальный исход.
Профилактика лептоспироза
Меры профилактики и противоэпидемические мероприятия:
- проведение борьбы с грызунами (дератизация);
- вакцинация восприимчивых домашних животных, спец. работников;
- соблюдение рекомендаций по купанию, использование защитной одежды;
- контроль за объектами централизованного водоснабжения;
- санитарно-гигиеническое просвещение населения. [1][4]
При отдыхе на природе не рекомендуется ходить босиком по влажной почве и купаться в водоёмах, которые могут быть заражены мочой животных. Следует избегать контакта с потенциальными переносчиками болезни (например, лисицами) и не пить сырую воду из водоёмов. Если на коже есть раны, то поездку на природу лучше отложить.
Соблюдение мер предосторожности на рабочем месте: фермеры и работники мясокомбинатов должны своевременно проводить плановую иммунизацию скоту, выявлять и лечить больных животных, использовать спецодежду, бытовые дезинфектанты для уборки, уничтожать грызунов.
Вакцина против лептоспироза
Профилактическая прививка от лептоспироза проводится домашним животным. Людей вакцинируют по эпидемическим показаниям, например при работе на специализированных производствах. Инактивированную вакцину применяют однократно с ревакцинацией через год.
У крупного рогатого скота пастереллёз протекает со сходными признаками с сибирской язвой, инфекционным ринотрахеитом, злокачественной горячкой, а у молодняка с диплококковой септицемией и сальмонеллёзом.
При постановке диагноза пастереллёз свиней необходимо дифференцировать от классической и африканской чумы, рожи, сибирской язвы, сальмонеллёза, инфлюэнцы, диплококковой септицемии, болезни Ауески, гемофиллёзного полисерозита и микоплазмоза.
Пастереллёз овец и коз необходимо отличать от бабезиоза; птиц – от чумы и тифа. Чумой болеют только куриные, а при тифе всегда резко увеличена селезёнка.
Пастереллез птиц необходимо дифференцировать от ньюкаслской болезни, спирохето-за, респираторного микоплазмоза. Ньюкаслская болезнь характеризуется геморрагическими явлениями, наличием геморрагического ободка между мышечным и железистым желудками и в местах ответвления слепых кишок. В кишечнике обнаруживают язвенно-некротические очаги. При спирохетозе резко увеличена селезенка (в 2—4 раза). При респираторном микоплазмозе основные изменения сосредоточены в воздухоносных мешках (чаще находят фибринозный аэросаккулит).
КЛОСТРИДИОЗЫ
Клостридиозы – группа токсикоинфекций животных и человека, вызываемых анаэробными микроорганизмами из рода клостридий. К клостридиозам относятся: эмфизематозный карбункул, злокачественный отек, брадзот овец, анаэробная энтеротоксемия овец, анаэробная дизентерия молодняка, столбняк, ботулизм и др.
Для клостридиозов характерно постоянное обитание возбудителя в кишечнике животных и человека; повсеместное распространение спор; неконтагиозность; спорадичность возникновения, связанная с климатом и условиями кормления и содержания животных.
Факторами передачи возбудителей является окружающая среда: почва, навоз, пастбища, трупы животных.
Патогенные клостридии продуцируют высокоактивные токсины, которым принадлежит ведущая роль в патогенезе вызываемых ими болезней, объединенных под общим названием – клостридиозы. Каждая из этих болезней имеет свои особенности и вызывается определенным видом или типом возбудителей и их ассоциациями.
Эмфизематозный карбункул (ЭМКАР)
Gangraena emphysematosa
Остро протекающая неконтагиозная токсикоинфекционная болезнь крупного рогатого скота (реже мелкого рогатого скота), характеризующаяся образованием быстро увеличивающихся крепитирующих припухлостей в области мускулатуры тела, хромотой и высокой летальностью за короткий промежуток времени.
Возбудителем является спорообразующая бактерия С. chauvoei.
К данному заболеванию восприимчивы: крупный рогатый скот, буйволы, в меньшей степени – овцы и лоси. Болеют животные всех возрастов, но наиболее подвержен молодняк в период от 3 мес до 3-4 лет, на который приходится около 30% всех случаев. При этом болезнь возникает преимущественно в первый и второй годы выгона на пастбище. Устойчивость к болезни телят до 3-месячного возраста обеспечивается наличием у них колострального иммунитета, полученного от иммунных коров, а у животных старше 3-4 лет – иммунизирующей субинфекцией. Однако известны случаи заболевания эмкаром как телят в первые недели жизни, так и старых животных. Часто заболевает крупный рогатый скот, привезенный в неблагополучную зону из других хозяйств или импортный. В основном эмкару подвержены упитанные животные (особенно на пастбище в жаркий сухой сезон), что связано с высоким содержанием гликогена в мышцах, а это является благоприятной средой для развития и токсинообразования возбудителя.
Источник возбудителя инфекции – больные животные, а факторы передачи – инфицированные спорами возбудителя почва, корма, пастбища, вода заболоченных стоялых водоемов, а также несвоевременно убранные трупы.
Споры могут находиться в почве или воде годами, создавая и поддерживая таким образом стационарность эпизоотических очагов болезни, ее энзоотичность, связанную с определенной местностью. У крупного рогатого скота в интенсивности эпизоотологического процесса отмечается четко выраженная летне-осенняя сезонность.
Возбудитель попадает в организм животного в основном алиментарным путем (через воду и корм), но возможен также трансмиссивный путь передачи, особенно у овец (кровососущими насекомыми). Недостаточно чисто выполненные кастрации, инъекции и другие манипуляции тоже способствуют возникновению заболевания. Овцы могут заразиться также при стрижке и тяжелых родах.

Рис.14. Нетель, павшая от эмкара. В области плечевого пояса отчетливо виден участок пораженных мышц. На разрезе ясно выступают явления острого геморрагического миозита с некротизирующими явлениями
Как правило, заражение происходит при попадании спор возбудителя в ЖКТ с кормом или водой: в связи с травмами слизистой оболочки (к осени травостой на пастбище становится сухим и грубым); а также через ранки на поверхности тела.
Проникая в кровь, возбудитель разносится по организму и оседает в частях тела с наиболее объемной мышечной массой. В среде, богатой гликогеном споры прорастают. Вегетативные формы начинают быстро размножаться. На месте локализации возбудителя возникает серозное или серозно-геморрагическое воспаление. Микробы разрушают кровеносные сосуды и вызывают распад тканей. Пораженные ткани пропитываются кровянистым экссудатом и пузырьками газа, который образуется в результате жизнедеятельности возбудителя. Впоследствии формируется быстро увеличивающийся карбункул.
Всасываясь в кровь, продукты распада поврежденных тканей и токсины вызывают интоксикацию организма. При этом происходит повышение температуры тела, ослабление сердечной деятельности, нарушение физиологических функций внутренних органов, особенно печени. Наступает общая интоксикация организма, резко повышается концентрация микробов в тканях и отмечается бактериемия, кардинально нарушается работа сердца и легких, что приводит к быстрой гибели животного.
Инфекционный процесс может протекать и без образования карбункула в виде сепсиса.
Инкубационный период болезни 1-3 суток, в отдельных случаях – 5 дней. Болезнь начинается внезапно и протекает остро (с повышением температуры до 41-42 С), заканчивается почти всегда летальным исходом.
Уже в ранний период наблюдается хромота. На отдельных частях тела (круп, поясница, шея, грудь, подчелюстная область), а иногда в ротовой полости или глотке появляются быстро увеличивающиеся ограниченные, горячие, болезненные отеки (карбункулы). Вскоре они становятся холодными, безболезненными, теряют отечность. Кожа над ними приобретает багрово-синюшный цвет, а при разрезе карбункулов, из них вытекает грязно-бурая пенистая жидкость с запахом прогорклого масла. При пальпации припухлостей слышится своеобразный хруст (крепитация), при перкуссии – выраженный тимпанический звук.
Далее отмечают общее угнетение, анорексию, отсутствие жвачки, животное с трудом поднимается. Расположенные регионарно лимфатические узлы резко увеличиваются и затвердевают. Одновременно развивается одышка, резкое ослабление сердечной деятельности, пульс достигает 100-120 ударов в минуту. Гибель наступает через 12-72 часа.
Сверхострое течение регистрируют редко – преимущественно у молодняка до 3-месячного возраста. Болезнь проявляется в септической форме, при этом отмечают высокую температуру и сильное угнетение, без образования карбункула. Животное гибнет через 6-12 часов.
У отдельных животных, особенно у старых, болезнь может проявляться в атипичной (абортивной) форме без повышения температуры. Отмечают снижение аппетита, небольшое угнетение, незначительную болезненность в отдельных областях мышц без образования отеков.
У овец эмкар протекает острее. Наблюдают пенистое истечение из естественных отверстий, скрежет зубами. Гибель – через 6-24 часа.
Читайте также:

