Дисбактериоз кишечника и лямблиоз
Обновлено: 24.04.2024
Рассмотрены особенности диагностики и лечения лямблиоза у детей. Определена роль диетотерапии и возможности применения энтеросорбентов в комплексном лечении пациентов с лямблиозом и сопутствующим дисбактериозом кишечника.
Peculiarities of diagnostics and treatment of lambliosis with children were considered. The meaning of dietary therapy and the possibilities of interosorbents use in complex therapy of patients with lambliosis and satellite intestine dysbacteriosis were specified.
Лямблиоз является одним из самых распространенных и часто встречающихся протозоозов, протекающим как в виде латентного паразитоносительства, так и в виде манифестных форм с преимущественным поражением тонкого кишечника. Основным источником инвазии является зараженный человек. Механизм передачи заболевания фекально-оральный. Пути распространения — водный, контактный, пищевой.
Воздействие лямблий на организм хозяина многообразно. Вегетативные формы, фиксируясь на поверхности энтероцитов, не только перекрывают всасывательную поверхность кишки и потребляют готовые питательные вещества, но и вызывают механическое и токсическое повреждение поверхности кишечника, запуская целый ряд патологических механизмов: сенсибилизацию организма продуктами распада лямблий и формирование аллергодерматозов, нарушение синтеза ферментов и развитие вторичного синдрома мальабсорбции, формирование абдоминального синдрома, нарушение функции печени, снижение синтеза иммуноглобулинов, формирование дисбиотических нарушений в кишечнике [1, 3–5].
Полиморфизм клинических признаков лямблиоза зачастую затрудняет диагностику данного заболевания [1, 12]. Согласно классификации ВОЗ нами ежегодно регистрируются: лямблиоз без клинических проявлений (латентный) в 2% случаев, лямблиоз с клиническими проявлениями (манифестный) в 98% случаев. Из манифестных форм кишечную форму заболевания мы наблюдаем в 15% случаев, билиарно-панкреатическую форму — в 9%, форму с внекишечными проявлениями — в 30%, смешанную форму — в 44% случаев соответственно.
Наши исследования показали, что в целом кишечный синдром при различных формах лямблиоза проявляется: болью в животе у 30% больных, диареей у 57%, запорами у 29%, тошнотой и анорексией у 70% пациентов соответственно. У 20–40% детей в зависимости от формы заболевания имеет место лактазная недостаточность. Дисбактериоз кишечника при лямблиозе мы регистрируем у всех детей и подростков — 100% [6].
Под дисбактериозом кишечника понимают клинико-лабораторный синдром, связанный с изменением качественного и/или количественного состава микрофлоры кишечника с последующим развитием метаболических и иммунологических нарушений и возможным развитием желудочно-кишечных расстройств [9]. Многими исследователями доказано, что дисбактериоз кишечника является не только сопутствующим клинико-лабораторным синдромом основной соматической патологии желудочно-кишечного тракта, но и может самостоятельно являться дебютом многих патологических состояний, особенно у детей раннего возраста.
Терапия лямблиоза преследует цель полной эрадикации лямблий из кишечника, поэтому ее успешность во многом зависит от комплексного подхода к лечению, включающего назначение: противолямблиозных средств, энтеросорбентов, препаратов, восстанавливающих функцию желчного пузыря, пробиотиков, пребиотиков, при необходимости антигистаминных средств, гепатопротекторов и иммунокорректоров [4, 5]. Очень важно при лечении лямблиоза правильно назначить диету, соответствующую возрасту ребенка, форме заболевания, сопутствующей патологии. Хорошо себя зарекомендовала диета, богатая мягкими пищевыми волокнами-энтеросорбентами, а также поддерживающая фитотерапия, оказывающая противовоспалительное, обволакивающее, регенерирующее действие на слизистую желудочно-кишечного тракта [3].
В настоящее время в медицинской практике используется большое количество энтеросорбентов, различающихся по лекарственной форме, по химической структуре, по механизму сорбции, селективности. Диапазон клинических эффектов энтеросорбции достаточно широк. Наиболее значимыми являются: дезинтоксикационный, антидиарейный, противовоспалительный, метаболический, цитопротекторный эффекты. Помимо этого энтеросорбенты (особенно пищевые волокна) обладают способностью поддерживать микробиоценоз кишечника [13].
Ввиду неоднородности кишечного синдрома при лямблиозе энтеросорбенты специалистами назначаются индивидуально: при запорах предпочтительны препараты, содержащие лигнин с лактулозой, при диарейном синдроме — препараты, содержащие смектит. Но, к сожалению, практика показывает, что не всегда наши пациенты при назначении энтеросорбентов чувствуют себя комфортно: в одних случаях усиливается газообразование и боль в животе, в других — происходит резкая смена диареи на запор, в-третьих — не всегда возможен длительный курс выбранного сорбента. Поиск альтернативных методов лечения привел к изучению клинико-лабораторной эффективности препарата Мукофальк у детей с лямблиозом и сопутствующим дисбактериозом кишечника.
1) оценить переносимость Мукофалька у детей;
2) изучить клиническую и лабораторную эффективность Мукофалька при лямблиозе у детей с диарейным синдромом и синдромом запора;
3) изучить лабораторную эффективность Мукофалька при сопутствующем дисбактериозе кишечника у детей.
В литературе имеются данные об успешном использовании Мукофалька в лечении пациентов с различными синдромами в гастроэнтерологической и гепатологической практике [2, 11, 15], при инфекционных болезнях: иерсиниозе, эшерихиозе и сальмонеллезной инфекции. Исследователями доказано, что Мукофальк не только адсорбирует бактерии, снижает эозинофильно-клеточную инфильтрацию слизистой, но и приводит к выраженному сдвигу рH в кислую сторону, ингибируя рост патогенных энтеробактерий [7, 8, 14].
Материалы и методы
Основная группа: 30 детей 3–14 лет с лямблиозом и сопутствующим дисбактериозом кишечника, получающие Мукофальк в комплексном лечении. Кишечный синдром проявлялся болями в животе, метеоризмом, 15 из 30 детей страдали синдромом диареи, 15 детей — запорами.
Контрольная группа: 60 детей 3–14 лет с лямблиозом и сопутствующим дисбактериозом кишечника, не получающие Мукофальк: 30 детей с синдромом диареи получали сорбенты, содержащие лигнин или смектит, 30 детей с запорами получали кремний- или лактулозосодержащие препараты.
По клиническому анализу крови анемия I–II степени выявлена у 30% наблюдаемых детей, повышенное СОЭ у 6,6%, увеличение в лейкоформуле эозинофилов у 30%, моноцитов — у 40% детей соответственно.
При копрологическом исследовании фекалий слизь наблюдали у 40% всех пациентов, количество лейкоцитов до 5–15 в поле зрения — у 26,6%, нейтральный жир — у 30%, жирные кислоты — у 20%, крахмал — у 43,3%, дрожжевые клетки — у 66,6% пациентов. В ряде случаев определяли повышенное содержание углеводов в кале.
Дефицит облигатной микрофлоры наблюдали у 60% детей основной и 58,3% детей контрольной групп. У детей 3–6 лет дисбактериоз кишечника был обусловлен условно-патогенными бактериями преимущественно одного-двух, редко трех видов, у детей старше 6 лет и подростков регистрировали в основном дефицитный дисбактериоз кишечника. Но во всех возрастных группах наблюдали тенденцию к росту клебсиелл, стафилококка, гемолитических эшерихий и грибов рода Candida (табл. 1).
Способ применения и дозы: дети 3–6 лет получали Мукофальк в дозе 1/4 пакета 2–3 раза в день, 6–12 лет 1/2 пакета 2–3 раза в день, старше 12 лет 1 пакет 2–3 раза в день. При запорах препарат рекомендовался предпочтительно между приемами пищи с достаточным количеством жидкости, при диарейном синдроме — предпочтительно с приемом пищи. После купирования кишечного синдрома Мукофальк был рекомендован 1 раз в день с пребиотической целью в течение 2–4 недель параллельно со следующими этапами лечения лямблиоза.
Критериями оценки эффективности были:
1) клиническая эффективность при кишечном синдроме;
2) лабораторная эффективность: клинические анализы (крови, мочи, исследование кала на копрограмму, простейшие), бактериологические анализы кала на дисбактериоз.
Результаты исследования
На фоне терапии Мукофальком ни у одного ребенка не было аллергических реакций и побочных явлений в виде усиления метеоризма, запоров или диареи. При неэффективности Мукофалька при запорах у детей назначение было увеличено на одну рекомендуемую нами дозу (1 прием).
После проведенного курса лечения у детей с диарейным синдромом основной и контрольной групп жалобы на жидкий стул, боли в животе и метеоризм купированы: в основной группе, получающей Мукофальк, у 13 из 15 больных (86,6%), в контрольной группе — у 22 из 30 больных (73,3%).
У детей же с синдромом запора после лечения жалобы на задержку стула, плотные каловые массы, боли в животе и метеоризм купированы в основной группе, получающей Мукофальк, у 14 из 15 детей, что составило 93,3% наблюдений и было достоверно выше (р < 0,05), чем в контрольной группе — у 19 из 30 детей (63,3%). Данные представлены в табл. 2.
Клинические показатели крови и мочи у детей после лечения были в пределах нормы у 28 детей основной (93,3%) и 54 детей контрольной группы (90%). Копрологические показатели нормализовались у 27 детей основной (90%) и 49 детей контрольной группы (81,6%).
Контроль эффективности лечения лямблиоза по рекомендациям разных авторов проводится через 5–6, 10–14 дней после лечения. Существует мнение, что при выделении лямблий в срок до трех недель после химиотерапии можно говорить о рецидиве заболевания, а в более поздние сроки — о реинфекции [12], хотя в некоторых источниках отмечено, что рецидивы лямблиоза могут возникать спустя 7 недель после окончания лечения [10].
По результатам паразитологических исследований пациентов через 10 дней после лечения санация кишечника от лямблий отмечена у 90% больных основной (27 детей) и 86,6% детей контрольной группы (52 ребенка). Через 20 дней в основной группе, продолжающей получать Мукофальк в пребиотической дозе, показатели не изменились (90%), в контрольной группе — несколько ухудшились, санация кишечника отмечена у 80% больных (48 детей).
По результатам собственных исследований и литературным данным эффективность первого курса комплексного лечения лямблиоза составляет 70–96,8% [1, 5, 6] и зависит от многих факторов: интенсивности инвазии, реактивности организма, выбранных препаратов для лечения, развивающейся резистентности лямблий к специфическим противолямблиозным средствам.
Всем наблюдаемым пациентам с рецидивом заболевания был назначен второй курс лечения, включающий противолямблиозные препараты, симптоматическую и патогенетическую терапию. Энтеросорбенты были рекомендованы соответственно поставленным целям исследования: основная группа получала Мукофальк в рекомендуемых дозировках, контрольная — сорбенты, содержащие лигнин или смектит в зависимости от кишечного синдрома. Через 4 недели после второго курса лечения в основной группе санация от лямблий была отмечена у 100% детей (30 человек), что было достоверно выше (р < 0,05), чем в контрольной группе — у 85% детей (51 ребенок). Результаты наблюдений представлены в табл. 3.
У детей основной группы, продолжающих получать Мукофальк после основных этапов эрадикации лямблий из кишечника в качестве пребиотика параллельно с пробиотиками, было отмечено улучшение бактериологических показателей каловых масс: повышение роста бифидумбактерий у 90% детей, лактобактерий — у 75% детей, кишечной палочки — у 75% детей. Максимальный санирующий эффект наблюдался при эшерихиозном дисбактериозе кишечника (обусловленном гем+ E. coli) — в 100%, кандидозном — в 91%, клебсиеллезном — в 90%, стафилококковом дисбактериозе кишечника — в 87,5% случаев соответственно. Результаты исследований представлены в табл. 4.
Исследования показали, что в основной группе пациентов после курса лечения сравнительно чаще, чем в контрольной, в кишечнике регистрировали рост бифидумбактерий (р < 0,05) и снижение роста гемолизирующей кишечной палочки (р < 0,05) и грибов рода Candida (р < 0,05).
Выводы
- При условии индивидуального терапевтического подхода переносимость препарата Мукофальк у детей начиная с 3-летнего возраста была хорошей. Отмечены приятные вкусовые качества, отсутствие аллергических реакций, удобство в применении.
- Главный критерий эффективности — клинический эффект по исследуемому кишечному синдрому наблюдался в целом у 90% пациентов (86,6% — при диарейном синдроме, 93,3% — при синдроме запора).
- Изучение микробного пейзажа фекалий после курса лечения выявило: повышение роста бифидумбактерий у 90% детей, лактобактерий — у 75% детей, кишечной палочки — у 75% детей, санацию желудочно-кишечного тракта от гемолизирующей кишечной палочки — в 100%, грибов рода Candida — в 91%, клебсиелл — в 90%, золотистого стафилококка — в 87,5% случаев. В основной группе пациентов после курса лечения сравнительно чаще, чем в контрольной, в кишечнике регистрировали рост бифидумбактерий (р < 0,05) и снижение роста гемолизирующей кишечной палочки (р < 0,05) и грибов рода Candida (р < 0,05).
- После окончательного курса лечения в основной группе пациентов санация от лямблий была отмечена у 100% детей, в контрольной группе — у 85% детей.
Заключение
Литература
Е. Е. Хасанова, кандидат медицинских наук
ГАУЗ РКИБ им. проф. А. Ф. Агафонова Минздрава Республики Татарстан, Казань

Лямбль Душан Федорович - отечественный терапевт, анатом, доктор медицинских наук, профессор (1860). В 1859 году Д.Ф. Лямбль стал первооткрывателем одноклеточного простейшего, носящего сейчас его имя, - Lamblia intestinalis. Эти простейшие могут находиться в двух формах - вегетативной и в виде цист.
Обитают лямблии в тонкой кишке человека, который и служит резервуаром паразита. Лямблиозу - присущи как нарушения функции тонкой кишки, так и бессимптомное носительство возбудителя, причем последнее встречается чаще.
Источником заражения лямблиями является человек, выделяющий в некоторые дни с испражнениями до 2 миллионов цист в сутки. Выделенные цисты малоустойчивы и вне кишечника быстро погибают. Заражение лямблиями происходит алиментарным путем. Факторами передачи являются загрязненные фекалиями, содержащими цисты лямблий, руки, вода, пищевые продукты, предметы ухода. Цисты лямблий в фекалиях при температуре 4-5оС сохраняют жизнеспособность до 3 недель, в воде при температуре 18оС до з месяцев. Особую значимость в детских коллективах имеют загрязненные руки и предметы обихода. Цисты лямблий могут разноситься мухами и тараканами. Продолжительность жизни лямблий в организме человека при отсутствии повторного заражения колеблется от 3 до 4о дней, в среднем 4 недели.
До сих пор единого мнения о степени патогенности лямблий нет. Роль лямблий в патологии внутренних органов часто преувеличивается, особенно в случаях, когда клиника рассматривается без учета биологических и морфологических особенностей этих простейших и взаимоотношений паразита и хозяина. Достоверно установлено, что лямблии обитают на поверхности слизистой оболочки и не способны внедрятся в ткань тонкого и толстого кишечника, желчного пузыря, печени, желудка в отличие от амеб и балантидий. Развитие деструктивных изменений при их паразитировании не наблюдалось, что подтверждалось на операциях желчного пузыря и кишечника.
Наблюдения группы ученых; Р.Ф. Акимовой, В.Т. Москалевым, Я.Д. Вишебским и др. показано, что рассматривать лямблии в качестве тканевых паразитов не представляется возможным, поскольку внутри ворсинок кишки они не обнаруживаются и воспалительной реакции в окружающей их ткани не вызывают.
Проведенные клинические и экспериментальные исследования еще раз опровергли наличие выделения лямблиями токсинов, а следовательно, и возможности интоксикации организма при наличии лямблиозной инвазии. Многочисленные, кропотливые клинические и экспериментальные исследования не подтвердили этиологической роли лямблий в развитии патологического процесса в пищеварительном тракте, и особенно в желчном пузыре и печени. Безуспешные попытки экспериментального заражения животных и волонтеров введением лямблий в желчный пузырь и гибель этих простейших при воздействии на них концентрированной желчи (куда их ввели), убедительно свидетельствуют о неспособности лямблий обитать в желчном пузыре и печени, т.к. желчь является агрессивной средой для них.
Ложным мнением считается возникновение и аллергического синдрома, проявляющегося эозинофилией, эозинофильными легочными инфильтратами, крапивницей, атопическим дерматитом, бронхиальной астмой при лямблиозной инвазии. При обследовании этих групп больных у них отмечались глистные инвазии, заболевания желудочно кишечного тракта, профессиональные вредности. Доказательств об аллергической роли лямблий так и не получено.
Лямблиоз в основном проявляется в форме бессимптомного носительства и только в 10-12% случаев отмечаются слабовыраженные функциональные растройства тонкой кишки. Довольно часто лямблии обнаруживаются на фоне расстройства пищеварения различной этиологии. Описание клиники лямблиоза в большинстве случаев сводится к описанию клиники имеющихся заболеваний органов пищеварения на фоне которых выявлен лямблиоз.
Постановка таких диагнозов, как лямблиозный холецистит, лямблиозный гепатит, лямблиозный язвенный колит, является следствием упрощенного толкования результатов исследования. Широкая инвазивность лямблиями и обнаружение их в сочетании с различными желудочно - кишечными заболеваниями нередко служат основанием для приписывания лямблиям ведущей роли в патологических процессах, причинно с ними не связанных.Это часто приводит врачей к диагностическим ошибкам и нередко несвоевременному распознованию тяжелых болезней.
Экспериментально установлено, что у здорового человека с нормальной кишечной флорой, попавшие вредные микробы яйца глистов, лямблии проходят транзитом через кишечник. У человека с наличием заболеваний органов пищеварения, с угнетением желудочной секреции, воспалением слизистой кишечника, панкреатите, наличием дисбактериоза этого не происходит.
Это открытие позволило нам расценивать обнаружение лямблиоза как проявление степени выраженности дисбактериоза кишечника (лямблии - индикатор дисбактериоза). Становится ясным теперь тот факт, что описываемая клиника лямблиоза, есть ни что иное, как клиника.
Хронического энтероколита с дисбактериозом, а порой протекающего с осложнениями в виде крапивницы, атопического дерматита и др.
Рассуждая таким образом, меняется и сам подход в лечении больных с лямблиозом. Теперь, все лечебные мероприятия врача должны быть направлены не на уничтожение лямблий, а на снятие воспаления слизистой кишечника и востановление его микроэкологии. При назначении такого лечения у пациентов быстро купировались клинические проявления болезни и по мере восстановления кишечной микрофлоры наступало очищение организма от лямблий.
Назначение противолямблиозных препаратов показано, не только при высокой степени обсемененности лямблиями и очень коротким курсом т.к. противолямблиозные препараты оказывают высокотоксичный эффект на организм, ухудшая тем самым состояние его интоксикации, слизистой кишечника и микрофлоры.
В заключении хочется отметить, что обнаружение лямблий (индикатор дисбактериоза) имеет большое практическое значение в тех случаях, когда нет условий для выполнения бактериологических анализов кала на дисбактериоз наличие лямблий 100% дисбактериоз кишечника, его IV фазы. Мы считаем, что метод лечения всегда качественен в руках авторов, поэтому приглашаем пациентов у которых выявили лямблиоз на лечение в центр гастроэнтерологии Дулькина Л.А.
Что такое лямблиоз? Причины возникновения, диагностику и методы лечения разберем в статье доктора Александрова Павла Андреевича, инфекциониста со стажем в 14 лет.
Над статьей доктора Александрова Павла Андреевича работали литературный редактор Маргарита Тихонова , научный редактор Сергей Федосов

Определение болезни. Причины заболевания
Лямблиоз — это острое и хроническое паразитарное заболевание человека в виде манифестных форм или носительства, вызываемое кишечными лямблиями, которые колонизируют слизистую оболочку преимущественно тонкого кишечника, нарушают процессы пристеночного пищеварения и способствуют развитию и усугублению поражения желудочно-кишечного тракта и других заболеваний.
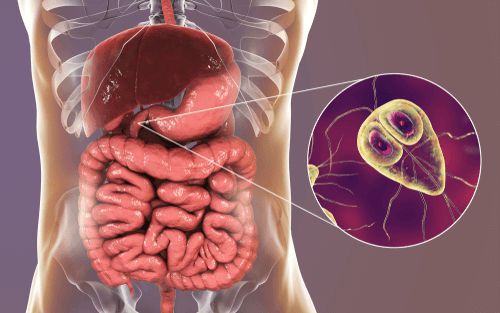
Этиология
Возбудитель — лямблия. Данный род паразитов включает в себя шесть типов, но заболевание человека вызывает только один тип — кишечная лямблия (Giardia duodenalis, Giardia lamblia, Giardia intestinalis). Это жгутиковое микроскопическое простейшее, впервые описанное чешским медиком-анатомом Д.Ф. Лямблем в 1859 году. Оно имеет до восьми генетических подтипов, но для человека патогенны только А и В (также имеют подтипы).
Вид — Giardia lamblia
Возбудитель лямблиоза (кишечная лямблия) существует в виде двух жизненных форм:
- вегетативная (трофозоиты) — стадия активного размножения внутри организма;
- цистная — образуется при неблагоприятных условиях среды.
Трофозоиты — это анаэробные, грушевидные микроорганизмы размерами 9-18 мкм. Они обитают в верхних отделах тонкого кишечника. Подвижны (имеют характерное движение в виде вращения вокруг продольной оси — боковое движение), тело спереди расширено и закруглено, сзади сужено и заострено. Имеют в составе два ядра (между ними пролегают опорные нити — аксостили) и парные органоиды — четыре жгутика и два медиальных тела.
Трофозоиты не имеют цитостома — органа заглатывания пищи и пищеварительной вакуоли, поэтому они всасывают пищу, переваренную хозяином (в основном, углеводы), всей поверхностью тела. Это называется осмотическим питанием.
Как выглядят лямблии:
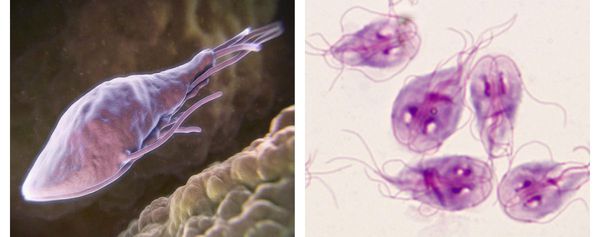
В передней их трети тела расположен присасывательный диск в виде специального углубления. С его помощью лямблии прикрепляются к ворсинкам слизистой оболочки тонкого кишечника. Цитоплазматическая мембрана задней поверхности имеет по краям булавовидные выросты, что также создаёт дополнительную прикрепляющую составляющую.
Размножаются путём продольного деления. Слабо устойчивы в условиях окружающей среды при покидании организма хозяина: при комнатной температуре даже в отсутствии агрессивных факторов быстро погибают.
Цистная форма неподвижна. Паразиты имеют овальную форму, лишены свободных жгутиков (сложно свёрнутые), их размеры достигают 10-14 мкм, окружены толстой, несколько отделённой от тела оболочкой (данная особенность имеет значение при распознавании вида).
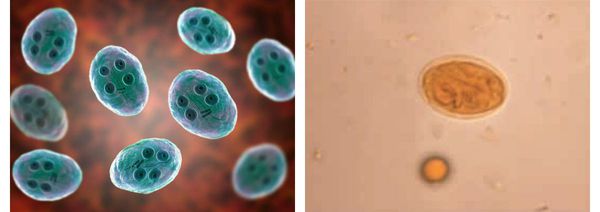
Зрелые цисты внутри имеют четыре ядра, незрелые — два ядра. Образуются в нижних отделах кишечника в процессе выхода из организма с фекалиями. Очень устойчивы во внешней среде: могут сохраняться месяцами в воде при температуре 4-20°C, при хорошей влажности способны сохраняться на контаминированных (обсеменённых) продуктах питания до недели. При кипячении цисты погибают мгновенно, а при высушивании и низкой влажности гибель наступает в течении суток. Устойчивы к бытовому хлорированию воды, действию щелочей и кислот, ультрафиолетовому излучению. Низкие температуры переносит относительно хорошо, но при этом снижая свою жизнеспособность. [1] [3] [6] [9]
Эпидемиология
Распространение заболевания повсеместное, преимущественно в странах с влажным тёплым климатом. Только официально выявляемые случаи в России приближаются к 150 тысячам в год.
Сезонность выражена неярко, некоторый всплеск заболеваемости отмечается в тёплое время года. Возрастной состав больных склоняется в сторону детей.
Источник заражения — люди (больные различными формами лямблиоза и паразитоносители), причём наибольшая заразность наблюдается в подостром периоде заболевания, когда в 1 г фекалий может содержаться до нескольких десятков миллионов цист. Лямблии животных (нечеловеческие типы паразитов) не имеют доказательной базы в плане распространения и заражения человека.
Факторами передачи паразитов выступает загрязнённая цистами термически не обработанная питьевая вода, пища, грязные руки (возможна прямая передача от человека к человеку). Определённую роль в передаче лямблий играют насекомые (тараканы, мухи) и животные (собаки, кошки) — они являются механическими переносчиками (паразиты располагаются на их теле, шерсти, лапках, транзитом в кишечнике).
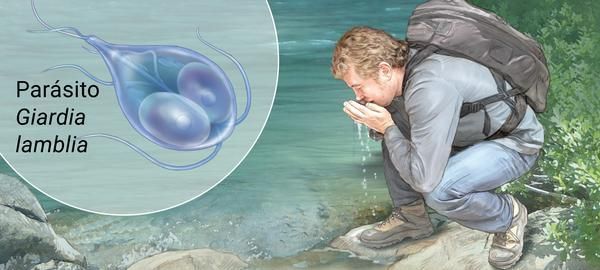
Механизм передачи — фекально-оральный (водный, пищевой и контактно-бытовой пути). Наиболее часто передача осуществляется:
- через водопроводную воду;
- при употреблении плохо промытых зелени и овощей (или промытых под водопроводной водой без последующей термической обработки);
- при нарушении правил санитарной гигиены, особенно в детских коллективах.
Доза заражения — от 10 до 100 цист (в зависимости от индивидуальных свойств иммунной реактивности кишечника). Возможны случаи невосприимчивости к паразитам: цисты лямблий, встречая агрессивно настроенную среду кишечника, проходят транзитом и выделяются в окружающую среду в неизменённом виде.
Иммунитет после лямблиоза нестойкий и ненапряжёный, возможно повторное заражение. Повышенный риск заболевания имеют лица с патологией иммунитета кишечника и дефицитом IgA. [2] [3] [5] [8] [10]
При обнаружении схожих симптомов проконсультируйтесь у врача. Не занимайтесь самолечением - это опасно для вашего здоровья!
Симптомы лямблиоза
Инкубационный период длится от нескольких дней до месяца и более. Чаще всего при заболевании не наблюдается вообще никаких клинических проявлений, особенно у взрослых.
К основным возможным симптомам лямблиоза относятся:
- Симптомы интоксикации и вегетативных изменений — повышенная утомляемость, плаксивость, раздражительность, нарушение ритма сна, головокружения, аритмии, субфебриллитет и другие.
- Симптомы поражения ЖКТ — дискомфорт и боли различной интенсивности и характера в различных отделах живота, тошнота, снижение аппетита, появление чувства горечи во рту, нарушения стула (запоры и поносы), налёт на языке и неприятный запах изо рта, снижение массы тела и другое.
- Симптомы поражения кожи — аллергические высыпания различного характера и локализации, атопический дерматит, бледность и шероховатость кожи, повышенная сухость покровов, хейлит (воспалительные изменения кожи губ и их слизистой), заеды (трещинки в уголках рта), нетипичное/неконтролируемое течение хронических патологий кожи.
- Усиление развития и обострения заболеваний, прямо не связанных с лямблиозом — бронхиальная астма, псевдоаллергические явления, гастриты, язвы желудка и двенадцатиперстной кишки, холецистит, неспецифический язвенный колит, артриты и другое.
- Симптомы мальабсорбции (потери питательных веществ) — авитаминозы, отставание в физическом и умственном развитии, дистрофия (эти проявления более характерны для детей).
Лямблиоз у детей
Как правило, у детей первыми симптомами лямблиоза становится появление субфебрильной или фебрильной температуры (37,1–38,0°C или 38,0–39,0°C), болей в животе, тошноты, иногда рвоты, метеоризма, жидкого стула. Живот при этом болезнен, вздут, урчит по ходу кишечника. Грудные дети становятся беспокойными, кричат, нарушается сон, симптомы лямблиоза усиливаются во время и после кормления, возможно появление аллергодерматозов и опрелостей. В динамике при отсутствии лечения это может приводить к нарушению роста и психоэмоционального развития, частым простудным или аллергическим заболеваниям, развитию хронических проблем органов ЖКТ.
У детей более позднего возраста и взрослых яркие симптомы лямблиоза наблюдаются редко — на первый план выходит постепенное развитие диспепсических явлений со стороны ЖКТ умеренного характера:
- метеоризм;
- дискомфорт и боли в животе преимущественно в околопупочной области и правом подреберье;
- нарушения стула в различных сочетаниях;
- появление налёта на языке;
- иногда горечь во рту и кожные проявления (усиление выраженности угревой сыпи, хронических полиэтиологических заболеваний, например, псориаза и дерматитов);
- возможны вегетативные расстройства, головные боли, головокружения, неустойчивость артериального давления, повышения температуры тела, чувствительность лимфоузлов.
Лямблиоз у беременных
Лямблиоз у беременных не имеет каких-либо специфичных отличий от лямблиоза у остальных людей, но может приводить к повышению риска развития у беременной В-12 дефицитной анемии и снижению веса плода (гипотрофии). [1] [3] [5] [7] [10]
Патогенез лямблиоза
Характерен так называемый "симптом манной крупы" — белёсые полусферические выбухания слизистой оболочки двенадцатиперстной кишки, представляющие собой зоны очагового отёка со скоплением увеличенного количества лейкоцитов.
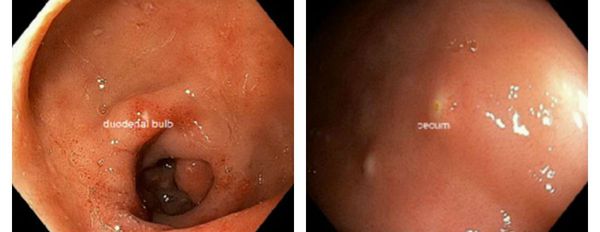
Посредством механического раздражения и выделения паразитами продуктов жизнедеятельности (токсическое влияние) происходит стимуляция образования слизи, повышение регенераторной функции кишечника, нарушение выработки факторов нейрогуморальной регуляции пищеварения (холецистоцикин и других) и двигательной активности гепатогастродуоденальной области. Это ведёт к дезорганизации висцеро-висцеральных связей области двенадцатиперстной кишки, поджелудочной железы и желчевыводящей системы, а также к нарушению функционирования органов ЖКТ, нарушению микробиоценоза кишечника, активизации анаэробной флоры, расстройствам расщепления и всасывания белков, жиров, углеводов, витаминов и микроэлементов.
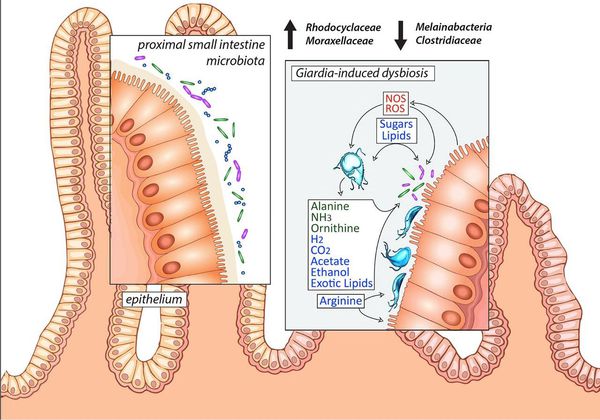
Возникает воспаление слизистой кишечника по типу реакций гиперчувствительности замедленного типа, происходит воздействие на иммунорегуляторные белки (мимикрия), снижение выработки иммуноглобулинов (в частности IgA) из-за нарушения всасывания белков и снижение фагоцитарной активности. Всё это в совокупности со всасываемыми продуктами жизнедеятельности лямблий становится причиной истощения иммунной системы (как кишечника, так и общего иммунитета), развития хронического поражения кишечника, провоцирует длительное обострение имеющихся хронических заболеваний и усугубление ряда аллергозависимых дерматозов. [1] [4] [7] [8]
Классификация и стадии развития лямблиоза
По клинической форме лямблиоз бывает:
- бессимптомным (носительство);
- кишечным — преимущественно симптомы кишечной формы, но можгут быть и гастритические проявления (дискомфорт в животе, неустойчивый стул, тошнота);
- билиарно-панкреатическим (рефлекторный) — дискомфорт в эпигастрии и правом подреберье, привкус горечи во рту, повышенная частота развития плохо контролируемых гастродуоденитов и панкреатитов;
- астено-невротическим — слабость, вялость, повышенная утомляемость, раздражительность, эмоциональная неустойчивость;
- токсико-аллергическим — периодические высыпания на теле, обострение хронических кожных заболеваний и бронхиальной астмы, эозинофилия;
- смешанным.
Течение лямблиоза бывает трёх типов:
- острым — до одного месяца;
- подострым — 1-3 месяца;
- хроническим — более трёх месяцев.
По наличию осложнений лямблиоз бывает:
Выделяют три степени заболевания:
Осложнения лямблиоза
Возможны специфические и неспецифические осложнения лямблиоза.
К специфическим относятся:
-
— зудящие обширные высыпания на теле;
- отёк Квинке — выраженный отёк подкожной клетчатки, иногда сопровождающийся зудоим и чувством удушья;
- офтальмопатия — нарушения восприятия органом зрения;
- артрит — дискомфорт и боли в суставах;
- гипокалиемическая миопатия — слабость определённых групп мышц.
К неспецифическим осложнениям относятся:
- наслоение интеркуррентных заболеваний (вторичная флора);
- белково энергетическая недостаточность (гипо- и авитаминоз, снижение веса, анемия и другие). [1][2][8][10]
Диагностика лямблиоза
Лабораторная диагностика лямблиоза включает в себя:
- Клинический анализ крови — в остром периоде наблюдается эозинофилия, базофилия и повышение СОЭ; в последующие периоды — умеренная эозинофилия или нормальное значение эозинофилов, иногда незначительная базофилия.
- Биохимический анализ крови — иногда отмечается повышение уровня общего билирубина и амилазы.
- Копроовоскопическое исследование кала — "золотой стандарт" диагностики. Оно позволяет выявить цисты (наиболее часто) и вегетативные формы лямблий (в редких случаях). В виду прерывистого цистообразования показано неоднократное исследование с некоторым интервалом (семь дней). Существует широко распространённое заблуждение о том, что кал нужно сдавать "тёплым" (свежим). На самом деле, в этом нет никакой необходимости. Так как данное исследование предполагает обнаружение цист лямблий, которые очень устойчивы во внешней среде, период от дефекации до исследования никоим образом не влияет на информативность результата анализа.
- Иммунохроматографический метод и ПЦР-диагностика кала (выявление антигенов и нуклеиновых кислот паразита) — имеет хорошую информативность и вполне может применяться в комплексе с другими методами исследований.
- ИФА-диагностика — малоинформативное исследование, так как локализация лямблий в просвете кишечника не создаёт условий для полноценного иммунного ответа, который наблюдается в основном у детей при остром заболевании, что создаёт значительное число ошибочных результатов как гипо-, так и гирпедиагностики.
- Дуоденальное зондирование (выявление вегетативных форм лямблий в двенадцатиперстной кишке) — может применяться в сложных диагностических случаях и при подозрении на коинвазирование (например, описторхами при описторхозе).
- УЗИ органов брюшной полости и ФГДС — позволяют выявить признаки нарушения моторики гепатобилиарной области. [2][3][5][6][9]
Дифференциальная диагностика предполагает исключение следующих заболеваний:
- паразитарные заболевания другой этиологии (как кишечной, так и внекишечной локализации);
- хронический гастродуоденит (симптомосходная симптоматика);
- кишечные инфекции (сальмонеллёз, дизентерия, ротавирус и другие);
- дисбиоз кишечника (сборное понятие, характеризующееся неустойчивостью стула, дискомфортом в животе различного характера, снижением веса и другими симптомами). [1][5][9]
Лечение лямблиоза
Лечение острой формы лямблиоза, которая возникает в основном у детей, должно осуществляться в стационаре и включать в первую очередь дезинтоксикационную и дегидратационную терапию, а также щадящее питание.
Медикаментозная терапия
При подтверждении диагноза проводится этиотропное лечение одним из противолямблиозных препаратов (нитрогруппа) в сочетании с желчегонными средствами, и лекарствами, улучшающими микрофлору кишечника.
При длительном хроническом течении в виду персистирующей колонизации лямблиями слизистой оболочки тонкого кишечника и местным иммунодефицитом курс лечения должен быть комплексным, включающим:
- диета (потреблять меньше углеводов);
- средства этиотропного воздействия (химиопрепарат);
- приём желчегонных препаратов;
- иммунотерапию (усиление фагоцитоза и восполнение дефицита IgA);
- устранение дисбиоза кишечника (пробиотики).
К сожалению, в последнее время всё чаще встречаются штаммы лямблий, устойчивых к различным видам противопаразитарной терапии, поэтому средняя вероятность успешной эрадикационного лечения не превышает 85%.
Гигиена при лечении лямблиоза
Лямблиоз редко передаётся между членами семьи, если соблюдать простейшие гигиенические правила: мыть руки после посещения уборной, перед едой и после контакта с животными.
Лечение народными средствами
Эффективность и безопасность методов народной медицины научно не доказана. Без адекватного лечения лямблиоз может привести к различным осложнениям: крапивнице, отёку Квинке, нарушениям зрения, артриту и слабости мышц.
Лечение лямблиоза у детей
Новорождённых от лямблиоза, как правило, не лечат, так как нет подходящих препаратов. В основном рекомендуется улучшать микрофлору и работу кишечника.
Детей старшего возраста лечат так же, как и взрослых, но подбирают необходимую дозировку и форму препарата.
Лечение лямблиоза у беременных
Беременным лечение, как правило, противопоказано (потенциальный вред препаратов превышает пользу от лечения), в основном предпочтение отдаётся улучшению флоры и работы кишечника.
Контроль излеченности
После курса лечения проводится паразитологический контроль методом копроовоскопии или ПЦР не ранее двух недель после завершения курса лечения длительностью в три месяца со сдачей анализа раз в месяц. [1] [3] [4] [5]
Прогноз. Профилактика
При назначении адекватного лечения прогноз благоприятен, осложнения редки.
Специфической профилактики не разработано. Основной упор следует делать на меры соблюдения санитарных норм:
Описана клиническая картина и лабораторные отклонения у 71 пациента с инвазией opisthorchis felineus. Из них у 24 человек выявлен лямблиоз. Проведен анализ различных форм описторхоза. Изучено влияние lamblia intestinalis на характер и выраженность клинических и лабораторных симптомов описторхоза. Доказано, что включение ротабиотика или медулака в комплексную терапию описторхоза и лямблиоза с дисбиотическими изменениями приводит к быстрой коррекции качественного и количественного состава микрофлоры кишечника.

1. Авдюхина Т.И., Константинова Т.Н., Кучеря Т.В. и др. Лямблиоз: Учебное пособие. – М.: РМАПО. 2003. – 32 с.
2. Бондаренко В.М., Мацулевич Т.В. Дисбактериоз кишечника как клинико-лабораторный синдром. Современное состояние проблемы. – М.: ГЭОТАР-Медиа, 2007. – 302 с.
3. Крылов Г.Г. Суперинвазионный описторхоз: пато- и морфогенез осложненных форм и микст-патологии / Г.Г. Крылов: Дис. . д-ра мед. наук. – М. – 2005. – 84 с.
4. Начева Л.И., Старченкова Т.Е., Бибик О.И., Додонов М.В. Описторхоз в Кемеровской области // Медицинская паразитология и паразитарные болезни. – №1. М., 2007. – С. 25 – 27.
5. Реброва О.Ю. Статистический анализ медицинских данных. Применение пакета прикладных программ STATISTICA. М.:Медиа Сфера, 2002. – 294 с.
6. Ballongue J, Schumann C, Quignon P. Effects of Lactulose and Lactitol on Colonic Microflora and Enzymatic Activity. Scand J Gastro-enterol 1997; 32 Suppl 222: 41-44.
7. Langlands S. Prebiotic carbohydrates modify the mucosa associated microflora of the human large bowel. Gut. 2004 Nov; 53(11): 1610-6.
8. Mack DJ, Smart L, Girdwood A, Scott PJW, Fulton JD, Erwin L. Infection prophylaxis with Lactulose. Age & Ageing 1993; 22(Suppl.2):8 (№ 18).
9. Mairiang, E., Mairiang, P. Clinical manifestation of opisthorchiasis and treatment. Acta Tropica 88 (2003) 221–227.
10. Thamavit W., Ngamying M., Boobpucknavig V. Enhancement of Den-induced hepatocellular nodule development by Opisthorhis viverrini infection in Syrian golden hamsters. // Carcino-Genesis, 1987. – Vol. 8. – P. 1351-1353.
На территории Свердловской области в течение последних 10 лет отмечаются стабильно высокие показатели заболеваемости описторхозом и лямблиозом. В 2013 году показатель заболеваемости описторхозом составил 36,64 на 100 тыс., а лямблиозом – 66,42 на 100 тыс. населения.
Несмотря на то, что в большинстве случаев лямблиоз у взрослых протекает в виде латентного паразитоносительства, встречаются и клинически манифестные формы. Выраженность клинических проявлений при лямблиозе обусловлена воспалительными и функциональными изменениями верхних отделов желудочно-кишечного тракта При лямблиозной инвазии изменяется качественный и количественный состав кишечной микрофлоры с последующим развитием метаболических и иммунологических нарушений, что усугубляет течение основного заболевания [1].
Одной из причин, ведущих к дисфункции в гастродуоденальной зоне, может быть описторхозная инвазия. В сложном патогенезе описторхоза выделяется несколько основных звеньев: хроническое воспаление, холестаз, присоединение вторичной инфекции, развитие аутоиммунных процессов, гиперчувствительность замедленного типа, формирование паразитарных гранулем. Повторные заражения opisthorchis felineus рассматриваются как дополнительное воздействие, усиливающее иммуносупрессию [3].
Большой интерес представляет изучение паразитоценозов, в частности сочетанной глистно-протозойной инвазии: opisthorchis felineus и lamblia intestinalis [3, 10].
Успех терапии хронической описторхозной инвазии и лямблиоза обеспечивается выполнением основных принципов: комплексность, планирование, специфичность, системность, этапный подход, кратность курсов дегельминтизации. Основной анитигельминтный препарат, использующийся в России для лечения описторхоза – празиквантел [4]. В литературе упоминаются противоречивые данные об антитрематодозной активности других лекарственных препаратов, к числу которых относится: албендазол, который хорошо зарекомендовал себя как антилямблиозный препарат [9]. Выставляя в основу лечения антигельминтик, нельзя забывать о купировании основных патогенетических синдромов, в том числе нарушение качественного и количественного состава микрофлоры кишечника.
Основные требования к современному пробиотику сводятся к следующему: препарат должен содержать от 2 млрд. жизнеспособных бактерий, сохранять стабильность, обладать способностью прикрепляться к стенкам кишечника, иметь доказанную клиническую эффективность и безопасность, обеспечивать антагонизм к условно-патогенной и патогенной микрофлоре, не должен разрушаться под воздействием кислой среды желудка и желчных кислот. Таким требованиям удовлетворяет ротабиотик, представляющий собой комбинацию пробиотических бактерий с инулином [7].
Активным веществом препарата медулак является лактулоза, синтетический дисахарид, не встречающийся в природе. Лактулоза является идеальным питательным субстратом для сахаролитических бактерий. В результате увеличивается биомасса таких бактерий. В такой ситуации возникает конкуренция за питательные вещества, что приводит к угнетению патогенной и условно-патогенной микрофлоры [6]. Лактулоза увеличивает поглощение аммиака из среды, уменьшает образование аммиака бактериями, ингибируект бактериальное разложение аминокислот при помощи механизма катаболического угнетения [8].
Цель исследования – определить эффективность медулака и ротабиотика в комплексной терапии при различных формах описторхозной инвазии инвазии и биинвазии – opisthorchis felineus и lamblia intestinalis на основе клинического обследования больных и оценки качественного и количественного состава микрофлоры кишечника.
Материалы
и методы исследования
Всего обследован 71 пациент: 39 мужчин и 32 женщины. Средний возраст больных составил 43,4±3,5 года.
1. Мужчины и женщины в возрасте старше 18 лет.
2. Впервые установленный клинически манифестный диагноз описторхоза или повторно выявленная инвазия, вызванная opisthorchis felineus специфически не леченная или после одного или двух курсов лечения в сроки не менее шести месяцев до начала исследования.
3. Добровольное согласие пациента на дегельминтизацию и лабораторное тестирование.
4. Выявление яиц opisthorchis felineus в кале и/или желчи.
5. Выявление цист, вегетативных форм lamblia intestinalis в кале и/или желчи и/или обнаружение антител к антигену lamblia intestinalis в крови.
1. Сопутствующая другая паразитарная патология.
2. Хроническое поражение печени, не обусловленное описторхозом.
3. Прием гепатотоксичных препаратов за шесть месяцев до начала исследования.
4. Алкогольная болезнь.
5. Беременные или кормящие женщины.
6. Острое инфекционное заболевание за три месяца до начала исследования.
Больные предъявляли жалобы на боль в правом подреберье и/или в эпигастрии (29,6 %), тяжесть в правом подреберье и/или в эпигастрии (36,6 %), тошноту (25,4 %), горечь во рту (36,6 %), снижение аппетита (33,8 %), неустойчивый стул (66,2 %), диарею (33,8 %), запоры (32,4 %), повышение температуры до субфебрильных цифр (59,2 %), кожный зуд (63,4 %), потливость (53,5 %), сердцебиение (42,3 %). Объективно определялось увеличение печени (100 %), дерматоз (36,6 %).
Учитывались данные эпидемиологического анамнеза: факторы риска заражения за несколько лет. Существенными считались факты диагноза острого или хронического описторхоза и проведение антипаразитарной терапии в прошлом. Пациенты с впервые выявленным описторхозом включены в группу 1 (n=37). Больные с описторхозным анамнезом более трех лет, специфически леченные в прошлом, при наличии факторов риска повторного заражения opisthorchis felineus у которых вновь были обнаружены яйца сибирской двуустки (суперинвазионный описторхоз), включены в группу 2 (n=34).
Лабораторными находками были гиперэозинофилия (у 66,2 %), гипербилирубинемия (45,1 %), повышение активности АЛТ (36,6 %), щелочной фосфатазы (62,0 %), ГГТП (59,2 %), повышение уровня холестерина (45,1 %), увеличение гамма-глобулиновой фракции белка (33,8 %), повышение уровня IgM (36,6 %), IgE (66,2 %), появление циркулирующих иммунных комплексов (63,4 %), С реактивного протеина (33,8 %).
В 100 % случаев описторхоз был подтвержден копроовоскопически и/или билиовоскопически.
Антитела класса IgG к антигенам opisthorchis felineus в крови выявлялись в 66,2 % случаев. Высокий титр антител (> 1/400) зафиксирован в 19,7 %. Низкий титр антител (
Копропротозооскопически в 18,3 % обнаружены цисты или вегетативные формы lamblia intestinalis. Одновременное присутствие цист и вегетативных форм отмечено в 5,6 %, только цист в 12,7 %.
При выявлении признаков лямблиозной инвазии (24 чел.) пациентов включали в группу А (33,8 %): А1 – пациенты группы 1 (n=8) и А2 пациенты группы 2 (n=16). При отсутствии лямблиоза пациентов наблюдали в группе В (n=47): В1 – пациенты группы 1 (n=29) и В2 – пациенты группы 2 (n=18).
Терапия включала три последовательных этапа: подготовительный, антигельминтное лечение и реабилитационный. На подготовительном этапе улучшали функцию желчевыводящих путей, уменьшали явления интоксикации, купировали острые аллергические реакции. По показаниям назначали желчегонные, ферменты, антибактериальные препараты, спазмолитики, глюкокортикостероиды, антигистаминные, адсорбенты, проводили процедуры дуоденального зондирования. Все пациенты принимали препарат холудексан per os 600 – 900 мг в сутки. Подготовительный этап продолжался в течение одного месяца.
В конце подготовительного этапа пациентам, у которых были выявлены цисты и/или вегетативные формы lamblia intestinalis, был назначен препарат гелмодол 800 мг в сутки в два приема по 400 мг per os во время приема пищи в течение 7 дней. Второй этап лечения был идентичный для всех больных: назначался препарат празиквантел в дозе 75 мг/кг веса per os в течение одного дня в три приема.
Реабилитационный этап был направлен на восстановление функций желчевыводящих путей, борьбу с интоксикацией, возникающей в связи с массовой гибелью паразитов и медикаментозной терапией. Пациенты получали препарат холудексан per os 600 – 900 мг в сутки. Реабилитационный этап продолжался в течение четырех месяцев.
Ведение пациентов с выявленным дисбактериозом кишечника (n=35; 49,3 %) определялось в зависимости от наличия или отсутствия диареи. При наличии диарейного синдрома (группа Р; n=15) на реабилитационном этапе пациенты рандомизированы: P+ (n=8) получали препарат ротабиотик по две капсулы три раза в сутки в течение 10 дней, Р– (n=7) ротабиотик не получали. При отсутствии диареи (группа М; n=20), больные рандомизированы на: M+ (n=12) принимали препарат медулак по 10 мл три раза в сутки per os во время приема пищи 10 дней на подготовительном этапе и 20 дней на реабилитационном этапе, M– (n=8), медулак не принимали. Доза медулака титровалась в зависимости от слабительного эффекта. Средняя суточная доза составила 21,5±0,5 мл
в сутки.
Контрольная копропротозооскопия и/или билипротозооскопия на наличие цист и/или вегетативных форм lamblia intestinalis выполнялась через 7 дней, 1 и 6 месяцев после антипротозойного лечения албендазолом (гелмодолом). Контрольная копроовоскопия и/или билиовоскопия на наличие яиц opisthorchis felineus проводились через 6 месяцев после антигельминтного лечения празиквантелом.
Статистическая обработка полученных данных проводилась c использованием пакета прикладных программ «STATISTICA 6,0 фирмы StatSoft Inc.
(США) [5].
Результаты исследования
и их обсуждение
На этапе скрининга при сравнении частот встречаемости признаков в группах 1 и 2 выявлены большие значения в группе 2 по следующим симптомам: боль в правом подреберье и/или в эпигастрии, тяжесть в правом подреберье и/или в эпигастрии, диарея, повышение температуры до субфебрильных цифр, кожный зуд, дерматоз, гиперэозинофилия, гипербилирубинемия, повышение активности АЛТ, щелочной фосфатазы, повышение уровня холестерина, увеличение гамма-глобулиновой фракции белка, IgE, появление циркулирующих иммунных комплексов (p<0,05).
У пациентов с суперинвазионным описторхозом реже выявляются антитела к opisthorchis felineus, чаще в низком титре, чаще определяются цисты или вегетативные формы lamblia intestinalis и антитела IgG к lamblia intestinalis в низком титре. Характерным для суперинвазии opisthorchis felineus оказалось также преобладание частоты выявления цист и/или вегетативных форм lamblia intestinalis у серонегативных по IgG к lamblia intestinalis пациентов.
Пациенты групп А1 и В1 существенно не отличались по частоте встречаемости основных клинических проявлений. Отмечена разница только по диарее: в группе А1 данный симптом встречался чаще (p<0,05). У пациентов, инвазированных lamblia intestinalis чаще определялся высокий титр к opisthorchis felineus (табл. 1).
Сравнение больных групп А2 и В2 также показало некоторое преобладание частоты встречаемости в группе А2 по диарее, а также по кожному зуду и дерматозу (p<0,05). Кровь больных, зараженных lamblia intestinalis при суперинвазионном описторхозе, чаще давала позитивный результат IgG к opisthorchis felineus в высоком титре (табл. 1).
Сравнивая клинические проявления у пациентов, инвазированных lamblia intestinalis, с разными формами описторхоза (группы А1 и А2), получены результаты практически сходные при сравнении групп 1 и 2. Преобладало значение частоты в группе А2 по симптомам: боль в правом подреберье и/или в эпигастрии, повышение температуры до субфебрильных цифр, кожный зуд, дерматоз, гиперэозинофилия, гипербилирубинемия, повышение активности АЛТ, щелочной фосфатазы, увеличение гамма-глобулиновой фракции белка, IgE, появление циркулирующих иммунных комплексов (p<0,05). IgG к opisthorchis felineus, чаще определялись в группе А1 и более высоком титре. Цисты и вегетативные формы lamblia intestinalis чаще выявлялись у больных с суперинвазионным описторхозом, в то время как только цисты – у пациентов с впервые выявленной описторхозной инвазией. У больных группы А2 реже выявляются антитела к lamblia intestinalis, реже одновременно тестируются и антитела и копропротозооскопические находки лямблий, но чаще определяются серонегативные варианты лямблиоза (табл. 1).
Анализируя клинику у пациентов без лямблиоза с различными формами описторхоза (группы В1 и В2) также не выявлено отличий от сравнения в целом групп 1 и 2. IgG к opisthorchis felineus в более высоком титре определялись в группе В1. В группе пациентов с суперинвазионным описторхозом чаще тестировались IgG к lamblia intestinalis при отсутствии цист и вегетативных форм лямблий, но в низком титре (табл. 1).
Частота выявления антител IgG к opisthorchis felineus, lamblia intestinalis, цист и вегетативных форм lamblia intestinalis в зависимости от формы инвазии ( %)
Лямблиоз у детей – паразитарная инвазия, вызываемая одноклеточными организмами – лямблиями. Лямблиоз у детей может протекать с диспепсическим, болевым, астено-невротическим, интоксикационным, аллерго-дерматологическим синдромами. Диагностика лямблиоза у детей предполагает проведение микроскопического и ПЦР исследования кала и дуоденального содержимого, ИФА крови. Лечение лямблиоза у детей включает специфическую противолямблиозную терапию, диетический режим, проведение тюбажей с холекинетиками, прием ферментативных препаратов и энтеросорбентов.

Общие сведения
Лямблиоз у детей – протозойная инфекция, вызываемая микроскопическими паразитами Lamblia intestinalis (лямблиями). Согласно эпидемиологическим данным, общая распространенность лямблиоза в популяции составляет 2-5%, их них более половины случаев заболевания приходится на детей. В организованных детских коллективах (яслях, садах, школах, интернатах) зараженность детей лямблиозом достигает 30-50%. Восприимчивость к лямблиозной инфекции среди детей младшего возраста в 3 раза выше, чем среди взрослых. Лямблиоз у ребенка может протекать под маской многочисленных заболеваний, поэтому его выявление и предупреждение распространения составляет сложную проблему детской гастроэнтерологии и педиатрии.

Причины
Возбудителем лямблиоза у детей и взрослых выступает Lamblia intestinalis (син.- Giardia lamblia, Giardia intestinales, Giardia duodenalis) - одноклеточный жгутиковый микроорганизм, паразитирующий в кишечнике. В организме человека лямблии могут существовать в двух формах – вегетативной (в верхних отделах тонкого кишечника - двенадцатиперстной и начальном отделе тощей кишки) и споровой (цистной) в толстой кишке, откуда выделяются с испражнениями во внешнюю среду. Вне организма хозяина вегетативные формы лямблий быстро погибают, цисты же сохраняют свою жизнеспособность до 60-70 дней во влажной среде и до 3-х месяцев в водопроводной воде.
Заражение детей лямблиозом происходит посредством фекально-орального механизма, при попадании цист паразитов в пищеварительный тракт ребенка с водой, пищей, при пользовании общими игрушками, посудой и предметами гигиены (носовыми платками, полотенцами), через грязные руки. Новорожденные дети могут заражаться лямблиозом в родах при прорезывании головки. В семьях, где один или несколько детей больны лямблиозом, обычно инфекция имеется у всех остальных членов семьи.
Патогенез
Особенности жизнедеятельности лямблий обусловливают их патогенное воздействие на организм ребенка. При попадании в организм человека лямблии паразитируют в просвете кишечника, многократно присасываясь и открепляясь от слизистой оболочки, чем вызывают повреждение энтероцитов. Вследствие механического повреждения слизистой оболочки в тонком кишечнике активизируется условно-патогенная и патогенная микрофлора. При исследовании кала у детей с лямблиозом нередко обнаруживаются грибы, H.pylori; снижение уровня бифидо- и лактобактерий, кишечной палочки. Дисбактериоз создает благоприятные условия для размножения лямблий в кишечнике, проникновения токсинов во внутреннюю среду организма.
Кроме этого, лямблии выделяют токсические продукты метаболизма, которые нарушают всасывание углеводов, жиров, белков, микроэлементов, витаминов и минеральных веществ в тонком кишечнике, формируя дефицит микронутриентов и поливитаминную недостаточность. При лямблиозе у детей страдает синтез пищеварительных ферментов, что находит свое выражение в развитии лактазной недостаточности и синдрома мальабсорбции.
Раздражение нервных окончаний стенки кишки запускает патологические висцеро–висцеральные рефлексы, способствуя развитию абдоминального синдрома. Сенсибилизация организма продуктами метаболизма и гибели лямблий вызывает различные формы аллергических проявлений.
Длительное персистирование лямблий, воздействие их токсинов и продуктов обмена на различные системы, вызывает у ребенка синдром хронической эндогенной интоксикации, невротические реакции, вторичную иммунную недостаточность.
Классификация
В соответствии с классификацией ВОЗ, различают бессимптомное лямблионосительство и клинически выраженный лямблиоз у детей. По особенностям клинических проявлений выделяют первичную инвазию (острый лямблиоз чаще встречается у детей младшей возрастной группы) и затяжную рецидивирующую инфекцию (хронический лямблиоз обычно регистрируется у старших детей и взрослых).
В зависимости от клинического варианта лямблиоз у детей может протекать в кишечной форме (в виде дуоденита, дискинезии двенадцатиперстной кишки, энтерита, энтероколита), гепатобилиарной форме (в виде дискинезии желчевыводящих путей, холангита, холецистита), как сопутствующее заболевание.
У детей разного возраста лямблиоз может приобретать клиническую форму с преобладанием болевого, диспепсического, аллерго-дерматологического, астено-невротического, интоксикационного синдрома или их сочетаний.
Симптомы лямблиоза у детей
Практически у всех детей с лямблиозом наблюдается абдоминальный синдром, характеризующийся приступообразной болью в животе (в эпигастрии, в районе пупка, правом подреберье), не связанной с приемом пищи. Иногда выраженность болевого синдрома у детей может напоминать клинику острого живота.
Диспепсический синдром у ребенка с лямблиозом может выражаться в снижении аппетита, наличии отрыжки, изжоги, тошноты, горечи во рту, вздутия живота. На фоне сопутствующего дисбиоза кишечника стул становится жидким, пенистым, зловонным; частота дефекаций увеличивается до 3-5 раз в сутки. При исследовании копрограммы обнаруживается стеаторея. Иногда у детей с лямблиозом отмечается чередование запоров и диареи. Следствием нарушения кишечного всасывания и расстройства стула служит снижение массы тела, гипотрофия.
Аллерго-дерматологические проявления лямблиоза у детей малоспецифичны. В ряде случаев на коже появляется мелкоточечная розовая сыпь по типу крапивницы, неукротимый кожный зуд; у подростков возникает или усиливается юношеская угревая сыпь. Может развиваться аллергический ринит, аллергический конъюнктивит, атопический дерматит, отек Квинке, бронхиальная астма. Иногда лямблиоз у детей заявляет о себе приступами артралгий и артрита.
Астено-невротический синдром при лямблиозе у детей является следствием угнетающего действия на ЦНС продуктов жизнедеятельности лямблий. Проявления синдрома находят свое выражение в повышенной утомляемости, снижении работоспособности и эмоционального тонуса ребенка, раздражительности, плаксивости, головных болях, головокружениях, появлении скрипа зубами (бруксизма), тиков.
Интоксикация при лямблиозе у детей сопровождается гепатолиенальным синдромом, лимфаденопатией, увеличением миндалин и аденоидов, беспричинным подъемом температуры тела до 37,5-38°С.
Хронический лямблиоз у детей не имеет ярко выраженных клинических проявлений. Его течение характеризуется сухостью и шелушением кожи, фолликулярным кератозом, обострением или манифестацией аллергических заболеваний, утяжелением течения соматической патологии, неустойчивостью стула, периодическим субфебрилитетом, признаками вегето-сосудистой дистонии и т. д.
Диагностика
Поскольку признаки инфекции не являются специфичными, дети с лямблиозом часто длительно и безрезультатно лечатся у аллерголога-иммунолога, детского дерматолога, детского пульмонолога. Обследованию на лямблиоз должны подвергаться дети с патологией ЖКТ, вегетативными и невротическими нарушениями, аллергическими заболеваниями, стойкой эозинофилией по данным гемограммы.
Наиболее доступной формой диагностики лямблиоза у детей считается выявление цист лямблий в кале. Для этого требуется, как минимум, трехкратная сдача анализа, однако, поскольку цистовыделение происходит непостоянно, циклично, лямблии в кале обнаруживаются не всегда. В некоторых случаях информативнее оказывается исследование дуоденального содержимого, полученного путем зондирования.
В настоящее время широко используется серологическая диагностика лямблиоза у детей (ИФА), направленная на выявление специфических антител к антигенам лямблий в крови, а также высокочувствительное ПЦР-исследование кала и дуоденального содержимого.
В рамках обследования детям с лямблиозом могут быть рекомендованы дополнительные диагностические процедуры: УЗИ органов брюшной полости, анализ кала на дисбактериоз, копрограмма, биохимическое исследование крови.
Лечение лямблиоза у детей
Целевой установкой терапии лямблиоза у детей является полная эрадикация паразита и устранение клинических проявлений. При подтверждении диагноза лямблиоза у детей должно проводиться лечение всех членов семьи и домашних питомцев.
Проведению противолямблиозной терапии предшествует подготовительный этап, включающий соблюдение диеты и режима питания и устранение холестаза. Для повышения эффективности лечения лямблиоза у детей рекомендуется соблюдение диеты: употребление каш, отрубей, сухофруктов, печеных овощей и фруктов; снижение доли легкоусвояемых углеводов. С целью устранения эндогенной интоксикации рекомендуется прием энтеросорбентов; при синдроме мальдигестии и мальабсорбции назначаются ферменты на основе панкреатина. При лямблиозе у детей показан прием холекинетиков, проведение слепых тюбажей по Демьянову. При выявлении дисбактериоза проводится соответствующая коррекция микробного пейзажа кишечника.
Для проведения этиотропной терапии лямблиоза у детей используются противолямблиозные препараты группы нитроимидазолов (метронидазол, тинидазол, ниридазол, орнидазол) и производные нитрофуранов (фуразолидон, нифуратель). Выбор препарата, схему и длительность лечения лямблиоза у детей определяет детский гастроэнтеролог. На 2-3 день приема противопаразитарных препаратов у детей могут обостриться аллергические проявления, усилиться боли в животе, однако это не является поводом для прекращения лечения.
После завершения назначенного курса должно быть проведено повторное обследование ребенка на лямблиоз. При упорном течении лямблиоза у детей проводятся два цикла лечения разными препаратами.
Прогноз и профилактика лямблиоза у детей
При проведении полного курса терапии клинико-лабораторная ремиссия достигается у 92-95% детей. Тем не менее, нередки случаи реинфекции и рецидива лямблиоза у детей. После завершения лечения дети должны наблюдаться педиатром с проведением 2-3–кратного обследования на лямблиоз. При отрицательных лабораторных результатах, но возобновлении типичных симптомов лямблиоза ребенку необходимо провести противорецидивный курс лечения.
Профилактика лямблиоза у детей требует выявления и лечения бессимптомных паразитоносителей и цистовыделителей; привития детям гигиенических навыков; использования кипяченой воды для питья и мытья фруктов; проведения противоэпидемических мероприятий в детских учреждениях.
Читайте также:

