Дисбактериоз у ребенка и лимфоузлы
Обновлено: 25.04.2024
На сервисе СпросиВрача доступна консультация педиатра по любой волнующей Вас проблеме. Врачи-эксперты оказывают консультации круглосуточно и бесплатно. Задайте свой вопрос и получите ответ сразу же!


Здравствуйте. Для диагностики глистных инвазий нужно сдать отпечаток на энтеробиоз, кал на яйца глистов и простейших, анализ крови на антитела к гельминтам.

Здравствуйте, Анастасия.
Увеличение брыжеечных лимфоузлов (мезаденит) может быть следствием не только глистной инвазии, но и вирусной и бактериальной инфекции.
Сдайте тогда общий анализ крови и кровь на антитела к глистам.
Кал малоинформативен, так как часто выдаёт ложно отрицательные результаты


Здравствуйте. Нужно сдать кал на яйцеглист. Соскоб на энтеробиоз и кровь на антитела к гельминтам. Но не обязательно это глистная инвазия. Это может быть обыкновенная инфекция. Будьте здоровы

Здравствуйте, необходимо сдать кал на яйца гельминтов 3х кратно с интервалом 3-4 дня, соскоб на энтеробиоз. ИФА кровь на (описторхии, токсокары, токсоплазмы). Также заброшинные лимфоузлы могут увеличиваться при инфекционном мононуклеозе. Сдайте ИФА кровь Ig M,G.

Здравствуйте!
Не обязательно паразиты могут давать такую картину, а зачастую они дают её не так часто
Я бы провела дифференциальную диагностику с другими заболеваниями желудочно-кишечного тракта
Для этого пожалуйста ответьте мне на вопросы ниже.
Расскажите пожалуйста локализацию болей, где конкретно болит, как долго сохраняется болевой синдром и чем он купируется и ли проходит самостоятельно?
Начинает болеть после еды или не связано?
Как давно у вас начались эти боли?
Юлия, ребёнок показывает, что болит в области живота. Боль начинается не зависимо от еды. Когда садится какать говорит, что болит живот (и его либо крепит, либо понос). Покакает, ему становится легче. Если понос, даю смету. Пол года уже точно это длится. Это происходит, 2-3 раза в месяц. А так в основном стул хороший, аппетит тоже. Иногда говорит, что чешется в попе.

Давайте сдадим с вами общий анализ крови, копрограмму, кал на яйца гельминтов, на цисты простейших, энтеробиоз
Можно сдать кровь (ифа) на антитела к простейшим и гельминтам, там вообще входят все, сразу с вами определимся есть что то или нет
Копрограмма покажет наличие или отсутствие воспаления
По общему анализу крови тоже можно уже будет много сказать
Поэтому можно начать с минимума - общий анализ крови +копрограмма
И потом уже определиться что сдавать дальше

Здравствуйте, Анастасия !
Увеличение лимфоузолов брыжейки кишечника чаще всего характерно для персистирующих вирусных инфекций : ЦМВ (цитомегаловирус); ВПГ (вирус простого герпеса); ВЭБ(вирус Эпштейна - Барра) !
Не переживайте, эти вирусы никакого отношения к коронавирусу не имеют, ими заражена большая часть населения земли !
Вам необходимо проведение анализа крови методом ПЦР(полимеразная цепная реакция ) или ИФА (иммуно-ферментный анализ) на эти вирусы !
Удачи Вам !

Здравствуйте!
1. Копрограмма, кал на паразитов методом обогащения 3х кратно с интервалом в 3 дня или методом парасепт, кал на диз.группу и посев.
2. На описторхи, токсокары и лямблии кровь методом ИФА.
3. Б/х анализ крови развернутый, ОАК, ОАМ.

1) паразиты/глисты у собак и еошек не пересекаются с человечексими.
2) Ваше состояние называется мезаденит (увеличение кишечных л/у), это состояние не надо лечить, проходит само. В нашем организме в ответ на какую-то инфекцию или воспаление активируется имунная система - лимфоузлы, в том числе внутрикишечные - часть этой системы.
3) Необходимо выявить причину - сходить к гастроэнтерологу, после адекватного расспроса и сбора анамне он определит тактику дальнейшйей диагностики
Дисбактериоз кишечника у детей - нарушение качественного и количественного состава кишечной микрофлоры, при котором в ней начинают преобладать условно-патогенные микроорганизмы. Дисбактериоз у детей раннего возраста проявляется срыгиваниями, низкими темпами прибавки массы тела, нарушением стула; у детей старшего возраста – отрыжкой, снижением аппетита, неустойчивым стулом, кишечными коликами. Подтверждение дисбактериоза у детей проводится с помощью бактериологического исследования испражнений, анализа копрограммы. Лечение дисбактериоза у детей включает соблюдение диеты, фаготерапию или антибактериальную терапию, прием пробиотиков и пребиотиков, иммунорегуляторов, витаминов.

Общие сведения
Дисбактериоз (дисбиоз) у детей характеризуется стойким нарушением микробиоценоза кишечника, изменением соотношения облигатной и факультативной микрофлоры кишечника в пользу последней. Проблема дисбактериоза у детей – наиболее актуальная в педиатрии, поскольку по данным современных исследований, нарушение биоценоза кишечника выявляется у 25-50% здоровых детей грудного возраста. Среди детей, больных соматическими и инфекционными заболеваниями (кишечными инфекциями, энтеритами, колитами, аллергическим дерматитом и др.), дисбактериоз кишечника различной степени тяжести обнаруживается практически в 100% случаев.
Рождение ребенка сопряжено с его переходом из стерильной внутриутробной среды в окружающий мир, заселенный многообразием различных микроорганизмов. Практически сразу организм новорожденного подвергается микробной колонизации. Основную часть облигатной микрофлоры ребенок получает от матери (во время продвижения по родовым путям, при грудном вскармливании), что является определяющим для его последующего здоровья. Иммунные факторы, присутствующие в молозиве и грудном молоке (секреторный IgA, лизоцим, лактоферрин, макрофаги, бифидус-фактор и др.), блокируют колонизацию кишечника условно-патогенной флорой. Поэтому для профилактики дисбактериоза у ребенка чрезвычайно важно его раннее прикладывание к груди матери (в первые 30 минут, но не позднее 2-х часов после рождения).
В течение первых 3-5 дней жизни микробный пейзаж кишечника становится более разнообразным, и в нем, наряду с полезными бактериям, в большом количестве поселяются условно-патогенные микроорганизмы. В результате этого на первой неделе у новорожденных детей развивается транзиторный дисбактериоз кишечника, проявляющийся срыгиваниями, неустойчивым водянистым стулом с примесью слизи, спастическими болями. Транзиторный дисбактериоз у детей обычно завершается на второй неделе жизни, по мере того, как бифидо- и лактобактерии вытесняют других представителей микробиоценоза кишечника. Однако при наличии отягощающих факторов нормальная микрофлора не формируется, и транзиторный дисбактериоз у детей переходит в истинный.

Причины у детей
Всех представителей кишечной микрофлоры в гастроэнтерологии принято разделять на 4 группы: облигатную, факультативную (условно-патогенную), транзиторную и патогенную флору. Транзиторная флора, не является типичной для организма человека, и носит временный, случайный характер. Представителями патогенной кишечной флоры являются возбудители инфекционных заболеваний (дизентерии, сальмонеллеза и др.), в норме не присутствующие в кишечнике.
Облигатная флора (бифидобактерии, лактобактерии, кишечная палочка) регулирует иммунитет; участвует в процессе пищеварения, обмене веществ, синтезе витаминов и ферментов; стимулирует моторику ЖКТ. Факультативная флора (золотистый и эпидермальный стафилококк, энтеробактер, протей, клебсиелла, клостридии, дрожжевых грибы рода кандида) в норме составляет не более 0,6% от общего количества микроорганизмов и при нормальном состоянии иммунной системы не вызывает заболеваний. Однако при снижении резистентности организма, изменении видового и количественного соотношения облигатной и факультативной микрофлоры у детей развивается дисбактериоз.
Причины, приводящие к дисбактериозу у детей, многообразны и начинают действовать уже во внутриутробном периоде или вскоре после рождения ребенка. Нарушение бактериального гомеостаза кишечника может быть связано с осложненным течением беременности и родов, поздним прикладыванием к груди, недоношенностью ребенка, наличием бактериального вагиноза у матери.
Развитие дисбактериоза у детей грудного возраста может быть обусловлено плохим питанием кормящей матери, возникновением у нее мастита, ранним переводом ребенка на искусственное вскармливание, частыми ОРВИ, диатезом.
У детей раннего, дошкольного и школьного возраста факторами развития дисбактериоза выступают нерациональное питание с преобладанием в рационе ребенка избытка углеводов и животного белка, загрязнение окружающей среды, длительное лечение антибактериальными и гормональными препаратами, стрессы. Изменению микробного равновесия ЖКТ способствуют кишечные инфекции, заболевания органов пищеварения (лактазная недостаточность, гастрит, панкреатит, энтероколит, запор), паразитарные инвазии (аскаридоз, лямблиоз), наличие несанированных очагов хронической инфекции (кариеса, тонзиллита), заболевания, протекающие со снижением иммунитета (сахарный диабет, онкопатология, цирроз печени, ВИЧ и др.).
Классификация
В зависимости от преобладающей условно-патогенной флоры различают протейную, стафилококковую, кандидозную, ассоциированную формы дисбактериоза кишечника у детей; по клиническому течению – латентный, локальный и генерализованный варианты.
Степень тяжести дисбактериоза у детей определяется видовым и количественным составом микрофлоры:
- I степень - преобладает анаэробная микрофлора; количество бифидобактерий не менее 107—108 ; условно-патогенные микроорганизмы не более двух видов, 102—104 КОЕ на 1 г фекалий.
- II степень - равное количество анаэробной и аэробной флоры; условно-патогенные микроорганизмы 106—107 КОЕ на 1 г фекалий; обычная кишечная палочка вытеснена гемолизирующей и лактозонегативной.
- III степень – преобладает аэробная флора, вплоть до полного подавления бифидо- и лактобактерий; количество условно-патогенных микроорганизмов значительно увеличено.
- IV степень – ассоциированный дисбактериоз у детей; абсолютное преобладание условно-патогенной микрофлоры, резистентной к антибиотикам.
Согласно клинико-бактериологическим критериям выделяют компенсированный, субкомпенсированный и декомпенсированный дисбактериоз у детей.
Компенсированный дисбактериоз у детей протекает в латентном варианте и соответствует I-II степени тяжести. Клинически ребенок остается здоровым, нормально развивается и прибавляет в массе; аппетит и стул в норме.
Субкомпенсированный дисбактериоз у детей соответствует локальному варианту, II-III степени тяжести. Отмечаются умеренно-выраженные клинические симптомы: вялость, плохой аппетит, плохая прибавка в массе, диспепсические расстройства.
Декомпенсированный дисбактериоз у детей может иметь локальное или генерализованное течение, III-IV степень тяжести. Значительно ухудшается общее состояние ребенка за счет рвоты, частого жидкого стула, интоксикации. На этом фоне легко возникают острые кишечные инфекции, энтероколиты, бактериемия и сепсис.
В клинической картине дисбактериоза у детей могут доминировать один или несколько характерных синдромов: диарейный, дискинетический, нарушения пищеварения и всасывания (мальдигестии и мальабсорбции), интоксикации, астеноневротический, дермоинтестинальный.
Симптомы дисбактериоза у детей
У новорожденных и грудных детей дисбактериоз сопровождается срыгиваниями, рвотой, метеоризмом, урчанием и спазмами по ходу кишечника. Ребенок недостаточно набирает массу тела, беспокойно ведет себя, плохо спит. Стул у ребенка с дисбактериозом обычно жидкий или кашицеобразный, обильный, пенистый с примесью комочков или слизи, необычного цвета (белого, зеленоватого), с гнилостным или кислым запахом.
При синдроме мальабсорбции развивается диарея, стеаторея, гипотрофия, полигиповитаминоз. Эндогенная интоксикация при дисбактериозе у детей сопровождается полидефицитной анемией, задержкой физического развития, снижением аппетита. Процессы брожения и гниения в кишечнике вызывают аутоаллергизацию и развитие дермоинтестинального синдрома (крапивницы, атопического дерматита). Проявлениями астеноневротического синдрома служат раздражительность, слабость, нарушение сна.
В более старшем возрасте дисбактериоз у детей может протекать с запорами, поносами или их чередованием; кишечными коликами, отрыжкой, неприятным запахом изо рта, чувством распирания желудка после еды. Вторичными внекишечными проявлениями дисбактериоза у детей, связанными с гиповитаминозом, нарушением обмена веществ, снижением иммунитета могут стать заеды в уголках рта, стоматит, фурункулез, угревая сыпь, ломкость волос и ногтей и др.
Генерализованный дисбактериоз обычно развивается у детей с иммунодефицитным состоянием и протекает по типу кандидамикоза с явлениями молочницы, глоссита, хейлита, поражением гладкой кожи, вульвита или баланопостита, висцерального кандидоза.
Диагностика
Установлению диагноза дисбактериоза предшествует обследование ребенка педиатром и детским гастроэнтерологом, проведение лабораторных анализов и дополнительных инструментальных исследований. С помощью физикального обследования детей оценивается состояние кожи и слизистых; пальпация живота выявляет болезненность по ходу кишечника.
Лабораторная диагностика обычно включает бактериологическое или биохимическое исследование кала на дисбактериоз. Микробиологическими критериями дисбактериоза у детей служат уменьшение количества бифидо- и лактобактерий, снижение или увеличение числа нормальных кишечных палочек, а также появление их измененных штаммов, обнаружение грамотрицательных палочек, увеличение количества кокков, грибов, клостридий. Биохимический анализ основан на определении уровня метаболитов летучих жирных кислот (пропионовой, уксусной, масляной), продуцируемых микроорганизмами, живущими в ЖКТ.
Для выяснения причины дисбактериоза у детей могут назначаться УЗИ органов брюшной полости, гастроскопия, биохимические пробы печени, анализ кала на лямблии и яйца гельминтов. Исследование копрограммы позволяет выявить степень нарушения расщепления и всасывания пищи.
При подозрении на дисбактериоз у детей важно исключить неспецифический язвенный колит, ОКИ, синдром мальабсорбции.
Лечение дисбактериоза у детей
Терапия дисбактериоза у детей начинается с подбора индивидуальной диетотерапии. В рацион детей, находящихся на смешанном вскармливании, вводятся кисломолочные продукты. В питании детей старшего возраста ограничиваются сахара, углеводы, животные белки; для восстановления нормальной кишечной микрофлоры рекомендуются молочнокислые продукты, обогащенные биокультурами, пищевые волокна.
При дисбактериозе кишечника у детей назначаются пробиотики – препараты, содержащие монокультуры или комбинации полезных бактерий; пребиотики, способствующие росту и размножению микробов нормальной флоры кишечника; симбиотики - комбинированные препараты.
С целью селективной деконтаминации кишечника при дисбактериозе у детей применяются бактериофаги, лизирующие патогенные бактерии, а при неэффективности – антибиотики (макролиды, цефалоспорины). Лечение кандидозного дисбактериоза у детей проводится противогрибковыми препаратами (нистатин, флуконазол).
В случае выраженных нарушений пищеварения назначаются ферменты, при интоксикации показан прием сорбентов. Часто болеющим детям рекомендуется иммуномодулирующая терапия адаптогенами, витаминотерапия.
Профилактика
Залогом формирования нормальной микрофлоры кишечника у ребенка является забота о своем здоровье будущей мамы: планирование беременности, сбалансированное питание во время беременности, лечение бактериального вагиноза, соблюдение режима дня и отдыха, исключение нервных потрясений.
Самыми первыми мерами по профилактике дисбактериоза должно быть раннее прикладывание ребенка к груди в родзале и сохранение грудного вскармливания детей на протяжении не менее полугода, постепенное введение прикормов. Необходимо лечение хронических заболеваний органов пищеварения, предупреждение кишечных инфекций. Для недопущения развития дисбактериоза антибиотикотерапия у детей должна проводиться под прикрытием пробиотиков или пребиотиков.
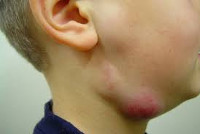
Лимфаденит у детей – это воспалительная реакция лимфатических узлов в ответ на локальные или общие патологические процессы в организме. Серозный лимфаденит у детей протекает с увеличением, уплотнением, болезненностью лимфоузлов; гнойный лимфаденит сопровождается местными (гиперемией, отеком) и общими симптомами (резким ухудшением самочувствия, лихорадкой). Диагноз лимфаденита у детей устанавливается на основании клинического осмотра, общего анализа крови, УЗИ и пункции лимфоузлов. В лечении лимфаденита у детей применяется консервативная тактика (антибактериальная, десенсибилизирующая, дезинтоксикационная терапия, местные аппликации, УВЧ) или хирургическое вскрытие и дренирование гнойного очага с обязательной ликвидацией первичного источника инфекции.
МКБ-10
Общие сведения
Лимфаденит у детей – инфекционный или неинфекционный воспалительный процесс в периферических органах лимфатической системы – лимфоузлах. Лимфадениту принадлежит одно из ведущих мест по частоте встречаемости в педиатрической практике, что обусловлено морфофункциональной незрелостью лимфатической системы ребенка. Чаще всего лимфаденит наблюдается у детей в возрасте от 1 до 6 лет и имеет более бурное течение, чем у взрослых. Лимфаденит у детей развивается вторично, осложняя течение основных инфекционно-воспалительных заболеваний, поэтому увеличение лимфатических узлов у ребенка может обнаруживаться различными детскими специалистами: врачом-педиатром, детским отоларингологом, детским стоматологом, детским хирургом, детским иммунологом, детским ревматологом и др.

Причины
Рост и развитие лимфоидных образований у детей продолжается до 6-10 лет; этот период связан с повышенной восприимчивостью к различным инфекционным агентам и недостаточной барьерно-фильтрационной функцией. Лимфоузлы, как элементы иммунной защиты, вовлекаются во все патологические процессы, протекающие в организме: распознавая и захватывая чужеродные частицы (бактерии, токсины, продукты распада тканей), они препятствуют их распространению из местного очага и попаданию в кровь.
Лимфаденит у детей чаще всего имеет неспецифический генез, его основными возбудителями являются гноеродные микроорганизмы, в первую очередь, стафилококки и стрептококки. При лимфадените у детей обычно имеется первичный очаг острого или хронического гнойного воспаления, из которого инфекция попадает в лимфоузлы с током лимфы, крови или контактным путем.
Более 70% случаев лимфаденита у детей связано с воспалительными процессами ЛОР-органов - тонзиллитом, синуситом, отитом. Лимфаденит у детей часто сопутствует инфекциям кожи и слизистых оболочек: фурункулам, пиодермии, гнойным ранам, экземе, стоматиту. Лимфаденит может осложнять течение различных бактериальных и вирусных инфекций у детей - скарлатины, дифтерии, ОРВИ, гриппа, паротита, ветряной оспы, кори. Наибольшее количество лимфаденитов у детей отмечается в осенне-зимний период вследствие увеличения числа инфекционных и обострения хронических заболеваний.
Лимфаденит у детей старше 6-7 лет может быть связан с воспалительными заболеваниями зубо-челюстной системы (пульпитом, периодонтитом, остеомиелитом). При этом нарастание симптомов лимфаденита у детей может происходить после затухания патологического процесса в первичном очаге. Причиной специфического лимфаденита у детей являются инфекционные заболевания с типичным для них поражением лимфатических узлов - туберкулез, инфекционный мононуклеоз, бруцеллез, актиномикоз, сифилис и др.
В некоторых случаях лимфаденит у детей может быть связан с заболеваниями крови (острыми и хроническими лейкозами), опухолями лимфоидной ткани (лимфосаркомой, лимфогрануломатозом), а также травматическим повреждением самих лимфоузлов. Лимфаденит обычно наблюдается у детей с лимфатико-гипопластическим диатезом, часто болеющих ОРВИ, имеющих в анамнезе сопутствующие герпесвирусные инфекции (ЦМВ, вирус Эпштейна-Барра) и хронические заболевания ЖКТ.
Классификация
В зависимости от типа возбудителя выделяют неспецифический и специфический лимфаденит у детей, который может иметь острое (до 2-х недель), подострое (от 2-х до 4-х недель) или хроническое (более месяца) течение. По характеру воспалительных изменений лимфатических желез у детей различают серозные (инфильтрационные), гнойные, некротические (с расплавлением узлов) лимфадениты и аденофлегмоны.
По очагу поражения лимфадениты у детей разделяют на регионарные (шейные, подчелюстные, подмышечные, паховые и т. д.) и генерализованные; по этиологическому фактору - одонтогенные (связанные с патологией зубо-челюстной системы) и неодонтогенные.
Симптомы
Как правило, при лимфадените у детей поражаются лимфоузлы в области лица и шеи (наиболее часто - подчелюстные и шейные с одной или обеих сторон, реже - околоушные, щечные, затылочные, заушные), в отдельных случаях – подмышечные, паховые.
Серозная стадия острого неспецифического лимфаденита у детей (1-3 сутки заболевания) проявляется болезненными, заметно увеличенными в размерах и плотно-эластичными на ощупь регионарными лимфоузлами, без потери их подвижности и развития местной кожной реакции. Общее состояние ребенка не нарушено, температура колеблется от нормальных до субфебрильных значений.
Переход острого лимфаденита в гнойную стадию (3-6 сутки заболевания) протекает с ярко выраженными местными признаками и резким ухудшением самочувствия детей. Наблюдаются признаки интоксикации: озноб, высокая температура (до 40ºС), головная боль, сильная слабость, отсутствие аппетита и нарушение сна. В области пораженных лимфоузлов возникают интенсивные тянущие или стреляющие боли, явления периаденита, местная гиперемия и отек кожи. Возможно развитие аденофлегмоны с появлением очагов флюктуации и выходом гнойного воспаления за пределы лимфоузла. Аденофлегмоны челюстно-лицевой области могут осложниться тромбозом кавернозного синуса, медиастинитом, сепсисом.
Хроническая форма лимфаденита у детей может развиться первично, если возбудителями являются слабовирулентные микроорганизмы, или стать продолжением острой формы заболевания. При хроническом течении вне обострения лимфоузлы увеличены, ограничены в подвижности, достаточно плотные, но безболезненные; самочувствие ребенка не нарушено; нагноение развивается редко. При наличии у ребенка очага хронической инфекции, длительно поддерживающего вялотекущий лимфаденит, лимфоузлы постепенно разрушаются и замещаются грануляционной тканью.
Туберкулезный лимфаденит у детей имеет продолжительное течение, ограничивается обычно шейной группой лимфоузлов, собранных в плотный, безболезненный, значительный пакет, похожий на ошейник. Туберкулезный лимфаденит у детей может осложняться казеозным распадом, образованием свищевых ходов, рубцовыми изменениями кожи.
Диагностика
Диагностика лимфаденита у детей включает тщательный физикальный осмотр, оценку клинической картины и анамнеза заболевания, исследование клинического анализа крови, УЗИ лимфатических узлов и ряд дополнительных дифференциально-диагностических исследований. Выявление лимфаденита у детей может потребовать обследования у врачей различных специальностей: педиатра, инфекциониста, детского отоларинголога, гематолога, хирурга, фтизиатра.
В ходе диагностики необходимо установить этиологию лимфаденита у детей, выявить первичный очаг гнойного воспаления. Вспомогательными методами выявления туберкулезного лимфаденита у детей служат туберкулиновые пробы, рентгенография грудной клетки, диагностическая пункция и бактериологический посев материала. При подозрении на онкологический процесс выполняется биопсия лимфатических узлов с цитологическим и гистологическим исследованием ткани.
Дифференциальная диагностика лимфаденитов различной локализации у детей проводится с опухолями слюнных желез, метастазами злокачественных новообразований, флегмоной, ущемленной паховой грыжей, остеомиелитом, системными заболеваниями (саркоидоз, лейкоз), диффузными заболеваниями соединительной ткани (ювенильный ревматоидный артрит, системная красная волчанка, дерматомиозит).
Лечение лимфаденита у детей
Лечение лимфаденита у детей определяется стадией, типом заболевания, степенью интоксикации и направлено на купирование инфекционно-воспалительных процессов в лимфоузлах и устранение первичного очага инфекции.
При остром серозном и хроническом неспецифическом лимфадените у детей применяют консервативную терапию, включающую антибиотики (цефалоспорины, полусинтетические пенициллины, макролиды), десенсибилизирующие средства, местное лечение (сухое тепло, компрессы с мазью Вишневского, УВЧ). Показаны общеукрепляющие препараты – кальция глюконат, аскорутин, витамины, иммуностимуляторы.
При отсутствии эффекта терапии или переходе лимфаденита в гнойную стадию, ребенка госпитализируют и проводят экстренное вскрытие, дренирование и санацию гнойного очага. В случае некротического лимфаденита у детей выполняют тщательный кюретаж полости, при необходимости производят удаление лимфоузла. В послеоперационном периоде показана комплексная противовоспалительная и дезинтоксикационная терапия. Лечение специфического туберкулезного лимфаденита у детей проводят в специализированных лечебных учреждениях.
Прогноз и профилактика
Прогноз лимфаденита у детей при своевременном адекватном лечении – благоприятный, при длительном хроническом течении возможно замещение лимфоидной ткани на соединительную; иногда в области пораженных лимфоузлов развивается нарушение лимфооттока (лимфостаз).
Предупреждение лимфаденита у детей заключается в устранении источников хронической инфекции, своевременном лечении зубов, травматических и гнойных поражений кожи и слизистых оболочек, повышении общей и местной сопротивляемости организма.
1. Лечение острых лимфаденитов шеи в детской хирургической практике: Автореферат диссертации/ Джабарова Е.В. - 2012.
2. Оптимизация диагностики и лечения лимфаденита лица и шеи у детей: Автореферат диссертации/ Анохина И.В. - 2013.
3. Лимфадениты, лимфангоиты, лимфоаденопатии челюстно-лицевой области: учеб.-метод. пособие/ Н.Н. Черченко. – 2007.
Причиной увеличения лимфоузлов в большинстве случаев являются процессы, не связанные с гемобластозами: чаще всего это общепедиатрические, инфекционные, иммунные и другие состояния Тот факт, что врач-педиатр достаточно часто обнаруживает у своих
Причиной увеличения лимфоузлов в большинстве случаев являются процессы, не связанные с гемобластозами: чаще всего это общепедиатрические, инфекционные, иммунные и другие состояния
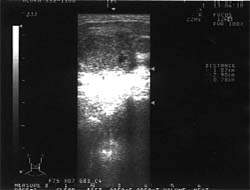 |
| Рисунок 1. Подчелюстные лимфатические узлы при лимфогранулематозе (УЗИ, 7,5 МГц) |
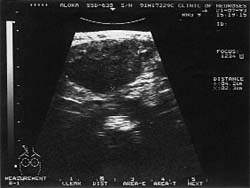 |
| Рисунок 2. Подчелюстной узел при туберкулезе (УЗИ, 7,5 МГц) |
Увеличение ЛУ может быть результатом лимфаденита (ЛА) и лимфаденопатии (ЛАП).
ЛА — воспаление лимфатических узлов, возникающее как осложнение после различных гнойно-воспалительных заболеваний и специфических инфекций (туберкулез, актиномикоз, чума и др.). ЛА, как правило, представляет собой вторичный процесс.
ЛАП — системное увеличение лимфатических узлов, не связанное с воспалением (воздействие некоторых медикаментов, пролиферация, метастазирование и т. п.).
Эпидемиология ЛА и ЛАП не разработана. Можно только отметить, что, по данным И. С. Тарасовой [6], при сплошных массовых исследованиях детей Брянской области ЛА встречается, как и следовало ожидать, несколько чаще (1,86% среди всех осмотренных), чем ЛАП (1,49% от общего контингента).
1. Увеличение отдельных ЛУ оценивается как небольшое, если они не теряют своей обычной УЗИ-картины, сохраняют капсулу, четкость и ровность контура, не изменяют топику органа. Такой тип характерен для инфекционных поражений, особенно туберкулеза, вирусного гепатита, коллагенозов, иммунодефицитов, гемобластозов у детей низкой группы риска.
2. Дальнейший рост ЛУ приводит к появлению сливающихся между собой масс, оттесняющих сосуды. Наблюдается при гнойном расплавлении группы лимфоузлов, при гемобластозах, метастазирующих опухолях.
3. Сдавление или оттеснение внутренних органов. При этом может возникнуть гидронефроз за счет сдавления мочеточников, значительное смещение матки, мочевого пузыря. Типично для крайне неблагоприятных вариантов миелолейкозов, лимфом Ходжкина и неходжкинских лимфом.
УЗИ-заключения могут быть подтверждены компьютерной томографией (КТ). Дополнительно КТ позволяет уточнить структуру ЛУ, их топографические соотношения, обнаружить другие группы ЛУ.
Если поверхностные лимфоузлы есть смысл оценивать только эхографически, а мезентериальные и забрюшинные ЛУ практически одинаково хорошо выявляются методами УЗИ и КТ, то внутригрудные ЛУ выявляются почти исключительно рентгенологически.
| Принятое в нашей стране и широко рекомендуемое в отечественной литературе сравнение размеров лимфоузлов с зерном, горохом, вишней, лесным и грецким орехом нерационально, дает несопоставимые результаты и должно быть изжито |
Такие методы диагностики, как изотопная сцинтиграфия и лимфография, могут применяться по очень строгим показаниям в специализированных клиниках или ограниченно при динамических исследованиях и не используются в широкой практике.
Достоверное выявление причин увеличения ЛУ возможно лишь гистологическими методами. При этом материал должен быть получен только путем открытой биопсии ЛУ, хотя современные методики тонкоигольной биопсии позволяют получить достоверные результаты. Рекомендовавшаяся ранее пункционная биопсия дает очень большой процент ложно-положительных и ложноотрицательных результатов.
Увеличение ЛУ схематически [5, 11] можно представить (с описанием некоторых практически значимых, но малоизвестных форм) как связанное с инфекцией (ЛА) и не связанное с инфекцией (ЛАП).
1. ЛА вирусной природы.
- цитомегалия.
- инфекционный мононуклеоз.
- корь.
- краснуха.
- орнитоз.
- синдром Ардмора.
2. ЛА при бактериальных инфекциях.
- кариес.
- абсцесс.
- болезнь кошачьей царапины. Вызывается Bortanella (Rochalimeae) hensella. Чаще доброкачественно протекающее со спонтанным выздоровлением двустороннее воспаление ЛУ (в т. ч. мезентериальных и внутригрудных) с общими и кожными неспецифическими симптомами, обусловленное ранениями кожи кошками, собаками, реже — посторонними острыми предметами. Описаны гранулематозный гепатит, спленомегалия, энцефалитические реакции, судорожный синдром [8, 10]. Наблюдается в основном у детей и подростков преимущественно поздней осенью и зимой.
- Боррелиоз. Известен как псевдолимфома. Лимфопролиферативное поражение ЛУ и кожи при заражении Borrelia burgdorferi после укуса клещами. Описаны переходы в злокачественные лимфомы.
- Туберкулез. Наряду с типичными формами туберкулеза следует помнить о т. н. атипичных микобактериозах. По данным Ф. Миллера [2], до 50% подчелюстных ЛА у детей до 5 лет вызываются атипичными штаммами микобактерий (в частности, типа avium), и вероятность микобактериального поражения ЛУ тем выше, чем младше ребенок (рис. 1).
- Сепсис.
- Аллергический субсепсис. Рассматривается и как вариант ювенильного ревматоидного артрита, т. н. болезнь Стилла.
- Сифилис. Темпы роста заболеваемости сифилисом детей значительно опережают аналогичный показатель у взрослых. Так, заболеваемость сифилисом среди взрослых возросла за 4 года в 15,8 раз, а среди детей — в 21 раз. 65,6% детей заразились половым путем [1].
- Генито-аноректальный симптомокомплекс — осложнение хронического ЛА при хламидиозе серотипов L1—L3 с перипроктитом, хронически рецидивирующими перианальными и промежностными свищами, стриктурами и фиброзом генитоуретрального трактов, элефатиазисом вульвы. Встречается в основном у больных женского пола.
3. ЛА при грибковых заболеваниях.
4. ЛА при паразитарных заболеваниях.
5. ЛА при протозойных инфекциях.
- токсоплазмоз. Субклинический вариант — шейный подострый некротизирующий ЛА. Клинически — болезненный, чаще шейный ЛА, со спонтанной ремиссией через 3 — 6 месяцев, лихорадка, экзантема. Нейтропения. Гистологически — коагуляционные некрозы с гистиоцитарными и иммунобластными клетками без гранулем, без нейтрофилов. Дифференциальная диагностика проводится со злокачественными лимфомами, туберкулезом, гистиоцитозом, а по данным гистологии (васкулит) — с системной красной волчанкой.
- кала-азар.
- малярия.
Формы, не связанные с инфекциями (ЛАП)
1. ЛАП медикаментозная.
- производные гидантоина (дифенин и др.) — противосудорожные препараты. При таком осложнении терапии ЛАП рассматривается как аутоиммунобластная.
- аллопуринол (используется при лечении гиперурикемий, в т. ч. и при миелопролиферативных состояниях).
- противолепрозные средства (используются в гастроэнтерологии для лечения хронических колитов, в ревматологии — для лечения артритов и спондилоартритов, особенно ассоциированных с антигеном гистосовместимости HLA В-27).
- поствакцинальные.
- на фоне инородных тел.
2. При системных процессах в организме.
- коллагенозы (в этом случае наибольшее увеличение ЛУ регистрируется все-таки при инфицированных вариантах диффузных болезней соединительной ткани, то есть имеется сочетание ЛА и ЛАП).
- локальный опухолевидный амилоидоз. Традиционно описывается как патология исключительно взрослых [4]. Однако мы обнаружили эту форму диспротеиноза у 2 из 44 детей с системным амилоидозом. Локальный опухолевидный амилоидоз у наших пациентов протекал с выраженной общей параспецифической реакцией, что в сочетании с пальпируемым образованием в брюшной полости привело первоначально к ошибочному диагнозу лимфомы.
- амилоидоз Любарха, генетически детерминированный. Генерализованная ЛАП, ортостатическая гипотония, обструктивная инфильтративная кардиомиопатия, спленомегалия, нейропатия, туннельный синдром.
- синдром Дорфмана-Розаи (интермиттирующая доброкачественная лимфаденопатия). Вероятно аутоиммунное заболевание с доброкачественной пролиферацией плазмоцитов, гистиоцитов, фибробластов. Пик заболеваемости — в первые 10 лет жизни. Протекает с двухсторонним шейным, часто генерализованным увеличением ЛУ, лихорадкой, лейкоцитозом, узловатой эритемой. По нашим наблюдениям, при поражении внутренних органов прогноз плохой. Прогноз ухудшается при наличии одновременно иммунодисфункции (ускорение СОЭ, диспротеинемия).
- десквамативная эритродермия Лейнера. Вероятнее всего дефект хемотаксиса лейкоцитов и дефицит фрагмента комплемента С5. Заболевание манифестирует в первые 3 — 4 месяца жизни. Проявляется генерализованным увеличением всех лимфоузлов, вторичной эритродермией, дистрофией ногтей, анемией, рвотой, диареей. Чаще встречается при грудном вскармливании. Известны семейные случаи. Прогноз благоприятный.
3. Гранулематозы
- саркоидоз.
- аллергический гранулематоз Чарг — Штрауса. Сочетается с атопией в анамнезе. Проявляется в виде бронхиальной астмы, выраженной эозинофилии, ЛАП, нейропатии, кожных язв, поражения сердца, легких, кишечника и васкулита мелких артерий и вен.
- мультицентрический ретикулогистиоцитоз. Системное гранулематозное заболевание с образованием кожных узлов, деструктивным артритом, поражением внутренних органов. Протекает по типу псориатической артропатии.
- ретикулез липомеланотический (синдром Паутриера-Ворингера) — локализованное или генерализованное увеличение ЛУ как сопровождение дерматозов, прежде всего меланоэритродермии.
4. ЛАП при гемобластозах.
- острые лейкемии.
- неходжкинские лимфомы.
- ходжкинские лимфомы (по старой терминологии — лимфогранулематоз).
- болезнь альфа-тяжелых цепей (средиземноморская лимфома). Наблюдается в основном в детском и юношеском возрасте, клиника обусловлена тяжелым синдромом мальабсорбции, являющимся результатом лимфопролиферативных процессов с инфильтрацией тонкой кишки и мезентериальной ЛАП.
- болезнь гамма-тяжелых цепей. Обусловлена моноклональной гаммапатией, протекает по типу лимфопролиферативного системного заболевания.
- гистиоцитарные синдромы
5. ЛАП при метастазировании солидных опухолей в ЛУ.
6. Паранеопластические реакции [12].
- ПОЭМК-комплекс. Паранеопластический симптомокомплекс (особенно часто при склерозирующих плазмоцитомах) = полинейропатия + органомегалия + эндокринопатия + дисглобулинемия (М-градиент) + поражение кожи.
7. ЛАП при первичных иммунодефицитных состояниях (ПИД).
- общая вариабельная иммунная недостаточность.
- аутоиммунный лимфопролиферативный синдром.
- гранулематоз септический. Гетерогенная группа дефектов иммунитета, объединенных незавершенным внутриклеточным фагоцитозом каталазо-позитивных микробов в результате дефицита перекиси водорода и атомарного кислорода [11]. В настоящее время известны 4 различных молекулярных дефекта: а) Х-хромосомно связанный рецессивный дефект тяжелых цепей цитохрома В558; б) аутосомно-рецессивно наследуемый дефект легких цепей цитохрома В558; в) дефект 47 kd цитозолфактора; г) дефект 65 kd цитозолфактора. Клинические признаки: острые абсцедирующие инфекции кожи, легких, желудочно-кишечного тракта, ЛУ, печени, селезенки, вызванные каталазо-позитивными бактериями (стафилококки, энтеробактерии), а также аспергиллами; хроническое гранулематозное воспаление в желудочно-кишечном тракте и мочевыводящих путях с возможным стенозированием; снижение образования атомарного кислорода и перекиси водорода в ответ на растворимые и опсонированные раздражители.
8. Генетически обусловленные ЛАП [9].
- синдром Клиппель — Треноне. Сочетание локальных лимфангиом и гемангиом.
- синдромы с наследственно обусловленными лимфатическими отеками. Синдромы Вевера-Смита и Мильроя.
- легочная мышечная гипертрофия — мышечный цирроз легкого. Разрастание гладкомышечных волокон периальвеолярно, перибронхиально, интерстициально, интерлобарно. Увеличение ЛУ ворот легких. ДД проводится с саркоидозом, туберкулезом, синдромами эмфиземы легких, альвеолярно-капиллярного блока. Диагноз верифицируется только гистологически.
9. Синдром приобретенного иммунодефицита (СПИД).
В процессе диагностики заболеваний, протекающих с увеличением ЛУ, объединяются усилия педиатров, инфекционистов, иммунологов, онкогематологов. Главная роль при этом отводится именно педиатру, так как большинство ЛА и ЛАП связано у детей с инфекционным процессом. В то же время нельзя настаивать на инфекционном генезе увеличения ЛУ, если двухнедельный курс антибиотикотерапии не привел к существенному улучшению клинико-лабораторной и инструментальной картины. В пользу онкогематологического генеза изменения ЛУ свидетельствует увеличение их диаметра до 4 см и более, каменистая плотность, бугристость, образование конгломератов ЛУ, их спаянность с окружающими тканями, внутригрудные конгломераты, особенно в верхнем средостении, внутрибрюшинные конгломераты.
Четкое знание многообразия причин увеличения ЛУ поможет педиатрам в диагностике и дифференциальной диагностике этого синдрома.
Литература
1. Государственный доклад о состоянии здоровья населения Российской Федерации в 1994 г. М., 1995. с. 43.
2. Миллер Дж. Туберкулез у детей и подростков. М.: Медицина, 1984. с. 296.
3. Назаренко О. Р. Сравнительная ценность эхографии в оценке состояния органов брюшной полости у детей с острым лимфобластным лейкозом. Автореф. дис. . к. м. н, М., 1997. с. 24.
4. Нихамкин Л. И. Локальный опухолевидный амилоидоз брыжейки. Архив патологии, 1966. 4. с. 76 — 78.
5. Самочатова Е. В., Владимирская Е. Б., Жесткова Н. М., Наволоцкий А. В. и др. Болезнь Ходжкина у детей. М.: Алтус. — 1997. 96.
6. Тарасова И. С. Клинико-гематологическая характеристика детей при различных дозовых радиационных нагрузках. Автореф. дис. . к.м.н. М., 1997. с. 25.
7. Чернов В. М., Финогенова Н. А., Шахталин В. В., Сидорович Г. И. Структура гематологической заболеваемости детей в г. Клинцы Брянской области. В кн.: Медицинские аспекты влияния малых доз радиации на организм детей и подростков. Обнинск — Москва, 1992. с. 92 — 95.
8. Dangman B. C., Albanese B. A., Kocia M. Cat scratch disease with fever of unknoun origin: imaging features and association with new causative agent Rochalimea henselae. Pediatrics, 1995. v. 5. p. 767 — 771.
9. Emery A., Rimoin D. Principles and practice of medical genetics. 1988. V. 1, 2.
10. Flexman J. Bortanella henselae is a causative agent of cat scratch disease in Australia. J.Infect., 1995. V. 31. № 3. p. 241 — 245.
11. Leiber B. Die klinischen Syndrome. Muenchen, 1990, Bdd. 1,2.
12. Siegenthaler W. Differentialdiagnose innerer Krankheiten. Stuttgard, 1993. s. 800.
Читайте также:

