Дискоидная красная волчанка и склеродермия
Обновлено: 22.04.2024
Системная красная волчанка (СКВ) – аутоиммунное заболевание, этиология которого остается неизвестной. Кожный синдром при СКВ зачастую имеет первостепенное диагностическое значение – поражение кожи в 20-30% случаев является самым ранним симптомом, а у 60-
Systemic lupus erythematosus: alertness in the practice of a dermatologist / M. M. Tlish, Zh. Yu. Naatyzh1, T. G. Kuznetsova, E. A. Chernenko /State Budgetary educational institution of higher professional education Kuban State Medical University of the Ministry of Healthcare of the Russian Federation, Krasnodar, Russia
Abstract. Systemic lupus erythematosus (SLE) is an autoimmune disease, the etiology of which remains unknown. Skin syndrome in SLE is often of paramount diagnostic value – skin lesion is the earliest symptom in 20-30% of cases, and in 60-70% it manifests itself at various stages of the course of the disease, which leads to the patient's primary referral to a dermatologist. Frequent diagnostic errors are due to the absence of clinical symptoms of systemic lesions in the presence of cutaneous manifestations of lupus erythematosus (LE). In this case, laboratory tests are an integral part of the algorithm for managing patients with LE at the stage of contacting a dermatologist. The most specific laboratory test is the determination of antinuclear antibodies by an indirect immunofluorescence reaction, referred to as antinuclear factor (ANF). An elevated ANF titer is included in the list of diagnostic criteria for SLE, its detection allows one to suggest a diagnosis of SLE and determine a further algorithm for the provision of medical care. The article presents two clinical cases illustrating that against the background of an isolated skin lesion and the absence of visible somatic pathology, abnormalities in immunological tests were identified. This made it possible to suspect the systemic course of the process at an early stage and refer patients to a rheumatologist's consultation, where the diagnosis of SLE was confirmed. For citation: Tlish M. M., Naatyzh Zh. Yu., Kuznetsova T. G., Chernenko E. A. Systemic lupus erythematosus: alertness in the practice of a dermatologist // Lechaschy Vrach. 2020; vol. 23 (11): 23-26. DOI: 110.26295/OS.2020.35.78.005
Согласно современным представлениям, системная красная волчанка (СКВ) – аутоиммунное заболевание неустановленной этиологии, характеризующееся гиперпродукцией органонеспецифических аутоантител с развитием иммуновоспалительного повреждения тканей внутренних органов [1]. Широкий ряд вырабатываемых аутоантител и их прямое или опосредованное воздействие на клеточные мишени обуславливают многообразие клинических проявлений при красной волчанке (КВ) [2]. СКВ может проявляться изолированным или сочетанным поражением систем и органов, включающим поражение кожи и слизистых оболочек (волчаночная бабочка, дискоидная эритема, фотосенсибилизация, алопеция, телеангиэктазии, сетчатое ливедо, язвы в полости рта), сердечно-сосудистой системы (перикардит, миокардит, эндокардит, коронарит), почек (волчаночный нефрит), центральной нервной системы (судороги, психоз), опорно-двигательного аппарата (артралгии, артриты), легких (плеврит, волчаночный пневмонит), гематологическими нарушениями (гемолитическая анемия, лейкопения, тромбоцитопения) и т. д. [3].
Ключевую роль в диагностике СКВ играет обнаружение клинических проявлений заболевания и данные лабораторной диагностики [3]. Кожный синдром при СКВ зачастую имеет первостепенное диагностическое значение – поражение кожи в 20-30% случаев является самым ранним симптомом, а у 60-70% проявляется на различных этапах течения болезни, что приводит к первичному обращению больного именно к дерматологу [4]. Поражения кожи при СКВ полиморфны и представлены различными изменениями – от незначительных телеангиэктазий до буллезных поражений [2]. Выделяют волчаночно-специфичные и волчаночно-неспецифичные поражения кожи, последние встречаются в несколько раз чаще. К волчаночно-специ-фичным относят различные проявления хронической, подострой и острой КВ [5]. Группа неспецифических поражений включает: фотосенсибилизацию, лейкоцитокластический и уртикарный васкулит, телеангиэктазии, сетчатое ливедо, злокачественный атрофический папулез и синдром Рейно [5]. Широкая вариабельность клинических проявлений кожного синдрома обуславливает необходимость проведения тщательного дифференциального диагноза [1].
Важным инструментом ранней диагностики системных заболеваний является обнаружение аутоантител с помощью лабораторных тестов [3]. Наиболее специ-фичными для СКВ являются антинуклеарные антитела (АНА) – это гетерогенная группа аутоантител к компонентам клеточного ядра, среди которых выделяют антитела к двуспиральной дезоксирибонуклеиновой кислоте (ДНК), гистонам, нуклеосомам, экстрагируемым ядерным антигенам, ядрышковым антигенам и другим клеточным структурам [6]. Стандартным методом обнаружения группы АНА является непрямая реакция иммунофлюоресценции (НРИФ) с использованием линии эпителиальных клеток аденокарциномы гортани человека (HЕp-2) [7]. Определение АНА методом НРИФ принято обозначать как антинуклеарный фактор (АНФ), содержание которого оценивается по максимальному выявленному титру в сыворотке крови, с указанием интенсивности и типа флюоресценции [8]. Количественное увеличение титра свыше 1:160 входит в перечень диагностических критериев СКВ согласно рекомендациям Американской коллегии ревматологов (American College of Rheumatology, ACR) и Европейской лиги борьбы с ревматизмом (European League Against Rheumatism, ULAR) и используется для оценки активности процесса, прогноза, так как является предиктором развития СКВ на доклинической стадии [8].
Длительное формирование патогномоничного клинического симптомокомплекса СКВ, отсутствие проведения необходимых лабораторных исследований и междисциплинарного взаимодействия являются причиной частых диагностических ошибок, приводящих к отсутствию своевременной противовоспалительной и иммуносупрессивной терапии у врача-ревматолога. Учитывая вышесказанное, считаем целесообразным привести собственные клинические наблюдения.
Клиническое наблюдение № 1
Данные со стороны других органов и систем: предъявляет жалобы на ноющие боли в мелких суставах кистей и коленных суставах, чувство утренней скованности. Соматически не обследована.
Объективно: кожный патологический процесс носит ограниченный симметричный характер, локализуется на коже крыльев носа, щек, подбородка. Представлен: эритематозные пятна, чешуйки, телеангиэктазии.
На коже лица (в области крыльев носа, щек, подбородка) расположены ярко-розовые эритематозные очаги, с четкими границами, слегка инфильтрированные, правильной округлой формы, диаметром 3-4 см, покрытые небольшим шелушением в центре очагов; в периферической зоне очагов визуализируются телеангиэктазии (рис. 1). Удаление чешуек сопровождается болезненностью (симптом Бенье–Мещерского).
.jpg)
Определена биодоза 20 секунд.
Результаты гистоморфологического исследования кожи из патологического очага на правой щеке: фолликулярный гиперкератоз; эпидермис с тенденцией к атрофии; вакуольная дистрофия клеток базального слоя. Под эпидермисом сосуды расширены. Во всех отделах дермы – густые диффузные и периваскулярные лимфогистиоцитарные инфильтраты с примесью нейтрофилов и плазмоцитов. Вокруг сально-волосяных фолликулов – густой лимфогистиоцитарный инфильтрат с примесью нейтрофилов, тучных клеток и фибробластов, проникающий в наружное эпителиальное влагалище. В дерме – участки мукоидного набухания коллагеновых волокон. Заключение: морфологическая картина может соответствовать красной волчанке.
Данные общеклинических исследований: общий и биохимический анализ крови – показатели в пределах нормы; общий анализ мочи – показатели в пределах нормы.
Настораживающими факторами в плане трансформации кожной формы в системный процесс у пациентки М. явились: дебют заболевания в молодом возрасте, длительная инсоляция в анамнезе, II фототип кожи, биодоза 20 секунд, наличие выраженного суставного синдрома.
Для исключения диагноза СКВ было проведено иммунологическое исследование:
- Антинуклеарный фактор на НЕр-2 клетках: 1:320 титр (норма менее 160); мелкогранулярный тип свечения.
- Антитела к двуспиральной ДНК (a-dsDNA) – 53 МЕ/мл (норма – менее 25 МЕ/мл).
- Анализ крови на антитела к фосфолипидам класса IgG (скрининг) – 10,13 МЕ/мл (референсные значения: до 10 МЕ/мл – не обнаружено).
- Анализ крови на антитела к фосфолипидам класса IgM (скрининг) – 12,68 МЕ/мл (референсные значения: до 10 МЕ/мл – не обнаружено).
С полученными данными больная направлена к ревматологу в Краевую клиническую больницу № 2, где был подтвержден диагноз СКВ. Больная взята на диспансерный учет ревматологом для определения дальнейшей тактики ведения и лечения.
Клиническое наблюдение № 2
Объективно: кожный патологический процесс носит распространенный характер, локализован на коже лица, шеи. Представлен: пятна, телеангиэктазии, чешуйки.
На коже лица в области щек, левой околоушной области и шеи расположены отечные эритематозные очаги розовато-красного цвета, диаметром 2–3 см, преимущественно правильно-округлой формы с небольшим шелушением, визуализируются единичные телеангиэктазии. Удаление чешуек сопровождается болезненностью (симптом Бенье–Мещерского) (рис. 2).
.jpg)
Результаты гистоморфологического исследования кожи из патологического очага: на коже левой щеки – фолликулярный гиперкератоз; участки паракератоза; эпидермис местами атрофичен; вакуольная дистрофия клеток базального слоя эпидермиса; подэпидермальные пузыри. В сосочковом слое – отек, стенки сосудов утолщены. В дерме – густые очаговые и периваскулярные лимфогистиоцитарные инфильтраты с примесью нейтрофилов. Вокруг сально-волосяных фолликулов – густой лимфогистиоцитарный инфильтрат с примесью нейтрофилов, тучных клеток и фибробластов, проникающий в наружное эпителиальное влагалище. В дерме – участки мукоидного набухания коллагеновых волокон. Заключение: морфологическая картина больше соответствует красной волчанке.
Данные общеклинических исследований: в общем и биохимическом анализах крови выявлены следующие отклонения – лейкоциты 3,7 × 10 9 /л; холестерин 8,7 ммоль/л.
Учитывая длительность течения кожного патологического процесса, отсутствие результатов обследования смежных специалистов, для исключения диагноза СКВ было проведено иммунологическое исследование:
- Антинуклеарный фактор на НЕр-2 клетках: 12 560 титр (норма менее 160); крупногранулярный тип свечения.
- Антитела к двуспиральной ДНК (a-dsDNA) – 0,5 МЕ/мл (норма – менее 25 МЕ/мл).
- Анализ крови на антитела к фосфолипидам класса IgG (скрининг) 16,65 МЕ/мл (референсные значения: до 10 МЕ/мл – не обнаружено).
- Анализ крови на антитела к фосфолипидам класса IgM (скрининг) – 14,68 МЕ/мл (референсные значения до 10 МЕ/мл – не обнаружено).
Таким образом, иммунологические исследования и их комплексный анализ являются неотъемлемой составляющей алгоритма ведения больных с КВ уже на этапе обращения к врачу-дерматологу и способствуют высокому качеству оказания медицинской помощи данному контингенту больных.
Литература/References
М. М. Тлиш, доктор медицинских наук, профессор
Ж. Ю. Наатыж 1 , кандидат медицинских наук
Т. Г. Кузнецова, кандидат медицинских наук
Е. А. Черненко
ФГБОУ ВО КубГМУ Минздрава России, Краснодар, Россия
Системная красная волчанка: настороженность в практике дерматолога/ М. М. Тлиш, Ж. Ю. Наатыж, Т. Г. Кузнецова, Е. А. Черненко
Для цитирования: Тлиш М. М., Наатыж Ж. Ю., Кузнецова Т. Г., Черненко Е. А. Системная красная волчанка: настороженность в практике дерматолога // Лечащий Врач. 2020; т. 23 (11), 23-26. DOI: 110.26295/OS.2020.35.78.005
Теги: аутоиммунное заболевание, кожный синдром, алгоритм лечения
Очаговая склеродермия – это хроническое заболевание соединительной ткани, характеризующееся преимущественным поражением кожных покровов. Клинически проявляется уплотнением (индурацией) различных участков кожи с последующей атрофией и изменением пигментации, образованием контрактур. Диагноз ставится на основании симптоматики, обнаружения в крови антинуклеарного фактора и антицентромерных антител. В сомнительных случаях проводится гистологическое исследование кожи. Лечение заключается в применении глюкокортикостероидов, иммунодепрессантов, антифиброзных средств, блокаторов кальциевых каналов и проведении ПУВА-терапии. В ряде случаев выполняются хирургические операции.
МКБ-10
Общие сведения
Очаговая (локализованная, ограниченная) склеродермия – хроническое аутоиммунное заболевание из группы диффузных болезней соединительной ткани. Патология встречается повсеместно, распространенность составляет от 0,3 до 3 случаев на 100 000 человек. Чаще страдают женщины европеоидной расы. Возраст манифестации очаговой склеродермии зависит от формы. Бляшечная склеродермия чаще встречается у взрослых (30-40 лет), линейная - у детей от 2 до 14 лет, склероатрофический лихен – у женщин старше 50 лет. При локализованной форме, в отличие от системной, поражение внутренних органов в большинстве случаев либо минимально, либо отсутствует. Имеется ассоциация склеродермии с патологиями щитовидной железы (тиреоидитом Хашимото, болезнью де Кервена).

Причины
Точная причина заболевания неизвестна. Предполагается этиологическая роль бактерии Borrelia burgdorferi, вызывающей лайм-боррелиоз, однако убедительных данных за эту теорию на сегодняшний день нет. В развитии склеродермии важную роль играет наследственная предрасположенность. Были выявлены более частые случаи очаговой склеродермии среди близких родственников. При проведении генетических исследований обнаружена взаимосвязь между определенными генами гистосовместимости (HLA – DR1, DR4) и локализованной формой заболевания. Провоцирующими факторами, способствующими возникновению склеродермии, являются переохлаждения, травмы, постоянные вибрационные воздействия на кожу, прием лекарственных препаратов (блеомицина). Триггерными эффектами также обладают различные химические соединения (хлорвинил, кремний, нефтепродукты, сицилий, эпоксидная смола, пестициды, органические растворители).
Патогенез
Выделяют три основных патогенетических механизма склеродермии – фиброз (разрастание соединительной ткани), аутоиммунное повреждение и сосудистые нарушения. Иммунная аутоагрессия заключается в выработке лимфоцитами антител к соединительной ткани и ее компонентам. Также лимфоциты синтезируют интерлейкины, которые стимулируют пролиферацию фибробластов, гладкомышечных клеток и образование коллагена. Разрастающаяся при этом соединительная ткань замещает нормально функционирующую ткань. В результате повреждения эндотелия сосудов антителами и пролиферирующими гладкомышечными клетками снижается уровень простациклина (вещества, обладающего антиагрегантными и вазодилатирующими свойствами). Это приводит к спазму микрососудов, повышению адгезии и агрегации форменных элементов крови, внутрисосудистой коагуляции и микротромбозу.
Классификация
Очаговая склеродермия подразделяется на множество форм. Наиболее распространенными являются бляшечная и линейная. У ряда пациентов могут наблюдаться одновременно несколько вариантов заболевания. Существует целый ряд классификаций, но наиболее оптимальной и широко используемой считается классификация клиники Мэйо, включающей следующие разновидности очаговой склеродермии:
- Бляшечная. Данная форма в свою очередь подразделяется на поверхностную (морфеа) и узловатую (келоидоподобную). Характерны типичные участки уплотнения кожи с атрофией и нарушением пигментации.
- Линейная. К ней относятся полосовидная, саблевидная формы, а также прогрессирующая гемиатрофия лица Парри-Ромберга. Очаги располагаются в виде линий по ходу сосудисто-нервного пучка.
- Генерализованная (многоочаговая). Проявляется сочетанием бляшечного и линейного вариантов. Очаги распространены по всему телу.
- Буллезная. При данной разновидности на коже возникают пузыри с жидкостным содержимым, оставляющие после себя эрозии.
- Пансклеротическая инвалидизирующая. Наиболее неблагоприятная форма очаговой склеродермии. Характеризуется тяжелым, прогрессирующим течением, плохо поддается лечению. Поражаются все слои кожи и ткани, лежащие под ней. Развиваются грубые контрактуры суставов и длительно незаживающие язвы на коже.
- Склероатрофический лихен Цумбуша (болезнь белых пятен). Характерно образование пятен белого цвета, сопровождающихся нестерпимым зудом. Преимущественная локализация пятен – половые органы.
Симптомы
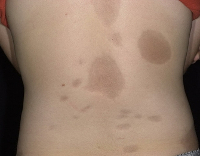
Для клинической картины типично образование на коже очагов, которые проходят три последовательных стадий развития – отек, индурацию (уплотнение) и атрофию. В начале заболевания на коже конечностей, шеи или туловища появляются пятна сиреневого или лилового цвета, имеющие нечеткие края. Размер пятен может сильно варьировать – от просяного зерна до размеров ладони и больше. На этом этапе пациент не испытывает каких-либо неприятных ощущений или боли. Затем пятна начинают отекать, кожа в центре очага уплотняется, становится блестящей, приобретает цвет слоновой кости. Пациент начинает ощущать зуд, покалывания, стянутость кожи, болезненность. Далее наступает стадия атрофии. Кожа в очагах истончается, прекращается рост волос, нарушается потоотделение, возникает стойкая дисхромия (гипер- или депигментация) и телеангиэктазии. Иногда развивается атрофодермия (участки западения кожи).
При линейной склеродермии очаги расположены по ходу нервов и сосудов. В случае локализации на коже лица очаги по внешнему виду напоминают рубец от удара саблей (саблевидная форма). Прогрессирующая гемиатрофия представляет собой глубокий процесс с поражением всех тканей половины лица - кожи, подкожной клетчатки, мышц и костей лицевого скелета, что приводит к выраженной деформации лица, обезображивающей внешний вид пациента. Также происходит атрофия половины языка и снижение вкусовой чувствительности.
Из внекожных признаков очаговой склеродермии стоит отметить офтальмологические и неврологические проявления при гемиатрофии Парри-Ромберга. Они включают выпадение ресниц и бровей на стороне поражения, западение глазного яблока из-за атрофии глазных мышц и орбитальной клетчатки, нейропаралитический кератит, головокружения, когнитивные нарушения, мигренозные головные боли, эпилептические припадки. Также возможно развитие феномена Рейно. Симптомы синдрома Рейно следующие – стадийное изменение окраски кожи пальцев рук вследствие вазоспазма и последующей гиперемии (бледность, цианоз, покраснение), сопровождающееся онемением, болью и покалыванием в пальцах рук. Остальные экстрадермальные проявления, характерные для системной склеродермии, встречаются крайне редко.
Осложнения
Наиболее распространенная проблема рассматриваемого заболевания – косметические дефекты. Серьезные осложнения, представляющие угрозу для жизни больного, возникают редко. К ним относятся нарушение мозгового кровообращения при гемиатрофии лица, ишемия и гангрена пальцев рук при феномене Рейно, выраженные контрактуры суставов, инвалидизирующие пациента. Через несколько лет после дебюта болезни могут развиться тяжелые поражения внутренних органов – фиброз легких, легочная гипертензия, фиброз миокарда, перикардит, стриктуры пищевода, острая нефропатия, почечная недостаточность.
Диагностика
Пациентов с очаговой склеродермией курируют врачи ревматологи и дерматологи. При постановке диагноза учитывается клиническая картина, семейный анамнез. Все методы диагностики направлены в первую очередь на определение степени вовлечения внутренних органов и исключение системной склеродермии. С этой целью применяются следующие исследования:
Очаговую склеродермию дифференцируют с другими формами склеродермии (системной, склеродермой Бушке), дерматологическим заболеваниями (саркоидозом кожи, липонекробиозом, склеродермоподобной формы поздней кожной порфирии, базально-клеточным раком), поражением мягких тканей (панникулитом, липодерматосклерозом, эозинофильным фасциитом). В дифференциальной диагностике принимают участие онкологи, гематологи.
Лечение
Этиотропной терапии не существует. Метод лечения и вид лекарственного средства необходимо подбирать с учетом формы заболевания, тяжести течения и локализации очагов. При линейной и бляшечной формах используются топические глюкокортикостероиды высокой и сверхвысокой активности (бетаметазон, триамцинолон), синтетические аналоги витамина Д. При выраженной индурации кожи эффективны аппликации с диметилсульфоксидом. В случае поражений внутренних органов с целью уменьшения фиброзообразования назначаются пеницилламин и инъекции гиалуронидазы.
При неглубоких процессах хорошим терапевтическим действием обладает ПУВА-терапия, которая включает облучение кожи ультрафиолетовыми волнами длинного спектра с одновременным пероральным или наружным применением фотосенсибилизаторов. Тяжелое поражение кожи служит показанием к применению иммунодепрессантов (метотрексата, такролимуса, микофенолата), синдром Рейно - блокаторов кальциевых каналов (нифедипина) и препаратов, улучшающих микроциркуляцию (пентоксифиллина, ксантинола никотината). При склероатрофическом лихене проводится низкоинтенсивная лазеротерапия. В случае развития контрактур суставов, значительно затрудняющих движения, или грубых деформаций скелета и косметических дефектов лица требуется хирургическая операция.
Профилактика и прогноз
В подавляющем большинстве случаев очаговая склеродермия имеет доброкачественное течение. Правильно подобранная терапия позволяет добиться регресса симптомов. Иногда наступают спонтанные ремиссии заболевания. Неблагоприятные исходы возникают при тяжелых формах (прогрессирующей гемиатрофии лица, пансклеротической инвалидизирующей склеродермии), а также поражении внутренних органов. Эффективных методов профилактики не разработано. Рекомендуется избегать или максимально ограничить контакт кожи с химическими соединениями (кремнием, сицилием, хлорвинилом, нефтепродуктами, органическими растворителями, пестицидами, эпоксидной смолой).
2. Ревматические заболевания/ Под ред. Дж.Х. Клиппела, Дж.Х. Стоуна, Л.Дж. Кроффорд, П.Х. Уайт – 2012.
3. Диффузные болезни соединительной ткани: руководство для врачей/ под ред. проф. Мазурова В.И. –2009.
Дискоидная красная волчанка – это хроническое воспалительное аутоиммунное заболевание кожи, развивающееся на фоне фотосенсибилизации (повышенной чувствительности к свету). Клинические проявления включают эритему, рубцовую атрофию кожи, фолликулярный гиперкератоз, выпадение волос, поражение ногтей. Диагноз ставится на основании симптоматики, анамнестических данных, наличия волчаночных клеток в крови, иммунологических тестов и гистологического исследования биоптата кожи. В качестве лечения применяются синтетические противомалярийные препараты, топические глюкокортикоиды, системные ретиноиды, солнцезащитные средства.
МКБ-10
Общие сведения
Дискоидная красная волчанка (ДКВ), или рубцующийся эритематоз – заболевание, относящееся к диффузным болезням соединительной ткани (коллагенозам). Данная патология является наиболее частой формой кожной красной волчанки. Средняя распространенность рубцующегося эритематоза составляет 1:100 000 человек. Чаще страдают представители европеоидной расы. Начало болезни приходится на молодой возраст (от 20 до 40 лет). Заболеваемости дискоидной волчанкой больше подвержены лица женского пола (соотношение с мужчинами 3:1). В редких случаях (1-5%) ДКВ может перейти в системную красную волчанку (СКВ).

Причины ДКВ
Эритематоз протекает по типу аутоиммунной реакции, точная причина возникновения которой неизвестна. Важное значение в развитии заболевания имеет наследственная предрасположенность, о чем свидетельствует большая встречаемость дискоидной волчанки среди близких родственников. В ходе исследований была установлена ассоциация ДКВ с антигенами тканевой совместимости HLA A1, A3, A10, A11, A18, B7, B8. Наиболее серьезным провоцирующим действием обладает ультрафиолетовое излучение.
К факторам, способствующим возникновению дискоидной волчанки, относятся постоянная травматизация кожи, хронические инфекции в организме, наличие аллергических болезней, прием лекарственных препаратов, повышающих чувствительность кожи к ультрафиолету (сульфаниламидов, тетрациклина, фторхинолонов, гризеофульвина, нейролептиков). В группе повышенного риска находятся люди, чей род деятельности связан с длительным пребыванием на открытом воздухе (работники сельскохозяйственной промышленности, строители, рыбаки). Также в группу риска входят лица с 1 фототипом кожи (кельтским) – это люди с нежной, тонкой, иногда веснушчатой кожей, имеющие светлый или рыжий цвет волос.
Патогенез
При дискоидной красной волчанке наблюдается патогенетическое сходство с СКВ, однако патологические реакции ограничиваются кожными покровами. В основе заболевания лежит аутоиммунное воспаление. Под действием ультрафиолетовых лучей в совокупности с другими провоцирующими факторами в клетках кожи нарушаются процессы метилирования ДНК (механизма регуляции транскрипции генов). Это приводит к повышению экспрессии белков, индуцирующих апоптоз (запрограммированную клеточную гибель) - p53, Fas и Fas-лиганда и гамма-интерферона.
Т- и В-лимфоциты стимулируют синтез цитокинов и антител к компонентам клеточных ядер (нуклеиновым кислотам, нуклеосомам). Образующиеся иммунные комплексы оседают на эндотелии сосудов, вызывая их повреждение. Выработку аутоантител у генетически предрасположенных лиц также способны вызывать антигены некоторых вирусов (Эпштейна-Барр, цитомегаловирус, парвовирус 19), имеющие сходную молекулярную структуру с белками клеточных мембран. Дополнительным повреждающим агентом выступает индукция свободнорадикального окисления липидов. Результатом этих процессов является массивное воспаление и разрушение клеток кожи.
Классификация
Традиционно дискоидную красную волчанку подразделяют на очаговую и диссеминированную (распространенную) – эти формы различаются количеством очагов поражения кожи и их локализацией. Также при диссеминированной форме отмечается наличие общей симптоматики (слабости, повышения температуры тела, болей в суставах) и высокого риска трансформации в СКВ. Помимо перечисленных форм, в ревматологии выделяют следующие виды ДКВ:
Симптомы ДКВ
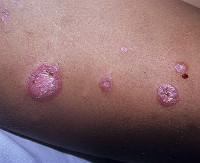
Дискоидная красная волчанка характеризуется хроническим течением, рецидивы возникают в основном летом или весной, когда длина солнечного дня максимальна. Чаще всего поражаются участки тела, подвергающиеся длительному солнечному излучению. Тремя наиболее типичными симптомами считаются эритема, фолликулярный гиперкератоз и рубцовая атрофия кожи.
При локализации очагов на волосистой части головы практически всегда возникает алопеция, которая оставляет после себя рубцы. При диссеминированной дискоидной волчанке очаги располагаются на груди, спине, локтях, ладонях, подошвах, обычно не имеют признаков шелушения и атрофии. Иногда поражаются ногтевые пластины. Ногти приобретают желтый цвет, становятся ломкими, деформируются. Очень редко в патологический процесс вовлекается слизистая оболочка полости рта. Очаги склонны к эрозированию, что вызывает жжение и боли во время приема пищи.
Осложнения
Серьезные осложнения дискоидной красной волчанки возникают редко. Иногда развивается вторичный гландулярный хейлит (воспаление мелких слюнных желез красной каймы губ). Диссеминированная форма ДКВ в некоторых случаях переходит в СКВ – тяжелое системное заболевание соединительной ткани, поражающее суставы и практически все внутренние органы (сердце, почки, легкие и центральную нервную систему). СКВ характеризуется упорным течением, трудно поддается терапии и имеет высокий риск летального исхода. Также может произойти трансформации стойких очагов дискоидной волчанки в плоскоклеточный рак кожи (сквамозно-клеточную карциному).
Диагностика
Пациентов с данной патологией курируют врачи ревматологи и дерматологи. При постановке диагноза дискоидной волчанки учитывается фототип кожи. На первичной консультации уточняется профессия пациента, прием фотосенсибилизирующих лекарственных средств, наличие инфекционных или аллергических заболеваний, близких родственников с ДКВ. Для диагностики проводят следующие методы исследования:
- Общие лабораторные тесты. В клиническом анализе крови отмечается увеличение скорости оседания эритроцитов, снижение уровня лейкоцитов, тромбоцитов, при инфекционных и аллергических патологиях - высокий уровень нейтрофилов и эозинофилов. При диссеминированной ДКВ возможен ложноположительный результат анализа на сифилис.
- Специальные ревматологические тесты. Примерно у 40% пациентов ДКВ обнаруживаются антинуклеарные антитела (ANA) и антитела к нуклеопротеинам (анти-Ro/SS-A, анти-La/SS-B). Волчаночные (LE) клетки встречаются у 5-7% пациентов. При реакции иммунной флюоресценции выявляются отложения иммуноглобулинов (IgG/IgM) и комплемента (положительный тест волчаночной полоски). Последний тест может быть положительным и при других заболеваниях, поэтому не является специфичным.
- Гистологическое исследование биоптата кожи. Биопсия кожи - наиболее достоверный метод для постановки диагноза. Характерны следующие признаки – атрофия эпидермиса, утолщение рогового слоя эпидермиса в устьях волосяных фолликулов, разрушение волокон коллагена, отек дермы, отложения в ней гиалина, периваскулярный лимфоцитарный инфильтрат.
Важно отличать диссеминированную форму ДКВ от системной красной волчанки, требующей более агрессивной терапии. Помощь в диагностике СКВ оказывает определение антител к двуспиральной ДНК и экстрагируемым ядерным ангигенам в крови пациента. Также дискоидную красную волчанку дифференцируют с другими формами кожной волчанки (острая, подострая), ревматологическими (дерматомиозит), дерматологическими заболеваниями (красный плоский лишай, псориаз, себорейный дерматит, экзема, фотодерматозы, эозинофильная гранулема лица, ангиолюпоид Брока-Потрие).
Лечение ДКВ
В большинстве случаев пациенты проходят лечение амбулаторно, но при тяжелом течении может потребоваться госпитализация в отделение ревматологии или дерматологии. Важным моментом является исключение приема фотосенсибилизирующих медикаментов и лечение сопутствующих аллергических или инфекционных заболеваний. Рекомендуется носить закрытую одежду, применять солнцезащитные крема или мази, содержащие вещества, которые задерживают ультрафиолетовые лучи (мексорил, двуокись титана, оксид цинка).
Основное патогенетическое лечение включает антималярийные аминохинолиновые препараты (Гидроксихлорохин), топические глюкокортикостероиды (тГКС), производные витамина А - ретиноиды (Изотретиноин, Ацитретин). Ввиду частого развития ретинопатий на фоне приема гидроксихлорохина обязателен регулярный осмотр офтальмолога. В зависимости от локализации дискоидных очагов применяются тГКС разной активности. При расположении очагов только на коже лица используют тГКС слабой и средней степени активности (Гидрокортизона ацетат, Метилпреднизолон), при поражении кожи конечностей и туловища рекомендуются тГКС сильной активности (Бетаметазон, Триамцинолон). Если дискоидные очаги имеются на ладонях и подошвах, назначаются тГКС сверхвысокой активности (Клобетазон).
Для подавления свободнорадикального повреждения клеток кожи эффективны антиоксиданты (альфа-токоферол). При неэффективности стандартного лечения прибегают к средствам, обладающим выраженным иммуносупрессивным действием – Такролимус, Метотрексат, Азатиоприн.
Прогноз и профилактика
В подавляющем большинстве случаев дискоидная волчанка имеет благоприятное течение. При грамотном подборе терапии и соблюдении всех рекомендаций наступает стойкая ремиссия. Основную проблему представляет трансформация ДКВ в более тяжелые заболевания, имеющие достаточно высокий процент летальности – СКВ и плоскоклеточную карциному. Профилактика рецидивов дискоидной волчанки заключается в ограничении времени пребывания на солнце, ношении закрытой одежды, применении солнцезащитных препаратов, исключении приема лекарств, повышающих чувствительность кожных покровов к ультрафиолетовому излучению.
1. Федеральные клинические рекомендации. Дерматовенерология 2015: Болезни кожи. Инфекции, передаваемые половым путем. 2016.
3. Федеральные клинические рекомендации по ведению больных с поражениями кожи при красной волчанке/ Самцов А.В., Чикин В.В. - 2015.
Системная красная волчанка – хроническое системное заболевание, с наиболее выраженными проявлениями на коже; этиология красной волчанки не известна, но ее патогенез связан с нарушением аутоиммунных процессов, в результате чего вырабатываются антитела к здоровым клеткам организма. Заболеванию в большей степени подвержены женщины среднего возраста. Заболеваемость красной волчанкой не велика – 2-3 случая на тысячу человек населения. Лечение и диагностика системной красной волчанки осуществляются совместными усилиями ревматолога и дерматолога. Диагноз СКВ устанавливается на основании типичных клинических признаков, результатов лабораторных анализов.




Общие сведения
Системная красная волчанка – хроническое системное заболевание, с наиболее выраженными проявлениями на коже; этиология красной волчанки не известна, но ее патогенез связан с нарушением аутоиммунных процессов, в результате чего вырабатываются антитела к здоровым клеткам организма. Заболеванию в большей степени подвержены женщины среднего возраста. Заболеваемость красной волчанкой не велика – 2-3 случая на тысячу человек населения.
Развитие и предполагаемые причины системной красной волчанки
Точная этиология красной волчанки не установлена, но у большей части пациентов обнаружены антитела к вирусу Эпштейна-Барр, что подтверждает возможную вирусную природу заболевания. Особенности организма, вследствие которых вырабатываются аутоантитела, также наблюдаются почти у всех больных.
Гормональная природа красной волчанки не подтверждена, но гормональные нарушения ухудшают течение заболевания, хотя спровоцировать его возникновение не могут. Женщинам с диагностированной красной волчанкой не рекомендован прием пероральных контрацептивов. У людей, имеющих генетическую предрасположенность и у однояйцевых близнецов заболеваемость красной волчанкой выше, чем в остальных группах.
В основе патогенеза системной красной волчанки лежит нарушение иммунорегуляции, когда в качестве аутоантигенов выступают белковые компоненты клетки, прежде всего ДНК и в результате адгезии мишенью становятся даже те клетки, которые изначально были свободны от иммунных комплексов.
Клиническая картина системной красной волчанки

При красной волчанке поражается соединительная ткань, кожа и эпителий. Важным диагностическим признаком является симметричное поражение крупных суставов, и, если возникает деформация суставов, то за счет вовлечения связок и сухожилий, а не вследствие поражений эрозивного характера. Наблюдаются миалгии, плевриты, пневмониты.
Но наиболее яркие симптомы красной волчанки отмечаются на коже и именно по этим проявлениям в первую очередь и ставят диагноз.

На начальных стадиях заболевания красная волчанка характеризуется непрерывным течением с периодическими ремиссиями, но почти всегда переходит в системную форму. Чаще отмечается эритематозный дерматит на лице по типу бабочки – эритема на щеках, скулах и обязательно на спинке носа. Появляется гиперчувствительность к солнечному излучению – фотодерматозы обычно округлой формы, носят множественный характер. При красной волчанке особенностью фотодерматозов является наличие гиперемированного венчика, участка атрофии в центре и депигментации пораженной области. Отрубевидные чешуйки, которыми покрывается поверхность эритемы, плотно спаяны с кожей и попытки их отделить, очень болезненны. На стадии атрофии пораженных кожных покровов наблюдается формирование гладкой нежной алебастрово-белой поверхности, которая постепенно замещает эритематозные участки, начиная с середины и двигаясь к периферии.
У некоторых пациентов с красной волчанкой поражения распространяются на волосистую часть головы, вызывая полную или частичную алопецию. Если поражения затрагивают красную кайму губ и слизистую оболочку рта, то очаги поражения представляют собой синюшно-красные плотные бляшки, иногда с отрубевидными чешуйками сверху, их контуры имеют четкие границы, бляшки склонны к изъязвлениям и причиняют боль во время еды.
Красная волчанка имеет сезонное течение, и в осенне-летние периоды состояние кожи резко ухудшается из-за более интенсивного воздействия солнечного излучения.

При подостром течении красной волчанки наблюдаются псориазоподобные очаги по всему телу, ярко выражены телеангиэктазии, на коже нижних конечностей появляется сетчатое ливедио (древоподобный рисунок). Генерализованная или очаговая алопеция, крапивница и кожный зуд наблюдаются у всех пациентов с системной красной волчанкой.
Во всех органах, где имеется соединительная ткань, со временем начинаются патологические изменения. При красной волчанке поражаются все оболочки сердца, лоханки почек, желудочно-кишечный тракт и центральная нервная система.
Если помимо кожных проявлений пациентов мучают периодические головные боли, суставные боли без связи с травмами и погодными условиями, наблюдаются нарушения со стороны работы сердца и почек, то уже на основании опроса можно предположить о более глубоких и системных нарушениях и обследовать пациента на наличие красной волчанки. Резкая смена настроения от эйфоричного состояния до состояния агрессии тоже является характерным проявлением красной волчанки.
У больных красной волчанкой пожилого возраста кожные проявления, почечный и артралгический синдромы менее выражены, но чаще наблюдается синдром Шегрена – это аутоиммунное поражение соединительной ткани, проявляющееся гипосекрецией слюнных желез, сухостью и резью в глазах, светобоязнью.
Дети, с неонатальной формой красной волчанки, родившиеся от больных матерей, уже в младенческом периоде имеют эритематозную сыпь и анемию, поэтому следует проводить дифференциальный диагноз с атопическим дерматитом.
Диагностика системной красной волчанки
Реакция Вассермана может быть ложноположительной, как и другие серологические исследования, что порой приводит к назначению неадекватного лечения. При развитии пневмонии проводят рентгенографию легких, при подозрении на плеврит - плевральную пункцию. Для диагностики состояния сердца - ЭКГ и эхокардиографию.
Лечение системной красной волчанки

Как правило, первоначальное лечение красной волчанки бывает неадекватным, так как ставятся ошибочные диагнозы фотодерматозов, экземы, себореи и сифилиса. И только при отсутствии эффективности назначенной терапии проводятся дополнительные обследования, в ходе которых и диагностируется красная волчанка. Полного излечения от этого заболевания добиться невозможно, но своевременная и корректно подобранная терапия позволяет добиться улучшения качества жизни пациента и избежать инвалидизации.
Пациентам с красной волчанкой нужно избегать прямых солнечных лучей, носить одежду, прикрывающую все тело, а на отрытые участки наносить крема с высоким защитным фильтром от ультрафиолета. На пораженные участки кожи наносят кортикостероидные мази, так как использование негормональных препаратов не приносит эффекта. Лечение необходимо проводить с перерывами, чтобы не развился гормонообусловленный дерматит.
В при неосложненных формах красной волчанки для устранения болевых ощущений в мышцах и суставах назначаются нестероидные противовоспалительные препараты, но с осторожностью следует принимать аспирин, так как он замедляет процесс свертывания крови. Обязателен прием глюкокортикостероидов, при этом дозы препаратов подбираются таким образом, чтобы при минимизации побочных эффектов защитить внутренние органы от поражений.
Метод, когда у пациента делают забор стволовых клеток, а потом проводят иммунодепрессивную терапию, после чего для восстановления иммунной системы вновь вводят стволовые клетки, эффективен даже в тяжелых и безнадежных формах красной волчанки. При такой терапии аутоиммунная агрессия в большинстве случаев прекращается, и состояние пациента с красной волчанкой улучшается.
Здоровый образ жизни, отказ от алкоголя и курения, адекватная физическая нагрузка, сбалансированное питание и психологический комфорт позволяют пациентам с красной волчанкой контролировать свое состояние и не допустить инвалидизации.
Волчанка красная системная — хроническое полисиндромное заболевание соединительной ткани и сосудов, развивающееся в связи с генетически обусловленным несовершенством иммунорегуляторных процессов.
Этиология. Предполагается значение вирусной инфекции на фоне генетически детерминированных нарушений иммунитета.
Патогенез: образование циркулирующих аутоантител, из которых важнейшее диагностическое и патогенетическое значение имеют антиядерные антитела; формирование циркулирующих иммунных комплексов, которые, откладываясь на базапьных мембранах различных органов, вызывают их повреждение и воспаление. Таков патогенез нефрита, дерматита, васкулита и др. Эта гиперреактивность гуморального иммунитета связана с нарушениями клеточной иммунорегуляции. В последнее время придается значение гиперэстрогенемии, сопровождающейся снижением клиренса циркулирующих иммунных комплексов и др. Доказано семейно-генетическое предрасположение. Болеют преимущественно молодые женщины и девочки-подростки. Провоцирующими факторами являются: инсоляция, беременность, аборты, роды, начало менструальной функции, инфекции (особенно у подростков), лекарственная или поствакцинальная реакция.
Симптомы, течение. Начинается болезнь постепенно с рецидивирующего полиартрита, астении. Реже бывает острое начало (высокая лихорадка, дерматит, острый полиартрит). В дальнейшем отмечается рецидивирующее течение и характерная полисиндромность.
Характерно поражение сердечно-сосудистой системы. Обычно развивается перикардит, к которому присоединяется миокардит. Сравнительно часто наблюдается бородавчатый эндокардит Либмана-Сакса с поражением митральных, аортальных и трикуспидальных клапанов. Признаки поражения сосудов входят в картину поражения отдельных органов. Тем не менее следует отметить возможность развития синдрома Рейно (задолго до типичной картины болезни), поражение как мелких, так и крупных сосудов с соответствующей клинической симптоматикой.
Поражения легких могут быть связаны с основным заболеванием в виде волчаночного пневмонита, характеризующегося кашлем, одышкой, незвонкими влажными хрипами в нижних отделах легких. Рентгенологическое исследование у таких больных выявляет усиление и деформацию легочного рисунка в базальных отделах легких; временами можно обнаружить очаговоподобные тоны. Поскольку пневмонит обычно развивается на фоне текущего полисерозита, .описанная рентгенологическая симптоматика дополняется высоким стоянием диафрагмы с признаками плевродиафрагмальных и плевроперикардиальных сращений и дисковидными ателектазами (линейные тени, параллельные диафрагме).
При исследовании желудочно-кишечного тракта отмечаются афтозный стоматит, диспепсический синдром и анорексия. Болевой абдоминальный синдром может быть связан как с вовлечением в патологический процесс брюшины, так и с собственно васкулитом — мезентериальным, селезеночным и др. Реже развиваются сегментарные илеиты. Поражение рети-кулоэндотелиапьной системы выражается в увеличении всех групп лимфатических узлов — весьма частом и раннем признаке системности болезни, а также в увеличении печени и селезенки. Собственно волчаночный гепатит развивается крайне редко. Однако увеличение печени может быть обусловлено сердечной недостаточностью при панкардите или выраженном выпотном перикардите, а также развитием жировой дистрофии печени.
Волчаночный диффузный гломерулонефрит (люпус-нефрит) развивается у половины больных обычно в период генерализации процесса. Встречаются различные варианты поражения почек — мочевой синдром, нефритический и нефротический. Для распознавания люпус-нефрита большое значение имеет прижизненная пункционная биопсия с иммуноморфологическим и электронно-микроскопическим исследованием биоптата почки. Развитие почечной патологии у больных с рецидивирующим суставным синдромом, лихорадкой и стойко повышенной СОЭ требует исключения волчаночного генеза нефрита. Следует помнить, что почти у каждого пятого больного с нефротическим синдромом имеет место системная красная волчанка.
Поражение нервно-психической сферы встречается у многих больных во всех фазах болезни. В начале болезни — астеновегетативный синдром, в последующем развиваются признаки поражения всех отделов центральной и периферической нервной системы в виде энцефалита, миелита, полиневрита. Характерно поражение нервной системы в виде менингоэнцефаломиелополирадикулоневрита. Реже наблюдаются эпилептиформные припадки. Возможны галлюцинации (слуховые или зрительные), бредовые состояния и др.
Лабораторные данные имеют диагностическое значение: определение большого числа LE-клеток, высоких титров антител к ДНК, особенно к нативной ДНК, к дезоксирибонуклеопротеиду, Sm-антигену.
При остром течении уже через 3–6 мес выявляется люпус-нефрит нередко по типу нефротического синдрома. При подостром течении отчетлива волнообразность с вовлечением в патологический процесс различных органов и систем и характерной полисиндромностью. Хроническое течение заболевания длительное время характеризуется редицивами полиартрита и (или) полисерозита, синдромами дискоидной волчанки, Рейно; лишь на 5–10-м году постепенно развивается характерная полисиндромность. В соответствии с клинико-лабораторной характеристикой выделяют три степени активности процесса; высокую (III степень), умеренную (II степень) и минимальную (I степень).
Лечение. Больные нуждаются в непрерывном многолетнем комплексном лечении. Лучшие результаты с развитием стойкой клинической ремиссии — при рано начатом лечении. При хроническом и подостром течении и I степени активности показаны нестероидные противовоспалительные препараты и аминохинолиновые производные. Первые рекомендуются при суставном синдроме. Важен подбор препарата с учетом его индивидуальной эффективности и переносимости: вольтарен (ортофен) по 50 мг 2–3 раза в день, индометацин по 25–50 мг 2–3 раза в день, бруфен по 400 мг 3 раза в день, хингамин (хлорохин, делагил) по 0,25–0,5 г/сут в течение 10–14 дней, а затем по 0,25 r/сут в течение нескольких месяцев. При развитии диффузного люпус-нефрита с успехом применяют плаквенил по 0,2 г 4–5 раз в день длительно под контролем за динамикой мочевого синдрома.
При остром течении с самого начала, а при подостром и хроническом течении при III, II степени активности патологического процесса показаны глюкокортикостерооды.. Начальная доза этих препаратов должна быть достаточной, чтобы надежно подавить активность патологического процесса. Преднизолон в дозе 40–60 мг/сут назначают при остром и подостром течении с III степенью активности и наличием нефротического синдрома или менингоэнцефалита. При этих же вариантах течения со II степенью активности, а также при хроническом течении с III и II степенью активности подавляющая доза должна быть 30–40 мг, а при I степени активности — 15–20 мг/сут. Лечение преднизолоном в подавляющей дозе проводят до наступления выраженного клинического эффекта (по данным снижения клинико-лабораторных показателей активности). По достижении эффекта дозу преднизолона медленно снижают, ориентируясь на предлагаемую схему (табл. 7).
Таблица 7. Примерная схема уменьшения доз преднизолона при достижении терапевтического эффекта
Одной из важнейших задач и залогом эффективности терапии являются подбор наименьшей дозы, которая позволяет поддерживать клинико-лабораторную ремиссию. Преднизолон в поддерживающей дозе 5–10 мг/сут назначают в течение нескольких лет.
Для уменьшения побочного эффекта гпкжокортикоидов рекомендуется сочетать эту терапию с препаратами калия, анаболическими стероидами, мочегонными и гипотензивными препаратами, транквилизаторами, противоязвенными мероприятиями. Наиболее серьезные осложнения: стероидная язва, септические инфекции, туберкулез, кандидоз, психозы.
При агрессивном течении болезни, высоком титре аутоантител, иммунных комплексов с успехом используется плазмаферез.
При неэффективности глюкокортикоидов назначают иммунодепрессанты (алкилирующего ряда или азатиоприн). Показания к назначению цитотоксических препаратов (обычно в комбинации с умеренными дозами кортикостероидов) следующие:
- 1 степень активности у подростков и в климактерическом периоде;
- нефротический и нефритический синдромы;
- необходимость быстро уменьшить подавляющую дозу преднизолона из-за выраженности побочного действия (быстрая и значительная прибавка в массе тела, чрезмерная артериальная гипертензия, стероидный диабет, выраженный остеопороз с признаками спондилопатии);
- необходимость снизить поддерживающую дозу преднизолона, если она превышает 15–20 мг/сут.
Наиболее часто применяют азатиоприн (имуран) и циклофосфан (циклофосфамид) в дозе 1–3 мг/кг (100–200 мг/ сут) в сочетании с 30 мг преднизолона. В этой дозе препарат назначают в течение 2–2,5 мес обычно в стационаре, затем рекомендуют поддерживающую дозу (50–100 мг в день), которую дают несколько месяцев и даже 1–2 года и более.
Чтобы обеспечить безопасность лечения, требуется тщательный контроль за анализом крови для предотвращения панцитопении; необходимо избегать присоединения инфекционных осложнений, диспепсических осложнений; при приеме циклофосфана опасность развития геморрагического цистита можно уменьшить путем назначения обильного питья (2 л жидкости и более в сутки).
Поскольку больные нуждаются в многолетнем лечении после выписки из стационара, они должны находиться под наблюдением терапевта или ревматолога в поликлинике. С целью улучшения переносимости многолетней кортикостероидной терапии в поликлинических условиях рекомендуется делагил по 0,25 г/сут и витамины группы В, аскорбиновая кислота в виде весенне-осеннего курса. Больным показано лечение в санаториях местного типа (кардиологических, ревматологических). Климатобальнеологическое, физиотерапевтическое лечение противопоказано, так как ультрафиолетовое облучение, инсоляция и гидротерапия могут вызвать обострение болезни.
Склеродермия системная — хроническое системное заболевание соединительной ткани и мелких сосудов с распространенными фиброзно-склеротическими изменениями кожи и стромы внутренних органов и симптоматикой облитерирующего эндартериита в форме системного синдрома Рейно.
Этиология неизвестна. Провоцируется охлаждением, травмой, инфекцией, вакцинацией и др.
В патогенезе ведущее значение имеет нарушение метаболизма коллагена, связанное с функциональной гиперактивностью фибробластов и гладкомышечных клеток сосудистой стенки. Не менее важным фактором патогенеза является нарушение микроциркуляции, обусловленное поражением сосудистой стенки и изменением внутрисосудистых агрегатных свойств крови. В известном смысле системная склеродермия — типичная коллагеновая болезнь, связанная с избыточным коллагенообразованием (и фиброзом) функционально неполноценными фибробластами и другими коллагенообразующими клетками. Имеет значение семейно-генетическое предрасположение. Женщины болеют в 3 раза чаще мужчин.
Симптомы, течение. Обычно заболевание начинается с синдрома Рейно (вазомоторных нарушений), нарушений трофики или стойких артралгий, похудания, повышения температуры тела, астении. Начавшись с какого-либо одного симптома, системная склеродермия постепенно или довольно быстро приобретает черты многосиндромного заболевания.
Поражение кожи — патогномоничный признак заболевания. Это распространенный плотный отек, в дальнейшем — уплотнение и атрофия кожи. Наибольшие изменения претерпевают кожа лица и конечностей; нередко кожа всего туловища оказывается плотной. Одновременно развиваются очаговая или распространенная пигментация с участками депигментации, телеангиэктазии. Характерны изъязвления и гнойнички на кончиках пальцев, длительно не заживающие и чрезвычайно болезненные, деформация ногтей, выпадение волос вплоть до облысения и другие нарушения трофики.
Нередко развивается фиброзирующий интерстициальный миозит. Мышечный синдром сопровождается миалгиями, прогрессирующим уплотнением, затем атрофией мышц, снижением мышечной силы. Лишь в редких случаях наблюдается острый полимиозит с болью, припухлостью мышцы и т. п. Фиброзирующие изменения в мышцах сопровождаются фиброзом сухожилий, что приводит к мышечно-сухожильным контрактурам — одной из причин сравнительно ранней инвалидизации больных. Поражение суставов связано главным образом с патологическими процессами в периартикулярных тканях (коже, сухожилиях, суставных сумках, мышцах). Артралгий наблюдаются у 80–90% больных, нередко сопровождаясь выраженной деформацией суставов за счет пролиферативных изменений околосуставных тканей; рентгенологическое исследование не выявляет значительных деструкции. Важный диагностический признак — остеолиз концевых, а в тяжелых случаях и средних фаланг пальцев рук, реже ног. Отложение солей кальция в подкожной клетчатке локализуется преимущественно в области пальцев и периартикулярных тканях, выражается в виде болезненных неровных образований, иногда самопроизвольно вскрывающихся с отторжением крошковидных известковых масс.
Поражение сердечно-сосудистой системы наблюдается почти у всех больных: поражаются миокард и эндокард, редко перикард. Склеродермический кардиосклероз клинически характеризуется болью в области сердца, одышкой, экстрасистолией, приглушением тонов и систолическим шумом на верхушке, расширением сердца влево. При рентгенологическом исследовании отмечаются ослабление пульсации и сглаженность контуров сердца, при рентгенокимографии — немые зоны в участках крупноочагового кардиосклероза; а в наиболее тяжелых случаях образуется аневризма сердца в связи с замещением мышечной ткани фиброзной. На ЭКГ обычно наблюдаются снижение вольтажа, нарушения проводимости вплоть до атриовентрикулярной блокады; инфарктоподобная ЭКГ бывает при развитии массивных очагов фиброза в миокарде. Если процесс локализуется в эндокарде, возможны развитие склеродермического порока сердца и поражение пристеночного эндокарда. Обычно страдает митральный клапан. Склеродермическому пороку сердца свойственно доброкачественное течение. Сердечная недостаточность развивается редко, главным образом при распространенном поражении мышцы сердца или всех трех его оболочек.
Поражение нервной системы проявляется полиневритами, вегетативной неустойчивостью (нарушение потоотделения, терморегуляции, вазомоторные реакции кожи), эмоциональной лабильностью, раздражительностью, плаксивостью и мнительностью, бессонницей. Лишь в редких случаях возникает картина энцефалита или психоза. Возможна симптоматика склероза сосудов головного мозга в связи с их склеро-дермическим поражением даже у лиц молодого возраста. Наблюдается поражение ретикулоэндотелиальной (попиадения, а у ряда больных и гепатоспленомегалия) и эндокринной (плюригландулярная недостаточность или патология той или другой железы внутренней секреции) систем.
Чаще имеет место хроническое течение, заболевание продолжается десятки лет с минимальной активностью процесса и постепенным распространением поражений на разные внутренние органы, функция которых долго не нарушается. Такие больные страдают преимущественно от поражения кожи, суставов и трофических нарушений. В рамках хронической системной склеродермии выделяют КРСТ-синдром (кальциноз, синдром Рейно, склеродактилия и телеангиэктазия), характеризующийся длительным доброкачественным течением с крайне медленным развитием висцеральной патологии. При подостром течении заболевание начинается сартрапгий, похудания, быстро нарастает висцеральная патология, а заболевание приобретает неуклонно прогрессирующее течение с распространением патологического процесса на многие органы и системы. Смерть обычно наступает через 1–2 года от начала заболевания.
Лабораторные данные не характерны. Обычно наблюдаются умеренная нормо- или гипохромная анемия, умеренные лейкоцитоз и эозинофилия, преходящая тромбоцитопения. СОЭ нормальна или умеренно повышена при хроническом течении и значительно увеличена (до 50–60 мм/ч) при подостром.
Лечение: применение противовоспалительных и общеукрепляющих средств, восстановление утраченных функций опорно-двигательного аппарата.
Активная противовоспалительная терапия кортикостероидами показана главным образом при подостром течении или в периоды выраженной активности процесса при хроническом течении. Преднизолон по 20–30 мг дают в течение 1–1,5 мес до достижения выраженного терапевтического эффекта, в дальнейшем очень медленно снижают, поддерживающую дозу (5–10 мг преднизолона) применяют долго, до получения стойкого эффекта. В период снижения доз гормональных препаратов можно рекомендовать нестероидные противовоспалительные средства. D-пеницилламин назначают по 150 мг 3–4 раза в день с постепенным повышением до 6 раз в день (900 мг) длительно, не менее года; особенно показан при быстром прогрессировании болезни; наиболее серьезное осложнение — нефротический синдром, требующий немедленной отмены препарата; диспепсические расстройства уменьшаются при временной отмене препарата, изменение вкуса может быть скорректировано назначением витамина В6. Аминохинолиновые препараты показаны при всех вариантах течения. Делагил (по 0,25 г 1 раз в день) или плаквенил (по 0,2 г 2 раза в день) можно назначать длительно, годами, особенно при ведущем суставном синдроме.
При хроническом течении рекомендуется лидаза (гиалуронидаза), под влиянием которой уменьшается скованность и увеличивается подвижность в суставах, преимущественно за счет размягчения кожи и подлежащих тканей. Лидазу вводят через день по 64 УЕ в 0,5% растворе новокаина п/к (12 инъекций на курс). Через 1–2 мес курс лечения лидазой можно повторить (всего 4–6 курсов в год). При выраженном ангиоспастическом компоненте (синдроме Рейно) показаны повторные курсы ангиотрофина (по 1 мл п/к, на курс 30 инъекций), калликреин-депо, андекалин (по 1 мл в/м, на курс 30 инъекций).
При всех вариантах течения болезни рекомендуется активная витаминотерапия, АТФ. При хроническом течении показаны бальнеотерапия (хвойные, радоновые и сероводородные ванны), парафиновые и грязевые аппликации, электрофорез гиалуронидазы, аппликации с 30–50% раствором диметил-сульфоксида (20–30 сеансов) на пораженные конечности. Важное значение имеют лечебная физкультура и массаж. При подостром течении рекомендуется утренняя гигиеническая гимнастика и активное положение в постели, при хроническом — настойчивое и длительное применение лечебной тмнастики в сочетании с массажем и различными трудовыми процессами (лепка из теплого парафина, плетение, пиление и т. п.).
Читайте также:

