Диспансерное наблюдение при микозе
Обновлено: 24.04.2024
В последние годы микозы с их разнообразной локализацией и клиническими проявлениями углубленно изучаются врачами самых различных специальностей. Так, по данным ВОЗ, 20% населения всего мира, т.е. каждый пятый житель планеты, поражены грибковой инфекцией [Аравийский Р.А. и сотр., 2004; Pontes Z.B. et al., 2009]. Широкое распространение грибов в природе, их постоянное присутствие как в окружающей среде, так и в организме обусловливает неизбежность контактов и инфицированность ими человека.
В настоящее время отмечается увеличение числа больных с микотическим поражением ЛОР-органов и, в частности, наружного и среднего уха, включая послеоперационные полости среднего уха. Рост числа больных обусловлен как существенным увеличением факторов риска развития микоза, так и бессистемным неконтролируемым применением местных антибактериальных препаратов при лечении отита. Кроме того, отмечено повышение удельного веса хронического грибкового воспаления с частыми рецидивами, не поддающимися медикаментозной коррекции, что, в свою очередь, приводит к увеличению сроков нетрудоспособности и инвалидизации населения [Гацко Ю.С., 2007, 2008; Тарасова Г.Д., 2007; Лучихин Л.А., 2008]. Это обусловило необходимость проведения настоящего исследования.
С целью определения частоты заболеваемости отомикозом, повышения эффективности диагностики и лечения грибкового поражения уха нами проведено исследование среди жителей г. Москвы, обратившихся в консультативно-диагностическое отделение МНПЦ оториноларингологии ДЗМ. Объект исследования - 1762 больных с воспалительными заболеваниями ушей, которые наблюдались и проходили лечение в период с января 2003 г. по декабрь 2007 г. Проведен ретроспективный анализ отчетной документации ЛОР-кабинетов городских поликлиник за 2003-2007 гг., включающий 500 амбулаторных карт больных с хронической воспалительной патологией уха.
Методы исследования: клиническое, эндомикроскопическое, микробиологическое, микологическое, рентгенологическое (включая КТ, МРТ), эпидемиологическое, статистическое.
Микологические исследования у больных отомикозом проводили в два этапа. Сначала применяли экспресс-методы - отомикроскопию (осмотр уха под операционным микроскопом), исследование нативных и окрашенных препаратов в световом и люминесцентном микроскопе с использованием просветляющих растворов, метиленового синего, комплекса красителей Грама. Впервые для быстрого обнаружения грибов при отомикозе нами применен метод окрашивания калькофлюором белым, который связывается с полисахаридами клеточных стенок грибов. Преимущество метода состоит в его простоте, оперативности, низкой стоимости, хорошей специфичности и отсутствии ложноположительных результатов. На основании результатов микроскопии определяли род гриба. Параллельно отбирали материал для микологических исследований, в ходе которых проводился посев патологического отделяемого на жидкие или твердые питательные среды с последующим подсчетом колоний, оценкой интенсивности роста, видовой идентификации и чувствительности к антимикотическим препаратам. Видовую идентификацию дрожжеподобных грибов проводили с помощью тест-систем API 20 (bioMerieux, Франция), плесневых по протоколу MI 38.
Примененный комплексный подход к диагностике отомикоза позволил установить грибковую природу заболевания у 405 из 1762 больных (22,98%), в том числе у 228 женщин (56,3%) в возрасте от 16 до 85 лет (средний возраст - 54,6±2,04 года) и у 177 мужчин (43,7%) в возрасте от 17 до 82 лет (средний возраст - 51,2±3,45 года).
С целью выявления особенностей этиологии, патогенеза, клинической картины и разработки оптимального лечения все больные отомикозом были разделены на 3 группы в соответствии с локализацией воспалительного процесса: 1-я группа - пациенты с наружным грибковым отитом (280 человек), 2-я группа - пациенты с грибковым поражением среднего уха (72 человека) и 3-я группа - пациенты с микотическим поражением послеоперационной полости среднего уха (53 человека). У 157 больных процесс был двусторонним. Длительность заболевания составила от 2 месяцев до 45 лет.
Анализ результатов исследования патогенов при различной локализации микоза выявил следующее. Всего подтверждено поражение грибами 562 ушей (24,9%), при этом монокультура гриба выявлена в 470 случаях, а еще у 92 имелись грибково-грибковые или грибково-бактериальные ассоциации.
В зависимости от локализации процесса выявлены различия. Так, при наружном грибковом отите основными возбудителями являлись плесневые грибы, выявленные у 180 больных (64,3%), при этом на долю рода Aspergillus приходилось 162 наблюдения (57,85%). Дрожжеподобные грибы определены как этиологический фактор в 100 наблюдениях (35,7%), при этом наиболее патогенный вид грибов Candida albicans выделен только у 21 больного.
На втором месте по значимости стоит вид Candida tropicalis, выделенный у 17 больных наружным грибковым отитом. При обследовании 40 больных с помощью метода окрашивания калькофлюором белым и микроскопии мазков в УФ-спектре наличие грибов рода Candida было установлено в 100% случаев при первичном осмотре. У всех пациентов присутствие гриба этого рода было подтверждено при микроскопии окрашенного мазка и при посеве на селективные питательные смеси. Установлена этиопатогенетическая значимость и других видов грибов рода Candida: C. tropicalis, C. krusei, C. sake, C. parapsilosis, C. pseudotropicalis, C. glabrata, C. hellermanii, C. ciferrii, C. dubliniensis, C. famata, C. globosa, C. curvata, C. intermedia, Candida spp. Эти данные важно учитывать при диагностике и лечении отомикоза.
Установлено, что у больных со средним грибковым отитом преобладающими возбудителями являлись дрожжеподобные грибы рода Candidа (79,2%), а доля плесневых грибов составляла 20,8%, что является главным отличием от больных с грибковым поражением наружного уха и послеоперационных полостей среднего уха. Среди грибов рода Candida доля Candida albicans составляла лишь 24,5% от всех видов дрожжеподобных грибов, а доля штаммов Candida non-albicans - 75,5%.
У 15 больных возбудителем среднего отита были различные плесневые грибы: Aspergillus niger - 10 наблюдений, у 2 больных возбудителем воспалительного процесса были грибы Aspergillus fumigatus, и у 2 больных - другие виды аспергилл. У одного больного причиной заболевания являлся гриб рода Mucor.
У больных с грибковым поражением послеоперационных полостей среднего уха преобладающими возбудителями были плесневые грибы, доля которых составила 94,3% от общего числа больных с этой патологией. Доминировали грибы рода Aspergillus, выделенные в 88,67% случаев, тогда как на долю грибов рода Candida пришлось лишь 5,7%. Установленный нами факт, что при микозе послеоперационных полостей среднего уха доминируют плесневые грибы, необходимо учитывать при выборе препарата для лечения.
Объективное клиническое обследование 280 больных с грибковым наружным отитом помогло нам выявить наиболее характерные клинические проявления как при плесневых, так и при кандидозных поражениях. Основными клиническими проявлениями грибкового наружного отита являются боль и окрашенные выделения из уха. При осмотре выявляется патологическое отделяемое в виде казеознонекротических масс, окрашенных в зависимости от гриба-возбудителя. При клиническом обследовании больных с грибковым средним отитом и микозе послеоперационных полостей выявлено, что основными жалобами были ушная боль, шум, наличие выделений, головокружение. Частота характерных жалоб представлена в таблице 1.
Таблица 1. Частота жалоб при локализации микотического процесса в разных отделах уха
Тщательный сбор анамнеза позволил установить факторы, провоцирующие развитие отомикоза. Нами установлено, что в патогенезе заболевания важную роль играет снижение общей противоинфекционной резистентности организма, формирующееся на фоне соматической патологии, например сахарного диабета. Местные факторы представлены в таблице 2.
Таблица 2. Основные факторы, провоцирующие развитие отомикоза у обследованных больных по данным анамнеза
При терапии отомикоза мы придерживались определенных принципов: лечение должно быть направлено не только на грибковую инфекцию, но и на устранение различного рода факторов, играющих роль в патогенезе данного микоза. Нами применялась системная и местная терапия. В ходе лечения проводилась смена препаратов с учетом чувствительности возбудителя.
Анализ течения заболевания показал, что, по сравнению с бактериальным, при грибковом поражении уха длительное время сохраняются патологические выделения, имеющие как специфический, так и неспецифический для микоза характер.
При лечении наружного грибкового отита мы применяли только местные лекарственные формы противогрибковых препаратов групп аллиламинов, азолов и полиенов в виде растворов и кремов. При лечении больных с грибковым средним отитом и поражением послеоперационных полостей среднего уха помимо местных форм применялись системные противогрибковые препараты групп азолов и аллиламинов. Продолжительность лечения составила от 14 до 48 дней. У 355 больных (87,6%) после одного курса лечения достигнуто излечение, подтвержденное микологическими исследованиями. У 50 больных один курс лечения оказался неэффективным, что потребовало проведения повторных курсов противогрибковой терапии. В отдаленном периоде (сроки наблюдения составили от 4-х мес. до 4,5 года) заболевание рецидивировало у 76 больных (18,8%).
Серьезной проблемой при лечении наружного грибкового отита остается изменение состояния кожи, сохраняющееся и после лабораторного излечения, подтвержденного неоднократными результатами микологических исследований.
Согласно рекомендации дерматологов, при терапии экзематозного поражения кожи препаратами выбора являются топические кортикостероиды в виде мазей и кремов, что противоречит концепции лечения грибковых заболеваний, т.к. роль кортикостероидов в развитии поверхностного микоза велика.
В арсенале практического врача имеются комбинированные лекарственные средства, имеющие в своем составе антибактериальные, противогрибковые препараты, кортикостероиды, анестетики.
Примером таких комбинаций являются: клотримазол, гентамицин, бетаметазон (в виде крема и мази Тридерм, Акридерм); изоконазол и дифлукортолон (мазь Травокорт); пимафуцин, натамицин, гидрокортизон (крем и мазь Пимафукорт); клотримазол, хлорамфеникол, беклометазон и лигнокаин (капли Кандибиотик). Однако входящие в их состав азоловые и полиеновые антимикотики, согласно данным наших исследований, высокоэффективны лишь при лечении кандидозного поражения.
Лекарственные формы в виде мази неудобны для самостоятельного применения пациентом при лечении отита, т.к. провести тщательную обработку наружного слухового прохода и послеоперационной полости среднего уха можно лишь под контролем зрения, а самостоятельный туалет уха при поврежденной барабанной перепонке недопустим в связи с высоким риском повреждения структур внутреннего уха.
Таким образом, средством выбора при лечении больных с наружным грибковым отитом и микозом послеоперационной полости среднего уха, вызванным дрожжеподобными грибами, может стать препарат Кандибиотик.
Кандибиотик обладает выраженными местными анестезирующим, противовоспалительным, противоаллергическим, антимикотическим и антибактериальным свойствами. Выпускается в виде ушных капель во флаконах темного стекла по 5 мл в комплекте с пробкой-пипеткой.
В его состав входят: действующие вещества - клотримазол, хлорамфеникол, беклометазона дипропионат, лигнокаина гидрохлорид; вспомогательные вещества - пропиленгликоль и глицерин.
Клотримазол - противогрибковое средство для местного применения из группы производных имидазола. Нарушает синтез эргостерола (основной структурный компонент клеточной мембраны грибов), изменяет проницаемость мембраны гриба, способствует выходу из клетки калия, внутриклеточных соединений фосфора и распаду клеточных нуклеиновых кислот. Провоцирует лизис грибковой клетки. Ингибирует трансформацию бластоспор Candida albicans в инвазивную мицелиальную форму. Клотримазол действует главным образом на растущие и делящиеся микроорганизмы. Штаммы грибов, имеющих естественную резистентность к клотримазолу, встречаются редко.
Хлорамфеникол - бактериостатический антибиотик широкого спектра действия, которое связано с нарушением синтеза белка рибосомами. Активен в отношении грамположительных и грамотрицательных бактерий. Ототоксический эффект при его применении не описан.
Беклометазона дипропионат - глюкокортикостероид. Оказывает противовоспалительное и противоаллергическое действие.
Лигнокаина гидрохлорид — местноанестезирующее средство. Вызывает обратимую блокаду проведения импульса по нервным волокнам за счет блокирования прохождения ионов натрия через мембрану.
Показаниями к применению препарата Кандибиотик являются аллергические и воспалительные заболевания уха, в том числе: острый и хронический диффузный наружный отит, острый средний отит, состояние после хирургических вмешательств на ухе.
Применение препарата Кандибиотик противопоказано при перфорации барабанной перепонки, однако входящие в его состав мощный анестетик и кортикостероид делают его препаратом выбора (в комплексном лечении) при остром среднем отите. Результаты исследований подтверждают быстрый обезболивающий эффект при остром среднем отите. Пиковый эффект при применении лидокаина наступает уже на 4-5 минуте после закапывания капель в наружный слуховой проход. А через 10 минут после закапывания интенсивность боли снижается вдвое у всех больных.
Благодаря кортикостероиду, входящему в состав препарата Кандибиотик, удается в короткие сроки уменьшить явления воспаления со стороны кожи наружного слухового прохода.
Противопоказанием к применению препарата Кандибиотик является повышенная чувствительность к компонентам препарата. Вопрос о целесообразности назначения препарата во время беременности должен решаться индивидуально после консультации врача. Несмотря на то, что в клинических и экспериментальных исследованиях отрицательное влияние на здоровье женщины или плода не установлено, не следует использовать препарат в больших количествах и в течение длительного времени.
Нежелательные явления, связанные с применением препарата Кандибиотик, отмечаются редко.
Кандибиотик применяют местно, закапывая по 4-5 капель в наружный слуховой проход больного уха 3-4 раза в день. Улучшение состояния наступает в течение 3-5 дней, курс лечения - 7-10 дней.
Таким образом, при лечении больных с длительно текущим воспалением в наружном и среднем ухе необходимо проведение комплексного микологического обследования патологического отделяемого из уха, включающего микроскопическое и культуральное исследования. При лечении больных отомикозом, вызванным дрожжеподобными грибами, может быть применен препарат Кандибиотик. Применение только местных лекарственных форм допустимо при лечении больных с наружным грибковым отитом. При лечении больных со средним грибковым отитом и микозом послеоперационных полостей среднего уха необходимо применение системных препаратов. Больные, перенесшие отомикоз, нуждаются в диспансерном наблюдении.
Микозы желудочно-кишечного тракта — патологические состояния, развившиеся вследствие поражения пищеварительных органов дрожжеподобными, плесневыми, диморфными грибами. Проявляются изменением вкуса, появлением налетов на видимых слизистых, диспепсией, жидким стулом, болевыми ощущениями разной локализации. Диагностируются с помощью эзофагогастродуоденоскопии, колоноскопии, электрогастрографии, микробиологического исследования биоптата, ИФА, РИФ, ПЦР. Для лечения используют антимикотики, пробиотики, иммуномодуляторы в сочетании с комплексной терапией основного заболевания, осложнившегося грибковой инфекций.
МКБ-10
Общие сведения

Причины микозов желудочно-кишечного тракта
Возбудителями микотической инфекции органов ЖКТ становятся плесневые, дрожжеподобные, диморфные грибы, в большинстве случаев являющиеся естественными комменсалами человеческого организма. 9 из 10 микозов пищеварительного тракта провоцируется Candida albicans — условно-патогенным микроорганизмом, который высеивается у 65-70% населения. Микотический процесс также может развиться в результате размножения так называемых кандид non-albicans (С. guilliermondii, С. kefyr, С. krusei, С. tropicalis и др.). Некандидозные формы микотических желудочно-кишечных болезней, вызванные возбудителями бластомикоза, гистоплазмоза, кокцидиомикоза, криптококкоза, паракокцидиомикоза, споротрихоза, возникают при диссеминации грибов из очагов на коже, в респираторном тракте, других органах. Аспергиллез пищеварительных органов, интестинальный зигомикоз диагностируются редко, обычно – при наличии тяжелой сопутствующей патологии.
Манифестации микозов часто предшествуют другие патологические состояния, способствующие патологической активации условно-патогенной флоры за счет снижения местной защитной реакции слизистой ЖКТ, угнетения иммунных сил организма. Специалисты в сфере гастроэнтерологии и микологии выделяют следующие предпосылки к развитию желудочно-кишечного микотического заболевания:
- Физиологическая иммунная недостаточность. Естественное снижение иммунитета наблюдается у беременных, связано с необходимостью поддержания гестации. Незрелость иммунной системы характерна для новорожденных, риск инфицирования возрастает при недоношенности и наличии генитального кандидоза у матери. В пожилом возрасте отмечается инволютивное угасание защитных сил.
- Патологический иммунодефицит. Несостоятельность иммунной системы лежит в основе ВИЧ-инфекции и ее клинически выраженной формы — СПИД. Нарушения иммунитета отмечаются при дисплазии тимуса, других первичных иммунодефицитах, онкогематологических и лимфопролиферативных болезнях (лейкозах, лимфогранулематозе, неходжкинских лимфомах), сахарном диабете, голодании.
- Ятрогенные факторы. Иммунная функция угнетается при использовании кортикостероидов, цитостатиков, других химиопрепаратов у пациентов, перенесших трансплантацию органа, принимающих лечение по поводу онкопатологии, ревматоидного артрита, СКВ, гломерулонефрита, других системных болезней. Развитию микозов способствует антибактериальная терапия.
- Повреждения слизистой оболочки ЖКТ. Инвазии грибов более подвержены больные, страдающие атрофическим гастритом, ахалазией кардии, бульбитом, гастроэзофагеальной рефлюксной болезнью, дисбиозом, болезнью Крона, другой желудочно-кишечной патологией. Инфицирование облегчается при ожогах, травматизации эпителия зубными протезами, твердой пищей, интубационной трубкой.
Патогенез
Механизм развития микозов желудочно-кишечного тракта основан на нарушении баланса между реактивностью организма и факторами патогенности грибов — протеолитическими ферментами инвазии (коагулазой, каталазой, козеиназой, фосфолипазой), фибриллярными белковыми комплексами, эндотоксинами. При иммунодефиците уменьшается активность интраэпителиальных лимфоцитов, В-клеток кишечника, снижается цитотоксичность Т-клеточных элементов, нарушается секреция интерферона, фагоцитоз. В результате возбудители микозов быстро обсеменяют эпителий, легко проникают через собственную пластинку слизистой, агрегируются в пейеровых бляшках.
При травмах, химических ожогах, заболеваниях пищеварительных органов, изменениях кислотности и ферментативного состава желудочного, кишечного соков ситуация усугубляется наличием участков пораженной слизистой, замедленной регенерацией эпителиальных клеток, нарушением защитной функции естественных секретов. У пациентов, принимающих антибиотики, дополнительным патогенетическим фактором становится гибель облигатных микроорганизмов (кишечной палочки, аэробных лактобацилл, анаэробных бифидобактерий), которые являются естественными антагонистами грибов и сдерживают их неконтролируемое размножение.
Классификация
При систематизации форм микотической инфекции ЖКТ учитывают вид возбудителя, локализацию и распространенность патологического процесса. С учетом этиологии различают кандидоз, являющийся самым частым видом микозов, и редкие формы грибкового поражения (аспергиллез, криптококкоз, зигомицетоз и др.). При поражении одного отдела пищеварительного тракта говорят о фокальном микозе, при массивном распространении инфекции — об инвазивном диффузном, при отсутствии признаков инвазии — о микотическом дисбиозе. Наиболее часто используют классификацию микозов по локализации поражения, в соответствии с которой выделяют:
- Орофарингеальные поражения. В структуре микотических инфекций ЖКТ занимают первое место. Обычно встречаются у новорожденных и пациентов с иммунодефицитными состояниями (СПИД, гемобластозы).
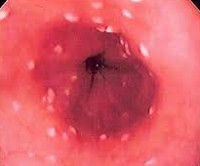
- Микотический эзофагит. Диагностируется у 1-7% больных. Чаще развивается при сниженном иммунитете. Может протекать как в поверхностной, так и в эрозивной форме с повышенной кровоточивостью.
- Микотические поражения желудка. Составляют до 5,2% микозов ЖКТ. Выявляются при гастродуоденальных язвах, хронических гастритах. В ряде случаев определяются ассоциации грибов и хеликобактера.
- Микозы кишечника. Обычно возникают на фоне микотического поражения верхних отделов пищеварительного тракта. Как правило, диагностируются у больных, получающих массивную антибиотикотерапию.
- Микотическая инфекция гепатобилиарной системы. Осложняет дискинезию желчных путей, холестаз, холецистолитиаз, лямблиоз. Диагностируется редко, в том числе из-за низкой настороженности.
Симптомы микозов ЖКТ
Клиническая картина заболевания различна в зависимости от распространенности поражения. При орофарингеальной локализации микоза у пациента возникают боли во время приема пищи, неприятный привкус во рту, на слизистой оболочке щек и языка появляются белые налеты. Поражение пищевода и желудка характеризуется болью при глотании, дисфагией, изжогой, отрыжкой, тошнотой и рвотой, дискомфортом в эпигастральной области, снижением аппетита. При прогрессировании заболевания в процесс вовлекаются нижележащие отделы желудочно-кишечного тракта, что клинически проявляется диареей с примесями слизи и крови, болезненностью в левой подвздошной области. Возможны нарушения общего состояния: субфебрильная температура тела, слабость, снижение трудоспособности, резкое уменьшение веса.
Осложнения
Вследствие проникновения микроорганизмов из пищеварительного тракта в забрюшинную клетчатку могут возникать гнойно-воспалительные процессы — парапроктит, паранефрит, межкишечные или поддиафрагмальные абсцессы. У пациентов со сниженной реактивностью организма имеется склонность к генерализации микозов с развитием септицемии, приводящей к распространению грибков на другие органы. Наиболее опасно микотическое поражение гепатобилиарной системы, которое может вызывать желтуху и печеночную недостаточность. При тяжелом течении заболевания формируются некрозы стенки кишечника, иногда – с перфорацией. Возможны профузные желудочно-кишечные кровотечения, пенетрация язв в соседние органы.
Диагностика
Постановка диагноза микозов желудочно-кишечного тракта затруднена из-за полиморфности и неспецифичности клинической картины заболевания, которая сходна с проявлениями других патологий пищеварительной системы. Для диагностики грибкового поражения требуется комплексное обследование пациента. Наиболее информативными являются следующие методы:
В клиническом анализе крови наблюдаются неспецифические признаки воспалительного процесса: повышение СОЭ, незначительный лейкоцитоз, может выявляться снижение уровня эритроцитов и гемоглобина, что обусловлено кровотечениями. Для исследования структуры всех слоев стенки пищеварительного тракта выполняется эндоскопическая ультрасонография. Дифференциальная диагностика осуществляется с воспалительными заболеваниями кишечника (терминальным илеитом, неспецифическим язвенным колитом), злокачественными новообразованиями, псевдомембранозным энтероколитом, желудочно-кишечным туберкулезом. Помимо осмотра гастроэнтеролога пациенту могут потребоваться консультации инфекциониста, онколога, фтизиатра.
Лечение микозов ЖКТ
Основными задачами являются терапия расстройства, вызвавшего активацию микотической флоры, и этиопатогенетическое воздействие на возбудителя грибковой инфекции. Лечение болезней пищеварительного тракта, иммунодефицитных и других патологических состояний проводят по протоколам соответствующих заболеваний. Для подавления грибкового процесса используют:
- Антимикотики. По результатам наблюдений, наиболее эффективной является терапия триазолами. Средства этой группы угнетают систему цитохрома P-450 и синтез эргостерола клеточных мембран, нарушая рост и репликацию кандид и криптококков. В качестве альтернативы с учетом особенностей возбудителя могут применяться полиены, аллиламины, эхинокандины.
- Пробиотики. Препараты, в которых содержатся непатогенные и нетоксигенные микроорганизмы, позволяют восполнить естественную микрофлору кишечника, нормализовать ее состав после проведенной антибактериальной терапии. Апатогенные бактерии стимулируют кишечный иммунитет, оказывают антагонистический эффект по отношению к грибам, нарушают их адгезию к слизистым.
При отсутствии противопоказаний проводится неспецифическая иммунотерапия стимуляторами естественного иммунитета (высокополимерные полисахаридные комплексы, регенеранты, производные пиримидина), Т- и В-лимфоцитов (полипептидные экстракты вилочковой железы, культур клеток костного мозга, селезенки). Возможно дополнительное использование растительных иммуномодуляторов, витаминно-минеральных комплексов.
Прогноз и профилактика
Исход болезни зависит от степени повреждения пищеварительных органов, состояния иммунной системы пациента, своевременности диагностики и терапии. Прогноз сомнительный при генерализации процесса и наличии тяжелых сопутствующих заболеваний. Для предупреждения развития микозов необходимо не допускать неоправданного применения антибактериальных средств, назначать профилактические курсы противогрибковых препаратов при длительном лечении цитостатиками, кортикостероидами, другими медикаментами с иммунодепрессорным эффектом, осуществлять диспансерное наблюдение за пациентами с иммунодефицитом.
2. Грибковые поражения желудочно-кишечного тракта/ Омаров Т.Р., Омарова Л.А.// Русский медицинский журнал – 2016 - №11.
3. Микозы пищеварительного тракта (обзор)/ Лесовой В.С., Липницкий А.В., Очкурова О.М.// Проблемы медицинской микологии – 2004 – Т.6, №2.
Читайте также:

