Дизентерийная амеба у ребенка
Обновлено: 26.04.2024
Этиология. С 1930 г. бациллы, выделяемые от больных дизентерией, официально были объединены в род Shigella, семейство Enterobacteriaceae. Идентификация шигелл осуществляется по их биохимическим и антигенным свойствам (О — антигенам), в соответствии с чем выделяют четыре группы шигелл (см. таблицу 1).
По своим морфологическим свойствам шигеллы представляют собой неподвижные, грамотрицательные бактерии. Общим и важнейшим свойством всех представителей рода Shigella является инвазивность, т. е. способность бактерий к инвазии в эпителиальные клетки кишечника с последующим размножением и паразитированием в них. Различные виды шигелл сильно отличаются по своим исходным биологическим свойствам, что, собственно, и определяет степень их вирулентности и патогенности для человека. Наиболее высокой вирулентностью обладают Sh. dysenteriae 1, что обусловлено прежде всего их способностью продуцировать один из мощнейших природных токсинов — Шига-токсин. Некоторые другие виды шигелл также способны продуцировать шига-подобные токсины, но с существенно более низкой активностью. Исключительно высокие вирулентные свойства Sh. dysenteriae 1 определяют крайне низкую инфицирующую дозу, которая составляет всего десятки или сотни микробных клеток. Для других видов шигелл инфицирующая доза определяется на один-два порядка выше.
Шигеллы относительно устойчивы к факторам внешней среды и способны длительно сохраняться на предметах домашнего обихода, в воде они сохраняют свою жизнеспособность до двух-трех недель, а в высушенном и замороженном состоянии — до нескольких месяцев. Высокие же температуры, наоборот, способствуют быстрой их гибели: при температуре +60°С — в течение 10 мин, а при кипячении — мгновенно. Достаточно высокую чувствительность шигеллы проявляют к дезинфицирующим средствам, ультрафиолетовым и прямым солнечным лучам.
Несмотря на разнообразие возбудителей шигеллезов, наибольшее эпидемическое значение для большинства стран мира имеют Sh. flexneri и Sh. sonnei. Хотя шигеллы распространены повсеместно (антропонозная инфекция), наиболее высокие показатели заболеваемости регистрируются в странах и регионах с низкой санитарией и высокой плотностью населения, что существенно облегчает возможность передачи возбудителя от человека к человеку. По расчетным данным, ежегодно в мире регистрируется около 140 млн случаев заболеваний шигеллезами. Восприимчивость к шигеллезной инфекции у лиц разных возрастных групп неодинакова. Наиболее восприимчивы к ним дети до двух-трех лет.
Патогенез. Основу патогенеза инфекционных заболеваний составляют особенности и характер взаимодействия микробов не только с клетками макроорганизма, но и с неспецифическими и специфическими защитными системами организма.
Шигеллы обладают достаточно выраженными вирулентными свойствами, вследствие чего заболевание может развиваться и при невысокой инфицирующей дозе (в сравнении с такими энтеропатогенными бактериями, как сальмонеллы и кишечные палочки). Благодаря относительной резистентности к действию желудочного сока и желчных кислот, шигеллы, не теряя своей вирулентности, проходят через желудочный барьер и проксимальные отделы тонкой кишки. В патогенезе заболевания выделяют тонко- и толстокишечные фазы, степень выраженности которых в конечном итоге и определяет вариант течения заболевания. У больных с типичным, колитическим вариантом острой дизентерии, тонкокишечная фаза клинически вообще не манифестируется, и заболевание изначально проявляется поражением дистального отдела толстой кишки. Тонкокишечная фаза обычно бывает непродолжительной и ограничивается двумя-тремя днями. Первичная транслокация шигелл через эпителиальный барьер осуществляется специализированными М-клетками, способными транспортировать как сами бактерии, так и их антигены в лимфатические образования кишечника (фолликулы, Пейеровы бляшки) с последующим их проникновением в эпителиальные клетки и резидентные макрофаги. Высвобождаемые в процессе транслокации шигелл токсические субстанции (экзо- и эндотоксины, энтеротоксины и т. д.) инициируют развитие синдрома интоксикации [3], который при шигеллезах всегда предшествует развитию диарейного синдрома.
Ключевым фактором вирулентности шигелл является их инвазивность, т. е. способность к внутриклеточному проникновению, размножению и паразитированию в клетках слизистой оболочки толстой кишки (преимущественно в дистальном отделе) и резидентных макрофагах собственной пластинки (см. рисунок 1). Посредством макроцитопиноза шигеллы проникают в цитоплазму эпителиальных клеток, где очень быстро лизируют фагосомальную мембрану, что приводит к повреждению клеток и их гибели. Последующее распространение шигелл происходит через базолатеральные мембраны эпителиальных клеток. Повреждение и разрушение эпителиальных клеток сопровождаются развитием воспалительной инфильтрации полиморфно-ядерными лейкоцитами собственной пластинки, формированием язв и эрозий слизистой оболочки толстой кишки, что клинически проявляется развитием диареи экссудативного типа. Способность к инвазии и внутриклеточному размножению шигелл кодируется генетическими механизмами, экспрессия которых происходит только в условиях in vivo. Несмотря на инвазивность, шигеллы не способны к глубокому распространению, в силу чего системной диссеминации возбудителя при шигеллезах, как правило, не происходит (за исключением Sh. dysenteriae 1).
Моторика кишечника является важным защитным механизмом, ограничивающим и препятствующим прикреплению и инвазии шигелл к эпителиальным клеткам, что наглядно демонстрируют затягивание и утяжеление инфекционного процесса у лиц, получающих препараты, подавляющие моторику кишечника.
Наблюдаемые у больных с шигеллезами дисбиотические изменения в составе нормальной микрофлоры толстого кишечника оказывают существенное влияние на скорость репарации слизистой в стадии реконвалесценции и восстановление функциональной активности кишечника.
После перенесенного заболевания у больных формируется непродолжительный (до одного года) типо- и видоспецифический иммунитет, в силу чего возможно реинфицирование.
Клиника. Клиническая картина шигеллезов весьма вариабельна, что нашло свое отражение в применяемой клинической классификации заболевания (см. таблицу 2). Хотя считается, что Sh. sonnei, как менее вирулентные штаммы шигелл, чаще вызывают более легкие формы заболевания, следует помнить, что этиология шигеллеза лишь предопределяет, но не определяет особенностей течения заболевания у конкретных больных (по форме, варианту и тяжести течения).
Хроническая форма дизентерии в настоящее время встречается достаточно редко и, по данным литературы, не превышает в 1-2% случаев, хотя существует мнение, что столь низкий ее удельный вес может быть обусловлен недостаточно разработанными критериями диагностики. Значительно чаще врачи в своей практической деятельности встречаются с острыми формами шигеллезов, которые и представляют наибольший интерес в плане адекватной оценки выявляемой у больного клинической картины заболевания, полноты обследования, правильности и своевременности проводимой терапии.
Инкубационный период при шигеллезах может варьировать от 8—12 ч (при гастроэнтеритическом варианте) до пяти дней (при колитическом варианте заболевания), составляя, в среднем, два–три дня.
Если примесь слизи в стуле является типичным признаком острой дизентерии, то кровь может присутствовать в микроскопических количествах и обнаруживаться только при копроцитоскопическом исследовании. Визуализируемая примесь крови в стуле определяется в виде прожилок. При более тяжелом течении заболевания дефекация может заканчиваться выделением небольшого количества слизи с прожилками крови.
Критериями тяжести течения колитического варианта острой дизентерии являются выраженность интоксикационного синдрома и характер поражения дистального отдела слизистой толстого кишечника (см. таблицу 3). Выраженного обезвоживания у больных при колитическом варианте острой дизентерии не выявляется ввиду отсутствия рвоты и скудного характера стула.
Гастроэнтероколитический вариант дизентерии также характеризуется острым началом заболевания: с озноба, лихорадки, головной боли и одновременным появлением синдрома гастроэнтерита — спастических болей в эпигастральной области, тошноты, рвоты, жидкого водянистого стула. Клинические признаки колита в первые сутки заболевания, как правило, отсутствуют и появляются лишь спустя один—три дня, что соответствует патоморфологическим этапам поражения слизистой желудочно-кишечного тракта. В зависимости от кратности рвоты и интенсивности диарейного синдрома, у больных достаточно рано выявляются признаки обезвоживания организма (сухость слизистых ротоглотки, бледность кожных покровов и цианоз, заостренные черты лица, снижение артериального давления, олигоурия и др.). С момента распространения патологического процесса на слизистую толстого кишечника проявления гастроэнтерита постепенно купируются: рвота прекращается, уменьшается объем испражнений, в стуле появляются патологические примеси (слизь и кровь). В зависимости от характера поражения слизистой дистального отдела толстой кишки, больные могут отмечать появление тенезмов и ложных позывов. При пальпации живота в первые дни заболевания отмечается урчание по ходу толстого кишечника, а в последующие дни появляется и нарастает болезненность и спазм сигмовидной кишки.
Тяжесть течения гастроэнтероколитического варианта дизентерии определяется на основании выраженности интоксикации и обезвоживания организма. В большинстве случаев оно не превышает II-III степени.
Редким вариантом течения острой дизентерии является гастроэнтеритический, характеризующийся большим сходством с пищевыми токсикоинфекциями.
Осложнения. Хотя наиболее высок риск развития осложнений у больных дизентерией, вызванной Sh. dysenteriae 1, на современном этапе прослеживается отчетливая тенденция к увеличению тяжелых форм дизентерии, обусловленных другими видами шигелл (в частности, Sh. flexneri), что, соответственно, отражается и на возможности развития осложнений. К числу наиболее грозных осложнений относятся: инфекционно-токсический шок; перфорация кишечника с развитием перитонита; энцефалический синдром (синдром фатальной энцефалопатии или синдром Ekiri), который преимущественно развивается у детей и иммунокомпрометированных пациентов при дизентерии, обусловленной Sh. sonnei или Sh. flexneri; бактериемия, выявляющаяся при дизентерии Sh. dysenteriae 1 в 8% случаев и крайне редко — при инфицировании другими видами шигелл (у детей до года, ослабленных, истощенных и иммунокомпрометированных пациентов); гемолитико-уремический синдром, развивающийся через неделю от начала заболевания и характеризующийся микроангиопатической гемолитической анемией, тромбоцитопенией и острой почечной недостаточностью. Нередко у больных могут развиваться осложнения, связанные с активизацией вторичной микрофлоры: пневмонии, отиты, инфекции мочевыводящих путей и др. К числу редких, но вероятных осложнений относятся реактивный артрит и синдром Рейтера (около 2% заболевших, экспрессирующих HLA-B27). В последние годы обсуждается возможная роль шигеллезов в формировании синдрома раздраженного кишечника.
Диагностика и дифференциальная диагностика. Специфическая диагностика шигеллезов основана на выделении и идентификации шигелл из испражнений больного и проведения серологических и/или иммунологических исследований, направленных на обнаружение антигенов шигелл или антител к ним. Без лабораторного подтверждения диагноз дизентерии может быть установлен только при типичной клинической картине.
Хотя диагностическая ценность эндоскопического исследования толстой кишки (ректороманоскопия и фиброколоноскопия) у больных с подозрением на шигеллезы ограничена, полученная при ее проведении информация позволяет: а) объективно оценить характер поражения слизистой толстой кишки; б) проводить дифференциальную диагностику и в) контролировать эффективность проводимой терапии.
В зависимости от характера поражения выделяют следующие варианты проктосигмоидита: катаральный, катарально-геморрагический, эрозивный, эрозивно-язвенный и фибринозный, которые, как правило, соответствуют тяжести течения заболевания.
При проведении дифференциальной диагностики в первую очередь необходимо исключить другие острые кишечные инфекционные заболевания, для которых типично развитие экссудативной диареи, а именно энтероинвазивные эшерихиозы, сальмонеллез, иерсиниоз (Y. enterocolitica), кампилобактериоз (Campylobacter jejuni), инфекция Clostridium difficile и амебиаз (протозойное заболевание, обусловленные Entamoeba histolytica). Кроме этого, необходимо помнить, что под маской шигеллезов могут дебютировать такие заболевания, как неспецифический язвенный колит и болезнь Крона.
Лечение. Лечение больных дизентерией может осуществляться не только в условиях специализированного инфекционного отделения, но и амбулаторно, что определяется клиническими и эпидемиологическими показаниями. В первую очередь следует госпитализировать пациентов со среднетяжелыми и тяжелыми формами заболевания, при затяжном и хроническом течении — пациентов с тяжелыми сопутствующими заболеваниями, детей до одного года и пожилых, а также лиц, представляющих эпидемическую опасность (независимо от варианта и тяжести течения заболевания) — работников пищевых предприятий и лиц, к ним приравненных.
Учитывая характер поражения слизистой кишечника, пациенты с дизентерией, особенно в острый период болезни, нуждаются в строгом соблюдении лечебного питания. Из рациона следует исключить любые продукты, оказывающие раздражающее (механическое, химическое и др.) действие. Ввиду формирующейся у больных недостаточности лактозы, из диеты исключается цельное молоко. Расширение диеты осуществляют постепенно, только по мере выздоровления больного. И все же переход на обычное питание следует осуществлять не ранее полного выздоровления, характеризующееся репарацией слизистой (см. таблицу 3).
Поскольку антибактериальная терапия всегда рекомендовалась для лечения больных дизентерией, серьезную проблему на сегодняшний день представляет формирование у шигелл резистентности к антимикробным препаратам, особенно в тех странах, где осуществляется их безрецептурная продажа и самолечение [5]. Недавно проведенные в нашей стране исследования [6] подтвердили высокую частоту резистентности у Sh. flexneri и Sh. sonnei к цефотаксиму (96,6 и 94,2%, соответственно), тетрациклину (97,7 и 92,8%), левомицетину (93,2 и 50,7%), ампициллину (95,5 и 26,1) и ампициллину/сульбактаму (95,5 и 23,2%). Резистентность не была выявлена лишь к ципрофлоксацину, норфлоксацину и налидиксовой кислоте.
Выбор антимикробного препарата и схема его применения у больных дизентерией определяются вариантом и тяжестью течения заболевания. При гастроэнтеритическом варианте антимикробная терапия не показана и больным назначают лишь патогенетическую терапию. При легком течении колитического и гастроэнтероколитического вариантов дизентерии больным целесообразно назначать фуразолидон по 0,1 г четыре раза в день или налидиксовую кислоту (невиграмон) по 0,5-1,0 г четыре раза в день в течение трех—пяти дней. Наиболее эффективными средствами для лечения больных со среднетяжелым и тяжелым течением дизентерии являются препараты фторхинолонового ряда (ципрофлоксацин, норфлоксацин и др.), цефалоспорины III поколения (цефотаксим), которые назначают в общетерапевтических дозах в течение пяти—семи дней. При тяжелом течении может проводиться комбинированная антибактериальная терапия (фторхинолоны и аминогликозиды; цефалоспорины и аминогликозиды).
Кроме антибактериальной терапии важное место в лечении больных дизентерией занимает патогенетическое лечение, включающее проведение дезинтоксикации и регидратации. В острый период заболевания больным целесообразно назначать десмол и смекту, обладающие противовоспалительным и мембраностабилизирующим действием на слизистую кишечника. После купирования интоксикационного синдрома больным показаны препараты, нормализующие процессы пищеварения и всасывания (дигестал, мезим-форте, панзинорм, фестал, холензим, ораза и др.). Коррекцию микробиоценоза кишечника следует проводить только в периоде реконвалесценции, когда купирована островоспалительная реакция. В этот же период больным показаны физиотерапевтические процедуры, ускоряющие процесс репарации слизистой толстого кишечника.
Литература
В. А. Малов, доктор медицинских наук, профессор
А. Н. Горобченко, кандидат медицинских наук
ММА им. И.М. Сеченова
Амебиаз у детей — это протозойная инвазия, вызванная патогенными штаммами Entamoeba histolytica и характеризующаяся воспалительно-язвенными поражениями кишечника, осложнениями со стороны других органов. Заболевание проявляется схваткообразными болями в животе, многократным стулом со слизисто-кровянистыми примесями, интоксикационным синдромом. Для диагностики инфекции выполняют микроскопию кала, серологические реакции, инструментальную визуализацию брюшной полости (УЗИ, колоноскопия). Лечение включает этиотропные противопротозойные препараты, симптоматические средства, пробиотики.
МКБ-10

Общие сведения
По данным ВОЗ, амебиазом заражены около 10% детей, причем большинство из них проживают в эндемичных регионах: Индии, Южной и Западной Африке, Центральной Америке. В России эндемичными областями являются Приморье, Закавказье. В последние годы эпидемиологическая ситуация ухудшается, что связано с завозом амебиаза путешественниками, мигрантами, беженцами. Инфицирование амебами возможно во всех возрастных группах, но чаще заражаются дети старше 5 лет.

Причины
Возбудителем амебиаза является дизентерийная амеба — Entamoeba histolytica, которая принадлежит к типу Sacromastigophora, отряду Amoebidae. Одноклеточный микроорганизм не имеет прочной клеточной стенки, произвольно изменяет форму клетки, активно передвигается с помощью ложноножек. Возбудитель имеет 3 формы: тканевую, которая живет в паренхиме внутренних органов, просветную, обитающую в кишечнике, и цисты, окруженные защитной оболочкой.
Заражение детей амебиазом имеет фекально-оральный механизм. Основным фактором передачи являются пищевые продукты, особенно овощи и фрукты, которые были плохо помыты и не прошли термическую обработку. Реже источником инвазии становится вода из неизвестных источников, предметы домашнего обихода (посуда, дверные ручки, белье), на которых могут оставаться цисты возбудителя. Передаче амебиаза способствуют тараканы и мухи, которые распространяют цисты на своих лапах.
Патогенез
Ребенок заражается при попадании в кишечник зрелых цист амебы, из которых после разрушения оболочки выходит 4 одноядерных микроорганизма. Они начинают размножаться, используя ресурсы тела хозяина, и трансформируются в малые просветные формы (Entamoeba histolytica forma minuta). Они не патогенны, могут длительное время существовать в ободочной кишке без клинических симптомов.
Классический амебиаз у детей развивается при превращении малой просветной амебы в эритрофаг — Entamoeba histolytica forma magna. Возбудители вырабатывают факторы патогенности цистолизины, разрушающие наружный эпителиальный слой кишечной стенки. В результате образуются язвы, отдельные участки некроза, которые со временем расширяются. Амебы обычно локализованы на границе здоровой и пораженной ткани, они также проникают в толщу стенки кишечника.
У зараженных детей при длительном существовании амебиаза формируется иммунная защита. При паразитировании возбудителя в кишечнике образуются местные антитела IgA против белка лектина, а после проникновения амебы в кровоток синтезируются защитные иммуноглобулины M, G. Клеточный иммунитет представлен макрофагами, натуральными киллерами, которые предупреждают реинфицирование у ребенка, перенесшего амебиаз.
Классификация
В детской инфектологии существует несколько подходов к систематизации болезни. По клиническим особенностям выделяют типичные формы (поражение кишечника), атипичные (латентное течение), молниеносный вариант амебиаза. По характеру течения бывает острый (до 3 месяцев), хронический рецидивирующий или непрерывно рецидивирующий варианты. Согласно классификации ВОЗ, выделяют следующие варианты:
- Бессимптомная инфекция — носительство малой вегетативной формы амебы в толстом кишечнике.
- Манифестная инфекция:
- кишечный амебиаз — амебная дизентерия, амебный колит;
- внекишечный амебиаз — печеночный, легочный, церебральный.
Симптомы амебиаза у детей
До 90% инфицированных детей являются здоровыми бессимптомными носителями амеб, поскольку в их кишечнике паразитируют непатогенные малые формы. Оставшиеся 10% зараженных сталкиваются с классическим инвазивным амебиазом. Инкубационный период для дизентерийной амебы составляет от 1-2 недель до нескольких месяцев. Манифестация заболевания провоцируется снижением иммунитета, действием экзогенных неблагоприятных факторов.
При внекишечной амебиазе, преимущественно проявляющемся поражением печени, ребенок испытывает сильную болезненность в правой подвздошной зоне. Болевой синдром усиливается во время глубокого дыхания, кашля, при резких движениях. Для амебного абсцесса характерны гектическая лихорадка, интоксикация, реже отмечается желтуха. При поражении легочной ткани появляется влажный кашель, болевые ощущения в грудной клетке, кровохарканье.
Осложнения
Язвенный дефект кишки при амебиазе в 3-5% случаев распространяется вглубь стенки, поражая все ее слои и вызывая перфорацию кишечника. Возникает риск начала калового перитонита, появления перитонеальных спаек. При заживлении дефектов у детей формируются рубцы, которые нарушают пассаж пищи по ЖКТ, провоцируют кишечную непроходимость. При длительно существующем нелеченом амебиазе развиваются амебомы — доброкачественные опухолевидные образования.
Распространение возбудителя по кровеносному руслу чревато вторичными септическими очагами в печени, легких, головном мозге, что встречается у 5-7% пациентов. Крайне редко абсцессы формируются в почках, поджелудочной железе. У детей первых лет жизни есть риск развития молниеносной формы амебиаза, сопровождающейся множественным некротическим поражением кишечника, массивной интоксикацией. Без лечения такой вариант заканчивается смертью ребенка.
Диагностика
При обследовании больного детский инфекционист пальпирует живот, определяет зоны болезненности, проверяет перитонеальные симптомы. Специалист оценивает тургор кожи, состояние слизистых оболочек, осматривает родничок у маленьких детей, что необходимо для исключения обезвоживания на фоне длительной диареи. Для верификации диагноза амебиаза проводятся следующие диагностические методы:
- УЗИ органов брюшной полости. При ультразвуковой диагностике врач оценивает размеры печени, определяет локальные изменения, указывающие на абсцесс. Обследование кишечника позволяет обнаружить неспецифические признаки воспаления, дефекты кишечной стенки.
- Колоноскопия. Эндоскопическая визуализация выполняется по строгим показаниям, чтобы диагностировать тяжелые некротические дефекты слизистой, произвести дифференциальную диагностику с другими язвенно-воспалительными дефектами толстого кишечника.
- Микроскопия кала. Выявление цист с 4 ядрами и больших вегетативных форм амебы является 100% подтверждением диагноза. Для получения достоверных результатов исследуют свежий кал, собранный не позже, чем 20-30 минут назад. При необходимости осуществляется микроскопия содержимого кишечных язв (после колоноскопии).
- Современные лабораторные методы. Обнаружение титра антител к амебе на уровне свыше 1:80 показательно при внекишечных формах амебиаза, когда сложно выявить цисты в кале. Исследование делается методом РНИФ, ИФА с парными сыворотками с интервалом от 2 до 3 недель. Также для точной диагностики Entamoeba histolytica исследуют кал методом ПЦР.
Лечение амебиаза у детей
Консервативная терапия
Лечение амебиаза в детском возрасте начинается с диеты: строгие ограничения в первые дни болезни с постепенным расширением меню до стола 4 по Певзнеру по мере нормализации стула. На время активного цистовыделения ребенка изолируют дома либо в инфекционном стационаре, чтобы прервать эпидемическую цепочку заражений. При инфицировании амебами проводятся:
- Этиотропная терапия. Для эрадикации возбудителя рекомендованы специфические противопротозойные средства из группы 5-нитроимидазолов. Системные тканевые амебициды эффективны при амебной дизентерии, внекишечной локализации поражения.
- Симптоматическое лечение. Для улучшения состояния инфицированных детей показаны жаропонижающие, анальгетики, спазмолитики. Для коррекции водно-электролитного баланса используют инфузионные кристаллоидные растворы. Сенсибилизацию организма при амебиазе устраняют антигистаминными средствами.
- Восстановительная терапия. По окончании приема этиотропных лекарств необходимо нормализовать кишечную микрофлору, избавиться от дисбактериоза. С этой целью назначают пробиотики, пребиотики, добавляют в диету обогащенные лакто- и бифидобактериями молочные продукты.
Хирургическое лечение
Помощь детских хирургов требуется при внекишечных локализациях амебиаза, выявлении у детей осложнений. Абсцессы печени и легких пунктируют под контролем УЗИ либо вскрывают открытым доступом. При обширном поражении кишечной стенки показана резекция поврежденного участка с наложением анастомоза или колостомы. При перитоните, разрыве абсцесса проводится неотложная лапаротомия для санации брюшной полости.
Прогноз и профилактика
Полное выздоровление от амебиаза происходит у детей, которым вовремя было начато этиотропное лечение. При позднем обращении или неадекватном подборе препаратов возможны осложнения, однако смертельные случаи в развитых странах встречаются редко. После излечения кишечной формы ребенок подлежит диспансерному наблюдению в течение полугода, внекишечной — на протяжении 12 месяцев, оперативного лечения — до 2-3 лет.
Профилактика амебиаза включает противоэпидемические меры: раннее выявление и изоляцию больного ребенка, тщательную дезинфекцию и соблюдение гигиенических требований лицами, которые осуществляют уход. Контактные лица подлежат обследованию на бессимптомное цистоносительство. Превентивные меры на общегосударственном уровне включают охрану окружающей среды от фекального загрязнения, борьбу с насекомыми-переносчиками.
1. Возрастные особенности кишечного амебиаза/ Г.А. Харченко, О.Г. Кимирилова// Российский вестник перинатологии и педиатрии. — 2018.
Амебиаз – паразитарное заболевание, вызываемое гистолитической амебой и протекающее с кишечными и внекишечными проявлениями. Кишечный амебиаз характеризуется обильным слизистым стулом с примесью крови, болью в животе, тенезмами, похуданием, анемией; внекишечный – формированием абсцессов печени, легких, головного мозга и пр. Диагноз амебиаза основан на данных клинической картины, ректороманоскопии, колоноскопии, микроскопии мазков содержимого абсцессов, серологического исследования, рентгенографии. В лечении амебиаза применяются медикаментозные средства (просветные и системные тканевые амебоциды, антибиотики), хирургические методы (вскрытие и дренирование абсцессов, резекция кишки).
МКБ-10
Общие сведения
Амебиаз – протозойная инфекция, проявляющаяся язвенным процессом в толстом кишечнике и поражением внутренних органов с образованием абсцессов. Амебиаз наиболее широко распространен в регионах с тропическим и субтропическим климатом; по уровню смертности среди паразитарных инфекций он занимает второе место в мире после малярии. В последние годы в связи со значительным ростом миграции и зарубежного туризма увеличилось число завозных случаев амебиаза в России. Амебиаз регистрируется в виде спорадических случаев, эпидемические вспышки редки. Амебиазом преимущественно поражаются пациенты среднего возраста.

Причины амебиаза
Возбудитель амебиаза - гистолитическая амеба (Entamoeba histolytica) относится к патогенным простейшим и имеет две стадии жизненного цикла: стадию покоя (цисту) и вегетативную (трофозоит), сменяющие друг друга в зависимости от условий существования. Вегетативные формы амебы (предцистная, просветная, большая вегетативная и тканевая) очень чувствительны к изменению температуры, влажности, рН, поэтому быстро погибают во внешней среде. Цисты проявляют значительную устойчивость вне организма человека (в почве сохраняются до 1 месяца, в воде - до 8 месяцев).
Зрелые цисты, попав в нижние отделы ЖКТ, трансформируются в непатогенную просветную форму, обитающую в просвете толстой кишки, питающуюся детритом и бактериями. Это стадия бессимптомного носительства амеб. В дальнейшем просветная форма либо инцистируется, либо превращается в большую вегетативную форму, которая за счет наличия протеолитических ферментов и специфических протеинов внедряется в эпителий кишечной стенки, переходя в тканевую форму. Большая вегетативная и тканевая формы патогенны, обнаруживаются при остром амебиазе. Тканевая форма паразитирует в слизистом и подслизистом слоях стенки толстой кишки, вызывая разрушение эпителия, нарушение микроциркуляции, образование микроабсцессов с дальнейшим некрозом тканей и множественными язвенными поражениями. Патологический процесс в кишечнике при амебиазе распространяется чаще всего на слепую и восходящую части толстой кишки, реже на сигмовидную и прямую кишку. Гистолитические амебы в результате гематогенной диссеминации способны попадать в печень, легкие, головной мозг, почки, поджелудочную железу с образованием в них абсцессов.
Основной источник заражения амебой - больные хронической формой амебиаза в период ремиссии, а также реконвалесценты и носители цист. Переносчиками цист амеб могут быть мухи. Пациенты с острой формой или с рецидивом хронического амебиаза не представляют эпидемической опасности, так как выделяют нестойкие во внешней среде вегетативные формы амеб. Заражение происходит фекально-оральным путем при попадании в ЖКТ здорового человека инфицированных зрелыми цистами пищевых продуктов и воды, а также бытовым путем через загрязненные руки. Кроме этого, возможна передача амебиаза при анальных половых сношениях, главным образом, среди гомосексуалистов.
Факторами риска заражения амебиазом служат несоблюдение личной гигиены, низкий социально-экономический статус, проживание в районах с жарким климатом. Развитие амебиаза может быть спровоцировано иммунодефицитным состоянием, дисбактериозом, несбалансированным питанием, стрессом.
Симптомы амебиаза
Инкубационный период амебиаза продолжается от 1 недели до 3-х месяцев (обычно 3-6 недель). По выраженности симптомов амебиаз может быть бессимптомным (до 90% случаев) или манифестным; по длительности заболевания - острым и хроническим (непрерывным или рецидивирующим); по тяжести течения - легким, средней тяжести, тяжелым. В зависимости от клинической картины выделяют 2 формы амебиаза: кишечную и внекишечную (амебные абсцессы печени, легких, мозга; мочеполовой и кожный амебиаз). Амебиаз может проявляться в виде микст-инфекции с другими протозойными или бактериальными кишечными инфекциями (например, дизентерией), гельминтозами.
Кишечный амебиаз является основной, наиболее распространенной формой заболевания. Ведущим симптомом кишечного амебиаза становится диарея. Стул обильный, жидкий, сначала калового характера с примесью слизи до 5-6 раз в сутки; затем испражнения приобретают вид желеобразной массы с примесью крови, а частота дефекации увеличивается до 10-20 раз в сутки. Характерны постоянные нарастающие боли в животе, в подвздошной области, больше справа. При поражении прямой кишки беспокоят мучительные тенезмы, при поражении червеобразного отростка – возникают симптомы аппендицита. Может отмечаться умеренное повышение температуры, астеновегетативный синдром. Острота процесса при кишечном амебиазе стихает через 4-6 недель, после чего наступает продолжительная ремиссия (несколько недель или месяцев).
Самопроизвольное выздоровление происходит крайне редко. Без лечения вновь развивается обострение, и кишечный амебиаз приобретает хроническое рецидивирующее или непрерывное течение (длительностью до 10 и более лет). Хронический кишечный амебиаз сопровождается расстройствами всех видов обмена: гиповитаминозом, истощением, вплоть до кахексии, отеками, гипохромной анемией, эндокринопатиями. У ослабленных больных, детей раннего возраста и беременных может развиться молниеносная форма кишечного амебиаза с обширными изъязвлениями толстой кишки, токсическим синдромом и летальным исходом.
Из внекишечных проявлений амебиаза наиболее частым является амебный абсцесс печени. Для него характерны одиночные или множественные гнойники без пиогенной оболочки, локализующиеся чаще всего в правой доле печени. Заболевание начинается остро - с озноба, гектической лихорадки, обильного потоотделения, болей в правом подреберье, усиливающихся при кашле, перемене положения тела. Состояние больных тяжелое, печень резко увеличена и болезненна, кожные покровы землистого оттенка, иногда развивается желтуха. Амебиаз легких протекает в виде плевропневмонии или абсцесса легкого с лихорадкой, болью в грудной клетке, кашлем, кровохарканьем. При амебном абсцессе головного мозга (амебном менингоэнцефалите) наблюдается очаговая и общемозговая неврологическая симптоматика, выраженная интоксикация. Кожный амебиаз возникает вторично у ослабленных больных, проявляется образованием малоболезненных эрозий и язв с неприятным запахом в перианальной области, на ягодицах, в зоне промежности, на животе, вокруг свищевых отверстий и послеоперационных ран.
Кишечный амебиаз может протекать с различными осложнениями: перфорацией кишечной язвы, кровотечением, некротическим колитом, амебным аппендицитом, гнойным перитонитом, стриктурой кишки. При внекишечной локализации не исключается прорыв абсцесса в окружающие ткани с развитием гнойного перитонита, эмпиемы плевры, перикардита или формированием свищей. При хроническом амебиазе в стенке кишки вокруг язвы формируется специфическое опухолевидное образование из грануляционной ткани – амебома, приводящая к обтурационной кишечной непроходимости.
Диагностика амебиаза
При диагностике кишечного амебиаза учитываются клинические признаки, эпидемиологические данные, результаты серологических исследований (РНГА, РИФ, ИФА), ректороманоскопии и колоноскопии. Эндоскопически при амебиазе обнаруживаются характерные язвы слизистой оболочки кишечника на разных стадиях развития, при хронических формах - рубцовые стриктуры толстой кишки. Лабораторным подтверждением кишечного амебиаза служит выявление тканевой и большой вегетативной форм амебы в испражнениях больного и отделяемом дна язв. Присутствие цист, просветных и прецистных форм возбудителя свидетельствует об амебном носительстве. Серологические реакции показывают наличие специфических антител в сыворотке крови больных амебиазом.
Внекишечные амебные абсцессы помогает визуализировать комплексное инструментальное обследование, включающее УЗИ органов брюшной полости, радиоизотопное сканирование, обзорную рентгенографию грудной клетки, КТ головного мозга, лапароскопию. Обнаружение в содержимом абсцессов патогенных форм возбудителя является доказательством его амебного происхождения. Дифференциальную диагностику амебиаза проводят с дизентерией, кампилобактериозом, балантидиазом, шистосомозом, болезнью Крона, неспецифическим язвенным колитом, псевдомембранозным колитом, новообразованиями толстой кишки; у женщин – с эндометриозом толстой кишки. Амебные абсцессы внекишечной локализации дифференцируют от абсцессов другой этиологии (эхинококкоза, лейшманиоза, туберкулеза).
Лечение амебиаза
Лечение амебиаза проводится амбулаторно, госпитализация необходима при тяжелом течении и внекишечных проявлениях. Для лечения бессимптомного носительства и профилактики рецидивов применяются просветные амебоциды прямого действия (этофамид, дилоксанида фуроат, препараты йода, мономицин). В терапии кишечного амебиаза и абсцессов различной локализации эффективны системные тканевые амебоциды (метронидазол, тинидазол, орнидазол). Для купирования колитического синдрома, ускорения репаративных процессов и элиминации патогенных форм амеб назначают йодхлороксихинолин. При непереносимости метронидазола показано использование антибиотиков (доксициклина, эритромицина). Сочетание препаратов, их дозы и длительность терапии определяется формой и тяжестью заболевания.
В отсутствие эффекта от консервативной тактики и угрозе прорыва абсцесса может потребоваться хирургическое вмешательство. При мелких амебных абсцессах возможно проведение пункции под контролем УЗИ с аспирацией содержимого или вскрытие с дренированием абсцесса и последующим введением в его полость антибактериальных и амебоцидных препаратов. При выраженных некротических изменениях вокруг амебной язвы или кишечной непроходимости выполняют резекцию кишки с наложением колостомы.
Прогноз и профилактика амебиаза
При своевременном специфическом лечении в большинстве случаев прогноз кишечного амебиаза благоприятный. В случае поздней диагностики амебных абсцессов других органов имеется риск летального исхода. Профилактика амебиаза включает раннее выявление и полноценное лечение больных и амебоносителей, соблюдение санитарно-гигиенического режима в быту, обеспечение качественного водоснабжения и очистки сточных вод, контроль безопасности пищевых продуктов, санитарное просвещение.
Дизентерия у детей – острая бактериальная кишечная инфекция, возбудителем которой являются различные виды шигелл. Дизентерия у детей проявляется интоксикационным (лихорадкой, недомоганием, слабостью, тошнотой) и колитическим синдромами (диареей с примесью крови и слизи, болями в животе, тенезмами). Дизентерию у детей подтверждают данные бактериологического исследования, ПЦР, ИФА, РНГА, копрограммы и ректороманоскопии. В лечении дизентерии у детей применяют диету, антибактериальную и дезинтоксикационную терапию, иммунокоррекцию, ферменты, пробиотики, физиотерапию.

Общие сведения
Дизентерия (шигеллез) – инфекционное заболевание, характеризующееся поражением слизистой оболочки толстого кишечника (преимущественно, его нижнего отдела), диареей и общим интоксикационным синдромом. Дизентерия занимает одно из ведущих мест среди острых кишечных инфекций, причем до 60-70% переболевших ею составляют дети. Более высокая восприимчивость к дизентерии наблюдается у детей от 2 до 7 лет, значительно реже заболевание встречается в первый год жизни ребенка. Проблемы снижения заболеваемости дизентерией среди детей, совершенствования методов диагностики, улучшения результатов лечения и реабилитации весьма актуальны для педиатрии и инфекциологии.

Причины дизентерии у детей
Дизентерию у детей вызывает большая группа антропофильных энтеробактерий рода Shigella, включающая 4 вида возбудителей (S. dysenteriae, S.flexneri, S.sonnei, S.boydii) и около 50 серотипов. Шигеллы - морфологически схожие между собой грамотрицательные, не образующие спор палочки, являющиеся факультативными анаэробами и различающиеся по биохимическим и серологическим свойствам. Возбудители дизентерии у детей достаточно устойчивы во внешней среде: долго сохраняются в воде и почве (до 3 мес.), продуктах питания (15-30 дней), хорошо переносят низкие температуры и высушивание; но чувствительны к нагреванию (погибают через 30 мин. - при 60°C, мгновенно – при 100°C), прямому солнечному свету и дезинфицирующим препаратам.
Источником заражения служит больной человек, часто с легким и стертым течением дизентерии, реже - реконвалесцент. Дети с дизентерией заразны для окружающих с первого дня болезни, так как выделяют с фекалиями большое количество шигелл.
Механизм заражения дизентерией – фекально-оральный; передача инфекции у детей осуществляется пищевым, водным (через водопровод, при купании в водоемах и бассейнах) и контактно-бытовым (через грязные руки, посуду, белье, игрушки) путями. Риск инфицирования дизентерией у детей возрастает при употреблении продуктов, не подвергнутых предварительной термической обработке, с истекшим сроком годности, немытых фруктов и овощей.
Дизентерия у детей возникает в виде спорадических случаев или эпидемических вспышек, развитию которых способствуют аварии водопровода и канализации, неблагоприятные метеоусловия (циклоны, наводнения, паводки). Типично возникновение семейных эпидемических очагов дизентерии: от больных членов семьи заражаются 40% детей. Пик заболеваемости дизентерией среди детей приходится на летне-осенний период. Формирование хронической дизентерии наблюдается у детей со сниженным иммунитетом, сопутствующими заболеваниями, при присоединении интеркуррентных инфекций (ОРВИ и др.).
Симптомы дизентерии у детей
Клинические особенности дизентерии зависят от вида возбудителя (Зонне, Флекснера и т.д.), характера течения (острый или хронический), выраженности проявлений (легкая, средней тяжести или тяжелая формы), обширности поражения ЖКТ (гастроэнтерит, колит, гастроэнтероколит), преморбидного фона и иммунитета ребенка.
Инкубационный период при дизентерии у детей продолжается от нескольких часов до недели (обычно 2-3 суток) и переходит в характерное острое начало заболевания. Уже в первые сутки инфекция проявляется выраженным недомоганием, лихорадкой (от 37,5 до 40°С), тошнотой, рвотой (однократной или повторной); в тяжелых случаях – угнетением сознания, судорогами, цианозом, тахикардией и гипотонией.
У детей первого года жизни дизентерия наблюдается, как правило, при рахите, анемии, диатезе, искусственном вскармливании. Симптомы развиваются постепенно, стул остается каловым с избытком слизи и зелени, редко с примесью крови; специфический токсикоз может быть не резко выражен, тяжесть состояния обусловлена нарушением гемодинамики и водно-минерального обмена. У грудных детей, больных дизентерией, имеется склонность к развитию вторичной бактериальной инфекции (пневмонии, отитов).
Дизентерия Зонне у детей чаще имеет субклиническое, стертое течение с гастроэнтеритическим поражением ЖКТ, без деструктивных изменений слизистой. Для дизентерии Флекснера у детей характерно более интенсивное поражение кишечника и более тяжелое течение.
При неосложненном течении дизентерии у детей клиническое выздоровление наступает обычно через 2–3 недели, но полное морфо-функциональное восстановление ЖКТ длится до 2 -3 месяцев и более; имеется риск обострения при нарушении диеты.
Тяжелые случаи дизентерии у детей могут осложниться формированием токсического мегаколона, перфорацией толстой кишки, перитонитом; в редких случаях - развитием гемолитико-уремического синдрома, почечной и сердечной недостаточности, токсико-инфекционного шока, летального исхода.
Хроническая дизентерия у детей нередко протекает при удовлетворительном общем состоянии, слабой интоксикации, наличии жидкого или полужидкого стула калового характера, иногда со слизью и прожилками крови. Длительное течение дизентерии ослабляет детей, приводит к гипотрофии, авитаминозу, анемии.
Диагностика дизентерии у детей
Дети с подозрением на дизентерию должны быть изолированы, осмотрены педиатром и инфекционистом. Диагноз дизентерии у детей ставят на основании эпидемиологического анамнеза, клинической картины, лабораторных данных.
Возбудителя кишечной инфекции идентифицируют путем бактериологического исследования кала и рвотных масс с обязательным определением чувствительности выделенной микрофлоры к антибиотикам. В сомнительных случаях для выявления шигелл и специфических антигенов в фекалиях и крови используют ПЦР и серологические методы (РНГА, РКА, ИФА). Результаты копрограммы и ректороманоскопии при диагностике дизентерии у детей имеют вспомогательное значение.
Лечение дизентерии у детей
Лечение дизентерии у детей определяется формой и тяжестью заболевания, возрастом и общим состоянием пациента и в зависимости от этого может проводиться в стационаре или амбулаторно. Комплексное лечение детей с дизентерией включает режим, лечебное питание, антимикробную и дезинтоксикационную терапию, иммунокоррекцию, восстановление функции пищеварительной системы.
В острый период дизентерии дети должны соблюдать постельный режим. Диета назначается согласно возрасту ребенка: в первые 1-3 суток питание дробное с уменьшением суточного объема пищи и увеличением кратности приема. У детей до года, находящихся на искусственном вскармливании вводят кисломолочные продукты (кефир, биолакт). Детям старше года показана механически и химически щадящая пища (рисовая и манная каши, овощной отвар, овощное пюре, мясной фарш, кисели, слизистые супы, творог).
При токсикозе и обезвоживании легкой степени ребенку дают пить солевые растворы; в тяжелых случаях показана инфузионная терапия. Болевой синдром купируют спазмолитическими средствами (дротаверин, папаверин).
При тяжелых и среднетяжелых формах дизентерии у детей применяют антибиотики (ампициллин, гентамицин, полимиксин М, налидиксовая к-та), нитрофураны (фуразолидон) с учетом чувствительности циркулирующих в данной местности штаммов. Целесообразно назначение поливалентного дизентерийного бактериофага.
Антидиарейные средства при дизентерии у детей грудного и раннего возраста не используют. Для восстановления функции и биоценоза кишечника при дизентерии у детей показаны ферменты (пенкреатин), пробиотики и пребиотики. В реабилитационном периоде детям, перенесшим дизентерию, рекомендованы препараты, повышающие иммунитет, витамины А, С, В, фитосборы, физио- и санаторно-курортное лечение.
Затяжные и хронические формы дизентерии у детей лечатся как острый процесс. Дизентерия у детей считается излеченной после нормализации клинической картины и отрицательного результата контрольного бактериологического исследования, но еще в течение 1 месяца необходимо наблюдение со стороны детского врача-инфекциониста.
Прогноз и профилактика дизентерии у детей
В случае проведения полноценной терапии дизентерия у детей полностью излечивается. При тяжелом течении дизентерии у детей и высоком уровне токсемии высока вероятность осложнений.
Предупредить дизентерию у детей можно при обязательном соблюдении правил личной гигиены; строгом контроле источников водоснабжения, норм хранения, приготовления и реализации пищевых продуктов; выявлении больных в дошкольных и школьных учреждениях, среди работников молочных кухонь, предприятий общественного питания; проведении карантинных и санитарных мероприятий.
Что такое дизентерия? Причины возникновения, диагностику и методы лечения разберем в статье доктора Александрова Павла Андреевича, инфекциониста со стажем в 14 лет.
Над статьей доктора Александрова Павла Андреевича работали литературный редактор Маргарита Тихонова , научный редактор Сергей Федосов

Определение болезни. Причины заболевания
Шигеллёзы, или дизентерия — это группа острых/хронических заболеваний, вызываемых бактериями рода Шигелла, которые поражают желудочно-кишечный тракт (преимущественно дистальный отдел толстой кишки). Манифестные формы (клиническая картина) дизентерии: синдром общей инфекционной интоксикации, синдром поражения желудочно-кишечного тракта (дистальный колит), синдром обезвоживания. При отсутствии адекватного лечения приводит к серьёзным осложнениям и хронизации.
Возбудитель дизентерии
семейство — кишечные бактерии (Enterobacteriaceae)
род — Шигелла (Shigella)
виды — 4 основных:
- Dysenteriae (серовары — шигелла Григорьева-Шига, Штутцера-Шмитца, Ларджа-Сакса);
- Flexneri (Флекснера);
- Boydii (Боудии);
- Sonnei (Зонне).
Являются факультативно-анаэробными (способны существовать как при наличии, так и при отсутствии кислорода), граммотрицательными, неподвижными палочками. Хорошо растут на обычных питательных средах.
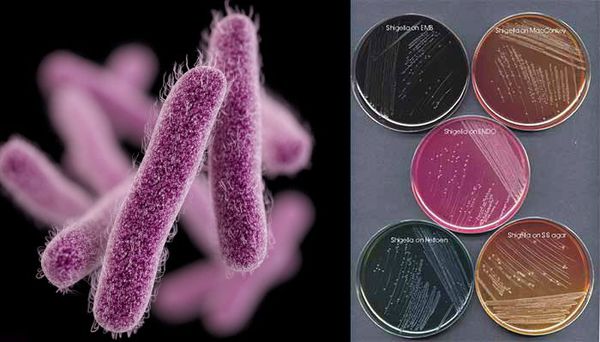
Имеют О-антиген (серологическая специфичность) и К-антиген (оболочечная структура). Клеточная стенка частично состоит из эндотоксина (липополисахарида), высвобождающегося при гибели микроорганизма. Бактерии вида Shigella Dysenteriae серовара Григорьева-Шига продуцируют высокоактивный цитотоксин, который нарушает синтез белка рибосомами клеток кишечного эпителия. Цитотоксин в совокупности с энтеротоксином (усиливающим секрецию жидкости и солей в просвет кишки) и нейротоксином (оказывающим нейротоксическое действие на сплетения Ауэрбаха) образует экзотоксином — токсин, выделяемый в процессе жизнедеятельности шигелл (Цитотоксин + энтеротоксин + нейротоксин = экзотоксин). Также у данной группы микроорганизмов происходит выделение гемолизинов — веществ, разрушающих эндотелий капилляров и вызывающий ишемию в тканях кишечника).
Факторы патогенности шигелл (механизм приспособления бактерий):
- адгезия (прикрепление к слизистой оболочке кишечника);
- инвазия (проникновение в эпителиальные клетки слизистой оболочки толстого кишечника);
- токсинообразование;
- внутриклеточное размножение.
Тинкториальные свойства (особенности микроорганизмов при окрашивании): быстро изменяют чувствительность к антибактериальным препаратам. Характерна высокая выживаемость во внешней среде (в воде, почве и пище при комнатной температуре сохраняются до 14 дней, в канализационных стоках — до 30 дней, при благоприятных условиях могут быть жизнеспособны до 4 месяцев). Способны к размножению в пищевых продуктах. При воздействии УФО (ультрафиолетового облучения) погибают за 10 минут, в 1% феноле — за 30 минут, при кипячении — мгновенно.
Интересная особенность: чем выше ферментативная активность возбудителя дизентерии, тем ниже вирулентность (минимальная доза возбудителя, способная заразить человека) и наоборот. [3] [6]
Эпидемиология
Антропоноз (повсеместное распространение).
Источник инфекции — человек (больной, носитель и лица с субклинической формой заболевания).
Минимальная инфицирующая доза для бактерии Григорьева-Шига — 10 микробных тел в 1 грамме вещества, для Флекснера — 10 2 бактерий, для Зонне — от 10 7 .
Длительное время в РФ превалировали случаи заражения, вызванные шигеллой Флекснера 2а, однако в настоящее время ввиду широкого развития туризма длительного преобладания какой-либо формы нет.
Механизм передачи — фекально-оральный (пищевой, водный, контактно-бытовой), из них преимущественно:
- Григорьева-Шига (контактно-бытовой путь);
- Зонне (с молоком и молочными продуктами);
- Флекснера (водный путь);
- Дизентериа (пищевой путь).
Наибольшую опасность представляют работники питания и водоснабжения. Больные заразны с начала болезни (конца инкубационного периода) и до трёх недель болезни.
Иммунитет непродолжителен и моноспецифичен (вырабатывается только к одному серотипу, который вызвал заболевание). [1] [4] [5]
При обнаружении схожих симптомов проконсультируйтесь у врача. Не занимайтесь самолечением - это опасно для вашего здоровья!
Симптомы дизентерии
Инкубационный период — от 1 до 7 дней.
Начало заболевания острое (развитие основных синдромов наблюдается в первые сутки заболевания), характерна лихорадка постоянного типа.
Читайте также:

