Эхинококкоз у детей клинические рекомендации
Обновлено: 18.04.2024
Башкирский государственный медицинский университет, Уфа;
Вектор Бест, Новосибирск
Тактика лечения детей с сочетанным эхинококкозом
Журнал: Хирургия. Журнал им. Н.И. Пирогова. 2017;(1): 48‑53
Башкирский государственный медицинский университет, Уфа;
Вектор Бест, Новосибирск
Материал и методы. Проанализированы результаты диагностики и лечения 51 ребенка с сочетанным эхинококкозом. У 40 (78,4%) пациентов выявлено сочетанное поражение печени и других органов, у 29 — сочетанный эхинококкоз печени и легких. Эхинококкоз обоих легких был у 14 детей, из них у 6 в сочетании с поражением печени. Сочетанный эхинококкоз трех органов отмечен у 5 пациентов. Результаты и обсуждение. При сочетанном эхинококкозе у детей наблюдается неравномерный рост паразитарных кист в различных тканях, из 40 наблюдений сочетанного поражения печени и других органов в 15 (37,5%) кисты печени имели малый размер. После этапных операций на органах со средними и большими эхинококковыми кистами у 7 пациентов по поводу кист малого размера проведена медикаментозная терапия. При сроках между этапами операций 1—3 мес отмечается быстрый рост оставшихся кист, что нередко приводит к осложнениям со стороны оставшейся кисты, особенно при эхинококкозе обоих легких. Из 51 пациента с сочетанным эхинококкозом послеоперационные осложнения отмечены у 6 (11,8%). Рецидив диагностирован у 2 (3,9%) детей. Летальных исходов не было. Вывод. Консервативная терапия по поводу мелких кист при сочетанном эхинококкозе позволяет сократить количество операций в 2 раза и одновременно является профилактикой рецидива заболевания. Сокращение срока между этапами операции до 11±2 сут при сочетанном эхинококкозе обоих легких предупреждает развитие осложнений.
Башкирский государственный медицинский университет, Уфа;
Вектор Бест, Новосибирск
Множественный и сочетанный эхинококкоз двух и более органов у детей встречается в 9,8—16,9% наблюдений и свидетельствует о массивном заносе онкосфер в организм ребенка с пониженной резистентностью [1—6]. Послеоперационные осложнения и рецидив чаще всего встречаются именно при такой форме эхинококкоза, а летальность при этом достигает 1,8—10,2% [2, 7]. Большинство хирургов придерживаются мнения, что при сочетанном эхинококкозе нескольких органов оптимальный срок между операциями составляет 1—4 мес [2, 8, 9], при двустороннем эхинококкозе легких — 1 мес [4], хотя одномоментные операции экономически более эффективны [10].
Таким образом, многие вопросы тактики лечения этой категории больных остаются дискутабельными, например, в какой последовательности и с каким интервалом между операциями производить хирургическое вмешательство [5, 11, 12].
Материал и методы
Нами проанализированы результаты диагностики и лечения 51 ребенка с сочетанным эхинококкозом, находившегося на лечении в Республиканской детской клинической больнице с 2000 по 2012 г. Возраст пациентов от 1 года до 15 лет.
По материалам нашей клиники, сочетанный эхинококкоз часто встречался у детей дошкольного возраста — у 24 (47,0%) и школьного — у 27 (53,0%). Возраст самой маленькой пациентки 1 год 10 мес.
У 40 (78,4%) детей выявлено сочетанное поражение печени и других органов, из них у 18 были множественные эхинококковые кисты печени. Чаще всего наблюдали сочетанный эхинококкоз печени и легких — у 29 больных. Сочетанный эхинококкоз трех органов отмечен у 5 пациентов. Эхинококкоз обоих легких мы наблюдали у 14 детей, из них у 6 в сочетании с поражением печени. Характер поражения представлен в табл. 1.

Таблица 1. Характер поражения при сочетанном эхинококкозе Примечание. * — осложненная эхинококковая киста печени.
Всем пациентам проводили комплексное клинико-лабораторное обследование: рентгенографию органов грудной клетки, УЗИ органов брюшной полости и забрюшинного пространства, эхокардиографию. Анализ эхосемиотики эхинококковых кист печени проводили согласно ультразвуковой классификации H. Gharbi и соавт. (1981 г.) и ВОЗ-IWGE 2003 г. [13]. Дети с сочетанным эхинококкозомразделены на3 группы в зависимости от тактики лечения: 1-я группа (n=7) — консервативное лечение противопаразитарным препаратом албендазол (немозол), что было одним из этапов лечения; 2-я группа (n=15) — многоэтапные операции, один из этапов — эндовидеоскопическая операция; 3-я группа (n=29) — традиционная операция на всех этапах.
Результаты и обсуждение
Анализ клинического материала показал неравномерный рост паразитарных кист в различных тканях при сочетанном эхинококкозе у детей. Из 40 наблюдений сочетанного поражения печени и других органов в 15 (37,5%) кисты печени имели малый размер. Из 29 детей с сочетанным эхинококкозом печени и легкого при наличии в печени мелких кист у 12 эхинококковые кисты в легких имели большой и гигантский размер, что связано с более быстрым ростом паразитарной кисты в легочной ткани. Соответственно и легочные осложнения встречались в 2 раза чаще. При сочетании эхинококкоза печени с поражением других органов малый размер кисты печени установили в 3 из 11 наблюдений. Клиническая симптоматика характеризовалась значительным разнообразием. На первый план выступали признаки поражения органа, в котором локализовалась киста наибольшего размера.
Дети с сочетанным эхинококкозом отставали в физическом развитии, дефицит массы тела составлял 21,2±2,3%, отмечалась анемия — Hb 107 г/л, эр. (3,20±0,31)·10 12 /л, а также лейкоцитоз (10,30±1,83)·10 9 /л, эозинофилия до 15±3%, увеличение СОЭ до 37,2±1,7 мм/ч. Однако проявления со стороны легких при сочетанном их поражении с другими органами были более выраженными.
Приводим клинические наблюдения.
Общий анализ крови: Hb 109 г/л, эр. 4,04·10 12 /л, л. 7,64·10 9 /л, э. 3%, лимф. 51%, мон. 5%, с. 41%; СОЭ 4 мм/ч. Биохимический анализ крови: общий белок 71,52 г/л, общий билирубин 10,5 ммоль/л, мочевина 2,5 ммоль/л, АЛТ 15 Е/л.
На рентгенограмме органов грудной клетки 09.09.08 на фоне неравномерности пневматизации легочной ткани в правом легком определяются две однородные, средней интенсивности тени округлой формы, диаметром 100 и 80 мм с четкими ровными контурами. В левом легком аналогичная тень диаметром 40 мм. Срединная тень оттеснена влево. Контуры купола диафрагмы слева четкие, справа завуалированы (рис. 1).

Рис. 1. Обзорная рентгенограмма органов грудной клетки больной X., 1 года 10 мес. В правом легочном поле определяются две эхинококковые кисты, в левом — одна.
УЗИ органов грудной клетки: в правом легком определяется два кистозных образования с двойным контуром, 105 и 85 мм в диаметре, в левом легком — третье, 40 мм в поперечнике. В правом реберно-диафрагмальном синусе отмечается незначительное количество жидкости. УЗИ органов брюшной полости: печень выступает из-под края реберной дуги на 1,5 см. В левой доле (III сегмент) определяется киста овальной формы с четкими ровными контурами, размером 14×10 мм, на остальном протяжении структура печени однородная, средней эхогенности. При эхокардиографии патологических изменений не выявлено.
Проведена предоперационная подготовка: десенсибилизирующая, антибактериальная и дезинтоксикационная терапия. 11.09 произведена торакотомия справа, эхинококкэктомия. Послеоперационный период протекал без осложнений. Пациентка выписана под наблюдение участкового педиатра и хирурга. Для проведения планового оперативного лечения по поводу эхинококковой кисты левого легкого поступила в клинику 27.10.08. За этот период отмечен рост кисты левого легкого до 50 мм. Произведена торакотомия слева и эхинококкэктомия 31.10. По поводу эхинококковой кисты печени (размер прежний — 14 мм) проведено 8 курсов противопаразитарной химиотерапии. Контрольный осмотр через 2 года. Пациентка здорова.
Приведенное клиническое наблюдение свидетельствует о тяжелом течении сочетанного эхинококкоза обоих легких и печени у ребенка в возрасте 1 года и 10 мес, обусловленном тем, что паразитарные кисты в правом легком достигли гигантских размеров. После первого этапа операции отмечен рост оставшейся эхинококковой кисты в левом легком (10 мм за 47 сут).
Общий анализ крови: Hb 117 г/л, эр. 4,4·10 12 /л, л. 13,5·10 9 /л, э. 12%; СОЭ 31 мм/ч. Биохимический анализ крови: общий белок 68 г/л, общий билирубин 10,9 ммоль/л, АЛТ 15 Е/л, мочевина 4,7 ммоль/л, креатинин 0,09 ммоль/л, глюкоза 4,9 ммоль/л.
На рентгенограмме органов грудной клетки в обоих легких определяются округлые множественные тени диаметром от 43 до 95 мм, в правом легком их 4, в левом 3. Эхинококковая киста, локализованная в верхней доле правого легкого, осложнена прорывом в бронх (рис. 2).

Рис. 2. Обзорная рентгенограмма органов грудной клетки больного А., 12 лет. В правом легком определяются 4, в левом легком — 3 эхинококковые кисты.
По данным УЗИ и КТ органов брюшной полости структура печени неоднородная за счет множества (до 20) кист, расположенных интрапаренхиматозно во всех отделах печени. Диаметр кист от 6 до 30 мм, плотность содержимого составляет 9—16 ед.Н. Некоторые кисты имеют четкий двойной контур, в стадии CL, CE1 (рис. 3).

Рис. 3. Компьютерные томограммы печени больного А., 12 лет. В паренхиме печени определяются множественные эхинококковые кисты.
В паренхиме печени определяются множественные эхинококковые кисты малого размера.
Установлен диагноз: множественный сочетанный эхинококкоз обоих легких и печени.
После предоперационной подготовки 19.12 выполнены хирургические вмешательства: переднебоковая торакотомия справа, эхинококкэктомия; затем 28.12 переднебоковая торакотомия слева, эхинококкэктомия. Послеоперационный период протекал без осложнений.
С учетом размера множественных эхинококковых кист печени и того факта, что они были расположены в глубине паренхимы, 30.12 начата противопаразитарная терапия: албендазол по 400 мг в сутки. Сопроводительная терапия: гепатопротекторы, энзимотерапия, пробиотики. Пациент выписан из стационара 12.01.13 на амбулаторное долечивание.
Диспансерное наблюдение проводилось с выполнением общего и биохимического анализов крови и ультразвукового мониторинга. После двух курсов противопаразитарной терапии по данным УЗИ печени отмечена положительная динамика, характеризующаяся изменением структуры, формы и уменьшением размера эхинококковых кист. Противопаразитарную химиотерапию проводили в течение 2 лет.
Контрольный осмотр 18.12.14 (через 2 года после операции и начала противопаразитарной химиотерапии). Жалоб нет. Масса тела 33 кг. Обе половины грудной клетки равномерно участвуют в акте дыхания, аускультативно дыхание проводится во все отделы. Живот мягкий, безболезненный. Печень у края реберной дуги. Показатели общего и биохимического анализов крови в пределах возрастной нормы. На рентгенограмме грудной клетки 18.12.14 очаговых теней нет (рис. 4).

Рис. 4. Рентгенограмма органов грудной клетки больного А., 15 лет, через 2 года после операции.
УЗИ органов брюшной полости и забрюшинного пространства 18.12: печень — размеры в норме, структура средней эхогенности, несколько неоднородна за счет очагов гипоэхогенности размером 10 мм и нескольких кальцинатов, дающих акустическую тень.

Рис. 5. Компьютерные томограммы печени больного А., 15 лет, после консервативной противопаразитарной химиотерапии.
Итак, два приведенных наблюдения сочетанного множественного эхинококкоза обоих легких и печени демонстрируют тяжесть течения заболевания. По поводу больших паразитарных кист в легких проводили поэтапные хирургические вмешательства. По поводу мелких интрапаренхиматозных эхинококковых кист печени провели консервативную противогельминтную терапию.
Вопрос о выборе последовательности операции при сочетанном эхикококкозе в каждом наблюдении решался индивидуально. При сочетанном эхинококкозе печени с другими органами брюшной полости и забрюшинного пространства (7), а также при множественном эхинококкозе печени проводили одномоментную эхинококкэктомию из поперечного разреза передней брюшной стенки. У 18 детей первая операция выполнена на легком, у 7 — на печени. В 4 наблюдениях при сочетании эхинококковой кисты нижней доли правого легкого и диафрагмальной поверхности печени проведена одномоментная санация; торакотомия, эхинококкэктомия легкого, затем диафрагмотомия и эхинококкэктомия из печени. Однако чаще всего при сочетанном эхинококкозе обоих легких, сочетанном эхинококкозе легких и печени оптимальной тактикой у детей являются этапные операции. Ретроспективный анализ материалов клиники показал быстрый рост оставшихся кист при общепринятых сроках между операциями 1—3 мес. В результате у 21 из 37 обследованных отмечены осложнения со стороны оставшейся кисты, особенно при эхинококкозе обоих легких. В связи с этим при сочетанном эхинококкозе нами сокращены сроки между этапами операции до 11±2 сут.
Консервативное лечение являлось вторым этапом терапии у 7 пациентов с сочетанным эхинококкозом; в том числе у 6 с сочетанным эхинококкозом легкого и печени и у 1 с множественными мелкими паразитарными кистами печени после лапароскопической эхинококкэктомии правой почки. В 2 наблюдениях первым этапом выполнена лапаротомия, эхинококкэктомия печени, затем по поводу единичной кисты в легком размером 15 мм проводили консервативное лечение. Такая тактика способствовала сокращению количества хирургических вмешательств и одновременно являлась профилактикой рецидива. Как видно из табл. 2, консервативная терапия, явившаяся одним из этапов лечения у 7 пациентов 1-й группы, позволила сократить количество операций в 2 раза по сравнению с больными 2-й и 3-й групп, которым хирургические вмешательства проводили в несколько этапов.

Таблица 2. Вид операционного доступа и число хирургических вмешательств при сочетанном эхинококкозе в сравниваемых группах
Показателем эффективности консервативной терапии являлось обнаружение дегенеративных изменений в эхинококковой кисте — ее формы, структуры и уменьшения размера при ультразвуковом мониторинге. Уровень статистической значимости различий с исходными данными через 3—6 мес составил p≤0,05, через 8—10 мес — уже р
Из 51 пациента с сочетанным эхинококкозом послеоперационные осложнения отмечены у 6 (11,8%). Рецидив диагностирован у 2 (3,9%) детей. Летальных исходов не было.
При изучении клинической картины заболевания у 51 ребенка с сочетанным эхинококкозом выявлен неравномерный рост паразитарных кист, локализующихся в различных тканях и находящихся на разных стадиях жизнедеятельности паразита. Из 40 наблюдений сочетанного поражения печени и других органов в 15 (37,5%) кисты печени имели малый размер. Это обстоятельство необходимо учитывать при планировании тактики лечения.
Таким образом, клиническая картина сочетанного эхинококкоза характеризуется неравномерным ростом эхинококковых кист в разных органах, у 37,5% детей кисты печени имеют малый размер, в связи с чем целесообразно проведение медикаментозной противопаразитарной терапии после этапных операций на органах со средними и большими кистами. Такая тактика позволяет сократить количество хирургических вмешательств в 2 раза и одновременно является профилактикой рецидива заболевания. Показателем эффективности консервативной терапии является обнаружение дегенеративных изменений в эхинококковой кисте при динамическом УЗИ — ее формы, структуры и уменьшения размера. Сокращение срока между этапами операции до 11±2 сут при сочетанном эхинококкозе обоих легких позволяет предупредить развитие осложнений.
Эхинококкоз печени - это одно из наиболее распространенных паразитарных заболеваний, в основе которого лежит образование кист в печени. Основными признаками данной патологии являются общая слабость, существенное снижение аппетита, уменьшение массы тела, чувство тяжести в области печени, тошнота после употребления жареной или жирной пищи, расстройство стула. Для диагностики эхинококкоза печени применяются общий анализ крови, иммунологические методы, УЗИ органов брюшной полости, магнитно-резонансная томография, ОФЭКТ печени, лапароскопия и др. Наиболее эффективное лечение – оперативное иссечение кист; также применяются противогельминтные препараты.
МКБ-10
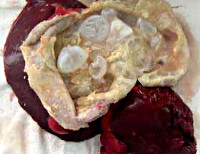
Общие сведения
Эхинококкоз печени – паразитарная патология, которая вызвана ленточным червем Echinococcus. Его личинки внедряются и размножаются в ткани органа, формируя кисты. Данное заболевание считается одним из наиболее распространенных гельминтозов. Встречаемость эхинококкоза в разных странах мира существенно различается. Болезнь в основном наблюдается в регионах, где активно занимаются сельскохозяйственной деятельностью.
Эхинококк паразитирует в человеческом организме исключительно в виде личинки, поражая не только печень, но и другие органы, такие как мозг и легкие. При этом вовлечение в процесс печени происходит в 65% всех случаев данного заболевания. Изучением патологии занимаются гастроэнтерология, инфектология. Лечение эхинококкоза входит в сферу деятельности таких специалистов, как инфекционист, гастроэнтеролог, гепатолог и хирург.

Причины
До внедрения в организм человека жизненный цикл эхинококка включает несколько стадий, которые следуют одна за другой. Заключительным хозяином среди домашних питомцев являются собаки и гораздо реже - кошки. Паразит обитает в кишечнике этих животных в виде зрелых червей. Их яйца с фекалиями переходят в водоемы, почву, на фрукты, овощи и так далее. В дальнейшем существует несколько вариантов попадания яиц в организм человека:
- Часть яиц проглатывается грызунами небольших размеров. В печени этих животных личинки эхинококка начинают созревать. После поедания грызунов дикими хищниками последние также заражаются паразитами. Поэтому при плохой термической обработке дичи охотники могут заболеть эхинококкозом печени.
- Другая часть яиц эхинококка оказывается в пищеварительной системе животных сельскохозяйственного предназначения, таких как свиньи, крупный рогатый скот и др. Яйца проникают в организм млекопитающего вместе с кормом, травой или водой, поражая его органы. Поэтому употребление в пищу мяса без соответствующей обработки может стать причиной развития эхинококкоза печени.
- Наиболее распространенным и актуальным для человека является третий путь попадания паразита в организм. Он отмечается при недостаточном соблюдении гигиенических правил, что особенно актуально для детей. Эхинококк может попасть в желудочно-кишечный тракт при употреблении немытых фруктов или игре с домашними животными, после которой не были тщательно вымыты руки.
В человеческом организме личинки изначально всасываются в кровь из кишечника и переходят в печень. В дальнейшем они способствуют возникновению эхинококкоза печени. Однако, многие паразиты не проходят из крови через печеночный барьер, распространяясь с кровотоком в другие органы.
Симптомы эхинококкоза печени
Эхинококкоз печени является хроническим заболеванием, которое не имеет резко выраженной симптоматики, заставляющей человека вовремя обратиться к врачу. После заражения симптомы начинают появляться не сразу, а через несколько месяцев или лет.
Чаще всего пациентов беспокоит общая слабость, уменьшение толерантности к физической нагрузке, снижение работоспособности, боли в голове, мелкая точечная сыпь на коже, периодическое незначительное повышение температуры. Данные клинические признаки являются следствием попадания в кровь токсических продуктов жизнедеятельности эхинококка и реакции организма на внедрение паразитов. Развитие эхинококка в печени происходит в несколько стадий, каждая из которых имеет свои клинические особенности.
Первая стадия
На первом этапе симптомов может вообще не наблюдаться. Поэтому зараженный человек чувствует себя нормально и ведет активный образ жизни. На данной стадии эхинококк внедряется в печеночную ткань и формирует защитную капсулу. Единственным проявлением заболевания может служить небольшой дискомфорт в правом подреберье после приема большого количества пищи.
Вторая стадия
Второй этап характеризуется четкой клинической симптоматикой. У больных нарушается аппетит и постепенно уменьшается масса тела. При приеме лекарственных средств у зараженных людей может наблюдаться более частое развитие побочных реакций, что связано со снижением детоксикационной функции печени на фоне эхинококкоза.
Специфичными симптомами, которые характерны для эхинококкоза печени, являются тошнота или рвота, тяжесть в области правого подреберья и диарея. Тошнота, как правило, развивается после употребления жирной, жаренной и острой пищи. Дискомфорт в правой половине живота беспокоит после еды или на фоне физической нагрузки. Больные эхинококкозом печени периодически отмечают диарею, которая связана с нарушением переваривания жирных кислот в кишечнике вследствие угнетения выработки желчи гепатоцитами.
Третья стадия
На третьем этапе развития эхинококкоз печени проявляется осложнениями, которые связаны с нарушением целостности эхинококковой кисты и распространением яиц паразита в другие органы. Как правило, при попадании паразита в кровь возникает аллергическая реакция, которая сопровождается спазмом бронхов и развитием дыхательной недостаточности. Кроме того, эхинококк может распространяться в костную ткань, мозг, легкие и другие органы, вызывая нарушение их функций.
Одним из самых частых осложнений считается нагноение содержимого кисты, которое при разрыве может выходить в брюшную или плевральную полость, вызывая гнойный перитонит или плеврит. При большом размере кистозной полости она может ущемлять близко расположенные сосуды и желчные протоки. Из кровеносных сосудов чаще всего сдавливается воротная вена, что проявляется повышением давления в венозной системе органов брюшной полости. В результате увеличивается селезенка и появляется асцит.
Реже эхинококковая киста сдавливает нижнюю полую вену, что приводит к развитию сердечной недостаточности. Это осложнение выражается одышкой, отеками нижних конечностей, почечной дисфункцией и нарушением кровоснабжения внутренних органов. Частым осложнением эхинококкоза печени является сдавление желчных путей, что сопровождается нарушением оттока желчи. Симптомы застоя желчи - пожелтение кожных покровов, зуд и расстройства стула с изменением его цвета.
Диагностика
Для диагностики эхинококкоза печени используются лабораторные и инструментальные методы обследования. Также осуществляется тщательный расспрос пациента, который позволяет уточнить возможные пути заражения данным паразитом. Как правило, высокий риск заболевания отмечается у людей, которые занимаются сельским хозяйством и часто контактируют с домашними животными.
- Лабораторная диагностика. Проводится общий анализ крови, клинический анализ мочи, иммунологические тесты (реакция связывания комплемента, реакция непрямой агглютинации) и аллергическая проба Каццони. В общем анализе крови отмечается повышение количества эозинофилов и увеличение скорости оседания эритроцитов. Иммунологические тесты используются для определения наличия антител к эхинококку в крови и содержимом кисты. Именно они позволяют точно диагностировать эхинококкоз печени. Поскольку при данном заболевании может нарушаться функция гепатоцитов, для ее оценки проводятся биохимические пробы печени.
- Инструментальная диагностика. Из инструментальных методов важную роль играет УЗИ печени и желчного пузыря, обзорная рентгенография органов брюшной полости, магнитно-резонансная томография и однофотонная эмиссионная компьютерная томография печени (ОФЭКТ печени). Данные визуализационные методики обследования позволят выявить кисту и определить ее размеры. Также они дают возможность оценить размеры печени, визуализировать расширенные желчные протоки, увеличенную селезенку или асцит.
- Инвазивная диагностика. Для того чтобы получить содержимое кисты и обнаружить паразитов, рекомендуется пункционная биопсия печени – но только с соблюдением методики, исключающей обсеменение окружающих тканей личинками эхинококка. Из инвазивных методик может быть использована лапароскопия, при помощи которой можно непосредственно осмотреть органы брюшной полости видеоэндоскопом.
Лечение эхинококкоза печени
Эхинококкоз печени является паразитарным заболеванием, которое никогда не проходит самостоятельно. При этом консервативные методы не позволяют добиться полного выздоровления. Поэтому единственным эффективным способом лечения является хирургическое вмешательство. На подготовительном этапе, перед операцией и в послеоперационном периоде показано назначение противогельминтного препарата мебендазола. Этот препарат тормозит рост кисты, уменьшает ее размеры, значительно снижает риск рецидивов патологии.
Наиболее эффективным методом лечения является оперативное удаление паразита. Операция сопряжена с высоким риском диссеминации личинок на окружающие ткани, поэтому должна проводиться специалистом, владеющим методикой малоинвазивных апаразитарных вмешательств, использующим современные инструменты. Из хирургических методик применяются иссечение кист печени и эндоскопическое дренирование кисты печени. После удаления кисты в образовавшуюся полость вводят гермициды (наиболее эффективны для предотвращения рецидива эхинококкоза печени 80-100% глицерин и 30% раствор хлорида натрия).
Прогноз и профилактика
Профилактика эхинококкоза печени направлена на предотвращение заражения данным паразитом. Необходимо тщательное мытье рук после контакта с животными и перед любым употреблением пищи. Также следует проводить полноценную термическую обработку мяса, что позволяет уничтожить находящиеся в нем личинки эхинококка.
Эхинококкоз печени при своевременном и грамотном оперативном вмешательстве излечим, однако при выявлении на поздних стадиях заболевания даже на фоне проведенного лечения значительно снижает качество жизни, а в некоторых случаях патология может приводить и к смерти пациента. Рецидивы возникают примерно у 7% больных.
Эхинококкоз – это паразитарная инвазия личиночной стадией ленточного гельминта эхинококка, протекающая с поражением внутренних органов (печени, легких, сердца, головного мозга и др.) и образованием в них эхинококковых кист. Неспецифические симптомы эхинококкоза включают слабость, крапивницу, преходящее повышение температуры; специфические зависят от места локализации паразита и могут быть представлены локальными болями, тошнотой, желтухой, кашлем, очаговой неврологической симптоматикой, кардиалгией, аритмией и пр. Диагностика эхинококкоза основывается на данных инструментальных исследований (рентгена, сцинтиграфии, УЗИ, КТ) и серологических проб. Лечение эхинококкоза хирургическое.
МКБ-10
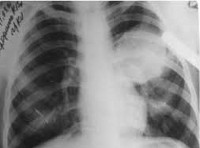
Общие сведения
Эхинококкоз – гельминтное заболевание из группы цестодозов, вызываемое паразитированием в организме человека эхинококка в стадии онкосферы. В мире наибольшая заболеваемость эхинококкозом отмечается в Австралии, Новой Зеландии, Северной Африке, Южной Америке, Южной Европе, Центральной Азии. В России гельминтоз встречается в Поволжье, Приуралье, Ставропольском и Краснодарском крае, Западной Сибири, на Дальнем Востоке.
В эндемичных регионах заболеваемость населения эхинококкозом достигает 5-10%. Распространенность эхинококкоза тесно связана с развитием животноводства. Учитывая тот факт, что при эхинококкозе могут поражаться различные внутренние органы, а единственно радикальным методом лечения является операция, заболевание лежит в сфере интересов торакоабдоминальной хирургии, нейрохирургии, кардиохирургии.

Причины эхинококкоза
Эхинококкоз человека вызывается личиночной стадией ленточного гельминта Echinococcus granulosus - лавроцистой. Окончательными хозяевами половозрелых гельминтов выступают животные (собаки, лисицы, волки, львы, рыси и др.), в кишечнике которых паразитируют цестоды. Человек, домашние и дикие травоядные животные (рогатый скот, свиньи, лошади, олени, лоси и др.) являются промежуточными хозяевами личиночных стадий и одновременно биологическим тупиком, поскольку не выделяют яйца эхинококка в окружающую среду и не могут служить источником инвазии.
Взрослые особи эхинококка – это мелкие гельминты длиной 2,5-8 мм и шириной 0,5-10 мм, имеющие головку с четырьмя присосками и двумя рядами крючьев, шейку и несколько члеников. В зрелых члениках содержатся яйца эхинококка с онкосферами и шестикрючной личинкой-зародышем внутри. Онкосферы выживают в большом диапазоне температур (от -30°С до +30°С), несколько месяцев сохраняются в почве, но вскоре погибают под действием солнечного света.
Из кишечника окончательного хозяина яйца с испражнениями выделяются во внешнюю среду. Заражение людей эхинококкозом происходит алиментарным (при употреблении загрязненных фекалиями овощей и фруктов, воды) или контактным путем (при разделке туш или контакте с животными, инвазированными эхинококком). Высокий риск заболеваемости эхинококкозом имеют лица, занятые животноводством и уходом за животными (животноводы, охотники, работники скотобоен и др.).
Патогенез
В ЖКТ человека под действием пищеварительных ферментов оболочка яйца и онкосферы растворяется, и наружу выходит личинка. С помощью крючьев она внедряется в слизистую кишки, откуда попадает в венозный кровоток и в портальную систему. Большая часть онкосфер оседает в печени; иногда через нижнюю полую вену онкосферы попадают в правые отделы сердца, а оттуда – в малый круг кровообращения и легкие. Реже через легочные вены и левые отделы сердца зародыши оказываются в большом круге кровообращения и могут быть занесены в любой орган: головной мозг, селезенку, почки, мышцы и др. В результате инвазии примерно в 70-80% случаев развивается эхинококкоз печени, в 15% - эхинококкоз легких, в остальных случаях происходит поражение других органов.
После оседания зародыша эхинококка в том или ином органе начинается пузырчатая или гидатидозная стадия развития паразита. Эхинококковый пузырь представляет собой кисту, покрытую двухслойно оболочкой, состоящей из внутреннего (зародышевого) и наружного (хитинового) слоев. Киста медленно увеличивается в размерах (примерно на 1 мм в месяц), однако спустя годы может достигать гигантских размеров. Внутри эхинококкового пузыря содержится прозрачная или беловатая опалесцирующая жидкость, в которой плавают дочерние пузыри и сколексы. Дочерние пузыри эхинококка могут образовываться и снаружи хитиновой оболочки; их общее количество может достигать 1000.
Проявления эхинококкоза связаны с сенсибилизирующим влиянием паразитарных антигенов и механическим давлением кисты на органы и ткани. Паразитирование эхинококка сопровождается выделением продуктов обмена, что приводит к развитию интоксикации и аллергической реакции замедленного типа. В случае полного разрыва кисты происходит истечение ее содержимого в плевральную или брюшную полость, что может вызвать анафилактический шок. Увеличивающаяся в размерах эхинококковая киста давит на окружающие структуры, нарушая функции пораженного органа. В некоторых случаях развивается нагноение кисты; реже возможно самопроизвольная гибель эхинококка и выздоровление.
Симптомы эхинококкоза
Эхинококкоз может бессимптомно протекать годами и десятилетиями; в случае возникновения клинической симптоматики патогномоничные признаки отсутствуют. Независимо от локализации паразита в организме, эхинококкоз проходит в своем развитии три стадии:
- I - бессимптомную. Течение латентного периода начинается от момента внедрения онкосферы в ткани и продолжается до тех пор, пока не появляются первые клинические признаки эхинококкоза.
- II - стадию клинических проявлений. Во время II стадии больных беспокоят боли в месте локализации кисты, слабость, крапивница, кожный зуд, а также специфические симптомы, обусловленные паразитированием кистозной формы эхинококка в том или ином органе.
- III - стадию осложнений. В стадии осложненного эхинококкоза может произойти разрыв кисты и истечение содержимого в брюшную или плевральную полость с развитием перитонита, плеврита. При нагноении эхинококковой кисты присоединяются высокая лихорадка, тяжелая интоксикация. Сдавление кистой органов и тканей может вызывать развитие механической желтухи, асцита, вывихов, патологических переломов.
Эхинококкоз печени
Для эхинококкоза печени характерны жалобы на тошноту, снижение аппетита, периодически возникающую диарею, тяжесть и боли в правом подреберье. Объективно обнаруживается гепатоспленомегалия; иногда эхинококковая киста печени пальпируется в виде округлого плотного образования. В случае сдавления кистой желчных протоков развивается механическая желтуха; при компрессии воротной вены возникает асцит, портальная гипертензия. Присоединение вторичной бактериальной флоры может приводить к формированию абсцесса печени. Наиболее тяжелым осложнением эхинококкоза печени служит перфорация кисты с развитием клиники острого живота, перитонита и тяжелых аллергических реакций. При этом происходит диссеминация эхинококков, в результате чего развивается вторичный эхинококкоз с множественный локализацией.
Эхинококкоз легких
Эхинококкоз легких протекает с повышением температуры тела, интоксикационным синдромом, болью в груди, кашлем, кровохарканьем. Давление кисты на легочную ткань приводит к формированию ателектазов легких. При прорыве пузыря в бронхи развивается сильный кашель, цианоз, нередко - аспирационная пневмония. Крайне опасным осложнением легочного эхинококкоза является прорыв кисты в плевру и перикард, что может привести к анафилактическому шоку, резкому смещению средостения, тампонаде сердца и внезапной смерти. Инфицирование эхинококковой кисты сопровождается формированием абсцесса легкого.
Эхинококкоз сердца
При эхинококкозе сердца беспокоят загрудинные боли, напоминающие стенокардию. Компрессия кистами венечных артерий может вызвать развитие инфаркта миокарда. Часто возникают нарушения ритма и проводимости: желудочковая тахикардия, неполная и полная блокады ножек пучка Гиса, полная поперечная блокада сердца. Причинами гибели пациента с эхинококкозом сердца могут стать злокачественные аритмии, сердечная недостаточность, тампонада сердца, кардиогенный шок, ТЭЛА, постэмболическая легочная гипертензия и др.
Эхинококкоз головного мозга
Клинка эхинококкоза головного мозга характеризуется гипертензионным синдромом и очаговой неврологической симптоматикой (нарушением чувствительности, парезами конечностей, эпилептиформными приступами).
Диагностика
Правильной диагностике эхинококкоза способствует подробно собранный эпидемиологический анамнез, указывающий на тесный контакт человека с животными, эндемичность заражения. При подозрении на эхинококкоз любой локализации назначаются серологические исследования крови (ИФА, РНИФ, РНГА), позволяющие обнаружить специфические антитела к эхинококку. Специфичность и чувствительность тестов достигает 80-98%. Примерно в 2/3 случаев оказывается информативной кожно-аллергическая проба - реакция Казони.
Диапазон инструментальной диагностики эхинококкоза включает ультразвуковые, рентгеновские, томографические, радиоизотопные методы. Перечень исследований зависит от локализации поражения:
- При эхинококкозе печени информативны УЗИ гепатобилиарной системы, ангиография чревного ствола (целиакография), МРТ печени, сцинтиграфия, диагностическая лапароскопия и др.
- Распознать эхинококкоз легких позволяет проведение рентгенографии легких и КТ грудной клетки, бронхоскопии, диагностической торакоскопии.
- Ведущими методами диагностики эхинококкоза головного мозга служат КТ или МРТ.
- При подозрении на поражение сердца выполняется ЭхоКГ, коронарография, вентрикулография, МРТ сердца.
При прорыве эхинококковой кисты в просвет полых органов сколексы паразита могут быть обнаружены в исследуемом дуоденальном содержимом, мокроте. Также в этих случаях прибегают к выполнению бронхографии, холецистографии, пункционной холангиографии. Эхинококковую кисту необходимо дифференцировать от альвеококкоза, бактериальных абсцессов, кист непаразитарной этиологии, опухолей печени, легких, головного мозга и пр.
Лечение эхинококкоза
Радикальное излечение эхинококкоза возможно только хирургическим путем. Оптимальным способом является проведение эхинококкэктомии – вылущивания кисты без нарушения целостности хитиновой оболочки. При наличии крупного пузыря вначале производится его интраоперационная пункция с аспирацией содержимого. Остаточная полость тщательно обрабатывается антисептическими растворами, тампонируется, дренируется или ушивается наглухо. В процессе операции важно не допустить попадания содержимого пузыря на окружающие ткани во избежание диссеминации эхинококка.
В случае невозможности иссечения кисты при эхинококкозе легкого выполняется клиновидная резекция, лобэктомия, пневмонэктомия. Аналогичная тактика используется при эхинококкозе печени. Если иссечение эхинококковой кисты печени представляется технически невозможным, осуществляется краевая, сегментарная, долевая резекция, гемигепатэктомия. В до- и послеоперационном периоде назначается противопаразитарная терапия препаратами празиквантел, альбендазол, мебендазол.
Прогноз и профилактика
В случае радикального удаления эхинококковых кист и отсутствия повторного заражения прогноз благоприятный, рецидивов эхинококкоза не возникает. В случае интраоперационной диссеминации сколексов через 1-2 года может возникнуть рецидив заболевания с формированием множественных эхинококковых пузырей и неблагоприятным прогнозом.
Эхинококкоз - лечение в Москве
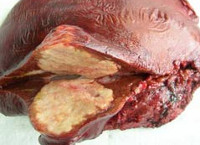
Комментарии к статье
Вы можете поделиться своей историей болезни, что Вам помогло при лечении эхинококкоза.
Эхинококкоз остается чрезвычайно актуальной проблемой не только медицины, но и социальной сферы. Наблюдается увеличение как числа заболевших, так и количества осложненных форм эхинококкоза [2, 3], при этом до 15% больных составляют дети до 14 лет. Несмотря на заметные успехи в диагностике и лечении данного заболевания, высокой остается частота до- и послеоперационных осложнений, показатель рецидивов заболевания колеблется от 2,7 до 30%, в ряде регионов летальность составляет 0,9-38,8% [2, 8, 9].
Перечисленные выше факторы требуют неотложных мер для комплексного решения проблем, касающихся диагностики, лечения и профилактики заболевания.
Традиционно в медицинской практике основным скрининговым методом выявления эхинококкоза служит УЗИ органов брюшной и грудной полости, рентгенография грудной клетки. В то же время в научной литературе недостаточно полно и однозначно определена роль иммуноферментного анализа (ИФА) в диагностике данного заболевания.
При лечении в зависимости от стадии заболевания, размеров паразитарных кист применяются различные методы: миниинвазивные (перкутанная пункционно-аспирационная эхинококкэктомия под контролем УЗИ или КТ, видеоторако- и видеолапароскопические вмешательства), традиционные эхинококкэктомия, перицистэктомия и резекция печени. Доказана достаточная эффективность консервативного лечения албендазолом, которое по рекомендации ВОЗ может применяться как самостоятельный метод [8, 11, 12, 15]. По данным некоторых авторов [11, 13], в 10-20% наблюдений албендазол оказывает угнетающее воздействие на белые и красные кровяные тельца и выраженное гепатотоксическое действие, проявляющееся резким повышением уровня трансаминаз. Однако исследований в области, касающейся методов консервативного лечения эхинококкоза у детей, недостаточно [4, 5]. В то же время многие авторы едины во мнении о необходимости послеоперационной противопаразитарной химиотерапии [3, 14]. Возникает проблема более глубокого анализа возможностей использования противопаразитарной химиотерапии как консервативного метода лечения эхинококкоза в педиатрической практике, что являлось целью нашего исследования.
Материал и методы
Тактику лечения эхинококкоза у детей выбирали в зависимости от размеров паразитарных кист и стадии заболевания, отдавая предпочтение щадящим, малотравматичным методам. При наличии эхинококковых кист диаметром до 35 мм отдавали предпочтение консервативной химиотерапии как самостоятельному методу лечения. Она была проведена в 7 наблюдениях при эхинококковых кистах печени и легких.
При единичных паразитарных кистах малых и средних размеров (до 100 мм), расположенных поверхностно, выполняли видеолапароскопическую эхинококкэктомию из печени. Операция произведена 75 пациентам, что составило 40,5% всех оперированных детей с эхинококкозом печени, выявленных со дня внедрения метода. Видеоторакоскопическая эхинококкэктомия из легких выполнены 11 детям.
При эхинококковых кистах больших и гигантских размеров, при множественном поражении органа и при локализации паразитарной кисты в глубине паренхимы проводилась традиционная эхинококкэктомия с ликвидацией остаточной полости.
Результаты и обсуждение
Башкортостан является эндемичным по эхинококкозу, где отмечается тенденция к увеличению количества больных детей. Считается, что у детей в отличие от взрослых чаще встречается эхинококкоз легкого [7, 8]. Нами также отмечено, что с 1974 по 1998 г. все наблюдения изолированного и сочетанного поражения легкого составили 53,9%, печени - 50,3%. Однако с 1999 по 2007 г. чаще диагностируется эхинококкоз печени (59,2%), чем легких (45,6%). Это, очевидно, связано с периодом широкого внедрения метода ультразвуковой диагностики заболеваний органов брюшной полости. Данный метод диагностики эффективен при паразитарных кистах малых и средних размеров. С 1999 по 2007 г. при ультрасонографии кисты, выявленные у 79,3% детей, имели малые и средние, у 20,7% - большие и гигантские размеры. Ранняя диагностика, позволяющая обнаружить кисты малых размеров, предоставляет дополнительные возможности для выбора более щадящих методов лечения.
ИФА, выполненный до операции у 79 детей с эхинококкозом печени, позволил выявить высокий титр антител у 38 (48%), низкий титр у 30 (38%), ложноотрицательный результат получен в 11 (13,9%) наблюдениях (табл. 1). Точность метода составила 91%, чувствительность - 86%. У 6 детей с ложноотрицательным результатом через 3-6 мес после операции обнаружены антитела, в том числе у 4 больных отмечено появление низкого, у 2 - высокого титра антител. К концу года у большинства оперированных больных прослеживается динамика снижения титра. Высокий титр антител в поздние сроки (т.е. через 3 года) во всех наблюдениях выявлялся при рецидиве заболевания. ИФА при поражении легких, выполненный до операции у 37 детей, выявил высокий титр в 10 (27%) наблюдениях, причем у 9 из 10 последних больных имелся осложненный эхинококкоз легких. Низкий титр антител отмечен у 11 (29,7%) и ложноотрицательный результат - у 16 (43,3%) пациентов. Точность метода составила 57%, чувствительность - лишь 55%. Через 3-6 мес после операции отмечается динамика повышения титра антител (табл. 2). К концу года после операции наблюдается тенденция к снижению титра антител. Высокий титр антител, выявленный через
3 года после операции, свидетельствовал о наличии рецидива заболевания.
Известно, что основные распространители эхинококкоза - собаки, одновременно они же являются проводниками не менее тяжелого паразитарного заболевания - токсокароза. В интересах исследования нами также проводилось определение антител к данному возбудителю. Известно, что прижизненно поставить диагноз токсокароза практически невозможно, поскольку обнаружить мигрирующие личинки довольно сложно [6]. Ведущими в диагностике токсокароза являются иммунологические методы. Титр специфической реакции 1:800 и выше свидетельствует о наличии заболевания с высокой долей вероятности, титр 1:200, 1:400 о носительстве токсокар или глазном токсокарозе [6, 9]. В наших исследованиях из 116 пациентов у 33 (28,4%) выявлен положительный результат реакции, в том числе у 25 при поражении печени, у 8 при поражении легких. У 23 (19,8%) детей титр антител составил 1:200, 1:400. Высокий титр антител выявлен у 10 (8,6%) обследованных: у 4 - 1:800, у 6 - в интервале от 1:1600 до 1:6400. После эхинококкэктомии титр антител на токсокароз сохранялся на прежнем уровне, в то же время при химиотерапии албендазолом отмечалась тенденция к значительному снижению титра. Указанные данные свидетельствуют скорее о наличии таксокароза в организме обследованных больных, чем о результате перекрестной реакции двух паразитарных заболеваний.

ИФА у последних 7 детей показал отсутствие антител к эхинококковому антигену у 5, низкий иммунный ответ у 2 больных. Основным диагностическим методом являлась ультросонография, на которой эхинококковая киста представлялась в виде округлого образования с четкими ровными гиперэхогенными контурами, что соответствовало I фазе жизнедеятельности паразита (см. рисунок а). Рисунок 1. Ультрасонограммы больного А., 8 лет. а - эхинококковая киста I сегмента печени. Двойной контур за счет хитиновой и фиброзной оболочек - эхографический признак, характерный для эхинококковых кист, в I фазе жизнедеятельности паразита не всегда определяется, что нередко вызывает определенные трудности при дифференциальной диагностике с непаразитарными кистами. В подобной ситуации у 2 больных нами проводилось динамическое наблюдение в течение 1-2 мес. За этот период отмечено увеличение размеров кисты, что характерно для эхинококкоза.
Консервативное лечение проводилось амбулаторно, только если пациент не относился к группе высокого риска. Препарат немозол (албендазол) назначался из расчета 10 мг/кг в сутки на 28 дней с перерывом 14 дней. 4 пациента получили 3 курса лечения, 3 детей - до 5 курсов. После каждого курса терапии проводился контрольный осмотр с клинико-лабораторным исследованием (общий анализ крови и мочи, биохимический анализ крови) и ультрасонографией печени. У большинства пациентов в конце первого курса лечения появлялись признаки интоксикации, связанные с разрушением оболочек эхинококковой кисты и всасыванием паразитарной жидкости, что сопровождалось повышением температуры тела, аллергическими проявлениями на коже, у 3 детей отмечены сыпь по типу крапивницы, кожный зуд. Общий анализ крови показал повышение уровня эозинофилов крови до 5-6%. ИФА выявил наличие высокого титра антител у 2 (1:800), низкого титра у 3 (1:100-1:200) и отсутствие антител у
Достаточно характерной являлась эхографическая картина: изменялась форма паразитарной кисты, появлялся двойной, неровный внутренний контур за счет отслойки хитиновой оболочки и отмечалось постепенное уменьшение размеров паразитарной кисты (см. рисунок, б). Рисунок 1. Ультрасонограммы больного А., 8 лет. б - эхинококковая киста I сегмента печени после одного курса химиотерапии. При дальнейшем наблюдении киста имела вид неоднородного жидкостного образования с гиперэхогенными слоистыми линейными структурами в просвете. Через 4-5 мес после лечения на месте бывшей кисты определялся участок неоднородности паренхимы (см. рисунок, в). Рисунок 1. Ультрасонограммы больного А., 8 лет. в - эхинококковая киста I сегмента печени после 3 курсов химиотерапии.
Консервативное лечение также назначено 2 пациентам при сочетанном эхинококкозе печени и легких после эхинококкэктомии из печени (в одном наблюдении удалены 20 кист). После первого курса медикаментозного лечения прекратился рост эхинококковой кисты легкого, после третьего-четвертого курса на рентгенограмме на месте паразитарных кист определялись участки затемнения (кальцификаты).
Консервативное лечение эхинококкоза у детей являлось комплексным и состояла из противопаразитарной и сопроводительной (посиндромной) терапии. В период аллергических проявлений детям назначались десенсибилизирующие препараты, после первого курса - гепатопротекторы, после третьего курса - энзимотерапия (вобензим по схеме) и пробиотики. Ранее проведенные нами исследования показали, что у детей с эхинококкозом имеются значительные нарушения микрофлоры кишечника [10]. Наиболее вероятно, что данные изменения являются вторичными, как следствие токсического воздействия продуктов жизнедеятельности паразита, поэтому в послеоперационном периоде необходима терапия, направленная на восстановление микрофлоры кишечника. Кроме того, на основании определения гуморального звена системы иммунитета у детей с эхинококкозом выявлен комбинированный характер изменений, патогномоничных для иммунного дисбаланса, в связи с чем в комплексном лечении использовали иммуномодулятор полиоксидоний. Мы не являемся сторонниками проведения химиотерапии на дооперационном этапе, особенно при больших и гигантских кистах. Дело в том, что в связи с разрушением хитиновой оболочки усиливается всасывание паразитарной жидкости. Это приводит к выраженной сенсибилизации организма до операции, к тому же имеется опасность разрыва паразитарной кисты во время хирургического вмешательства. Первоначально, исходя из опасности токсического действия препарата, мы чрезвычайно осторожно использовали албендазол, только для профилактики рецидива заболевания при осложненных формах. Однако практика показала, что токсическое действие препарата удается снизить при его использовании в комплексе с сопроводительной терапией. В дальнейшем мы стали более широко внедрять комплексное лечение не только для профилактики, но и как самостоятельный метод при кистах малых размеров. Препарат действительно токсичен, в самом начале комплексного лечения в одном наблюдении потребовалась его отмена в связи с аллергической реакцией. Однако эффективность данного метода подтверждается практикой при комплексном и своевременном назначении сопроводительной терапии.
Профилактика рецидива заболевания чрезвычайно важна в связи тем, что ретроспективный анализ данных нашей клиники при эхинококкозе печени показал возникновение рецидива у 11 (4,6%) больных, при поражении легких - у 4 (2,2%). Рецидив выявлялся в сроки от 1 года до 3 лет. Кроме того, у 12 пациентов во время диспансерного наблюдения обнаружен эхинококк других органов. Это свидетельствует о том, что у детей нередки сочетанные поражения и эхинококк может находиться на разных стадиях развития.
Послеоперационная профилактическая химиотерапия проведена у 115 пациентов при поражении печени (67), легкого (39), при сочетанном поражении печени и легкого (15) и при редких локализациях паразита (4). С начала внедрения химиотерапии, т.е. за последние 5 лет, рецидива заболевания у наблюдаемых детей не было. Исключением является ребенок, оперированный по поводу эхинококковой кисты головного мозга, у которого наступил рецидив, несмотря на проведенную химиотерапию. Вероятно, это связано с тем, что немозол недостаточно проникает через гематоэнцефалический барьер.
Проведение противопаразитарной химиотерапии оправдано еще тем, что у 28,4% пациентов до операции и во время диспансерного наблюдения сохраняется высокий титр антител к токсокарозу. Албендозол (немозол) является активным антигельминтным средством, в том числе к токсокарозу. После проведения химиотерапии отмечается стойкая тенденция к снижению титра антител.
Наши исследования показали что, результаты химиотерапии в качестве самостоятельного метода лечения можно оценить как успешные во всех наблюдениях. Противопаразитарная химиотерапия является радикальным методом лечения эхинококкоза у детей при кистах малых размеров. Она должна проводиться под врачебным контролем и сопровождаться посиндромной терапией. Такая тактика дает возможность снизить до минимума побочные реакции. Профилактическая химиотерапия в послеоперационном периоде позволяет снизить до минимума вероятность возникновения рецидива заболевай и, кроме того, провести эрадикацию других паразитов, например возбудителя токсокароза.
Таким образом, широкое применение ультразвукового исследования в эндемичных очагах позволяет выявлять эхинокковые кисты малых размеров, что в свою очередь дает дополнительные возможности для консервативного лечения эхинококкоза у детей.
Консервативное лечение должно быть комплексным, т.е. состоять из противопаразитарной и посиндромной терапии.
Иммуноферментный анализ наряду с ультрасонографией во время диспансерного наблюдения способствует своевременному выявлению рецидива заболевания и проведению консервативного лечения.
Комплексное использование ранней диагностики и методов лечения позволяет существенно повысить эффективность лечения эхинококкоза у детей.
Читайте также:

