Экстракорпоральные методы детоксикации при сепсисе
Обновлено: 25.04.2024
Сепсис. ДВС синдром при сепсисе
Активация при сепсисе системы гемостаза обусловлена эндото-ксемией и бактериальными липополисахаридами. Центральным медиатором сепсиса является фактор некроза опухоли (TNF—tumor necrosis factor), который вырабатывается в ответ на поступление эндотоксина. Вторичный медиатор — интерлейкин-1, концентрация которого резко возрастает после поступления в сосудистое русло TNF. Вслед за выработкой этих провоспалительных медиаторов происходит повышение уровня интерлейкина-6, который активизирует синтез в печени белков острой фазы.
Полисахариды грампозитивных бактерий также могут посредством цитокинов активизировать систему гемостаза, что резко увеличивает риск ДВС.
Иногда ДВС индуцируется фулминантной вирусной инфекцией. Тяжело протекающие инфекции сопровождаются обычно лейкоцитозом. Нейтрофильные лейкоциты вырабатывают ряд субстанций (в том числе нейтрофильную эластазу), которые вызывают дефицит AT III, а гепаринотерапия усугубляет этот процесс.
Следует иметь в виду, что применение бактерицидных антибиотиков увеличивает риск возникновения септического шока вследствие массивного поступления в русло эндотоксинов из разрушенных бактерий. Молниеносные формы сепсиса возникают на фоне иммуносупрессивнои терапии. Смертность при септическом шоке достигает 40 %. Септический шок, рефракторный к терапии, быстро, в течение нескольких часов приводит к полиорганной недостаточности и ДВС-синдрому.
В ряде случаев не удается установить возбудителя инфекции в гемокультуре больных сепсисом. Концепция системного воспалительного ответа предполагает наличие сепсиса при отсутствии (невозможности определения) возбудителя в крови в случаях выраженной характерной клиники:
• фебрильная температура (> 38 °С) или гипотермия (> 35,5 °С встречается у 10 % больных);
• тахикардия;
• тахипноэ, гипервентиляция с респираторным алкалозом. Для лабораторных показателей характерно:
• лейкоцитоз > 15 000 /мм3 или лейкопения > 3500 /мм3;
• сдвиг лейкоцитарной формулы влево, токсическая зернистость;
• изменения коагуляции — снижение числа тромбоцитов более чем на 30 % за 24 ч, снижение AT III;
• метаболические сдвиги — гиперлактатемия, гипергликемия, гипофосфатемия.
Для сепсиса характерен дефицит системы естественных антикоагулянтов, причем снижение AT III происходит ранее основных клинических проявлений сепсиса. При снижении содержания AT III ниже 60 % смертность резко возрастает.
Причины сепсиса
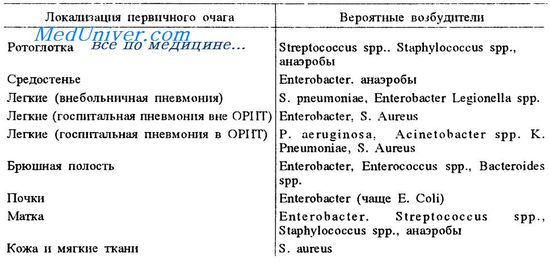
Количество тромбоцитов при сепсисе снижается вследствие тромбоцитопении потребления — тромбоциты связываются с фибрином, адгезируют к поврежденному эндотелию, секвестрируются в легких и печени. Тромбоцитопатия — снижение агрегирующих свойств тромбоцитов — может быть вызвана длительным применением антибиотиков.
Лечение сепсиса, септического шока и ДВС-синдрома должно носить комплексный характер и основываться на следующих принципах:
1. Хирургическое лечение очага инфекции (санация и дренирование).
2. Антибиотикотерапия, основанная на идентификации возбудителя и определении его чувствительности к соответствующей группе антибиотиков.
3. Адекватная оксигенация — необходима ранняя ИВЛ в различных режимах.
4. Инфузионная терапия — высока опасность гипергидратации, особенно в условиях тканевой гипоксии и повышения капиллярной проницаемости. Трансфузия эритроцитов не только повышает кислородтранспортную функцию крови, но и обеспечивает эффективность трансфузионной терапии. Критическим для септических больных считается содержание гемоглобина менее 70—80 г/л. Предпочтительна трансфузия свежезаготовленной эритроцитной массы.
5. Применение катехоламинов. Содержание фактора некроза опухоли (TNF) при сепсисе значительно возрастает (TNF — медиатор, обладающий выраженным кардиодепрессйвным действием).
6. Препараты AT III.
В 1985 году В. Blauhut опубликовал результат клинических исследований по применению препарата AT III (кубернина HS). У пациентов с клиникой септического шока и ДВС, которым был назначен кубернин HS, отмечено ускоренное восстановление показателей коагуляции, хотя и не было отмечено снижение смертности.
Некоторые исследователи рекомендуют поддерживать содержание AT III на уровне 140 %, это возможно при введении препарата в суммарной дозе 18 000 ЕД. Содержание AT III не должно снижаться менее 80 %.
9. Поливалентные иммуноглобулины используются для нейтрализации эндотоксинов. Отмечено снижение смертности при их применении у кардиохирургических больных.
10. Методы экстракорпоральной детоксикации: гемофильтрация, плазмаферез.
Экстракорпоральная детоксикация при сепсисе. Анестезиологическое пособие у больных септическим шоком.
Гемосорбция. Выполнение гемосорбции при сепсисе и септическом шоке имеет свои особенности, в частности, продолжительность эффективной работы колонки объемом 200 мл составляет 20-30 минут при скорости перфузии 100 мл/мин. За один сеанс гемосорбции необходима, как минимум, трехкратная замена колонок. Общий объем сорбированной крови должен составлять 4-6 л.
У больных с сепсисом в течение 12-24 часов после сеанса гемосорбции отмечается улучшение реологических свойств крови, а при наличии синдрома мультиорганной дисфункции - снижается уровень креатинина. Однако в целом позитивного влияния гемосорбции в течение сепсиса и мультиорганной дисфункции не выявлено.
Плазмоферез. Плазмоферез у больных сепсисом и септическим шоком показан для коррекции гемокоагуляционных нарушений. Экстракция плазмы с большим количеством биологически активных веществ и одновременным замещением ее донорской плазмой является патогенетически обоснованным средством борьбы с синдромом ДВС у этой категории больных.
К недостаткам, существенно ограничивающим использование плазмофереза, относятся отсутствие достаточного количества донорской плазмы, а также все возрастающая возможность инфицирования больного (гепатит, ВИЧ-инфекция, сифилис).
Гемодиализ. Применение гемодиализа показано пациентам с сепсисом, приведшим к развитию ОПН. Скорость кровотока через контур аппарата составляет 200-300 мл/мин, что обусловливает достаточно высокие требования к состоянию сердечно-сосудистой системы и делает невозможным использование метода при септическом шоке.
Гемофильтрация. Гемофильтрация является методом в терапии больных с сепсисом и септическим шоком, осложненным синдромом мультиорганной дисфункции. Процедура заключается в постоянном, многосуточном проведении гемофильтрации и имеет целью регуляцию процессов воспаления, постоянное выведение токсических метаболитов, коррекцию объемов водных секторов организма. Гемофильтрация, особенно в сочетании с методами респираторной поддержки (ИВЛ), значительно повышает эффективность лечения респираторного дистресс-синдрома.
Невысокий поток крови через гемофильтр компенсируется постоянным проведением процедуры без существенного влияния на гемодинамические показатели. Объем замещаемой жидкости в течение суток достигает 20 л и более.

Анестезиологическое пособие у больных септическим шоком
Оперативное вмешательство с целью удаления или активного дренирования первичного очага должно быть предельно коротким, максимально простым, малотравматичным и надежным.
Методом выбора в таких ситуациях является тотальная внутривенная анестезия с управляемой ИВЛ. Введение в наркоз осуществляется методом "crash-induction", который заключается в следующем. После 5-минутной преоксигенации (RO2 = 1,0) и выполнения приема Селлика вводится недеполяризирующий миорелаксант (4 мг ардуана), затем препарат для вводного наркоза (кетамин 2 мг/кг или диприван 2-3 мг/кг). Без вспомогательной вентиляции интубируется трахея больного, раздувается манжета интубацнонной трубки и начинается ИВЛ в режиме PEEP с Fi02 = 0,5. Для поддержания анестезии используются кетамин (2 мг/кгч) или диприван (5-10 мг/кг-ч) в сочетании с фентанилом (300-400 мкг/ч). Возможно использование мононаркоза оксибутиратом натрия (до 250 мг/кг).
В послеоперационном периоде показана продленная ИВЛ до элиминации анестетиков и стабилизации жизненно важных функций организма.
Критериями адекватности проводимой терапии септического шока являются улучшение общего состояния больного, исчезновение цианоза, порозовение кожи, ее потепление на кистях и стопах, уменьшение одышки и тахикардии, нормализация артериального давления и ЦВД, сердечного выброса, возрастание темпа диуреза.
SOFA (sepsis-related organ failure assessment) - шкала оценки органной недостаточности, связанной с сепсисом. Нарушение функции каждого органа (системы) оценивается отдельно в динамике на фоне интенсивной терапии. При сумме баллов не более 12 предполагаются множественные органные дисфункции, 13-17 баллов - предполагается переход дисфункции в недостаточность. Сумма баллов около 24 указывает на высокую вероятность летального исхода.
Информация на сайте подлежит консультации лечащим врачом и не заменяет очной консультации с ним.
См. подробнее в пользовательском соглашении.

Хорошилов С.Е.
Актуальность
- Абдоминальный сепсис — одна из наиболее сложных проблем современной медицины
- Транслокация эндотоксина через энтеро-гематический барьер является ведущим патогенетическим фактором
- Расстройства тканевой перфузии приводят к циркуляторной и тканевой гипоксии, которая ведёт к полиорганной недостаточности
- Экстракорпоральная детоксикация — высокоэффективный компонент современной интенсивной терапии
СЕПСИС – состояние ЭНДОТОКСИКОЗА


Цель работы
Улучшить результаты лечения абдоминального сепсиса путём комплексного применения экстракорпоральных методов под контролем тканевой перфузии
Характеристика больных
В исследование включено 68 больных с абдоминальным сепсисом.
Характеристика больных
Нозологические группы абдоминального сепсиса

Группы больных
- В первую группу (n=23) вошли больные, которым проводилась селективная сорбция эндотоксина в сочетании с ГДФ на сверхпроницаемых диализаторах.
- Во второй группе (n=37) больным проводилась продлённая ГДФ.
Тяжесть состояния
APACHE II 18.5±1.38.
Этапы контроля:
Лабораторные и инструментальные показатели контролировались исходно, а также через 6 и 12 часов от начала экстракорпоральной детоксикации
Экстракорпоральные методы лечения
Сочетанное применение селективной гемосорбции и гемодиафильтрации
Концентрация эндотоксина в крови более 2 ед/мл являлась показанием к проведению селективной сорбции ЛПС (LAL-тест)
Селективная гемосорбция - Hospal BSM-21sc. Скорость гемоперфузии 100 мл/мин

Гемодиафильтрация
Показанием для проведения продленной гемодиафильтрации являлась почечная недостаточность
Выполнялась на аппарате Multifiltratе (Fresenius) в режиме CVVHDF.
Кровоток 200-220 мл/мин, расход диализирующего раствора 4800 мл/ч.
Диализатор EMiC2, гемофильтр AV1000S

Средняя продолжительность гемосорбции была равна 3.57±1.18 ч Длительность ГДФ варьировала в зависимости от клинической необходимости и в среднем составила 10.79±0.8 ч.
Диагностика
Ультразвуковая допплеровская флоуметрия позволяет
- Оценить компоненты тонуса микрососудов амплитуды микрокровотока на основе колебаний
- Исследовать основные параметры микрокровотока непосредственно во лечебного воздействия
X Vas – максимальная систолическая скорость по кривой средней скорости
X Vam – средняя скорость по кривой средней скорости
X Vakd – конечная диастолическая скорость по кривой средней скорости
X Qam – средняя скорость объёмного кровотока по кривой средней скорости (мл/сек/см3)
X RI – индекс периферического сопротивления
Результаты и обсуждение
Исходные показатели КЩС

Исходные значения маркеров воспаления

Исходные показатели тканевой перфузии по данным ультразвуковой допплерографии


Корреляционные связи между исходными параметрами
- Корреляционная связь между Qam и эндотоксинемией (r=- 0,311, p <0,05), связь между Vam и эндотоксинемией (r=- 0,282, p<0,05).
- Корреляционная связь между уровнем прокальцитонина и линейной скоростью кровотока (r= ˗0,51, p <0,05), а также объемной скоростью кровотока (r= ˗0,49 p<0,05)
Изменение уровня эндотоксина, ед/мл

*Достоверность различий в сравнении с исходными значениями (p<0,05)
Изменение маркеров воспаления

*Достоверность различий в сравнении с исходными значениями (p<0,05)
Изменение КЩС

*Достоверность различий в сравнении с исходными значениями (p<0,05)
Влияние сочетанного применения ГДФ и селективной сорбции ЛПС на тканевую перфузию (1 группа)

*Достоверность различий в сравнении с исходными значениями (p<0,05)
Влияние ГДФ на тканевую перфузию (2 группа)

*Достоверность различий в сравнении с исходными значениями (p<0,05)
Визуальная характеристика допплерограмм

Взаимосвязь эндотоксинемии и тканевой перфузии

- Изменение уровня эндотоксинемии и линейная скорости кровотока (r=0,8, p <0,05).
- Изменение уровня эндотоксинемии и объемная скоростью кровотока (r=0,58, p <0,05).
- Снижение ЧСС и снижение ЛПС в крови (r=0,416, p <0,05).
Взаимосвязь эндотоксинемии и тканевой перфузии

Дата публикации заявки: 20.03.2012
Дата начала действия патента: 20.09.2010
Патент на изобретение No 2445125 от 2012
Патент Способ получения сетчатого полимерного сорбента для селективной сорбции эндотоксина из плазмы крови.

Экспериментальная часть, этап 1: Элиминация эндотоксина в изотоническом растворе натрия хлорида путём изолированной перфузии на полимерном сорбенте
Материал и методы
- Эндотоксин (10.000.000 ЕЭ) в 2 л 0,8% р-ра натрия хлорида
- Перфузия полимерного сорбента 100 мл/мин при t 37°С
- Хромогенный ЛАЛ-теста по конечной точке (реагенты Pyrochrome)
Результаты
Снижение концентрации эндотоксина в растворе
- через 30 мин – в 1,7 раза
- через 60 мин – в 7,7 раз
- через 120 мин – в 18,5 раз
- Цельная свежезаготовленная кровь 400 мл
- Перфузия 100 мл/мин
- Биохимический анализ крови
- Оценка морфологии клеток крови методом атомной силовой микроскопии
- Несмотря на многочисленные нерандомизированные исследования два метаанализа показали, что продленная заместительная почечная терапия и интермиттирующий гемодиализ эквивалентны по эффективности (одинаковая краткосрочная выживаемость)
- Целесообразно использовать продленные варианты заместительной почечной терапии для контроля водного баланса при нестабильности гемодинамики
- Критерий ОПН - увеличение креатинина 25% в течение 7 дней
- Летальность
- специальной аппаратуры
- сосудистого доступа.
- Высокообъемная гемофильтрация с замещением 90 мл/кг/час является эффективным средством стабилизации гемодинамики при септическом шоке, поэтому целесообразно её включение в комплекс противошоковой интенсивной терапии
- Использование сверхвысокопроницаемых диализаторов позволяет достичь сходных эффектов за счет диффузионного массопереноса и может быть рекомендовано особенно при продолжительном использовании или появлении сложностей с сосудистым доступом
- При сепсисе, вызванным грамм (-) флорой наиболее эффективной представляется ранняя LPS-сорбция, которая возможно позволяет предотвратить развитие септического шока и (или) его тяжелых осложнений
- Для обоснованного применения LPS-сорбции следует включить определение эндотоксина и маркеров реакции на него (LAL-тест, ЕАА, пресепсин, и . ) в рутинную практику лабораторного мониторинга

Экспериментальная часть, этап 1: Элиминация эндотоксина в изотоническом растворе натрия хлорида путём изолированной перфузии на полимерном сорбенте

*Shoji H., Minaga M., Sakai Y., Kunitomo T., Takeyama T., Tani T., Kodama M. Design and development of endotoxin detoxifying column PMX and its clinical application. // Jpn. J. Artif. Organs. 1993. Vol. 22. Is. 1. P. 204-211.
! Устойчивый градиент концентрации эндотоксина на входе и на выходе из устройства более 2 часов
Экспериментальная часть, этап 2: Изучение эффективности и безопасности гемоперфузии на цельной донорской крови
Материал и методы

Экспериментальная часть, этап 2: Изучение эффективности и безопасности гемоперфузии на цельной донорской крови


Экспериментальная часть, этап 3: Эффективность полимерного сорбента на модели эндотоксического шока (у крупного животного)
Материал и методы
Экспериментальная часть, этап 3: Эффективность полимерного сорбента на модели эндотоксического шока у свиньи

Комплексная экстракорпоральная детоксикация при сепсисе с использованием сверхпроницаемых диализаторов и инновационных сорбентов

*Полимерный сорбент на основе сверхсшитого полистирола, патент на изобретение RU 2 653 125 C1 [07.05.2018 Бюл. No 13].
Заключение
ОПУБЛИКОВАНО В ОТЧЁТНОМ ПЕРИОДЕ (2016-2017)
Хорошилов С. Е., Марухов А. В., Никулин А. В. Применение плазмафереза в ферментативной фазе тяжелого острого панкреатита: новый взгляд на испытанный метод // Medicine (Almaty). — 2017. — No4 (178). — С. 287-292 [УДК 616-036.882-08]
Хорошилов С. Е., Никулин А. В. Патогенез, диагностика и эфферентное лечение рабдомиолиза, осложнённого острой почечной недостаточностью // Тверской медицинский журнал. — 2017. — No5. — С. 10-15.
Хорошилов С. Е., Никулин А. В. Детоксикация при критических состояниях: понимание научной проблемы в 21 веке // Общая реаниматология. — 2017. Юбилейный выпуск
ОПУБЛИКОВАНО В ОТЧЁТНОМ ПЕРИОДЕ (2018)

Хорошилов С.Е.




Токсины
Alle Ding' sind Gift und nichts ohn' Gift; allein die Dosis macht, dass ein Ding kein Gift ist.
Всё есть лекарство и всё есть яд – лекарство от яда отличает только доза

Филипп Ауреол Теофраст Бомбаст фон Гогенгейм (1493 г. - 1541 г.)
Актуальность

Размер эндогенных ТОКСИЧЕСКИХ СУБСТАНЦИЙ (D)

Экстракорпоральная детоксикация способствует уменьшению летальности при сепсисе


Заместительная почечная терапия

Методы экстракорпоральной терапии крови при ССВО / сепсисе
Заместительная почечная терапия может использоваться в комплексном лечении больных с ССВО/сепсисом
При ССВО/сепсисе без острой почечной недостаточности заместительная почечная терапия в стандартном виде в составе комплексной терапии мало эффективна и является плохим поводом для дальнейших исследований
Другие методы экстракорпоральной терапии, включая HVHF, технологии обработки плазмы, гемосорбцию, могут быть более полезными, но плохо изучены


Заместительная почечная терапия – значение дозы


С. Ronco et al. Effects of different doses in continuous veno-venous hаеmоfiltrаtiоn, Lancet, 356, 26 – 30, 2000

1 группа, 36 чел, 90 мл /кг /час
2 группа, 17 чел, 35 мл /кг /час
Высокообъемная гемофильтрация при септическом шоке

АРАСНЕ II 29,1 ± 3,6 баллов
SAPS 53,9 ± 7,1 баллов
ИНОТРОПНАЯ ПОДДЕРЖКА - 53 (100 %) больных
ИВЛ - 43 (81%) больных
Среднее артериальное давление во время высокообъёмной и стандартной гемофильтрации при септическом шоке

Изменение дозы симпатомиметиков течение 1 суток по группам

Эффективность высокообъёмной гемофильтрации для предупреждения повреждения почек при септическом шоке

АКШ с протезированием клапанов (n = 843)
Неолигурическая ОПН – 14.5%
ОПН, требующая гемодиализа – 83.3%
Loef BG, Epema AH, Smilde TD, et al: Immediate postoperative renal function deterioration in cardiac surgical patients predicts in-hospital mortality and long-term survival. J Am Soc Nephrol 2005; 16:195-200
Высокообъемная гемофильтрация требует применения



Дислокация перфузионного катетера


Низкопоточный гемодиализ с применением Ultraflux EMiC2 позволяет объединить преимущества конвективного и диффузионного массопереноса

Enhanced Middle Molecule Clearance
Эффективное удаление средних молекул
Сверхвысокопроницаемый капиллярный диализатор
Коэффициент просеивания Ultraflux® EMiC®2

Элиминация миоглобина при проведении высокообъемной гемофильтрации и гемодиализа с сверхвысокопроницаемым диализатором

Актуальность
Распределение летальности при ТСТ
Э.Н. Лебедев и др., НИИСП им. И.И. Джанелидзе, С.-Петербург

В настоящее время на первое место среди факторов, влияющих на уровень летальности при тяжелой сочетанной травме, выходят осложнения, связанные с развитием инфекции, – сепсис, септический шок и полиорганная недостаточность
Ермолов А.С., Соколов В.А. Гнойно-септические осложнения при сочетанной травме // Здоровье столицы - М., 2002.
Marshall J.C., Christou N.V., Meakins J.L.
The gastrointestinal tract: the "undrained abscess" of multiple organ failure
Ann. Surg. -1993. - Vol. 218, N2.-P. 111-119.

Селективная гемосорбция эндотоксина – целенаправленное воздействие на доказанное ключевое этиопатогенетическое звено

Селективные сорбенты для элиминации ЛПС


Актуальность
Опыт ГВКГ им. Н.Н. Бурденко


Влияние ЛПС-сорбции на показатели активности системного воспаления и периферическую гемодинамику




Влияние комбинированной экстракорпоральной детоксикации на ультразвуковые показатели тканевой перфузии


Исходная допплерографическая картина

Допплерографическая картина после завершения ЭКД

Допплерографическая картина после завершения ЭКД

ВЫВОДЫ

C. Hamilton-Davies et al., Yearbook of Int. Care and Emerg. Med. – 1996 (с изменениями)

Хорошилов С.Е., Никулин А.В., Бажина Е.С.
ФГБНУ НИИ общей реаниматологии им. В.А. Неговского, Москва; ФГКУ Главный военный клинический госпиталь им. акад. Н.Н. Бурденко Минобороны России, Москва
Абдоминальный сепсис (АС) – одна из самых сложных проблем современной медицины, актуальность которой определяется большим количеством больных, высокой летальностью (40% при тяжелом сепсисе и 63% при септическом шоке) и большими экономическими затратами на лечение.
Основным источником эндогенной интоксикации при АС является желудочно-кишечный тракт. Инициирующим звеном патогенеза АС является попадание в кровоток фрагментов оболочки грамотрицательных бактерий, по химической структуре относящихся к липополисахаридам. Высвобождение эндотоксина происходит при разрушении стенок бактерий. Попадание эндотоксина в кровеносное русло сопровождается нарушениями микроциркуляции: увеличивается проницаемость сосудистой стенки, развивается распространенное повреждение клеток эндотелия. Рост капиллярной проницаемости, ведущий к потере жидкой части крови в интерстициальный сектор внеклеточного пространства с развитием гиповолемии и гипоперфузии органов и тканей, затрудняет транспорт кислорода и в конечном итоге приводит к формированию полиорганной недостаточности.
Одним из возможных подходов в лечении сепсиса и септического шока может быть применение экстракорпоральных методов, нацеленных на селективное удаление эндотоксина путем гемосорбции. Однако элиминация эндотоксина из циркулирующей крови при уже запущенном каскаде воспалительных реакций не приведет к полному регрессу системного воспалительного ответа (СВО), поскольку присутствующие в крови цитокины продолжают поддерживать воспалительную реакцию организма.
Вместе с тем отсутствие исследований микроциркуляторного русла в ответ на детоксикационное воздействие экстракорпоральных методов лечения требует изучения для наиболее эффективного воздействия на тканевую перфузию и улучшение микроциркуляции при септическом шоке.
Материал и методы
Проведен анализ лечения 15 больных с АС и септическим шоком. В исследование включены лица моложе 60 лет, у которых отсутствовали гемодинамически значимые стенозы магистральных артерий верхних конечностей и клинические проявления ИБС в анамнезе (ангинозные боли, недостаточность кровообращения, нарушения сердечного ритма сердца). Выраженный атеросклеротический процесс сам по себе значительно ухудшает показатели микрогемодинамики, а ИБС приводит к снижению сердечного выброса, что уменьшает репрезентативность получаемых данных. У всех больных выявлен тяжелый сепсис или септический шок. При диагностике ориентировались на расширенные клиниколабораторные признаки сепсиса, позволяющие объективно оценить тяжесть состояния, в том числе при невыявленном источнике инфекции. Тяжесть состояния больных, оцениваемая по шкале APACHE II, к началу экстракорпорального лечения составляла 21,8±2,9 балла. По шкале SOFA тяжесть состояния больных исходно была в среднем равна 11,3±2,7 балла.
Ранняя диагностика сепсиса предусматривала определение прокальцитонина (> 2 нг/мл) у всех больных, что позволяло уточнить бактериальное происхождение СВО.
Лечение предусматривало стабилизацию гемодинамики введением норадреналина в дозе 260±19 нг/кг/мин, системную антибактериальную терапию, защиту желудочно-кишечного тракта и пр. в соответствии с рекомендательным протоколом Surviving Sepsis Campaign (2012).
Состояние больных к началу исследования было крайне тяжелым, что было обусловлено развитием АС и септического шока.
Семи больным с сепсисом без признаков ОПН (согласно критериям RIFLE) проводилась селективная гемоперфузия адсорбером AltecoLPS-Adsorber (Lund, Швеция) на гемопроцессоре Hospal BSM-21sc. Восьми больным с неолигурической ОПН выполнялась гемодиафильтрация (ГДФ) в интермиттирующем режиме. Использовались гемофильтры AV1000S и EMiC2 на аппаратах искусственной почки Fresenius 4008 H и B. Braun Dialog+ с кровотоком 220 мл/мин и дозой замещения 55 мл/кг/ч без ультрафильтрации. Продолжительность ГДФ составила 8 ч. Антикоагуляция проводилась продленной инфузией гепарина в дозе 500–1000 ЕД в час под контролем АЧТВ для достижения целевых значений 80–100 с.
Проводился неинвазивный мониторинг гемодинамики. Микроциркуляция изучалась методом ультразвуковой флоуметрии, основанной на эффекте Допплера с использованием волны 660 нм, так как данная длина волны позволяет работать в зоне микроциркуляторного кровотока, определяя такие характеристики, как линейную и объемную скорости кровотока по срезу изучаемой ткани. Исследование микроциркуляции проводилось методом высокочастотной ультразвуковой допплерографии на отечественном аппарате допплерографе ММ-Д-К (Минимакс-допплер-К), ООО СП “Минимакс”, Санкт-Петербург (регистрационное удостоверение № ФСР 2007/00810 от 18 сентября 2007 г.) с определением показателей микроциркуляции на ногтевом валике среднего пальца кисти. В процессе лечения (исходно, во время детоксикации и через 2 ч после ее окончания) оценивали состояние тканевой перфузии. Прибор позволяет оценить изменения перфузии тканей (жидкостный обмен), когда в области УЗ-сканирования не лежат сосуды диаметром более 1 мм, для чего использовали непрерывный высокочастотный ультразвуковой датчик 20–25 МГц.
Спектрограммы анализировали по качественным и количественным характеристикам.
Оценивали регистрируемые прибором: скоростные показатели кровотока: Vas – максимальная систолическая скорость по кривой средней скорости; Vam – средняя скорость по кривой средней скорости; Vakd – конечная диастолическая скорость по кривой средней скорости; показатели объемного кровотока: Qam – средняя скорость объемного кровотока по кривой средней скорости (мл/сек/см3 ); RI – индекс периферического сопротивления, или индекс Пурсело, отражающий состояние сопротивления кровотоку дистальнее места измерения. Измеряется в условных единицах и рассчитывается по формуле:
где Vs – максимальная систолическая скорость по кривой максимальной скорости (огибающей) в см/с, Vd – конечная диастолическая скорость по кривой максимальной скорости в см/с. При оценке статистической значимости различий и изменений в качестве порогового было принято значение p
Материал и методы
Результаты исследования и их обсуждение
Влияние селективной гемосорбции эндотоксина на тканевую перфузию.
При сравнении средних значений тканевой перфузии выявлено, что показатели линейных скоростей кровотока, как и показатели объемной скорости кровотока Qam, были существенно ниже нормы. После проведения гемосорбции линейные показатели скоростей кровотока увеличились (табл. 1), также происходило увеличение Qam на фоне некоторого снижения RI.

В процессе лечения происходила нормализация спектральной картины периферического кровотока, т. е. преобладающий в начале лечения венозный компонент постепенно заменялся артериальным. Изменение спектральной картины можно объяснить исчезновением патологического артериоло-венулярного шунтирования к концу гемосорбции, этим же вызвано увеличение объемной скорости и рост линейных скоростей кровотока, а также уменьшение RI.
Качественная характеристика кривой скорости допплерограммы в норме меняется в зависимости от вида и калибра сосуда. Крупная артерия дает остропиковую форму кривой (быстрая систола сердечных сокращений) и более пологую кривую диастолической скорости кровотока. Чем меньше артериальный сосуд, тем более пологий диастолический спуск и менее острую вершину максимума систолической скорости имела допплерограмма. Смешанный кровоток (при отсутствии дифференцировки сосудов микроциркуляции) характеризовался волнообразной картиной окрашенного спектра без острых пиков. Распределение цвета в допплерограмме – от ярко красного через оранжевый до светло-желтого, почти белого на изолинии зависело от степени снижения периферического кровотока. При этом регистрировалась картина интегральной по срезу скоростной характеристики жидкостного обмена в ткани – тканевой перфузии. Измерения проводили под углом 60o, так как при таком расположении луча датчика по отношению к тканям достигался максимальный по звуку и амплитуде сигнал. В результате огибающая кривая имела сглаженный, пульсирующий вид, цветовой спектр был смешанный артериовенозный.
Влияние гемодиафильтрации на тканевую перфузию при септическом шоке
Исходные значения показателей тканевой перфузии между группами больных не различались. Было выявлено, что у больных под влиянием ГДФ показатели линейной скорости кровотока к концу 2-го часа ГДФ не изменялись (табл. 2). Напротив, Qam во время ГДФ несколько увеличился. Показатель RI, наоборот, значимо снизился по сравнению с исходным значением. В то же время после прекращения ГДФ отмечен статистически значимый рост Qam в сравнении с исходным значением наряду с существенным ростом линейных скоростей кровотока.

В начале (как правило, в первые 30 мин ГДФ) лечения преходящая артериальная гипотензия требовала временно увеличить дозу вазопрессорной поддержки. После адаптации больного к экстракорпоральной циркуляции регистрируется позитивное влияние ГДФ на периферический кровоток (см. табл. 2), которое сохранялось на протяжении суток при условии, что адекватно выполнены необходимые дренирующие хирургические вмешательства, направленные на устранение источника инфекции.
Метод ультразвуковой флуометрии позволил оценить тонус микрососудов на основе амплитуды микрокровотока, обусловленной сокращением мышечной стенки сосуда и диаметром просвета сосудов. Показатель шунтирования можно оценить благодаря пространственной локализации воздействий нейрогенного механизма (мишенью являются артериолы и артериальный участок шунта) и миогенного механизма (мишень – прекапилляры).
Необходимо отметить сопоставимое воздействие как сорбции, так и ГДФ на периферический кровоток. При селективной гемосорбции улучшение тканевой перфузии наступает быстрее, однако после ГДФ лечебный эффект оказывался более стойким и сохранялся дольше, причем реакция микроциркуляторного русла опережала стабилизацию показателей системной гемодинамики.
Материал и методы
Представленные в работе данные подтверждают наличие выраженных расстройств тканевой перфузии при септическим шоке. Они характеризуются снижением показателей линейной и объемной скоростей кровотока соответственно тяжести состояния больных, что подтверждает положение о наличии артериоло-венулярного шунтирования при септическом шоке.
При анализе результатов лечения септического шока методами экстракорпоральной детоксикации выявлено, что одним из механизмов положительного воздействия эфферентного лечения является улучшение тканевой перфузии, которую можно использовать как в качестве критерия эффективности лечебного воздействия. Поэтому в оценке лечебного эффекта различных методов лечения, в том числе и экстракорпоральных, должна быть оценка показателей микроциркуляции объективными методами.
Читайте также:

