Эндокардит при системной красной волчанки
Обновлено: 17.04.2024
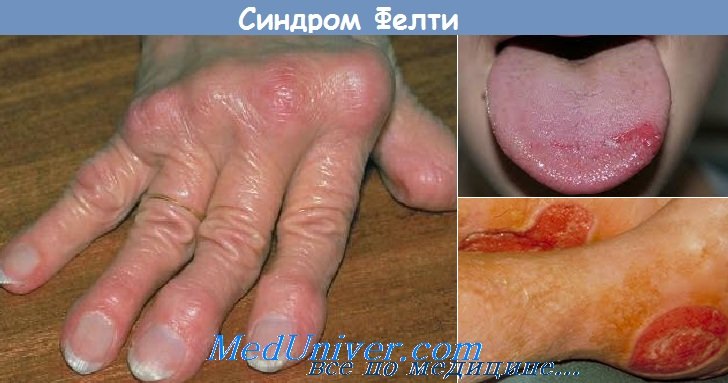
Болезнь Стилл—Шоффара. Синдром Фелти. Системная красная волчанка. Болезнь Либман—Сакса.
Клинические формы проявления ревматизма определяются двумя факторами:
1) вирулентностью возбудителя и
2) сопротивляемостью организма.
Альбертини (Albertini) наглядно представил эти соотношения в виде схемы, представленной на рисeyrt, нами расширенной.
Если вирулентность микроорганизма мала, а резистентность макроорганизма велика, то клиническая картина болезни соответствует ревматизму. При усилении вирулентности возбудителя и снижении сопротивляемости макроорганизма могут возникнуть различные родственные болезни, которые соответственно схеме, ведут, скажем, через синдромы Фелти и Стилл — Шоффара, болезнь Либман—Сакса и фибропластический эндокардит Леффлерак затяжному септическому эндокардиту. Если вирулентность достигает еще большей степени, а сопротивляемость организма продолжает снижаться, то налицо септическая бактериемия с гнойными метастазами, которые могут наблюдаться также и в суставах.
Болезнь Стилл—Шоффара (Still— Chauffard). Эта болезнь поражает главным образом детский, но также и юношеский возраст. От ревматизма ее отличает прежде всего всегда имеющееся увеличение селезенки и общее увеличение лимфатических узлов. Анемия, которая при ревматическом полиартрите часто неясно выражена, здесь особенно обращает на себя внимание; анемия гипохромная. Посевы крови стерильны. Полиартритические явления носят значительно менее острый воспалительный характер, чем при ревматизме1.
Синдром Фелти (Felty) наблюдается преимущественно у женщин, но бывает и у мужчин. Увеличение лимфатических узлов не столь выражено, как при болезни Стилла, но селезенка всегда увеличена. От болезни Стилл — Шоффара синдром Фелти отличается появлением выраженной лейкопении — до 2000 — с относительным лимфоцитозом. Лейкопения может периодически усиливаться до агранулоцитоза. Описаны случаи, когда изменения крови вместе с повышениями температуры и болями в суставах повторялись через каждые 3 недели, так что предполагалась связь с менструальным циклом.
Кожные пигментации при синдроме Фелти — третий симптом, говорящий против болезни Стилла, которая иногда протекает также и с летучими экзантемами.
Культуры крови остаются отрицательными.
Системная красная волчанка.
Болезнь Либман—Сакса (Libman — Sacks). Синдром Либман—Сакса приближается к картине затяжного септического эндокардита.
Поражаются почти исключительно женщины (88,9% из 163 больных, Dubois), преимущественно в молодом возрасте. Из 163 больных Dubois 30% заболели в возрасте между 10 и 19 годами, 27,6% — между 20 и 29 годами, 19% — между 30 и 39 годами, 10,4% — между 40 и 49 годами. После 50 лет болезнь наблюдалась только в 6% случаев. В противоположность синдромам Стилла и Фелти прогноз неблагоприятный, но при современных методах лечения (стероидные гормоны и синтетические противомалярийные препараты) наблюдались многолетние ремиссии. Длительность от нескольких месяцев до нескольких лет.
Суставные симптомы всегда незначительны, на первый план выступают явления со стороны почек характера очагового нефрита: гематурия, цилиндрурия, протеинурия без повышения артериального давления. Селезенка увеличена редко и незначительно. Почти всегда клинически определяется вовлечение серозных оболочек с выпотами (перикардит, плеврит и асцит).
Эндокардит клинически в большинстве случаев просматривается, так как патологоанатомически речь идет главным образом о поражении пристеночного эндокарда. Изменчивые шумы и нарушения ритма наблюдаются довольно часто.
Неопределенные желудочно-кишечные явления (понос, дуоденальный стаз и т. д.) наблюдаются приблизительно в 20% случаев (Brown и сотрудники). Явления со стороны легких разнообразны. Наряду с незначительными затемнениями, преимущественно в нижних отделах, наблюдаются картины милиарных высыпаний. Посевы крови всегда стерильны. В крови лейкопения, которая может доходить до агранулоцитоза, но в противоположность синдрому Ф е л т и не усиливается периодически, хотя и развивается приступообразно. РОЭ резко ускорена. Температура часто очень высокая. Около 1/3 случаев дает более или менее выраженную ложноположительную реакцию Вассермана (Dubois). Содержание гамма-глобулинов повышено.
Информация на сайте подлежит консультации лечащим врачом и не заменяет очной консультации с ним.
См. подробнее в пользовательском соглашении.
Эндокардит Леффлера – это редкая форма рестриктивной кардиомиопатии с поражением оболочек сердца в результате их инфильтрации эозинофилами. Симптомы включают лихорадку, потерю веса, кардиалгию, одышку и другие проявления сердечной недостаточности. В дальнейшем возникают признаки тромботических поражений печени, селезенки, легких. Диагностика производится посредством лабораторных анализов, исследования работы сердца (ЭКГ, ЭхоКГ), допплерографии и рентгенографии органов грудной клетки. Лечение предполагает устранение причин гиперэозинофильного синдрома, терапию сердечной недостаточности и профилактику тромбозов. В ряде случаев назначается хирургическое вмешательство.
МКБ-10
Общие сведения
Эндокардит Леффлера (эозинофильный эндокардит) был описан в 1936 году швейцарским врачом Вильгельмом Леффлером при наблюдении двух больных с быстро прогрессирующей сердечной недостаточностью. В настоящее время данная патология считается клиническим вариантом гиперэозинофильного синдрома с преимущественным поражением сердечно-сосудистой системы.
Чаще всего заболевание регистрируется у мужчин средней (30-40 лет) возрастной группы, но может возникать у лиц любого возраста и пола при высоком количестве эозинофилов в крови. Частота встречаемости выше у людей негроидной расы, жителей Юго-Восточной Азии и Южной Америки. Такое региональное распределение совпадает с распространенностью генетически обусловленного идиопатического гиперэозинофильного синдрома (ГЭС).

Причины
Главным этиологическим фактором заболевания выступает выраженное увеличение уровня эозинофилов в периферической крови. В результате создаются условия для инфильтрации данными клетками миокарда и эндокарда с развитием специфического воспаления. Достоверно выяснено, что именно появление эозинофилии предшествует возникновению сердечно-сосудистых нарушений. Причинами повышенного образования эозинофилов могут быть различные факторы и патологические состояния:
- Идиопатический гиперэозинофильный синдром. Редкое состояние неясной этиологии, проявляющееся пролиферацией эозинофильных гранулоцитов в костном мозге. Предположительно обусловлено мутациями – делецией 4-й хромосомы в области гена FIP1L1/PDGFRA, отвечающего за контроль гемопоэза. Характеризуется продолжительной выраженной эозинофилией, сопровождается высоким риском развития лейкоза.
- Аутоиммунные заболевания. Некоторые патологии (системная красная волчанка, ревматоидный артрит) могут осложняться появлением вторичных форм ГЭС. Последний провоцирует поражение оболочек сердца по типу эндокардита Леффлера.
- Аллергические и паразитарные болезни. При этих состояниях всегда наблюдается рост уровня эозинофилов. Крайне редко их количество достигает уровня, достаточного для инфильтрации миокарда или эндокарда. В основном такой вариант патологии обнаруживается у детей с высокой реактивностью иммунной системы.
- Онкологические заболевания. Эозинофильный лейкоз и другие опухолевые процессы кроветворной системы характеризуются быстрым активным делением слабо дифференцированных клеток. Их большое количество наряду с облегченным проникновением в ткани (в том числе сердца) способно провоцировать воспаление эндокарда.
Развитие эозинофильного эндокардита описано и при других состояниях, сопровождающихся повышенным образованием данных клеток: синдроме Глейча, поражениях селезенки, костного мозга. Установлено, что только наличия большого количества эозинофилов недостаточно для возникновения заболевания. Необходимым условием является их активация с выделением содержимого гранул – поражение сердца возникает при дегрануляции не менее 15% от объема циркулирующих клеток. Это объясняет то обстоятельство, почему в разных случаях при примерно равном количестве гранулоцитов выраженность эндокардита может сильно отличаться.
Патогенез
Ввиду редкости эндокардита Леффлера патогенез этого состояния изучен недостаточно. Понимание некоторых этапов заболевания строится не на клинических и исследовательских данных, а на общем видении иммунологических процессов. При наличии в крови большого количества активированных эозинофилов некоторые из них проникают в ткани сердца.
В процессе дегрануляции они выделяют катионные белки и стимуляторы воспаления, приводя к повреждению клеток. Кроме того, данные протеины обладают способностью запускать процесс коагуляции, тем самым провоцируя внутрисосудистое тромбообразование. Это обстоятельство в сочетании с изменением эндометрия ведет к развитию пристеночных тромбов внутри камер сердца. Их фрагменты в виде эмболов разносятся с током крови, вызывая инфаркты в почках, селезенке, головном мозге.
Отек, дистрофия структур эндокарда и миокарда способствуют разрастанию соединительной ткани, деформирующей хорды, а в дальнейшем и клапаны сердца. Все это, наряду с уменьшением количества кардиомиоцитов, приводит к снижению объема выброса, регургитации крови и возникновению сердечной недостаточности. Ослабленная работа сердца становится причиной многочисленных вторичных нарушений – отека легких, дистрофии печени, гипоксии. Без лечения больные эндокардитом Леффлера могут умереть от ХСН или осложнений, вызванных тромбоэмболией сосудов жизненно важных органов (легких, мозга, почек).
Симптомы эндокардита Леффлера
Клиническая картина патологии характеризуется выраженной стадийностью, длительность каждого этапа заболевания индивидуальна у разных больных и колеблется от 2-3 недель до нескольких месяцев. Первоначально у пациентов возникают жалобы на повышенную температуру тела, боли в области печени, потливость, слабость. Эти проявления соответствуют гиперэозинофильному синдрому и предшествуют поражению сердца. В некоторых случаях у больных имеются симптомы СКВ, ревматоидного артрита, бронхиальной астмы и других состояний, способных спровоцировать пролиферацию эозинофилов.
Осложнения
Эндокардит Леффлера способен вызывать ряд тяжелых осложнений, которые создают угрозу жизни больного. На начальных этапах заболевания, протекающих по типу кардита, может развиваться острая сердечная недостаточность из-за поражения миокарда и уменьшения его сократительной функции. Особенно опасна тромбоэмболия – значительная часть летальных исходов при эндокардите возникает по причине ишемических нарушений в органах (почках, головном мозге, структурах ЖКТ).
У лиц с идиопатическим ГЭС существует риск появления онкологической патологии – лейкоза или лимфомы. При отсутствии лечения и развитии терминальной фибротической стадии заболевания смерть наступает из-за полиорганной недостаточности в результате резко сниженной функции сердца.
Диагностика
Диагностика эндокардита Леффлера осуществляется врачом-кардиологом, который ввиду сложной этиологии состояния должен кооперироваться с иммунологами, ревматологами или онкологами. Важно доказать взаимосвязь между высоким уровнем эозинофилов и сердечно-сосудистыми симптомами, поскольку это влияет на лечение и прогноз. Клиническая картина и результаты диагностических исследований могут изменяться на различных этапах развития патологии, что также следует учитывать при определении заболевания. Для выявления и подтверждения наличия эозинофильного эндокардита используют следующие методики:
- Опрос и общий осмотр. На некротической стадии проявлениями заболевания выступают жалобы на боль в груди, сильное похудение, кашель, периодическое повышение температуры тела. При прогрессировании болезни осмотр позволяет обнаружить неврологические расстройства, увеличение размеров печени и селезенки, асцит. При аускультации сердца обнаруживаются нарушения ритма, сторонние шумы (например, шум митральной недостаточности).
- Рентгенография. У большинства больных на рентгенограмме грудной клетки определяется кардиомегалия, выраженность которой зависит от стадии заболевания. Застой в малом круге кровообращения на фоне ХСН проявляется увеличением тени корней легкого и усилением легочного рисунка.
- Ультразвуковые исследования.ЭхоКГ выявляет утолщение в области верхушки сердца, которое ассоциируется с фиброзным процессом или тромботическими отложениями. Исследование подтверждает утолщение и деформацию хорд, створок клапанов (главным образом, трикуспидального и митрального). Ультразвуковая допплерография сердца определяет нарушение гемодинамики в камерах органов – вентрикулоатриальную регургитацию крови.
- Электрокардиография. На ЭКГ имеются изменения ST-сегмента, расширение зубца Т и нерегулярный сердечный ритм. По мере прогрессирования кардиомегалии возникает отклонение электрической оси сердца влево. Нередко выявляется блокада одной из ножек пучка Гисса.
- Лабораторные анализы. Общий анализ крови подтверждает высокое количество эозинофилов и неспецифические признаки воспаления – увеличение СОЭ, лейкоцитоз. Иногда обнаруживаются слабо дифференцированные гранулоциты, что свидетельствует о неопластическом процессе в кроветворной системе. Биохимическое исследование крови свидетельствует о росте уровня АсАТ и белков плазмы.
В рамках дополнительной диагностики может назначаться обследование органов выделения, МРТ головного мозга, МСКТ сердца, легких, печени и брюшной полости. Они используются для выявления осложнений, обусловленных эндокардитом Леффлера, а также для определения возможных причин ГЭС. Дифференциальную диагностику проводят с другими воспалительными поражениями сердца (бактериальными или вирусными эндокардитами, миокардитами и перикардитами). Необходимо выяснить происхождение эозинофилии, что важно для дальнейшего лечения патологии.
Лечение эндокардита Леффлера
При подтвержденном диагнозе эозинофильного эндокардита назначается сложное многокомпонентное лечение. Оно не ограничивается только мероприятиями в сфере терапевтической кардиологии, важно устранить главный этиологический фактор – гиперэозинофильный синдром. Нужно минимизировать риск осложнений со стороны других органов, возникающих вследствие тромбоза и сердечной недостаточности. Каждое направление лечения подразумевает использование особых лекарственных средств и терапевтических мероприятий. Отдельным методом является хирургическое вмешательство, направленное на устранение последствий склеротических процессов в эндокарде. Все лечебные процедуры при эндокардите Леффлера разделяют на следующие группы:
- Устранение причины ГЭС. Относится к этиотропному лечению, поскольку направлено против главного фактора заболевания – эозинофилии крови. Идиопатические и неопластические варианты ГЭС лечат посредством использования иматиниба (ингибитор тирозинкиназы) и цитостатических средств. Высокий уровень эозинофилов аллергического или аутоиммунного генеза корригируют назначением кортикостероидов.
- Терапия сердечной недостаточности. Является базовым методом консервативного лечения. Применяют сердечные гликозиды, бета-адреноблокаторы, ингибиторы АПФ и другие традиционные средства. При развитии застойных явлений и отеков назначают петлевые диуретики при условии контроля за кислотно-щелочным и электролитным равновесием крови.
- Профилактика осложнений. Главной угрозой при данной патологии является тромбообразование с последующей эмболией сосудов различных органов. Для снижения скорости внутрисосудистого свертывания крови используют низкомолекулярный гепарин и иные антикоагулянты.
- Хирургическое лечение. В тяжелых случаях при возникновении рестриктивной ХСН показано оперативное вмешательство – эндокардэктомия (декортикация сердца). Кардиохирург удаляет фиброзные разрастания в камерах органа, производит пластику атриовентрикулярных клапанов и хорд. Эндокардэктомия считается очень сложной операцией с относительно высокой смертностью, выполняется лишь в специализированных кардиохирургических центрах.
Больному показана госпитализация в кардиологическое отделение и строгий постельный режим. Дополнительные лечебные мероприятия назначаются при наличии показаний. Тромбоэмболии некоторых органов (кишечника, селезенки, почек) могут быть основанием для проведения хирургических операций. При развитии ХСН требуется инфузионная терапия для устранения метаболического ацидоза и электролитных нарушений.
Прогноз и профилактика
Прогноз эндокардита Леффлера зависит от этиологии гиперэозинофильного синдрома и его реакции на лечебные мероприятия. При ГЭС невыясненного генеза перспективы лечения неопределенные, даже использование значительных доз кортикостероидов лишь несколько снижает уровень эозинофилов – при этом смертность от патологии остается высокой. Однако часто специалистам удается выяснить причины эозинофилии и разработать этиотропную терапию, что значительно повышает выживаемость больных.
Специфической профилактики не существует. При выявлении повышенного количества эозинофильных гранулоцитов рекомендуется производить периодический мониторинг картины крови. При сохранении такого состояния более месяца и исключении его очевидных причин (паразитарные и аллергические болезни) следует обратиться к гематологу.
2. Редкий клинический случай париетальный эндокардит Леффлера (эозинофильный эндомиокардит) в кардиологическом отделении республиканской клинической больницы/ Содномова Л.Б. Шпак И.А. Эрдынеева Э.Б.// Acta Biomedica Scientifica. - 2009.
Дискоидная красная волчанка – это хроническое воспалительное аутоиммунное заболевание кожи, развивающееся на фоне фотосенсибилизации (повышенной чувствительности к свету). Клинические проявления включают эритему, рубцовую атрофию кожи, фолликулярный гиперкератоз, выпадение волос, поражение ногтей. Диагноз ставится на основании симптоматики, анамнестических данных, наличия волчаночных клеток в крови, иммунологических тестов и гистологического исследования биоптата кожи. В качестве лечения применяются синтетические противомалярийные препараты, топические глюкокортикоиды, системные ретиноиды, солнцезащитные средства.
МКБ-10
Общие сведения
Дискоидная красная волчанка (ДКВ), или рубцующийся эритематоз – заболевание, относящееся к диффузным болезням соединительной ткани (коллагенозам). Данная патология является наиболее частой формой кожной красной волчанки. Средняя распространенность рубцующегося эритематоза составляет 1:100 000 человек. Чаще страдают представители европеоидной расы. Начало болезни приходится на молодой возраст (от 20 до 40 лет). Заболеваемости дискоидной волчанкой больше подвержены лица женского пола (соотношение с мужчинами 3:1). В редких случаях (1-5%) ДКВ может перейти в системную красную волчанку (СКВ).

Причины ДКВ
Эритематоз протекает по типу аутоиммунной реакции, точная причина возникновения которой неизвестна. Важное значение в развитии заболевания имеет наследственная предрасположенность, о чем свидетельствует большая встречаемость дискоидной волчанки среди близких родственников. В ходе исследований была установлена ассоциация ДКВ с антигенами тканевой совместимости HLA A1, A3, A10, A11, A18, B7, B8. Наиболее серьезным провоцирующим действием обладает ультрафиолетовое излучение.
К факторам, способствующим возникновению дискоидной волчанки, относятся постоянная травматизация кожи, хронические инфекции в организме, наличие аллергических болезней, прием лекарственных препаратов, повышающих чувствительность кожи к ультрафиолету (сульфаниламидов, тетрациклина, фторхинолонов, гризеофульвина, нейролептиков). В группе повышенного риска находятся люди, чей род деятельности связан с длительным пребыванием на открытом воздухе (работники сельскохозяйственной промышленности, строители, рыбаки). Также в группу риска входят лица с 1 фототипом кожи (кельтским) – это люди с нежной, тонкой, иногда веснушчатой кожей, имеющие светлый или рыжий цвет волос.
Патогенез
При дискоидной красной волчанке наблюдается патогенетическое сходство с СКВ, однако патологические реакции ограничиваются кожными покровами. В основе заболевания лежит аутоиммунное воспаление. Под действием ультрафиолетовых лучей в совокупности с другими провоцирующими факторами в клетках кожи нарушаются процессы метилирования ДНК (механизма регуляции транскрипции генов). Это приводит к повышению экспрессии белков, индуцирующих апоптоз (запрограммированную клеточную гибель) - p53, Fas и Fas-лиганда и гамма-интерферона.
Т- и В-лимфоциты стимулируют синтез цитокинов и антител к компонентам клеточных ядер (нуклеиновым кислотам, нуклеосомам). Образующиеся иммунные комплексы оседают на эндотелии сосудов, вызывая их повреждение. Выработку аутоантител у генетически предрасположенных лиц также способны вызывать антигены некоторых вирусов (Эпштейна-Барр, цитомегаловирус, парвовирус 19), имеющие сходную молекулярную структуру с белками клеточных мембран. Дополнительным повреждающим агентом выступает индукция свободнорадикального окисления липидов. Результатом этих процессов является массивное воспаление и разрушение клеток кожи.
Классификация
Традиционно дискоидную красную волчанку подразделяют на очаговую и диссеминированную (распространенную) – эти формы различаются количеством очагов поражения кожи и их локализацией. Также при диссеминированной форме отмечается наличие общей симптоматики (слабости, повышения температуры тела, болей в суставах) и высокого риска трансформации в СКВ. Помимо перечисленных форм, в ревматологии выделяют следующие виды ДКВ:
Симптомы ДКВ
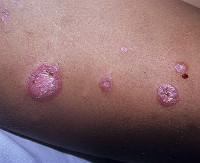
Дискоидная красная волчанка характеризуется хроническим течением, рецидивы возникают в основном летом или весной, когда длина солнечного дня максимальна. Чаще всего поражаются участки тела, подвергающиеся длительному солнечному излучению. Тремя наиболее типичными симптомами считаются эритема, фолликулярный гиперкератоз и рубцовая атрофия кожи.
При локализации очагов на волосистой части головы практически всегда возникает алопеция, которая оставляет после себя рубцы. При диссеминированной дискоидной волчанке очаги располагаются на груди, спине, локтях, ладонях, подошвах, обычно не имеют признаков шелушения и атрофии. Иногда поражаются ногтевые пластины. Ногти приобретают желтый цвет, становятся ломкими, деформируются. Очень редко в патологический процесс вовлекается слизистая оболочка полости рта. Очаги склонны к эрозированию, что вызывает жжение и боли во время приема пищи.
Осложнения
Серьезные осложнения дискоидной красной волчанки возникают редко. Иногда развивается вторичный гландулярный хейлит (воспаление мелких слюнных желез красной каймы губ). Диссеминированная форма ДКВ в некоторых случаях переходит в СКВ – тяжелое системное заболевание соединительной ткани, поражающее суставы и практически все внутренние органы (сердце, почки, легкие и центральную нервную систему). СКВ характеризуется упорным течением, трудно поддается терапии и имеет высокий риск летального исхода. Также может произойти трансформации стойких очагов дискоидной волчанки в плоскоклеточный рак кожи (сквамозно-клеточную карциному).
Диагностика
Пациентов с данной патологией курируют врачи ревматологи и дерматологи. При постановке диагноза дискоидной волчанки учитывается фототип кожи. На первичной консультации уточняется профессия пациента, прием фотосенсибилизирующих лекарственных средств, наличие инфекционных или аллергических заболеваний, близких родственников с ДКВ. Для диагностики проводят следующие методы исследования:
- Общие лабораторные тесты. В клиническом анализе крови отмечается увеличение скорости оседания эритроцитов, снижение уровня лейкоцитов, тромбоцитов, при инфекционных и аллергических патологиях - высокий уровень нейтрофилов и эозинофилов. При диссеминированной ДКВ возможен ложноположительный результат анализа на сифилис.
- Специальные ревматологические тесты. Примерно у 40% пациентов ДКВ обнаруживаются антинуклеарные антитела (ANA) и антитела к нуклеопротеинам (анти-Ro/SS-A, анти-La/SS-B). Волчаночные (LE) клетки встречаются у 5-7% пациентов. При реакции иммунной флюоресценции выявляются отложения иммуноглобулинов (IgG/IgM) и комплемента (положительный тест волчаночной полоски). Последний тест может быть положительным и при других заболеваниях, поэтому не является специфичным.
- Гистологическое исследование биоптата кожи. Биопсия кожи - наиболее достоверный метод для постановки диагноза. Характерны следующие признаки – атрофия эпидермиса, утолщение рогового слоя эпидермиса в устьях волосяных фолликулов, разрушение волокон коллагена, отек дермы, отложения в ней гиалина, периваскулярный лимфоцитарный инфильтрат.
Важно отличать диссеминированную форму ДКВ от системной красной волчанки, требующей более агрессивной терапии. Помощь в диагностике СКВ оказывает определение антител к двуспиральной ДНК и экстрагируемым ядерным ангигенам в крови пациента. Также дискоидную красную волчанку дифференцируют с другими формами кожной волчанки (острая, подострая), ревматологическими (дерматомиозит), дерматологическими заболеваниями (красный плоский лишай, псориаз, себорейный дерматит, экзема, фотодерматозы, эозинофильная гранулема лица, ангиолюпоид Брока-Потрие).
Лечение ДКВ
В большинстве случаев пациенты проходят лечение амбулаторно, но при тяжелом течении может потребоваться госпитализация в отделение ревматологии или дерматологии. Важным моментом является исключение приема фотосенсибилизирующих медикаментов и лечение сопутствующих аллергических или инфекционных заболеваний. Рекомендуется носить закрытую одежду, применять солнцезащитные крема или мази, содержащие вещества, которые задерживают ультрафиолетовые лучи (мексорил, двуокись титана, оксид цинка).
Основное патогенетическое лечение включает антималярийные аминохинолиновые препараты (Гидроксихлорохин), топические глюкокортикостероиды (тГКС), производные витамина А - ретиноиды (Изотретиноин, Ацитретин). Ввиду частого развития ретинопатий на фоне приема гидроксихлорохина обязателен регулярный осмотр офтальмолога. В зависимости от локализации дискоидных очагов применяются тГКС разной активности. При расположении очагов только на коже лица используют тГКС слабой и средней степени активности (Гидрокортизона ацетат, Метилпреднизолон), при поражении кожи конечностей и туловища рекомендуются тГКС сильной активности (Бетаметазон, Триамцинолон). Если дискоидные очаги имеются на ладонях и подошвах, назначаются тГКС сверхвысокой активности (Клобетазон).
Для подавления свободнорадикального повреждения клеток кожи эффективны антиоксиданты (альфа-токоферол). При неэффективности стандартного лечения прибегают к средствам, обладающим выраженным иммуносупрессивным действием – Такролимус, Метотрексат, Азатиоприн.
Прогноз и профилактика
В подавляющем большинстве случаев дискоидная волчанка имеет благоприятное течение. При грамотном подборе терапии и соблюдении всех рекомендаций наступает стойкая ремиссия. Основную проблему представляет трансформация ДКВ в более тяжелые заболевания, имеющие достаточно высокий процент летальности – СКВ и плоскоклеточную карциному. Профилактика рецидивов дискоидной волчанки заключается в ограничении времени пребывания на солнце, ношении закрытой одежды, применении солнцезащитных препаратов, исключении приема лекарств, повышающих чувствительность кожных покровов к ультрафиолетовому излучению.
1. Федеральные клинические рекомендации. Дерматовенерология 2015: Болезни кожи. Инфекции, передаваемые половым путем. 2016.
3. Федеральные клинические рекомендации по ведению больных с поражениями кожи при красной волчанке/ Самцов А.В., Чикин В.В. - 2015.
Синдром Либмана-Сакса (Libman-Sacks) - синонимы, авторы, клиника
Синонимы синдрома Либмана-Сакса. Эндокардит Libman. Эндокардит Libman—Sacks. Бородавчатый атипичный эндокардит (Libman). Абактериальный эндокардит. Висцеральная форма красной волчанки. S. Kaposi—Libman—Sacks.
Определение синдрома Либмана-Сакса. Атипичный абак-териальный бородавчатый эндокардит, представляющий собой, по современным воззрениям, висцеральное проявление красной волчанки.
Авторы. Libman Emanuel — американский врач, Нью-Йорк, 1872—1946. Sacks В. — современный американский врач, Нью-Йорк. Kaposi-Kohn Moritz — венгерский дерматолог, 1837—1902. Еще в 1872 г. Kaposi характеризовал красную волчанку как системное заболевание. Заслугой Libman и Sacks является патологоанатомическое изучение поражений сердца при этом заболевании (1923).
Симптоматология синдрома Либмана-Сакса:
1. Общие проявления: высокая температура, плохое общее состояние.
2. Атипичный абактериальный эндокардит, особенно поражающий правые отделы сердца, часто без существенных . клинических симптомов.
3. Склонность к развитию перикардита, плеврита, перитонита или полисерозита.
4. Частое развитие артериита малых и среднего калибра сосудов.
5. Склонность к скоропроходящим артральгиям и полиартритам, миальгиям или миозиту. 6. Проявления очагового нефрита (альбуминурия, умеренная гематурия, отсутствие гипертонии, отсутствие задержки мочевых шлаков).
7. Увеличение селезенки, печени и лимфатических узлов (может отсутствовать).
8. Частое наличие высыпаний красной волчанки на коже (лицо, кисти) и слизистых оболочках.
9. Могут развиться симптомы поражения центральной нервной системы: эпилептиформные припадки, менингеальные явления, параличи и т. д.
10. Морфология крови: гипохромная анемия, лейкопения (не обязательный признак); склонность к петехиальным кровоизлияниям в кожу.
11. Резко ускоренная СОЭ.
12. Отрицательные культуры крови (дифференциально-диагностический признак).
13. Частая гипергаммаглобулинемия (фактор Haserick).
14. Иногда появление клеток красной волчанки в мазках из костного мозга.
15. Иногда изменения глазного дна.
16. Приступообразное течение заболевания (недели, месяцы, годы); возможны ремиссии. Прогноз сомнительный. 17. Чаще заболевают молодые женщины и девушки (дифференциально-диагностический признак).
Существует связь с дерматомиозитом (S. Wagner—Unverricht), узелковым периартериитом (S. Kussmaul — Meier), ревматическим артритом и комплексом гемолитических анемий.
Дифференциальный диагноз. Подострый бактериальный эндокардит. Ревматическая инфекция. Туберкулезная волчанка. Синдром карциноида. S. Prasad—Koza (см.). S. Beam—Kunkel (см.).
Редактор: Искандер Милевски. Дата обновления публикации: 18.3.2021
Читайте также:

