Энтеробактерии кишечные инфекции микробиология
Обновлено: 25.04.2024
Инфекции вызванные энтеробактериями. Механизмы развития
Энтеробактерии (кишечные бактерии) — представители большого семейства (более двадцати родов и свыше ста видов) факультативных грамотрицательных палочковидных анаэробов, хорошо растущих на питательных средах, восстанавливающих нитраты и ферментирующих глюкозу. Способны вызывать множество различных заболеваний.
Энтеробактерии распространены повсеместно. Они составляют основу нормальной микрофлоры организма человека и животных; в большом количестве их обнаруживают в почве и воде. Заражение происходит при контакте с животными, другими людьми и контаминированными предметами. Очень часто заболевания вызывают условно-патогенные представители нормальной микрофлоры человека.
Численность энтеробактерии зависит от их локализации в организме, его состояния (здоровый или больной) и проводимой антимикробной терапии.
Патогенез инфекции вызванной энтеробактериями
Капсулы энтеробактреий. Многие микроорганизмы обладают полисахаридной капсулой (например, бактерии рода Klebsiella, Escherichia coli и Salmonella typhi). Основной фактор вирулентности Salmonella typhi — капсульный Vi-антиген, поэтому для профилактики тифа применяют вакцину, содержащую его. Чаше всего менингит и септицемию у новорождённых вызывает Escherichia coli K1.
Существуют определённые биохимические и структурные сходства между Escherichia coli К1, N. meningitidis группы В и антигенами центральной нервной системы человека, что даёт некоторое преимущество вышеперечисленным микроорганизмам.
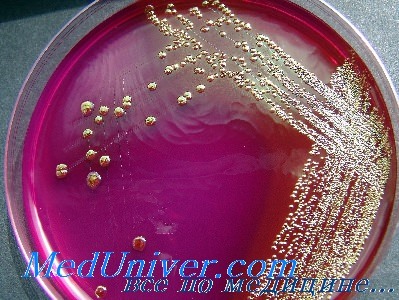
Энтеробактерии - Escherichia coli
Токсины энтеробактерий. Энтеротоксигенные штаммы Escherichia coli (ЕТЕС). Продуцируют термолабильный (LT) и термостабильный (ST) токсины, которые воздействуют на энтероциты, усиливая секрецию жидкости, вызывая диарею. Термолабильный токсин на 70% гомологичен по структуре с холерным экзотоксином. Так же как и последний, он разрушается при высокой температуре и способствует увеличению содержания циклической формы аденозинмонофосфата (цАМФ) в клетках кишечника.
Стабильный при высокой температуре, ST-токсин усиливает синтез циклической формы гуанилмонофосфата. Штаммы Escherichia coli, продуцирующие эти токсины, вызывают диарею путешественников (заболевание, при котором в течение непродолжительного времени возникает диарея).
Энтероагрегативные штаммы Escherichia coli (EAggEC). Некоторые штаммы Escherichia coli при прикреплении к энтероцитам вызывают их агрегацию. Они не поражают сами клетки, но вызывают хроническую диарею. Возбудители покрыты волокнистыми (фибриллярными) компонентами, которые предположительно обеспечивают их способность к адгезии. Некоторые штаммы продуцируют ST-подобный или гемолизинподобный токсины.
Энтерогеморрагические штаммы Escherichia coli (EHEC). Название штаммов связано с воздействием токсина возбудителей на клетки почек обезьян в тестах in vitro. Вызываемая ими геморрагическая диарея обычно сопровождается гемолизом и острой почечной недостаточностью (гемолитико-уремический синдром). Эти штаммы продуцируют вероток-син. Энтерогеморрагические штаммы Escherichia coli — представители нормальной микрофлоры кишечника крупного рогатого скота. Заражение человека происходит при несоблюдении санитарно-гигиенических норм во время работы на скотобойнях и предприятиях пищевой промышленности.
Токсин, подобный веротоксину Шига (Shiga toxin), — основной фактор вирулентности Shigella dysenteriae.
Обмен генетической информацией. Энтеробактерии могут получать генетическую информацию от других микроорганизмов посредством транспозонов, интегронов или плазмид. При этом гены, кодирующие устойчивость к антибиотикам, распространяются от одной бактерии к другой. Кроме того, с помощью обмена генетической информацией энтеробактерии могут приобретать различные факторы патогенности. При получении возбудителем ряда связанных между собой генов возникает так называемый островок патогенности.
Именно благодаря этой способности некоторые штаммы рода Salmonella могут поражать клетки кишечника. В условиях лечебных учреждений обычно выживают антибиотико-резистентные штаммы. В отделениях интенсивной терапии некоторых больниц периодически регистрируют вспышки инфекций, вызванных мультирезистентными штаммами Klebsiella pneumoniae.
Редактор: Искандер Милевски. Дата обновления публикации: 18.3.2021

Энтеробактерии (лат. enterobacteriaceae) — семейство грамотрицательных (как и другие протеобактерии) палочкообразные (бациллы), споронеобразующие бактерии, длиной 1-5 мкм, со жгутиками для передвижения. Эти бактерии — факультативные анаэробы, расщепляют углеводы с образованием муравьиной кислоты и других конечных продуктов формиатного брожения. Некоторые из них могут разлагать лактозу.
Множество представителей семейства являются частью микрофлоры кишечника человека и животных. Они представляют большое число нормальной микрофлоры человеческого организма и значительное количество патогенных микробов: сальмонелла, кишечная палочка, чумная палочка и др. Энтеробактерии определяют в различных отделах желудочно-кишечного тракта здорового человека: в тощей кишке – от 0 до 103 КОЕ/мл, в подвздошной — от 10 2 до 10 6 КОЕ/мл. В норме в составе факультативной микрофлоры кишечника они не должны превышать количество 10 4 КОЕ/г.
Другая часть этих бактерий обнаруживается в воде и почве или паразитирует на различных растениях и животных. Хорошо изучена кишечная палочка — модельный организм, используемый в молекулярной биологии и генетике, в связи с изученностью её генетики и биохимии.
Энтеробактерии в воде и почве месяцами остаются жизнеспособными, но за несколько минут гибнут от дезинфектантов и при очень высоких температурах через 1 час.
Эти бактерии вырабатывают сахаролитические, протеолитические и др. ферменты, определение которых имеет таксонометрическое значение. Образуют индол, а глюкозу, лактозу, маннит ферментируют до кислоты и газа.
Факторами патогенности являются:
- эндотоксин, который освобождается после разрушения микробных клеток и адгезины,
- цитотоксин,
- экзотоксин.
Бактерии могут проникать в макрофаги и размножаться в них. Патологический процесс усугубляется на фоне снижения активности фагоцитоза, падения барьерной функции тканей. Снижение в кишечнике полезной нормофлоры и нарушение колонизационной и защитной функции может приводить к проникновению в лимфу и кровь. Коли-бактериозы возникают при снижении количества полезной микрофлоры кишечника и иммунитета. После перенесённого заболевания невосприимчивость не формируется.
Какие заболевания вызывают энтеробактерии?

энтреробактерии e.coli
Группа энтеробактерий включающая: сальмонеллы, шигеллы, эшерихии, клебсиеллы, собственно энтеробактер, серрации, протей, морганеллы, провиденции и иерсинии в норме обитают в желудочно-кишечном тракте человека, но при снижении защитных свойств слизистой кишечника, могут вызывать инфекции желудочно-кишечного тракта или других органов.
Энтеробактерии — представители родов citrobacier, ewardsiella, enterobacter, escherichia, hafnia, klebsiella, proteus, providencia, salmonella, serratia, yersinia вызывают инфекции мочеполовой системы (в том числе циститы, пиелонефриты, цервициты и т.п.). До 80% бактерий, обнаруживаемых в моче — энтеробактерии.
Энтеробактерии становятся причиной различных заболеваний человека. Условно – патогенные бактерии вызывают гнойно-воспалительные процессы различной локализации: как эндогенные процессы — развиваются инфекции мочевыводящих путей (уретрит, цистит, пиелонефрит), половой системы (вагинит, трихомиоз, цервицит), дыхательных путей (пневмония), желудочно-кишечного тракта (холециститы, сальмонеллез, дизентерия, чума) и другие, так называемые коли-бактериозы, а как экзогенные – нагноение ран. Разные формы ОКЗ – острых кишечных заболеваний обусловлены патогенным действием различных энтеробактерий и чем агрессивнее токсины бактерий, тем тяжелее состояние, особенно у маленьких детей.
Escherichia coli – кишечная палочка в норме определяется в желудочно-кишечном тракте и синтезирует секреторные иммуноглобулины и колицины. Они тормозят рост некоторых патогенных энтеробактерий и препятствуют проникновению их в слизистую оболочку стенки кишечника. E. сoli участвует синтезе витамина К (свертываемость). Некоторые патогенные штаммы кишечной палочки могут поражать слизистую кишечника, что проявляется кровавым водянистым поносом или диареей путешественников.
У детей диарея, вызываемая патогенной энтерогеморрагической кишечной палочкой, может осложняться гемолитико-уремическим синдромом и почечной недостаточностью. Эта бактерия может поражать кровь, желчный пузырь, легкие, мочевыводящие пути и кожу. У новорожденных детей, особенно недоношенных, кишечная палочка может стать патогенным возбудителем бактериемии и менингита.
Инфекции, обусловленные клебсиеллами (Klebsiella), энтеробактериями (Enterobacteriaceae) и серрациями (Serratia), обычно встречаются в больницах, чаще при снижении способности бороться против инфекций. Эти бактерии также часто поражают мочевыводящие, половые органы. Пневмония, вызванная клебсиеллами, наиболее распространена у больных сахарным диабетом и у злоупотребляющих алкоголем и имеет часто тяжелое течение.
Симптоматика инфекций, вызываемых энтеробактериями.
Симптомы инфекционного заболевания могут быть различны, в зависимости от места развития воспалительного процесса, однако все больные жалуются на общую слабость, повышение температуры, проявления интоксикации и боли в месте заболевшего органа. Для определения патогенных энтеробактерий обязательно нужно сдать анализы – кровь, мочу, мокроту, мазки или кал, в зависимости от локализации воспалительного процесса, пройти до обследование, для выявления функциональных нарушений.
Важно соблюдать правила личной гигиены, следить за качеством, чистотой овощей-фруктов, питаться, учитывая индивидуальные особенности, избегать контакта с инфекционными больными и поддерживать свой иммунитет в норме.
Как быстро восстановиться после инфекции?
Восстановление и сохранение достаточного количества полезной нормофлоры кишечника – лакто- и бифидобактерий, способствует защите слизистой кишечника от проникновения патогенных бактерий и их токсинов в кровь и лимфу, выведению токсинов, созданию среды, в которой патогенные микроорганизмы не могут продолжать свою жизнедеятельность и выводятся из организма человека. Важно, что продукты жизнедеятельности полезных бактерий помогают иммунитету сохранять активность в борьбе с вредными бактериями.
Синбиотический биокомплекс Нормофлорины – содержащий живые активные лакто- и бифидобактерии и их метаболиты с противовоспалительным, антисептическим, иммуногенным и питательным действием на слизистые за многие годы зарекомендовал себя, как активный помощник и борец против патогенных бактерий для малышей и взрослых, беременных и больных с различными заболеваниями. Достаточно быстро при употреблении Нормофлоринов снимается интоксикация и восстанавливается функция кишечника, общее самочувствие.
Рекомендуется: как можно раньше начать принимать Нормофлорины в возрастных дозировках – Л – за 10-15 мин до еды утром (+ обед при запорах), Д – обед или вечер за 20 мин до еды, Б – на ночь или в микроклизме. Длительность приема 3-4 недели, до полного восстановления функции кишечника и улучшения общего самочувствия. Желательно 10-14 дней натощак принимать сорбенты – для выведения токсинов – зостерин или пекто, они уменьшают гнилостные, бродильные процессы, повышенное газообразование, улучшают работу кишечника.
Важно закрепить эффект восстановления микрофлоры, улучшить работу поджелудочной железы, печени, кишечника, иммунитет – для этого хорошо далее в течение месяца использовать функциональное питание – Гармония жизни. В её составе также содержатся живые полезные лакто- и бифидобактерии, их метаболиты и пектин. Вкусно, полезно и эффективно!

В 1885 году английский ветеринар Дениел Салмон обнаружил сальмонеллу, а в 1887 году Киёси Сига (первоначально его фамилия в транскрипции читали как Шига) обнаружил возбудителя дизентерии — шигеллу, одновременно с русским исследователем Алексеем Григорьевым.
Внешний вид под микроскопом
Энтеробактерии — не окрашивающиеся по методу Грама палочковидные бактерии, не образующие спор и скоплений в виде цепочек. Многие роды имеют жгутики для передвижения. Форма и размеры клеток варьируют: они могут быть прямыми и изогнутыми, длиной от 1 до 5 мкм.
Где обитает
В человеческом организме энтеробактерии, в частности, Эшерихия коли (кишечная палочка) населяют кишечник человека, животных и птиц. Для патогенных микроорганизмов этого класса местом обитания могут стать легкие и дыхательные пути, суставы, носовые и лобные пазухи, мочевой пузырь, почки и даже лимфоузлы.
Классификация
Царство
Bacteria
Тип
Proteobacteria
Класс
Gammaproteobacteria
Порядок
Enterobacteriales
Семейство
Enterobacteriaceae
Свойства
Энтеробактерии — грамотрицательные палочки, относящиеся к факультативным анаэробам. Для биохимического определения часто используется способность к усваиванию сахаров — глюкозы и лактозы.
В процессе расщепления глюкозы они могут образовывать углекислый газ, что также является одним из признаков, помогающих в определении не только рода, но и группы. Например, патогенные эшерихии в большинстве случаев не выделяют СО2, так же, как и шигеллы. Бактерии рода Протей и Сальмонелла продуцируют сероводород. Некоторые энтеробактерии продуцируют индол.
Оптимальная температура для развития энтеробактерий — 32-37°С. В то же время иерсинии, например, могут размножаться и при +5°С.
Функции
Эшерихия коли, то есть кишечная палочка, имеет множество серогрупп, часть из которых патогенна, другая является нормальным представителем флоры кишечника, преимущественно толстой кишки. Здесь они являются одним из компонентов иммунной системы, поскольку образуют налет на слизистой, препятствующий колонизации этой части пищеварительного тракта патогенными бактериями. Кроме того, кишечная палочка продуцирует витамины группы К.
Заболевания
Самые распространенные болезни — энтерит, колит, дизентерия, острое пищевое отравление Реже — воспаления различных органов, гнойные инфекции кожи и слизистых. Иерсиния пестис вызывает бубонную и легочную чуму.
Лечение

Сегодня мы закончим разговор о микроорганизмах из семейства Enterobacteriaceae, которое, как мы помним, является одним из самых проблематичных источников внутрибольничных инфекций, потому что возбудители умеют делиться и передавать в рамках почти всего семейства свои механизмы резистентности, и это при том, что изначально почти каждый представитель имеет природную устойчивость к целым классам антибиотиков.
Материалы предназначены исключительно для врачей и специалистов с высшим медицинским образованием. Статьи носят информационно-образовательный характер. Самолечение и самодиагностика крайне опасны для здоровья. Автор статей не дает медицинских консультаций: клинический фармаколог — это врач только и исключительно для врачей.
Автор: врач – клинический фармаколог Трубачева Е.С.
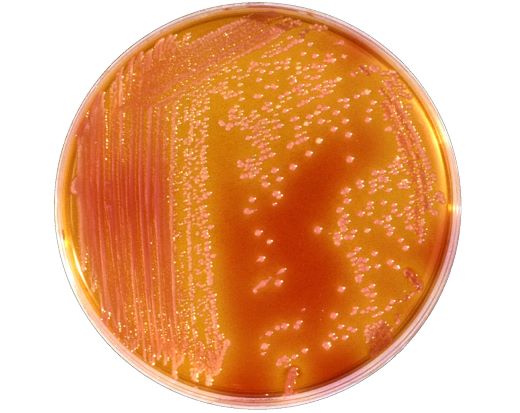
Сегодня мы закончим разговор о микроорганизмах из семейства Enterobacteriaceae, которое, как мы помним, является одним из самых проблематичных источников внутрибольничных инфекций, потому что возбудители умеют делиться и передавать в рамках почти всего семейства свои механизмы резистентности, и это при том, что изначально почти каждый представитель имеет природную устойчивость к целым классам антибиотиков.
Героями сегодняшнего разговора станут энтеробактеры, серрации, морганеллы. Конечно, есть и другие представители и, возможно, в постковид они начнут встречаться намного чаще, но пока нам в рамках Азбуки достаточно вышеперечисленных плюс кишечные палки и клебсиеллы, о которых мы говорили ранее.
Enterobacter spp.
Микробиологические аспекты
Род энтеробактера включает несколько видов, но наиболее клинически значимыми из них являются:
Очень важно помнить, что энтеробактеры проявляют природную устойчивость к большому спектру антибиотиков, таким как бета-лактамы, к которым они продуцируют хромосомные AmpC бета-лактамазы, плазмидные бета-лактамазы расширенного спектра, а также карбапенемазы. Так как клинически значимые представители Enterobacter spp. обитают в желудочно-кишечном тракте человека, то основным источником инфицирования для пациента становится медицинский персонал, который просто по факту своей ежедневной работы в больнице с антибиотиками является резервуаром всевозможных антибиотикорезистентностей.
Клинически значимые аспекты
Enterobacter spp. является причиной:
- Инфекций мочевыводящих путей: катетер – или инструментально-ассоциированных (как результат эндоскопических манипуляций контаминированным инструментарием).
- Внутрибольничных пневмоний, в том числе вентилятор-ассоциированных.
- Инфекций кожи и мягких тканей, таких как раневые инфекции, инфицирование пролежней, ожоговые инфекции и послеоперационные инфекции. Кроме того в случае полимикробного характера инфицирования пролежней возможно развитие сепсиса как исхода раневой инфекции.
- Инфекций кровотока – катетер – и инструмент-ассоциированные.
- Инфекций центральной нервной системы — менингиты, чаще всего внутрибольничные, как следствие нейрохирургических вмешательств.
- Неонатальных инфекций, таких как некротический энтероколит, сепсис и менингит.
Чем лечить?
Ответ будет традиционным – лучше вообще не инфицировать, тогда не придется ломать голову, чем все это лечить. В основе терапии лежит обязательное микробиологическое исследование с определением антибиотикочувствительности.
В случае выявления представителей Enterobacter spp. при лечении тяжелых инфекций предпочтение следует отдавать комбинированной терапии, и самыми подходящими будут пиперациллин-тазобактам в комбинации с аминогликозидами или фторхинолонами. А для преодоления резистентности, вызванной бета-лактамазами расширенного спектра, можно использовать карбопенемы.
Для лечения инфекций мочевыводящих путей самым первым и наиважнейшим является удаление мочевого катетера до момента прекращения пиурии. Далее лечим либо исходя из профиля антибиотикограммы, либо ципрофлоксацином в правильно подобранной дозе, либо, как было указано выше, рассматриваем назначение нитрофуранов и фосфомицина.
Serratia spp.
Клинические аспекты
Что вызывает?
- Катетер-ассоциированные инфекции и как их исход – сепсис.
- Инфекции мочевыводящих путей как следствие медицинских манипуляций необработанным инструментом.
- Раневые инфекции в послеоперационном периоде.
- Нозокомиальные пневмонии как следствие интубации.
- Септические артриты.
- Конъюнктивиты и кератиты.
- И редко вызывали остеомиелиты и эндокардиты
Терапевтические аспекты
В первую очередь про серрацию надо узнать, а значит, необходимо микробиологическое исследование. Во-вторую, вспомнить о природной устойчивости. В-третью, держать в уме то, что очень часто цефалоспорины третьего и четвертого поколения тоже не будут работать, так как посредством плазмид получают устойчивость от родственников по семейству Enterobacteriaceae, например, от родной сестры – клебсиеллы. Точно таким же образом серрация может оказаться устойчивой и к карбопенемам. К фторхинолонам резистентность так же уже давно описана.
Так чем лечить?
Лучше вообще не заражать – потому что если бак. лаборатория дает серрацию, то ниоткуда кроме как с наших рук она появиться не может, так как ни ходить, ни летать сия зверюшка до сих пор не научилась.
В случае развития тяжелых инфекций – сепсиса, вентилятор-ассоциированной пневмонии и т. п., и только при документированной чувствительности, препаратами выбора могут быть цефепим или меропенем, или ципрофлоксацин в вену в стандартных дозировках. Если чувствительность утеряна, то зовем клинического фармаколога, а если такового нет, то смотрим в сторону амикацина, пиперациллина-тазобактама и азтреонама, только помним об их побочных эффектах. Курс лечения соблюдать жизненно необходимо, чтобы зверюшка еще куда-нибудь не мутировала и новыми механизмами защиты не обзавелась. Обычно речь идет о 10-14 днях (но так как польза превышает вред, то нефротоксичность аминогликозидов со временем отступит, а ототоксичность – тут уж как повезет).
Инфекции мочеполового тракта лечим так же с учетом чувствительности, и если таковая располагает, то препаратом выбора становятся фторхинолоны, либо комбинация двух антибиотиков, например фторхинолон с карбапенемом или бета-лактам с аминогликозидом.
Эндокардиты с остеомиелитами бывают хоть и редко, но крайне метко, а потому снова сначала исследуем чувствительность, потом индивидуально в каждом случае подбираем антибиотики (а лучше зовем клинического фармаколога, пусть он мучается). И снова крайне важно соблюдение сроков лечения, для эндокардита это порядка четырех, а то и шести недель внутривенной антибактериальной терапии, а для остеомиелита не менее двух недель. Почему нельзя меньше? Потому что последует мутация и новый рецидив, а антибиотиков просто может не хватить, ибо, как и сестра-клебсиелла, серрация тоже умеет в панрезистентность.
В заключении хочется повторить, что и в этом случае проще помыть руки, чем разгребать последствия инфицирования серрацией. Мытье рук и проще, и дешевле, и, что самое главное, спокойнее.
Morganella spp.
Морганеллы будут последними представителями семейства Enterobacteriaceae, которых мы обсуждаем в рамках нашей Азбуки. Если кому-то станет интересно покопаться дальше, то к их услугам всегда будет четырехтомник по медицинской микробиологии под редакцией Лабинской, конкретно второй и третий том, в которых все очень подробно расписано, правда, чтение это для неподготовленного человека будет довольно сложным. Но вернемся к нашей морганелле.
Микробиологические аспекты
Морганелла существует только одна – M.morganii, но имеет два подвида – M.morganii и M.sibonii, которые отличаются только по ферментации треалозы, и никакого клинического значения данное отличие не имеет.
Конечно, и морганелла умеет в природную устойчивость к антибиотикам, а именно к пенициллинам, цефалоспоринам первого и второго поколения, макролидам и ко-тримоксазолу. При этом сохраняет высочайшую чувствительность к аминогликозидам, пиперациллину, цефалоспоринам третьего и четвертого поколения, фторхинолонам и карбопенемам. То есть данную зверюшку есть чем победить.
Клинические аспекты
Морганелла является представителем нормальной микрофлоры человека и самостоятельно крайне редко что-то вызывает. Этим крайне редким являются инфекции мочевыводящих путей, чему способствуют крайне пожилой возраст, длительная госпитализация, мочевой катетер и иммунодефицит любой этиологии.
В плане приобретенной антибиотикорезистентности морганелла обзавелась факторами устойчивости к фторхинолонам, что и понятно, учитывая какие именно заболевания она вызывает и чем их чаще всего лечат.
Что еще может вызывать?
- Крайне редко – сепсис, как исход инфекции мочевыводящих путей.
- Раневую хирургическую инфекцию.
- Септический артрит.
- Неонатальный сепсис и хореоамнионит.
- Менингит.
- Перикардит.
Но стоит иметь в виду, что данные ситуации крайне редки, и стоит изначально подумать не об этом возбудителе, а о том, какой за ним может прятаться в виду контаминации материала, и лучше бы все еще раз пересеять и перепроверить.
Терапевтические аспекты
Если результат микробиологического исследования сомнений не вызывает и вы убеждены, что имеете дело с морганеллами, то препаратами выбора становятся карбопенемы, и только в случае их недоступности и документированной бактериологом чувствительности, можно посмотреть в сторону цефалоспоринов, например, цефтазидима (для которого нужна отдельная цефалоспориназа, чтобы он был инактивирован), а лучше цефтазидим-авибактама. Хотя если недоступны карбопенемы, то и Завицефте, скорее всего, взяться будет неоткуда.
Какие препараты могут быть использованы в качестве резервных? Решать этот вопрос также необходимо только после получения результата микробиологии и чувствительности в идеале по МПК, и только после этого рассматривать назначение цефепима или ципрофлоксацина, или аминогликозидов (они, к слову, в случае морганеллы могут обоснованно выступать в качестве монотерапии инфекций мочевыводящих путей).
Читайте также:

