Эритематозная гастропатия кандидоз пищевода
Обновлено: 24.04.2024
Оппортунистические инфекции, включая микозы органов пищеварения, представляют собой актуальную проблему современной гастроэнтерологии.
Оппортунистические инфекции, включая микозы органов пищеварения, представляют собой актуальную проблему современной гастроэнтерологии. Диагностика и лечение кандидоза пищевода в ряде случаев сопряжены с определенными трудностями.
Дрожжеподобные грибы рода Candida — одноклеточные микроорганизмы размерами 6–10 мкм. Эти дрожжи диморфны: в различных условиях они образуют бластоспоры (клетки-почки) и псевдомицелий (нити удлиненных клеток). Эта морфологическая особенность имеет, как будет показано ниже, важное клиническое значение.
Исход контакта с дрожжеподобными грибами рода Candida обусловлен состоянием системы антифунгальной резистентности индивида. В большинстве случаев такой контакт формирует транзиторное кандидоносительство, когда структуры и механизмы антифунгальной резистентности обеспечивают деконтаминацию макроорганизма. В то же время у лиц с нарушениями в системе антифунгальной резистентности контакт может сформировать как персистирующее носительство, так и кандидоз. Таким образом, кандидоз пищеварительного тракта имеет типичные черты оппортунистический инфекции.
Однако решающее значение в системе антифунгальной резистентности имеет функция клеток фагоцитарного ряда — полиморфноядерных лейкоцитов, в первую очередь, и, в меньшей степени, мононуклеарных фагоцитов и естественных киллеров. Специфический антифунгальный гуморальный ответ реализуется за счет синтеза В-клетками специфических противокандидозных антител классов IgA, IgM, IgG и в определенной степени IgE. Наконец, сложная кооперация дендритных клеток, Т-хелперов 1 и 2 типа, а также Т-регуляторных клеток обеспечивает адекватный специфический клеточный иммунный ответ.
Дефекты в описанной выше системе антифунгальной резистентности являются факторами, способствующими возникновению кандидоза, или так называемыми факторами риска. Группы риска по развитию кандидоза пищеварительного тракта представлены ниже.
Заболевания эндокринной системы, в первую очередь сахарный диабет, аутоиммунный полиэндокринный синдром, гипотиреоз, ожирение и др.
В указанных группах кандидоз выявляют чаще обычного. Отметим, что иногда причину нарушения антифунгальной резистентности определить не удается.
Патогенез кандидоза пищеварительного тракта характеризуется последовательным прохождением грибами следующих этапов — адгезии, инвазии, кандидемии и висцеральных поражений. На первом этапе дрожжи адгезируются к эпителиоцитам какого-либо участка слизистой оболочки. В дальнейшем дефекты в системе резистентности позволяют дрожжам через трансформацию в псевдомицелий внедряться (инвазироваться) в слизистую оболочку и подлежащие ткани. Цитопения — решающий фактор, который позволяет инвазирующим грибам достигать стенки сосудов, разрушать ее и циркулировать в сосудистом русле. Такой этап называют кандидемией. В отсутствие адекватной терапии кандидемия приводит к образованию очагов инвазивного кандидоза в висцеральных органах, например, печени, легких, центральной нервной системе и др.
Парадоксально, но внедрение грибов рода Candida чаще наблюдается в участках, представленных многослойным эпителием (полость рта, пищевод) и значительно реже в однослойный эпителий (желудок, кишечник).
На практике клиницисту приходится сталкиваться преимущественно с кандидоносительством, частота которого у здоровых лиц достигает в полости рта 25%, а в кишечнике — до 65–80%.
Объем обследования при кандидозе органов пищеварения включает изучение анамнеза и клинической картины, оценку рутинных клинических тестов, эндоскопические исследования, микологические (культуральные, морфологические и серологические) и иммунологические тесты.
Показаниями для эндоскопического исследования с целью исключения кандидоза пищевода является: группа риска, клинические признаки эзофагита и верифицированный кандидоз других локализаций (например, орофарингеальный, кандидоз урогенитальной системы, диссеминированный кандидоз).
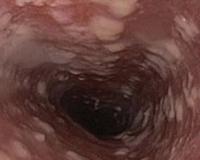
Эндоскопические признаки кандидоза пищевода — гиперемия и контактная ранимость слизистой оболочки, а также фибринозные налеты различной локализации, конфигурации и размеров. Среди всего разнообразия визуальных признаков кандидоза пищевода можно выделить три группы типичных изменений:
Фибринозный (псевдомембранозный) эзофагит. Наблюдают бело-серые или бело-желтые рыхлые налеты в виде округлых бляшек диаметром от 1 до 5 мм, выступающие над ярко гиперемированной и отечной слизистой оболочкой. Контактная ранимость и гиперемия слизистой оболочки заметно выражены.
Напомним, что схожие эндоскопические изменения могут наблюдаться при рефлюкс-эзофагите, пищеводе Барретта, герпес-эзофагите, плоских лейкоплакиях, красном плоском лишае, ожоге или опухоли пищевода. Поэтому диагностика кандидоза пищевода основана на эндоскопическом исследовании и лабораторном изучении биопсийных материалов из пораженных участков. Необходимо учитывать, что при однократной биопсии чувствительность лабораторных методов недостаточна.
С целью обнаружения псевдомицелия используют морфологические микологические методы: цитологический — с окраской мазков по Романовскому–Гимза, и гистологический — с окраской биоптатов ШИК-реакцией. Таким образом, учет диморфности Candida spp. является ключом к дифференциальному диагнозу между кандидозом и кандидоносительством. В современных условиях клиницист должен требовать от морфолога точного описания морфологических структур гриба, ведь обнаружение отдельных дрожжевых клеток, как правило, свидетельствует о кандидоносительстве, а обнаружение псевдомицелия позволяет подтвердить диагноз кандидоза.
К недостатку морфологических методов можно отнести их ограниченную чувствительность при эндоскопической биопсии. Известно, что биопсионные щипцы позволяют получить для изучения миниатюрный фрагмент ткани, и вероятность обнаружения информативного признака при однократной биопсии недостаточна.
Культуральное исследование биоматериалов слизистых оболочек с определением вида возбудителя становится строго необходимым при рецидивирующем течении кандидоза или резистентности к стандартной антимикотической терапии.
Чувствительность и специфичность серологических тестов диагностики кандидоза пищевода (иммуноферментный анализ с антигеном Candida, уровень специфического IgE, тест латекс-агглютинации Platelia) пока не достигли требуемой точности и в практике применяются редко.
Кандидоз пищевода, даже протекающий субклинически, опасен своими осложнениями — стриктурой, кровотечением, перфорацией и диссеминацией микотического поражения.
Рентгенографический метод при кандидозе органов пищеварения малоинформативен, так как не уточняет этиологии процесса, но при развитии осложнений (например, стриктура, язва, перфорация) приобретает решающее значение.
Развитие стриктуры пищевода отмечают у 8–9% пациентов с кандидозным эзофагитом. Чаще они локализованы в верхней или средней трети грудного отдела пищевода и вызывают перманентную дисфагию. Другим частым осложнением кандидоза верхних отделов органов пищеварения является кровотечение, вызванное контактной ранимостью слизистой оболочки. Такое хроническое малоинтенсивное кровотечение приводит к анемии, а у пациентов с цитопенией кровотечение может развиваться стремительно (нередко наблюдается рвота алой кровью и псевдомембранозными массами) и приводить к серьезной потери крови. Клиническая картина перфорации пищевода характеризуется, кроме интенсивного болевого синдрома, развитием пневмомедиастинума и подкожной эмфиземы в области шеи.
Лечение кандидоза пищевода основано на применении антифунгальных препаратов. Общий принцип действия всех антифунгальных средств — угнетение биосинтеза эргостерина клеточной стенки дрожжей. Антифунгальные средства, используемые для лечения кандидоза в целом, можно разделить на три группы. Первая группа — полиеновые антимикотики, практически нерезорбируемые при приеме per os. К ним относят амфотерицин В, нистатин и натамицин. Вторая группа — азольные антимикотики, относительно хорошо резорбируемые при приеме per os. К ним относятся: кетоконазол, флуконазол, итраконазол, вориконазол, позаконазол. Третья группа — эхинокандины: каспофунгин, анидулафунгин, микафунгин.
Цель лечения кандидоза слизистых оболочек верхних отделов пищеварительного тракта — устранение симптомов и клинико-лабораторных признаков заболевания, а также предотвращение рецидивов.
Нужно подчеркнуть, что при кандидозе пищевода местная терапия неэффективна. У больных с выраженной одинодисфагией, которые не способны глотать, должна использоваться парентеральная терапия.
Препаратом выбора для лечения кандидоза пищевода является флуконазол 100–200 мг/сут, назначаемый перорально или внутривенно в течение 2–4 нед. Подчеркнем, что как средство лечения кандидоза пищевода флуконазол превосходит по эффективности и кетоконазол, и итраконазол в капсулах из-за непостоянной абсорбции последних.
Лишь в случаях непереносимости флуконазола или резистентности возбудителя (чаще это C. krusei, C. glabrata, C. pseudotropicalis) показаны препараты второй линии (также в течение 2–4 недель ). Препаратами второй линии при кандидозе пищевода являются:
5)вориконазол внутривенно 6 мг/кг/сут каждые 12 часов в первый день, а затем 4 мг/кг/сут каждые 12 часов;
Необходимо добавить, что применение нерезорбируемых антимикотиков (нистатин, натамицин) неэффективно.
Несмотря на высокую эффективность флуконазола у пациентов с сохраняющимся иммунодефицитным состоянием высока вероятность рецидивов кандидоза пищевода. Необходимо помнить, что безрецидивного течения кандидоза можно достичь только у больных с полной коррекцией фонового состояния. Так, например, при СПИДе рецидивы кандидоза прекращаются только при успешной антиретровирусной терапии, обеспечивающей снижение вирусной нагрузки и увеличение числа CD4-лимфоцитов.
Для предотвращении рецидивов может быть эффективна длительная поддерживающая терапия флуконазолом (100мг/день) или назначение дозы флуконазола 200 мг еженедельно.
Литература
2.Шевяков М. А. Кандидоз слизистых оболочек пищеварительного тракта (лекция) // Проблемы медицинской микологии. 2000. Т.2, №2. С. 6–10.
3.Yoo S.S., Lee W.H., Ha J., Choi S., Kim H.J., Kim T.H., Lee O.J. Prevalence of esophageal disorders in the subjects examined for health screening // Korean J. Gastroenterol. 2007, Nov. 50 (5): 306–312.
4.Климко Н.Н. и др. Проект рекомендаций по лечению кандидоза // Проблемы медицинской микологии. 2001. Том 3, №3. С.12–25.
5.Шевяков М.А., Климко Н.Н., Антонов В.Б., Иншаков Л.Н., Колб З.К. Диагностика кандидоза пищевода // Проблемы медицинской микологии. 1999. Т.1, №4. С. 14–18.
6.Шевяков М.А., Антонов В.Б., Загорская Е.А. Стриктуры пищевода кандидозной этиологии // Вестник хирургии им. И.И.Грекова. 1991, № 3. С.39–41.
7.Pappas P.G., Rex J.H., Sobel J.D., Filler S.G., Dismukes W.E., Walsh T.J., Edwards J.E. Practical guyde of candidiasis treatment // Clinical Infection Diseases. 2004. Vol. 38. P. 161–189.
8.Gilbert D.N., Moellering R.C., Sande M.A. The Sandford Guide to antimicrobial therapy, Thirty-first edition, 2001. P 71.
9.Kalogeropoulos N.K., Whitehead R. Campylobacter-like organisms and Candida in peptic ulcers and similar lesions of the upper gastrointestinal tract: astudy of 247 cases // J. Clin. Pathol. 1988. Vol. 41. №10. P. 1093–1098.
10.Шевяков М.А., Колб З.К., Борзова Ю.В. Рецидивирующий кандидоз пищевода у ВИЧ-неинфицированных больных. (Тезисы докладов 7-х Кашкинских чтений) // Проблемы медицинской микологии. 2004, Т.6. №2, С.131.
11.Laine L. Thenatural history of esophageal candidiasis after successful treatment in patients with AIDS // Gastroenterology. 1994, Vol.107, №3. P.744–746.
12.Parente F. et al. Prevention of symptomatic recurrences of esophageal candidiasis in AIDS patient after the first episode: a prospective open study // American Journal of Gastroenterology. 1994. Vol. 89. №3. P.416–420.
М.А. Шевяков, доктор медицинских наук, профессор СПбМАПО, Санкт-Петербург
Кандидоз пищевода — это микотическая инфекция, которая вызвана грибками рода Кандида (Candida). Заболевание проявляется затруднениями при глотании, загрудинными болями и дискомфортом. При длительном существовании кандидоза возникает потеря веса, тяжелые авитаминозы. Основу диагностики грибковой инфекции составляет осмотр пищевода при ЭФГДС с последующим морфологическим анализом биоптатов для выявления частиц возбудителя. Дополнительно проводится микробиологический посев биоматериала. Для лечения пищеводного кандидоза применяют различные по химической структуре противогрибковые препараты системного действия.
МКБ-10
Общие сведения
Кандидоз пищевода (кандидозный эзофагит) считается оппортунистической инфекцией. Среди пациентов общего профиля частота заболевания составляет 1-2%, при наличии сахарного диабета микоз встречается намного чаще — в 5-10% случаев. У больных с ВИЧ-инфекцией и СПИДом распространенность грибкового поражения пищевода достигает 30%. Уровень заболеваемости кандидозом среди людей пожилого возраста в 2 раза выше, чем в среднем в популяции, в старческом возрасте (после 75 лет) — в 6 раз выше. Инфекция иногда возникает у детей на фоне первичных иммунодефицитов.

Причины
Возбудителями инфекционного заболевания пищевода являются грибки рода Candida. Всего насчитывается более 150 видов грибов Кандида, но в 60-90% случаев патология вызвана C. albicans. При иммуносупрессии возрастает роль других видов — C. glablata, C. kefir, C. lucitanies и C. krusei. Микроорганизмы в естественных условиях находятся в форме бластомицетов или псевдомицелия. Развитию кандидоза способствует ряд предрасполагающих факторов:
- Иммунодефициты. Поражение слизистых пищеварительного тракта грибами Кандида является одним из маркеров прогрессирующей ВИЧ-инфекции. Высокая заболеваемость наблюдается при первичных генетически обусловленных иммунодефицитах: синдроме Ди Джорджи, синдроме Брутона, болезни Вискотта-Олдрича и др.
- Лекарственная иммуносупрессия. Частота кандидоза возрастает при продолжительном лечении кортикостероидами, которые угнетают активность иммунной системы. Негативное влияние оказывает лучевая и химиотерапия онкологических больных, которая нарушает местные и общие факторы иммунной защиты.
- Эндокринные заболевания. Вероятность появления микоза повышается у страдающих сахарным диабетом, аутоиммунным полиэндокринным синдромом, гипотиреозом. Антифунгальная резистентность снижается при ожирении и других проявлениях метаболического синдрома.
- Местные факторы. К локальным причинам микотического процесса относят хронические воспалительные и атрофические изменения в эзофагеальной стенке, ксеростомию, дегенеративно-деструктивные нарушения в полости рта. Патология вдвое чаще встречается у тех, кто пользуется съемными зубными протезами.
Факторы риска
Факторы риска развития кандидоза пищевода: истощение, авитаминозы, хронические соматические болезни, сопровождающиеся астенией. Вероятность микоза возрастает после операций по трансплантации органов.
Широкая распространенность кандидоза у пожилых людей связана с инволютивным угасанием функций иммунитета, нарушениями микроциркуляции вследствие атеросклероза, атрофией слизистого слоя пищевода. В формировании кандидоза большую роль имеет полипрагмазия, а именно неконтролируемое применение антибиотиков, гормонов и антисекреторных препаратов.
Патогенез
Первым этапом механизма развития заболевания является адгезия (прикрепление) клеток грибка к поверхности эзофагеальной слизистой. В дальнейшем микроорганизмы способны трансформироваться в нитевидную форму и внедряться в более глубокие слои стенки пищевода. Поражение тканей происходит вследствие продукции возбудителем специфических ферментов. Большое значение в манифестации кандидоза играют дефекты Т-клеточного звена иммунитета.
Характер инфекции определяется состоянием факторов антифунгальной защиты организма. При правильной работе иммунной системы возникает транзиторное носительство. При дефектах иммунитета обычно встречается персистирующее носительство без клинических симптомов. При наличии у человека одной или нескольких предпосылок развивается типичный кандидоз.
Классификация
Согласно анатомической классификации, поражение пищевода грибками-кандидами относится к поверхностным формам кандидоза. В практической гастроэнтерологии широко применяется эндоскопическая классификация, которая необходима для систематизации различных вариантов поражения эзофагеальной слизистой. Клиницисты выделяют 3 варианта изменений в пищеводе при кандидозе:
- Катаральный эзофагит. Характеризуется гиперемией слизистой пищевода и умеренной отечностью. На кандидозную инфекцию указывает тонкий паутинообразный налет на эпителии, контактная кровоточивость.
- Фибринозный эзофагит. В пищеводе образуются беловато-серые налеты в виде бляшек размером до 0,5 см. Гиперемия, отечность и кровоточивость слизистой оболочки выражены интенсивнее, чем при катаральной форме.
- Фибринозно-эрозивный эзофагит. Кандидоз проявляется множественными налетами грязно-серого цвета, после удаления которых на слизистой оболочке визуализируются эрозии. Характерна спонтанная кровоточивость.
Симптомы кандидоза пищевода
Типичные признаки кандидоза пищевода — затруднения и боли в момент глотания. Человек испытывает дискомфорт при употреблении твердой и сухой пищи, тогда как при питье неприятные ощущения не беспокоят. Болезненность ощущается при прохождении пищевого комка по пищеводу. Некоторые пациенты для облегчения боли и жжения запивают каждый кусочек пищи водой.
Характерен дискомфорт за грудиной, который возникает независимо от употребления продуктов питания. Реже появляется отрыжка с неприятным запахом, изжога. При тяжелом поражении пищевода во время еды бывают очень сильные боли, поэтому больные сокращают объем порций и кратность приема пищи. Вследствие длительного недоедания отмечается потеря массы тела, присоединяются симптомы авитаминоза.
Осложнения
Вследствие контактной ранимости слизистой типичны постоянные малоинтенсивные кровотечения при травмировании пищевода кусочками плохо пережеванной пищи. Хроническая кровоточивость приводит к железодефицитной анемии. У пациентов, страдающий тромбоцитопенией, возможно профузное кровотечение с геморрагическим шоком. Очень опасна перфорация пищевода, которая проявляется болевым шоком, пневмомедиастинумом и подкожной эмфиземой шеи.
Диагностика
При кандидозе пищевода отсутствуют патогномоничные симптомы, поэтому диагностический поиск включает ряд лабораторных и инструментальных методов. Иногда при осмотре врач-гастроэнтеролог замечает очаги грибкового поражения ротовой полости, что косвенно указывает на микотическую этиологию дисфагии. Для подтверждения диагноза используются следующие методы исследования:
Лечение кандидоза пищевода
Основу терапии кандидозной инфекции составляют специфические антифунгальные средства. Они угнетают синтез химических веществ, входящих в клеточную стенку грибов. Существует 3 группы антимикотиков, которые различаются по степени усвояемости при пероральном приеме. Чаще всего в клинической практике используются азольные противогрибковые средства, которые необходимо принимать в течение 2-3 недель.
При неэффективности стандартной схемы антимикотик меняют либо переходят на парентеральное введение лекарства. Прием препарата длится до полного исчезновения клинико-лабораторных симптомов. Для больных со СПИДом обязательным условием излечения является снижение вирусной нагрузки и повышение уровня CD4-клеток. Для этого рекомендуют современные схемы антиретровирусной терапии.
Прогноз и профилактика
Вероятность полного выздоровления зависит от условий и причин, вызвавших кандидоз. У людей с нормальным иммунным статусом прогноз благоприятный — для излечения требуется 1 курс противогрибковой терапии. Если больной принадлежит к категории носителей ВИЧ-инфекции либо по состоянию здоровья принимает иммуносупрессоры, существует риск рецидива грибковой инфекции.
Меры первичной профилактики включают контролируемое назначение иммуносупрессоров и антибиотиков, раннее выявление и лечение орофарингеального кандидоза. Для предотвращения рецидивов иммунокомпрометированным пациентам показан ежедневный прием противогрибкового препарата в невысокой дозе. Реже прибегают к профилактическому еженедельному приему удвоенных дозировок антимикотика.
1. Особенности кандидоза пищевода у больных пожилого и старческого возраста/ Д.М. Албегова// Проблемы медицинской микологии. — 2012.

Эритематозная гастропатия — это воспаление, покраснение и отёчность слизистой оболочки желудка, вызванное влиянием ряда негативных факторов или бактериальным поражением. Довольно часто параллельно диагностируется эритематозная гастродуоденопатия, связанная с поражением привратника желудка и части двенадцатиперстной кишки.
Вышеописанные состояния не считаются самостоятельной нозологией, эти симптомы диагностируются во время клинических обследований пациента. При обнаружении гастропатий рекомендуется в кратчайшие сроки пересмотреть образ жизни и систему питания, чтобы избежать развития гастрита и последующей язвенной болезни пищеварительного тракта.
Эритематозная гастропатия и гастродуоденопатия могут спровоцировать развитие бульбопатии — воспалительного процесса в петле, соединяющей двенадцатиперстную кишку с кишечником. Вышеописанные патологии могут встречаться одновременно или последовательно в результате воздействия химикатов или патогенных микроорганизмов.
Патогенез
Эритематозная гастропатия считается кислотозависимым заболеванием, которое запускается при дисбалансе защитных и агрессивных факторов. Самым агрессивным компонентом является хеликобактер пилори.
Классификация
Патология подразделяется на 2 вида:
- Очаговая эритематозная гастропатия. Характерно поражение только части слизистой оболочки (привратник, антральный отдел). На слизистых стенках появляются небольшие по площади очаги воспалительного процесса. Очаговая гастропатия легче поддаётся лечению, чем другие формы. Эффективна диетотерапия.
- Распространённая гастропатия. Воспалительный процесс и покраснение охватывает всю слизистую оболочку желудка. При отсутствии адекватной, грамотной терапии патология переходит в острый гастрит с последующим развитием язвенной болезни пищеварительного тракта.
Также гастропатия подразделяется на несколько форм:
- Эрозивная. Поражается верхний отдел желудка. На слизистой стенке образуются вогнутые эрозии небольшого диаметра (около 7 мм). При отсутствии своевременной терапии развивается гастрит. Главная трудность в диагностике заключается в отсутствии клинической симптоматики, которая может помочь в диагностике. Патология является случайной находкой при обследовании.
- Застойная. На слизистых оболочках появляются маленькие ранки. Пациенты предъявляют жалобы на чувство дискомфорта после приёма пищи, отрыжку, изжогу.
- Папулёзная. Поражает нижний отдел желудка в виде небольших язв на слизистой стенке. Развивается на фоне повышенной кислотности желудочного сока. Протекает практически бессимптомно.
- Антральная гастропатия. Характерно поражение нижнего, антрального отдела желудка, в результате чего пищевой комок медленно продвигается к двенадцатиперстной кишке и трудно измельчается. Происходит застаивание пищи, запускаются процессы брожения. При отсутствии своевременно и грамотной терапии развивается гастрит с атрофическим поражением слизистых оболочек ЖКТ.
Эритематозно-экссудативная гастропатия является находкой при проведении гастроскопии. Экссудативная форма предполагает выработку небольшого количества экссудата при появлении повреждений слизистых оболочек желудка.
В зависимости от степени поражения эпителиального слоя гастропатию подразделяют на:
- Эритематозная гастропатия 1 степени воспаления. Поражения эпителиального слоя в пищеварительном тракте при 1 степени носят минимальный характер. Патология протекает бессимптомно.
- Эритематозная гастропатия 2 степени воспаления. Изменения эпителиального слоя незначительны, но заметны. Для 2 степени характерно прогрессирующее течение. Ситуация усугубляется при воздействии повреждающих факторов. У взрослых пациентов заболевание приобретает хронический характер.
Эритематозная бульбопатия
Хронический воспалительный процесс поражает луковицу двенадатиперстной кишки, а точнее её начальный отдел, который располагается сразу же за конечным отделом желудка. Слизистая оболочка приобретает отёчный вид и на ней образуются красные овальные пятна. При появлении эрозивных дефектов говорят об эрозивной бульбопатии, которая является самой тяжёлой формой бульбита.
Эритематозная колопатия
Характеризуется появлением эритематозных пятен на стенках тонкого и толстого кишечника. При воздействии неблагоприятных факторов эритемы переходят в эрозии и язвы.
Причины
Эритематозная гастродуоденопатия и гастропатия развиваются под вдиянием ряда неблагоприятных факторов:
- Стресс. Психотравмирующие факторы стимулируют выработку гормона адреналина, который усиливает выработку соляной кислоты. Длительное воздействие желудочного сока с высокой концентрацией приводит к раздражению слизистой стенки желудка, её покраснению с последующим формированием язвенных поражений и эрозий.
- Несбалансированное питание, рацион. Длительное употребление в пищу раздражающих и тяжёлых блюд вызывает воспаление в слизистой оболочке желудка.
- Бесконтрольный приём медикаментов. Некоторые лекарственные средства оказывают негативное воздействие на работу органов пищеварительного тракта, нарушая их нормальное функционирование. Довольно часто дуоденопатия развивается именно на фоне приёма препаратов.
- Присутствие Хеликобактер Пилори в организме. H.pylori способна внедрятся в слизистую оболочку желудка, запуская воспалительные процессы в ней.
- Наследственность. Риск развития эритематозной гастропатии очень велик, если патология была когда-либо диагностирована у ближайших родственников. У предрасположенных пациентов влияние даже незначительных на первых взгляд факторов может запустить развитие патологического процесса.
- Ведение нездорового образа жизни. Отсутствие постоянного кислородного обмена, малоподвижный образ жизни, присутствие вредных привычек приводят к застойным явлениям в организме, которые негативно сказываются на работе пищеварительного тракта.
Симптомы
Эритематозная гастропатия характеризуется определённой клинической картиной. Основные симптомы:
- неприятные ощущения в эпигастральной области после приёма пищи; ;
- отрыжка;
- рвота (редко);
- нарушения стула (рвота/понос);
- тошнота;
- специфический привкус во рту с гнилостным компонентом;
- потеря веса из-за отсутствия аппетита;
- снижение работоспособности, ухудшение общего самочувствия, вялость и апатия.
Эритематозная гастропатия дополнительно проявляется отложением белого налёта на языке, особенно по утрам.
Анализы и диагностика
Лабораторные методы исследования:
- анализ каловых масс (присутствие скрытой крови, оценка количественно/качественного состава, выявление нетипичных примесей);
- анализ крови;
- анализ мочи;
- рН-метрия;
- исследование желудочного сока.
Инструментальные методы исследования эритематозной гастропатии и дуоденопатии:
- Манометрия. Позволяет оценить эвакуаторную способность пищеварительного тракта за счёт определения скорости моторики.
- Электрогастроэнтерография.
- Фиброгастродуоденоскопия.
- Колоноскопия.
- УЗИ желудка, кишечника.
В затруднительных ситуациях назначают компьютерную томографию, МРТ и другие методы лучевой диагностики. Очень важно грамотно отдифференцировать дуоденопатию от язвенной болезни пищеварительного тракта, гастрита, язвенного колита и другой патологии ЖКТ воспалительного и невоспалительного характера.
Чаще всего эритематозная гастропатия является случайной находкой при обследовании пищеварительного тракта по другим поводам. При необходимости проводится биопсия взятого из стенки желудка материала.
Лечение эритематозной гастропатии
В зависимости от причины, спровоцировавшей эритематозную гастропатию, назначается соответствующее медикаментозное лечение. При неэффективности диеты и лекарственной терапии показано оперативное вмешательство. Гастродуоденопатия лечится по такой же схеме.

При этом, глубокие слои слизистой в процесс не вовлекаются. В целом, гастропатии характеризуются отсутствием воспалительного процесса/незначительной его выраженностью, то есть, характерные для воспаления морфологические изменения в слизистой оболочке желудка, отсутствуют. Является одним из наиболее часто встречающихся нарушений целостности слизистой желудка. Различают очаговую (локализация процесса, ограничена незначительной площадью) эритематозную гастропатию и диффузную ее форму (при поражении большой поверхности слизистой).
Возникает под воздействием различных повреждающих факторов, основными из которых являются:
- Дефекты питания (употребление продуктов, раздражающих слизистую – жареная пища, соления, маринад, острые специи/приправы, копчёности, сильногазированные напитки).
- Злоупотребление алкоголем, курение.
- Неправильный режим питания (переедания, ужин перед сном, отсутствие завтрака, длительные промежутки между приемами пищи).
- Частые/длительные стрессы.
- Прием фармакологических препаратов (аспирин, НПВС).
Эритематозная гастропатия, выявленная в процессе обследования желудка, как таковая, при отсутствии других специфических изменений слизистой показанием для назначения медикаментозной терапии не является. Скорее, она должна вызывать озабоченность состоянием здоровья и настороженность в отношении существующего риска развития заболеваний желудка. По сути, она является сигналом необходимости коррекции образа жизни и в первую очередь, коррекции питания.
Диета при эритематозной гастропатии очаговой формы предусматривает нормализацию режима питания и умеренность в приеме пищи, исключение из рациона продуктов, раздражающих слизистую оболочку (специи/приправы, лук, чеснок, овощи с грубой клетчаткой — редис, репа, соления, маринады, копчёности, жареная пища, напитки, содержащие углекислоту), отказ от употребления алкоголя/курения. Пища/напитки не должны быть слишком горячими и холодными. Как правило, такие ограничения в рационе на протяжении 2-3 недель нормализуют состояние слизистой желудка.
Диета при эритематозной гастропатии диффузной (распространенной) формы предусматривает более строгие ограничения. За основу может быть принята лечебная Диета №1, которая, являясь физиологически полноценной, предусматривает умеренное щажение слизистой желудка от различных неблагоприятных факторов (механических, химических, термических). При этом, в первые 7-10 дней рекомендуется протертый вариант диеты с постепенным переходом на не протёртый вариант.
Диетическое питание предусматривает:
- Полноценность рациона питания (количество пищевых нутриентов должно соответствовать физиологическим нормам).
- Исключение продуктов, усиливающих секрецию желудочного сока/раздражающих слизистую — свежие хлебобулочных изделий, жирных блюд, различных пряностей/приправ, крепких мясных/рыбных бульонов, лука, чеснока, консерв, фаст-фуда, копчёностей, а также сырых овощей, особенно содержащих грубую растительную клетчатку – бобовые, редис, ржаной хлеб, редька, корень сельдерея. Исключаются алкогольсодержащие напитки, крепкий чай, кофе.
- Ограничивается соль и употребление соленых продуктов (соления, маринады).
- Дробный характер питания — не допускаются длительные перерывы между едой, порции небольшие.
- Кулинарная обработка продуктов включает приготовление на пару, варку. Категорически запрещена жареная пища. В период обострения блюда подают протертыми.
- Блюда должны быть теплыми (35-40 градусов), но не горячими/не холодными.
Рекомендуется включать в рацион питания продукты, не возбуждающие секрецию — легкие супы, отварное мясо (птица, кролик, говядина), нежирные сорта белой рыбы, молоко, некислый (кальцинированный) творог, паровой омлет/яйцо всмятку, протёртые каши/овощи, кисели, отвар шиповника, некрепкий чай.
Из круп предпочтение отдается овсяным хлопьям, манной и гречневой крупе, рису, а через 7-10 дней рацион круп расширяется. При наличии повышенной кислотности рекомендуется ограничить в рационе питания легкоусвояемые углеводы (конфеты, сахар, варенье, мед и другие сладости), что позволяет снизить секреторную активность.
Дополнительно рекомендуется прием растительных отваров, способствующие репаративным процессам в слизистой (календула, шалфей, ромашка, зверобой, листья подорожника, чабрец) или аптечных желудочных сборов.
На сервисе СпросиВрача доступна консультация гастроэнтеролога онлайн по любой волнующей Вас проблеме. Врачи-эксперты оказывают консультации круглосуточно и бесплатно. Задайте свой вопрос и получите ответ сразу же!

Екатерина, Подскажите пожалуйста, биопсию пищевода, что мне взяли покажет Кандиду? Или там нужен какой-то другой особый анализ? Я могу что-то дополнительно сдать сама?


Здравствуйте. Надо ждать результат биопсии, сдать кровь на гастропанель, антитела к внутреннему фактору Кастла, к париетальным клеткам. Вы так и не написали, как уреазный тест. При это не бойтесь, в зависимости от того, что найдется, назначается лечение. Чем вам помочь сейчас(есть ли жалобы)?
Инесса, благодарю за ответ! Дыхательный тест сдала только сегодня, потому что мне биопсию на хелик не взяли( Сегодня второй день после процедуры, самое странное, что нет сильного чувство голода, Болит вверху в Эпигастральная области, слева около пупка. Съела кокосовый йогурт, тошнит( ну и сейчас конечно я в диком стрессе нахожусь(
Как так, 2019-м перед беременностью проверялась, в целом везде все было хорошо. Сейчас уже даже без биопсия пишут про атрофии пищевода, и какой-то кандидоз появился.
Если кандидоз не подтвердится, что тогда может быть это за налёт? Я боюсь,что они мне и тест на Кандиду не сделают(( как с хелик было. И в совокупности хелик и Кандида это же просто безвыходность ((

Не впадайте в ужас! Грибковые поражения пищевода проходят самостоятельно и лечения требуют редко, лечатся успешно. За кандидоз могли принять фибрин-воспалительный налет. Давайте пока Будем принимать Гастрофарм 1т 3 раза в день за 30 минут до еды и фосфалюгель 1 доза 3 раза в день через 1, 5-2 часа после приема пищи 3 раза в день до получения результатов уреазного теста теста и биопсии. Атрофии в пищеводе у вас не нашли , она в теле желудка.
Читайте также:

