Escherichia coli klebsiella spp enterobacter spp proteus spp salmonella spp
Обновлено: 19.04.2024

Разработчик сайтов, журналист, редактор, дизайнер, программист, копирайтер. Стаж работы — 25 лет. Область интересов: новейшие технологии в медицине, медицинский web-контент, профессиональное фото, видео, web-дизайн. Цели: максимально амбициозные.
- Запись опубликована: 15.01.2022
- Reading time: 9 минут чтения
Необходимость антибактериальной терапии инфекционной диареи до сих пор остается спорным вопросом. Пациенты с легкими симптомами и явным улучшением самочувствия не нуждаются в лечении антибиотиками. Однако существуют определенные состояния, когда необходимо применение лекарств.
Когда инфекционную диарею нужно лечить?
Тип инфекционной диареи, когда обязательно антибактериальное лечение:
- дизентерийный шигеллез;
- холера;
- псевдомембранозный энтероколит, вызванный паразитами;
- заболевания, передающиеся половым путем.
Инфекционная диарея, когда показания менее ясны, но лечение обычно рекомендуется:
- длительное или затяжное инфицирование иерсинией,
- раннее течение кампилобактериоза,
- инфекции aeromonas и plesiomonas, а также
- вспышки энтеропатогенной кишечной палочки;
- понос у детей в младшего возраста.
Если тип микроорганизма/возбудителя диареи известен (например, при установленных очагах брюшного тифа) или есть возможность определить его в кратчайшие сроки (например, когда клиника располагает современным оборудованием, лабораторией, использующей диагностику методами ПЦР), то лечение сразу начинают максимально эффективным препаратом для этого типа ИД.
Эмпирическая антимикробная терапия ИД проводится в следующих случаях:
- Младенцы в возрасте до 3 месяцев с подозрением на бактериальную этиологию.
- Больные иммунокомпетентные люди с лихорадкой, болями в животе, кровавым поносом и бактериальной дизентерией (частый скудный стул с примесью крови, гипертермия, спазмы в животе, тенезмы), предположительно вызванными шигеллами.
- Недавно путешествовавшие по миру, с температурой тела ≥38,5°C и/или признаками сепсиса.
- Пациенты с клиническими признаками сепсиса, при подозрении на брюшной тиф.
- Лица со злокачественными новообразованиями, подавленным иммунитетом.
- Пациенты, имеющие клапанные, сосудистые или ортопедические протезы, аномалии сердечно-сосудистой системы, страдающие гемолитической анемией (особенно при сальмонеллезе), очень пожилого возраста.
- Лечение также рекомендуется при длительных симптомах и при рецидиве.
Следует избегать антимикробной терапии у людей с инфекциями, связанными с кишечной палочкой STEC O157 и другими STEC, продуцирующими шигатоксин 2 (или если генотип токсина неизвестен).
Рекомендации к выбору препаратов:
- Эмпирическая противомикробная терапия у взрослых проводится или фторхинолонами (ципрофлоксацин), или азитромицином, в зависимости от особенностей местной чувствительности и анамнеза поездок.
- Детям назначают или цефалоспорины III поколения, в т.ч. младенцам и пациентам с неврологическими поражениями, или азитромицин, в зависимости от чувствительности.
- Если предполагается брюшной тиф, вначале применяют Аб широкого спектра (после сбора крови, кала и мочи). Когда станут доступны результаты тестов, препарат меняют с учетом чувствительности.
Доказательства эффективности антибактериального лечения:
- противомикробные препараты уменьшают тяжесть и продолжительность некоторых кишечных инфекций (КИ), особенно вызывающих острую водянистую диарею;
- полезны при бактериальных КИ, вызывающих системное поражение;
- существует множество изученных антибиотиков, в т.ч. целенаправленных.
Эффективность варьируется от определенно эффективной до возможной и/или сомнительной. Под эффективностью понимается сокращение продолжительности заболевания, тяжести и осложнений (см. Таблицу 1).
Таблица 1. Антимикробная терапия острой инфекционной диареи
| Возбудитель | Эффективность | Препарат выбора (рекомендуемый, первой линии) | Альтернативный препарат |
| Бактерии: |
Амеба дизентерийная Entamoeba histolytica
Криптоспоридиум парвум Cryptosporidium parvum
Возбудитель изоспороза Isospora belli
* Триметоприм/сульфаметоксазол имеет ограниченное значение из-за моделей резистентности.
Пояснения для выбора лечения
- Противомикробная терапия не показана при острой вирусной диарее, вызванной ротавирусом, кишечными аденовирусами и небольшими вирусами с круглой структурой.
- При острой водянистой диарее лечение в основном поддерживающее. Антибиотикотерапия спорна. При их неоправданном применении риск резистентности к антибиотикам увеличивается, высока возможность побочных эффектов (например, синдром Стивенса-Джонсона или псевдомембранозный колит). Исключение: тяжелая водянистая диарея и вызванная холерой требуют приема Аб.
- Азитромицин – хороший выбор для беременных женщин и детей, когда фторхинолоны не одобрены, и при их непереносимости.
- Лечение любого типа инфекционной диареи обязательно сопровождается восполнением жидкости (регидратацией).
- Антибиотики рекомендуются для лечения дизентерии, вызванной большинством организмов.
- Эффективность и необходимость антибактериальной терапии кампилобактерной инфекции зависит от нескольких причин: 1) Доказано, что при диарее из-за кампилобактериоза,антибиотики не изменяют естественное течение болезни, если их начинают принимать > через 4 дня после развития симптомов. 2) Также доказано, что раннее начало приема эритромицина сокращает продолжительность болезни.
- Перед назначением лечения ИД, вызванной Campylobacter spp. необходимо учитывать время появления симптомов.
- Лечение E coli O157:H7 в настоящее время не рекомендуется. Антимикробная терапия при инфекции EHEC остается спорной по двум причинам: 1) антибиотики существенно не улучшают исход, особенно если начать прием через несколько дней после идентификации возбудителя; 2) имеются неофициальные данные о том, что Аб могут способствовать развитию гемолитического уремического синдрома, вторичного по отношению к инфекции EHEC. Считается, что усиливается лизис организмов и высвобождение SLT и эндотоксина.
- Инфекцию EIEC, если она тяжелая, с признаками системного поражения, можно лечить антибиотиками, рекомендованными при дизентерийном шигеллезе, но роль для массового применения не установлена.
Лечение бактериальной диареи, в т.ч. диареи путешественников
- в большинстве случаев бактериальными;
- в меньшей степени, вирусными патогенами;
- реже паразитами.
Длится около 7 дней. При диарее путешественников, основной форме острой водянистой диареи, антимикробная терапия однозначно эффективна. Это подтверждается многими рандомизированными контролируемыми исследованиями.
Распределение возбудителей существенно различается в зависимости от региона путешествия. Например, исследовании FoodNet, проведенном в США в период с 2004 по 2009 год, большинство случаев брюшного тифа, паратифа и инфекции Shigella dysenteriae были связаны с поездками. Особое внимание следует уделить при посещении тропических районов в течение длительного времени.
Диарея путешественников возникает в основном из-за бактериальных энтеропатогенов (примерно 80%), наиболее часто выделяются энтеротоксигенные кишечные палочки (ЭТЭК). Доказано, что антибиотики широкого спектра действия эффективны, но растет их устойчивость к триметоприм-сульфаметоксазолу и ампициллину, и поэтому они менее подходят для эмпирической терапии. Хинолоновые антибиотики теперь – препараты выбора.
Стандартные дозы Ципрофлоксацина, Норфлоксацина (см. таблицу 1) в течение 3–5 дней позволяют снизить тяжесть и продолжительность болезни минимум на 50%. Аналогичная эффективность продемонстрирована с режимами однократной дозы Ципрофлоксацина.
Ципрофлоксацин
- таблетки 500 мг;
- раствор д/инфузий 200 мг/100 мл.
Механизм действия . Спектр действия широкий. Относится к группе фторхинолонов. Действует бактерицидно следующим образом: ингибирует фермент ДНК-гиразу, что приводит к нарушению репликации ДНК, синтеза клеточных белков. В результате: прекращаются деление и рост микроорганизмов→клетка повреждается→гибнет.
- на грамотрицательные организмы в фазу покоя и размножения (поскольку вызывает лизис стенки клеток),
- на грамположительные – только в фазу деления.
- грамотрицательные аэробы: Escherichia coli, Salmonella spp., Shigella spp., Citrobacter spp., Klebsiella spp., Enterobacter spp., Proteus mirabilis, Proteus vulgaris, Serratia marcescens, Hafnia alvei, Edwardsiella tarda, Providencia spp., Morganella morganii, Vibrio spp., Yersinia spp., Haemophilus spp., Pseudomonas aeruginosa, Moraxella catarrhalis, Aeromonas spp., Pasteurella multocida, Plesiomonas shigelloides, Campylobacter jejuni, Neisseria spp.;
- внутриклеточные возбудители: Legionella pneumophila, Brucella spp., Chlamydia trachomatis, Listeria monocytogenes, Mycobacterium tuberculosis, Mycobacterium kansasii, Mycobacterium avium-intracellulare;
- грамположительные аэробы: Staphylococcus spp. (Staphylococcus aureus, Staphylococcus haemolyticus, Staphylococcus hominis, Staphylococcus saprophyticus), Streptococcus spp. (Streptococcus pyogenes, Streptococcus agalactiae).
- Streptococcus pneumoniae;
- Enterococcus faecalis.
К действию устойчивы:
- Corynebacterium spp.;
- Bacteroides fragilis;
- Pseudomonas cepacia;
- Pseudomonas maltophilia;
- Ureaplasma urealyticum;
- Clostridium difficile;
- Nocardia asteroides.
Эффект на Treponema pallidum изучен недостаточно, но данных о его отсутствии больше.
Резистентность развивается медленно, поскольку ферментов для инактивации препарата у бактериальных клеток нет.
Дозирование для различных типов инфекционной диареи представлены в таблице 1.
Рифаксимин
В последнее время возрастает интерес к невсасывающемуся местно активному антибиотику рифаксимину для лечения и диареи путешественников и диареи других видов. Показано, что это лекарство по эффективности аналогично ципрофлоксацину. Но характеризуется потенциальным преимуществом – минимальной системной абсорбцией.
Торговое наименование – Альфа нормикс . Форма выпуска:
- таблетки с содержанием рифаксимина 200 мг;
- суспензия 100 мг/5 мл.
Механизм действия . Спектр действия широкий (грам+ и грам-, анаэробные и аэробные), относится к группе рифамицина. Действует бактерицидно:
- вначале происходит необратимое связывание β-субъединицы фермента ДНК-зависимой РНК-полимеразы;
- затем происходит прекращение синтеза РНК, белков бактерий.
- грам- аэробы: Salmonella spp., Shigella spp., энтеропатогенные EPEC штаммы Escherichia coli, виды Proteus spp., Pseudomonas spp., Campylobacter spp., Yersinia spp., Enterobacter spp., Klebsiella spp., Helicobacter pylori;
- грамотрицательные анаэробы: Bacteroides spp., в т.ч. Bacteroides fragilis, Fusobacterium nucleatum;
- грам+ аэробы: Streptococcus spp., Staphylococcus spp., Enterococcus spp., Enterococcus fecalis,;
- грам+ анаэробы: Clostridium spp., в т.ч. Clostridium difficile, Clostridium perfrigens, Peptostreptococcus spp.
Другие эффекты рифаксимина:
- пролиферация микроорганизмов при СИБР уменьшается;
- выработка бактериями токсических соединений и аммиака уменьшается (при заболеваниях печени особенно важно);
- действует на бактерии в дивертикулах и вокруг них (отсюда снижает риск развития дивертикулита и остальных осложнений дивертикулеза);
- при колоректальных операциях уменьшает число осложнений.
Развитие резистентности оценивается как низкое.
- острые ЖКТ инфекции;
- диарея путешественников;
- другие типы инфекционной диареи с учетом чувствительности;
- СИБР;
- симптоматическое лечение дивертикулеза (локализация – ободочная кишка);
- печеночная энцефалопатия;
- ВЗК;
- профилактика осложнений при операциях на ободочной, прямой кишке и анусе.
Дозирование. Прием независимо от еды, запить 200 мл воды.
- При инфекционной диарее: лицам старше 12 лет – 1 таблетка (200 мг) 4 раза/сутки. Курс при диарее путешественника – 3 дня.
- СИБР: лицам старше 12 лет по 2 таб (400 мг) или 20 мл суспензии 2-3 раза/сутки.
- ВЗК: по 1-2 таб 2-3 раза/сутки, после 12 лет.
- Симптомы дивертикулеза, дивертикулита: по 200-400 мг 2-3 раза/сутки, старше 12 лет.
- Печеночная энцефалопатия: по 400 мг 3 раза/сутки, после 12 лет.
- Профилактика осложнений операций: 400 мг 2 раза/сутки, начало приема за 3 дня до вмешательства.
Детям и при затруднении приема таблеток назначают суспензию, 200 мг=10 мл.
В среднем курс лечения – 7 дней, повторный – через 3-5 недель. Врач может изменить курс, дозировку, частоту приема.
Противопоказан до 12 лет, при непереносимости, кишечной непроходимости, сильной диарее с кровью.

Энтеробактерии (лат. enterobacteriaceae) — семейство грамотрицательных (как и другие протеобактерии) палочкообразные (бациллы), споронеобразующие бактерии, длиной 1-5 мкм, со жгутиками для передвижения. Эти бактерии — факультативные анаэробы, расщепляют углеводы с образованием муравьиной кислоты и других конечных продуктов формиатного брожения. Некоторые из них могут разлагать лактозу.
Множество представителей семейства являются частью микрофлоры кишечника человека и животных. Они представляют большое число нормальной микрофлоры человеческого организма и значительное количество патогенных микробов: сальмонелла, кишечная палочка, чумная палочка и др. Энтеробактерии определяют в различных отделах желудочно-кишечного тракта здорового человека: в тощей кишке – от 0 до 103 КОЕ/мл, в подвздошной — от 10 2 до 10 6 КОЕ/мл. В норме в составе факультативной микрофлоры кишечника они не должны превышать количество 10 4 КОЕ/г.
Другая часть этих бактерий обнаруживается в воде и почве или паразитирует на различных растениях и животных. Хорошо изучена кишечная палочка — модельный организм, используемый в молекулярной биологии и генетике, в связи с изученностью её генетики и биохимии.
Энтеробактерии в воде и почве месяцами остаются жизнеспособными, но за несколько минут гибнут от дезинфектантов и при очень высоких температурах через 1 час.
Эти бактерии вырабатывают сахаролитические, протеолитические и др. ферменты, определение которых имеет таксонометрическое значение. Образуют индол, а глюкозу, лактозу, маннит ферментируют до кислоты и газа.
Факторами патогенности являются:
- эндотоксин, который освобождается после разрушения микробных клеток и адгезины,
- цитотоксин,
- экзотоксин.
Бактерии могут проникать в макрофаги и размножаться в них. Патологический процесс усугубляется на фоне снижения активности фагоцитоза, падения барьерной функции тканей. Снижение в кишечнике полезной нормофлоры и нарушение колонизационной и защитной функции может приводить к проникновению в лимфу и кровь. Коли-бактериозы возникают при снижении количества полезной микрофлоры кишечника и иммунитета. После перенесённого заболевания невосприимчивость не формируется.
Какие заболевания вызывают энтеробактерии?

энтреробактерии e.coli
Группа энтеробактерий включающая: сальмонеллы, шигеллы, эшерихии, клебсиеллы, собственно энтеробактер, серрации, протей, морганеллы, провиденции и иерсинии в норме обитают в желудочно-кишечном тракте человека, но при снижении защитных свойств слизистой кишечника, могут вызывать инфекции желудочно-кишечного тракта или других органов.
Энтеробактерии — представители родов citrobacier, ewardsiella, enterobacter, escherichia, hafnia, klebsiella, proteus, providencia, salmonella, serratia, yersinia вызывают инфекции мочеполовой системы (в том числе циститы, пиелонефриты, цервициты и т.п.). До 80% бактерий, обнаруживаемых в моче — энтеробактерии.
Энтеробактерии становятся причиной различных заболеваний человека. Условно – патогенные бактерии вызывают гнойно-воспалительные процессы различной локализации: как эндогенные процессы — развиваются инфекции мочевыводящих путей (уретрит, цистит, пиелонефрит), половой системы (вагинит, трихомиоз, цервицит), дыхательных путей (пневмония), желудочно-кишечного тракта (холециститы, сальмонеллез, дизентерия, чума) и другие, так называемые коли-бактериозы, а как экзогенные – нагноение ран. Разные формы ОКЗ – острых кишечных заболеваний обусловлены патогенным действием различных энтеробактерий и чем агрессивнее токсины бактерий, тем тяжелее состояние, особенно у маленьких детей.
Escherichia coli – кишечная палочка в норме определяется в желудочно-кишечном тракте и синтезирует секреторные иммуноглобулины и колицины. Они тормозят рост некоторых патогенных энтеробактерий и препятствуют проникновению их в слизистую оболочку стенки кишечника. E. сoli участвует синтезе витамина К (свертываемость). Некоторые патогенные штаммы кишечной палочки могут поражать слизистую кишечника, что проявляется кровавым водянистым поносом или диареей путешественников.
У детей диарея, вызываемая патогенной энтерогеморрагической кишечной палочкой, может осложняться гемолитико-уремическим синдромом и почечной недостаточностью. Эта бактерия может поражать кровь, желчный пузырь, легкие, мочевыводящие пути и кожу. У новорожденных детей, особенно недоношенных, кишечная палочка может стать патогенным возбудителем бактериемии и менингита.
Инфекции, обусловленные клебсиеллами (Klebsiella), энтеробактериями (Enterobacteriaceae) и серрациями (Serratia), обычно встречаются в больницах, чаще при снижении способности бороться против инфекций. Эти бактерии также часто поражают мочевыводящие, половые органы. Пневмония, вызванная клебсиеллами, наиболее распространена у больных сахарным диабетом и у злоупотребляющих алкоголем и имеет часто тяжелое течение.
Симптоматика инфекций, вызываемых энтеробактериями.
Симптомы инфекционного заболевания могут быть различны, в зависимости от места развития воспалительного процесса, однако все больные жалуются на общую слабость, повышение температуры, проявления интоксикации и боли в месте заболевшего органа. Для определения патогенных энтеробактерий обязательно нужно сдать анализы – кровь, мочу, мокроту, мазки или кал, в зависимости от локализации воспалительного процесса, пройти до обследование, для выявления функциональных нарушений.
Важно соблюдать правила личной гигиены, следить за качеством, чистотой овощей-фруктов, питаться, учитывая индивидуальные особенности, избегать контакта с инфекционными больными и поддерживать свой иммунитет в норме.
Как быстро восстановиться после инфекции?
Восстановление и сохранение достаточного количества полезной нормофлоры кишечника – лакто- и бифидобактерий, способствует защите слизистой кишечника от проникновения патогенных бактерий и их токсинов в кровь и лимфу, выведению токсинов, созданию среды, в которой патогенные микроорганизмы не могут продолжать свою жизнедеятельность и выводятся из организма человека. Важно, что продукты жизнедеятельности полезных бактерий помогают иммунитету сохранять активность в борьбе с вредными бактериями.
Синбиотический биокомплекс Нормофлорины – содержащий живые активные лакто- и бифидобактерии и их метаболиты с противовоспалительным, антисептическим, иммуногенным и питательным действием на слизистые за многие годы зарекомендовал себя, как активный помощник и борец против патогенных бактерий для малышей и взрослых, беременных и больных с различными заболеваниями. Достаточно быстро при употреблении Нормофлоринов снимается интоксикация и восстанавливается функция кишечника, общее самочувствие.
Рекомендуется: как можно раньше начать принимать Нормофлорины в возрастных дозировках – Л – за 10-15 мин до еды утром (+ обед при запорах), Д – обед или вечер за 20 мин до еды, Б – на ночь или в микроклизме. Длительность приема 3-4 недели, до полного восстановления функции кишечника и улучшения общего самочувствия. Желательно 10-14 дней натощак принимать сорбенты – для выведения токсинов – зостерин или пекто, они уменьшают гнилостные, бродильные процессы, повышенное газообразование, улучшают работу кишечника.
Важно закрепить эффект восстановления микрофлоры, улучшить работу поджелудочной железы, печени, кишечника, иммунитет – для этого хорошо далее в течение месяца использовать функциональное питание – Гармония жизни. В её составе также содержатся живые полезные лакто- и бифидобактерии, их метаболиты и пектин. Вкусно, полезно и эффективно!

В летний период становятся актуальны заболевания вызванные инфекционными агентами.
Особенно активны микроорганизмы семейства энтеробактерий – грамотрицательные, палочкообразные, с жгутиками для передвижения и прикрепления, факультативные анаэробы: кишечная палочка, сальмонелла, клебсиелла и др. Так, клебсиелла – klebsiella, может существовать в почве, воде, месяцами оставаясь жизнеспособной, сохраняется на пище и пыли.
Клебсиеллы могут попасть в организм через желудочно-кишечный тракт, с плохо вымытых рук, овощей и фруктов, с водой, с почвой. Однако, этот микроорганизм входит в группу условно-патогенной микрофлоры и определяется у абсолютно здоровых детей и взрослых, считается одним из элементов нормальной флоры кишечника.
При этом, клебсиелла является одной из самых распространённых внутрибольничных инфекций, т.к. она устойчива к действию факторов окружающей среды, высоким температурам. Хотя, за несколько минут она гибнет от дезинфектантов, а при очень высоких температурах через 1-1,5 часа. При несоблюдении надлежащих правил гигиены, санитарных норм в помещениях, встречаются случаи заражения новорожденных клебсиеллой в роддомах. Малыш постоянно плачет и не может заснуть, его беспокоят колики и частый понос. А причина — клебсиелла – бактерия, устойчивая к губительному действию внешней среды, покрытая плотной капсулой.
Факторы развития клебсиеллеза
Клебсиеллы относятся к одному семейству с бактериями рода Serratia и Enterobacter. Этими возбудителями, особенно Serratia, обладающий наибольшей лекарственной устойчивостью, обусловливаются вспышки инфекции в стационарах, в связи с загрязнением ряда медикаментозных средств, лекарственных растворов, применяемых в терапии органов дыхания. Их трудно, но можно дифференцировать только с помощью специальных проб. Klebsiella Enterobacter и Serratia, вызывающие внутрибольничную пневмонию, инфекцию мочевого тракта, бактериемию, обладают различной чувствительностью к противомикробным препаратам.

Позитивное окрашивание. Клетка K. pneumaniae. Ув. x6000
Если защита организма человека по какой то причине ослаблена: снижен общий иммунитет, часто грипп, ОРВИ, применение антибиотиков, употребление загрязненных, некачественных продуктов, сахарный диабет, алкоголизм и др., клебсиелла начинает активно размножаться, выделять токсины, вызывая эндотоксимию и воспалительные процессы в разных органах. Развиваются такие заболевания, как воспаление легких, воспалительные заболевания мочевыводящих путей, менингит, конъюнктивит, кишечные инфекции, сепсис и достаточно редкие болезни – озена (зловонный насморк), риносклерома.
Наиболее часто клебсиелла вызывает пневмонию и поражение кишечника. У взрослых людей чаще встречается пневмония, вызванная палочкой Фридлендера. В связи с особенностью иммунитета новорожденных и недостаточностью у них нормальной микрофлоры на коже, в дыхательных путях и особенно в кишечнике — клебсиелла — Klebsiella oxytoca — чаще вызывает поражения желудочно-кишечного тракта — толстого кишечника.
Симптомы клебсиеллы (клебсиеллёза) в ЖКТ у грудничков
Симптомы клебсиеллы у малышей схожи с симптомами дисбактериоза: вздутие, метеоризм, колики, срыгивание. Но чаще проявляются — жидким стулом со слизью, кровью и резким запахом, повышением температуры, лихорадкой, болями в животе и сильным обезвоживанием организма. В зависимости от того, какой иммунитет у малыша, течение заболевания может протекать как в лёгкой форме, так и грозить тяжелыми инфекционными осложнениями. Если клебсиелла в организме быстро размножается, выделяет токсины, нарастает интоксикация, обезвоживание, то заболевание может проявиться в течение нескольких часов и потребует срочной госпитализации ребенка.
Поэтому, при любом расстройстве стула, необходимо обратиться к врачу, сдать кал ребёнка на анализ, пройти обследование, чтобы точно выявить, какие именно бактерии вызвали изменение состояния ребёнка. Большую роль в восстановлении иммунитета и нормальной микрофлоры у новорожденного играет грудное вскармливание. При высокой обсеменённости клебсиеллой и тяжёлой форме заболевания, лечении ребенка в больнице, назначают сложную терапию с применением антибиотиков. Если заболевание грудничка протекает в лёгкой форме, то для коррекции микрофлоры кишечника назначают пробиотики. Синбиотики – Нормофлорины Л и Б – обладают активным противовоспалительным, антисептическим и питательным действием, что важно при клебсиеллёзной инфекции. Ребенок может чувствовать себя нормально, а при обследовании находят в анализах повышение количества клебсиелл. Тогда препараты с лакто- и бифидобактериями назначают для вытеснения излишнего количества клебсиеллы, повышения иммунитета, улучшения собственной полезной микрофлоры.
Симптомы клебсиеллы в других органах и системах
Если клебсиеллы попадают в мочевыделительную систему, то они способны вызывать уретрит, пиелонефрит, со стойким рецидивирующим течением, плохо поддающимся терапии и часто измененной чувствительностью к антибиотикам. В редких случаях клебсиеллёза, возможно такое осложнение, как – озена — зловонный насморк, с поражением слизистой носа, образованием гнойных, болезненных, кровоточащих корок.
Симптомы и признаки инфекций мочевыводящих путей, желчного пузыря и в брюшной полости, вызываемых клебсиеллами, не отличаются от симптоматики, обусловленной кишечной палочкой. Развиваются они чаще у больных сахарным диабетом и у пациентов, получающих антимикробные препараты, к которым устойчив возбудитель заболевания. Клебсиелла является также важным этиологическим фактором септического шока.
Клебсиелла известна как фактор развития легочных заболеваний, однако, среди причин, вызывающих бактериальную пневмонию, имеет около 1% всех случаев. Встречается преимущественно у мужчин в возрасте старше 40 лет, с хроническими бронхолегочными заболеваниями, больных сахарным диабетом и лиц с алкоголизмом. У пожилых людей, грамотрицательные бактерии заселяют ротоглотку и могут распространиться по дыхательному тракту, вызывая пневмонию или гнойный бронхит.
Клинические симптомы клебсиеллёзной пневмонии сходны с проявлениями при пневмококковой пневмонии, но чаще характеризуются более тяжелым течением: внезапным началом, ознобов, стойким повышением температуры тела, продуктивным кашлем, иногда с прожилками крови и резким запахом, с сильными плевральными болями, появлением одышки. Больные часто находятся в прострации и бредовом состоянии, за счет интоксикации. Чаще всего очаг воспаления располагается в правой верхней доле легкого, но может быстро прогрессировать, если лечение не проводится и распространиться с одной доли на другую. Появляются цианоз и одышка, могут возникнуть желтуха, рвота, диарея. Выявляется, при обследовании, образование плеврального выпота, уплотнение легочной ткани, или некротизирующая пневмония, с быстрой кавернизацией. На фоне интоксикации определяется снижение количества лейкоцитов в периферической крови, а не повышение, как при воспалении. Гораздо чаще наблюдаются абсцессы и эмпиемы легких. Это объясняется способностью клебсиелл вызывать деструкцию ткани. Не всегда выявляются характерные признаки при рентгеновском обследовании: уменьшение объема легкого, его уплотнение, эмфизематозные изменения. При медленном прогрессировании инфекционного воспалительного процесса может развиться хронический некротизирующий пневмонит, напоминающий туберкулез, с продуктивным кашлем, слабостью, выраженной анемией.
Лечение клебсиеллезов
Лечение заболеваний, вызванных клебсиеллой, зависит от локализации и выраженности патологического процесса. Антибиотики назначают в тяжелых случаях по чувствительности, при легком течении или только обнаружении в анализах повышения клебсиелл — не применяют. Обязательно используют разнообразные препараты, восстанавливающие кишечную микрофлору.
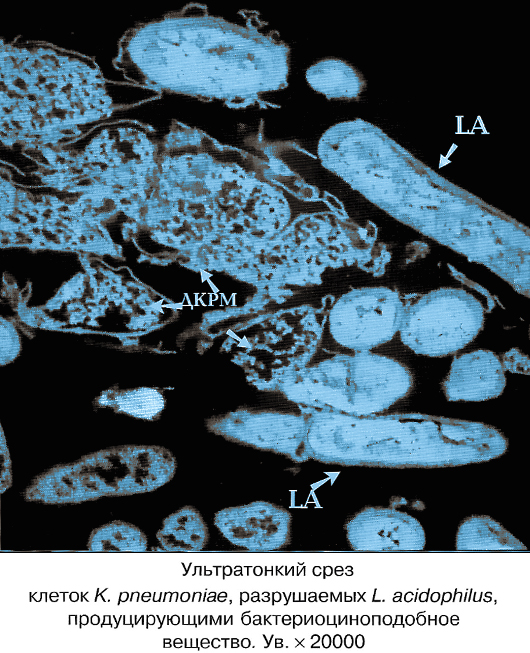
Клебсиелла пневмония
Как правило, антимикробную терапию рекомендуют начинать еще до получения результатов посева и определения лекарственной чувствительности к антибиотикам. В этом случае биокомплексы Нормофлорины, содержащие продукты жизнедеятельности живых лакто- и бифидобактерий с активным антисептическим, противовоспалительным действием, оказывают лечебный эффект при клебсиеллёзах, что доказано научными исследованиями и многолетней практикой, как у новорожденных, беременных, кормящих, так и взрослых и пожилых.

Сегодня мы закончим разговор о микроорганизмах из семейства Enterobacteriaceae, которое, как мы помним, является одним из самых проблематичных источников внутрибольничных инфекций, потому что возбудители умеют делиться и передавать в рамках почти всего семейства свои механизмы резистентности, и это при том, что изначально почти каждый представитель имеет природную устойчивость к целым классам антибиотиков.
Материалы предназначены исключительно для врачей и специалистов с высшим медицинским образованием. Статьи носят информационно-образовательный характер. Самолечение и самодиагностика крайне опасны для здоровья. Автор статей не дает медицинских консультаций: клинический фармаколог — это врач только и исключительно для врачей.
Автор: врач – клинический фармаколог Трубачева Е.С.
Сегодня мы закончим разговор о микроорганизмах из семейства Enterobacteriaceae, которое, как мы помним, является одним из самых проблематичных источников внутрибольничных инфекций, потому что возбудители умеют делиться и передавать в рамках почти всего семейства свои механизмы резистентности, и это при том, что изначально почти каждый представитель имеет природную устойчивость к целым классам антибиотиков.
Героями сегодняшнего разговора станут энтеробактеры, серрации, морганеллы. Конечно, есть и другие представители и, возможно, в постковид они начнут встречаться намного чаще, но пока нам в рамках Азбуки достаточно вышеперечисленных плюс кишечные палки и клебсиеллы, о которых мы говорили ранее.
Enterobacter spp.
Микробиологические аспекты
Род энтеробактера включает несколько видов, но наиболее клинически значимыми из них являются:
Очень важно помнить, что энтеробактеры проявляют природную устойчивость к большому спектру антибиотиков, таким как бета-лактамы, к которым они продуцируют хромосомные AmpC бета-лактамазы, плазмидные бета-лактамазы расширенного спектра, а также карбапенемазы. Так как клинически значимые представители Enterobacter spp. обитают в желудочно-кишечном тракте человека, то основным источником инфицирования для пациента становится медицинский персонал, который просто по факту своей ежедневной работы в больнице с антибиотиками является резервуаром всевозможных антибиотикорезистентностей.
Клинически значимые аспекты
Enterobacter spp. является причиной:
- Инфекций мочевыводящих путей: катетер – или инструментально-ассоциированных (как результат эндоскопических манипуляций контаминированным инструментарием).
- Внутрибольничных пневмоний, в том числе вентилятор-ассоциированных.
- Инфекций кожи и мягких тканей, таких как раневые инфекции, инфицирование пролежней, ожоговые инфекции и послеоперационные инфекции. Кроме того в случае полимикробного характера инфицирования пролежней возможно развитие сепсиса как исхода раневой инфекции.
- Инфекций кровотока – катетер – и инструмент-ассоциированные.
- Инфекций центральной нервной системы — менингиты, чаще всего внутрибольничные, как следствие нейрохирургических вмешательств.
- Неонатальных инфекций, таких как некротический энтероколит, сепсис и менингит.
Чем лечить?
Ответ будет традиционным – лучше вообще не инфицировать, тогда не придется ломать голову, чем все это лечить. В основе терапии лежит обязательное микробиологическое исследование с определением антибиотикочувствительности.
В случае выявления представителей Enterobacter spp. при лечении тяжелых инфекций предпочтение следует отдавать комбинированной терапии, и самыми подходящими будут пиперациллин-тазобактам в комбинации с аминогликозидами или фторхинолонами. А для преодоления резистентности, вызванной бета-лактамазами расширенного спектра, можно использовать карбопенемы.
Для лечения инфекций мочевыводящих путей самым первым и наиважнейшим является удаление мочевого катетера до момента прекращения пиурии. Далее лечим либо исходя из профиля антибиотикограммы, либо ципрофлоксацином в правильно подобранной дозе, либо, как было указано выше, рассматриваем назначение нитрофуранов и фосфомицина.
Serratia spp.
Клинические аспекты
Что вызывает?
- Катетер-ассоциированные инфекции и как их исход – сепсис.
- Инфекции мочевыводящих путей как следствие медицинских манипуляций необработанным инструментом.
- Раневые инфекции в послеоперационном периоде.
- Нозокомиальные пневмонии как следствие интубации.
- Септические артриты.
- Конъюнктивиты и кератиты.
- И редко вызывали остеомиелиты и эндокардиты
Терапевтические аспекты
В первую очередь про серрацию надо узнать, а значит, необходимо микробиологическое исследование. Во-вторую, вспомнить о природной устойчивости. В-третью, держать в уме то, что очень часто цефалоспорины третьего и четвертого поколения тоже не будут работать, так как посредством плазмид получают устойчивость от родственников по семейству Enterobacteriaceae, например, от родной сестры – клебсиеллы. Точно таким же образом серрация может оказаться устойчивой и к карбопенемам. К фторхинолонам резистентность так же уже давно описана.
Так чем лечить?
Лучше вообще не заражать – потому что если бак. лаборатория дает серрацию, то ниоткуда кроме как с наших рук она появиться не может, так как ни ходить, ни летать сия зверюшка до сих пор не научилась.
В случае развития тяжелых инфекций – сепсиса, вентилятор-ассоциированной пневмонии и т. п., и только при документированной чувствительности, препаратами выбора могут быть цефепим или меропенем, или ципрофлоксацин в вену в стандартных дозировках. Если чувствительность утеряна, то зовем клинического фармаколога, а если такового нет, то смотрим в сторону амикацина, пиперациллина-тазобактама и азтреонама, только помним об их побочных эффектах. Курс лечения соблюдать жизненно необходимо, чтобы зверюшка еще куда-нибудь не мутировала и новыми механизмами защиты не обзавелась. Обычно речь идет о 10-14 днях (но так как польза превышает вред, то нефротоксичность аминогликозидов со временем отступит, а ототоксичность – тут уж как повезет).
Инфекции мочеполового тракта лечим так же с учетом чувствительности, и если таковая располагает, то препаратом выбора становятся фторхинолоны, либо комбинация двух антибиотиков, например фторхинолон с карбапенемом или бета-лактам с аминогликозидом.
Эндокардиты с остеомиелитами бывают хоть и редко, но крайне метко, а потому снова сначала исследуем чувствительность, потом индивидуально в каждом случае подбираем антибиотики (а лучше зовем клинического фармаколога, пусть он мучается). И снова крайне важно соблюдение сроков лечения, для эндокардита это порядка четырех, а то и шести недель внутривенной антибактериальной терапии, а для остеомиелита не менее двух недель. Почему нельзя меньше? Потому что последует мутация и новый рецидив, а антибиотиков просто может не хватить, ибо, как и сестра-клебсиелла, серрация тоже умеет в панрезистентность.
В заключении хочется повторить, что и в этом случае проще помыть руки, чем разгребать последствия инфицирования серрацией. Мытье рук и проще, и дешевле, и, что самое главное, спокойнее.
Morganella spp.
Морганеллы будут последними представителями семейства Enterobacteriaceae, которых мы обсуждаем в рамках нашей Азбуки. Если кому-то станет интересно покопаться дальше, то к их услугам всегда будет четырехтомник по медицинской микробиологии под редакцией Лабинской, конкретно второй и третий том, в которых все очень подробно расписано, правда, чтение это для неподготовленного человека будет довольно сложным. Но вернемся к нашей морганелле.
Микробиологические аспекты
Морганелла существует только одна – M.morganii, но имеет два подвида – M.morganii и M.sibonii, которые отличаются только по ферментации треалозы, и никакого клинического значения данное отличие не имеет.
Конечно, и морганелла умеет в природную устойчивость к антибиотикам, а именно к пенициллинам, цефалоспоринам первого и второго поколения, макролидам и ко-тримоксазолу. При этом сохраняет высочайшую чувствительность к аминогликозидам, пиперациллину, цефалоспоринам третьего и четвертого поколения, фторхинолонам и карбопенемам. То есть данную зверюшку есть чем победить.
Клинические аспекты
Морганелла является представителем нормальной микрофлоры человека и самостоятельно крайне редко что-то вызывает. Этим крайне редким являются инфекции мочевыводящих путей, чему способствуют крайне пожилой возраст, длительная госпитализация, мочевой катетер и иммунодефицит любой этиологии.
В плане приобретенной антибиотикорезистентности морганелла обзавелась факторами устойчивости к фторхинолонам, что и понятно, учитывая какие именно заболевания она вызывает и чем их чаще всего лечат.
Что еще может вызывать?
- Крайне редко – сепсис, как исход инфекции мочевыводящих путей.
- Раневую хирургическую инфекцию.
- Септический артрит.
- Неонатальный сепсис и хореоамнионит.
- Менингит.
- Перикардит.
Но стоит иметь в виду, что данные ситуации крайне редки, и стоит изначально подумать не об этом возбудителе, а о том, какой за ним может прятаться в виду контаминации материала, и лучше бы все еще раз пересеять и перепроверить.
Терапевтические аспекты
Если результат микробиологического исследования сомнений не вызывает и вы убеждены, что имеете дело с морганеллами, то препаратами выбора становятся карбопенемы, и только в случае их недоступности и документированной бактериологом чувствительности, можно посмотреть в сторону цефалоспоринов, например, цефтазидима (для которого нужна отдельная цефалоспориназа, чтобы он был инактивирован), а лучше цефтазидим-авибактама. Хотя если недоступны карбопенемы, то и Завицефте, скорее всего, взяться будет неоткуда.
Какие препараты могут быть использованы в качестве резервных? Решать этот вопрос также необходимо только после получения результата микробиологии и чувствительности в идеале по МПК, и только после этого рассматривать назначение цефепима или ципрофлоксацина, или аминогликозидов (они, к слову, в случае морганеллы могут обоснованно выступать в качестве монотерапии инфекций мочевыводящих путей).

Энтеробактерии (лат. Enterobacteriaceae) — семейство грамотрицательных палочкообразных споронеобразующих бактерий, факультативные анаэробы.
Семейство энтеробактерий включает большое число представителей нормальной микрофлоры человеческого организма и, в то же время, значительное количество патогенных микробов.
Систематика энтеробактерий
Энтеробактерии (Enterobacteriaceae) входят в порядок энтеробактерии (лат. Enterobacteriales), класс гамма-протеобактерии (лат. γ proteobacteria), тип протеобактерии (лат. Proteobacteria), царство бактерии.
По современным представлениям в состав Enterobacteriaceae входят следующие роды бактерий: Atlantibacter, Biostraticola, Buttiauxella, Cedecea, Citrobacter (цитробактер), Cronobacter, Enterobacillus, Enterobacter (энтеробактер), Escherichia (эшерихии), Franconibacter, Gibbsiella, Izhakiella, Klebsiella (клебсиеллы), Kluyvera, Kosakonia, Leclercia, Lelliottia, Mangrovibacter, Pluralibacter, Pseudocitrobacter, Raoultella, Rosenbergiella, Salmonella (сальмонеллы), Shigella (шигеллы), Shimwellia, Siccibacter, Trabulsiella, Yokenella.
В качестве кандидатов рассматриваются роды: Aschnera, Curculioniphilus, Cuticobacterium, Gillettellia, Ishikawaella, Macropleicola, Moranella, Phlomobacter, Profftia, Riesia, Rohrkolberia, Schneideria, Stammerula.
До недавнего времени состав родов семейства энтеробактерий был следующий: Alishewanella, Alterococcus, Aquamonas, Aranicola, Arsenophonus, Averyella, Azotivirga, Brenneria, Buchnera, Budvicia, Buttiauxella, Cedecea, Citrobacter, Dickeya, Edwardsiella, Enterobacter, Erwinia, Escherichia, Ewingella, Grimontella, Hafnia, Klebsiella, Kluyvera, Leclercia, Leminorella, Moellerella, Morganella, Obesumbacterium, Pantoea, Pectobacterium, Photorhabdus, Plesiomonas, Pragia, Proteus (протей), Providencia, Rahnella, Raoultella, Salmonella, Samsonia, Serratia, Shewanella, Shigella, Sodalis, Tatumella, Thorsellia, Tiedjeia, Trabulsiella, Wigglesworthia, Xanthomonas, Xenorhabdus, Xylella, Yersinia (иерсинии), Yokenella. Роды Blochmannia и Phlomobacter рассматривались как кандидаты в семейство Enterobacteriaceae.
Примечания. 1. Исходя из соображений определённости и удобства пользования мы ориентируемся на систематику Национального центра биотехнологической информации США (National Center for Biotechnology Information), не утверждая, что она чем-то лучше или хуже других.
2. Неклассифицированные в отдельные виды штаммы, имеющие в своих названиях цифро-буквенные коды и т.п. штаммы и виды в данной статье не приведены.
Энтеробактерии — возбудители заболеваний

-
— ряд патогенных серотипов могут быть причиной различных инфекционных заболеваний, протекающих с интоксикацией, лихорадкой, обычно с поражением желудочно-кишечного тракта (различные диареи, в том числе диарею путешественников, геморрагический колит, гемолитико-уремического синдром и другие), реже — мочевыводящих, желчевыводящих путей, других органов или с развитием сепсиса
-
была причиной кишечной инфекции 2011 года со смертельными исходами в Германии и других странах Европы
Энтеробактерии — представители родов Citrobacier, Enterobacter, Echerichia, Klebsiella, Salmonella могут вызывать инфекции мочеполовой сферы (в том числе циститы, пиелонефриты, острые и хронические простатиты, эпидидимиты и орхиты и т.п.). Бактериурия — наличие бактерий в моче человека может быть только в том случае, если почки, мочевой пузырь или мочеточники инфицированы патогенными бактериями. До 80% бактерий, обнаруживаемых в моче, — энтеробактерии.
Энтеробактерии могут быть причиной вагинитов (воспаления влагалища), цервицитах (воспаления канала шейки матки), других воспалительных гинекологических заболеваниях. Энтеробактерии во влагалище обычно выявляются у пациенток, не соблюдающих правила личной гигиены.
Энтеробактерии могут быть инфекционным агентом при перитоните.
Энтеробактерии — нормальная флора кишечника человека
Энтеробактерии присутствуют в различных отделах желудочно-кишечного тракта здорового человека. Их количество увеличивается от проксимальных отделов (в тощей кишке обнаруживается от 0 до 10 3 КОЕ/мл энтеробактерий, в подвздошной — от 10 2 до 10 6 КОЕ/мл) к дистальным.
Публикации для профессионалов здравоохранения затрагивающие проблематику, связанную с энтеробактериями
Антимикробные препараты, активные в отношении энтеробактерий
Читайте также:

