Если внутриутробная инфекция из-за гайморита
Обновлено: 19.04.2024
При беременности у женщины происходит природное снижение иммунитета абсолютно во всех случаях. Это норма, необходимый процесс для вынашивания ребенка, профилактика отторжения плода как чужеродного в принципе организма. Потому инфекции, которые до момента зачатия дремали, становятся активными. Это опасно для плода, особенно в первые 3 месяца после зачатия.
Факты о ВУИ
В менее чем 10 беременностях из 100 инфекция передается будущему малышу от его мамы. И примерно 0,5% новорожденных появляются на свет с соответствующими симптомами. Но, если в организме матери присутствует та или иная инфекция, это еще не полная гарантия того, что она будет и у ребенка.
Часть инфекционных болезней, которые угрожают развитию эмбриона, для матери проходят безсимптомно, не нанося особого вреда ее организму. В основном плод заражается той же инфекцией, что и мать, если она заразилась этой болезнью впервые.
Если у беременной вовремя обнаружить и пролечить болезнь, то риск для будущего малыша минимальный.
Как заражается эмбрион?
ВУИ развивается тремя путями:
- гематогенным или трансплацентарным, как например, вирусы, листериоз, токсоплазмоз, сифилис (заражение в первом триместре приводит к уродствам малыша и порокам развития; при заражении эмбриона в последние 3 месяца гестации новорожденный появляется на свет с симптоматикой острой формы заболевания)
- восходящим (так могут передаваться герпетическая инфекция, хламидиоз, микоплазмоз; ребенок заражается через половые пути женщины, в основном это происходит при родах. Если инфекция попала в околоплодные воды, у ребенка будет поражен ЖКТ, дыхательный пути, кожа)
- нисходящим (инфекция попадает к эмбриону через маточные трубы, что бывает, если у матери развивается оофорит, аднексит)
Возбудители ВУИ
Большая часть бактерий и вирусов может передаваться еще нерожденному ребенку, что вызывает серьезные последствия. Те вирусы, которые провоцируют острые респираторные вирусные заболевания, к плоду не попадают. Они могут быть опасны для малыша, только если беременная женщина имеет высокую температуру.
Краснухой мать может заразиться воздушно-капельным путем. Не обязательно при этом находиться вплотную к больному человеку, заражение вероятно и на расстоянии. При этом последствием для плода станет фетальный синдром краснухи.
Цитомегаловирус передается через биологические жидкости. В основном это слюна, но может быть сперма и моча, а также кровь. У ребенка инфекция может проявиться соответствующей симптоматикой после рождения, а может протекать в латентной форме.
Вирус простого герпеса 2 передается в основном при незащищенном половом акте. Если такое случилось у беременной, то ее ребенок родится с врожденной формой герпеса. Парвовирус В19, как и краснуха, передается воздушно-капельным путем беременной женщине. В итоге у плода возникает водянка и анемия.
Ветряная оспа передается не только по воздуху, но и бытовым путем. Ребенок получает при внутриутробном инфицировании пороки развития (если заражение произошло в первом триместре). Если заражение случилось перед родами, то будет врожденная форма данного заболевания, и это очень опасное состояние.
Листериоз (это бактериальная инфекция) может развиться у беременной, если она кушает зараженные сыры, мясо или овощи. У ребенка развивается в итоге пнемония и/или сепсис. Сифилис беременным передается половым путем, если партнер был заражен. У ребенка после рождения развивается эта болезнь со всеми вытекающими последствиями. Туберкулез, что также является бактериальной инфекцией, передается по воздуху. Эмбрион может умереть в утробе матери, родиться раньше срока, с врожденной формой туберкулеза.

Последствия внутриутробной инфекции
Врожденное заражение может быть острым или хроническим. Последствия острого инфицирования:
- шок
- пневмония
- тяжелый сепсис
Симптомы острой внутриутробной инфекции у новорожденных:
- уменьшающаяся с каждым днем активность
- длительный сон
- плохое питание
Но в большинстве случаев симптоматики нет. Отдаленные последствия ВУИ:
- задержка двигательного развития
- психические проблемы
- нарушения зрения
- частичная или полная глухота
Если инфекция проникла через матку, последствиями могут быть:
- мертворождение
- антенатальная гибель эмбриона
- выкидыш
Если плод выжил, у него будут такие проявления ВУИ:
- Лихорадка
- Кожные высыпания
- Водянка плода
- Анемия
- Желтуха и увеличенная печень
- Пневмонии
- Миокардит
- Хориоретинит, катаракта
- Микро- и гидроцефалия
Внутриутробное инфицирование опасно вне зависимости от срока гестации. Но некоторые возбудители болезней опаснее всего в первые 3 месяца. Яркий пример — вирус краснухи. Очень серьезные последствия будут при заражении на самой последней недели беременности матери ветряной оспой. Последствия могут быть самыми разными. О них можно узнать у своего врача по результата УЗИ, анализов, сроку беременности и обнаруженному возбудителю болезни. Это значит, что каждый случай индивидуален в плане протекания болезни и в плане последствий.
Группы риска по внутриутробному заражению
Осторожными нужно быть женщинам, которые:
- проживают в семье с детьми, которые ходят в детсад, школу, другие учреждения
- работают в сфере медицины, контактируя с носителями болезней или больными людьми
- работают в дошкольных и школьных детских учреждениях
- имеют 2 и больше медицинских аборта
- больны воспалительными патологиями, протекающими в хронической форме
- имеют несвоевременное излитие околоплодных вод
- имеют в анамнезе пороки развития эмбриона и антенатальную гибель плода
- когда-то родили зараженного ребенка (одного или больше)
Симптомы и последствия
Ниже перечислены признаки, которые указывают на инфекцию у беременной:
- кашель, одышка
- сыпь
- лимфоузлы болезненны и увеличены
- высокая температура
- болезненность и припухлость суставов
- насморк, слезотечение, конъюнктивит
- боль в груди
Но эти симптомы в некоторых случаях указывают на аллергическую реакцию. Если это так, то нет риска внутриутробной инфекции малыша. В любом случае, при появлении одного и больше из выше перечисленных признаков нужно идти на очную консультацию к врачу.
ЦМВ (цитомегаловирус)
ЦМВ (цитомегаловирус) относится к группе герпесовирусов. Им заражаются при половых контактах, при тесных бытовых контактах, а также через кровь (если была сделана операция грязными инструментами или переливание от больного донора). Если имело место первичное заражение беременной, то вирус попадает в плаценту, а оттуда к малышу. У ребенка может не быть последствий, что и бывает в большинстве случаев. Но 10 из 100 детей, у которых были больные матери, рождаются с симптоматикой ВУИ.
Последствиями внутриутробного заражения ЦВМ могут стать выкидыши и мертворождения, а также:
- нейросенсорная тугоухость
- недовес при рождении
- гидроцефалия
- микроцефалия
- пневмония
- гепатоспленомегалия
- задержка психомоторного развития
- слепота различных степеней
Если имело место тяжелое сочетанное поражение, 1/3 новорожденных умирают в первые 2-3 месяца после родов. Также очень вероятны такие отдаленные последствия как умственная отсталость, слепота и глухота. Если заражение легкое, то последствия мене серьезные. На сегодня нет лекарства, которое бы помогло при проявлениях цитомегаловируса у недавно рожденных детей. При заражении беременной ЦВМ беременность не прерывают, потому что у ребенка может и не быть симптомов. Врачи прописывают для беременной лечение, чтобы минимизировать развитие осложнений.
ВПГ (вирус простого герпеса)
Врожденная герпетическая инфекция развивается, если у беременной был ВПГ, особенно 2 тип (который передается половым путем). Симптомы появляются в первый месяц после рождения. В основном ВУИ происходит при первичном инфицировании беременной. Ребенок подхватывает инфекцию в большинстве случаев при родах, когда проходит через родовые пути. Но возможность передачи возбудителя болезни через плаценту также нужно учитывать.
Последствия герпеса для ребенка:
- вялость, плохой аппетит
- выкидыш, мертворождение
- характерные высыпания на коже
- лихорадка
- нарушение свертываемости крови
- желтуха
- поражение мозга
- поражение глаз
- пневмония
Тяжелый врожденный герпес чреват инвалидизацией ребенка:
Краснуха
Краснуха очень опасна для эмбриона! Она вызывает различные уродства. Самый высокий риск приходится на беременность до 16-й недели. Последствия ВУИ возбудителем данной болезни:
- микроцефалия
- маловесность при рождении
- выкидыш, мертворождение
- пороки сердца
- глухота (в половине случаев ВУИ)
- катаракта
- поражение кожи
- пневмония
- гепатоспленомегалия
- менингит и энцефалит
Парвовирус В19
Последствия для ребенка при ВУИ:
- отеки
- анемия
- поражение мозга
- гепатит
- миокардит
Ветряная оспа
Если больная заразилась ветрянкой, это очень опасно для плода. Если беременная заразилась, а ей в скором времени срок рожать, то есть риск, что ее ребенок умрет. Плод заражается в 25 случаях из 100, но симптомы проявляются не всегда.
Врожденная ветрянка у малышей имеет такие признаки:
- повреждение мозга
- атрофия зрительного нерва, недоразвитие глаз
- недоразвитие конечностей
- сыпь, рубцы зигзагообразной формы
- пневмония
Новорожденных при ВУИ ветрянкой не лечат, потому что симптоматика не прогрессирует. Если мать заразилась за 5 суток до дня родов и позже, врачи могут советовать ввести новорожденному иммуноглобулин, потому что ему не передались антитела от матери.
Гепатит В
- гепатит В с последующим выздоровлением
- рак печени
- носительство и хроническая форма гепатита типа В
- острая форма гепатита (развивается печеночная недостаточность, ребенок умирает)
- задержка психомоторного развития
- нехватка кислорода
- маловесность
- выкидыш, мертворождение
ВИЧ-инфекция
Вирус иммунодефицита человека (ВИЧ) поражает особые иммунные лимфоциты. Заражение происходит в основном половым путем. Ребенок заражается, прибывая в утробе матери, или проходя при рождении через инфицированные половые пути роженицы. Если не лечить ребенка с врожденной формой ВИЧ, он не выживет даже двух лет, потому что вирус быстро прогрессирует в слабом организме. Смерть происходит от инфекций, которые у здоровых детей не могут привести к летальному исходу.
Чтобы обнаружить ВИЧ у новорожденного, в основном применяется ПЦР. В первые 3-6 месяцев после рождения нет смысла делать анализ на антитела. Важно обнаруживаться ВИЧ у тех, кто ждет ребенка. Им весь срок дают антиретровирусные лекарства, то есть в основном с 4-й недели гестации дается зидовудин. Они не должны кормить грудью своег7о новорожденного. Это в разы повышает шансы здоровья малыша.
Листериоз
Эта болезнь вызывается бактерией листерией. Она может проникать к эмбриону через плаценту, чего не могут многие бактерии. Пути заражения описаны выше. У беременной проявлений болезни может и не быть. В части случаев присутствуют:
- высокая температура
- понос
- рвота
- симптомы, похожие на таковые при гриппе
Последствия заражения плода:
- множественные гнойные очаги, сыпь
- сепсис
- менингит
- лихорадка
- отказ от еды
- мертворождение, спонтанный аборт
Если симптоматика проявилась в первые 7 дней после родов, то дети умирают в 60 случаях из 100. Потому, если у беременной точный диагноз листериоза, ей на 2 недели приписывают ампициллин. ВУИ также лечится, если ребенок действительно заразился от матери.
Сифилис
Первичный сифилис у беременных, который не лечили, передается почти в 100 случаях из 100. Из 10 детей погибают при этом 6, у других обнаруживается врожденная форма болезни. У больной беременной сначала образуется первичная язва, а потом болезнь переходит в латентную форму, время от времени обостряясь.
Заражение эмбриона происходит, даже если у матери болезнь протекает в скрытой форме, с 4-й недели гестации. Последствия ВУИ такие:
- глухота задержка психического развития
- поражение глаз, ушей, рук, ног, зубов
- трещины на коже
- высыпания на кожных покровах
- анемия, желтуха у малыша
- преждевременные роды или рождение мертвого плода
Токсоплазмоз
Передается человеку в основном от кошек, но может передаваться и от других животных. Заразиться беременная может, когда убирает за питомцем или кушает недостаточно термически обработанное мясо, грязные овощи. К моменту беременности большинство женщин уже болели этой болезнью, потому ребенку она не передастся.
При первичном заражении в период беременности в 50 случаях из 100 возбудитель преодолевает плацентарный барьер, заражая эмбрион. Последствия ВУИ для младенца:
- гидро-, микроцефалия
- поражение глаз
- желтуха, увеличение печени и селезенки , менингит, судороги
- мертворождение, выкидыш
- задержка психомоторного развития
TORCH-инфекции
Торч-инфекциями называются такие:
Они опасны при заражении беременной. Некоторые протекают в скрытой или стертой форме, потому их нужно выявлять анализами. Потому на этапе планирования зачатия пара сдает анализы на TORCH-инфекции. Если в организме будущей мамы не обнаруживаются антитела к возбудителю краснухи, ей делают прививку. Также во время беременности лучше не контактировать с кошками, чтобы не заразиться токскоплазмозом.
Диагностика внутриутробной инфекции
Беременным делают анализ крови, который позволяет обнаружить гепатиты В и С, а также сифилис. Регулярно делают мазки из влагалища на микрофлору. Используется метод ПЦР, который позволяет обнаружить циркулирующие в крови вирусы при наличии таковых.
УЗИ безопасна для беременных. Она не показывает наличие инфекции, но дает возможность обнаружить пороки, вызванные инфекцией, и задержку внутриутробного развития плода. Также УЗИ является методом контроля при выполнении кордоцентеза. ВУИ подозревают, если на УЗИ обнаруживаются такие признаки:
- сформировавшиеся пороки развития
- много- или маловодие
- отек плаценты, амниотические тяжи
- синдром задержки внутриутробного развития
- увеличение живота и расширение чашечно-лоханочной системы почек
- увеличение сердца, печени и селезенки
- множественные отложения кальция в мозге, печени, кишечнике
- увеличение желудочков мозга
Сероиммунологический метод диагностики базируется на определении иммуноглобулинов. Он рекомендован женщинам из групп риска, которые перечислены выше. Иногда необходимы такие методы как кордоцентез и амниоцентез. При первом методе берется кровь из пуповины, чтобы выявить имеющуюся там инфекцию. Амниоцентез означает исследование околоплодных вод.
У новорожденного, если у врача имеется подозрение на ВУИ, берут анализы биологических жидкостей, например, слюны или крови.
Внутриутробные инфекции – группа заболеваний плода и новорожденного, развивающихся вследствие заражения в дородовом периоде или в родах. Внутриутробные инфекции могут приводить к гибели плода, самопроизвольному аборту, задержке внутриутробного развития, преждевременным родам, формированию врожденных пороков, поражению внутренних органов и ЦНС. Методы диагностики внутриутробных инфекций включают микроскопические, культуральные, иммуноферментные, молекулярно-биологические исследования. Лечение внутриутробных инфекций проводится с использованием иммуноглобулинов, иммуномодуляторов, противовирусных, антибактериальных препаратов.

Общие сведения
Внутриутробные инфекции – патологические процессы и заболевания, обусловленные антенатальным и интранатальным инфицированием плода. Истинная распространенность внутриутробных инфекций не установлена, однако, согласно обобщенным данным, с врожденными инфекциями рождается не менее 10% новорожденных. Актуальность проблемы внутриутробных инфекций в педиатрии обусловлена высокими репродуктивными потерями, ранней неонатальной заболеваемостью, приводящей к инвалидизации и постнатальной гибели детей. Вопросы профилактики внутриутробных инфекций лежат в плоскости рассмотрения акушерства и гинекологии, неонатологии, педиатрии.

Причины внутриутробных инфекций
Внутриутробные инфекции развиваются в результате инфицирования плода в дородовом периоде или непосредственно во время родов. Обычно источником внутриутробной инфекции для ребенка выступает мать, т. е. имеет место вертикальный механизм передачи, который в антенатальном периоде реализуется трансплацентарным или восходящим (через инфицированные околоплодные воды) путями, а в интранатальном - аспирационным или контактным путями.
Реже происходит ятрогенное инфицирование плода в период беременности при проведении женщине инвазивной пренатальной диагностики (амниоцентеза, кордоцентеза, биопсии ворсин хориона), введении плоду препаратов крови через сосуды пуповины (плазмы, эритроцитарной массы, иммуноглобулинов) и т. д.
В антенатальном периоде инфицирование плода обычно связано с вирусными агентами (вирусами краснухи, герпеса, цитомегалии, гепатита В и С, Коксаки, ВИЧ) и внутриклеточными возбудителями (токсоплазмоза, микоплазмоза).
В интранатальном периоде чаще происходит микробная контаминация, характер и степень которой зависит от микробного пейзажа родовых путей матери. Среди бактериальных агентов наиболее распространены энтеробактерии, стрептококки группы В, гонококки, синегнойная палочки, протей, клебсиелла и др. Плацентарный барьер непроницаем для большинства бактерий и простейших, однако при повреждении плаценты и развитии фетоплацентарной недостаточности, может произойти антенатальное микробное инфицирование (например, возбудителем сифилиса). Кроме этого, не исключается и интранатальное вирусное заражение.
Факторами возникновения внутриутробных инфекций служат отягощенный акушерско-гинекологический анамнез матери (неспецифические кольпиты, эндоцервициты, ЗППП, сальпингофориты), неблагополучное течение беременности (угроза прерывания, гестозы, преждевременная отслойка плаценты) и инфекционная заболеваемость беременной. Риск развития манифестной формы внутриутробной инфекции существенно выше у недоношенных детей и в том случае, когда женщина инфицируется первично во время беременности.
Известно, что тяжесть проявлений инфекционного процесса у беременной и у плода может не совпадать. Бессимптомное или малосимптомное течение инфекции и у матери может вызвать тяжелые поражения плода, вплоть до его гибели. Это связано с повышенным тропизмом вирусных и микробных возбудителей к эмбриональным тканям, преимущественно ЦНС, сердца, органа зрения.
Классификация
Этиологическая структура внутриутробных инфекций предполагает их деление на:
- вирусные (вирусный гепатит, герпес, краснуха, ОРВИ, цитомегалия, эпидемический паротит, энтеровирусная инфекция)
- бактериальные (туберкулез, сифилис, листериоз, сепсис)
- паразитарные и грибковые (микоплазмоз, токсоплазмоз, хламидиоз, кандидоз и др.)
Для обозначения группы наиболее распространенных внутриутробных инфекций используется аббревиатура TORCH-синдром, объединяющий токсоплазмоз (toxoplasmosis), краснуху (rubella), цитомегалию (cytomegalovirus), герпес (herpes simplex). Буквой О (other) обозначаются другие инфекции, в числе которых - вирусные гепатиты, ВИЧ-инфекция, ветряная оспа, листериоз, микоплазмоз, сифилис, хламидиоз и др.).
Симптомы внутриутробных инфекций
Наличие внутриутробной инфекции у новорожденного может быть заподозрено уже во время родов. В пользу внутриутробного инфицирования может свидетельствовать излитие мутных околоплодных вод, загрязненных меконием и имеющих неприятный запах, состояние плаценты (полнокровие, микротробозы, микронекрозы). Дети с внутриутробной инфекцией часто рождаются в состоянии асфиксии, с пренатальной гипотрофией, увеличенной печенью, пороками развития или стигмами дисэмбриогенеза, микроцефалией, гидроцефалией. С первых дней жизни у них отмечается желтуха, элементы пиодермии, розеолезных или везикулезных высыпаний на коже, лихорадка, судорожный синдром, респиратрные и кардиоваскулярные расстройства.
Ранний неонатальный период при внутриутробных инфекциях нередко отягощается интерстициальной пневмонией, омфалитом, миокардитом или кардитом, анемией, кератоконъюнктивитом, хориоретинитом, геморрагическим синдромом и др. При инструментальном обследовании у новорожденных могут обнаруживаться врожденная катаракта, глаукома, врожденные пороки сердца, кисты и кальцификаты мозга.
В перинатальном периоде у ребенка отмечаются частые и обильные срыгивания, мышечная гипотония, синдром угнетения ЦНС, серый цвет кожных покровов. В поздние сроки при длительном инкубационном периоде внутриутробной инфекции возможно развитие поздних менингитов, энцефалитов, остеомиелита.
Рассмотрим проявления основных внутриутробных инфекций, составляющих TORCH-синдром.
Врождённый токсоплазмоз
Внутриутробное инфицирование одноклеточным протозойным паразитом Toxoplasma Gondii приводит к тяжелым поражениям плода – задержке развития, врожденным порокам развития мозга, глаз, сердца, скелета.
После рождения в остром периоде внутриутробная инфекция проявляется лихорадкой, желтухой, отечным синдромом, экзантемой, геморрагиями, диареей, судорогами, гепатоспленомегалией, миокардитом, нефритом, пневмонией. При подостром течении доминирую признаки менингита или энцефалита. При хронической персистенции развивается гидроцефалия с микроцефалией, иридоциклит, косоглазие, атрофия зрительных нервов. Иногда встречаются моносимптомные и латентные формы внутриутробной инфекции.
К числу поздних осложнений врожденного токсоплазмоза относятся олигофрения, эпилепсия, слепота.
Врождённая краснуха
Внутриутробная инфекция возникает из-за заболевания краснухой при беременности. Вероятность и последствия инфицирования плода зависят от гестационного срока: в первые 8 недель риск достигает 80%; последствиями внутриутробной инфекции могут служить самопроизвольное прерывание беременности, эмбрио- и фетопатии. Во II триместре риск внутриутробного инфицирования составляет 10-20%, в III – 3-8%.
Дети с внутриутробной инфекцией обычно рождаются недоношенными или с низкой массой тела. Для периода новорожденности характерна геморрагическая сыпь, длительная желтуха.
Классические проявления врожденной краснухи представлены триадой Грега: поражением глаз (микрофтальмией, катарактой, глаукомой, хориоретинитом), ВПС (открытым артериальным протоком, ДМПП, ДМЖП, стенозом легочной артерии), поражением слухового нерва (сенсоневральной глухотой). В случае развития внутриутробной инфекции во второй половине беременности у ребенка обычно имеется ретинопатия и глухота.
Кроме основных проявлений врожденной краснухи, у ребенка могут выявляться и другие аномалии: микроцефалия, гидроцефалия, расщелины нёба, гепатит, гепатоспленомегалия, пороки развития мочеполовой системы и скелета. В дальнейшем внутриутробная инфекция напоминает о себе отставанием ребенка в физическом развитии, ЗПР или умственной отсталостью.
Врождённая цитомегалия
Внутриутробное заражение цитомегаловирусной инфекцией может приводить к локальному или генерализованному поражению многих органов, иммунодефициту, гнойно-септическим осложнениям. Врожденные дефекты развития обычно включают микроцефалию, микрогирию, микрофтальмию, ретинопатию, катаракту, ВПС и др. Неонатальный период врожденной цитомегалии осложняется желтухой, геморрагическим синдромом, двусторонней пневмонией, интерстициальным нефритом, анемией.
К отдаленным последствиям внутриутробной инфекции относятся слепота, нейросенсорная глухота, энцефалопатия, цирроз печени, пневмосклероз.
Врождённая герпетическая инфекция
Внутриутробная герпес-инфекция может протекать в генерализованной (50%), неврологической (20%), слизисто-кожной форме (20%).
Генерализованная внутриутробная врожденная герпетическая инфекция протекает с выраженным токсикозом, респираторным дистресс-синдромом, гепатомегалией, желтухой, пневмонией, тромбоцитопенией, геморрагическим синдромом. Неврологическая форма врожденного герпеса клинически проявляется энцефалитом и менингоэнцефалитом. Внутриутробная герпес-инфекция с развитием кожного синдрома сопровождается появлением везикулярной сыпи на кожных покровах и слизистых оболочках, в т. ч. внутренних органов. При наслоении бактериальной инфекции развивается сепсис новорожденных.
Внутриутробная герпес-инфекция у ребенка может приводить к формированию пороков развития - микроцефалии, ретинопатии, гипоплазии конечностей (кортикальной карликовости). В числе поздних осложнений врожденного герпеса - энцефалопатия, глухота, слепота, задержка психомоторного развития.
Диагностика
В настоящее время актуальной задачей является пренатальная диагностика внутриутробных инфекций. С этой целью на ранних сроках беременности проводится микроскопия мазка, бактериологический посев из влагалища на флору, ПЦР-исследование соскоба, обследование на TORCH-комплекс. Беременным из группы высокого риска по развитию внутриутробной инфекции показана инвазивная пренатальная диагностика (аспирация ворсин хориона, амниоцентез с исследованием амниотической жидкости, кордоцентез с исследованием пуповинной крови).
Возможно выявление эхографических маркеров внутриутробных инфекций с помощью акушерского УЗИ. К косвенным эхографическим признакам внутриутробного инфицирования относятся маловодие или многоводие; наличие гиперэхогенной взвеси в околоплодных водах или амниотических тяжей; гипоплазия ворсин хориона, плацентит; преждевременное старение плаценты; отечный синдром плода (асцит, перикардит, плеврит), гепатоспленомегалия, кальцификаты и пороки развития внутренних органов и др. В процессе допплерографического исследования кровотока выявляются нарушения плодово-плацентарного кровотока. Кардиотокография обнаруживает признаки гипоксии плода.
После рождения ребенка с целью достоверной верификации этиологии внутриутробной инфекции используются микробиологические (вирусологические, бактериологические), молекулярно-биологические (ДНК-гибридизация, ПЦР), серологические (ИФА) методики обследования. Важное диагностическое значение имеет гистологическое исследование плаценты.
По показаниям новорожденные с внутриутробными инфекциями в первые сутки жизни должны быть осмотрены детским неврологом, детским кардиологом, детским офтальмологом и др. специалистами. Целесообразно провести ЭхоКГ, нейросонографию, офтальмоскопию, исследование слуха методом вызванной отоакустической эмиссии.
Лечение внутриутробных инфекций
Общие принципы лечения внутриутробных инфекций предполагают проведение иммунотерапии, противовирусной, антибактериальной и посиндромной терапии.
Иммунотерапия включает применение поливалентных и специфических иммуноглобулинов, иммуномодуляторов (интерферонов). Противовирусная терапия направленного действия осуществляется, главным образом, ацикловиром. Для противомикробной терапии бактериальных внутриутробных инфекций используются антибиотики широкого спектра действия (цефалоспорины, аминогликозиды, карбапенемы), при микоплазменной и хламидийной инфекциях – макролиды.
Посиндромная терапия внутриутробных инфекций направлена на купирование отдельных проявлений перинатального поражения ЦНС, геморрагического синдрома, гепатита, миокардита, пневмонии и т. д.
Прогноз и профилактика
При генерализованных формах внутриутробных инфекций летальность в неонатальном периоде достигает 80%. При локальных формах возникают серьезные поражения внутренних органов (кардиомиопатии, ХОБЛ, интерстициальный нефрит, хронический гепатит, цирроз и т. д.). Практически во всех случаях внутриутробные инфекции приводят к поражению ЦНС.
Профилактика внутриутробных инфекций заключается в проведении предгравидарной подготовки, лечении ЗППП до наступления беременности, исключении контактов беременной с инфекционными больными, коррекции программы ведения беременности у женщин групп риска. Женщины, ранее не болевшие краснухой и не получавшие прививки против краснухи, должны быть вакцинированы не позднее, чем за 3 месяца до предполагаемой беременности. В ряде случаев внутриутробные инфекции могут являться основанием для искусственного прерывания беременности.
Рассмотрена проблема внутриутробного инфицирования и внутриутробной инфекции (ВУИ) плода, факторы риска внутриутробных инфекций, патогенетические механизмы возникновения, развития и воздействия ВУИ, подходы к диагностике и лечению.
The issue of fetal intrauterine infecting and intrauterine infection (IUI) was considered, as well as the risk factors of intrauterine infections, pathogenic mechanisms of their occurrence, development and effect of IUI, and approaches to the diagnostics and treatment.
Проблема внутриутробной инфекции особо актуальна в современных условиях в связи с распространенностью и тяжестью воспалительных процессов. Проблема внутриутробного инфицирования и внутриутробной инфекции (ВУИ) плода является одной из ведущих в акушерской практике и в перинатологии в связи с высоким уровнем инфицирования беременных, рожениц и родильниц, опасностью нарушения развития плода и рождения больного ребенка. Наличие инфекции у матери является фактором риска ВУИ плода, но не всегда означает его заболевание [1, 5–7, 13].
Внутриутробная инфекция — группа инфекционно-воспалительных заболеваний плода и детей раннего возраста, которые вызываются различными возбудителями, но характеризуются сходными эпидемиологическими параметрами и нередко имеют однотипные клинические проявления. Заболевания развиваются в результате внутриутробного (анте- и/или интранатального) инфицирования плода. При этом в подавляющем большинстве случаев источником инфекции для плода является мать. Истинная частота врожденных инфекций до настоящего времени не установлена, но, по данным ряда авторов, распространенность данной патологии в человеческой популяции может достигать 10%. В структуре перинатальной смертности ВУИ составляет более 30% [1, 5–7].
Кроме этого, ВУИ относятся к тяжелым заболеваниям и во многом определяют уровень младенческой смертности.
Согласно данным многих авторов, причиной внезапной смерти грудных детей является инфекционное заболевание, протекающее без ясной симптоматики. В числе причин или фоновых состояний скоропостижной смерти могут быть ВУИ [2].
Под внутриутробным инфицированием понимают процесс внутриутробного проникновения микроорганизмов к плоду, при котором отсутствуют признаки инфекционной болезни плода. Как правило, инфекционный процесс затрагивает плаценту, в которой развивается плацентит, хориоамнионит и т. д. Диагноз внутриутробного инфицирования у новорожденного устанавливается на основании выделения возбудителя из клеток крови, ликвора и других источников, выявления IgM и низкоавидных IgG в пуповинной крови, а также при морфологическом исследовании плаценты [1, 5–7].
Внутриутробное инфицирование не означает неизбежного развития инфекционного заболевания. Для выявления ВУИ необходимо наличие данных лабораторного исследования в сочетании с клинической картиной инфекционного заболевания. Под ВУИ подразумевают не только процесс распространения инфекционных агентов в организме плода, но и вызванные ими морфофункциональные нарушения различных органов и систем, характерные для инфекционной болезни (сепсис, пневмония, менингит, гепатит и т. д.), возникшей анте- или интранатально и выявляемой пренатально или после рождения [10, 11].
Инфекционно-воспалительные заболевания во время беременности имеют особенности: инфицирование плода и новорожденного может быть вызвано как острой инфекцией матери, так и активацией хронической, персистирующей инфекции во время беременности; большая часть заболеваний беременных, приводящих к внутриматочной инфекции, протекает в латентной или субклинической форме; активация персистирующей инфекции возможна при любом нарушении гомеостаза в организме беременной (стресс, острые респираторные вирусные инфекции, переохлаждение и др.) [1, 2].
Возможный спектр возбудителей внутриутробной инфекции весьма разнообразен и широк. Это бактерии (грамположительные и грамотрицательные; аэробные и анаэробные), грибы, простейшие, внутриклеточные микроорганизмы (микоплазмы, хламидии), вирусы. Чаще всего наблюдается сочетание возбудителей — бактериально-вирусная смешанная инфекция [3, 4, 10, 11].
Зачастую ВУИ ассоциируются с наличием инфекций TORCH — то есть синдромом комплекса. Данный термин образован первыми буквами латинских названий наиболее часто верифицируемых врожденных инфекций: T — токсоплазмоз (Тoxoplasmоsis), R — краснуха (Rubella), С — цитомегалия (Cytomegalia), Н — герпес (Herpes) и О — другие инфекции (Оther). К последним относят сифилис, листериоз, вирусные гепатиты, хламидиоз, ВИЧ-инфекцию, микоплазмоз и др. [9, 11].
Принимая во внимание, что источником инфекции для плода всегда является его мать, особое значение приобретают следующие факторы риска внутриутробных инфекций:
- хронические очаги инфекции в организме матери (в том числе наличие воспалительных заболеваний органов малого таза, урогенитальные инфекции);
- первичное инфицирование во время беременности, активация инфекционного процесса;
- патологическое снижение общего и местного иммунитета;
- наличие экстрагенитальной патологии (анемия, тромбофилии, аутоиммунные заболевания);
- повышение проницаемости плацентарного барьера во II и III триместрах беременности при невынашивании беременности и плацентарной недостаточности;
- отягощенный акушерско-гинекологический диагноз;
- неблагоприятные социально-бытовые факторы [1, 9, 11].
Патогенетические механизмы возникновения, развития и воздействия ВУИ разнообразны и зависят от многих факторов:
- срока беременности, при котором происходит инфицирование (чем раньше, тем прогноз будет более неблагоприятным);
- вида возбудителя, его вирулентности, массивности обсеменения;
- первичности или вторичности инфекционного процесса у беременной;
- путей проникновения инфекции к плоду (восходящий, нисходящий, гематогенный);
- степени распространенности и интенсивности воспалительного процесса;
- состояния организма матери, его иммунологической толерантности.
Влияние инфекции на эмбрион и плод заключается в воздействии комплекса следующих факторов:
- патологическое воздействие микроорганизмов и их токсинов (инфекционное заболевание, гипоксия плода, задержка развития плода);
- нарушение процесса имплантации и плацентации (низкая плацентация, предлежание плаценты);
- снижение метаболических процессов и иммунологической защиты плода [1, 9, 11].
Таким образом, реализуется ли внутриутробное инфицирование в ВУИ или нет, зависит от ряда факторов, которые мы представили выше.
Учитывая неспецифичность клинических проявлений ВУИ во время беременности, диагностика данной патологии в большинстве случаев затруднена и возможна лишь в результате сочетания клинических и лабораторно-диагностических методов обследования.
Клинический метод исследования позволяет выявить различные осложнения гестационного периода, такие как невынашивание беременности и синдром задержки роста плода (СЗРП). Кроме этого, немаловажное значение имеет наличие проявлений инфекции у матери (отит, гайморит, пиелонефрит, цистит и т. д.).
Методы, позволяющие оценить состояние фетоплацентарной системы:
- эхография (плацентометрия, поведенческая активность плода, его тонус, количество околоплодных вод, степень зрелости плаценты);
- допплерография (МПК, ФПК);
- кардиотокография (КТГ).
Микробиологические и серологические исследования:
- микроскопия влагалищных мазков (повышенное содержание лейкоцитов, кокковая флора, признаки дисбиоза, грибковая флора);
- бактериальный посев (наличие анаэробных и аэробных бактерий, грибковой флоры);
- ПЦР-диагностика (геномы ВПГ-1, ВПГ-2, ЦМВ, микоплазмы, уреаплазмы, хламидии);
- иммуноферментный анализ (ИФА): обнаружение в сыворотке специфических антител к возбудителям (IgM, IgG, IgA) в диагностически значимых титрах.
Исследование хориона (биопсия хориона): бактериологический метод, ПЦР-диагностика.
Исследование околоплодных вод (амниоцентез): бактериологический метод, ПЦР-диагностика.
Исследование пуповинной крови плода (кордоцентез): бактериологический метод, ПЦР-диагностика и специфический иммунный ответ (IgM) плода.
Морфологическое исследование плаценты, данные аутопсии.
Предположительный диагноз внутриутробного инфицирования и ВУИ помогают поставить косвенные методы:
- наличие у матери клиники инфекционного заболевания;
- наличие специфического иммунного ответа;
- результаты УЗИ, допплерометрии, КТГ.
К прямым методам диагностики внутриутробного инфицирования и ВУИ относятся: выявление возбудителя в материале, полученном при биопсии хориона, амниоцентезе (ПЦР, бактериологический метод), кордоцентезе (ПЦР, бактериологический метод и определение уровня специфических IgM).
Характер течения беременности при внутриутробной инфекции зависит от срока воздействия возбудителя.
На ранних этапах зародыша (1–3 недели беременности) из-за отсутствия механизмов взаимодействия инфекционного агента и плодного яйца реализации воспалительной реакции чаще всего не происходит. Контакт с инфекцией может закончиться альтернативным процессом и гибелью плодного яйца. Повреждение эмбриона инфекцией на 4–12 неделях беременности связано с вирусной инфекцией, проникновением микроорганизмов через хорион. Плод еще не имеет защитных механизмов. Нарушение закладки органов и систем вызывает тератогенный и эмбриотоксический эффект [13, 15].
В I триместре беременности специфических клинических признаков наличия ВУИ нет, косвенно о ней свидетельствуют некоторые эхографические признаки:
- повышенный локальный тонус матки;
- отслойка хориона;
- изменение формы плодного яйца (деформация);
- прогрессирование истмико-цервикальной недостаточности (функционального характера);
- гипоплазия хориона;
- увеличение или персистенция желточного мешка;
- несоответствие размеров эмбриона размерам полости плодного яйца (увеличение, уменьшение);
- отсутствие редукции хорионической полости.
Инфекционные фетопатии возникают с 16-й недели, когда происходит генерализация инфекции у плода. Могут возникать такие пороки развития, как фиброэластоз эндокарда, поликистоз легких, микро- и гидроцефалия (ранние фетопатии) [12–15].
В III триместре плод реагирует на внедрение возбудителя локальной реакцией. Могут возникнуть энцефалит, гепатит, пневмония, интерстициальный нефрит. Влияние вирусов чаще всего проявляется признаками незрелости, дисэмбриогенетическими стигмами, затяжным адаптационным периодом, значительной потерей массы тела в раннем постнатальном периоде. Данные эхографии во II и III триместрах беременности, указывающие на развитие инфекции у плода:
- СЗРП;
- гипоксия плода;
- фетоплацентарная недостаточность;
- многоводие или маловодие;
- неиммунная водянка плода;
- увеличение или уменьшение толщины плаценты, наличие патологических включений;
- контрастирование базальной мембраны;
- наличие взвеси в околоплодных водах;
- кальцификаты в печени и селезенке и головном мозге плода;
- поликистоз легких, почек плода;
- эхогенные фиброзные включения на папиллярных мышцах и створках клапанов сердца плода;
- расширение петель кишечника плода (гипоксия, энтерит) [12–15].
После верификации диагноза ВУИ лечебные мероприятии проводят с помощью этиотропной, антимикробной терапии: препараты пенициллинового ряда и макролиды. Целесообразность назначения антимикробных препаратов не вызывает сомнения, если ВУИ обусловлено наличием патогенных возбудителей (бледная спирохета, токсоплазма, хламидии, гонококк и т. д.) [8, 14].
В настоящее время одним из наиболее дискутабельных вопросов в акушерстве является выяснение истинной этиологической роли генитальных микоплазм (Mycoplasma hominis, Mycoplasma genitalis, Ureaplasma urealyticum) в развитии патологии матери и плода. Инфицирование плода генитальными микоплазмами происходит преимущественно интранатально: в 18–55% — у доношенных новорожденных и в 29–55% — у недоношенных [3, 16, 20].
Актуальность проблемы урогенитального микоплазмоза обусловлена не только значительным распространением этой инфекции в популяции, но и неоднозначностью ее оценки как эпидемиологами, так и клиницистами [16].
По данным различных исследователей, микоплазмы являются возможной причиной развития конъюнктивитов, врожденных пневмоний, респираторного дистресс-синдрома, хронических заболеваний легких, менингита и неонатального сепсиса. Вопрос о терапии микоплазменной инфекции до настоящего времени остается открытым. В схемах терапии предусматривается 7–10-дневные курсы макролидов [1, 3, 21, 22].
Во время беременности противовирусная терапия при генитальном герпесе, цитомегаловирусной инфекции, вирусе ветряной оспы проводится с помощью этиотропных препаратов (ацикловир) начиная со II триместра гестационного периода. Целью лечения является профилактика рецидивирования и антенатального инфицирования [14, 17, 19].
Трихомонадная инфекция относится к группе негонококковых воспалительных заболеваний мочеполовых органов. Лечение трихомониаза во время беременности осуществляется с помощью метронидазол-содержащих препаратов начиная со II триместра гестационного периода [8].
Появление новых методов диагностики, разработка и внедрение новых лекарственных средств не изменяют ситуацию с внутриутробными инфекциями, оставляя это по-прежнему актуальной проблемой в акушерстве. Все это обуславливает неуклонный рост инфекции в человеческой популяции, высокий процент рецидивов инфекции даже у пациентов, получавших курс антибиотикотерапии в соответствии с действующими инструкциями и схемами лечения. Проблема осложняется тем, что в настоящее время отсутствует единая концепция механизма рецидивирования, недостаточно изучена роль микст-инфекции в возникновении, течении и персистировании инфекции, не учитываются особенности гормонального и иммунного статуса больного, не сформированы диагностические критерии контроля излеченности патологического процесса. Это все вместе взятое является стимулом для продолжения исследований, направленных на решение данных проблем. Несмотря на то что роль вирусных и бактериальных инфекций в этиологии и патогенезе многих патологических процессов не вызывает сомнений, вопрос о значении инфекций в качестве моновозбудителя на сегодняшний день окончательно не решен. Актуальным по-прежнему остается вопрос разработки алгоритма лабораторной диагностики заболеваний.
Только совершенствование диагностических подходов, разработка оптимальных алгоритмов и методов обследования и предупреждение распространения резистентных штаммов путем адекватного отношения к каждому пациенту индивидуально (обязательное проведение посевов на определение чувствительности к антибиотикам до назначения терапии) может изменить данную ситуацию.
Исследование выполнено за счет гранта Российского научного фонда (проект № 15-15-00109).
Литература
В. Н. Кузьмин 1 , доктор медицинских наук, профессор
К. Н. Арсланян, кандидат медицинских наук
Э. И. Харченко, кандидат медицинских наук
ГБОУ ВПО МГМСУ им. А. И. Евдокимова МЗ РФ, Москва
Каковы диагностические признаки острых и хронических синуситов? Показаны ли антибиотики, и если да, то в каком случае? Каких пациентов стоит направлять к специалистам? Oбзоры, касающиеся диагностики и лечения болезней придаточных
Каковы диагностические признаки острых и хронических синуситов?
Показаны ли антибиотики, и если да, то в каком случае?
Каких пациентов стоит направлять к специалистам?
Oбзоры, касающиеся диагностики и лечения болезней придаточных пазух носа (ППН), чаще всего вызывают множество новых вопросов, поскольку точный диагноз осложняется неспецифичностью неинвазивных методов обследования. Эмпирическое лечение, особенно с помощью антибиотиков, как правило, считается успешным, хотя во многих случаях наступает спонтанное выздоровление без какого-либо лечения.
Цель этого обзора — осветить современные представления о природе воспаления ППН и дать логические и фактические обоснования медикаментозного либо хирургического лечения.
Анатомия и физиология. Носовая полость и ППН наделены важными физиологическими функциями. Преимущественно через полость носа проходит вдыхаемый и выдыхаемый воздух, поэтому нос должен обладать защитными механизмами, способными оградить воздухоносные пути от вдыхаемых патогенов и инородных тел.
 |
| Рисунок 1. Слизь стекает назад в носоглотку вследствие движений ресничек |
Железы реснитчатого эпителия носа и ППН производят поверхностный слизистый слой. Он задерживает частички веществ, а реснички, находящиеся в постоянном движении, проталкивают их назад, в носоглотку (см. рис. 1).
И верхнечелюстная, и лобная пазухи вентилируются через каналы, в свою очередь проходящие через переднюю решетчатую область. Очень важно, чтобы эти пути оставались проходимыми, поскольку нормальный отток слизи нужен для поддержания воздухонаполнения пазух.
Важная роль передних клеток решетчатого лабиринта и среднего носового хода в физиологии ППН подтверждается тем, что эта область получила название “остеомеатальный комплекс” (рис. 2). Считается, что легкое ограниченное воспаление в этой области может привести к вторичному инфицированию верхнечелюстного и фронтального синуса. Это во многом справедливо, хотя патогенез синуситов более сложен.
 |
| Рисунок 2. Нормальный средний носовой ход — область “остиомеатального комплекса” |
Микробиология. Носовая полость и ППН заселены нормальной бактериальной флорой; в норме там обнаруживаются те же микроорганизмы, что и в инфицированных пазухах. Многие инфекционные процессы в пазухах имеют вирусную природу; бактерии присоединяются вторично.
При остром синусите чаще всего выделяют Streptococculs pneulmoniae, Heamophiluls influlenzae и Moraxella catarrhalis.
При хронических синуситах обычно присутствуют те же микроорганизмы, а также анаэробы, такие как штаммы Fulsobacteriulm, Staphylococculs aulreuls, изредка грамотрицательные бактерии, например штаммы Pseuldomonas. В последние годы участились случаи диагностики синуситов, вызванных грибами, как правило, у иммунодефицитных пациентов. Чаще всего обнаруживаются штаммы Aspergilluls, а выраженность клинических проявлений зависит от имунного статуса пациента.
 |
| Рисунок 3. Гной в среднем носовом ходе при остром синусите |
Все больше диагностируется аллергических синуситов, часто ассоциированных с назальными полипами.
Клиника. С позиций оториноларингологической хирургии понятия об анатомии, физиологии и патологии ППН в корне изменились с появлением жесткой эндоскопии носовой полости и возможности компьютерного сканирования (КТ) синусов.
Однако ни один из этих диагностических методов не доступен для врача общей практики, которому нередко приходится ставить диагноз и лечить синусит на основании клинических симптомов.
Часто жалобы больных при остром и хроническом синуситах совпадают, поэтому своевременный подход предполагает, что при попытке различать эти состояния врач опирается скорее на патофизиологию, чем на соображения длительности заболевания.
 |
| Рисунок 4. Компьютерное сканирование синусов |
Синусит считается острым, когда инфекция разрешается под действием медикаментозной терапии, не оставляя значительных повреждений слизистых. Острые эпизоды могут быть рецидивирующими по своей природе; хронический синусит — постоянное заболевание, которое не поддается только медикаментозному лечению. При разграничении этих состояний проблема заключается в том, что для хирургического лечения всегда находятся показания, хотя в действительности многим пациентам достаточно длительной медикаментозной терапии. Кроме того, хирургическое вмешательство не дает стопроцентного успеха.
У многих пациентов с острым синуситом в анамнезе началу заболевания предшествует простуда. Симптомы, позволяющие предположить развитие острого синусита:
- гнойные выделения из носа;
- заложенность носа;
- боли и болезненность при обследовании;
- лихорадка и озноб.
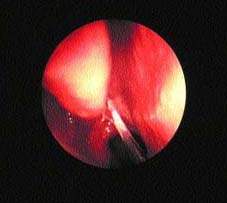
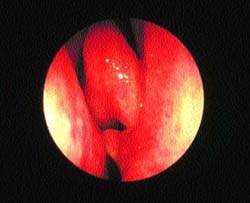
В некоторых случаях имеются местные симптомы, позволяющие заподозрить вовлечение различных синусов. При диагностике наиболее достоверным симптомом является жалоба на гнойные выделения из носа или выявление их при обследовании (рис. 3).
Если пациент страдает головными или лицевыми болями при отсутствии гнойных выделений, скорее всего, это не синусит.
При невылеченном синусите инфекция иногда распространяется за пределы пазух, приводя к серьезным осложнениям. Чаще это случается при инфицировании лобной и решетчатой пазух; более всего осложнениям подвержены дети.
При распространении инфекции из фронтального синуса вперед мягкие ткани лба становятся отекшими и болезненными. Первоначально развивается целлюлит, затем субпериостальный абсцесс. Распространение через заднюю стенку фронтального синуса приводит к внутричерепным осложнениям, таким как менингит, субдуральная эмпиема или абсцесс передней доли.
При воспалении решетчатой пазухи инфекция распространяется через тонкую кость бумажной пластинки, приводя к поражению глазницы, сопровождающемуся целлюлитом и орбитальным абсцессом. Нелеченые инфекции глазницы почти всегда ведут к слепоте.
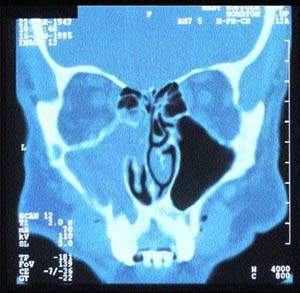 |
| Рисунок 5. Компьютерная томограмма синусов, демонстрирующая односторонний хронический синусит |
При подозрении на осложненный синусит, особенно при отеке мягких тканей глазницы у ребенка, необходима срочная консультация оториноларинголога и уточнение диагноза путем компьютерного сканирования.
Клиническая картина хронического синусита разнообразна. Как и при острой инфекции, заложенность носа и гнойное отделяемое являются постоянными симптомами.Температура не повышается либо повышается умеренно, а жалобы на общее недомогание, головную и лицевую боль типичны. Дополнительно многие пациенты жалуются на снижение обоняния, при этом они чувствуют отвратительный запах гноя в носу.
Простое клиническое обследование носовой полости с помощью отоскопа позволяет обнаруживать крупные полипы; маленькие полипы видны только при эндоскопии носа.
| Промывание верхнечелюстного синуса под местной анестезией теряет былую популярность, так как редко приносит длительное облегчение |
За прошедшее десятилетие участились случаи диагностики острых и хронических синуситов у детей, особенно в Северной Америке. Диагностика и лечение детских синуситов осложняется многими факторами.
Рецидивирующие симптомы поражения верхних дыхательных путей у детей проявляются достаточно часто и, как правило, свидетельствуют о наличии заболевания миндалин и аденоидов, а не первичного синусита. Компьютерное томографическое сканирование детей с симптомами поражения верхних дыхательных путей часто выявляет аномалии ППН, особенно верхнечелюстных.
Клинический опыт показывает, что симптомы синуситов у детей часто сами проходят с возрастом, при этом до сих пор не установлено, вырастают ли из “сопливых” детей “сопливые” взрослые.
Нет сомнения в том, что хронический синусит встречается и у детей, особенно если имеется нарушение функции реснитчатого эпителия. Однако большинство британских лор-хирургов считают, что, насколько это возможно, необходимо придерживаться консервативных методов лечения детей.
Обследование. В общей практике диагноз “синусит”, как правило, ставится на основании клинических данных.
 |
| Рисунок 6. “Шпора” перегородки носа, врезающаяся в среднюю носовую раковину, — возможная причина “контактных болей” |
Плоскостная рентгенография пазух чрезвычайно неспецифична и малоинформативна для выявления патологических изменений. Аномалии на таких рентгенограммах обнаруживаются у половины населения. Так, на рентгенограмме может быть выявлено утолщение слизистой верхнечелюстной пазухи, что не совпадает с результатами прямой эндоскопии. Несмотря на это, к плоскостным снимкам прибегают довольно часто, особенно при хронических симптомах.
В руководстве, изданном Королевской коллегией радиологов, говорится, что плоскостная рентгенография не является обязательным рутинным исследованием при заболеваниях ППН].
Наиболее специфичным методом оценки анатомии и патологии пазух носа является компьютерная томография, как правило, в проекции венечного шва (рис. 4).
Компьютерное сканирование пазух дает точную информацию об анатомии пациента и наличии патологических изменений (рис. 5). Однако это исследование следует проводить только после специализированного обследования, включающего и назальную эндоскопию.
Острый синусит. При остром синусите единого мнения о выборе антибиотика и продолжительности курса лечения не существует. С одной стороны, согласно рекомендации североамериканских ринологов, антибиотики следует принимать по крайней мере 14 дней или еще 7 дней после исчезновения симптомов. Согласно данным некоторых исследований, антибиотики не имеют преимуществ по сравнению с плацебо, когда речь идет о лечении синуситоподобных симптомов в общей практике .
Наличие столь противоположных точек зрения нередко только сбивает с толку врача общей практики, сталкивающегося с острым синуситом. Опасность назначения длительного курса антибиотиков заключается в развитии антибиотикорезистентности; кроме того, больные нередко отказываются от продолжительного лечения. Неадекватное лечение скрывает в себе риск остаточной инфекции, при этом всегда сохраняется, хоть и небольшая, вероятность развития осложнений.
 |
| Рисунок 7. Перед направлением к специалисту следует попробовать провести интраназальную стероидную терапию |
Многие пациенты, поступающие с симптомами синусита, выздоравливают спонтанно, без приема антибиотиков; задача врача — своевременно определить, есть ли возможность такого выздоровления.
Предполагается, что успешно решить этот вопрос может помочь КТ-сканирование. Пациенты с уровнем жидкости или при наличии тотального затемнения верхнечелюстных пазух нуждаются в антибиотиках, в то время как больные, у которых при сканировании не выявлено никаких отклонений или речь идет только об утолщении слизистой оболочки, скорее всего, могут выздороветь спонтанно.
Английские врачи общей практики не имеют непосредственного доступа к КТ, и вряд ли она будет им предоставлена для диагностики острого синусита, так как пациент при этом подвергается значительному облучению, а кроме того, исследование стоит достаточно дорого.
С чисто симптоматических позиций наличие гнойного отделяемого из носа и заложенность носа — более достоверные признаки инфицирования пазух, чем другие симптомы, такие как головные и лицевые боли. Для больных с первой группой симптомов оправданно назначение антибиотиков.
При выборе антибиотика необходимо учитывать возможность присутствия пенициллин-резистентных штаммов.
Препаратами первого ряда являются амоксиклав, эритромицин и цефалоспорины, например цефиксим. Те же антибиотики могут быть назначены при хронических инфекциях; в этом случае также полезны производные хинолона, такие как ципрофлоксацин.
Часто при остром синусите в качестве дополнительных средств используются противоотечные препараты, как местные, так и системные. Местные противоотечные, например ксилометазолин, уменьшают отек слизистой и улучшают проводимость воздуха, что теоретически ускоряет выздоровление.
Паровые ингаляции, часто с ароматическими добавками, например с ментолом, приносят облегчение пациенту, усиливая ощущение тока воздуха в носовой полости, но объективно не способствуют выздоровлению.
Хронический синусит. Наличие хронической инфекции ППН подразумевает или собственно заболевание слизистой, или анатомическое препятствие аэрации пазух. В любом случае хронический синусит не поддается только антибиотикотерапии.
Краеугольным камнем лечения в данном случае является стероидная терапия, как правило, с назальным путем введения. Смысл назначения стероидов в уменьшении воспалительного отека и улучшении вентиляции пазух.
Местные стероиды назначают в каплях или в форме спрея. Часто оказываются эффективны местные бетаметазоновые капли, которые нужно вводить, соблюдая правильное положение (голова наклонена вниз) (рис. 7), и применять не более шести недель во избежание возникновения системных побочных эффектов. Преимущество новых стероидных спреев (триамцинолон, будезонид) заключается в однократном примении в течение дня, что удобнее для пациента.
Пациентов следует направлять на консультацию к специалисту, если адекватное медикаментозное лечение оказалось неэффективным или при подозрении на более серьезные заболевания, такие как неоплазия или гранулематоз Вегенера. Часто курс интраназальных стероидов облегчает состояние пациентов с рецидивирующими острыми и хроническими синуситами. Такой курс следует провести перед направлением к оториноларингологу.
Имеется ряд симптомов, заставляющих заподозрить неоплазию и требующих раннего направления к специалисту: односторонние кровянистые выделения из носа, онемение лица, диплопия, глухота, обусловленная выпотом в среднем ухе, и определение интраназального объемного образования при обследовании.
Некоторым пациентам показано хирургическое лечение, причем в основном хирурги предпочитают эндоскопическую этмоидэктомию. Пункции верхнечелюстного синуса под местной анестезией теряют былую популярность, так как редко приносят длительное облегчение и чрезвычайно не нравятся пациентам.
Новые хирургические и анестезиологические методики позволяют в большинстве центров проводить операции на пазухах на базе дневного стационара и избегать рутинной послеоперационной тампонады носа.
Лечение лицевых болей. Значительную часть рабочего времени ринолога занимает диагностика пациентов с лицевыми и головными болями. С появлением синусовой хирургии в лечении заболеваний, сопровождающихся этими симптомами, удалось добиться впечатляющих результатов.
Часто симптомы, присущие синуситу, и жалобы, типичные для мигреней и кластерных головных болей, во многом совпадают.
Если у пациента с лицевыми болями отсутствует заложенность носа или гнойные выделения, а результаты эндоскопии и КТ-сканирования нормальные, то, скорее всего, проблема не в носе и придаточных пазухах, и синусовая хирургия здесь неэффективна, хотя не следует сбрасывать со счетов возможность воздействия плацебо.
Недавно возник интерес к так называемой контактной боли. Предполагается, что при этом состоянии носовая перегородка находится в патологическом контакте с боковой стенкой носа. Обычно это происходит, когда от перегородки отходит острая шпора, упирающаяся в среднюю носовую раковину (рис. 6). Как правило, пациенты жалуются на боль вокруг центральной части лица, отдающую в лоб и глазницы.
Читайте также:

