Этиология инфекционного процесса что это
Обновлено: 19.04.2024
Авторы: Денисова А.Р. 1 , Максимов М.Л. 2, 3, 4
1 ФГАОУ ВО Первый МГМУ им. И.М. Сеченова Минздрава России (Сеченовский Университет), Москва
2 ФГБОУ ДПО РМАНПО Минздрава России, Москва, Россия
3 КГМА — филиал ФГБОУ ДПО РМАНПО Минздрава России, Казань, Россия
4 РНИМУ им. Н.И. Пирогова Минздрава России, Москва
В Российской Федерации ежегодно болеют гриппом и острыми респираторными вирусными инфекциями (ОРВИ) другой этиологии около 30 млн человек. Масштабы заболеваемости ОРВИ делают актуальным поиск новых способов профилактики и лечения ОРВИ, адекватного контроля эпидемий и пандемий гриппа. Средства этиотропной терапии направлены против возбудителя заболевания, в данном случае против респираторных вирусов. Специфические противовирусные препараты воздействуют непосредственно на возбудителя инфекции, препятствуя его размножению в организме. Один из подходов к терапии ОРВИ и гриппа заключается в применении препаратов, имеющих несколько точек приложения и обладающих комбинированным действием, которые сочетают в себе прямое противовирусное, иммуномодулирующее и симптоматическое действие. В ситуациях с неуточненным возбудителем и лабораторно подтвержденной вирусной микст-инфекцией следует отдавать предпочтение противовирусным препаратам широкого спектра действия. Большое значение в терапии ОРВИ и гриппа имеют препараты, способные оказывать воздействие как на возбудителя инфекции (уточненного или неуточненного), так и на проявления интоксикационно-воспалительного синдрома (лихорадка, озноб, боль, отек, катаральные явления), например препарат Нобазит ® .
Ключевые слова: острые респираторные вирусные инфекции, ОРВИ, вирус гриппа, профилактика, противовирусные препараты.
Для цитирования: Денисова А.Р., Максимов М.Л. Острые респираторные вирусные инфекции: этиология, диагностика, современный взгляд на лечение. РМЖ. Медицинское обозрение. 2018;26(1(II)):99-103.
Denisova A.R. 1 , Maksimov M.L. 2
1 Sechenov University, Moscow
2 Kazan State Medical Academy
Each year about 30 million Russian people suffer from influenza and acute respiratory viral infections (ARVI) of another etiology. That’s why it is necessary to search for the new ways to prevent and treat ARVI and evaluate the efficacy of existing drugs, to study the new combined drugs for the adequate control of epidemics and pandemics of influenza. Means of etiotropic therapy affect the causative agent of the disease, i.e. respiratory viruses. Specific antiviral drugs affect directly on the pathogen, preventing its reproduction
in the body. One of the approaches to the treatment of acute respiratory viral infections and influenza is the use of drugs with several application points and synergistic action. In cases with an unspecified pathogen in a suspected or laboratory-confirmed viral mixed infection, antiviral drugs with a broad spectrum of action should be preferred. Acute respiratory viral infections and influenza can be treated with the use of the drugs that affect both the causative agent of infection (specified or unspecified) and the manifestations
of intoxication-inflammatory syndrome (fever, chills, pain, edema, catarrhal phenomena), for example, the drug Nobazit ® .
Key words: acute respiratory viral infections, ARVI, influenza virus, prevention, antiviral drugs.
For citation: Denisova A.R., Maksimov M.L. Acute respiratory viral infections: etiology, diagnosis, modern view of treatment //
RMJ. Medical Review. 2018. № 1(II). P. 99–103.
Статья посвящена этиологии, диагностике и лечению острых респираторных вирусных инфекций. Рассмотрена возможность применения препарата Нобазит.
Острые респираторные вирусные инфекции (ОРВИ) разной этиологии и грипп, по данным ВОЗ, как и прежде, занимают одно из первых мест среди всех инфекционных заболеваний. На долю этих нозологий приходится около 90–95% всех случаев инфекционных заболеваний. В Российской Федерации ежегодно болеют гриппом и ОРВИ другой этиологии около 30 млн человек, а ежегодный экономический ущерб оценивается в сумму около 40 млрд рублей [1]. Научное сообщество ученых мира озабочено малой эффективностью вакцинации и возрастающей резистентностью патогенных микроорганизмов к противовирусным препаратам, имеющимся в настоящее время в арсенале практикующих врачей. В данной ситуации актуальны поиск новых способов профилактики и лечения ОРВИ, адекватного контроля эпидемий и пандемий гриппа, оценка эффективности применяемых препаратов. Вклад отечественных ученых в создание противовирусных препаратов достаточно весом.
В настоящее время известно более 200 видов вирусов, вызывающих ОРВИ. Интенсивность, частота и доминирование тех или иных респираторных вирусов зависят от времени года и климатических особенностей.
Наиболее распространены вирусы гриппа, парагриппа, аденовирусы, коронавирусы, метапневмовирус человека, респираторно-синцитиальный вирус, риновирусы человека, бокавирусы. Кроме того, в последние годы причиной ОРВИ чаще стали выступать энтеровирусы (ЕСНО, Коксаки), реовирусы, вирус Эпштейна — Барр и др. — они могут сами вызывать поражение респираторного тракта или выступать дополнительными патогенами при наиболее распространенных вирусах [2–3].
Независимо от возбудителя входными воротами и местом локализации для инфекции являются верхние дыхательные пути, где происходит наиболее интенсивное размножение вирусов в эпителиальных клетках. Возбудители ОРВИ распространяются воздушно-капельным путем — при кашле, чихании, разговоре и посредством контаминированных предметов обихода. Длительность выживания респираторных вирусов во внешней среде составляет от 7 до 12 дней.
Вирусы
Возбудители гриппа — РНК-содержащие вирусы семейства Orthomyxoviridae. Выделяют 3 рода Influenzavirus, каждый из которых включает по одному виду вируса гриппа — А, В и С.
Вирус гриппа А обладает способностью к изменению своей поверхностной структуры посредством изменчивости поверхностных белков гемагглютинина (Н) и нейраминидазы (N). В результате могут происходить как точечные изменения в этих белках (дрейф), так и полная замена одного из поверхностных белков на новый (шифт). Это приводит к тому, что наша иммунная система не успевает достаточно быстро адаптироваться к изменчивому вирусу и выработать дифференцированный иммунный ответ. В результате отмечаются высокая восприимчивость, повсеместное распространение, короткие интервалы между эпидемиями и вовлечение всех групп населения, в т. ч. детей, подростков и пожилых людей [4, 5]. Эпидемический сезон гриппа и ОРВИ 2015–2016 гг. в РФ характеризовался доминированием вируса гриппа А(Н1N1) pdm 09, сезон 2016–2017 гг. — доминированием вируса гриппа А (Н3N2) [6].
Вирус гриппа В
выделяют только у человека. Он уступает вирусу гриппа А по уровню вирулентности, контагиозности и эпидемиологической значимости, характеризуется более плавной и медленной изменчивостью. Эпидемии, вызванные гриппом В, менее интенсивны и менее длительны, их продолжительность 3–4 нед.
Вирус гриппа С чаще всего выявляют у людей. Он в большинстве случаев протекает в легкой и бессимптомной форме [2–3].
За последние годы на территории РФ и в мире наблюдается сочетанная циркуляция вирусов типа А и В [6].
Вирусы парагриппа. Выделяют вирусы парагриппа человека пяти типов. Они, в отличие от вирусов гриппа, не обладают способностью к изменчивости. Каждой группе вируса парагриппа присущи определенные особенности. Несмотря на то что основная группа этих вирусов размножается в эпителии слизистой оболочки верхних дыхательных путей, особенно носа и гортани, эти вирусы поражают нижние дыхательные пути и вызывают бронхиолиты и бронхопневмонии. Вирусы парагриппа-1 и парагриппа-2 вызывают круп у детей [3].
Аденовирусы. Это ДНК-содержащие вирусы, которые объединяют 47 серотипов человека и 80 серотипов млекопитающих. Классификация ВОЗ подразделяет аденовирусы на 7 подгрупп (A, B, C, D, E, F, G), каждая из них, в свою очередь, включает до 19 различных серотипов. В зависимости от места локализации в организме человека они могут вызывать заболевания респираторного тракта, энтериты и конъюнктивиты. Источником инфекции служат больные люди и здоровые вирусоносители. Пути передачи аденовирусов — воздушно-капельный, фекально-оральный и контактный. Они устойчивы во внешней среде и активны при комнатной температуре до 14 дней. Все эти особенности обусловливают риск инфицирования в течение всего года с максимальными показателями в осенне-зимний период. Во время вспышек среди организованных детей заболевают от 30 до 80% дошкольников и до 40% школьников [5, 7].
Респираторно-синцитиальный вирус (РСВ). Его отличие заключается в отсутствии нейраминидазы и гемагглютинина, тропности к поверхностному эпителию слизистой нижних дыхательных путей, что делает его причиной бронхитов и бронхиолитов. Основной путь передачи — воздушно-капельный, но описаны и случаи передачи через предметы личного обихода. При комнатной температуре вирус сохраняется в течение 6 часов.
РСВ поражает людей всех возрастных групп, вызывая и спорадические заболевания, и вспышки респираторных инфекций, наиболее ярко выраженные в популяциях детей младшего возраста и пожилых людей. С РСВ связано до 70% случаев бронхитов и бронхиолитов, до 58,2% пневмоний. Перенесенный в первые годы жизни бронхиолит способствует формированию бронхиальной астмы [8].
Риновирусы. В настоящее время выделено 113 серологических типов риновирусов человека. Это РНК-содержащие вирусы, которые тропны к эпителию верхних дыхательных путей и вызывают обильные водянистые выделения из носа (профузный насморк). Основной путь передачи этих возбудителей — воздушно-капельный, однако не исключено инфицирование и через контаминированные предметы личного обихода. Из-за широкой циркуляции разнообразных серотипов вирусов и формирования кратковременного иммунитета продолжительность эпидемии может варьировать от нескольких месяцев до нескольких лет (редко встречающиеся разновидности).
Коронавирусы. Распространены повсеместно среди всех групп населения. Коронавирусная инфекция характеризуется сезонными подъемами заболеваемости и эпидемическими вспышками с интервалом в 2–3 года. В основном коронавирус участвует в инфекционных процессах, вызванных другими вирусами. Чаще всего он ассоциируется в патологических процессах, вызванных вирусами гриппа А, парагриппа, риновирусами, РСВ и аденовирусами [5].
Смешанные формы инфекции достигают 70–85% общего объема заболеваемости. Смешанные формы инфекции с участием коронавирусов отличаются тяжелым течением [3].
Метапневмовирусная инфекция. Метапневмовирус человека (МПВЧ) — первый человеческий представитель рода Metapneumovirus подсемейства Pneumovirinae в семействе Paramyxoviridae. Выделяют два генотипа МПВЧ — А и В, которые могут циркулировать параллельно во время эпидемии, но чаще один из них доминирует.
МПВЧ распространен по всему миру и имеет сезонную циркуляцию, сравнимую с таковой у вирусов гриппа и РСВ. У взрослых и детей инфекция может протекать бессимптомно, но в иных случаях вызывает клинические проявления от легких форм инфекций верхних дыхательных путей до тяжелой пневмонии [3].
Диагностика гриппа и ОРВИ
К основным методам лабораторной диагностики,
рекомендованным на территории РФ, относятся следующие:
полимеразно-цепная реакция — основана на обнаружении РНК или ДНК вирусов;
иммунофлюоресцентный и иммуноферментный анализ мазков из полости носа или с задней стенки глотки;
иммунохроматографический тест для экспресс-диагностики гриппа непосредственно при осмотре пациента [9–10];
вирусологический метод (получение культуры возбудителя);
серологическая диагностика (определение титра специфических антител в парных сыворотках).
Этиологическая диагностика гриппа и ОРВИ должна проводиться в случаях:
госпитализации больного по поводу острой инфекции дыхательных путей;
заболевания лиц с высоким риском неблагоприятного исхода — детей до 1 года, беременных, лиц с хроническими заболеваниями;
регистрации очагов ОРВИ с множественными случаями заболеваний в организованных коллективах детей и взрослых с круглосуточным пребыванием [11].
Клиническая картина ОРВИ существенно варьирует в зависимости от этиологии возбудителя, состояния иммунной системы, возраста пациента и наличия сопутствующей патологии. Но в подавляющем большинстве при гриппе и ОРВИ можно выделить три основных синдрома — интоксикационный, катаральный и геморрагический [12]. Симптомы, которые возникают в первые дни и часы заболевания, обусловлены развитием локальной воспалительной реакции в воротах инфекции. Дальнейшее развитие симптоматики зависит от активности факторов врожденного иммунитета и скорости запуска высокоспецифичных иммунных реакций, направленных на полную элиминацию вируса. Иногда возникает чрезмерная локальная воспалительная реакция, которая приводит к массивной гибели окружающих тканей и вирусемии, вследствие чего развиваются такие грозные осложнения, как отек легких, инфекционно-токсический шок, острый респираторный дистресс-синдром, полиорганная недостаточность. Таким образом, даже при наличии обычных симптомов ОРВИ с первых часов целесообразно назначение сочетания противовирусных и патогенетических препаратов (противовоспалительных и антиоксидантных).
Лечение
Заключение
На сегодняшний день не существует универсального противовирусного препарата, способного защитить от всех патогенов, ответственных за возникновение гриппа и других ОРВИ, т. к. вирусы, в силу своей изменчивости, со временем вырабатывают резистентность. Этим и обусловлена потребность в препаратах, действующих не на конкретный белок вируса, а обладающих комплексным действием на клеточные и гуморальные иммунные механизмы противовирусной защиты.
Для развития инфекционного заболевания необходимо наличие ряда факторов.
Пути передачи возбудителей инфекционных заболеваний
Существуют различные способы передачи патогенных микроорганизмов. В некоторых случаях эпидемические штаммы хорошо переносят неблагоприятные условия и способны к быстрому распространению.
Большинство патогенных микроорганизмов приспосабливаются к тем или иным способам передачи. Следует отметить, что распространение возбудителей, вызывающих поражение дыхательной системы, облегчается при помощи кашля, который они вызывают. В то же время рвота и диарея, возникающие при заболеваниях, передающихся посредством фекально-орального механизма, способствуют попаданию возбудителей (находящихся в большом количестве в желудочно-кишечном тракте) в окружающую среду.
Внедрение возбудителя инфекции в организм хозяина
Для роста и размножения микроорганизмы должны проникнуть в ткани хозяина, а потому обладают широким спектром методов и механизмов прикрепления. Выбор органов-мишеней зависит от того, с какими рецепторами может взаимодействовать тот или иной возбудитель. Так, Neisseria gonorrhoeae прикрепляется к слизистой оболочке половых органов при помощи фимбрий, а вирус гриппа взаимодействует с клетками хозяина посредством гемагглютинина.
Эти свойства учитывают при определении сродства к рецепторам и исследовании патогенности видоспецифичных (определённые штаммы поражают определённые организмы) и межвидовых патогенов.
Некоторые бактерии обладают специальными механизмами, позволяющими им достичь эпителия млекопитающих. Например, для достижения энтероцитов Vibrio cholerae вырабатывает муциназу. Взаимодействие Н. pylori с сиалированными белками слизистой оболочки желудка зависит от степени сиалирования поверхностных структур возбудителя.
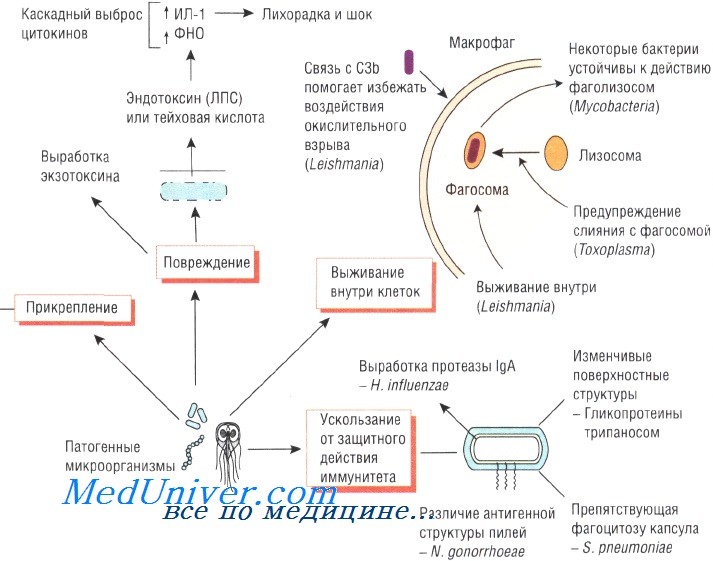
Патогенез инфекционного заболевания
Giardia lamblia прикрепляется к слизистой оболочке тощей кишки при помощи специальной присоски. Эритроциты, поражённые Plasmodium falciparum, продуцируют белок, стимулирующий адгезию к сосудам мозга, что приводит к развитию церебральной формы малярии.
Некоторые бактерии образуют полисахаридную биоплёнку, облегчающую микробное заселение искусственных протезов и имплантов (например, катетеров), постоянно находящихся в организме. Кроме того, некоторые штаммы стафилококков имеют гены, стимулирующие их прикрепление к пластиковым поверхностям и биомолекулам, покрывающим внутрисосудистые устройства.
При продолжительном повреждении тканей различные штаммы S. aureus могут связываться с некоторыми молекулами организма хозяина (фибронектин, вибронектин и коллаген). Различные штаммы Escherichia coli используют фимбрий, или пили, для прикрепления к маннозе или групповым антигенам крови и, соответственно, они вызывают инфекционные заболевания желудочно-кишечного тракта или мочевыводящих путей. ВИЧ связывается с CD4 и некоторыми другими антигенами.
Таким образом, каждый штамм обладает определёнными генами, обусловливающими его способность к внедрению в организм хозяина.
Инвазия возбудителя инфекционного заболевания
Существует множество механизмов, при помощи которых микроорганизмы преодолевают слизистые оболочки и различные типы клеточных мембран. После этого они должны закрепиться в организме хозяина и начать интенсивно размножаться.
Некоторые бактерии, например рода Helicobacter и Neisseria, продуцируют IgA-протеазу, разрушающую IgA. Таким образом, эти возбудители нейтрализуют одну из важнейших защитных систем слизистой оболочки организма.
Подвижность возбудителя инфекционного заболевания
Способность микроорганизмов передвигаться в поисках новых источников питания или в ответ на хемотаксические сигналы приводит к заметному усилению их патогенности. Например, штаммы Vibrio cholerae, обладающие жгутиками, намного более вирулентны, нежели неподвижные штаммы.
Устойчивость возбудителя инфекции к защитным механизмам иммунной системы
Для выживания в организме хозяина возбудителям необходимо противостоять защитным механизмам иммунной системы. Бактерии, поражающие дыхательную систему, продуцируют IgA-протеазу, разрушающую иммуноглобулины. Staphylococcus aureus секретирует протеин А, связывающий иммуноглобулины и препятствующий опсонизации и активации системы комплемента.
Один из важнейших механизмов противостояния иммунной системе — устойчивость к фагоцитозу. Полисахаридная капсула препятствует захвату Streptococcus pneumoniae полиморфноядерными нейтрофилами. Кроме того, некоторые микроорганизмы
Липополисахариды грамотрицательных бактерий обусловливают их устойчивость к действию комплемента, а Trypanosoma способна изменять свои поверхностные антигены во избежание их взаимодействия с антителами.
Редактор: Искандер Милевски. Дата обновления публикации: 18.3.2021
Информация на сайте подлежит консультации лечащим врачом и не заменяет очной консультации с ним.
См. подробнее в пользовательском соглашении.

Внешние факторы не могут ни породить в организме, ни вызвать в нем ничего сверх того, что у него имеется в виде исторически развившихся потенций [8]. Каковы бы ни были внешние условия, они не могут напрямую произвести никаких изменений в организме. Эти изменения возникнут только при наличии соответствующего внутреннего основания. В конечном итоге именно внутренний фактор решает вопрос о возникновении болезни; он же придает ей свои черты в клиническом и морфологическом выражении.
Познание общепатологических механизмов немыслимо без анализа узловых проблем инфекционного процесса. Эволюционное становление воспалительной реакции определялось прежде всего бактериальной инвазией, что убедительно показано еще И.И. Мечниковым. В то же время понять специфические проявления той или иной инфекции, обособленно изучая микро- и макроорганизм, невозможно. Сущность инфекционного процесса открывается лишь в их взаимодействии. Более того, многие важные свойства патогенные микробы вообще не обнаруживают при их росте на искусственных питательных средах [6].
Патогенез инфекционных болезней не исчерпывается непосредственными результатами жизнедеятельности их возбудителей и повреждениями, причиняемыми бактериальными токсинами. Основные симптомы многих инфекционных болезней (лихорадка, кашель, понос и даже нагноение) носят приспособительный характер и отображают не столько повреждение, сколько активную реакцию организма. Так, пирогенные свойства микробных липополисахаридов долгое время представлялись совершенно бесспорными. Между тем выяснилось, что повышение температуры в таких случаях вызывает не сам эндотоксин, а эндогенные пирогены, выделяющиеся из погибающих лейкоцитов. Таким образом, речь идет не о повреждении, а об особом механизме, вступающем в действие под влиянием микробной инвазии и ведущем к температурной реакции, имеющей приспособительное значение. Образование эндогенного пирогена - уникальное свойство фагоцитов, специализирующихся на защите организма [6].
Однако в биологическом взаимодействии паразита с хозяином микроб также занимает свою активную позицию, направленную на выживание вида. Существование в природе многочисленных возбудителей инфекций поддерживается с помощью двух основных механизмов сохранения их видового состава: 1) путем длительной персистенции микробов в организме и 2) путем периодической смены хозяина в процессе бактериовыделения и последующего внедрения в новый организм. По-видимому, у возбудителей с узкой экологической нишей вероятность сохранения вида более надежно обеспечена при их длительном персистировании в организме, чем в процессе беспрерывной смены хозяина. Так, у Mycobacterium tuberculosis сохранение вида в значительной степени определяется их способностью к длительной персистенции, что обусловлено исключительно тесной адаптацией этих бактерий к одному виду хозяина [14]. Основными механизмами персистенции микробов в организме хозяина являются внутриклеточное паразитирование, антигенная мимикрия, образование L-форм, а также механизмы подавления факторов защиты макроорганизма [5, 12, 14]. Они являются биологической основой хронизации инфекционного процесса.
Эпителиальные клетки, подобно фагоцитам мезенхимального происхождения, способны к фагоцитозу. Б.М. Ариэль [2] выдвинул гипотезу, согласно которой при инфекционном процессе в определенных условиях может восстанавливаться фагоцитарная функция эпителия, присущая низко организованным животным и репрессированная в филогенезе. В ходе инфекционного процесса конвергентно сближаются морфологические и функциональные свойства фагоцитов и эпителиальных клеток различного гистогенеза. Эпителий дополняет элиминативную функцию мезенхимных элементов, когда они уже исчерпали свои возможности. Не обладая достаточно эффективными механизмами внутриклеточного разрушения бактерий, эпителиоциты транспортируют их в собственную оболочку, где они, встречаясь с фагоцитами, могут быть уничтожены. Здесь прослеживается один из механизмов отклонения тканевого гомеостаза - нарушение фагоцитарно-элиминативной функции эпителиального пласта. При повреждении (или истощении) этой функции микробы задерживаются, а затем размножаются в цитоплазме эпителиоцитов.
При изучении патогенных факторов микробов целесообразна сравнительная оценка скоростей развития некробиотических и репаративных изменений в тканях. Лишь в том случае, если первая скорость превышает вторую, патогенные факторы микробов приводят к развитию морфологически документируемого повреждения. При инфекционном процессе в первую очередь повреждаются не клетки как таковые, а клеточные популяции, ткани, состоящие из клеток разной дифференцированности и связанные единством происхождения и функции. Основное повреждающее действие на ткани при инфекционном процессе оказывают токсические факторы. Морфологические признаки такого повреждения проявляются в нарушении клеточной дифференцировки и межклеточных контактов, обеспечивающих целостность эпителия как тканевой системы.
Для хронического инфекционного процесса характерно волнообразное течение: фаза обострения при благоприятном течении заболевания сменяется фазой ремиссии и т.д. В фазе ремиссии хронического воспалительного процесса в зоне поражения находят признаки хронического воспаления - макрофагально-лимфоцитарную инфильтрацию (в фазе обострения - нейтрофильную). Что ее поддерживает? Значит, имеет место персистенция причинного фактора [12]. Морфологически в этой фазе наблюдается хроническая (перманентная) дисрегенерация. В чем ее сущность?
Здесь вырисовывается универсальный приспособительный механизм. В фазу ремиссии патогенная инфекция уходит во внутриклеточное персистирование, уклоняясь от иммунной защиты. В ответ на это организм активно включает механизм апоптоза, направленный на элиминацию микробной инфекции. Апоптоз, в свою очередь, вызывает активацию регенераторных процессов. Так поддерживается феномен приспособительного усиления пролиферативной активности ткани в зоне хронического инфекционного процесса (в регенерирующих тканях). В фазе обострения усиление пролиферативных процессов гораздо более выражено в связи с массовой гибелью клеток в зоне воспаления.
Инфекционный процесс во многих случаях начинается не с взаимодействия патогенного микроорганизма с восприимчивым макроорганизмом как таковым, а прежде всего с взаимодействия с микрофлорой хозяина. Микробы-антагонисты на слизистых оболочках осуществляют защитное действие. Так, кишечная микроэкологическая система является частью гомеостатической системы организма. Микроэкология желудочно-кишечного тракта (ЖКТ) включена в систему защиты организма, и при ее нарушении становится источником инфекционного процесса. Основной механизм защиты слизистой ЖКТ - колонизационная резистентность. Пристеночная микрофлора повышает колонизационную резистентность кишечника, конкурируя с патогенными микроорганизмами за взаимодействие с рецепторами эпителиальных клеток слизистой оболочки ЖКТ. Она способствует нормальному течению метаболических процессов в эукариотных клетках [7].
Таким образом, персистенция микробной инфекции в условиях отклонения тканевого гомеостаза барьерных тканей является фундаментальной биологической основой хронизации инфекционного процесса.
Читайте также:

