Ферменты казеин связки структурные белки дифтерийный токсин
Обновлено: 24.04.2024
Культуральные свойства дифтерийной палочки. Культуральные особенности биоваров дифтерии. Биохимическая активность палочки Клебса-Лёффлера. Бактериоцины дифтерии.
Культуральные свойства дифтерийной палочки. Дифтерийная палочка хорошо растёт при 36-37 °С; оптимум рН 7.4-8,0. Питательные среды должны содержать аминокислоты, витамины, ионы металлов (Са2+, Mg2+ Fe2+ и др.), играющие роль ростовых факторов. На сывороточных средах (например, среде Лёффлера) дают рост уже через 10-12 ч; за это время контаминирующая микрофлора обычно не успевает развиться. Наибольшее распространение получили среды с теллуритом, так как возбудитель резистентен к высоким концентрациям теллурита калия или натрии, ингибирующим рост сопутствующей микрофлоры.
На таких средах дифтерийная палочка образует серовато-чёрные колонии в результате восстановления теллурита до металлического теллура, аккумулирующегося внутри бактерий (рис. 8, см. цветную вклейку). В жидких средах образуют помутнение и осадок; их образование и характер варьируют у различных биоваров.
Биохимическая активность дифтерии
Палочка Клебса-Лёффлера сбраживает с образованием кислоты глюкозу, мальтозу, галактозу, декстрин; не разлагает сахарозу, лактозу, маннит. Способность разлагать крахмал и гликоген варьирует у различных штаммов, что используют для внутривидовой дифференцировки.
Дифтерийная палочка не гидролизует мочевину и не образует индол. Отсутствие способности ферментировать сахарозу и разлагать мочевину — дифференцирующий признак, отличающий дифтерийную палочку от других коринебактерий. Другой дифференцирующий признак — способность разлагать цистин. С. diphtheriae продуцирует каталазу, гиалуронидазу, нейраминидазу, ДНКазу, уреазу и др.
Цистиназная активность — дифференцирующий признак дифтерийной палочки. Дифтерийная палочка лизирует эритроциты морской свинки и кролика.
Биовары возбудителя дифтерии существенно различаются по культуральным и биохимическим свойствам. Среди дифференциально-диагностических биохимических тестов наиболее часто учитывают различия в способности разлагать углеводы и мочевину.
Бактериоцины дифтерии
Дифтерийная палочка образует бактериоцины (корицины), обладающие узким спектром действия. Гены, кодирующие синтез бактериоцинов, передаются плазмидами. Бактериоцины дифтерийной палочки образуют как токсигенные, так и нетоксигенные штаммы.
- Вернуться в оглавление раздела "Микробиология."
Информация на сайте подлежит консультации лечащим врачом и не заменяет очной консультации с ним.
См. подробнее в пользовательском соглашении.
Выявление дифтерийной палочки. Принципы микробиологической диагностики дифтерии. Диагностика дифтерии. Культивирование дифтерии. Определение токсигенности дифтерийной палочки.
С целью раннего выявления дифтерии и определения носителей дифтерийной палочки необходимы выделение и идентификация возбудителя, а также определение его способности к токсинообразованию. Материалом для исследования служат дифтеритические плёнки, слизь из носоглотки или отделяемое из подозрительных поражений кожных покровов.
Забор материала на дифтерию проводят двумя стерильными тампонами: один используют для посева, с другого делают мазки и окрашивают их по Граму и Найссеру. Взятый материал следует доставлять в лабораторию не позднее чем через 3 ч.
Бактериоскопия дифтерийной палочки
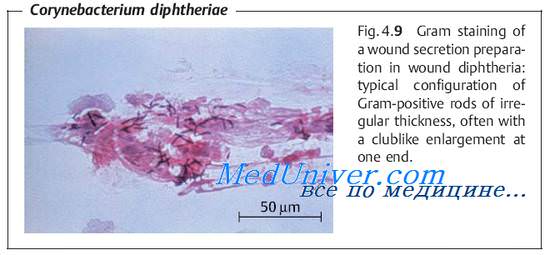
Окраска по Граму не является специфичной, так как дифтерийные палочки сравнительно плохо воспринимают красители, но позволяет косвенно идентифицировать непатогенные коринебактерии, располагающиеся в виде палисада (параллельно) или в виде китайских иероглифов. Окраска по Найссеру позволяет выявить характерные зёрна Бабеша-Эрнста и отличить дифтерийную палочку от ложнодифтерийной палочки С. pseudodiphtheriticum (С. hofmannii), часто обитающей в носоглотке.

Культивирование дифтерийной палочки
Бактерии дифтерии выделяют посевом на элективные среды с теллуритом (например, Клауберга II или Маклёода), ложнодифтерийная палочка (палочка Хофманна) теллур не восстанавливает (см. рис. 8 на вклейке). Для выделения чистой культуры дифтерии часть подозрительной колонии засевают на скошенный агар (или среду Ру), вторую часть — на твёрдую питательную среду для определения токсигенности и (не обжигая петли) проводят определение цистиназной активности (проба Пизу). При положительном результате наблюдают образование коричневого облачка вокруг линии укола. Чистую культуру идентифицируют на средах Хйсса, пользуясь укороченным пёстрым рядом (глюкоза, мальтоза, сахароза, мочевина), что позволяет отличить С. diphtheriae от непатоген пых коринебактерии (рис. 14-3).
Определение токсигенности дифтерийной палочки
Определение токсигенности дифтерийной палочки in vivo. Проводят подкожным или внутрикожным заражением 0,5-1,0 мл бактериальной культуры морских свинок массой 250 г. За 24 ч до заражения одно животное иммунизируют дифтерийным антитоксином. При положительном результате неиммунизированные животные погибают в течение 3-5 сут.
Фаготипирование дифтерийной палочки
Для дифференциальной диагностики возбудителей используют набор из 9 кори нефагов. С его помощью можно типировать большинство токсигенных и нетоксигенных штаммов биовара gravis.

Дифтерия - это острое инфекционное заболевание, опасное для жизни. Наиболее восприимчивы к нему дети в возрасте 3–7 лет, в последние годы увеличилась заболеваемость подростков и взрослых.
Дифтерия – это острое инфекционное заболевание, опасное для жизни. Оно протекает в виде острого воспаления верхних дыхательных путей, преимущественно глотки (примерно 90% случаев), носа, кожи в местах ее повреждения, глаз или половых органов.
Основную угрозу, однако, представляет не воспаление, а отравление токсином, который вырабатывает бактерия – возбудитель заболевания, при этом преимущественно поражаются сердечно-сосудистая и нервная системы.
Возбудитель дифтерии и пути заражения
Возбудителем дифтерии являются Corynebacterium diphteriae – грамположительные бактерии в виде палочек с характерными колбовидными утолщениями на концах, которые в мазках располагаются попарно, под углом в виде римской цифры V по отношению друг к другу. Дифтерийные палочки в процессе жизнедеятельности выделяют дифтерийный токсин, фермент нейраминидазу и другие биохимически активные соединения.
Синтез дифтерийного токсина микробными клетками контролируется специальным геном tox. Бактерии могут терять его в процессе жизнедеятельности, утрачивая вместе с ним и свою способность вырабатывать токсин (токсигенность). И, наоборот, изначально нетоксигенные штаммы могут приобретать патогенные свойства, к счастью, это случается крайне редко.
Заболевание передается воздушно-капельным путем от больных дифтерией или от здоровых носителей инфекции, значительно реже – через предметы обихода.
Группа риска
Наиболее восприимчивы к заражению дифтерией дети в возрасте 3–7 лет, но в последние годы увеличилась заболеваемость подростков и взрослых.
Источником инфекции являются больные люди или здоровые носители токсигенных бактерий. Наиболее заразны страдающие дифтерией зева, носа и гортани, так как они активно выделяют возбудителей заболевания с выдыхаемым воздухом. Больные дифтерией глаз, кожи могут распространять инфекцию контактным путем (руки, предметы быта). Здоровые носители бактерий гораздо менее заразны, но отсутствие у них каких-либо внешних признаков их состояния не позволяет контролировать распространение ими инфекции, ведь выявить их можно только случайно в ходе массовых диспансерных обследований. В результате большинство случаев заражения дифтерией обусловлено контактом со здоровыми носителями дифтерийной палочки.
Инкубационный период (время от момента заражения до появления первых признаков заболевания) составляет 2–10 дней.
Дифтерийный токсин
Токсин, вырабатываемый дифтерийной палочкой, состоит из нескольких компонентов. Один из них – фермент гиалуронидаза разрушает гиалуроновую кислоту капилляров и увеличивает их проницаемость, что приводит к выходу из сосудов и пропитыванию окружающих тканей плазмой крови с отложением белка фибриногена. Второй компонент – некротоксин разрушает клетки эпителия с выделением из них фермента тромбокиназы. Тромбокиназа способствует превращению фибриногена в фибрин и образованию на поверхности тканей фибринной пленки. При действии дифтерийного токсина на небные миндалины, которые покрыты несколькими слоями эпителиальных клеток, формируется фибиринная пленка, проникающая вглубь эпителия миндалин и плотно спаянная с ним.
Третий (основной) компонент – собственно токсин способен блокировать процессы клеточного дыхания и синтеза белковых молекул. Наиболее чувствительными к его действию являются капилляры, клетки миокарда и нервные клетки. В результате развивается дистрофия миокарда и инфекционно-токсический миокардит, повреждение капилляров приводит к инфекционно-токсическому шоку, повреждение шванновских клеток (вспомогательные клетки нервной ткани) приводит к демиелинизации нервных волокон (разрушение электроизолирующего слоя миелина с нарушением проведения нервных импульсов по нервным волокнам). Кроме того, дифтерийный токсин вызывает общую интоксикацию организма.
Симптомы и течение
Дифтерия зева обычно начинается с небольшого повышения температуры, незначительной болезненности при глотании, покраснения и отечности миндалин, формированию на них специфического пленчатого налета, увеличения передних верхних шейных лимфатических узлов. Цвет пленок – обычно белый в первые 2–3 дня заболевания, но потом приобретает серый или желтовато-серый цвет. Примерно через неделю заболевание, или заканчивается выздоровлением (легкая форма, как правило, у привитых от дифтерии), или переходит в более тяжелую токсическую форму, обусловленную системным действием дифтерийного токсина.
Токсическая форма дифтерии всегда протекает очень тяжело. Она характеризуется очень высокой температурой тела (39,5-41,0°С), сильными головными болями, сонливостью, апатией. Кожа становится бледной, во рту отмечается сухость, у детей возможна многократная рвота и боль в животе. Отек миндалин становится резко выраженным, может приводить к полному закрытию входа в глотку, распространяется на мягкое и твердое небо, часто также на носоглотку, дыхание затрудняется, голос часто становится гнусавым. Налет распространяется на все ткани ротоглотки. Классическим признаком токсической формы дифтерии зева является отек подкожной клетчатки в области шеи, а иногда и грудной клетки, в результате чего кожа приобретает студнеобразную консистенцию. Передние верхние шейные лимфатические узлы значительно увеличены и болезненны.
Дифтерия носа протекает на фоне нормальной или слегка повышенной температуры тела, интоксикация отсутствует. Из носовых ходов видно серозно-гнойное или кровянисто-гнойное отделяемое. На крыльях носа, щеках, лбу и подбородке появляются участки мокнутия, а затем сухие корочки. Внутри носа видны пленчатые налеты. Патологический процесс может также поражать придаточные пазухи носа. При токсической форме наблюдается отек подкожной клетчатки щек и шеи.
Дифтерия глаза протекает как банальный конъюнктивит и характеризуется умеренной гиперемией и отеком конъюнктивы века, небольшим количеством серозно-гнойного отделяемого из конъюнктивального мешка (катаральная форма). Пленчатая форма проявляется выраженным отеком век, наличием на их конъюнктиве трудно снимаемых пленок серовато-белого цвета. Токсическая форма также сопровождается отеком клетчатки вокруг глазницы.
Дифтерия кожи приводитк длительному не заживлению любых повреждений кожи, гиперемии, на коже присутствует грязно-серый налет, отмечается плотная инфильтрация окружающей кожи.
Диагностика
Диагностику дифтерии проводят на основании данных осмотра больного и результатов анализов. При осмотре за диагноз дифтерия говорят следующие признаки: наличие характерных пленок, а также затруднение дыхания и свистящий шум на вдохе, не характерные для ангины, лающий кашель. Диагноз дифтерии по характерным клиническим признакам при заболевании, протекающем в легкой форме, поставить сложнее.
Общий анализ крови – признаки острого воспалительного процесса.
Исследования мазка под микроскопом (бактериоскопия) – выявление имеющих характерный вид бактерий Corynebacterium diphteriae.
Бактериологическое исследование – посев биологического материала на специальную питательную среду и культивирование колоний микроорганизмов.
Определение уровня (титра) антитоксических антител (высокий титр – 0,05 МЕ/мл и выше позволяет исключить дифтерию).
Серологическое исследование – определение специфических антител в сыворотке крови с помощью методов РПГА, ИФА и др.
Дифтерию зева нужно дифференцировать от острого тонзиллита (фолликулярная и лакунарная формы), ангины Симановского-Венсана (грибковое поражение), сифилитической ангины, ложнопленочной ангины при инфекционном мононуклеозе, паратонзиллярным абсцессом, эпидемическим паротитом, лейкозом. У детей необходимо отвести диагноз ложного крупа.
Лечение
Всех заболевших дифтерией, вне зависимости от тяжести состояния, необходимо госпитализировать в инфекционную больницу.
Лечение состоит в следующем:
Диета – витаминизированная, калорийная, прошедшая тщательную кулинарную обработку еда.
Этиотропная терапия (то есть направленная на устранение причины заболевания) – введение противодифтерийной сыворотки (ПДС), доза и количество раз введения зависят от тяжести и формы заболевания. При легкой форме ПДС вводится однократно внутримышечно в дозе 20–40 тыс. МЕ, при среднетяжелой форме – 50–80 тыс. МЕ однократно или, при необходимости, повторно в той же дозе через 24 часа. При лечении тяжелой формы заболевания суммарная доза увеличивается до 90–120 тыс. МЕ или даже до 150 тыс. МЕ (инфекционно-токсический шок, ДВС-синдром). При этом 2/3 дозы вводится сразу, и в течение первых суток госпитализации должно быть введено 3/4 суммарной дозы.
Антибиотики: при легких формах – эритромицин, рифампицин внутрь, при среднетяжелых и тяжелых формах – инъекционное введение пенициллинов или цефалоспоринов. Продолжительность курса – 10–14 дней. Антибиотики не влияют на дифтерийный токсин, но уменьшают количество бактерий, его вырабатывающих.
Местное лечение – полоскания и орошения дезинфицирующими растворами.
Дезинтоксикационная терапия – глюкозо-солевыми растворами с учетом суточной потребности в жидкости и ее потерь (среднетяжелая и тяжелая форма).
Глюкокортикостероиды – при среднетяжелой и тяжелой формах.
Лечение бактерионосителей проводят антибиотиками: тетрациклины (дети старше 9 лет), эритромицин, цефалоспорины на фоне общеукрепляющей терапии и устранения хронических очагов инфекции.
Осложнения
Среди наиболее серьезных осложненийдифтерии на сердечно-сосудистую систему можно выделить миокардиты, нарушения сердечного ритма.
Неврологические осложнения дифтерии обусловлены поражением различных черепных и периферических нервов и проявляются параличом аккомодации, косоглазием, парезами конечностей, а в более тяжелых случаях параличом дыхательных мышц и мышц диафрагмы.
Вторичными осложнениями дифтерии являются такие тяжелые патологические состояния как острые нарушения мозгового кровообращения (тромбозы, эмболия), метаболическая энцефалопатия, отек головного мозга, токсические поражения почек, дифтерийный гепатит, а также инфекционно-токсический шок и ДВС-синдром (синдром дессиминированного внутрисосудистого свертывания – тяжелое нарушение системы свертывания крови). Токсическая форма дифтерии может приводить к острой почечной, сердечно-сосудистой, дыхательной или полиорганнной недостаточности.
Неспецифическими осложнениями дифтерии являются паратонзиллярный абсцесс, отит, пневмония.
Вакцинация
Вакцинация от дифтерии проводится анатоксином, то есть инактивированным токсином. В ответ на его введение в организме образуются антитела не к Corynebacterium diphteriae, а к дифтерийному токсину.
Согласно российскому прививочному календарю, вакцинация детей в возрасте до года проводится в 3, 4–5 и 6 месяцев. Первая ревакцинация проводится в 18 месяцев, вторая – в 7 лет, третья – в 14. Взрослые должны ревакцинироваться от столбняка и дифтерии каждые 10 лет.

Партнер номинации — компания Cytiva.
Генеральный партнер конкурса — международная инновационная биотехнологическая компания BIOCAD.
Молекулярный аппарат трансляции и его консервативность
Трансляционный цикл на множестве этапов может быть нарушен или замедлен многочисленными и разнородными по химическому строению ингибиторами. Ключевые компоненты трансляционного аппарата клетки — это рибосомы и факторы трансляции (белки, помогающие рибосоме реализовывать разные этапы трансляционного цикла), а также большое количество вспомогательных белков, необходимых для обеспечения синтеза нужными материалами: например, аминоацил-тРНК-синтетазы (АРСазы) — ферменты, соединяющие тРНК с соответствующей ей аминокислотой; или регуляторы биосинтеза белка — компоненты сигнальных путей, связанных с трансляцией. При подборе ингибиторов нельзя не учитывать, что многие из этих молекул есть у всех живых организмов, и некоторые из них довольно консервативны. А значит, одни и те же вещества могут действовать как на про-, так и на эукариот, что не всегда приемлемо.
Каждый живой организм на Земле может быть отнесен к одному из трех доменов жизни: это максимально удаленные друг от друга в эволюционном смысле группы — эукариоты (здесь ищите самые известные царства: животных, растений и грибов), бактерии и археи [2]. Эта удаленность означает, что они давно разошлись (то есть их последний общий предок жил давно [3]), и у представителей групп накопилось множество отличий. Но есть и признаки, по которым представители различных доменов похожи друг на друга. Речь идет об основополагающих признаках: например, способности удваивать ДНК, синтезировать на ее основе РНК и в конце концов получать закодированный в ней белок. Трансляция относится к самым консервативным биологическим процессам.
При ближайшем рассмотрении оказывается, что устройство белоксинтезирующего аппарата довольно схоже у представителей разных доменов. К примеру, основные факторы инициации и элонгации у бактерий имеют гомологов у архей, а рибосомы архей по многим аспектам строения очень напоминают рибосомы эукариот (что даже позволило создать из рибосом дрожжей гибридные рибосомы, в которых одна из субъединица очень напоминала рибосомную субъединицу архей [4]). В пределах этих трех доменов есть отличия, но мы видим, что трансляционная машинерия в целом очень консервативна, и таких отличий не так много. Это является несомненным свидетельством общности (монофилетичности) происхождения жизни.
Ингибиторы трансляции как антибиотики
Чаще всего исследователям приходится подбирать ингибиторы биосинтеза белка у бактерий и заботиться о том, чтобы они не действовали на эукариот, так как это позволяет применять такое вещество в качестве антибиотика. Больше половины используемых сейчас антибиотиков подавляет именно трансляцию, действуя на рибосому , [5]. И здесь на первый план зачастую выходят те тонкие различия, которые все-таки можно отыскать в строении аппарата трансляции у представителей разных доменов.
Трансляционный цикл
Схема может показаться сложной, но в действительности это не так. Попробуйте выхватить взглядом желтую 40S-субъединицу (в свободном от других компонентов трансляции виде ее можно найти рядом со стадией i.1) и пройтись по циклу, как в настольной игре, посмотрев на все, что успевает с ней за это время произойти. Особенно любознательным предлагаем покликать по элементам схемы и прочитать о каждом из этапов дополнительно.
Этапы трансляции
Трансляционный цикл принято подразделять на несколько этапов:
Отдельно происходит активация аминокислот с помощью аминоацил-тРНК-синтетаз (см. e.1 на рисунке 1).
Некоторые трансляционные факторы известны уже очень давно, для них понятна функция, известны ортологи у архей и бактерий (подробнее про гомологичные взаимоотношения генов можно прочитать здесь [7]) и выяснено, являются ли они строго необходимыми для синтеза белка — ведь некоторые вирусные мРНК, например, могут обходиться без целого ряда факторов инициации трансляции [8], [9]. Роль других участников была открыта относительно недавно. Примером таких белков служат факторы DENR и MCTS1 (см. область рециклинга (r) на рисунке 1), изучением которых, кстати, занимается наша лаборатория.
На рисунке 1 (см. s.1, s.2) также изображена часть путей внутриклеточного сигналинга, которые непосредственно регулируют трансляцию. Кроме того, существует еще и сложнейший процесс сборки рибосомы из рибосомной РНК и белков, который протекает по большей части в ядре. Его также можно подавить низкомолекулярными веществами, но о них известно гораздо меньше, а их специфичность часто оставляет желать лучшего.
Типы ингибиторов
С ингибиторами трансляции удобно знакомиться, если классифицировать их согласно мишеням, на которые они воздействуют.
Ингибиторы эукариотической рибосомы
Многие из ингибиторов действуют на рибосомы. При этом они могут быть универсальными (подавлять трансляцию у всех доменов живого), а могут — специфичными (например, к рибосоме эукариот или даже каких-то узких таксономических групп). Специфичность действия, как правило, определяется тонкими различиями в строении места связывания: структурные исследования показывают, что часто достаточно замены одного нуклеотида в рРНК или разницы в единственной аминокислотной позиции рибосомного белка, чтобы конфигурация участка не позволяла ингибитору связаться. Подавляющее большинство ингибиторов рибосомы действует на стадии элонгации, однако существуют и другие типы, перечисленные в таблице 1 (заметьте, что пункты могут перекрываться).
Если классифицировать по сайтам связывания, то выделяют: ингибиторы пептидилтрансферазного центра; ингибиторы транслокации, узнающие E-сайт; ингибиторы, связывающиеся в пептидном тоннеле; ингибиторы, взаимодействующие с декодирующим центром; ингибитор, связывающийся с ГТФаза-активирующим центром (пока достоверно описан только один такой пример).
Пока не так много веществ этого типа допущены до практического применения (самое известное из них — гомохаррингтонин (рис. 2)), но их число постепенно растет. Клинические и доклинические испытания проходили, например, такие ингибиторы пептидилтрансферазного центра, как ликорин, нарциклазин и бруцеантин, а ингибитор транслокации эметин используется как антигельминтное и противомалярийное средство.
Интересные случаи применения
Гомохаррингтонин. Рибосом-направленные ингибиторы элонгации
Гомохаррингтонин — ингибитор пептидилтрансферазного центра в виде полусинтетического аналога омацетаксина мепесукцината (продаваемого под торговой маркой Synribo; рис. 2) активно применяется для лечения хронического миелоидного лейкоза, а также проходит испытания в терапии ряда других онкологических заболеваний. Кроме того, его широко используют в научной работе: его способность прекращать трансляцию новоинициировавших рибосом (при этом не трогая рибосомы, которые уже успели синтезировать несколько пептидных связей) применяется для картирования старт-кодонов в мРНК.
Аталурен и гентамицин. Вещества, вызывающие ошибки декодирования
Рисунок 4. Гентамицин. Пока что препарат прошел клинические испытания только как антибиотик, однако у его производных есть потенциал и в терапии генетических заболеваний. Препарат, продаваемый в аптеках, представляет собой смесь более четырех похожих веществ. Его стоимость куда ниже, чем у аталурена: купить тюбик мази для наружного применения можно за 40 рублей. Однако в нынешнем виде гентамицин нельзя принимать в дозах, достаточных для устранения эффектов нонсенс-мутаций: из-за воздействия на рибосомы митохондрий он имеет побочные эффекты в виде нефро- и ототоксичности.
Чтобы понять, как именно ингибиторы могут подавлять активность рибосомы, полезно вспомнить ее общее строение. Это удобно сделать с помощью интерактивного аплета (см. рис. 5).
Рисунок 5. Пристальный взгляд на эукариотическую рибосому. В верхней кнопочной панели можно изучить структурные элементы рибосомы. Для того чтобы узнать о структурном элементе или сайте связывания, наведите курсор на кнопку. В нижней панели можно найти распространенные ингибиторы, которые действуют на разные части эукариотической рибосомы, визуализированные в предыдущем разделе. В виде на лиганд взаимодействующие основания выделены оранжевым. Встроенный в статью этот апплет очень маленький, поэтому рекомендуем открыть полноэкранную версию.
- Чтобы увидеть лиганд-белковые взаимодействия, можно кликнуть на лиганд в режиме его просмотра.
- Из-за большого размера структур и их сложности для просмотра рекомендуется пользоваться компьютером со стабильным подключением.
- При переходе между видом рибосомы и видом на лиганд структура перезагружается.
- К сожалению, выделение структурных элементов из прошлого раздела в структурах с ингибиторами не поддерживается.
- В будущем рисунок будет совершенствоваться, при клике на хищную рибосому читатель может найти более совершенную версию, которая периодически обновляется.
Для показа структурных элементов использована структура дрожжевой рибосомы, полученная методом криоэлектронной микроскопии группой Р. Бекманна (6SNT). Для визуализации используется веб-плагин MolStar.
Ингибиторы трансляционных факторов
Трансляционные факторы — белки, помогающие рибосоме реализовывать разные этапы трансляционного цикла. Чаще всего эти факторы жизненно необходимы для нормального синтеза белка в клетках или митохондриях/пластидах, которые, как правило, тоже имеют свой трансляционный аппарат.
Эта группа веществ взаимодействует с факторами в растворе, блокируя их активность или препятствуя присоединению к рибосоме (во втором случае они могут контактировать не только с фактором, но и с рибосомой, что приводит к неоднозначности в классификации: иногда их относят к ингибиторам рибосомы).
Ингибиторы факторов инициации трансляции
Инициация трансляции в эукариотических клетках устроена сложнее, чем у бактерий: факторов инициации здесь больше, и многие из них являются эукариот-специфичными. Поэтому и набор мишеней для ингибиторов довольно разнообразен. Со всем многообразием факторов инициации и их набором у трех доменов живого удобно ознакомится в таблице 2.
* — IF3 бактерий не гомологичен a/eIF1, но очень похож на него по пространственной структуре.
** — Каталитические γ- и ε-субъединицы у архей отсутствуют, поэтому вопрос о наличии целостного aIF2B и даже об участии остальных субъединиц в трансляции неясен: на этот счет в научной литературе до сих пор ведутся споры.
Ингибиторы факторов элонгации
На данный момент известно большое количество ингибиторов фактора eEF2 (транслоказы), однако некоторые вещества действуют и на eEF1A, доставляющий аминоацил-тРНК. Бóльшая часть и тех, и других препятствует диссоциации факторов с рибосомы после гидролиза ГТФ, что блокирует цикл элонгации. Некоторые их этих ингибиторов (сордарин и его производные) обладают специфичностью к eEF2 грибов, но не связываются с фактором из человеческих клеток, что позволяет использовать их в качестве противогрибковых средств. Среди известных веществ из этой категории нельзя не упомянуть плитидепсин (аплидин), который, согласно работе, недавно опубликованной в журнале Science, показывает хорошие результаты в борьбе с вирусом SARS-CoV-2 [15].
Ингибиторы аминоацил-тРНК-синтетаз
Помимо рибосом и фактор-направленных ингибиторов, специфичное влияние на биосинтез белка могут оказывать вещества, блокирующие вспомогательные компоненты трансляционной машинерии — в первую очередь ингибиторы аминоацил-тРНК-синтетаз (АРСаз). Фундаментальной основой трансляции является генетический код (соответствие между триплетами нуклеотидов и аминокислотами). Осуществляют это соответствие не столько рибосома (хотя в ее функции, разумеется, входит контроль правильного декодирования триплетов — то есть соответствия тРНК кодону в мРНК), сколько АРСазы, навешивающие аминокислотный остаток на нужную тРНК. Из примерно 20 аминоацил-тРНК-синтетаз эукариот (точное их число может варьировать от вида к виду) специфичные ингибиторы известны как минимум для семи.
При ингибировании АРСаз в клетке уменьшается концентрация Аа-тРНК, и темпы трансляции снижаются. От этого сильнее всего страдают клетки с высокой интенсивностью белкового синтеза — к примеру, иммунные и раковые. Поэтому ингибиторы АРСаз имеют важное медицинское значение: они обладают иммуносупрессорным эффектом и применяются при лечении опухолей. Их также используют в качестве фунгицидов и антималярийных препаратов. Большинство ингибиторов этого типа высокоспецифичны по отношению к конкретным АРСазам, однако вещество пурпуромицин препятствует присоединению аминокислотного остатка к любой тРНК. На рисунке 1 ингибиторы АРСаз обозначены e.1.
Ингибиторы сигнальных путей, связанных с регуляцией трансляции
Существует несколько сигнальных путей, которые тонко регулируют трансляцию на разных уровнях. Эти пути образуют сложную сеть и на схеме отображены лишь частично. Ключевые регуляторные каскады, контролирующие эффективность трансляции в клетке, — это пути PI3K/AKT/mTOR и MAPK/ERK/Mnk, а также набор киназ α-субъединицы фактора eIF2. Ингибиторы mTOR представляют особую ценность из-за выраженных комплексных эффектов на организм, у них множество применений в медицине: к примеру, они используются при лечении рака или как иммуносупрессоры при трансплантациях органов. Самый известный пример лекарств последнего типа — это рапамицин (сиролимус), который ингибирует один из двух комплексов киназы mTOR (mTORC1). С этим лекарством, а также с другими ингибиторами mTOR связаны и надежды на замедление темпов старения: показано, что некоторые из этих веществ ощутимо продлевают период здоровой жизни у мышей [16]. На рисунке 1: s.1–s.9.
Немного о научной группе
Наша лаборатория расположена в отделе взаимодействия вирусов с клеткой НИИ физико-химической биологии имени А.Н. Белозерского МГУ. Основные направления исследований — изучение механизмов биосинтеза белка, молекулярная вирусология и анализ возрастных изменений в живых организмах на молекулярном и клеточном уровне. В отделе работают несколько научных сотрудников, аспирантов и множество студентов, руководитель отдела — к.б.н. Сергей Дмитриев. В исследованиях мы применяем широкий арсенал методов молекулярной биологии, генной инженерии, биохимии, системной биологии и биоинформатики. Со списком публикаций отдела можно ознакомиться на сайте МГУ.
Рисунок 6. Структуры из нашей лаборатории. А пока можете посмотреть на структуры белков, которыми занимается лаборатория и которые были получены нашими партнерами с помощью рентгеноструктурного анализа и криоэлектронной микроскопии. Также вы можете открыть полноэкранную версию апплета.
Читайте также:

