Фкр по ведению детей с острой респираторной инфекцией острым назофарингитом
Обновлено: 26.04.2024
Э.Б. Белан
Волгоградский государственный медицинский университет, Волгоград, Россия
Острый и хронический назофарингит – одна из наиболее частых причин обращения за медицинской помощью. К основным этиологическим факторам обеих форм заболевания относятся респираторные вирусы, хотя могут также иметь значение представители семейства Herpesviridae, микоплазменные, хламидийные, бактериальные возбудители. В статье приводятся данные о современных подходах к диагностике и лечению назофарингита.
Введение
По данным ВОЗ, заболевания органов дыхания – одна из наиболее часто встречающихся форм патологии, занимая до 60% в структуре заболеваемости населения планеты [1]. Слизистая оболочка носоглотки, непосредственно контактирующая с разнообразными объектами окружающей среды, является одним из самых уязвимых мест как для инфекционного, так и для неинфекционного поражения.
По характеру течения выделяют две основные формы заболевания: острую и хроническую. Классификация назофарингита по степени тяжести возможна в зависимости от уровня температуры и степени выраженности общих неспецифических симптомов.
Острый назофарингит
Острый назофарингит (ОНФ; J00 по МКБ-10) у детей представляет одну из форм острой респираторной вирусной инфекции (ОРВИ) [2]. К настоящему времени описано более 200 вирусов – возбудителей ОРВИ [3]. Наиболее частые причины заболевания – это риновирусы, менее частые – корона-, адено-, миксо- и парамиксовирусы. Относительно редко у взрослых (у детей значительно чаще) возбудителями ОРВИ становятся респираторно-синцитиальный вирус (РСВ), вирусы Коксаки и ECHO, представители семейства Herpesviridae [4]. На рисунке приведена частота выделения различных респираторных вирусов при ОРВИ у детей [6].
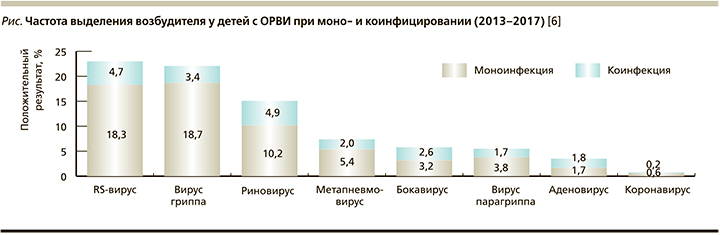
ОНФ (насморк) ежегодно поражает практически каждого жителя России независимо от возраста [3]. Это связано как с высокой контагиозностью возбудителей, так и с разнообразностью их видового состава (вирусы парагриппа, гриппа, адено-, рино-, энтеровирусы и т.д.). Особую проблему представляет непрерывное новое штаммо- и видообразование, обусловленное генетической лабильностью многих возбудителей [3]. Способствовать хронизации процесса, затяжному и/или осложненному течению ОНФ могут представители семейства Herpesviridae [4]. Одновременное коинфицирование несколькими возбудителями приводит к более тяжелому течению ОНФ (см. рисунок).
Несмотря на то, что в качестве приоритетных возбудителей назофарингитов рассматриваются различные вирусные агенты, бактериальная флора может быть первичной причиной заболевания, а также осложнять течение вирусной инфекции. В качестве наиболее частых бактериальных агентов – возбудителей назофарингитов рассматриваются Streptococcus pneumoniae, Streptococcus pyogenes, Haemophilus influenzaе и Moraxella catarrhalis [4].
У детей раннего возраста стрептококковый ОНФ ассоциируется с высокой лихорадкой, интоксикацией, выраженной ринореей, шейным лимфаденитом [7]. Бактериальные осложнения при попадании инородного тела могут быть также вызваны микроорганизмами Prevotella, Fusobacterium, Peptostreptococcus, с активностью которых связаны менее выраженные симптомы [7].
Инкубационный период большинства ОРВИ составляет 2–7 дней. Максимальное выделение вируса происходит на 3-и сутки после заражения (этот период характеризуется и наиболее выраженными симптомами), резко снижается к 5-му дню заболевания (появление вирусспецифических IgM), хотя у некоторых больных его неинтенсивное выделение может сохраняться в течение 2 недель (до достижения титра вирусспецифических IgG, достаточного для элиминации возбудителя) [2].
Ведущим симптомокомплексом при ОРВИ является катаральное воспаление дыхательных путей. При этом развитие симптомов – не столько следствие повреждающего действия возбудителя на эпителиальные клетки, сколько результат их десквамации и реакции иммунной системы, прежде всего факторов врожденного иммунитета. Синтез провоспалительных цитокинов (интерлейкины-1, -6, -8 и др.) ответствен за развитие пирогенной реакции при инфекционных болезнях, индукцию системной и локальной воспалительной реакции, при этом показана прямая связь между уровнем секретируемых цитокинов и тяжестью симптомов [9]. Увеличение назальной секреции при ОРВИ связано с повышением проницаемости сосудов и гиперсекрецией слизи, а помутнение назального секрета и возможное появление ее желтоватого или зеленоватого оттенка – с миграцией активированных лейкоцитов в очаг реакции. Данные симптомы не обязательно свидетельствуют о присоединении бактериальной флоры и необходимости назначения антибиотиков [2]. Несмотря на участие иммунных механизмов в развитии клинических симптомов ОРВИ, их следует рассматривать в качестве патогенетического, но не патогенного фактора и стремиться обеспечить нормальное функционирование иммунной системы при заболевании.
Несмотря на сходство клинических проявлений ОРВИ различной этиологии, существуют особенности клинического течения гриппа, РСВ-инфекции и др. Начало заболевания острое или подострое, при гриппе – с резким внезапным ухудшением состояния; лихорадка при гриппе и аденовирусной инфекции высокая, длительная, при РСВ-инфекции может отсутствовать вообще; симптомы интоксикации в наибольшей степени выражены при гриппе, несколько менее – при адено- и РСВ-инфекции, при наиболее частой – риновирусной – могут отсутствовать вообще; напротив, назальные симптомы максимально выражены в последнем случае, а также при аденовирусной этиологии заболевания; при гриппе, парагриппе и РСВ-инфекции доминирует сухой кашель (с бронхообструктивным компонентом или без него); лимфаденит характерен только для ОРВИ аденовирусной этиологии [10].
Основной причиной хронического ринофарингита (ХНФ), как и ОНФ, служат респираторные вирусы, однако местная иммунокомпрометация, лежащая в основе хронизации процесса, способствует более частой активации оппортунистических инфекций и/или присоединению бактериальной флоры.
Несмотря на то что представители семейства Herpersviridae рассматриваются как редкие возбудители ринофарингитов, по нашим данным [5], у 121 из 352 детей дошкольного возраста с рецидивирующими симптомами ринофарингита диагностировано моноинфицирование цитомегаловирусом (64/121; 52,9%), вирусом Эпштейна–Барр (38/121; 31,4%), вирусом простого герпеса (10/121; 12,0%) и вирусом герпеса 6-го типа (5/121; 4,1%) с наличием IgG к данным возбудителям, у 14 из 352 детей определены маркеры ≥2 герпесвирусных инфекций.
Хронический назофарингит (ХНФ)
Клиника ХНФ обычно характеризуется катаральными явлениями в носоглотке, сопровождающимися заложенностью носа, ринореей, длительным сухим непродуктивным кашлем, дискомфортом или болью в горле, при отсутствии или минимальных системных симптомах.
Диагностика
Диагностика ОРВИ базируется на клинико-эпидемиологических данных, результатах инструментального и лабораторного обследования [2, 12, 13]. Целью лабораторного обследования при ОРВИ стал поиск у детей бактериальных очагов, не определяемых клиническими методами, в т.ч. при ухудшении течения коморбидной патологии при ее наличии.
Клинический анализ крови у взрослых относится к обязательным методам исследования при ОРВИ (типичны нормоцитоз и ускорение СОЭ), для детей он целесообразен только при выраженных общих симптомах с лихорадкой [2, 12, 13].
Клинический анализ мочи (при неосложненном течении ОРВИ в нем не должно быть изменений) у взрослых остается обязательным методом исследования, детям его рекомендуется проводить при наличии лихорадки без катаральных явлений [2, 12, 13].
Определение уровня С-реактивного белка рекомендовано для исключения тяжелой бактериальной инфекции у детей с фебрильной лихорадкой (повышение температуры выше 38°С), особенно в отсутствие видимого очага инфекции (вероятность – 85% при уровне С-реактивного белка >30–40 мг/л) [2].
Плановых вирусологического и бактериологического исследований в настоящее время не рекомендуется, исключение составляют экспресс-тест на грипп у пациентов с высокой лихорадкой и экспресс-тест на стрептококк при подозрении на острый стрептококковый тонзиллит. Микробиологическое исследование показано при неэффективности антибактериальной терапии первой или даже второй линии, назначаемой эмпирически. При вовлечении пазух в патологический процесс идеальным материалом для исследования служит аспират или промывные воды из полости синуса; мазок из среднего носового хода или носоглотки в таких случаях не всегда обеспечивает достоверную информацию [14, 15].
Инструментальные исследования (рентгенография органов грудной клетки при подозрении на пневмонию, рентгенография придаточных пазух носа при подозрении на развитие синусита; ЭКГ при наличии кардиальных симптомов) при неосложненном течении ОРВИ не проводятся. Детям с симптомами ОРФ не рекомендуется проводить рентгенографию пазух носа в первые 12 дней болезни.
Консультация врача-оториноларинголога и отоскопия рекомендованы детям во всех случаях ОРВИ. При тяжелом/среднетяжелом течении болезни или отказе от госпитализации рекомендована консультация врача-инфекциониста. Напротив, при ХРФ помимо клинико-анамнестических и объективных данных обследования показан посев мазка из носоглотки для определения этиологически значимой микрофлоры (бактериальной, грибковой) или определение в мазке ДНК представителей семейства Herpesviridae (вирус простого герпеса, вирус герпеса 6-го типа, цитомегаловирус, вирус Эпштейна–Барр) [3].
Оценки иммунного статуса у больных ринофарингитом, как правило, не требуется, однако консультация аллерголога-иммунолога целесообразна, поскольку не менее чем у половины детей с ХНФ диагностируется аллергический ринит [5].
Важно подчеркнуть, что ринофарингит – одна из частых причин полипрагмазии, избыточного назначения диагностических и лечебных процедур, использования лекарственных средств с недоказанной эффективностью или не по показаниям [2, 16, 17].
Лечение
Основу лечения ОНФ составляет симптоматическая и элиминационная терапия в целях разжижения секрета, удаления слизи, восстановления проходимости носовых ходов, в т.ч. с помощью деконгестантов (до 12 лет только топических).
К сожалению, возможности противовирусной терапии ОРВИ в настоящее время ограничены. Специфическая этиотропная терапия (занамивир, озельтамивир) доступна и абсолютно оправданна только при гриппе и должна назначаться в максимально ранние сроки; на другие вирусы ингибиторы нейраминидазы не действуют.
В остальных случаях не позднее 1–2-го дня болезни можно рассмотреть целесообразность назначения препаратов группы интерферонов-α (назальные формы, ректальные суппозитории) или интерфероногенов, хотя надежных доказательных данных в отношении их эффективности нет [2, 11].
Антибактериальные препараты в лечении ринофарингитов, как правило, не используются. Если заболевание имеет вирусную этиологию, антибиотики могут быть показаны только в случае наличия иммунодефицита с риском развития бактериального процесса, а также при хронической патологии легких. При доказанной роли бактериальной флоры могут быть также использованы топические формы антибактериальных препаратов, D3, фитопрепаратов, гомеопатических средств и т.д., относящихся к категории средств с недоказанной эффективностью.
Литература
3. Свистушкин В.М., Мустафаев Д.М. Острые респираторные вирусные инфекции: принципы рациональной терапии. РМЖ. 2014;26:1897–1902.
4. Gostry A.V., Simonova A.V., Mikhailova N.A. Chronic pharyngitis: etiology, pathogenesis, treatment. Mew approaches to the estimation of etiopathogenesis. The Russian archives of internal medicine. 2019;9(1):32–43.
5. Белан Э.Б., Садчикова Т.Л., Панина А.А., и др. Оптимизация терапии рецидивирующего ринофарингита, ассоциированного с цитомегаловиусом или вирусом Эпштейна–Барр у детей. Фарматека. 2015;14(307):63–6.
6. Kurskaya O., Ryabichenko T., Leonova N., et al. Viral etiology of acute respiratory infections in hospitalized children in Novosibirsk City, Russia (2013–2017). PLoS ONE. 2018;13(9):e0200117. Doi: 10.1371/journal.pone.0200117.
7. Mc Gann K.A., Long S.S. Respiratory Tract Symptom Complexes In book: Principles and Practice of Pediatric Infectious Diseases. 2018. Р. 164–72.
8. Снимщикова И.А., Агафонов Б.В., Гострый А.В. Клинико-диагностическое значение метода масс-спекирометрии микробных маркеров при рецидивирубщем течении хронического фарингита. Лечащий врач. 2018;7:58–62.
9. Lund V.J., Grouin J.M., Ecceis R., Bouter .C, Chabolle F.Efficacy of fusafungine in acyte rhinopharingitis: A pooled analysis. Rhinology. 2004;43:207–12.
10. Зайцев А.А. Фармакотерапия острых респираторных вирусных инфекций. Терапевтический архив. 2013;3:102–6.
11. Баранов А.А., Лобзин Ю.В. Федеральные клинические рекомендации по оказанию медицинской помощи детям с острой респираторной вирусной инфекцией (острый ринофарингит). М., 2015.
12. Cocularda S.A.Y., Ozlem N.A.S., Figen G. Approach to common cold in children. J Pediatr Res. 2015;2(1):1–6.
13. Грипп и острые респираторные инфекции: современная рациональная этиотропная терапия. Алгоритмы оказания медицинской помощи больным. Методические рекомендации
14. Thomas M., Yawn B.P., Price D., et al. EPOS primary care guidelines: European position paper on the primary care diagnosis and management of rhinosinusitis and nasal polyps 2007 – a summary. Prim Care Respir J. 2008;17(2):79–89. Doi: 10.3132/pcrj.2008.00029.
15. Chow A.W., Benninger M.S., Brook I., et al. IDSA Clinical Practice Guideline for Acute Bacterial Rhinosinusitis in Children and Adults. Clin Infect Dis. 2012;54(8):72–112. Doi: 10.1093/cid/cir1043.
16. Pessey J.J., Mégas F., Arnould B., Baron-Papillon F. Prevention of Recurrent Rhinopharyngitis in At-Risk Children in France A Cost-Effectiveness Model for a Nonspecific Immunostimulating Bacterial Extract (OM-85 BV) Pharmacoeconomics. 2003;21(14):1053–68. Doi: 10.2165/00019053-200321140-00005.
17. Trichard M., Chaufferin G., Nicoloyannis N. Pharmacoeconomic comparison between homeopathic and antibiotic treatment strategies in recurrent acute rhinopharyngitis in children. Homeopathy.2005;94(1):3–9. Doi:10.1016/j.homp.2004.11.021.
Об авторах / Для корреспонденции
Авторы: Каннер Е.В. 1 , Усенко Д.В. 1 , Максимов М.Л. 2, 3, 4 , Горелова Е.А.
1 ФБУН ЦНИИ Эпидемиологии Роспотребнадзора, Москва, Россия
2 ФГБОУ ДПО РМАНПО Минздрава России, Москва, Россия
3 КГМА — филиал ФГБОУ ДПО РМАНПО Минздрава России, Казань, Россия
4 РНИМУ им. Н.И. Пирогова Минздрава России, Москва
Для цитирования: Каннер Е.В., Усенко Д.В., Максимов М.Л., Горелова Е.А. Современные подходы к терапии острого ринофарингита у детей. РМЖ. 2014;21:1541.
Острые респираторные вирусные инфекции (ОРВИ) по-прежнему остаются ощутимой медицинской и социально-экономической проблемой. ОРВИ составляют около 90% всей инфекционной патологии [1]. При ежегодных сезонных эпидемических подъемах заболеваемости ОРВИ страдают более 10% населения [2]. По данным ВОЗ, взрослый человек переносит ОРВИ дважды в год. Временная нетрудоспособность взрослого населения вследствие ОРВИ в России ежегодно составляет 25–30% от общей временной нетрудоспособности, что обусловливает существенный экономический ущерб. Кроме того, респираторные вирусы снижают функциональную активность иммунной системы, что приводит к тяжелому клиническому течению заболеваний и присоединению различных бактериальных осложнений.
Наибольшая заболеваемость острыми респираторными инфекциями встречается у детей раннего возраста, дошкольников и младших школьников. Максимум заболеваемости традиционно приходится на осенне-зимний период и начало весны.
К факторам, влияющим на повышенную частоту заболеваемости ОРВИ у детей, следует относить: анатомо-физиологические особенности респираторного тракта (узкие просветы дыхательных путей, недостаточное развитие эластической ткани и др.), запаздывание созревания иммунной системы, условия жизни (питание, бытовые условия) и др. Особо следует отметить пассивное курение, приводящее к снижению местного иммунитета слизистых респираторного тракта и повышению аллергизации организма. Одним из важных факторов, влияющих на частоту простудных заболеваний, является проживание в экологически неблагоприятных районах. Повышение содержания различных ксенобиотиков в воздухе, воде, продуктах питания сопровождается их накоплением в организме, что приводит к изменениям клеточного метаболизма, нарушениям гомеостаза и иммунной защиты [3].
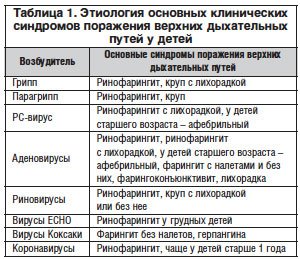
Основные возбудители острых инфекций верхних отделов респираторного тракта – вирусы. Одним из самых актуальных является риновирус. Он – причина по крайней мере 25–40% всех ОРЗ. Наряду с риновирусами причинами острых респираторных заболеваний (ОРЗ) являются аденовирусы, вирусы парагриппа, респираторно-синцитиальный (РС) вирус, а в период эпидемических вспышек – вирусы гриппа. В последние годы значительное внимание уделяют метапневмовирусам – наиболее частой причине ОРЗ у детей первого года жизни; бокавирусам человека, которые чаще поражают детей на 2–3-м году жизни [4]. В таблице 1 [В.К. Таточенко, 1987] приведены основные синдромы поражения верхних дыхательных путей в зависимости от вирусов, вызывающих заболевания респираторного тракта.
Одно из проявлений ОРВИ – острый инфекционный ринофарингит (изолированный острый инфекционный ринит у детей встречается крайне редко).
Методы лабораторной диагностики играют решающую роль при наблюдении заболевшего ребенка только в случаях тяжелого или осложненного течения ринофарингита, когда ребенка помещают в стационар [5]. Среди них выделяют методы идентификации возбудителя (антигена) и выявления нарастания титра специфических антител в динамике заболевания. В последние годы наиболее достоверным методом идентификации возбудителя является метод полимеразной цепной реакции [6, 7]. Он позволяет идентифицировать большинство вирусов, а также микоплазмы, хламидии и ряд других бактерий. Метод иммунофлюоресценции – универсальный метод, сочетающий точный морфологический анализ с высокой специфичностью и разрешающей способностью [6, 7]. Он прост в выполнении, высокочувствителен и позволяет получить положительный результат через несколько часов от начала исследования в отношении любого антигенного вещества вирусной, бактериальной или другой природы.
Инкубационный период при остром ринофарингите составляет обычно от 1 до 4 дней. Часто первыми симптомами ринофарингита являются першение и боли в горле. Глотка богата нервными рецепторами, т. к. получает чувствительную, двигательную и вегетативную иннервацию из глоточного сплетения. Это сплетение, расположенное на наружной поверхности среднего сфинктера под щечно-глоточной фасцией, формируется за счет ветвей языкоглоточного и блуждающего нервов, а также симпатических волокон верхнего шейного ганглия. Чувствительная иннервация глотки в основном осуществляется языкоглоточным нервом, однако в области глоточных устьев слуховых труб имеются нервные связи со второй ветвью тройничного нерва. В иннервации гортаноглотки также принимает участие верхний гортанный нерв – ветвь блуждающего нерва. Богатство нервных связей объясняет иррадиацию боли при заболеваниях глотки в ухо, нижнюю челюсть и т. д.
Для первых часов клинической картины характерны: заложенность носа, нарушения носового дыхания; затем появляются ринорея и чиханье. Может появиться ночной кашель (обычно в начале ночи), который возникает за счет стекания слизи по задней стенке глотки (так называемый drip-синдром). Другими частыми симптомами являются гиперемия и отечность слизистой зева в области задней стенки глотки, некоторая болезненность при глотании, что иногда вызывает отказ ребенка от еды и даже позывы на рвоту. Ринофарингит может сопровождаться лихорадочной реакцией. Отмечаются общее недомогание и кашель за счет раздражения и сухости слизистой оболочки глотки при дыхании через рот [7].
У детей первого года жизни острый ринофарингит может протекать достаточно тяжело вследствие узости носовых ходов и малого вертикального размера носовой полости. Это вызывает выраженное нарушение носового дыхания, одышку, беспокойство, отказ от сосания, срыгивания, что может привести к развитию аспирации [7]. Дети грудного возраста становятся беспокойными, капризными, у них нарушается сон, ухудшается аппетит.
Средняя продолжительность заболевания в неосложненных случаях – 5–10 сут. Обычно на 3–5-й день отделяемое из носа становится слизисто-гнойным, носовое дыхание улучшается, постепенно уменьшаются выделения из носа, и наступает выздоровление.
При микоплазменной и хламидийной этиологии заболевание имеет тенденцию к затяжному течению – свыше 2 нед., нередко сопровождается развитием трахеита и/или бронхита.
Осложнением ринофарингита является присоединение бактериальной инфекции, обычно вызванной микрофлорой, колонизирующей верхние дыхательные пути ребенка, с развитием синуситов, бронхита, острого среднего отита, пневмонии. Это отмечается у ослабленных и иммунокомпрометированных детей. Другое осложнение ринофарингита – обострение хронической легочной патологии: декомпенсация бронхолегочной дисплазии, обострение хронического бронхита, бронхиальной астмы и др. [7].
Обычно дифференциальная диагностика острого ринофарингита требуется только при его затяжном течении, когда необходимо исключить неинфекционную природу заболевания: аллергический и вазомоторный риниты, поллиноз, инородное тело в полости носа, а также (крайне редко) дифтерию носа. При этом основное значение имеют сбор анамнеза и осмотр ЛОР-врачаом, в т. ч. эндоскопия полости носа, рентгенограмма носа, а иногда и носоглотки (фиброскопия), ультразвуковое сканирование [7].
Ребенок до определенного возраста может не предъявлять конкретных жалоб, поэтому в первую очередь учитываются объективные проявления: изменение окраски слизистой оболочки ротоглотки, отказ от плотной пищи или появление капризности при ее приеме.
В отличие от сосудосуживающих капель Протаргол борется с причиной инфекционно-воспалительного процесса ЛОР-органов, подавляет жизнедеятельность возбудителей инфекции и уменьшает воспалительный процесс. Сосудосуживающее действие у Протаргола мягкое, осложнений со стороны кровеносных сосудов не возникает, поэтому его можно применять в течение длительного времени.
В отличие от других эффективных антибактериальных химиотерапевтических препаратов Протаргол обладает не только противомикробным, но и противовирусным и иммуностимулирующим свойствами. В результате исследования раствора Протаргола в различных концентрациях на культуре клеток отмечено угнетение репродукции вирусов, вызывающих инфекционный ринотрахеит и вирусную диарею, при концентрации 0,25–0,5% [14].
При остром насморке детям младше 6 лет Протаргол закапывают по 1–2 капли 3 р./сут, взрослым и детям старше 6 лет – по 2–3 капли 3 р./сут. Взрослые и дети старше 6 лет также могут использовать спрей (по 1 впрыску 3 р./сут). Обычно бывает достаточно недельного курса лечения Протарголом, но при хроническом насморке препарат назначают курсами по 14 и более дней. В этом случае он мягко воздействует на кровеносные сосуды полости носа, суживает их, что уменьшает поступление к слизистой оболочке крови. Отсутствие дополнительного питания способствует тому, что разрастание слизистой оболочки уменьшается или останавливается.
Протаргол оказывает бактериостатический и бактерицидный эффекты на штаммы, вызывающие ОРЗ, такие как Staphylococcus spp., Streptococcus spp., Moraxella spp. и др.
Таким образом, использование Протаргола, обладающего активным антисептическим и противовоспалительным действием, способствует раннему выздоровлению и предупреждению осложнений острого ринита. Многолетний опыт клинического применения Протаргола свидетельствует о его хорошей эффективности и высоком профиле безопасности в лечении детей с острым ринитом в любой его фазе.

Литература
1. Об усилении мероприятий по профилактике гриппа и других острых респираторных вирусных инфекций. Приказ МЗ РФ № 25 от 27.01.1998 г.
2. Ратникова Л.И., Стенько Е.А. Новый подход к терапии острых респираторных вирусных инфекций и гриппа // Поликлиника. 2009. № 2. С. 70–72.
3. Ключников С. О. Лечение кашля при ОРВИ у часто болеющих детей // РМЖ. 2012. № 2 (Педиатрия). С. 68–72.
4. Козулина И.С. Новые инфекционные агенты – метапневмовирус и бокавирус человека: Автореф. дис. . канд. мед. наук. М., 2010.
5. Острые респираторные заболевания у детей: лечение и профилактика. Научно-практическая программа Союза педиатров России. М.: Международный фонд охраны здоровья матери и ребенка, 2002.
6. Ключников С.О., Зайцева О.В., Османов И.М. и др. Острые респираторные заболевания у детей. Пособие для врачей // Рос. вестн. перинатологии и педиатрии. 2008. № 3. С. 1–36.
7. Самсыгина Г.А., Богомильский М.Р. Инфекции верхних дыхательных путей. Педиатрия. Национальное руководство. Т. 2. М.: ГЭОТАР-Медиа, 2009. С. 56–62.
8. Battist N. The evaluation of the analgesic and antiinflammatory effects of flurbiprofen mouth wash and 100 mg tablets in oral medicine // Minerva Stomatol. 1994. Vol. 43. № 4. Р. 141–144.
9. Benzimoj S.I., Langford J.H., Homan H.D. et al. Efficacy and safety of the anti-inflammatory throat lozenge flurbiprofen 8.75 mg in the treatment of sore throat // Fundament. Clin. Pharmacol. 1999. Vol. 13. Р. 189.
10. Benzimoj S.I., Langford J.H., Christian J. et al. Efficacy and tolerability of the anti-inflammatory throat lozenge Flurbiprofen 8.75 mg in the treatment of sore throat // Clin. Drug Invest. 2001. Vol. 21. № 3. Р. 183–193.
11. Ключников С.О., Зайцева О.В., Османов И.М., Крапивкин А.И., Кешишян Е.С., Блинова О.В., Быстрова О.В. Острые респираторные заболевания у детей. Пособие для врачей // Российский вестник перинатологии и педиатрии. 2008. № 3. С. 1–36.
12. Лопатин А.С., Овчинников А.Ю., Свистушкин В.М., Никифорова Г.Н. Топические препараты для лечения острого и хронического ринита // Русский медицинский журнал. 2003. Т. 11. № 8. С. 446–448.
13. Гаращенко Т. И. Современная терапия аллергических ринитов у детей // Русский медицинский журнал. 2002. Т. 10. № 5. С. 273–278.
14. Красочко П.А. Применение Т-активина и протаргола для лечения респираторных болезней телят / П.А. Красочко, Т.И. Помирко, П.И. Яровой // Ветеринария. 1990. № 11. С. 22–23.
Острые респираторные инфекции (ОРИ) по-прежнему занимают лидирующие позиции в структуре инфекционной патологии детского возраста. Основным этиологическим фактором ОРИ являются вирусы. Клинические симптомы ОРИ во многом схожи: повышение температуры тела, головная боль, гиперемия зева, насморк, кашель, конъюнктивит, увеличение регионарных лимфоузлов. Лечение пациентов с ОРИ должно быть комплексным и включать, при необходимости, противовирусные препараты. Идентификация конкретного вируса в настоящее время не является стандартной процедурой в повседневной клинической практике. Отдельные симптомы ОРИ могут быть выражены значительно, что требует назначения лекарственных препаратов. Лечение ОРВИ должно быть комплексным и включать: противовирусные этиотропные препараты; патогенетическую терапию; симптоматическую терапию; средства, усиливающие противовирусный и антибактериальный иммунный ответ; в случае развития бактериальных осложнений — антибактериальные средства. Поскольку ОРИ широко распространены и приводят к потере работоспособности, они относятся к социально значимым заболеваниям, требующим мер, обеспечивающих скорейшее выздоровление. Поэтому лекарственные средства, помогающие восстановить здоровье и работоспособность при ОРИ, приобретают соответствующую значимость. Однако в детском возрасте не все противовирусные препараты разрешены к применению, в частности, из-за возможного токсического действия. В этом случае целесообразно использовать препарат рекомбинантного интерферона альфа-2b в сочетании с высокоактивными антиоксидантами витаминами Е и С, клиническая эффективность и безопасность которого доказаны в многочисленных исследованиях.
Ключевые слова: острые респираторные инфекции, вирусы, дети, рекомбинантный интерферон альфа-2b.
Для цитирования: Николаева С.В., Хлыповка Ю.Н., Горелов А.В. Острые респираторные инфекции у детей: оптимизация тактики терапии. РМЖ. 2019;10:42-45.
Acute respiratory infections in children: optimizing treatment strategy
S.V. Nikolaeva 1 , Yu.N. Khlypovka 1,2 , A.V. Gorelov 2,3
1 Central Research Institute of Epidemiology of the Russian Federal Service for Supervision of Consumer Rights Protection and Human Well-Being, Moscow
2 Central Clinical Hospital and Polyclinic, Moscow
3 Sechenov University, Moscow
Acute respiratory infections (ARIs) still rank first among infectious diseases in children. Viruses are the most common causative agents of ARIs. Clinical symptoms of ARIs are similar, i.e., fever, headache, hyperemic pharynx, rhinitis, cough, conjunctivitis, and enlarged regional lymph nodes. Treatment for ARIs should be complex and include, if needed, antivirals. Current-ly, identification of a specific virus is not a standard procedure in routine clinical practice. Some symptoms of ARIs can be significant thus requiring additional drugs. Treatment for ARIs should include antivirals (etiological therapy), pathogenic and symptomatic therapy, medications to boost antiviral and antibacterial immune response, and antibiotics (if bacterial complications occur). Considering that ARIs are common disorders, drugs which reduce ARI duration and time to recover working capacity are socially important. However, not all antivirals can be used in children due to their potential toxicity. In these cases, recombinant interferon alfa-2b in combination with highly active antioxidants vitamins E and C is recommended. Numerous studies have demonstrated clinical efficacy and safety of this agent.
Keywords: acute respiratory infections, viruses, children, recombinant interferon alfa-2b.
For citation: Nikolaeva S.V., Khlypovka Yu.N., Gorelov A.V. Acute respiratory infections in children: optimizing treatment strategy. RMJ. 2019;10:42–45.
Статья посвящена вопросам оптимизации тактики терапии острых респираторных инфекций у детей
Актуальность
Основным этиологическим фактором ОРИ являются вирусы, немаловажную роль среди которых играют вирусы гриппа, риновирусы, респираторный синцитиальный вирус, аденовирусы, метапневмовирусы, коронавирусы, бокавирусы, а также вирусы парагриппа. Вирусы обладают выраженным тропизмом к эпителию слизистой оболочки дыхательных путей, что обусловливает высокую заболеваемость и быстрое распространение ОРИ. По нашим данным, на долю вирусных ОРИ в 2018–2019 гг. пришлось 87,5% всех случаев поражения дыхательных путей у детей. Доминирующим агентом являлся риновирус (в 14,8% случаев), бокавирус служил причиной ОРИ в 2% случаев, респираторно-синцитиальный вирус — в 9,1%. Грипп занимал одно из ведущих мест в этиологической структуре заболевших детей, его выявляли в 9,4% случаев. У 7,8% детей ОРИ имели сочетанный характер, при этом отмечались вирусно-вирусные и вирусно-бактериальные ассоциации (рис. 1).

В среднем дети переносят от 5 до 8 эпизодов ОРИ в год, большей частью — в легкой форме. Высокую частоту ОРИ можно объяснить значительным разнообразием возбудителей и высокой контагиозностью респираторных вирусов [2]. Помимо этого существует сложность идентификации возбудителей и способность микроорганизмов формировать устойчивость к лекарственным средствам. Все это способствует тому, что ОРИ вирусной этиологии часто носят массовый характер.
Особенности клиники ОРИ в зависимости от этиологии
Клинические симптомы ОРИ во многом схожи: повышение температуры, головная боль, гиперемия зева, насморк, кашель, конъюнктивит, увеличение регионарных лимфоузлов. Вместе с тем имеются некоторые особенности клинических проявлений, т. к. каждая группа респираторных вирусов имеет свои отличительные характеристики из-за преимущественной локализации поражения респираторного тракта (табл. 1). Так, при гриппе происходит поражение эпителия верхних (задняя стенка глотки), нижних (трахеобронхит) дыхательных путей, а также паренхимы легких (пневмония). При аденовирусной инфекции часто развиваются конъюнктивит, полиаденит, возможна гепатомегалия. При парагриппе у детей первых лет жизни чаще отмечается развитие обструктивного ларингита. Риновирус поражает эпителиальный покров носа с развитием ринита; в последние годы рассматривается связь перенесенной риновирусной инфекции с последующим развитием бронхиальной астмы. При респираторно-синцитиальной инфекции чаще развиваются бронхообструкция и бронхиолит [3, 4].
![Таблица 1. Основные клинические синдромы при гриппе и ОРВИ [5]](https://www.rmj.ru/upload/medialibrary/9df/42-2.jpg)
Идентификация конкретного вируса в настоящее время не является стандартной процедурой в повседневной клинической практике, и предположить, какова этиология этих инфекций, можно, учитывая сезон их возникновения, жалобы пациентов и данные физикального осмотра. Отдельные симптомы ОРИ могут быть выражены значительно, что требует применения лекарственных препаратов. Лечение ОРВИ должно быть комплексным и включать: противовирусные этиотропные препараты; патогенетическую терапию; симптоматическую терапию; средства, усиливающие противовирусный и антибактериальный иммунный ответ; в случае развития бактериальных осложнений — антибактериальные средства. В лечении ОРИ и гриппа используют широкий спектр противовирусных средств: 1) этиотропные препараты; 2) препараты интерферона; 3) индукторы интерферона; 4) гомеопатические препараты. Поскольку ОРИ — это широко распространенные заболевания с ежегодным охватом миллионов людей, любое лекарственное средство, ускоряющее выздоровление и восстановление работоспособности, чрезвычайно важно и приобретает социально значимый эффект.
Терапевтические возможности при ОРИ
В детском возрасте применение большинства противовирусных препаратов ограничено из-за их узкой специфичности, возможности вызывать побочные реакции, токсичности, возрастных ограничений. В этом случае у детей с ОРИ целесообразно применять лекарственные средства, не имеющие известных побочных действий, с доказанной эффективностью их применения у детей, в т. ч. детей раннего возраста. Таким препаратом, например, является рекомбинантный интерферон альфа-2b в сочетании с высокоактивными антиоксидантами витаминами Е и С (Виферон), успешное применение которого при гриппе и других ОРИ у детей доказано лечебной практикой. Препарат представлен в следующих лекарственных формах: свечи ректальные, мазь и гель для интраназального применения.
Одним из первых исследований по изучению эффективности препарата интерферона альфа-2b с антиоксидантами витаминами Е и С у детей при лечении ОРИ и гриппа было открытое сравнительное контролируемое рандомизированное исследование [6], проведенное в параллельных группах с участием 100 детей в возрасте от 4 мес. до 17 лет, госпитализированных в стационар по поводу ОРИ или гриппа. В группе детей, получавших препарат, наблюдались нормализация температуры тела, купирование интоксикации, исчезновение катаральных явлений и респираторного синдрома в среднем на 2 дня быстрее, чем в контрольной группе. Изучение показателей интерферонового статуса выявило способность препарата интерферона альфа-2b стимулировать активность иммунокомпетентных клеток к продукции α-ИФН и γ-ИФН и снижать уровень провоспалительных цитокинов (ИЛ-1β, ИЛ-8 и ФНО-α). Кроме того, на фоне приема препарата у большинства детей происходило восстановление исходно низкого в начале заболевания содержания sIgA в носовом секрете и сыворотке крови, а также статистически значимое снижение количества IgE в крови к моменту выздоровления (с 48,5±6,2 до 31,2±4,7 КЕ/л). Внутрибольничное инфицирование среди детей, получавших препарат, развивалось в среднем в 2 раза реже, чем в контрольной группе.
Эффективность различной противовирусной терапии (интерферон альфа-2b в суппозиториях ректальных и осельтамивир) изучали у 57 госпитализированных детей в возрасте от 6 мес. до 13 лет с гриппом и ОРИ в период пандемии 2009–2010 гг. [7]. Благодаря всасыванию через обильно кровоснабжаемую прямую кишку ректальные суппозитории оказывают быстрое действие, не перегружая желудок и печень. В первые сутки пребывания в стационаре дети были обследованы методом ПЦР на наличие вируса гриппа А/H1N1/sw, при этом данный вирус был выявлен у 28 (49,1%) детей. При анализе динамики клинических симптомов, вне зависимости от нозологической формы заболевания у детей, получавших препарат интерферона альфа-2b, была отмечена тенденция к уменьшению длительности кашля по сравнению с детьми, принимавшими осельтамивир (3,5±0,7 и 4,3±2,0 дня соответственно). Таким образом, применение рекомбинантного интерферона альфа-2b в терапии ОРИ и пандемического гриппа А/H1N1/sw эффективно, особенно у детей раннего возраста, что очень актуально в условиях возрастных ограничений многих противовирусных препаратов и в сезон массовой заболеваемости ОРИ и гриппом.
Еще в одном исследовании по изучению эффективности препарата интерферона альфа-2b в сочетании с витаминами Е и С приняли участие 277 детей [8], которых разделили на 3 группы по возрасту: I — от 1 года до 3 лет, II —
от 4 до 7 лет, III — от 8 до 14 лет. В каждой возрастной группе выделили 2 подгруппы. В основной подгруппе больные получали препарат интерферона альфа-2b в суппозиториях ректальных, в контрольной подгруппе — плацебо. Включение в терапию препарата оказывало положительное влияние на интерфероновый статус, корректировало пролиферацию цитотоксических клеток и естественных киллеров, способствовало повышению числа активированных Т-лимфоцитов и фагоцитов, а также усилению продукции IgA. Анализ интегрированных показателей выздоровления (балльный метод) показал, что у больных детей, получавших препарат интерферона альфа-2b в сочетании с антиоксидантным комплексом (витаминами Е и С), отмечалось более быстрое выздоровление.
При лечении ОРИ и гриппа целесообразно использование не только ректальных суппозиториев интерферона альфа-2b, но и местных лекарственных форм этого препарата (мазь, гель). И.Н. Захарова и соавт. провели сравнительное плацебо-контролируемое исследование клинико-иммунологической эффективности препарата интерферона альфа-2b в форме мази в комплексной терапии ОРИ у госпитализированных детей в возрасте от 1 года до 14 лет [9]. Препарат назначали интраназально 50 детям, вошедшим в основную группу, а в группе сравнения дети интраназально получали плацебо. В результате при применении мази с препаратом интерферона уменьшалась частота осложнений ОРИ (23,7 и 45% в группе сравнения соответственно), достоверно снижалась частота трансформации острого ринита в гнойный (7,9 и 20% в группе получавших плацебо, р≤0,01). Отмечена тенденция к сокращению длительности интоксикации, преобладанию критического варианта купирования лихорадки, уменьшению продолжительности и выраженности респираторного синдрома и сокращению сроков элиминации вирусов со слизистой оболочки носа. У детей, получавших препарат интерферона альфа-2b в форме мази, происходило увеличение индуцированной продукции α-интерферона в 2 раза, повышение уровня sIgА в смывах из носовой полости в ранние сроки заболевания, снижение уровня провоспалительного цитокина ИЛ-8. В группе сравнения таких изменений не выявлено.
Еще в одном клиническом исследовании по изучению терапевтической эффективности, безопасности и переносимости препарата интерферона альфа-2b в форме мази при лечении ОРИ и гриппа у детей приняли участие 100 пациентов в возрасте от 1 года до 9 лет 10 мес. [10]. Выявлено положительное влияние применения препарата на течение болезни: уменьшалась продолжительность катаральных симптомов, длительность сухого кашля, ускорялся переход сухого кашля во влажный, быстрее купировался токсикоз и нормализовалось общее состояние. Выявлен выраженный противовирусный эффект: происходила элиминация этиологически значимых вирусов в смывах из носоглотки у 91,6% детей, в то время как в группе контроля — только у 28%.
Еще одна форма препарата — гель — также эффективна в лечении гриппа и ОРИ. В открытом рандомизированном сравнительном клиническом исследовании, проведенном в 2011 г. [11] на базе отделения респираторных вирусных инфекций у детей ГУ НИИ гриппа РАМН, оценивали эффективность препарата интерферона альфа-2b геля у детей в возрасте от 4 мес. до 17 лет, госпитализированных в стационар с ОРИ. Методом случайной выборки были сформированы 2 группы по 50 человек. I группа получала препарат интерферона альфа-2b гель и симптоматическую терапию, а II (контрольная) группа получала только базисную симптоматическую терапию. Длительность терапии в обеих группах составила 7–10 дней. В этиологии заболевания, установленной у большинства детей основной (92%) и контрольной (82%) групп, доминировали вирусы гриппа и аденовирусы в виде моноинфекции или в сочетании, в ряде случаев обнаруживали более трех возбудителей. На фоне терапии препаратом интерферона альфа-2b гелем у детей наблюдалась статистически значимо более быстрая, чем в контрольной группе, нормализация температуры тела и купирование всех проявлений интоксикации и катарального синдрома. Было показано, что использование препарата интерферона альфа-2b в виде геля сокращает период присутствия вирусных антигенов в носоглотке пациентов. Так, уже через два дня после начала лечения у детей основной группы имело место статистически значимое сокращение числа повторного обнаружения вирусных антигенов в отличие от детей контрольной группы. Кроме того, в носовом секрете и в сыворотке крови у детей, получавших препарат интерферона альфа-2b, отмечалось повышение уровня секреторного IgA по сравнению с пациентами контрольной группы. Изучение показателей интерферонового статуса выявило умеренную способность геля к стимуляции выработки эндогенного интерферона (ИФН-α, ИФН-γ) к моменту выздоровления, что подтверждает иммуномодулирующее действие препарата. При изучении влияния препарата интерферона альфа-2b геля на динамику уровней провоспалительных цитокинов ИЛ-1β, ИЛ-8 и ФНО-α отмечена более быстрая их нормализация, повышение уровня ИЛ-1β практически не регистрировалось, тогда как в контрольной группе в 30% случаев выявлялось повышение уровня ИЛ-1β, сопровождавшееся более длительным течением заболевания. Кроме того, у большинства пациентов, получавших исследуемый препарат, наблюдались либо стабилизация, либо снижение уровня IgE по сравнению с исходным уровнем (с 53,3±6,5 до 37,3±4,9 КЕ/л) в отличие от детей контрольной группы.
Таким образом, применение препарата интерферона альфа-2b с антиоксидантами (витаминами Е и С) в комплексной терапии детей с ОРИ и гриппом приводит к более быстрому и выраженному купированию клинических проявлений заболевания, сокращению сроков выделения вирусных патогенов и более быстрой ликвидации иммунного дисбаланса, что позволяет рекомендовать интерферон альфа-2b для лечения ОРИ и гриппа у детей, в т. ч. детей раннего возраста.
Заключение
Таким образом, для каждой клинической ситуации и для каждого пациента в случае заболевания ОРИ или гриппом целесообразно использовать лекарственные препараты, действие которых направлено на уменьшение длительности заболевания и более легкое его течение. Причем необходимо учитывать все потенциальные риски и возможный исход, поскольку любое фармакологическое вмешательство оправдано только в том случае, если потенциальная польза превышает потенциальные риски применения препаратов. При принятии решения о назначении фармтерапии необходимо учитывать состояние больного, особенности болезни, риски потенциальных побочных эффектов лекарственных средств. В этом отношении препарат интерферона альфа-2b с витаминами Е и С отвечает требованиям эффективности и безопасности, а результаты исследований свидетельствуют о целесообразности его назначения при лечении ОРИ и гриппа у детей.
Острая респираторная вирусная инфекция (ОРВИ) (риниты, синуcиты, фарингиты и пр.) может быть вызвана более чем 200 типами вирусов, однако наиболее распространенными возбудителями являются риновирус, коронавирус, респираторно-синцитиальный вирус или метапневмовирус. Вирус, повреждая эпителиальную выстилку, создает условия для активации микробной флоры (пневмококк, гемофильная палочка и др.), возникают вирусно-бактериальные ассоциации.
Лечение острой респираторной инфекции зависит от стадии заболевания и включает этиотропную терапию (борьбу с вирусом), симптоматическую терапию и мероприятия, направленные на предупреждение и лечение бактериальных осложнений. Средством для профилактики бактериального воспаления в полости носа и глотки является препарат, содержащий коллоидное серебро (Сиалор ® ), оказывающий вяжущее, антисептическое и противовоспалительное действие.
Протеинат серебра диссоциирует с образованием ионов серебра, которые препятствуют размножению бактерий, связываясь с их ДНК. В основе противовоспалительного механизма действия коллоидного раствора серебра на поврежденную слизистую оболочку лежит способность к образованию защитной альбуминатной пленки, уменьшающей проницаемость слизистой оболочки для бактерий и обеспечивающей нормальное функциональное состояние клеток, способствуя быстрому восстановлению слизистой оболочки. Все это особенно важно для профилактики вторичной бактериальной инфекции при ОРВИ.
Ключевые слова: острая респираторная вирусная инфекция (ОРВИ), лечение, профилактика бактериальных осложнений, серебра протеинат, Сиалор.
Guidelines for the acute respiratory viral infection treatment
A.I. Kryukov 1,2 , A.B. Turovskii 1,3 , I.G. Kolbanova 1 , K.M. Musaev 1 , A.B. Karasov 1
1 Sverzhevskiy Otorhinolaryngology Healthcare Research Institute, Moscow
2 Pirogov Russian National Research Medical University, Moscow
3 City Clinical Hospital named after V.V. Versaev, Moscow
Acute respiratory viral infection (ARVI) (rhinitis, sinusitis, pharyngitis, etc.) can be caused by more than 200 types of viruses, and the most common are rhinovirus, coronavirus, respiratory syncytial virus, or metapneumovirus. The virus, damaging the epithelial lining, creates the conditions for the microbial flora activation (pneumococcus, hemophilic bacillus, etc.), so that virus-bacterial associations arise. Acute respiratory infection treatment depends on the disease stage and can pursue 3 goals: causal therapy (virus control); symptomatic therapy; measures aimed at preventing and treating bacterial complications. A drug (Sialor ® ) for the bacterial inflammation prevention in the nasal cavity and pharynx contains colloidal silver, which has an astringent, antiseptic and anti-inflammatory effect. Silver proteinate dissociates to form silver ions, which inhibit the bacteria growth by binding to their DNA. The anti-inflammatory action mechanism of the colloidal silver solution on the damaged mucous membrane is based on the ability to form a protective albuminate film, which reduces the mucous membrane permeability for bacteria and ensures the normal functional state of cells, contributing to the rapid restoration of the mucous membrane. All this is especially important for secondary bacterial infection prevention in acute respiratory viral infections.
Keywords: acute respiratory viral infection (ARVI), treatment, bacterial complications prevention, silver proteinate, Sialor.
В статье рассмотрены основные принципы лечения острой респираторной вирусной инфекции, акцент сделан на возможности профилактики вторичной бактериальной инфекции.
Введение
В России основная нагрузка в лечении острой респираторной вирусной инфекции (ОРВИ) (ринитов, синуситов, фарингитов и пр.) ложится на врачей общего профиля — врачей общей практики, терапевтов и педиатров. У взрослых простуда встречается от 4 до 6 раз в год, у детей — от 6 до 8 раз в год; острая респираторная инфекция является причиной 40% случаев временной нетрудоспособности, в 30% случаев — причиной пропуска школьных занятий.
Простуда может быть вызвана более чем 200 типами вирусов, однако наиболее распространенными возбудителями являются риновирус, коронавирус, респираторно-синцитиальный вирус или метапневмовирус. Именно вирус, повреждая эпителиальную выстилку, создает условия для активации микробной флоры (пневмококк, гемофильная палочка и др.), возникают вирусно-бактериальные ассоциации.
Передача инфекции происходит главным образом контактным путем — через прикосновение к зараженным поверхностям с последующим попаданием в респираторный тракт, а не воздушно-капельным путем, как это было принято считать ранее. Иногда передача возбудителя инфекции возможна через предметы обихода, игрушки, белье или посуду.
Инкубационный период большинства вирусных инфекций — от 2 до 7 дней. Выделение вирусов больным максимально на 3-и сут после заражения, резко снижается к 5-м сут; неинтенсивное выделение вируса может сохраняться до 2 нед. Симптомы, вызванные простудными заболеваниями, обычно длятся от 1 до 2 нед., и большинство пациентов чувствуют себя лучше уже после 1-й нед. заболевания. Подавляющее большинство случаев простуды разрешается спонтанно. Осложнения встречаются крайне редко и, как правило, возникают у младенцев, очень пожилых людей с ослабленным иммунитетом и больных с хроническими заболеваниями.
Симптомы ОРВИ являются результатом не столько повреждающего влияния вируса, сколько реакции системы врожденного иммунитета. Пораженные клетки эпителия выделяют цитокины, в т. ч. интерлейкины, количество которых коррелирует как со степенью привлечения фагоцитов в подслизистый слой и эпителий, так и с выраженностью симптомов. Увеличение назальной секреции связано с повышением проницаемости сосудов, количество лейкоцитов в секрете может повышаться многократно, меняя его цвет с прозрачного на бело-желтый или зеленоватый, однако это не является признаком бактериального воспаления.
Принципы лечения ОРВИ
Лечение острой респираторной инфекции зависит от стадии заболевания и включает этиотропную терапию (борьбу с вирусом), симптоматическую терапию и мероприятия, направленные на предупреждение и лечение бактериальных осложнений (табл. 1).

Для профилактики бактериального воспаления также используют местные антибактериальные средства для введения в полость носа в виде мазей, капель, спреев. Эти препараты должны воздействовать на основные патогены и быть безопасными для слизистой оболочки.
Особенности этиотропной терапии ОРВИ
Этиотропная терапия рекомендована при гриппе А (в т. ч. H1N1) и В в первые 24–48 ч болезни [3]. Эффективны ингибиторы нейраминидазы: осельтамивир (с возраста 1 год) по 4 мг/кг/сут, занамивир ингаляционно (всего 10 мг) 2 р./сут, 5 дней [3]. Однако следует помнить, что для достижения оптимального эффекта лечение должно быть начато при появлении первых симптомов заболевания, кроме того, на вирусы, не содержащие нейраминидазы, данные препараты не действуют.
Противовирусные препараты с иммунотропным действием (иммуностимуляторы и т. д.) не обладают значимым клиническим эффектом, их назначение нецелесообразно [5, 6]. Достоверность результатов исследований эффективности использования иммуномодуляторов при респираторных инфекциях невысока.
Симптоматическое лечение ОРВИ
Ведущая роль в лечении респираторной инфекции принадлежит симптоматической терапии.
Адекватная гидратация способствует разжижению секрета и облегчает его отхождение.
Рекомендуется проводить элиминационную терапию, т. к. она эффективна и безопасна. Введение в нос физиологического раствора 2–3 р./сут обеспечивает удаление слизи и восстановление работы мерцательного эпителия [2, 6]. Рекомендуется назначение сосудосуживающих капель в нос (деконгестанты) коротким курсом — не более 5 дней. Данные препараты не укорачивают длительность насморка, но могут облегчить симптомы заложенности носа, а также восстановить функцию слуховой трубы.
С целью снижения температуры тела у детей рекомендуют применять парацетамол до 60 мг/кг/сут или ибупрофен до 30 мг/кг/сут [4, 7, 14]. У взрослых также можно применять ацетилсалициловую кислоту и нимесулид.
Противокашлевые, отхаркивающие, муколитики, в т. ч. многочисленные патентованные препараты с различными растительными средствами, не рекомендуются для использования при ОРВИ ввиду неэффективности [7, 8].
Ингаляции паровые и аэрозольные не рекомендованы к использованию, т. к. не показали эффекта в рандомизированных исследованиях, а также не рекомендованы Всемирной организацией здравоохранения (ВОЗ) для лечения ОРВИ [9, 10].
Антигистаминные препараты не показали эффективности в уменьшении симптомов ринита и ОРВИ [11].
Витамин C не оказывает значимого профилактического действия на среднестатистическое население, однако указанный эффект наблюдается у людей, находящихся в условиях стресса, например спортсменов [12].
В последнее время широкое распространение получили системные деконгестанты (фенилэфрин, псевдоэфедрин) и комплексные препараты, содержащие деконгестанты (симпатомиметики), жаропонижающие, анальгезирующие, антигистаминные, антисептические компоненты и аскорбиновую кислоту в различных комбинациях. Данные препараты удобны в использовании и показывают сравнимую с другими препаратами своих групп эффективность, однако их применение возможно только с возраста 12 лет (табл. 2).

Для устранения сухости, саднения и болезненности в глотке лечение в основном местное и состоит в исключении раздражающей пищи, назначении полосканий теплыми щелочными и антибактериальными растворами, применении других местных симптоматических средств. Особый интерес представляют комбинированные препараты, например 2,4-дихлорбензиловый спирт и амилметакрезол в сочетании с различными биодобавками, для устранения клинических проявлений заболевания, способные снимать неприятные ощущения в горле, обладающие выраженным антибактериальным действием. При выраженном болевом синдроме в глотке системные анальгетики часто оказываются малоэффективными и применяются лишь в качестве антипиретиков. В этих случаях также применяются комбинированные препараты, содержащие в своем составе местные анестетики. В основном они представлены препаратами в виде аэрозолей и леденцов для рассасывания.
В состав аэрозолей обычно входят антибактериальные (хлоробутанолгидрат, фурациллин, сульфаниламид, сульфатиазол, хлоргексидин) компоненты, ментол, камфора, масла эвкалиптовое, вазелиновое, камфорное, касторовое, оливковое, мяты перечной, анисовое. Они обладают местноанестезирующим, антисептическим, противовоспалительным действием. Леденцы имеют сходный состав (антибактериальный компонент, ментол, масла), уменьшают болевые ощущения в горле и обладают дезодорирующим действием.
Профилактика бактериальных осложнений
Препараты для профилактики бактериального воспаления при ОРВИ назначаются преимущественно местно, их целесообразно начинать использовать на завершающей стадии (5–7-й день) заболевания. Для этих целей используются полоскания растворами антисептиков (табл. 3).

Для профилактики бактериального воспаления в полости носа целесообразно использовать местные антибактериальные средства, такие как антибактериальные мази, содержащие мупироцин, возможно использование капель и спреев с антибиотиками.
Особняком среди препаратов для профилактики бактериального воспаления в полости носа и глотки стоит препарат, содержащий коллоидное серебро, — серебра протеинат (Сиалор ® ). Этот препарат оказывает вяжущее, антисептическое и противовоспалительное действие. В России традиционно 1–2% раствор протеината серебра использовали для местного лечения бактериальных инфекций верхних дыхательных путей, глаз, органов мочеполовой системы, в Советском Союзе протеинат серебра выпускался с 1964 г. в форме 2% раствора.
Протеинат серебра диссоциирует с образованием ионов серебра, которые препятствуют размножению бактерий, связываясь с их ДНК, таким образом, Сиалор ® обладает бактерицидным и бактериостатическим действием на большинство грамположительных и грамотрицательных бактерий, таких как Streptococcus pneumoniae, Staphylococcus aureus, Moraxella catarrhalis, грибковую флору и др.
В основе противовоспалительного механизма действия коллоидного раствора серебра на поврежденную слизистую оболочку лежит способность к образованию защитной альбуминатной пленки, возникающей за счет осаждения белков. Данная пленка уменьшает проницаемость слизистой оболочки для бактерий и обеспечивает нормальное функциональное состояние клеток, способствуя быстрому восстановлению слизистой оболочки. Все это особенно важно для профилактики вторичной бактериальной инфекции при ОРВИ.
Благодаря широкому антибактериальному спектру действия и уникальной способности к образованию защитной пленки на поверхности слизистой оболочки Сиалор ® обладает крайне широкими показаниями к применению. Этот препарат активно используется в повседневной практике не только для лечения, но и для профилактики инфекций полости носа и носоглотки в осенне-зимний период. Хорошие результаты дает терапия препаратом и при таких неинфекционных воспалительных заболеваниях, как аллергический и вазомоторный риниты.
Раствор готовят непосредственно перед применением (200 мг препарата растворяют в 10 мл воды для инъекций), хранят при комнатной температуре, можно использовать в течение 30 дней после приготовления. В очищенные носовые ходы вводят 1–2 капли 3 р./сут детям 3–6 лет,
2–3 капли (1–2 орошения для форм выпуска с насадкой-
распылителем) 3 р./сут детям старше 6 лет и взрослым
в каждый носовой ход. Длительность курса лечения составляет 5–7 дней [15].
Заключение
Правильная дифференциальная диагностика, оценка состояния пациента и своевременнное лечение ОРВИ с учетом стадии заболевания и грамотным подбором препаратов позволяют быстро купировать симптомы, значительно сократить сроки заболевания и время нетрудоспособности пациентов. Таким образом, при должном патогенетическом подходе, используя 1–2 лекарственных препарата, можно не только эффективно бороться со всем симптомокомплексом респираторных инфекций, но и предупредить развитие их осложнений.
Читайте также:

