Флора желудочно кишечная инфекция
Обновлено: 10.05.2024
Около 60% микрофлоры находится в желудочно-кишечном тракте. Любой сбой в слаженной работе микромира способен вызвать проблемы многих систем и функций.
1. Что такое дисбактериоз? Часто можно встретить другие обозначения — дисбиоз и синдром усиленного микробного роста.
2. Можно ли назвать дисбиоз и СИБР самостоятельными заболеваниями? Требуют ли они лечения?
СИБР и дисбиоз — это вторичные синдромы, сопутствующие многим патологическим процессам.
Нарушение баланса кишечной микрофлоры отмечается при синдроме раздраженного кишечника, диарее путешественников, антибиотико-ассоциированной, воспалительных заболеваниях кишечника и другой патологии. Однако это не означает, что СИБР и дисбиоз не нужно диагностировать и лечить. Расстройства микробиоценоза кишечника и увеличение числа условно-патогенной и патогенной микрофлоры кишечника (золотистый стафилококк, энтеропатогенная кишечная палочка, энтеробактер, протей, клебсиелла, синегнойная палочка, шигеллы, кампилобактер, клостридии, кандиды и др.) требуют терапии, т. к. вызывают и поддерживают местное воспаление, сопровождаются интоксикацией и могут привести к развитию сепсиса. При субкомпенсированном и декомпенсированном кишечном дисбиозе лечение обязательно.
3. В чем причины проблем с кишечной микрофлорой?
Дисбиоз развивается вследствие инфекционных заболеваний и постинфекционных состояний; после антибиотико-, гормоно- и
полихимиотерапии, применения слабительных средств и сорбентов; хирургического удаления части кишечника. Играют роль избыточное, несбалансированное и беспорядочное питание; дефицит пищевых волокон в рационе; употребление продуктов с обилием консервантов, красителей, ксенобиотиков; радиационные повреждения кишечника; гидроколонотерапия.
СИБР появляется при гипо- и анацидных состояниях желудка; лактазной и дисахаридазной недостаточности, целиакии; хроническом панкреатите и холецистите, воспалительных заболеваниях тонкой кишки (болезнь Крона, болезнь Уиппла, васкулиты); нейропатиях и миопатиях; опухолях кишечника и хронических запорах.
4. Как диагностировать нарушения микробиоценоза?
Поскольку в кишечнике живут более 500 видов бактерий (их общая масса может достигать 2,5 кг), определить нарушения количественного и качественного состава микрофлоры непросто. Применяются следующие методики:
классический бактериологический анализ кала (посев на дисбиоз) с определением основных видов микроорганизмов;
посев на бактериальные среды кишечного содержимого, полученного эндоскопически (для определения СИБР);
дыхательный тест с лактулозой, ксилозой, меченной изотопом углерода 14С;
бактериологическое исследование кала путем ПЦР, FISH-методом, изучение микробных метаболитов (индикан, фенол, паракрезол, аммиак и др.);
хромато-масс-спектрометрия родового состава микроорганизмов, позволяющая обнаружить живые и мертвые микроорганизмы и узнать их концентрации.+
5. Как проявляется дисбактериоз?
Симптомы неспецифичны; могут наблюдаться при заболеваниях желудочно-кишечного тракта, не сопровождающихся нарушением микробиоценоза. Основные признаки — диспепсический синдром (отрыжка, неприятный вкус во рту, повышенное газообразование, вздутие живота, урчание, понос, боли и зуд в области заднего прохода), синдром малдигестии (нарушение переваривания и всасывания жиров, мяса, углеводов), боль в животе, аллергические реакции (вздутие живота, жидкий пенистый стул, кожный зуд, крапивница, отек Квинке, бронхоспазм, полиартралгии).
Весьма характерно наличие внутренней интоксикации: слабость, быстрая утомляемость, отсутствие аппетита, головные боли, повышение температуры. При длительном течении развивается синдром мальабсорбции, проявляющийся поливитаминной недостаточностью, снижением массы тела, анемией.
За сутки в пищеварительном тракте образуется несколько литров газа, который в основном поглощается кишечной стенкой. Около 600 мл ежедневно выделяется через прямую кишку, а при избыточном росте бактерий его количество увеличивается до 2 л и более.+
6. Какое лечение необходимо при СИБР и дисбиозе?
Показания к уничтожению микробного загрязнения (к деконтаминации) — СИБР и наличие высоких титров условно-патогенной микрофлоры, представляющей угрозу переноса микробов в тонкую кишку. Для этого применяется несколько групп лексредств:+
препараты спорообразующей транзиторной флоры;
Антибиотики не должны всасываться из кишечника и подавлять рост нормальной микрофлоры. Этим требованиям отвечает рифаксимин — местный кишечный антисептик, который хорошо переносится и не вызывает бактериальной резистентности. Препарат имеет широкий спектр действия против условно-патогенных и патогенных грамположительных (стрептококки, стафилококки, энтерококк, туберкулезная палочка), грамотрицательных (шигелла, сальмонелла, иерсиния, протей, кишечная палочка, пептострептококк, холерный вибрион), аэробных бактерий, а также анаэробных грамположительных (клостридии, пептококк) и грамотрицательных (бактероиды, пилорический хеликобактер). Это лексредство с успехом используется для лечения острых кишечных инфекций, коррекции СИБР, санации толстой кишки при дисбактериозе и печеночной энцефалопатии. Рифаксимин применяется в течение недели по 400 мг 3 раза в сутки. При этом уровень выдыхаемого водорода снижается в 3–5 раз уже к третьему дню терапии, что свидетельствует о быстрой санации тонкой кишки.
Можно использовать и другие антибактериальные препараты: производные оксихинолов (интетрикс), нитрофуранов (нифуроксазид, или стопдиар), нитроимидазолы (метронидазол, тинидазол), энтерофурил. Метронидазол и тинидазол показаны при контаминации анаэробными микроорганизмами. Интетрикс и нифуроксазид обладают антимикробным действием по отношению к шигеллам, сальмонеллам, иерсиниям, кампилобактеру, протею, клебсиелле, патогенным коккам, а интетрикс также подавляет рост грибов и амеб. Длительность терапии при СИБР — 12–14 дней.
Эффективное средство лечения СИБР — энтерол, представляющий собой непатогенные дрожжевые грибы рода сахаромицеты булардии, полученные из тропических растений и плодов и обладающие генетически детерминированной устойчивостью по отношению почти ко всем группам антимикробных препаратов. Антимикробное действие энтерола установлено в отношении к широкому спектру условно-патогенных микроорганизмов и простейших. В то же время энтерол не подавляет рост облигатных микроорганизмов в полости кишки. Эти грибы обладают антивирусным и трофическим эффектом (синтезируют полиамины) и через 2–5 дней после окончания приема полностью выводятся из организма без побочных явлений. Энтерол используется в качестве антидиарейного и антисептического средства при острых кишечных инфекциях (в качестве альтернативы антибиотикам при невозможности их применения), антибиотико-ассоциированной диарее, псевдомембранозном колите, паразитарных диареях, дисбактериозе, СИБР.
При толстокишечном дисбиозе IV степени и неэффективности кишечных антисептиков необходимы антибиотики общерезорбтивного действия, предпочтительно фторхинолоны (офлоксацин, ципрофлоксацин, норфлоксацин, пефлоксацин); при псевдомембранозном колите — ванкомицин, метронидазол, энтерол, бацитрацин.
Показания к назначению антибиотиков: микробное загрязнение тонкой кишки; генерализованная форма дисбактериоза; выраженный интоксикационный синдром; упорный диарейный синдром; тяжелый иммунодефицит.
Применение бактериофагов при кишечном дисбиозе не оправдало возлагаемых на них надежд: оно провоцирует мутации бактерий.
Для снятия симптомов дисбиоза используют регуляторы кишечной моторики (дебридат, метеоспазмил, мотилиум, дицетел, мукофальк, имодиум), энтеросорбенты (смекта, энтеросгель, энтеродез).
7. Какие биологические препараты применяют для лечения дисбиоза?
Есть несколько групп биологических средств коррекции нарушений микрофлоры кишечника. Эубиотики, или пробиотики, содержат живые облигатные микроорганизмы; симбиотики — комбинацию из нескольких видов живых организмов; пребиотики — стимуляторы роста нормальных микроорганизмов; синбиотики — живые бактерии; пребиотические комплексы — рациональную комбинацию из пробиотиков, пребиотиков, сорбентов, витаминов, микроэлементов.
8. Как воздействуют пробиотики?
В широком смысле слова это живые микроорганизмы и вещества микробного и другого происхождения, оказывающие благоприятный эффект на физиологические функции, биохимические и поведенческие реакции организма через оптимизацию его микроэкологического статуса.
Выделяют 4 поколения пробиотиков. К 1-му относятся однокомпонентные (колибактерин, бифидумбактерин, лактобактерин), т. е. содержащие 1 штамм бактерий.
Препараты 2-го поколения (бактисубтил, биоспорин, споробактерин и др.), основанные на использовании неспецифических для человека микроорганизмов, являются самоэлиминирующимися антагонистами патогенной микрофлоры.
Препараты 3-го поколения включают поликомпонентные пробиотики, в составе которых несколько симбиотических штаммов бактерий одного вида (ацилакт, аципол и др.) или разных видов (линекс, бифиформ) с взаимоусиливающим действием.
К 4-му поколению относят иммобилизованные на сорбенте бифидосодержащие препараты (бифидумбактерин форте, пробифор). Сорбированные бифидобактерии эффективно колонизируют слизистую оболочку кишечника, оказывая более выраженное протективное действие, чем несорбированные аналоги.
Эффекты воздействия данных лексредств на организм человека:
синтез нутриентов и антиоксидантов (витаминов С, К, группы В, фолиевой кислоты, короткоцепочечных жирных кислот, бутирата, оксида азота);
защитная функция (колонизация слизистой толстого кишечника, выработка лизоцима, бактериоцинов, снижение продукции эндотоксинов, снижение мутагенности);
иммуномодулирующая (стимуляция макрофагов, синтеза IgA, подавление синтеза IgE, модулирование цитокинового ответа);
пищеварительная (расщепление углеводов, клетчатки, жиров, белков, деконъюгация желчных кислот);
цитопротективная (нейтрализация токсических субстратов и метаболитов, стимуляция регенерации и дифференцировки эпителия кишечника, антиканцерогенный эффект бутирата через регуляции апоптоза).
9. Что такое пребиотики?
Это препараты или БАД немикробного происхождения. Они не перевариваются в кишечнике, положительно влияют на организм, стимулируя рост и/или метаболическую активность нормальной микрофлоры кишечника. Типичные представители пребиотиков — соединения, относящиеся к классу низкомолекулярных углеводов: дисахариды, олигосахариды, которые широко распространены в природе. Пребиотики не должны подвергаться гидролизу пищеварительными ферментами и абсорбироваться в верхних отделах пищеварительного тракта. Они селективно стимулируют 1 вид или определенную группу микроорганизмов толстой кишки.
В качестве пребиотиков используют олигосахариды (соевый олигосахарид, фруктоолигосахариды); моносахариды (ксилоза); дисахариды (лактулоза); полисахариды (пектины, декстрин, инулин), пищевые волокна трав (псиллиум), злаковых (отруби, Рекицен-РД), фруктов; пептиды (соевые, молочные); ферменты (протеазы сахаромицетов и др.); аминокислоты (валин, аргинин, глутаминовая кислота); антиоксиданты (каратиноиды, глутатион, витамины А, С, Е, соли селена); ненасыщенные жирные кислоты; органические кислоты (уксусная, пропионовая, лимонная); другие вещества (лецитин, парааминобензойная кислота, лактоферрин, лектины, экстракты водорослей, растительные и микробные экстракты).
Пребиотики лучше использовать на начальных этапах дисбиоза, а также для его профилактики.
10. Назначают ли при дисбиозе фитотерапию?
Лечение лекарственными травами может стать профилактическим и вспомогательным методом коррекции. Наиболее известные растения, обладающие антибактериальным действием по отношению к определенным патогенным микроорганизмам:
абрикос — подавляет гнилостные микроорганизмы, протей, клебсиеллу, синегнойную палочку;
барбарис (берберин) — гемолитические стафилококки, стрептококки, дизентерийные бактерии, энтеробактер;
брусника (сок) — рост кандид;
земляника — золотистый стафилококк, энтеробактер;
клюква (ягоды) — гнилостные бактерии рода протей и клебсиеллы;
смородина черная — грибы и золотистый стафилококк, вирусы гриппа;
черника — стафилококк, шигеллы;
шиповник — грамположительные бактерии;
яблоки — патогенные кишечные палочки, вирусы гриппа А.
Их лечебный эффект несильный и наблюдается только после длительного воздействия.
В зависимости от формы и выраженности дисбиоза пациентам с нарушениями кишечной микрофлоры для домашнего лечения можно рекомендовать при:
стафилококковом дисбактериозе — эвкалипт, зверобой, аир, календулу, барбарис, мать-и-мачеху, исландский мох. В рационе должны присутствовать ягоды черники, рябины, земляники, малины; чеснок, хрен;
микотическом кандидозном дисбактериозе — липу, тимьян, почки березы, эвкалипт, мяту, мелиссу, фенхель, шалфей, аир, исландский мох, валериану, веронику, девясил, бадан. Надо употреблять в пищу бруснику, морковь, черемшу; дрожжевой, картофельный, тыквенный и рисовый экстракты;
гнилостном дисбактериозе — крапиву, бруснику, тмин, смородину, лапчатку прямостоячую, бадан, почки березы, чистотел, полынь горькую, маклею, лопух. Показаны абрикосы, ягоды смородины, рябины, брусники; топинамбур, красный сладкий перец;
протейном дисбактериозе — эвкалипт, календулу, аир, подорожник, зверобой, ольху, бадан, полынь, лапчатку прямостоячую. Полезны клюква, малина, смородина, перец, чеснок, лук.
Различают 3 степени нарушений микробиоценоза.
Легкая. Количество бифидофлоры снижено незначительно, анаэробы преобладают над аэробами, условнопатогенная флора представлена не более чем 2 видами в титрах до 10 6 .
Средняя. Увеличивается количество аэробов. Снижается титр бифидофлоры. Число анаэробов и аэробов примерно одинаковое. Появляются атипичные формы кишечной палочки, повышается титр условнопатогенных микроорганизмов.
Тяжелая. Количество аэробов превышает число анаэробов. Резко снижен титр бифидо и лактобактерий. Увеличено число условнопатогенной флоры — 10 7 и выше. Пациенты жалуются на расстройство стула, метеоризм; есть признаки интоксикации: повышенная температура, слабость, быстрая утомляемость.
Анатолий Близнюк, доцент кафедры поликлинической терапии БГМУ, кандидат мед.наук
Медицинский вестник, 25 июня 2014
Роза Исмаиловна Ягудина, д. фарм. н., проф., зав. кафедрой организации лекарственного обеспечения и фармакоэкономики и зав. лабораторией фармакоэкономических исследований Первого МГМУ им. И. М. Сеченова.
Евгения Евгеньевна Аринина, к. м. н., ведущий научный сотрудник лаборатории фармакоэкономических исследований Первого МГМУ им. И. М. Сеченова.
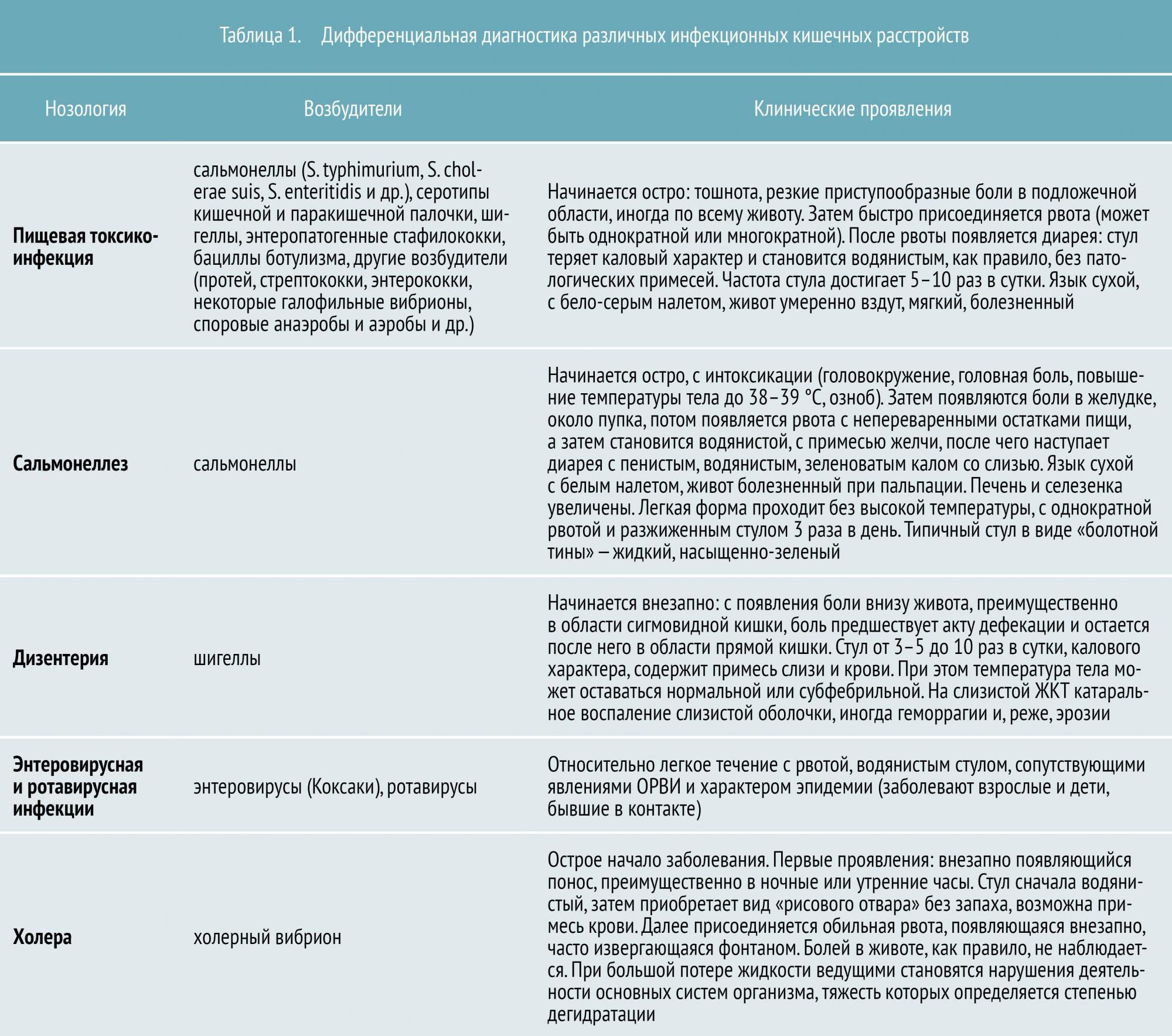
С наступившим летом тема нашей статьи приобрела особую актуальность. Кишечные инфекции — это целая группа инфекционных заболеваний, поражающих в основном желудочно-кишечный тракт. Острые кишечные инфекции по своей распространенности уступают только острым респираторным заболеваниям. Пик заболеваемости обычно приходится на лето, но и в холодное время года часто встречаются кишечные инфекции, вызываемые преимущественно вирусами. Однако наиболее частая причина возникновения этих заболеваний — попадание возбудителей инфекции с загрязненными продуктами и водой в желудочно-кишечный тракт.
Всего в настоящее время известно около 30 инфекционных кишечных заболеваний. К наиболее распространенным относятся:
- пищевая токсикоинфекция (в основном стафилококковой этиологии)
- сальмонеллез
- дизентерия
- энтеровирусная и ротавирусная инфекция
- холера
Осложнения кишечных инфекций:
- бактериальные инфекции органов дыхания и среднего уха
- дисбактериоз кишечника
- кишечное кровотечение
- перфорация стенки кишки
- инвагинация кишечника
- бактериально-токсический шок
Возбудители кишечной инфекции
Помимо инфекционных агентов из естественной среды источником заражения может стать уже заболевший человек. Выделяя большое количество патогенных микроорганизмов (микробы выделяются с испражнениями, рвотными массами, иногда с мочой), больной заражает предметы, находящиеся вокруг, и, если не соблюдать меры предосторожности, может возникнуть цепная реакция в распространении инфекции.
Практически все возбудители кишечных инфекций чрезвычайно живучи. Они способы подолгу существовать в почве, воде и на различных предметах (ложках, тарелках, дверных ручках и мебели). Инфекционные микроорганизмы во внешней среде не только не погибают, но и сохраняют способность к размножению, а размножаются они наиболее активно в теплых и влажных условиях. Однако самая благоприятная среда для развития бактерий — это кисломолочные и мясные продукты.
Установлена связь отдельных форм острых кишечных инфекций с видами пищи. Так, дизентерия чаще возникает при употреблении молока и молочных продуктов, а кишечные инфекции, вызванные стафилококком, — при употреблении молочных продуктов и кондитерских изделий с кремом. Иерсиниозы обычно развиваются при употреблении сырых овощей, салатов и другой растительной пищи.
Возбудителями кишечных инфекций могут быть как бактерии (сальмонеллы, шигеллы, иерсинии, энтеропатогенные кишечные палочки, стафилококки), так и их токсины (пищевые токсикоинфекции). Вирусы (ротавирусы, энтеровирусы, астровирусы, парвовирусы) пока на втором месте по частоте встречаемости, однако в последнее время вирусные инфекции получают всё более широкое распространение. И на последнем месте — простейшие (лямблии, амебы, бластоцисты).
После попадания патогенов в организм человека, как правило, проходит бессимптомный инкубационный период, который продолжается от 6 до 48 часов — от попадания микроорганизмов в ротовую полость до момента поступления их в кишечник, где происходит их бурное размножение. После того как патогенные микроорганизмы размножились, начинается стадия клинических проявлений.
N. B.! При появлении симптомов, напоминающих острую кишечную инфекцию, необходимо срочно обратиться к инфекционисту для правильного подбора терапии и профилактики осложнений.
Наступает острый период — от 1 до 14 дней, в это время клинические проявления со стороны ЖКТ выражены максимально. Как правило, период заканчивается, когда нормализуется температура и прекращается ведущий симптом (понос или рвота).
Период реконвалесценции — не менее 2 недель, а в некоторых случаях при отсутствии лечения до нескольких лет. В этот период функция желудочно-кишечного тракта, как правило, восстанавливается не полностью — может быть неустойчивый стул.
В основном все кишечные инфекции протекают с достаточно похожими симптомами. Они всегда начинаются внезапно. В самом начале заболевания появляется резкая слабость, вялость, снижение аппетита, головная боль, повышение температуры — неспецифические симптомы, которые могут напоминать симптомы респираторных вирусных инфекций. Однако вскоре возникают тошнота, рвота, схваткообразные боли в животе, понос с примесью слизи, гноя или крови (например, при дизентерии), также могут беспокоить жажда и озноб. Среди клинических проявлений со стороны желудочно-кишечного тракта, как правило, сильнее всего выражены симптомы, связанные с пораженным органом:
- тошнота, рвота и боли в эпигастральной области (при гастрите);
- понос (при энтерите);
- рвота и понос (при гастроэнтерите);
- кровь в стуле и его нарушения (при колите);
- поражения всего кишечника (при энтероколите).
Одно из самых неблагоприятных последствий кишечной инфекции — это дегидратация организма из‑за рвоты и/или поноса и, как следствие, нарушение водно-электролитного обмена. Результатом резкой дегидратации может стать даже шок.
Однако иногда кишечные инфекции могут не иметь видимых симптомов, но сопровождаются выделением возбудителей. В плане распространения инфекции такое носительство наиболее опасно: ничего не подозревающий человек становится постоянным источником инфекции, заражая окружающих.
Врачу важно провести дифференциальную диагностику между кишечной инфекцией и соматическими заболеваниями со сходными симптомами: диареей, связанной с приемом лекарственных препаратов, острым аппендицитом, инфарктом миокарда, пневмонией, внематочной беременностью и т. д.
Диагностика и лечение кишечной инфекции
- Выделение из крови возбудителя и его антигенов (токсинов)
- Бактериологическое исследование: выделение и типирование возбудителя в посевах кала, других биологических секретов и экскретов организма больного
- Вирусологическое исследование: выделение вируса из кала в посевах на культуре клеток или при электронной микроскопии
- Микроскопическое исследование: обнаружение паразитов в мазках нативного кала после обработки специальными красителями
- Выявление сывороточных антител к антигенам возбудителя и роста их титра: серологическое обследование с использованием специальных диагностикумов в реакциях (РПГА, РИГА, ИФА и т. п.); прирост титра в 4 раза.
Основные принципы терапии кишечных инфекций:
- борьба с возбудителем (антибактериальная терапия);
- борьба с обезвоживанием (как правило, для устранения недостатка жидкости пациентам назначают солевые растворы);
- устранение диареи (энтеросорбенты);
- соблюдение щадящей диеты (исключение свежих овощей и фруктов, молочных продуктов, сладкого).
Во время болезни необходимо соблюдать диету, помогающую замедлить перистальтику кишечника. Рекомендуются продукты с высоким содержанием танина (черника, черемуха, крепкий чай); вещества вязкой консистенции (слизистые супы, протертые каши, кисели); сухари; индифферентные вещества — паровые блюда из нежирного мяса и рыбы. Важный этап в лечении кишечных инфекций — исключение из рациона жареных и жирных блюд, сырых овощей и фруктов.
Главное направление лечебной тактики — нейтрализация экзотоксинов в кишечнике (энтеросорбенты) и регидратация — компенсация патологических потерь жидкости и электролитов специально разработанными глюкозо-солевыми растворами. Объем вводимых растворов зависит от степени обезвоживания и массы тела больного, а скорость введения составляет 1–1,5 л/ч. Дезинтоксикационная и регидратационная терапия в 85–95 % случаев может осуществляться перорально.
Антибиотики может назначить только инфекционист с учетом проведенных лабораторных тестов и выявленного возбудителя инфекции. Однако при выраженной диарее для ускоренной санации обоснованным является назначение антибактериальных ЛС, которые не всасываются или плохо всасываются из кишечника и обладают широким спектром действия (например, энтерофурил или ко-тримоксазол). Эффективными средствами альтернативной этиотропной терапии, в качестве препаратов от острой кишечной инфекции, являются энтеросорбенты и пробиотики. Этиотропное действие пробиотиков связано с выраженной антагонистической активностью в отношении всех возбудителей острых кишечных инфекций (ОКИ) бактериальной этиологии и опосредованным иммуномодулирующим действием на местное звено иммунитета.
Обзор лекарств для лечения кишечных инфекций
Нифуроксазид (энтерофурил)
Безрецептурное противомикробное средство широкого спектра действия, производное 5‑нитрофурана. Антимикробная активность нифуроксазида вызвана наличием в его составе NO2‑группы, которая угнетает активность дегидрогеназы и нарушает синтез белков в патогенных бактериях.
Нифуроксазид не оказывает действия на сапрофитную флору, не нарушает равновесия нормальной кишечной флоры. При острой бактериальной диарее восстанавливает эубиоз кишечника. При инфицировании энтеротропными вирусами препятствует развитию бактериальной суперинфекции. Этот препарат для лечения кишечной инфекции можно назначать беременным и кормящим женщинам, детям начиная с одного месяца. Терапия нифуроксазидом не должна превышать 7 дней, при этом запрещено употреблять алкоголь.
Безрецептурный препарат в форме вагинальных и ректальных суппозиториев. Обладает иммуномодулирующим, противовирусным, антихламидийным действием. Кипферон — комплексная лекарственная форма, содержащая человеческий рекомбинантный интерферон-α2 и комплексный иммуноглобулиновый препарат (КИП). Разрешен к применению у детей на первом году жизни.
Ко-тримоксазол (сульфаметоксазол + триметоприм)
Механизм действия ко-тримоксазол а обусловлен двойным блокированием метаболизма микроорганизмов. Триметоприм обратимо ингибирует дигидрофолатредуктазу микроорганизмов, нарушает образование из дигидрофолиевой кислоты тетрагидрофолиевой, продукцию нуклеиновых кислот, пиримидиновых и пуриновых оснований; подавляет размножение и рост бактерий. Сульфаметоксазол, который по строению схож с парааминобензойной кислотой, захватывается бактерией и препятствует включению парааминобензойной кислоты в дигидрофолиевую кислоту. В связи с тем что ко-тримоксазол угнетает жизнедеятельность кишечной палочки, снижается образование в кишечнике никотиновой кислоты, рибофлавина, тиамина и прочих витаминов B-комплекса. Это лекарство, помогающее от кишечной инфекции, отпускается по рецепту, применяется с 2‑месячного возраста.
Бактисубтил — споры бактерий Bacillus cereus IP. Рецептурный препарат от кишечной инфекции бактисубтил сохраняет и корригирует физиологическое равновесие кишечной флоры. Споры бактерий, содержащиеся в препарате, устойчивы к действию желудочного сока. Прорастание бактерий в вегетативные формы происходит в кишечнике, затем они высвобождают энзимы, которые расщепляют углеводы, жиры, белки. В результате образуется кислая среда, предотвращающая процессы гниения. Препарат препятствует нарушению синтеза витаминов группы В и Р в кишечнике, его нельзя запивать горячим, а также сочетать с алкоголем. Детям его назначают с семилетнего возраста. Бактисубтил резистентен к действию различных антибиотиков и сульфаниламидных препаратов, поэтому может быть назначен одновременно с ними.
Декстроза + калия хлорид + натрия хлорид + натрия цитрат (регидрон)
Регидратирующее средство для перорального приема восстанавливает водно-электролитное равновесие, нарушенное при обезвоживании организма; корректирует ацидоз. Содержимое одного пакетика растворяют в литре свежепрокипяченной охлажденной питьевой воды. Приготовленный раствор нужно хранить в холодильнике и использовать в течение 24 часов. В раствор нельзя добавлять никакие другие компоненты, чтобы не нарушить действие препарата. Отпускается без рецепта.
Безрецептурное лекарственное средство природного происхождения, обладающее протективным действием в отношении слизистой оболочки кишечника и выраженными адсорбирующими свойствами. Являясь стабилизатором слизистого барьера, образует поливалентные связи с гликопротеинами слизи и увеличивает продолжительность ее жизни, образуя физический барьер, который защищает слизистую оболочку пищеварительного тракта от отрицательного действия ионов Н+, соляной кислоты, желчных солей, микроорганизмов, их токсинов и других раздражителей. Обладает селективными сорбционными свойствами, защищает слизистую оболочку пищеварительного тракта от отрицательного воздействия. В терапевтических дозах не влияет на моторику кишечника.
Профилактика кишечных инфекций, в том числе и острых
Для профилактики кишечных инфекций важно регулярно мыть руки и проводить влажную уборку в квартире. Лучше сразу же выкидывать продукты с истекшим сроком годности, не покупать их в местах с непонятными условиями хранения — как бы ни были привлекательны, скажем, грибочки у бабушки возле метро — а фрукты и овощи есть только тщательно вымытыми.
Избежать распространения болезни поможет ранняя диагностика и изоляция больного с кишечной инфекцией. В очаге инфекции нужно обработать поверхности дезинфицирующими растворами, прокипятить посуду. Выписку пациентов проводят только после отрицательного результата контрольного обследования кала. Всем, кто перенес кишечную инфекцию, в течение месяца необходимо регулярно проходить диспансерное наблюдение в поликлинике.
Информацию из данного раздела нельзя использовать для самодиагностики и самолечения. В случае боли или иного обострения заболевания диагностические исследования должен назначать только лечащий врач. Для постановки диагноза и правильного назначения лечения следует обращаться к Вашему лечащему врачу.
Хеликобактериоз: причины появления, симптомы, диагностика и способы лечения.
Определение
Хеликобактериоз – инфекционное заболевание, поражающее пилорический отдел желудка, или привратник, и двенадцатиперстную кишку. Его возбудителем является уникальная патогенная микроаэрофильная грамотрицательная бактерия хеликобактер пилори (H. pylori). Свое название бактерия получила за счет отдела желудка, в котором она обитает – пилорического.
В результате микроорганизм еще сильнее колонизирует слизистую оболочку, формирует ее повышенную восприимчивость к соляной кислоте и провоцирует воспаление, приводящее к развитию язвенных дефектов.
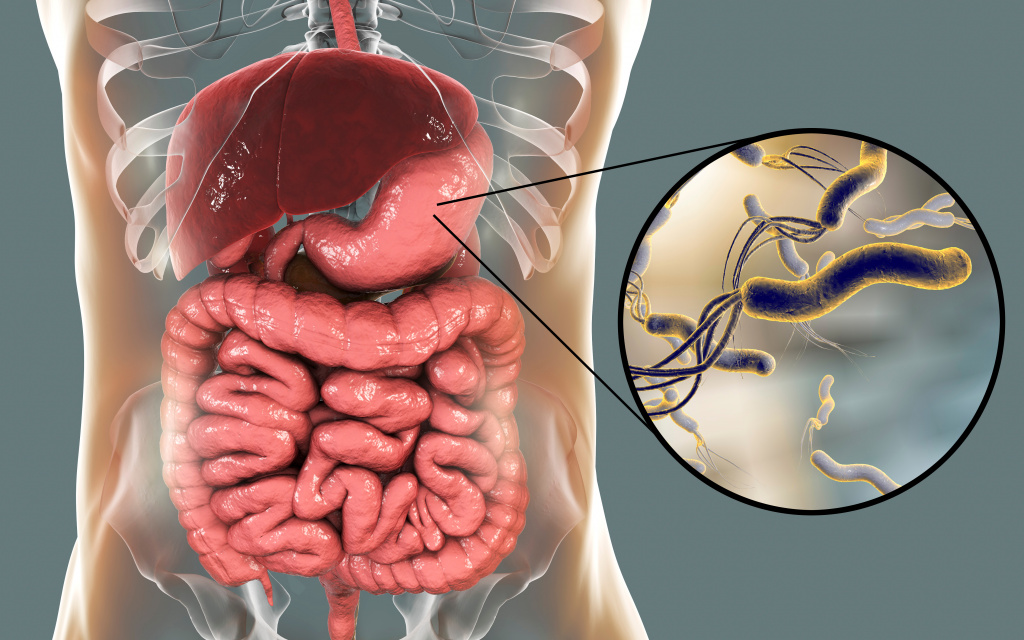
Хеликобактер пилори – спиралевидная бактерия длиной 3,5 и шириной 0,5 микрон. Она имеет жгутики, с помощью которых свободно перемещается по стенке желудка либо надежно на ней закрепляется. Бактерия H. pylori очень изменчива, ее штаммы (разновидности) отличаются друг от друга способностью прикрепляться к слизистой оболочке желудка, вызывать воспалительный процесс и обладают разной степенью патогенности.

Хеликобактер пилори, колонизирующая слизистую оболочку желудка, — частая причина ее воспалительных изменений, она признана этиологическим фактором гастрита, а сам гастрит — инфекционным заболеванием. В зависимости от состояния защитных факторов желудка возникший инфекционный процесс может протекать латентно или с выраженной клинической симптоматикой воспаления. Согласно современным представлениям, H. pylori вызывает хронический гастрит у всех зараженных лиц. Это может привести к язвенной болезни, атрофическому гастриту, аденокарциноме желудка или низкодифференцируемой лимфоме желудка. H. pylori относится к канцерогенам первого порядка.
Результаты многочисленных исследований дают основание предполагать возможную патогенетическую или опосредованную роль инфекции H. pylori в развитии и/или течении заболеваний, не относящихся к пищеварению: кардио-, цереброваскулярных, аутоиммунных заболеваний, заболеваний крови, кожи, нервной системы и многих других.
Патоген отличается относительной устойчивостью к окружающей среде: при кипячении хеликобактерии гибнут практически мгновенно, при обработке дезинфицирующими составами — в течение нескольких минут.
Причины появления хеликобактериоза
Заразиться бактерией можно при контакте с загрязненной водой или продуктами питания. Инфицирование возможно во время проведения эндоскопии и при использовании других плохо стерилизованных медицинских инструментов, которые имели прямой контакт со слизистой желудка пациента.
Бытовой способ передачи (например, через поцелуи, личные вещи и проч.) также возможен, о чем свидетельствует выделение бактерии из слюны и зубного налета.
Распространенность инфекции варьируется в зависимости от географического региона, возраста пациента, его этнической принадлежности и социально-экономического статуса. По данным Департамента здравоохранения г. Москвы (2019), распространенность этой инфекции в Москве составляет 60,7–88%, в Санкт-Петербурге - 63,6%, в Восточной Сибири достигает 90%.
Классификация заболеваний
Заболевания, связанные с H. pylori:
- гастрит,
- дуоденит,
- гастродуоденит,
- эзофагит,
- язвенная болезнь желудка,
- язвенная болезнь двенадцатиперстной кишки,
- железодефицитная анемия неясного генеза,
- рак желудка,
- рак двенадцатиперстной кишки.
Основной жалобой, с которой больные с признаками Helicobacter-инфекции обращаются к врачу, являются желудочные боли. Локализация симптома может меняться и переходить в область расположения двенадцатиперстной кишки.
Боли бывают острыми, ноющими, тупыми, возникают в верхних отделах живота слева и по центру в околопупочной области. Дискомфорт может возникать при длительном голодании, натощак или через определенное время после приема пищи.
Симптоматика хеликобактериоза зависит от клинической формы заболевания и может включать:
- чувство тяжести в животе после еды;
- нарушение аппетита, связанное с внезапными приступами тошноты (если слизистая желудка сильно травмирована);
- беспричинная рвота на фоне нормальной температуры тела;
- изжога (жгучие ощущения в пищеводе и даже гортани) и отрыжка с неприятным кислым или горьким привкусом;
- хронические запоры (отсутствие дефекации в течение трех суток и более);
- разжижение каловых масс, появление пенистой или водянистой консистенции;
- кишечные спазмы и вздутие живота.
- снижение аппетита до полного его отсутствия;
- тошнота может сменяться рвотой со сгустками крови;
- резкое снижение массы тела, не являющееся нормой;
- сухость во рту и привкус металла;
- появление белого налета на языке;
- неприятный запах изо рта при отсутствии кариеса;
- заеды в уголках рта;
- кровоточивость десен.
Диагностика хеликобактериоза
Долгое время хеликобактериоз может никак себя не проявлять, при этом провоцируя развитие язвы, аденокарциномы или мальтомы желудка. В особой зоне риска люди, чьи родственники имеют эти заболевания в анамнезе.
Диагностика может быть инвазивной (эндоскопия с последующей биопсией желудочных тканей) и неинвазивной (лабораторные исследования).
Согласно международным рекомендациям, методами выбора для диагностики бактерии и оценки эффективности лечения H. pylori служат дыхательный̆ тест с мочевиной, меченной 13С и определение специфических антигенов H. pylori в кале иммунохроматографическим методом.
Синонимы: Дыхательный тест с 13С-меченной мочевиной. 13 UBT; 13C-UBT. Краткая характеристика 13С-уреазного дыхательного теста Дыхательный тест в текущей модификации предназначен для лиц старше 12 лет. 13С-уреазный дыхательный тест относится к неинвазивным безопасным методам исследования.
Информацию из данного раздела нельзя использовать для самодиагностики и самолечения. В случае боли или иного обострения заболевания диагностические исследования должен назначать только лечащий врач. Для постановки диагноза и правильного назначения лечения следует обращаться к Вашему лечащему врачу.
Ротавирусная инфекция: причины появления, симптомы, диагностика и способы лечения.
Определение
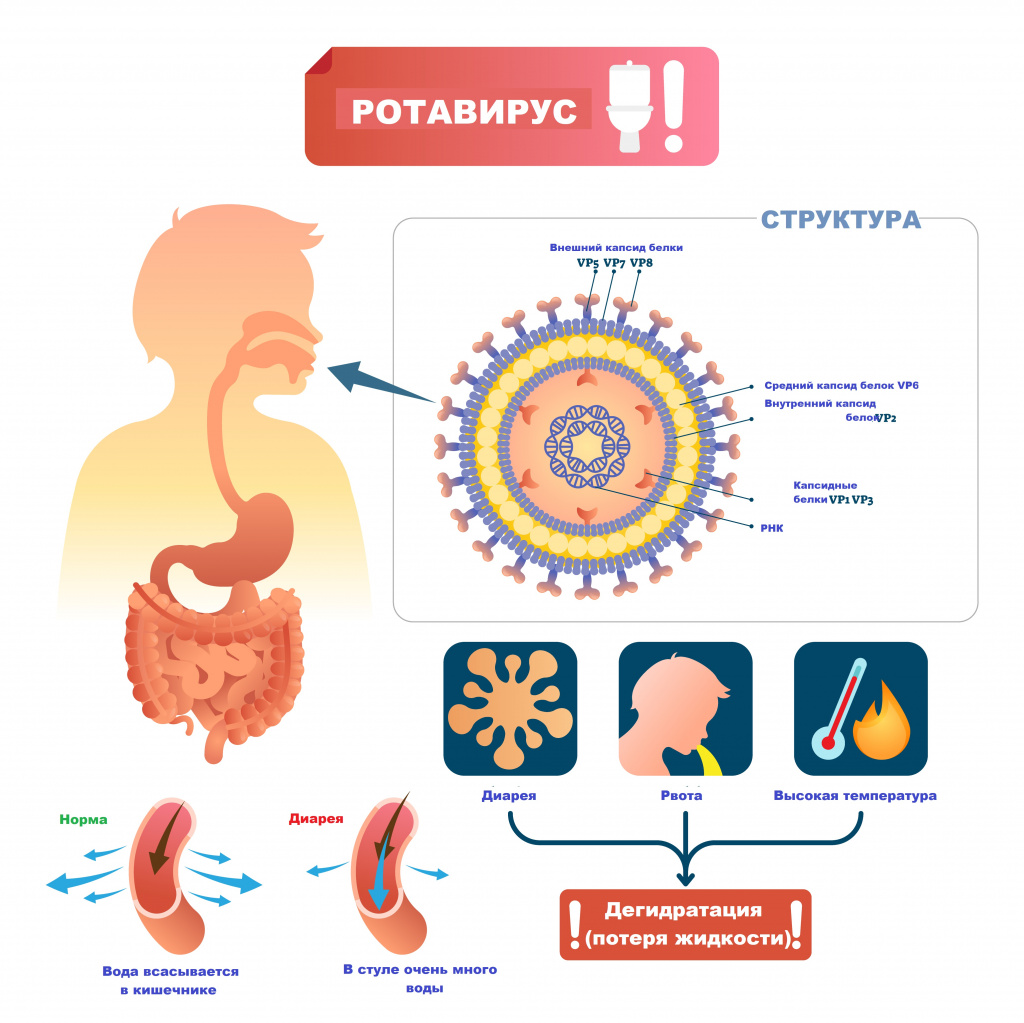
Ротавирусная инфекция (ротавирус) – это острое инфекционное заболевание, вызываемое ротавирусом и характеризующееся поражением желудочно-кишечного тракта по типу гастроэнтерита с развитием синдрома дегидратации (обезвоживания).
Причины появления ротавирусной инфекции
Возбудителем заболевания выступает вирус семейства Reoviridae, рода Rotavirus. Ротавирусы устойчивы к воздействию факторов окружающей среды, в питьевой воде, открытых водоемах и сточных водах они сохраняют жизнеспособность до нескольких месяцев, на овощах и фруктах – до 30 дней.
Основной источник и резервуар ротавирусной инфекции – больной человек в конце инкубационного периода и в первые дни болезни, выделяющий с фекалиями вирус, а также вирусоносители. Механизм передачи возбудителя – фекально-оральный.
- контактно-бытовой (через грязные руки и предметы обихода);
- водный (при употреблении воды, в которой присутствуют вирусы);
- пищевой (чаще всего при употреблении молока, молочных продуктов);
- реже – воздушно-капельный путь.
Ротавирусным гастроэнтеритом болеют люди любого возраста, но максимальная заболеваемость отмечается у детей первых двух лет жизни, людей пожилого возраста и лиц с нарушением функционирования иммунной системы.
Наблюдается зимне-весенняя сезонность, спорадические случаи заболевания регистрируются в течение всего года.
Ротавирусы проникают внутрь эпителия слизистой оболочки двенадцатиперстной кишки и верхних отделов тощей кишки. Размножение и накопление вируса приводит к гибели зрелых эпителиоцитов кишки и их отторжению. В результате нарушается абсорбция углеводов и простых сахаров, и они накапливаются в избыточном количестве. В просвете кишечника повышается осмотическое давление, нарушается всасывание воды и электролитов. Возникает водянистая диарея. Образование большого количество органических кислот, водорода, углекислого газа в процессе ферментации нерасщепленных дисахаридов кишечной микрофлорой ведет к повышению газообразования в кишечнике.
У детей с иммунными нарушениями ротавирус может стать причиной развития гепатита, нефрита, пневмонии, экзантемы, энцефалита с высоким риском летального исхода.
Классификация заболевания
Формы ротавирусной инфекции:
- типичная (гастрит, гастроэнтерит, энтерит);
- атипичная (стертая, бессимптомная);
- вирусоносительство.
- легкое;
- среднетяжелое;
- тяжелое.
- гладкое;
- негладкое (с обострениями и рецидивами).
- острое (до 1 месяца);
- затяжное (до 3 месяцев);
- хроническое (более 3 месяцев).
Инкубационный период ротавирусной инфекции составляет от 14 часов до 7 дней (в среднем 1-4 дня). Заболевание чаще всего начинается остро с повышения температуры тела от субфебрильных до фебрильных значений, появляются симптомы интоксикации (вялость, слабость, снижение аппетита), диарея и повторная рвота.
Кишечная дисфункция характеризуется жидким, водянистым, пенистым стулом желтого цвета без патологических примесей. При обильном жидком стуле развивается обезвоживание.
В тяжелых случаях возможно уменьшение количества мочи вплоть до полного ее отсутствия, снижение артериального давления.
В течение 3–6 дней могут присутствовать умеренные или сильные схваткообразные или постоянные боли в верхней половине живота. У детей младшего возраста в начале заболевания могут наблюдаться катаральные явления, которые предшествуют дисфункции кишечника: покашливание, насморк или заложенность носа, редко – конъюнктивит, катаральный отит. У детей раннего возраста на фоне высокой температуры могут развиться генерализованные судороги, сопровождающиеся потерей сознания.
Для легких форм ротавирусной инфекции характерны следующие симптомы:
- температура тела 37,1-38,0°C;
- умеренная интоксикация в течение 1–2 дней;
- нечастая рвота;
- стул жидкой кашицей до 5-10 раз в сутки.
- температура тела 38,0-39,0°C;
- выраженная интоксикация;
- повторная рвота в течение 1,5-2 дней;
- обильный водянистый стул от 10 до 20 раз в сутки;
- обезвоживание I–II степени.
- бурным началом;
- значительными потерями жидкости (обезвоживание II–III степени),
- многократной рвотой;
- водянистым стулом более 20 раз в сутки;
- снижением артериального давления.
Типичный ротавирусный гастроэнтерит характеризуется доброкачественным циклическим течением, наличием специфических признаков заболевания, а также обнаружением возбудителя в фекалиях.
К атипичным формам ротавирусного гастроэнтерита относятся:
- стертая и субклиническая формы со слабо выраженными и быстро проходящими симптомами;
- бессимптомная форма с отсутствием клинических признаков болезни, но с нарастанием титров специфических антител в крови;
- носительство ротавирусов после перенесенного острого ротавирусного гастроэнтерита, у здоровых лиц в очагах с инфекционной диареей;
- хроническая форма, сохраняющаяся более 3 месяцев.
Сочетание поражения желудочно-кишечного тракта и симптомов интоксикации, развитие обезвоживания, наличие ротавирусной инфекцией у лиц, контактирующих с больным, имеют большое значение в диагностике заболевания.
Окончательный диагноз ротавирусной инфекции ставится только на основании лабораторного подтверждения. Используют:
- методы, основанные на обнаружении ротавируса и его антигенов в фекалиях (электронная и иммуноэлектронная микроскопия, РЛА, ИФА);
- методы обнаружения вирусной РНК в копрофильтратах (метод молекулярных зондов – ПЦР и гибридизации, электрофорез РНК в полиакриламидном геле или агарозе);
- методы обнаружения специфических антител к ротавирусам в сыворотке крови (ИФА, РСК, РТГА, РНГА).
Читайте также:

