Фурамаг при кишечной палочке в моче
Обновлено: 18.04.2024
Кафедра урологии и хирургической андрологии Российской медицинской академии последипломного образования, Москва
Антибактериальная терапия острого цистита в эру растущей резистентности возбудителей
Журнал: Терапевтический архив. 2014;86(4): 125‑129
Синякова Л.А. Антибактериальная терапия острого цистита в эру растущей резистентности возбудителей. Терапевтический архив. 2014;86(4):125‑129.
Siniakova LA. Antibacterial therapy for acute cystitis in the age of growing pathogen resistance. Terapevticheskii Arkhiv. 2014;86(4):125‑129. (In Russ.).
Кафедра урологии и хирургической андрологии Российской медицинской академии последипломного образования, Москва
Аннотация. Острый цистит относится к неосложненным инфекциям нижних мочевых путей, причем частота рецидивирования после первого эпизода цистита составляет 50%. Основным методом лечения указанных заболеваний является антибактериальная терапия, эффективность которой всецело зависит от правильного выбора препарата на этапе начальной эмпирической терапии. В работе представлены рекомендации Европейской ассоциации урологов, российские национальные рекомендации, основанные на результатах как международных (ARESC), так и российских исследований (ДАРМИС) по изучению возбудителей инфекций мочевых путей и их чувствительности к антибактериальным препаратам. Препаратами выбора для лечения острого цистита в России в настоящее время являются фосфомицина трометамол и фуразидина калиевая соль.
Кафедра урологии и хирургической андрологии Российской медицинской академии последипломного образования, Москва
Острый цистит (ОЦ) относится к неосложненным инфекциям нижних мочевых путей (ИНМП). Инфекции мочевыводящих путей (ИМП) относятся к самым распространенным инфекционным заболеваниям, которые требуют значительных финансовых затрат. В Европе отсутствуют адекватные данные о распространенности различных ИМП и их влиянии на качество жизни пациентов. Отсутствуют также данные, касающиеся экономических затрат, связанных с этими инфекциями, в частности системы здравоохранения. В то же время для эффективной работы системы здравоохранения подобная информация крайне необходима. Данные, полученные в других странах и популяциях, например в США, могут быть лишь отчасти применены к ситуации в Европе. В США на ИМП приходится более 7 млн визитов к врачу в год, из них более 2 млн связаны с циститом [1]. Около 15% всех амбулаторно назначаемых в США антибиотиков общей стоимостью более 1 млрд долларов в год выписываются по поводу ИМП [2]. Более того, прямые и непрямые затраты на внебольничные ИМП превышают 1,6 млрд долларов США в год [1].
В рекомендациях Европейской ассоциации урологов (EAU) по ведению больных с инфекциями почек, мочевых путей и мужских половых органов (2008) все исследования классифицированы в соответствии с уровнями доказательности (УД) данных, и каждая разработанная на их основе рекомендация отнесена в соответствующую категорию (табл. 1, 2).
Анализ мочи с помощью тест-полосок как альтернатива микроскопии мочевого осадка - разумная альтернатива общему анализу мочи для постановки диагноза неосложненного ОЦ [3, 4] (УД: 2а, СР: В).
Бактериологическое исследование мочи рекомендовано в следующих случаях: если пациентка получала антибиотики в последние 3 мес; при наличии признаков пиелонефрита; у мужчин; у женщин с осложненными или рецидивирующими ИМП, или в возрасте старше 65 лет; при планировании эмпирической терапии фторхинолонами или цефалоспоринами в регионах, где уровень резистентности к препаратам выше 10%; в случае, если недавно проводившаяся антимикробная терапия была неэффективна 7 (УД: 4, СР: В).
На основании бактериурии более 10 3 КОЕ/мл в средней порции мочи можно поставить микробиологический диагноз у женщин с клиническими признаками неосложненного ОЦ [9] (УД: 3, СР: В).
Антибактериальная терапия (АБТ) является основным методом лечения неосложненной ИНМП. Ее эффективность зависит не только от чувствительности возбудителей, но и от концентрации препарата в очаге инфекции, а также тяжести основного и сопутствующих заболеваний у пациентки, фармакокинетических особенностей препарата, возможных побочных эффектов. Решающую роль для эффективного лечения урогенитальной инфекции играет эмпирическая антибиотикотерапия, которая при неосложненной инфекции должна начинаться немедленно после установления диагноза.
Рекомендуется проведение АБТ, потому что клиническая эффективность намного выше у женщин, которые получали антибиотики, по сравнению с плацебо [8, 9] (УД: 1а, СР: В). При выборе антибиотиков для эмпирической терапии следует руководствоваться следующим: спектр и чувствительность уропатогенов, вызывающих ИМП; эффективность при специальных показаниях в клинических исследованиях; толерантность; побочные эффекты; стоимость; доступность.
В соответствии с этими принципами и доступными особенностями чувствительности возбудителей в Европе и во многих странах терапией первого ряда при их наличии считаются фосфомицина трометамол (однократно в дозе 3 г), пивмециллины (по 400 мг в течение 3 дней) и макрокристаллы нитрофурантоина (100 мг 2 раза в день в течение 5 дней) 10 (УД: 1а, СР: А). Ко-тримаксозол в дозе 160/800 мг 2 раза в день в течение 3 дней или триметоприм по 200 мг 2 раза в день в течение 5 дней могут применяться как терапия первого ряда в тех областях, где констатирована резистентность Escherichia coli E. coli выявлена к фосфомицину трометамолу, причем во всех странах (98,3%), к нитрофурантоину - 94,8% в 6 из 10 стран, к ципрофлоксацину - 92,3% в 3 странах, поэтому указанные препараты, проявляя высокую клиническую и микробиологическую эффективность, рекомендованы EAU как препараты выбора для лечения неосложненных ИНМП.
Целью АБТ при ОЦ является быстрое купирование симптомов, профилактика рецидивов и осложнений. Короткие курсы АБТ при ОЦ имеют следующие преимущества: высокая степень соблюдения больными схемы назначенного лечения, меньшая стоимость лечения, низкая частота нежелательных реакций, снижение селекции резистентных штаммов. Однако назначение коротких курсов лечения возможно только в отсутствие факторов риска, к которым относят возраст старше 65 лет; беременность; длительность сохранения симптомов более 7 дней; рецидив инфекции; использование диафрагм и спермицидов; сахарный диабет.
Если еще в 2005 г. фторхинолоны являлись по рекомендации EAU препаратами выбора для лечения больных неосложненными ИНМП, уже в 2006 г. по результатам международного исследования ARESC мы убедились, что 92% чувствительность E. coli к фторхинолонам выявлена только в 3 из 10 стран. Резистентность грамотрицательных бактерий является значительной проблемой во всем мире, особенно среди энтеробактерий, продуцирующих β-лактамазы расширенного спектра (19-й Европейский конгресс по клинической микробиологии и инфекционным болезням, Хельсинки, 2009).
Проведенное в 2010-2011 гг. в России исследование ДАРМИС показало, что резистентность E. coli к фторхинолонам даже при неосложненных инфекциях нижних мочевых путей приближается к 10%, а при осложненных ИМП почти достигает критических для неэффективной эмпирической терапии - 20% (табл. 3).
Наиболее активными пероральными препаратами в отношении E. coli были фосфомицин (98,4%), фуразидин калия (фурамаг) (95,7%), нитрофурантоин (94,1%) и пероральные цефалоспорины третьего поколения (цефтибутен и цефиксим).
Необходимо учитывать, что для эффективного применения антимикробных препаратов - основного и обязательного компонента терапии ИМП, недостаточно данных о структуре возбудителей без данных о чувствительности уропатогенов в регионе. Несмотря на то что основной возбудитель ИМП E. coli чувствительна ко многим антибиотикам, рациональный выбор препарата в настоящее время ограничен уровнем резистентности уропатогенов. Общепринято, что антимикробные препараты не должны применяться в качестве эмпирической терапии, если уровень резистентности к ним превышает 10-20% в популяции. Именно поэтому для определения возможности использования антимикробных препаратов различных групп в качестве эмпирической и этиотропной терапии ИМП крайне необходимы данные, позволяющие определить изменения этиологии и резистентности возбудителей к ним.
Полученные в ходе исследования ДАРМИС (2011) результаты позволяют проанализировать частоту выделения резистентных штаммов возбудителей ИМП. Вполне естественно, что в связи с доминированием E. сoli в этиологической структуре ИМП наибольший практический интерес представляют прежде всего данные по суммарной устойчивости всех выделенных возбудителей семейства Enterobacteriaceae (табл. 4), особенно кишечной палочки.
Таким образом, препаратами выбора для лечения неосложненных ИМП в России являются фосфомицин и фуразидин калия (фурамаг), в качестве альтернативных препаратов можно использовать цефалоспорины третьего поколения и фторхинолоны (табл. 5) [15] (УД: 1b, СР: В).
Следует применять короткие курсы АБТ у пациенток без факторов риска (1-3 дня), что повышает степень соблюдения больными схемы назначенного лечения, снижает риск развития побочных реакций, дисбиозов кишечника и влагалища, не приводит к селекции резистентных штаммов возбудителей. Длительность лечения нитрофуранами и цефалоспоринами третьего поколения должна составлять не менее 5 сут.
Длительность курса лечения зависит от выбранного препарата. Фосфомицина трометамол - антибиотик широкого спектра действия, при ОЦ назначается однократно, его пиковая концентрация при приеме 3 г препарата достигается через 4 ч и сохраняется в течение 80 ч (см. рисунок) [16]. Рисунок 1. Разрушение фосфомицином формирующейся биопленки уропатогенных штаммов E. coli [16]. МИК - минимальная ингибирующая концентрация.
Несмотря на более чем 60-летний опыт применения нитрофуранов в клинической практике, E. сoli как основной возбудитель ИМП проявляет низкий уровень резистентности к указанной группе препаратов. Сохранение высокой чувствительности возбудителя к нитрофуранам можно объяснить следующим. Наряду с фосфомицина трометамолом препараты нитрофуранового ряда имеют достаточно ограниченные показания к применению - острый и рецидивирующий цистит, посткоитальная профилактика, профилактика осложнений перед инвазивными урологическими вмешательствами (цистоскопия и др.). В то же время нитрофураны обладают многонаправленным механизмом действия на микробную клетку. Это и позволяет нитрофуранам в течение многих десятилетий сохранять высокую не только клиническую, но и микробиологическую эффективность. В европейских странах одним из препаратов выбора для лечения НИМП является нитрофурантоин макрокристаллический, который в России отсутствует.
Фурамаг - фуразидина калиевая соль в сочетании с магния карбонатом основным в соотношении 1:1, поэтому при приеме внутрь он имеет более высокую биодоступность, чем обычный фуразидин (фурагин). Концентрация фуразидина в крови и тканях после приема фурамага (сохраняется от 3 до 7-8 ч) сравнительно небольшая, концентрация в моче выше, чем в крови (обнаруживается через 3-4 ч). Фурамаг незначительно биотрансформируется (меньше 10%), при снижении функции почек интенсивность метаболизма возрастает. Фурамаг выделяется почками путем клубочковой фильтрации и канальцевой секреции (85%), частично подвергается обратной реабсорбции в канальцах. При низких концентрациях в моче преобладают процессы фильтрации и секреции, при высоких уменьшается секреция и увеличивается реабсорбция. При кислой реакции мочи увеличивается реабсорбция, при щелочной - выведение. Фурамаг активен в отношении грамположительных и грамотрицательных микроорганизмов (Streptococcus, Staphylococcus, E. coli, Enterococcus, Salmonella, Shigella, Proteus, Klebsiella, Enterobacteriaceae), простейших (Lamblia) и др. Препарат нарушает окислительно-восстановительные реакции в микробной клетке, разрушает микробную стенку и/или цитоплазматическую мембрану. Фурамаг - бактерицидный препарат, инактивирует и изменяет протеины бактериальной рибосомы и другие макромолекулы [17]. Эффективность и безопасность фурамага доказаны в многочисленных клинических исследованиях у взрослых и детей [18]. Фурамаг в отличие от других нитрофуранов содержит помимо фуразидина калия, магния карбонат основной, что обеспечивает значительно более высокую биодоступность и позволяет достигать оптимальных терапевтических концентраций в моче при применении в меньшей дозе, чем нитрофурантоин и фурагин. Это объясняет очень низкую частоту побочных эффектов фурамага по сравнению с другими нитрофуранами. Кроме того, в экспериментах на животных доказано, что фурамаг в 3,5 раза менее токсичен, чем фурагин, и в 8,4 раза - чем нитрофурантоин [19].
Высокая эффективность фурамага при НИМП у женщин продемонстрирована в многоцентровом исследовании, включавшем 114 пациенток с ОЦ. Фурамаг назначался по 150 мг/сут в течение 5 или 7 дней. Клиническая и бактериологическая эффективность препарата составляла 96 и 95,5% соответственно, не различаясь при 5- и 7-дневном применении. Эти данные позволили рекомендовать 5-дневный курс фурамага (150 мг/сут) при острых НИМП у женщин, в том числе в постменопаузе. Важно, что фурамаг даже при длительном лечении не вызывает дисбиоза.
В Федеральное руководство по использованию лекарственных средств (2014) фуразидин калия (фурамаг) внесен в качестве препарата выбора при неосложненных ИНМП (ОЦ, рецидивирующий цистит). Длительность лечения при ОЦ составляет 5 сут.
Таким образом, основным методом лечения ОЦ, который относится к неосложненным ИМП, является АБТ. Эффективность лечения ОЦ зависит от правильности выбора препаратов для эмпирической терапии с учетом знания принципов АБТ, данных о структуре возбудителей и чувствительности уропатогенов в регионе.
Основано на официальной инструкции по применению препарата, утверждено компанией-производителем и подготовлено для печатного издания справочника Видаль 2021 года.
Владелец регистрационного удостоверения:
Контакты для обращений:
Лекарственная форма
Форма выпуска, упаковка и состав препарата Фурамаг ®
Капсулы твердые желатиновые, размер №3, желтого цвета; содержимое капсул - порошок от оранжево-коричневого до красновато-коричневого цвета, допускается наличие частиц белого, оранжевого и оранжево-коричневого цвета.
| 1 капс. | |
| фуразидин калия | 50 мг, |
| что соответствует содержанию фуразидина | 43.7 мг |
Вспомогательные вещества: магния гидроксикарбонат - 50 мг, тальк - 3 мг, крахмал кукурузный - 2.5 мг, натрия стеарилфумарат - 0.5 мг.
Состав твердой желатиновой капсулы №3: титана диоксид (Е171) - 1.32%, краситель хинолиновый желтый (Е104) - 1.2%, желатин - 97.48%.
10 шт. - упаковки ячейковые контурные (3) - пачки картонные.
Фармакологическое действие
Противомикробное средство широкого спектра действия, относящееся к группе нитрофуранов.
Резистентность к Фурамагу развивается медленно и не достигает высокой степени.
Активен в отношении грамположительных кокков: Streptococcus spp., Staphylococcus spp.; грамотрицательных палочек: Escherichia coli, Salmonella spp., Shigella spp., Klebsiella spp., Enterobacter spp.
К препарату устойчивы: Pseudomonas aeruginosa, Enterococcus spp., Acinetobacter spp., большинство штаммов Proteus spp., Serratia spp.
Механизм действия связан с ингибированием синтеза нуклеиновых кислот.
В зависимости от концентрации оказывает бактерицидное или бактериостатическое действие.
В отношении Staphylococcus spp., Escherichia coli, Aerobacter aerogenes, Bacterium citrovorum, Proteus mirabilis, Proteus morganii Фурамаг ® , по сравнению с другими нитрофуранами, более активен.
Фурамаг ® проявляет более высокую активность к Enterococcus faecalis, Staphylococcus spp. по сравнению с другими группами антибактериальных препаратов.
Против большей части бактерий бактериостатическая концентрация составляет от 1:100 000 до 1:200 000. Бактерицидная концентрация примерно в 2 раза больше.
Под влиянием нитрофуранов в микроорганизмах происходит подавление дыхательной цепочки и цикла трикарбоновых кислот (цикла Кребса), а также угнетение других биохимических процессов микроорганизмов, в результате чего происходит разрушение их оболочки или цитоплазматической мембраны.
В результате действия нитрофуранов микроорганизмы выделяют меньше токсинов, в связи с чем улучшение общего состояния пациента возможно еще до выраженного подавления роста микрофлоры. Нитрофураны, в отличие от многих других противомикробных средств, не только не угнетают иммунную систему организма, а наоборот активизируют ее: повышают титр комплемента и способность лейкоцитов фагоцитировать микроорганизмы. Нитрофураны в терапевтических дозах стимулируют лейкопоэз.
Фармакокинетика
После приема препарата внутрь фуразидин абсорбируется в тонком отделе кишечника путем пассивной диффузии. Всасывание нитрофуранов из дистального сегмента тонкого кишечника превышает всасывание из проксимального и медиального сегментов соответственно в 2 и 4 раза (следует учитывать при одновременном лечении урогенитальных инфекций и заболеваний ЖКТ, в частности хронических энтеритов). Нитрофураны плохо всасываются из толстой кишки.
C max в плазме крови сохраняется от 3 до 7 или 8 ч, в моче фуразидин обнаруживается через 3-4 ч.
Являясь смесью калиевой соли фуразидина и магния карбоната основного в соотношении 1:1, Фурамаг ® при пероральном введении имеет более высокую биодоступность, чем простой фуразидин (после приема капсулы Фурамага в кислой среде желудка не происходит превращение фуразидина калия в плохо растворимый фуразидин).
В организме фуразидин распределяется равномерно. Клинически важно высокое содержание действующего вещества в лимфе (задерживает распространение инфекции по лимфатическим путям). В желчи концентрация его в несколько раз выше, чем в сыворотке крови, а в ликворе - в несколько раз ниже, чем в сыворотке. В слюне содержание фуразидина составляет 30% от его концентрации в сыворотке крови. Концентрация фуразидина в крови и тканях сравнительно небольшая, что связано с быстрым его выделением, при этом концентрация в моче значительно выше, чем в крови.
В отличие от нитрофурантоина (фурадонина), после приема препарата Фурамаг ® рН мочи не меняется. Через 4 ч после приема препарата концентрация фуразидина в моче значительно превышает ту концентрацию, которая образуется после приема той же дозы фурагина.
Выводится почками путем клубочковой фильтрации и канальцевой секреции (85%), частично подвергается обратной реабсорбции в канальцах. При низких концентрациях фуразидина в моче преобладает процесс фильтрации и секреции, при высоких концентрациях уменьшается секреция и увеличивается реабсорбция. Фуразидин, являясь слабой кислотой, в кислой моче не диссоциирует, подвергается интенсивной реабсорбции, что может усилить развитие системных побочных эффектов. При щелочной реакции мочи выведение фуразидина усиливается.
Фармакокинетика в особых клинических случаях
При снижении выделительной функции почек интенсивность метаболизма возрастает.
Этой статьей мы начинаем рассмотрение представителей микробиологического мира, с которыми чаще всего встречаем в ежедневной клинической практике, и темой сегодняшнего разговора будет кишечная палочка, она же Escherichia coli (E.coli).
Материалы предназначены исключительно для врачей и специалистов с высшим медицинским образованием. Статьи носят информационно-образовательный характер. Самолечение и самодиагностика крайне опасны для здоровья. Автор статей не дает медицинских консультаций: клинический фармаколог — это врач только и исключительно для врачей.
Автор: Трубачева Е.С.,
врач – клинический фармаколог
Этой статьей мы начинаем рассмотрение представителей микробиологического мира, с которыми чаще всего встречаем в ежедневной клинической практике, и темой сегодняшнего разговора будет кишечная палочка, она же Escherichia coli (E.coli).
Микробиологические аспекты
E.coli относится к типичным представителям семейства Enterobacteriaceae, являясь грамотрицательной бактерией, факультативным анаэробом в составе нормальной кишечной микрофлоры человека. Но тут же становится патогеном, выбравшись из среды нормального обитания, хотя отдельные штаммы являются патогенными и для желудочно-кишечного тракта. То есть кишечная палочка относится к кишечным комменсалам, кишечным патогенам и внекишечным патогенам, каждый из которых мы кратко разберем.
К штаммам E.coli, действующим как кишечные патогены и встречающимся чаще других, относятся:
- Штамм серотипа O157:H7 (STEC O157) или так называемый энтерогеморрагический штамм E.coli, который является причиной 90% случаев геморрагических колитов и 10% случаев гемолитико-уремического синдрома. Встречается достаточно часто, а если вы работаете в стационарах плановой помощи, то это один из обязательных анализов для принятия решения о госпитализации, так что так или иначе он на слуху. Проблема инфицирования этим возбудителем связана с употреблением плохо термически обработанной пищи и передачи штамма контактным путем от человека к человеку, проще говоря, через руки.
- Второй крайне опасный высоко-патогенный штамм кишечной палочки – O104:H4, вызвавший в Германии 2011 году эпидемию с высоким уровнем смертности среди пациентов с пищевыми токсико-инфекциями вследствие развития гемолитико-уремического синдрома. Если помните, это была очень громкая история с перекрытиями границ для испанских огурцов, потом вообще для всей плодоовощной продукции из Европы в Россию, пока искали хотя бы источник, не говоря уж о виновнике тех событий. Окончательно виновными тогда были обозначены листья салата, в поливе которых использовалась вода с признаками фекального заражения, а затем речь пошла уже о пророщенных семенах, которые так же полили фекально-зараженной водичкой. Так вышли на конкретный штамм E.coli – O104:H4, который, подвергшись санации антибиотиком, выплескивает эндотоксин, вызывающий гемолиз и острую почечную недостаточность. В итоге – массовая летальность пациентов, получавших антибиотики.
Затем тот же штамм обнаружился при вспышке ПТИ в Финляндии, но к тому времени пациентов с диареями до появления микробиологических результатов перестали лечить бактерицидными антибиотиками и ситуация была купирована в зародыше.
И третий громкий (для нашей страны) случай – это массовое заболевание питерских школьников в Грузии, где так же был выявлен этот штамм (пресс-релиз Роспотребнадзора по данному случаю лежит здесь).
Когда кишечная палочка выступает внекишечным патогенном? Почти всегда, когда обнаруживается вне места своего нормального обитания.
- Заболевания мочевыводящий путей. Здесь E.coli является абсолютным лидером и играет ведущую роль в развитии:
- Острых циститов
- Пиелонефритов
- Абсцессов почек и
- Простатитов
Этот факт объясняется близким анатомическим расположением двух систем и огрехами в личной гигиене, что позволяет на этапе эмпирической терапии вышеперечисленных заболеваний сразу же назначать препараты, активные в отношении кишечной палочки.
- Заболевания желудочно-кишечного тракта:
- Диарея путешественников
- Интраабдоминальные абсцессы и перитониты, чаще всего носящие вторичный характер (прободение кишки в результате первичного заболевания, либо при дефектах оперативного вмешательства)
- Инфекции центральной нервной системы у очень ослабленных пациентов, результатом чего будет развитие менингитов. Встречается в основном у лиц старческого возраста и новорожденных. Кроме того, в случае внутрибольничного заражения менингит может развиться в результате плохой обработки рук медицинского персонала перед оперативным вмешательством или перевязками.
- Инфекции кровотока, а именно сепсис, как продолжение развития заболеваний мочевыводящих путей, ЖКТ и билиарного тракта вследствие метастазирования очага инфекции. Лечению поддается крайне тяжело, особенно если задействованы внутрибольничные штаммы, летальность чрезвычайно высокая.
- Инфекции кожи и мягких тканейкак следствие раневых инфекций после вмешательств на органах брюшной полости.
- Внутрибольничные пневмонии, вызванные устойчивыми штаммами кишечной палочки, целиком связаны с дефектами ухода за пациентом и фактором чистоты, точнее ее отсутствия, рук медицинского персонала или ухаживающих родственников. Факт внутрибольничного заражения доказывается элементарно, что будет наглядно продемонстрировано в следующем разделе.
- Послеродовые (и не только) эндометриты. Вынуждены упомянуть и эту патологию, так как инфицирование кишечной палочкой встречается все чаще и чаще, а большой настороженности нет. Как результат, можно очень сильно промахнуться с антибактериальной терапией и, как следствие, прийти к экстирпации органа в виду неэффективности антибиотикотерапии. Натолкнуть на мысль может более позднее, чем обычно, поступление и более агрессивное, чем обычно течение. Дополнительный осмотр прианальной области так же может натолкнуть на вероятность развития именно такого инфицирования.
(часть вторая) Практические вопросы диагностики и лечения.
Когда мы можем заподозрить, что перед нами пациент с инфекцией, вызванной кишечной палочкой?
- Пациенты с диареей, приехавшие из отпуска и все-таки смогшие прийти на прием (диарея путешественников или энтеротоксигенные штаммы E.coli).
- Пациенты со всеми заболеваниями мочевыделительной системы, в том числе беременные, но строго с наличием симптоматики (не надо лечить бессимптомную бактериурию, иначе вырастите резистентные штаммы и создадите проблему и себе, и женщине, и роддому в последующем).
- В стационарах – нозокомиальные пневмонии, послеоперационные менингиты, перитониты, сепсисы и т. д., носящие вторичный характер.
Подтвердить или полностью исключить кишечную палочку из возбудителей может только микробиологическое исследование. Конечно, в современных условиях микробиология уже становится практически эксклюзивом, но мы пришли учиться, а учится надо на правильных примерах, поэтому далее будет рассмотрен ряд антибиотикограмм, выполненных автоматизированными системами тестирования. Вдруг вам повезет, и в вашем лечебном учреждении все уже есть или в ближайшее время будет, а вы уже умеете с этим всем работать?
Если вы читаете данный цикл по порядку, то в базовом разделе по микробиологии был выложен ряд антибиотикограмм некоего микроорганизма в контексте нарастания антибиотикорезистентности, и это была наша сегодняшняя героиня – кишечная палочка.
- Начнем с дикого и крайне симпатичного штамма E.coli, который живет в кишечнике и обеспечивает синтез витамина К. С ним сталкиваются доктора амбулаторной службы у пациентов с инфекциями мочевыводящих путей или в случае госпитализации у пациентов, которые не получали антибиотики около года. И именно такую чувствительность мы имеем в виду, когда назначаем эмпирическую антибиотикотерапию
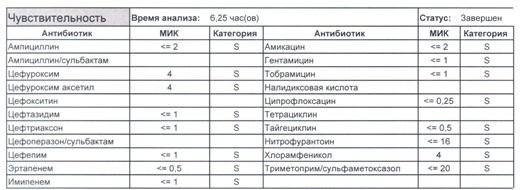
- Как видите, зверь чувствителен абсолютно ко всему, и это как раз тот случай, когда можно свободно пользоваться табличными материалами справочников или клинических рекомендаций, так как механизмы резистентности полностью отсутствуют.
- Если в ваши руки попал пациент, которого в течение последнего полугодия лечили антибиотиками пенициллинового ряда, то антибиотикограмма может выглядеть следующим образом.
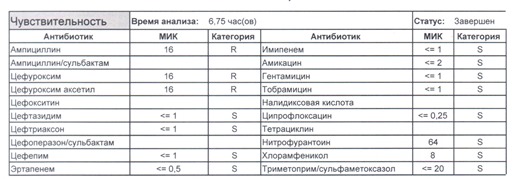
Если такая кишечная палочка окажется внекишечным патогенном, и перед вами будет беременная и ИМП (самый частый случай), то нам необходимо преодолеть резистентность к пенициллинам, то есть подавить деятельность пенициллиназ. Соответственно высокую эффективность продемонстрируют препараты с ингибиторами бета-лактамаз, чаще всего амоксициллина/клавуланат, как наиболее безопасный и эффективный. Единственное, пациентку необходимо предупредить, что в результате стимуляции рецепторов кишечника может развиться антибиотик-ассоциированная диарея.
- Отдельно хотелось бы обратить внимание на следующий штамм E.coli, как типичного обладателя бета-лактамаз расширенного спектра. И эти БЛРС чаще всего вырабатываются в результате неуемного использования цефалоспоринов третьего поколения и совершенно конкретного его представителя – цефтриаксона.
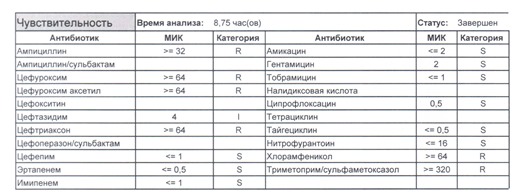
В каких ситуациях мы можем увидеть (или подумать) о таком звере:
- Пациент сам рассказывает, что получал цефтриаксон в промежутке полугодия
- Пациент был переведен из другого стационара (хотя там можно будет и следующую картинку обнаружить)
- Пациент ничего не получал, и вообще в больнице не лежал, но возбудитель попал с рук медицинского персонала, вызвав внутрибольничную инфекцию
- И самый простой случай – посев был взят в момент проведения терапии цефтриаксоном
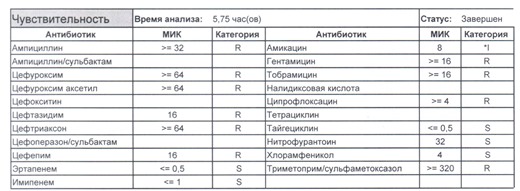
Подобный пациент не придет к вам своими ногами, его не увидит амбулаторная служба, это абсолютно стационарные больные, и если их привезут, то только из другого лечебного учреждения. Чаще всего это пациенты палат интенсивной терапии или реанимации, и такой возбудитель носит на 100% нозокомиальный характер.
Когда можем его обнаружить:
- вторичные перитониты,
- нозокомиальные пневмонии,
- пиелонефриты,
- послеоперационные менингиты,
- сепсис и т. п.
- Для эрадикации такого возбудителя нужен не просто отдельный обученный специалист и имеющая весь набор препаратов резерва аптека, но и напряженная работа эпидемиологической службы, так как подобный пациент должен быть изолирован в отдельную палату, а лучше изолятор (не подумайте, что бред – при правильной организации такие вещи вполне реальны) с проведением карантинных мероприятий, так как основная проблема появления подобного рода возбудителей в том, что они очень быстро разбегаются по всему корпусу (или стационару, если корпуса не изолированы) и обсеменяют все и вся, нанося вред другим ослабленным тяжелой болезнью пациентам и заселяя кишечники всего медицинского персонала.
- И еще одно крайне мерзкое свойство таких возбудителей – они умеют осуществлять горизонтальный перенос механизмов резистентности с другой флорой семейства Enterobacteriaceae, и даже если вы избавились от E.coli, неприятным сюрпризом может стать ее подруга клебсиелла, наносящая еще больший вред и по сути добивающая больного. Избавится полностью от этих возбудителей невозможно, для этого надо избавится от медицинского персонала как основных носителей, но контролировать можно – мероприятия подробно расписаны в действующих СанПиН 2.1.3.2630-10. Так что в случае выявления подобного возбудителя речь пойдет не только о лечении того пациента, у которого он обнаружен, но и проведения мероприятий по недопущению инфицирования всех остальных пациентов (а это, напомню, почти всегда ПИТ или ОРИТ), находящихся рядом.
- И в заключение необходимо упомянуть о панрезистентной E.coli, вооруженной полным спектром механизмов резистентности. В антибиотикограмме будут тотальные R, а МПК возбудителей пробьют все возможные потолки. К счастью для автора, она с таким зверем пока не сталкивалась, что связано с наличием работающей системы эпиднадзора, поэтому картинки не будет, хотя ее несложно представить. Такие пациенты, если кишечная палочка окажется патогеном, а не колонизатором (мало ли с чьих рук, например, в рану упала), к сожалению, почти не выживают, так как изначально являются крайне тяжелыми соматически, а кишечная палочка обычно подводит черту к их существования на бренной земле.
- Не допускать развития такой, не побоюсь этого слова, зверюги в ваших стационарах, а если появилась – гонять эпидемиологическую службу, чтобы избавляла руки и поверхности от такого рода заражения, что возможно только при условии наличия достаточного количества расходных материалов, перчаток и дезинфицирующих средств.
А теперь подведем небольшой итог нашего непростого разговора:
- Кишечная палочка – возбудитель очень серьезный и не следует его недооценивать. В ее типах также необходимо четко ориентироваться.
- В первую очередь о ней мы думаем при лечении инфекций мочевыводящих путей, особенно у беременных.
- Если перед нами пациент с признаками кишечной инфекции, то подход к терапии антибиотиками должен быть сугубо индивидуальным, и если состояние позволяет, то до получения микробиологии – вообще без антибиотиков. Если не позволяет – это должны быть бактериостатики.
- Мы никогда не лечим только анализ, и даже микробиологическое заключение, мы всегда лечим пациента со всем комплексом его симптомов и синдромов. Но микробиология помогает решить как дифференциально-диагностические задачи, что и позволяет отделить безусловный патоген от мирно живущего комменсала.
- Микробиологическая диагностика носит ключевое значение как для подтверждения самого возбудителя, так и для выбора необходимого антибиотика
- В случае выявления резистентных и панрезистентных возбудителей, помимо лечения самого пациента должна в полной мере задействоваться эпидемиологическая служба лечебного учреждения
Приведенная научная информация является обобщающей и не может быть использована для принятия решения о возможности применения конкретного лекарственного препарата.
Владелец регистрационного удостоверения:
Лекарственная форма
Форма выпуска, упаковка и состав препарата Фурагин
10 шт. - упаковки ячейковые контурные (1) - пачки картонные.
10 шт. - упаковки ячейковые контурные (2) - пачки картонные.
10 шт. - упаковки ячейковые контурные (3) - пачки картонные.
10 шт. - упаковки ячейковые контурные (4) - пачки картонные.
10 шт. - упаковки ячейковые контурные (5) - пачки картонные.
10 шт. - упаковки ячейковые контурные (1350) - коробки картонные.
10 шт. - флаконы полимерные (1) - пачки картонные.
20 шт. - флаконы полимерные (1) - пачки картонные.
30 шт. - флаконы полимерные (1) - пачки картонные.
40 шт. - флаконы полимерные (1) - пачки картонные.
50 шт. - флаконы полимерные (1) - пачки картонные.
Фармакологическое действие
Противомикробное средство широкого спектра действия, относится к группе нитрофуранов. Механизм действия связан с ингибированием синтеза нуклеиновых кислот. Под влиянием нитрофуранов происходит подавление активности дыхательной цепочки и цикла трикарбоновых кислот (цикла Кребса), а также угнетение других биохимических процессов микроорганизмов, что приводит к разрушению их оболочки или цитоплазматической мембраны.
Активен в отношении грамположительных кокков: Staphylococcus spp., Streptococcus spp.; грамотрицательных палочек: Escherichia coli, Salmonella spp., Shigella spp., Klebsiella spp.
К фуразидину устойчивы: Pseudomonas aeruginosa, Enterococcus spp., Acinetobacter spp., большинство штаммов Proteus spp., Serratia spp.
В зависимости от концентрации оказывает бактерицидное или бактериостатическое действие. Против большей части бактерий бактериостатическая концентрация составляет от 10 до 20 мкг/мл. Бактерицидная концентрация примерно в 2 раза выше.
Фармакокинетика
После приема внутрь фуразидин абсорбируется из тонком отделе кишечника путем пассивной диффузии. Всасывание нитрофуранов из дистального сегмента тонкого кишечника превышает всасывание из проксимального и медиального сегментов соответственно в 2 и 4 раза (следует учитывать при одновременном лечении урогенитальных инфекций и заболеваний ЖКТ, в частности хронических энтеритов). Нитрофураны плохо всасываются из толстой кишки.
C max в плазме крови сохраняется от 3 до 7 или 8 ч, в моче фуразидин обнаруживается через 3-4 ч.
В организме фуразидин распределяется равномерно. Клинически важно высокое содержание препарата в лимфе (задерживает распространение инфекции по лимфатическим путям). В желчи концентрация его в несколько раз выше, чем в сыворотке, а в ликворе - в несколько раз ниже, чем в сыворотке. В слюне содержание фуразидина составляет 30% от его концентрации в сыворотке. Концентрация фуразидина в крови и тканях сравнительно небольшая, что связано с быстрым его выделением, при этом концентрация в моче значительно выше, чем в крови.
Метаболизируется в незначительной степени (<10%).
Выводится почками путем клубочковой фильтрации и канальцевой секреции (85%), частично подвергается обратной реабсорбции в канальцах. При низких концентрациях фуразидина в моче преобладает процесс фильтрации и секреции, при высоких концентрациях уменьшается секреция и увеличивается реабсорбция. Фуразидин, являясь слабой кислотой в кислой моче не диссоциирует, подвергается интенсивной реабсорбции, что может усилить развитие системных побочных эффектов. При щелочной реакции мочи выведение фуразидина усиливается.
При снижении выделительной функции почек интенсивность метаболизма возрастает.
Показания активных веществ препарата Фурагин
Для приема внутрь: урогенитальные инфекции (острый цистит, уретрит, пиелонефрит); гинекологические инфекции; инфекции кожи и мягких тканей; тяжелые инфицированные ожоги; с профилактической целью при урологических операциях (в т.ч. цистоскопии, катетеризации).
Для наружного и местного применения: инфекционно-воспалительные заболевания полости рта и глотки, инфицированные раны.
Открыть список кодов МКБ-10| Код МКБ-10 | Показание |
| J02 | Острый фарингит |
| J03 | Острый тонзиллит |
| J31.2 | Хронический фарингит |
| J35.0 | Хронический тонзиллит |
| K05 | Гингивит и болезни пародонта |
| K12 | Стоматит и родственные поражения |
| L01 | Импетиго |
| L02 | Абсцесс кожи, фурункул и карбункул |
| L03 | Флегмона |
| L08.0 | Пиодермия |
| L08.8 | Другие уточненные местные инфекции кожи и подкожной клетчатки |
| N10 | Острый тубулоинстерстициальный нефрит (острый пиелонефрит) |
| N11 | Хронический тубулоинтерстициальный нефрит (хронический пиелонефрит) |
| N30 | Цистит |
| N34 | Уретрит и уретральный синдром |
| N41 | Воспалительные болезни предстательной железы |
| N70 | Сальпингит и оофорит |
| N71 | Воспалительная болезнь матки, кроме шейки матки (в т.ч. эндометрит, миометрит, метрит, пиометра, абсцесс матки) |
| N72 | Воспалительная болезнь шейки матки (в т.ч. цервицит, эндоцервицит, экзоцервицит) |
| N73.0 | Острый параметрит и тазовый целлюлит |
| T79.3 | Посттравматическая раневая инфекция, не классифицированная в других рубриках |
| Z29.2 | Другой вид профилактической химиотерапии (введение антибиотиков с профилактической целью) |
Режим дозирования
Способ применения и режим дозирования конкретного препарата зависят от его формы выпуска и других факторов. Оптимальный режим дозирования определяет врач. Следует строго соблюдать соответствие используемой лекарственной формы конкретного препарата показаниям к применению и режиму дозирования.
Принимают внутрь после еды. Взрослым - по 50-100 мг 3 раза/сут, детям старше 3 лет - по 25-50 мг (не более 5 мг/кг массы тела) 3 раза/сут. Курс лечения 7-10 дней. При необходимости повторения курса лечения следует сделать перерыв в течение 10-15 дней. Для профилактики инфекции (в т.ч. при урологических операциях, цистоскопии, катетеризации) - 50 мг однократно за 30 мин до процедуры.
Применяют наружно 2-3 раза/сут для промывания ран или смачивания перевязочного материала.
Применяют местно 2-3 раза/сут в виде полосканий полости рта и глотки.
Побочное действие
Со стороны пищеварительной системы: редко - тошнота, рвота, потеря аппетита, нарушения функции печени.
Со стороны ЦНС и периферической нервной системы: редко - головная боль, головокружение, полиневрит.
Аллергические реакции: редко - кожная сыпь (в т.ч. папулезные высыпания).
Противопоказания к применению
Хроническая почечная недостаточность тяжелой степени; беременность; период лактации (грудного вскармливания); детский возраст до 4 лет; повышенная чувствительность к фуразидину и другим нитрофуранам.
Применение при беременности и кормлении грудью
Применение при нарушениях функции почек
Применение у детей
Противопоказан в детском возрасте до 3 лет.
Особые указания
Для уменьшения вероятности развития побочных эффектов фуразидин запивают большим количеством жидкости.
При появлении побочных эффектов применение следует прекратить (токсические явления чаще проявляются у пациентов со сниженной выделительной функцией почек).
В период лечения пациенту рекомендуется воздержаться от употребления алкоголя, поскольку возможно усиление побочных эффектов.
Не принимать удвоенную дозу для компенсации пропущенной дозы.
С осторожностью применять при дефиците глюкозо-6-фосфатдегидрогеназы.
Лекарственное взаимодействие
При комбинации фуразидина с ристомицином, хлорамфениколом, сульфаниламидами повышается риск угнетения кроветворения (не следует применять одновременно).
Не рекомендуется одновременно с нитрофуранами применять препараты, способные подкислять мочу (в т.ч. аскорбиновую кислоту, кальция хлорид).

Пациентка жаловалась на слабость, частые повелительные позывы к мочеиспусканию при минимальном количестве мочи, дискомфорт в нижних отделах живота при наполненном мочевом пузыре и в конце акта мочеиспускания. Вышеуказанные жалобы начались после переохлаждения, за 10 дней до обращения к врачу.
Со слов пациентки, кроме переохлаждения к рецидивам приводили стрессы, снижающие иммунитет организма, а также периодически — половые акты.
Анамнез
Пациентка страдает хроническим циститом последние 8 лет. В среднем отмечает 3-4 обострения в год. У уролога постоянно не наблюдалась, лечилась самостоятельно приёмом "Монурала" и растительных диуретиков ("Цистон", "Канефрон").
Пациентка замужем, есть ребёнок. Половой партнёр один. Хронические заболевания и операции отрицает. У рологический анамнез не осложнён. Аллергию на лекарства отрицает. Перенесённые инфекционные заболевания, туберкулёз, гепатит, венерические болезни отрицает.
Обследование
При осмотре состояние удовлетворительное. Температура тела 36.9 °C . Живот при пальпации мягкий и безболезненный, не вздут. Область почек визуально не изменена. При пальпации область почек безболезненна. Симптом Пастернацкого (болезненные ощущения при постукивании в области почек) отрицательный с обеих сторон.
При объективном осмотре пациентка отмечает дискомфорт при пальпации надлобковой области. Мочеиспускание учащённое, дискомфортное. Ноктурия (мочеиспускание по ночам): 1-2 раза. Макрогематурию (примесь крови в моче) отрицает. Стул в норме. Вес 55 кг.
- В общем анализе мочи: лейкоциты 15-20 в п/зр, эритроциты 5-10 в п/зр, эпителий +++, слизь ++.
- В бактериологическом посеве мочи: Escherichia coli (кишечная палочка) 10*5 КОЕ/мл , чувствительность ко всем группам антибиотиков, кроме фосфомицина.
- УЗИ почек, мочевого пузыря: УЗ-признаков патологии не выявлено.
- Смотровая цистоскопия: область треугольника Льето ( передне-центральная часть дна мочевого пузыря) буллёзно изменена (имеются буллы — полости, заполненные серозной жидкостью), обложена фибрином.
По заключению гинеколога, в мазках нет воспалительных изменений. Данных за гинекологическую патологию не выявлено.
Диагноз
Лечение
-
по 50 мг х 3 раза в день — 10 дней (при дискомфорте в нижних конечностях MgB6 по 2 таблетке х 3 раза в день). 1 чайная ложка х 3 раза в день — 7 дней, затем 2 раза в день — 21 день. 1 капсула х 1 раз в день — 3 месяца, курсами весна/осень.
- Обильное питье (не менее двух литров жидкости).
- Диета с исключением алкоголя, сильно острой и солёной пищи.
- Половой покой в течение 10 дней.
После купирования очередного обострения проводился профилактический курс препаратом "Уро-ваксом". Лечение пациентка перенесла хорошо.
После проведённого лечения обострение хронического цистита было купировано. При дальнейшем наблюдении в течение всего 2019 года пациентка не отмечала обострений заболевания.
- общий анализ мочи — без патологии в осадке мочи;
- бактериологический посев мочи — роста микрофлоры не выявлено.
Заключение
Читайте также:

