Гематогенная инфекция плодного пузыря
Обновлено: 24.04.2024
Кафедра акушерства и гинекологии №1 Башкирского государственного медицинского университета
Кафедра акушерства и гинекологии №1 Башкирского государственного медицинского университета
Кафедра акушерства и гинекологии №1 Башкирского государственного медицинского университета
Кафедра акушерства и гинекологии №1 Башкирского государственного медицинского университета
Кафедра акушерства и гинекологии №1 Башкирского государственного медицинского университета
Кафедра акушерства и гинекологии №1 Башкирского государственного медицинского университета
Кафедра акушерства и гинекологии №1 Башкирского государственного медицинского университета;
Клинический родильный дом №4, Уфа
Внутриутробное инфицирование плода: современный взгляд на проблему
Журнал: Российский вестник акушера-гинеколога. 2013;13(5): 16‑20
Хамадьянов У.Р., Русакова Л.А., Хамадьянова А.У., Тихонова Т.Ф., Хамадьянова С.У., Галимов А.И., Иваха В.И. Внутриутробное инфицирование плода: современный взгляд на проблему. Российский вестник акушера-гинеколога. 2013;13(5):16‑20.
Khamad'ianov UR, Rusakova LA, Khamad'ianova AU, Tikhonova TF, Khamad'ianova SU, Galimov AI, Ivakha VI. Intrauterine fetal infection: the present view of the problem. Russian Bulletin of Obstetrician-Gynecologist. 2013;13(5):16‑20. (In Russ.).
Кафедра акушерства и гинекологии №1 Башкирского государственного медицинского университета
В статье на основании данных современной литературы и результатов ранее выполненных собственных исследований представлены вопросы этиологии и патогенеза, диагностики, лечения и профилактики внутриутробной инфекции (ВУИ). Особое внимание обращено на роль инфекционного фактора в реализации ВУИ и значение цитокинового статуса. Приведена интерпретация диагностических тестов при ВУИ на современном этапе.
Кафедра акушерства и гинекологии №1 Башкирского государственного медицинского университета
Кафедра акушерства и гинекологии №1 Башкирского государственного медицинского университета
Кафедра акушерства и гинекологии №1 Башкирского государственного медицинского университета
Кафедра акушерства и гинекологии №1 Башкирского государственного медицинского университета
Кафедра акушерства и гинекологии №1 Башкирского государственного медицинского университета
Кафедра акушерства и гинекологии №1 Башкирского государственного медицинского университета
Кафедра акушерства и гинекологии №1 Башкирского государственного медицинского университета;
Клинический родильный дом №4, Уфа
Прогрессирующий рост числа случаев внутриутробного инфицирования плода является одной из наиболее актуальных проблем современного акушерства и перинатологии. Этому способствует полиэтиологичность данной патологии, отсутствие четкой взаимосвязи между выраженностью клинических проявлений инфекции у матери и степенью поражения плода, многофакторное воздействие инфекционного агента на плод.
Несмотря на повышенное внимание к проблеме внутриутробной инфекции (ВУИ), нерешенными остаются многие вопросы. В дальнейших поисках и разработке нуждаются вопросы диагностики, лечения и профилактики ВУИ. До сих пор нет четких критериев лечебной тактики, не обобщены данные об эффективности комплексной терапии.
Эпидемиология, этиология и патогенез внутриутробной инфекции
В развитии инфекционного процесса у плода имеют значение вид возбудителя, его вирулентность, пути проникновения инфекции от матери к плоду, защитные резервы организма матери и способность плода к иммунному ответу [11].
Известно, что большинство бактерий существуют в природе в виде специфически организованных биопленок (biofilms) [2, 25, 27]. Такая форма существования создает бактериям массу преимуществ. Бактерии в биопленках имеют повышенную выживаемость в присутствии агрессивных веществ, факторов иммунной защиты и антибиотиков [27]. В этой связи одной из основных проблем практической медицины становится проблема лечения заболеваний микробного происхождения.
В нашем исследовании [15, 17] по результатам бактериологического анализа видового состава вагинального биотопа было выявлено наиболее сильное влияние Streptococcus faecalis (p=0,00171), E. coli (p=0,01424) и Staphylococcus epidermidis (p=0,02714) на реализацию внутриутробного инфицирования плода. При оценке возбудителей, выявленных в цервикальном канале беременных путем полимеразной цепной реакции (ПЦР) и иммуноферментного анализа (ИФА), установлено следующее: в группе без реализации ВУИ микоплазмы, хламидии и уреаплазмы составили 8%, ЦМВ - 20%, ВПГ - 36%, кандида - 3%, ассоциации - 60%. При анализе группы новорожденных с реализацией ВУИ были выделены наиболее частые возбудители. Так, микоплазмы, хламидии и ВПГ встречались в 50%, ЦМВ-инфекция была выявлена в 45% случаев, реже встречались уреаплазмы (20%) и кандида (15%), ассоциации наблюдались в 95%. Частота обнаружения патогенных возбудителей у новорожденных с признаками ВУИ была выше, чем у пациентов без реализации инфекции.
Основным источником инфекции при ВУИ является мать ребенка, из организма которой возбудитель проникает в организм плода (вертикальный механизм передачи). При этом инфицирование происходит как восходящим, трансплацентарным и трансовариальным путями, так и контактным, и аспирационным (непосредственно во время родов) путями. Причем для антенатальных инфекций наиболее типичен гематогенный, а для интранатальных - восходящий пути инфицирования [4, 10, 20, 21].
Влияние ВУИ на эмбрион и плод заключается в воздействии комплекса следующих факторов [22]:
1. Патологическое действие микроорганизмов и их токсинов (инфекционное заболевание, гипоксия плода, задержка развития плода).
2. Нарушение процесса имплантации и плацентации (низкая плацентация, предлежание плаценты).
3. Снижение метаболических процессов и иммунной защиты плода.
В патогенезе возникновения и развития ВУИ особое значение имеет срок беременности [13, 22]. Плод до 14 нед беременности не реагирует на инфекционные антигены, так как у него отсутствуют иммунокомпетентные клетки, иммуноглобулины и не проявляются иммунные реакции. С началом II триместра беременности механизм воздействия восходящей инфекции меняется из-за слияния decidua vera и deciduas capsularis в единый комплекс deciduas parietalis. В это время восходящая инфекция может проникнуть к плоду из влагалища или шеечного канала. С этого срока беременности внутренний зев шеечного канала соприкасается с водными оболочками плода и при наличии инфекции микроорганизмы проникают в околоплодные воды. Антимикробные свойства амниотическая жидкость приобретает лишь после 20-й недели беременности, когда в ответ на воздействие инфекционного агента развивается воспалительная пролиферативная реакция, ограничивающая дальнейшее проникновение инфекции, благодаря появлению лизоцима, комплемента, интерферонов, иммуноглобулинов [1, 22]. В III триместре беременности антибактериальная защита околоплодных вод возрастает. В этот период в воспалительной реакции тканей плода преобладает роль экссудативного компонента, когда в ответ на проникновение инфекции развиваются воспалительные лейкоцитарные реакции у плода (энцефалит, гепатит, пневмония, интерстициальный нефрит) [22].
Особенно опасным при ВУИ во II и III триместрах беременности является повреждение мозга плода, что может приводить к умственной отсталости, задержке психомоторного развития детей [3, 7]. Внутриутробное поражение возбудителями инфекции структур ЦНС у плода сопровождается различными тяжелыми нарушениями в формировании мозга (гидроцефалия, субэпендимальные кисты, кистозная дегенерация вещества мозга, аномалии развития коры, микроцефалия). Возможно также развитие вентрикулита (деформация сосудистого сплетения, неоднородность или удвоение отражения от эпендимы желудочков) [11].
Таким образом, инфицирование плода в более поздние сроки беременности не приводит, как правило, к формированию грубых пороков развития, но может нарушать функциональные механизмы дифференцировки клеток и тканей [10, 11, 13].
Изменения состояния плода и функционирования фетоплацентарной системы, вызванные внутриутробным инфицированием плода, отражаются на составе и свойствах амниотической жидкости [1, 9, 26, 30]. При попадании в амниотическую жидкость инфекционного агента происходит его беспрепятственное размножение с последующим развитием хориоамнионита [1, 9]. Плод оказывается в инфицированной среде, что создает благоприятные условия для заражения плода контактным путем, т.е. через кожу, слизистые оболочки, респираторный и желудочно-кишечный тракты.
1. При заглатывании и аспирации инфицированных вод у новорожденного появляются признаки внутриутробной инфекции (пневмония, энтероколит, везикулез, омфалит, конъюнктивит и др.).
3. Многоводие при внутриутробном инфицировании обычно носит вторичный характер и служит проявлением поражения почек или мочевыводящих путей плода. Причиной его развития является и изменение соотношения процессов продукции и резорбции околоплодных вод клетками амниотического эпителия на фоне амнионита.
4. В генезе симптомокомплекса плацентарной недостаточности при ВУИ основная роль принадлежит сосудистым расстройствам.
5. Типичным проявлением внутриутробного инфицирования служат невынашивание беременности и преждевременные роды [24]. Преждевременное развитие родовой деятельности и несвоевременный разрыв плодных оболочек обусловлены действием бактериальных фосфолипаз, запускающих простагландиновый каскад, и повреждающим действием воспалительных токсинов на плодные оболочки.
6. В связи с тем что фосфолипазы грамотрицательных бактерий способствуют разрушению сурфактанта в легких плода, у новорожденного развиваются респираторные расстройства.
В современной литературе [4, 9, 29] имеется немало работ, посвященных изучению взаимосвязи иммунологических показателей и тяжести инфекционно-воспалительного процесса во время беременности. Все чаще в зарубежной и отечественной литературе появляются данные о взаимосвязи бактериальной инвазии и синтеза цитокинов клетками амниона, хориона, децидуальной и плодовыми тканями [5, 29]. Размножение микроорганизмов в амниотической жидкости приводит к повышению уровня липополисахаридов, которые активируют синтез цитокинов клетками фетального трофобласта. Перспективным при ВУИ представляется изучение изменений в системе цитокинов, которая обеспечивает процессы межклеточной кооперации, роста и дифференцировки лимфоидных клеток, гемопоэза и нейроиммуноэндокринных взаимодействий. Цитокины в предымплантационном периоде и в ходе развития беременности активно продуцируются множеством материнских и эмбриональных клеток, в частности, децидуальными клетками матки и клетками трофобласта. При этом установлено, что клеточные культуры обладают неодинаковой способностью к синтезу цитокинов под влиянием липополисахаридов. Так, фактор некроза опухоли (ФНО) продуцируется клетками амниона, интерлейкины (ИЛ)-6 и ИЛ-8 - амнионом и хорионом, а ИЛ-1 продуцируется только хорионом [9, 11, 28]. По данным Н.В. Орджоникидзе [14], из множества провоспалительных (ИЛ-1, ИЛ-2, ИЛ-6, ИЛ-8, ИЛ-15, ФНО и др.) и противовоспалительных (ИЛ-4, ИЛ-10, ИЛ-13, трансформирующий фактор роста и др.) цитокинов основными маркерами воспалительного процесса в тканях и органах человека считают ИЛ-1, ИЛ-6, ИЛ-10, ФНО [9, 16, 28].
Клиническая характеристика внутриутробной инфекции
В предымплантационный период под воздействием инфекционного агента зародыш гибнет (альтеративное воспаление) или продолжает развиваться.
Инфекционное повреждение эмбриона на 3-12-й неделе обычно связано с вирусной инфекцией, свободно проникающей через хорион. Плод еще не имеет систем противоинфекционной защиты, и в период органогенеза, плацентации ВУИ приводит к формированию пороков развития (тератогенный) или гибели эмбриона (эмбриотоксический эффект) [5, 23].
Инфекционные фетопатии возникают с 16-27-й недели гестации, когда происходит генерализация инфекции у плода, формирование псевдопороков (фиброэластоз миокарда, поликистоз легких, гидроцефалия, гидронефроз). При заражении после 28 нед плод приобретает способность к специфической локальной реакции на внедрение возбудителя, в результате возможны ВУИ (энцефалит, пневмония, гепатит, интерстициальный нефрит), недонашивание беременности, задержка внутриутробного развития, гибель плода [2, 3, 10].
В настоящее время выделяют следующие типы внутриутробных поражений при ВУИ [20, 21]:
- бластопатия - при сроке гестации 0-14 дней; возможны гибель эмбриона, самопроизвольный выкидыш или формирование системной патологии, сходной с генетическими заболеваниями;
- эмбриопатия - при сроке 15-75 дней; характерны пороки развития на органном или клеточном уровнях (истинные пороки), самопроизвольный выкидыш;
- ранняя фетопатия - при сроке 76-180 дней; характерно развитие генерализованной воспалительной реакции с преобладанием альтеративного и экссудативного компонентов и исходом в фиброзно-склеротические деформации органов (ложные пороки), прерывание беременности;
- поздняя фетопатия - при сроке 181 день до родов; возможно развитие манифестной воспалительной реакции с поражением различных органов и систем (гепатит, энцефалит, тромбоцитопения, пневмония).
ВУИ часто не имеет ярких клинических проявлений [4, 10, 15, 17]. Редко первые признаки у новорожденного имеются сразу после рождения, чаще проявляются в течение первых 3 сут жизни. При инфицировании в постнатальном периоде симптомы инфекционного процесса выявляются в более поздние сроки. Клинические появления врожденного бактериального или микотического поражения кожи у новорожденного могут иметь характер везикуло-пустулеза [4]. Конъюнктивит, ринит и отит, появившиеся на 1-3-е сутки жизни, также могут быть проявлениями ВУИ. Врожденная аспирационная пневмония может проявиться и на 2-3-й день жизни. С момента рождения у детей наблюдаются признаки дыхательной недостаточности: одышка, цианоз, часто притупление перкуторного звука и мелкопузырчатые влажные хрипы. Течение внутриутробной пневмонии тяжелое, поскольку в результате аспирации выключаются из дыхания обширные участки легкого (нижняя и средняя доли) вследствие обтурации бронхов инфицированными околоплодными водами, содержащими примесь мекония, чешуек кожи плода. Энтероколит у новорожденных возникает в результате проникновения возбудителя вместе с околоплодными водами в желудочно-кишечный тракт. Диспепсические явления обычно развиваются на 2-3-е сутки жизни. Характерны вялое сосание, срыгивание, вздутие кишечника, гепатоспленомегалия, расширение венозной сети передней брюшной стенки, частый жидкий стул. При микробиологическом исследовании кишечного содержимого преобладание клебсиелл, протея и синегнойной палочки. Поражение ЦНС при ВУИ у новорожденных может быть как первичным (менингит, энцефалит), так и вторичным, обусловленным интоксикацией. При поражении сосудистых сплетений боковых желудочков мозга развивается врожденная гидроцефалия. Необходимо уделять внимание таким симптомам, как вялость, плохое сосание, срыгивание, замедленное восстановление или вторичное снижение массы тела, задержка заживления пупочной ранки, развитие омфалита. Типичными симптомами инфекционной интоксикации у новорожденного являются нарушения дыхания и тканевого метаболизма. Отмечается бледно-цианотичная окраска кожных покровов с выраженным сосудистым рисунком. Интоксикация сопровождается нарушением экскреторной функции печени и почек, увеличением селезенки и периферических лимфоузлов.
Современные методы диагностики внутриутробных инфекций
Превалирование ВУИ среди причин неблагоприятных исходов, высокий уровень инфицированности у беременных и родильниц обусловливают необходимость поиска достоверных методов ее диагностики. Неспецифичность клинических проявлений ВУИ создает диагностические трудности, что диктует необходимость сочетанного применения клинических и лабораторных методов исследования. В последнее десятилетие основными методами диагностики ВУИ являются бактериологические и иммунологические [10, 11, 21].
Можно выделить 3 этапа в диагностике внутриутробного инфицирования: 1) диагностика во время беременности; 2) ранняя диагностика в момент рождения ребенка; 3) диагностика при развитии клинических признаков инфекции в раннем неонатальном периоде [12].
Любые изменения гомеостаза в организме матери находят свое отражение в клеточных и химических показателях амниотической жидкости, которые очень тонко характеризуют течение патологического процесса, в связи с чем амниотическая жидкость может служить важным диагностическим материалом [1, 6, 16]. По мнению И.В. Бахаревой [1], наиболее значимым в диагностике ВУИ является определение антимикробной активности амниотической жидкости, основанной на миграции в ней лейкоцитов при скоплении в околоплодной оболочке бактерий, превышающем 103 КОЕ/мл. Появление в околоплодных водах большого числа лейкоцитов, увеличение цитоза за счет эпителиоцитов без обнаружения микрофлоры могут свидетельствовать о ВУИ.
В настоящее время большое значение придается ультразвуковым методам исследования, с помощью которых можно определить косвенные признаки ВУИ плода (многоводие, вентрикуломегалия, микроцефалия, гепатомегалия, увеличение толщины плаценты, мелкодисперсная взвесь в околоплодных водах) и структурные изменения в различных органах [4, 11, 18, 26].
Нами был разработан необходимый перечень диагностических мероприятий с целью раннего выявления ВУИ [19].
В комплекс обследования беременных женщин вошли:
1. Общеклинический и биохимический анализы крови и мочи с определением стандартных показателей.
2. Определение возбудителей TORCH-комплекса с помощью ПЦР в вагинальных мазках, околоплодных водах.
3. Определение антител в крови к хламидиям, микоплазмам и уреаплазмам, ЦМВ и ВПГ методом ИФА.
4. Проведение аминного теста, pH-метрии влагалищного содержимого.
5. Бактериоскопическое исследование содержимого влагалища, цервикального канала и уретры.
6. Бактериологическое исследование материнской поверхности плаценты, околоплодных вод, содержимого кишечника.
7. Определение уровня провоспалительных (ИЛ-1β, ФНО) и противовоспалительного (ИЛ-10) цитокина в околоплодных водах, сыворотках венозной крови матери и пуповинной крови плода.
8. Ультразвуковое сканирование плода, околоплодных вод и плаценты.
9. Гистоморфологическое исследование плаценты.
В комплекс обследования новорожденных вошли:
1. Оценка по шкале Апгар, измерение массы тела и длины при рождении, динамика нарастания массы тела до выписки из родильного дома.
2. Определение антител в крови к хламидиям, микоплазмам и уреаплазмам, ЦМВ и ВПГ методом ИФА.
3. Бактериологическое исследование соскобов с конъюнктивы, задней стенки глотки и вульвы.
4. Выявление клинических признаков ВУИ совместно с врачом-неонатологом.
Комплексное исследование видового состава микроорганизмов родовых путей, околоплодных вод, плаценты, новорожденного, определение антигенов и антител к предполагаемому возбудителю в пуповинной крови и амниотической жидкости, гистологическое исследование последа позволяют определить путь инфицирования ребенка, природу возбудителя и уточнить объем дополнительных диагностических исследований при ВУИ, а также определить лечебно-профилактические мероприятия в раннем неонатальном периоде.
М.А. Башмакова - д-р мед. наук, профессор, ведущий научный сотрудник Института акушерства и гинекологии им. Д.О. Отта РАМН
Т.А. Плужникова - ведущий сотрудник Санкт-Петербургского городского научно-практического центра профилактики, диагностики и лечения невынашивания беременности, канд. мед. наук
Одной из наиболее частых причин невынашивания беременности (НБ) является урогенитальная инфекция (УГИ). Она вызывает большой процент осложнений беременности (гестоз, угроза прерывания беременности, многоводие, пиелонефрит беременных, плацентарная недостаточность, преждевременная отслойка плаценты и др.), внутриутробные поражения плода и новорожденного.
Наступление беременности сопровождается изменением иммунного статуса женщины. Развивается иммунодефицит, который при угрозе прерывания и невынашивании беременности усугубляется. Поэтому подверженность беременной женщины инфекционным заболеваниям очень велика. Кроме того, при беременности часто обостряются заболевания, протекающие латентно (хронический тонзиллит, пиелонефрит и др.). Это увеличивает частоту осложнений беременности и родов, неблагоприятных исходов для плода и новорожденного.
Во влагалище здоровой небеременной женщины в норме присутствуют аэробные и анаэробные микроорганизмы: лактобациллы, коринебактерии, эпидермальный стафилококк, бактероиды, молочнокислые стрептококки и др. У здоровых беременных уже в I триместре беременности происходит снижение численности их видов и количества: число коринебактерии, бактероидов, стрептококков, стафилококков уменьшается, а количество лактобацилл и бифидобактерий повышается (Е.Ф. Кира, Ю.В. Цвелен, И.А. Симчера, 1998).
Особенностью возбудителей генитальных инфекций являются их частые ассоциации. Так, генитальные микоплазмы обнаруживаются вместе с условнопатогенной флорой, грибами рода Candida, трихомонадами, гонококками; хламидии - с гонококками, вирусом генитального герпеса, стрептококками группы В.
Клиника
Оценка роли бессимптомной инфекции и колонизации мочеполовых органов разнообразными микроорганизмами, равно как и манифестной инфекции гениталий, показала, что в основе части неразвивающихся беременностей, самопроизвольных выкидышей, преждевременных родов лежит инфекционный процесс очагового характера в эндометрии и шейке матки - хламидии, микоплазмы, либо в мочеполовых органах - стрептококки группы В, грамотрицательная флора.
При беременности часто встречается бактериальный вагиноз и урогенитальный кандидоз (УГК), которые могут стать причиной осложнения течения беременности и явиться причиной ее невынашивания.
Так как термин "бактериальный вагиноз" официально принят в мире и 1984 г., а в России признан в 1990 году, остановимся более подробно на характеристике этого заболевания.
Бактериальный вагиноз (БВ) - это полимикробное инфекционное заболевание, обсуловленное уменьшением или исчезновением лактобацилл и увеличением в 100-1000 раз численности анаэробов и др. микробов. Его этиологическим фактором выступают ассоциации анаэробных микроорганизмов (Е.Ф. Кира). Возможно присутствие гарднерелл. В настоящее время очень остро стоит вопрос о заболеваниях, передающихся половым путем (ЗППП). Среди 20 возбудителей этой группы заболеваний наиболее часто причиной невынашивания беременности являются:
- генитальные микоплазмы,
- стрептококки группы В,
- хламидии,
- простой генитальный вирус II типа,
- цитомегаловирус (ЦМВ).
Колонизация или инфекция гениталий беременной женщины, вызванная микоплазмами (Ureaplasma urealyticum, Mycoplasma hominis, Mycoplasma genitalium), часто не проходит бесследно. Частота обнаружения М. hominis у беременных женщин на протяжении многих лет остается примерно одинаковой и составляет 17-20%. Частота встречаемости U. urealyticum у беременных женщин - 25-30%. Чаще колонизация влагалища микоплазмами наблюдается при изменениях его биоценоза в сторону нарастания представителей потенциально патогенных микроорганизмов. Всегда ли генитальные микоплазмы вызывают патологические процессы в организме беременных? Всегда ли приводят к невынашиванию беременности? - На сегодняшний день эти вопросы выяснены не окончательно.
У беременных женщин с угрозой невынашивания беременности в 4.8% случаев с мочой выделяются стрептококки группы В (СГВ). Длительное время (по нашим данным, до 3 лет - С.Л. Зацнорская, 1995) эти микроорганизмы могут персистировать в урогенитальном тракте женщины. При повторных беременностях возможно инфицирование плодного яйца тем же серотипом, которое может стать причиной неразвивающейся беременности или септического аборта. Передача стрептококков группы В от матери плоду наблюдается в 37.0% случаев. Как известно, в настоящее время генитальный хламидиоз часто встречается у женщин в период их репродуктивного пика - в возрасте от 20 до 30 лет и даже моложе.
Глубокие гормональные сдвиги во время беременности, измененная иммунологическая реактивность могут отражаться на клинической картине заболевания, активировать инфекцию, оказывать неблагоприятное влияние на течение, исход беременности, на плод и новорожденного ребенка. Частота встречаемости урогенитального хламидиоза среди беременных женщин, по нашим данным, равна 6.7-8.0%. Передача возбудителя ребенку возможна как при наличии, так и при отсутствии явных клинических проявлений инфекции у матери (вероятность ее передачи - 50-70%). Плод инфицируется как при непосредственном контакте с родовыми путями матери, так и внутриутробно: при заглатывании или аспирации околоплодных вод. Следует особо отметить, что частота перинатальной смертности плода в группе женщин с хламидиозом гениталий составляет 5.45%. В НИИ акушерства и гинекологии им. Д.О. Отта РАМН впервые описаны латентные эндометриты хламидийной этиологии (А.М. Савичева, 1991). Они также могут быть причиной антенатального инфицирования плода, самопроизвольных выкидышей, неразвивающихся беременностей, преждевременных родов. При исследованиях методом электронной микроскопии в ткани плаценты были обнаружены антигены к хламидиям и микоплазмам (Л.Б. Забжицкая, 1998).
В перинаталыюй патологии определенную роль с учетом тяжести последствий внутриутробного инфицирования плода играют вирусы герпетической группы.
Изучение цитомеголовирусной инфекции (ЦМВ) показало, что среди беременных женщин высока частота так называемой иммунной прослойки (92% женщин имеет антитела к ЦМВ). Были установлены группы риска по развитию внутриутробной инфекции среди беременных женщин и их новорожденных. В НИИ акушерства и гинекологии им. Д.О. Отта РАМН впервые дана оценка риска развития внутриутробной цитомегалии у беременных женщин Санкт-Петербурга, равная 0.5-1.0%. По данным литературы, при ЦМВ частота выкидышей достигает 31.5% (Н.А. Фарбер и др., 1990).
В развитии патологических процессов в урогениталиях, приводящих к невынашиванию беременности, существенную роль играют не столько патогенные микроорганизмы, полученные женщиной извне (хламидии, гонококки), сколько условнопатогенные бактерии, населяющие половые органы в норме, что, возможно, обусловлено измененной иммунологической реактивностью во время беременности.
При оценке условнопатогенной микрофлоры у женщин с невынашиванием беременности и при наличии воспалительных заболеваний влагалища выделяются:
- дрожжеподобные грибы рода Candida (в основном Candida albicans) - в 12%,
- стрептококки группы Д - в 31.5%,
- золотистые стафилококки - в 1.5%.
Кроме этого, в некоторых случаях при нарушенных микробиотических процессах во влагалище выделяются кишечные палочки, клебсиеллы, анаэробные микроорганизмы.
Особо следует подчеркнуть тот факт, что во время беременности клетки влагалищного эпителия становятся более эластичными и пролиферируют, выделяя большое количество гликогена. При этом во влагалище увеличивается численность лактобацилл и дрожжеподобных грибов. По мере увеличения срока беременности численность этих микроорганизмов растет. Это положение имеет огромное значение при назначении этиотропной противомикотической терапии. В норме у 40-60% беременных во влагалище находят дрожжеподобные грибы. Лишь при наличии мицелия и вегетирующих форм дрожжеподобных грибов при соответствующей клинической картине заболевания должны назначаться противогрибковые препараты.
При урогенитальной инфекции высока частота осложнений беременности, особенно невынашивания беременности (табл. 1).
Таблица 1
ОСОБЕННОСТИ ТЕЧЕНИЯ БЕРЕМЕННОСТИ ПРИ УРОГЕНИТАЛЬНОЙ КОЛОНИЗАЦИИ ИНФЕКЦИИ (по данным НИИ акушерства и гинекологии им. Д.О. Отта)
| ХАРАКТЕР ОСЛОЖНЕНИЙ | МИКОПЛАЗМА (%) | УРЕАПЛАЗМА (%) | ХЛАМИДИИ (%) | КАНДИДА (%) | СТРЕПТОКОККИ В (%) | БАКТЕРИАЛЬНЫЙ ВАГИНОЗ (%) |
| Угроза прерывания беременности | 66.0 | 67.5 | 31.7 | 48.0 | 32.1 | 58.0 |
| Неразвивающаяся беременность | 8.0 | 1.2 | 0.9 | - | 3.2 | 8.0 |
| Спонтанные аборты | 9.4 | 6.2 | 11.0 | 3.5 | 31.1 | 8.0 |
| Преждевременные роды | 16.0 | 8.8 | 12.7 | 13.5 | 24.7 | 13.8 |
| Многоводие | 17.0 | 12.5 | 8.2 | 10.0 | 8.7 | 18.1 |
| Пиелонефрит беременных | 21.4 | 7.0 | 8.2 | - | 29.7 | - |
| Гестоз | 49.0 | 23.7 | 47.3 | 17.0 | 72.4 | - |
| Несвоевременное излитие околоплодных вод | 39.0 | 12.5 | 27.7 | 21.0 | 44.1 | 48.7 |
При поражении эндометрия возбудителями инфекции нарушается процесс плацентации и развития последа, что способствует развитию вторичной плацентарной недостаточности. Они могут поражать плаценту (плацентит) и оболочки (хорионамнионит), вызывать образование патогенных иммунных комплексов, что существенно нарушает функцию последа как органа, обеспечивающего плоду адекватное питание и дыхание, что в свою очередь приводит к задержке развития и гипотрофии плода, и преждевременному возбуждению родовой деятельности.
При наличии урогенитальной инфекции роды часто осложняются несвоевременным отхождением околоплодных вод (НОВ), аномалией родовой деятельности, лихорадкой в родах, гипоксией внутриутробного плода. Особенно высок процент НОВ при обнаружении в моче грамотрицательной флоры или генитальной инфекции (в 3-4 раза выше, чем у здоровых рожениц). НОВ способствует возникновению амниотической инфекции и развитию хорионамнионита. Это оказывает неблагоприятное воздействие не только на мать, но и на плод. В родах нередко развивается слабость родовой деятельности (при микоплазменной инфекции) или быстрые роды - при стрептококках группы В.
Большое значение в исходе беременности и родов для плода и новорожденного при инфекционных заболеваниях матери имеет лечение беременной и роженицы, а также способ родоразрешения.
Лечение урогенитальной инфекции
Урогенитальная инфекция является одной из главных причин невынашивания беременности. Поэтому при планировании беременности необходимо комплексное всестороннее обследование будущих родителей для выявления явных и скрытых очагов инфекции, характера возбудителя и проведения этиотропной терапии.
При наступлении беременности у женщин из группы риска по невынашиванию беременности следует осуществить комплексное микробиологическое обследование и при обнаружении УГИ провести соответствующее лечение.
Лечение инфекционных заболеваний у беременных должно быть комплексным с индивидуальным подходом к каждой больной. Оно включает антибактериальную и десенсибилизирующую общеукрепляющую терапию, мероприятия, направленные на повышение иммунологической реактивности беременной, нормализацию функции печени, профилактику и лечение осложнений беременности и родов, профилактику внутриутробного инфицирования плода, его гипоксии и гипотрофии.
Антибактериальная терапия проводится с учетом характера возбудителя и его чувствительности к препарату, фармакокинетики применяемых средств, срока беременности в момент лечения и состояния внутриутробного плода. Обязательно назначение эубиотиков (табл. 2 и 3).
Таблица 2
АНТИБАКТЕРИАЛЬНЫЕ И ПРОТИВОВИРУСНЫЕ ПРЕПАРАТЫ, ПРИМЕНЯЕМЫЕ ПРИ БЕРЕМЕННОСТИ
| МИКРООРГАНИЗМЫ | НИСТАТИН | ПИМАФУЦИН | ЭРИТРОМИЦИН | СУМАМЕД | ВИЛЬПРАФЕН | РОВАМИЦИН | РУЛИД | МАКРОПЕН | КЛАЦИД | АМПИЦИЛЛИН | БЕНЗИЛПЕНИЦИЛЛИН | ОКСАЦИЛЛИН | ГЕНТАМИЦИН | ЦЕФАЛОСПОРИНЫ | ЛИНКОМИЦИН | СУЛЬФАДИМЕЗИН | ЭТАЗОЛ | НИТРОФУРАНЫ | НИТРОКСОЛИН | МЕТРОНИДАЗОЛ | НАЛИДИКСОВАЯ КИСЛОТА | АЦИКЛОВИР |
| Анаэробы | + | + | + | + | + | + | ||||||||||||||||
| Гарднереллы | + | + | + | + | ||||||||||||||||||
| Трихомонады | + | + | + | |||||||||||||||||||
| М. hominis | + | + | + | |||||||||||||||||||
| U. urealyticum | + | + | + | + | + | + | ||||||||||||||||
| Гонококки | + | + | + | + | + | + | + | + | + | + | + | + | + | |||||||||
| Хламидии | + | + | + | + | + | + | + | + | + | |||||||||||||
| Стрептококки | + | + | + | + | + | + | + | + | + | + | + | + | + | + | + | + | + | |||||
| Кишечная палочка | + | + | + | + | + | + | + | |||||||||||||||
| Стафилококки | + | + | + | + | + | + | + | + | + | + | + | |||||||||||
| Candida | + | + | ||||||||||||||||||||
| Клебсиеллы | + | + | + | + | + | |||||||||||||||||
| V. herpes | + |
При назначении лечения женщинам с УГИ половые партнеры подлежат обследованию и лечению. Рекомендуется воздержание от половой жизни до излечения.
Что такое антенатальная гибель плода? Причины возникновения, диагностику и методы лечения разберем в статье доктора Кондратенко Юлии Николаевны, гинеколога со стажем в 17 лет.
Над статьей доктора Кондратенко Юлии Николаевны работали литературный редактор Маргарита Тихонова , научный редактор Светлана Симанина и шеф-редактор Лада Родчанина

Определение болезни. Причины заболевания
Антенатальная гибель плода — это внутриутробная смерть плода, наступившая до начала родов, но после 21 недели беременности. Является причиной 39-42 % мертворождений. У таких детей отсутствует сердцебиение, дыхание, движения и пульсация сосудов пуповины [12] .
Согласно первым комплексным оценкам, каждый год на свет появляется более 7200 мертворождённых детей. Даже в высокоразвитых странах Европы и Северной Америки показатель мертворождения не опускается ниже 1,3 % [9] . Уровень мертворождения в России в 2018 году был равен 5,51 %. При этом доля антенатальной гибели плода составила 91,8 %. Однако за последние пять лет показатель перинатальной смертности (гибели ребёнка до и после родов) стал снижаться [13] .
Чаще внутриутробная гибель плода наблюдается у девочек-подростков в силу незрелости организма, а также у беременных 35 лет и старше. К этому возрасту у женщины , как правило, возникает ряд хронических заболеваний, снижается овариальный резерв — запас фолликулов в яичниках. Всё это является риском неразвивающейся беременности по причине хромосомной патологии плода.
Также риск антенатальной потери выше у женщин с более чем двумя родами в анамнезе, привычным невынашиванием беременности , искусственными абортами, многоплодными беременностями, наличием послеоперационного рубца на матке и при экстракорпоральном оплодотворении (ЭКО) [23] .
Существует множество причин внутриутробной гибели плода. Они могут быть как со стороны самого плода, так и стороны матери [8] .
Непосредственной причиной смерти является дистресс-синдром плода . Он подразумевает под собой все нарушения функционального состояния плода, в первую очередь, его движений и сердцебиения.
Опосредованные причины антенатальной гибели плода :
- Врождённые аномалии развития плода — синдром Дауна, синдром Патау, синдром Эдвардса и др. . Чаще всего это происходит при:
- инвазивной диагностике и лечении беременной — амниоцентезе (во время удаления излишков околоплодных вод, введения лекарств или пункции амниотической оболочки), пунктировании сосудов пуповины и др.;
- нарушении стерильности во время введения препаратов крови внутрь матки через сосуды пуповины (например, при переливании эритроцитарной массы плоду с гемолитической болезнью);
- преждевременном разрыве околоплодных оболочек в случае пролонгированной беременности;
- общих инфекциях беременной — TORCH-инфекциях, сифилисе , туберкулёзе, урогенитальном хламидиозе и ВИЧ-инфекции[13] .
- Экстрагенитальные заболевания матери — сахарный диабет, нарушения работы щитовидной железы, почек и надпочечников, травмы, злоупотребление алкоголем и курение , особенно при наличии воспалений урогенитального тракта.
- Особенности течения беременности :
- различные формы позднего токсикоза;
- угроза прерывания беременности;
- истмико-цервикальная и фетоплацентарная недостаточность ;
- инфекционные заболевания;
- нарушение кровотока в матке и плаценте;
- тазовое предлежании плода.
- Неустановленные причины .
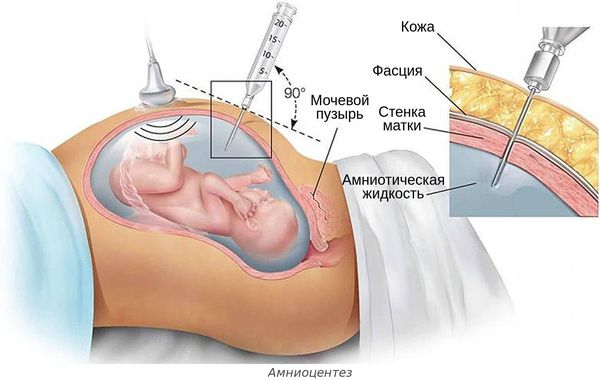
Инфекция может быть вирусной (цитомегаловирусы, вирусы простого герпеса, краснухи, Коксаки, ВИЧ), бактериальной (хламидии, микоплазмы, уреаплазмы, стрептококки группы В, энтеробактерии, кишечная палочка) и грибковой (кандидоз).
При обнаружении схожих симптомов проконсультируйтесь у врача. Не занимайтесь самолечением - это опасно для вашего здоровья!
Симптомы антенатальной гибели плода
Процесс внутриутробной гибели плода далеко не всегда может сопровождаться изменениями в самочувствии женщины. Иногда беременная отмечает более частые шевеления плода, но позже происходит их полное прекращение. Это говорит об острой гипоксии плода — снижении содержания кислорода в организме [2] . Однако часто гибель малыша наступает незаметно для матери и врача, что приводит к поздней диагностике антенатальной смерти плода [4] .
В течение первых трёх дней гибели малыша пациентка может обратить внимание на изменения своего состояния:
- прекращаются шевеления плода;
- уменьшается размер молочных желёз, снижается их напряжение;
- живот перестаёт увеличиваться в объёме;
- возникает слабость, недомогание, тяжесть внизу живота.
Если с момента гибели плода в утробе матери прошло несколько недель, могут присоединяться признаки воспалительной реакции:
- повышение температуры до 38 ℃;
- сильные тянущие боли внизу живота;
- головная боль и головокружение;
- сонливость;
- нарушение сознания [16] .
Патогенез антенатальной гибели плода
Несмотря на то, что внутриутробная гибель плода является общемировой проблемой, вопросы её патогенеза остаются нерешёнными [5] [14] [21] [25] . В связи с этим проводится множество исследований, в частности исследования плаценты — предполагается, что её изменения являются основной или одной из главных причин смерти плода. Установить фактическую причину при аутопсии (вскрытии) мертворождённого довольно трудно [3] [6] [15] [22] [24] .
Суть патогенеза заключается в нарушении функции плаценты, развитии хронической плацентарной недостаточности, нарушении кровоснабжения плода, его росте и развитии. Поражаются внутренние органы плода — развивается внутриутробная пневмония, менингит и др. В какой-то момент происходит нарушение нормального функционирования плаценты, развивается острая плацентарная недостаточность и плод погибает.
Профессором И. В. Бариновой в 2015 году были представлены два типа плодовых потерь при внутриутробной гипоксии. Каждому из них характерно своеобразное сочетание патогенетических факторов, связанных с матерью, плацентой и плодом.
Патогенез первого типа отличается комплексом таких признаков, как ранняя тяжёлая преэклампсия и васкулопатия, т. е. патологическое изменение сосудов базальной пластинки плаценты (неполноценная перестройка спиральных артерий, необходимая для улучшения кровоснабжения плода, острый атероз, тромбоз и кровотечения). Всё это нарушает циркуляцию материнской крови в плаценте [1] .
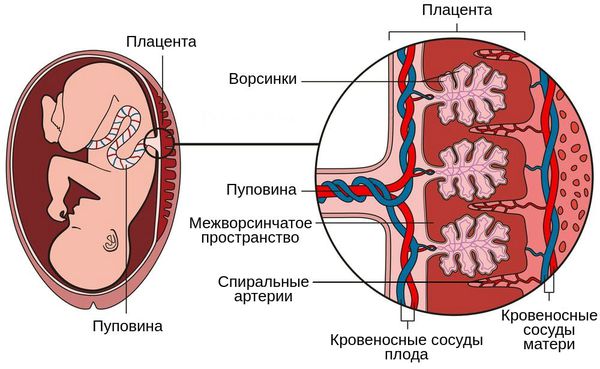
Патогенез второго типа обусловлен нарушением циркуляции в плодовой части плаценты, незрелостью ворсин относительно срока беременности, а также васкулопатией сосудов плода и тромбозом ворсин.
Эти основные звенья патогенеза антенатальной гибели позволяют своевременно профилактировать и назначать патогенетическую терапию фетоплацентарной недостаточности [1] .
Классификация и стадии развития антенатальной гибели плода
Пока не существует общепринятой классификации внутриутробной гибели плода. Однако изучение причин перинатальной смертности привело к появлению двух понятий:
- "Необъяснимое" мертворождение — внезапная гибель малыша наступает по неизвестным причинам. Установить их можно только после анатомического вскрытия плода и исследования плаценты. Зачастую выявляются аномалии опорно-двигательной и нервной системы, несовместимые с жизнью, а также поражения сердечно-сосудистой системы, в частности фатальная аритмия — нарушение сердечного ритма.
- Мертворождение, связанное с задержкой роста плода — гибель плода обусловлена нарушениями обмена веществ, поступления кислорода и кровоснабжения плода из-за материнских факторов, а также факторов, связанных с плодом и плацентой [8] .
Полноценное гистологическое исследование внутриутробно погибшего плода необходимо для установления причины его смерти. Некоторые матери отказываются от него, но это неправильно. Дело в том, что у многих женщин с гибелью плода в анамнезе повышается риск повторных потерь при следующих беременностях [26] . Поэтому исследование причин мертворождения позволит предотвратить повторение этой трагедии в будущем.
Осложнения антенатальной гибели плода
При своевременном обращении к доктору антенатальная гибель плода не приводит к осложнениям. Если же пациентка обратилась за медицинской помощью спустя больше двух недель после смерти ребёнка, то у неё с большой вероятностью могут развиваться такие осложнения, как:
- Кровотечение во время и после родов.
- Гнойно-септические осложнения:
- хориоамнионит — воспаление стенок плодного пузыря и заражение инфекцией околоплодных вод;
- послеродовой метроэндометрит — воспаление мышечной и слизистой оболочки стенки матки;
- инфекции послеоперационной раны — может возникнуть, если роды проходили путём кесарева сечения, например, при раннем отделении плаценты;
- послеродовой сепсис — заражение крови.
Чтобы избежать их, необходимо тщательно наблюдать за состоянием пациентки и выполнять профилактические мероприятия:
- плановое проведение родов при высоком риске кровотечения;
- профилактика анемии ;
- гемостатическая терапия;
- пережатие пуповины ребёнка не раньше первой минуты после рождения;
- строгое соблюдение стерильности при выполнении кесарева сечения и вагинальных исследований во время родов;
- использование индивидуальных комплектов при родоразрешении;
- отказ от катетеризации мочевого пузыря и эпизиотомии (рассечения задней стенки влагалища) без явной необходимости;
- профилактический приём антибиотиков после выполнения инвазивной диагностики или при длительном безводном периоде;
- ранняя выписка из родильного дома (на третьи сутки после родов) [16] .
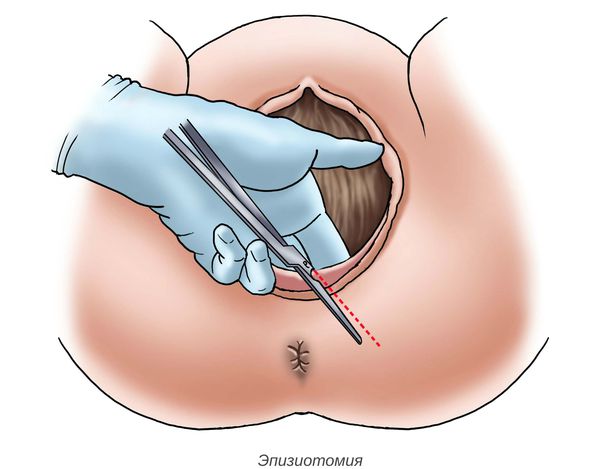
Антенатальная гибель плода является серьёзным состоянием при многоплодной беременности . В случае дихориальной беременности (когда малыши развиваются независимо друг от друга: каждый имеет свои жизненно важные структуры — плодный мешок и плаценту) гибель близнеца не влияет на другого ребёнка. При монохориальной беременности (когда у малышей одна плацента на двоих) риски повреждения второго плода существенно выше:
- в 12 % случаев происходит гибель второго ребёнка;
- в 18 % случаев у него диагностируются неврологические нарушения.
В связи с этим рекомендован контроль показателей эхокардиографии (УЗИ сердца), оценка мозгового кровотока (УЗИ головного мозга) и МРТ выжившего плода [18] .
Помимо прочих осложнений у женщины может возникнуть депрессия , тревожное и посттравматическое расстройство на почве пережитой трагедии или чувства вины. У неё может развиться страх перед будущей беременностью, желание избежать её [26] . В этих случаях пациентке требуется психотерапевтическая помощь.
Диагностика антенатальной гибели плода
После того как женщина обращается к врачу с жалобами на недомогание и отсутствие шевеления плода, врач направляет пациентку на диагностическое обследование. Оно позволяет поставить точный диагноз.
Постановка диагноза внутриутробной гибели плода включает следующие этапы обследования:
- Выслушивание сердечных сокращений плода специальным стетоскопом. Обычным медицинским стетоскопом в данном случае услышать сердцебиение невозможно. Для этого существует деревянный акушерский стетоскоп. Он отличается широкой воронкой, которая плотно прикладывается к животу беременной.
- Выслушивание сердечных сокращений фетальным аудиодопплером и/или монитором . Фетальный допплер можно использовать даже в домашних условиях, начиная с 12-ой недели беременности. Для этого женщине нужно лечь на спину и для чёткого сигнала нанести гель на те участки живота, которые будут соприкасаться с датчиком. Сам допплер нужно передвигать медленно, без резких движений. Длительность исследования — 3-7 минут.
- Ультразвуковое исследование плода (УЗИ). Этот метод является одним из самых достоверных для диагностики внутриутробной гибели плода. С его помощью доктор констатирует отсутствие сердцебиения у малыша [16] .

Анализы для диагностики внутриутробной гибели плода на позднем сроке беременности не так важны. Отсутствия шевелений плода в течение нескольких дней и сердцебиения по данным УЗИ достаточно для правильной постановки диагноза.
Лечение антенатальной гибели плода
При подтверждённом диагнозе антенатальной гибели плода показана экстренная госпитализация и принятие решения о методе и сроке родоразрешения. Чем меньше интервал между установленным диагнозом и родоразрешением, тем меньше риск возникновения осложнений во время и после родов.
Выбор метода определяется индивидуально, на основании клинических данных и особенностей акушерской ситуации. Оптимальным вариантом родоразрешения при антенатальной гибели плода являются роды через родовые пути. Но иногда выполняется кесарево сечение, например при раннем отделении плаценты от стенок матки, обильном или продолжающемся кровотечении из половых путей.
При родоразрешении беременных с антенатальной гибелью плода, осложнившейся септическим состоянием, показано экстренное оперативное вмешательство. Объём операции решается индивидуально, возможна удаление матки с плодом (экстирпация).
После родов важно тщательно наблюдать за состоянием роженицы, провести профилактику послеродового кровотечения и гнойно-септических осложнений. Необходимо обратить внимание на выделения из половых путей (гнойные или кровянистые ), температуру тела, появление озноба, слабости, тянущих болей внизу живота.
Во всех случаях внутриутробной гибели плода показано патологоанатомическое исследование плода и последа (его оболочки). Отказ от исследования по желанию родственников оформляется в соответствии с нормами действующего законодательства [19] .
Самым тяжёлым остаётся вопрос о том, когда же произошла гибель плода. Раньше считалось, что в основе определения времени гибели лежит оценка выраженности процессов мацерации — размягчения и разрыхления тканей плода [20] . Однако наличие признаков мацерации не всегда позволяет достоверно судить о давности наступления гибели, т. к. время её развития зависит от причин гибели малыша.
Прогноз. Профилактика
Потеря беременности является показанием к проведению медицинской, психологической и социальной реабилитации пациенток. Необходим полный комплекс диагностических исследований для выяснения причины гибели плода. Выбор алгоритма обследования базируется на данных анамнеза, особенностях течения беременности и результатах патологоанатомического исследования плода и последа.
Женщины с внутриутробной гибелью плода в анамнезе входят в группу риска данного осложнения при последующих беременностях. Поэтому наступление беременности у таких пациенток требует выполнения комплекса мероприятий по подготовке организма женщины к полноценному зачатию, вынашиванию и рождению здорового ребёнка [10] . Оптимальный интервал между беременностями должен составлять не менее 6 месяцев, чтобы минимизировать потенциальные сложности течения последующей беременности [26] .
При неустановленной причине гибели плода в анамнезе необходимо учитывать данный факт при выработке тактики родоразрешения последующих беременностей.
Профилактика антенатальной гибели плода предполагает:
- ведение здорового образа жизни;
- диагностику и адекватное лечение соматических и хронических инфекционных заболеваний;
- своевременное выявление генетической патологии;
- лечение высокого артериального давления;
- контроль уровня глюкозы в крови при сахарном диабете [26] ;
- предупреждение травм живота;
- прекращение контакта с бытовыми токсичными веществами;
- ликвидацию профессиональных вредностей (переход на другую работу);
- адекватное назначение лекарств в период беременности;
- приём фолиевой кислоты до зачатия;
- комплексное антенатальное наблюдение за состоянием плода [7] ;
- регистрацию шевелений плода на 28 неделе беременности;
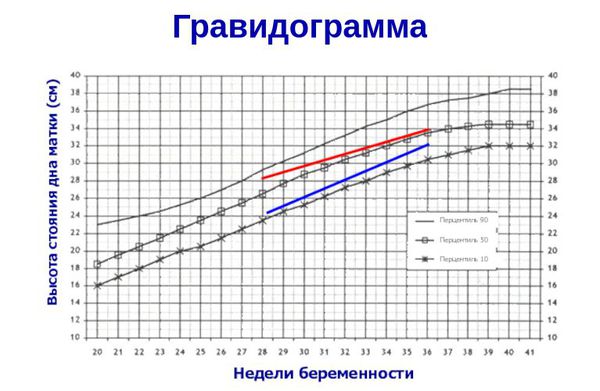
- ведение гравидограммы с 24 недели беременности (сводной таблицы данных, регистрирующей динамику течения беременности) — повышает качество диагностики задержки развития плода и снижает риск потери малыша в 1,8 раз [11] .
Курение увеличивает риск перинатальной смертности на 27 % [17] . Однако чаще антенатальная гибель плода наблюдается у беременных, употребляющих алкоголь — в 6,25 % случаев [8] . Поэтому отказ от вредных привычек значительно увеличивает шансы родить здорового ребёнка.
Кафедра акушерства, гинекологии и перинатологии факультета повышения квалификации и последипломной подготовки специалистов Кубанского государственного медицинского университета
Кафедра акушерства, гинекологии и перинатологии факультета повышения квалификации и последипломной подготовки специалистов Кубанского государственного медицинского университета;
Городская больница №2
Краевой перинатальный центр, Краснодар
Кафедра акушерства, гинекологии и перинатологии факультета повышения квалификации и последипломной подготовки специалистов Кубанского государственного медицинского университета
Краевой перинатальный центр, Краснодар
Кафедра акушерства, гинекологии и перинатологии факультета повышения квалификации и последипломной подготовки специалистов Кубанского государственного медицинского университета
Роль инфекции в преждевременном разрыве плодных оболочек
Журнал: Российский вестник акушера-гинеколога. 2012;12(6): 35‑39
Новикова В.А., Пенжоян Г.А., Рыбалка Е.В., Аутлева С.Р., Сикальчук О.И., Асеева Е.В. Роль инфекции в преждевременном разрыве плодных оболочек. Российский вестник акушера-гинеколога. 2012;12(6):35‑39.
Novikova VA, Penzhoian GA, Rybalka EV, Autleva SR, Sikal'chuk OI, Aseeva EV. Role of infection in premature rupture of the membranes. Russian Bulletin of Obstetrician-Gynecologist. 2012;12(6):35‑39. (In Russ.).
Кафедра акушерства, гинекологии и перинатологии факультета повышения квалификации и последипломной подготовки специалистов Кубанского государственного медицинского университета
Кафедра акушерства, гинекологии и перинатологии факультета повышения квалификации и последипломной подготовки специалистов Кубанского государственного медицинского университета
Кафедра акушерства, гинекологии и перинатологии факультета повышения квалификации и последипломной подготовки специалистов Кубанского государственного медицинского университета;
Городская больница №2
Краевой перинатальный центр, Краснодар
Кафедра акушерства, гинекологии и перинатологии факультета повышения квалификации и последипломной подготовки специалистов Кубанского государственного медицинского университета
Краевой перинатальный центр, Краснодар
Кафедра акушерства, гинекологии и перинатологии факультета повышения квалификации и последипломной подготовки специалистов Кубанского государственного медицинского университета
Проблема преждевременных родов считается приоритетной для изучения акушерами-гинекологами и неонатологами, так как, с одной стороны, 60-70% недоношенных детей обусловливают раннюю неонатальную смертность [16], с другой, преждевременные роды являются серьезным фактором риска развития послеродовых гнойно-воспалительных осложнений [14]. Число случаев преждевременных родов составляет 6-10% от всех родов и различается в зависимости от срока беременности: в период с 22 до 28 нед беременности - 5-7% от всех случаев преждевременных родов, в период с 29 до 34 нед беременности - 33-42%, в период с 34 до 37 нед беременности - 50-60% [1]. По механизму возникновения преждевременные роды делятся на самопроизвольные и индуцированные. Факторами риска развития преждевременных родов с преждевременным разрывом плодных оболочек (ПРПО) могут быть: низкое социально-экономическое положение женщины; экстрагенитальные заболевания (артериальная гипертензия, нарушение функции щитовидной железы, заболевания сердца, анемия с уровнем гемоглобина менее 90 г/л и др.); наркомания и курение; профессиональные вредности; наследственность; перенесенная вирусная инфекция; преждевременные роды в анамнезе; истмико-цервикальная недостаточность (ИЦН); пороки развития матки; перерастяжение матки (многоводие, многоплодная беременность, макросомия при сахарном диабете); хирургические операции во время беременности, особенно на органах брюшной полости, или травмы [1].
Динамическое изменение видовой структуры возбудителей заболеваний, формирование устойчивых к антибиотикам штаммов, увеличение иммунокомпетентных лиц среди беременных и родильниц диктуют необходимость периодического пересмотра стратегии и тактики лечения [8]. Разработка и совершенствование методов диагностики, рациональной комплексной терапии и профилактики привели к значительному снижению частоты и тяжести агрессивных форм послеродовой инфекции (сепсиса, перитонита, гнойного мастита). Тем не менее до сих пор отсутствует тенденция к значительному уменьшению частоты наиболее распространенных у беременных и родильниц гнойно-воспалительных заболеваний: эндомиометрита, раневой инфекции, пиелонефрита [18, 21].
Необходимо подчеркнуть, что дородовое излитие вод связано с 40% преждевременных родов и, как следствие, часто является причиной неонатальной заболеваемости и смертности [17]. Три основные причины неонатальной смертности связаны с ПРПО при недоношенной беременности: незрелость органов и систем, сепсис и гипоплазия легких. ПРПО представляет риск для матери прежде всего в связи с хориоамнионитом. Доказана связь между восходящей инфекцией из нижних отделов генитального тракта и ПРПО. Каждая третья пациентка с ПРПО при недоношенной беременности имеет положительные результаты посевов содержимого из генитального тракта, более того, исследования доказали возможность проникновения бактерий через интактные мембраны. Имеется множество публикаций, в которых обсуждаются вопросы выявления плодов с внутриутробной инфекцией (ВУИ), профилактического назначения антибиотиков, токолитиков и кортикостероидов, оптимального гестационного возраста для родоразрешения [3, 9-13, 19, 22, 23, 25]. Известно, что вероятность развития родовой деятельности при излитии околоплодных вод находится в прямой зависимости от гестационного срока: чем меньше срок, тем больше период до развития регулярной родовой деятельности (латентный период). В пределах первых суток после преждевременного излития вод спонтанные роды начинаются: в 26% при массе плода 500-1000 г, в 51% при массе плода 1000-2500 г, в 81% при массе плода более 2500 г.
ПРПО встречается в 2-4% при одноплодной и в 7-20% при многоплодной беременности, является причиной увеличения заболеваемости не только новорожденного, но и матери, может явиться причиной неонатальной смерти [6, 7, 26, 31].
ПРПО осложняет течение 10% беременностей и только в 3% наблюдений ПРПО происходит в сроке менее 37 нед. Тем не менее 1 /3 преждевременных родов происходит вследствие ПРПО в недоношенном сроке беременности. ПРПО в США ежегодно осложняет течение доношенной беременности в 400 000 случаев, при недоношенной - в 120 000 случаев [27].
Таким образом, преждевременные роды, обусловленные инфекцией, являются прогнозируемым фактором риска развития осложнений беременности и родов как для женщины, так и для плода и новорожденного. В.М. Сидельникова и соавт. [15] указывали, что в последние 10 лет необходимость понимания связи между инфекцией и преждевременными родами возросла. При ПРПО в сроке 34 нед и более длительная (более 12-24 ч) выжидательная тактика не показана, так как повышает риск внутриматочной инфекции без улучшения исходов для плода. Но решение о вмешательстве должно приниматься, основываясь прежде всего на комплексной клинической оценке ситуации после получения информированного согласия пациентки [17]. Острая необходимость снижения частоты данной патологии требует своевременного поиска мер профилактики как преждевременных родов, особенно с ПРПО, так и послеродовых гнойно-воспалительных заболеваний.
В настоящее время существует необходимость однозначно трактуемых рекомендаций по методу преиндукции преждевременных родов с ПРПО (показания и противопоказания для различных методов, дозировка, кратность введения, курсовая доза фармпрепарата в зависимости от паритета, срока беременности, состояния шейки матки и т.д).
Терапевтическую тактику определяют, разделяя сроки беременности в зависимости от того, в каком сроке ПРПО произошел: менее 23 нед, 23-31 нед, 32-33 нед, 34-36 нед. Если имеются признаки хориоамнионита, рекомендована антибактериальная терапия широкого спектра действия [29].
Увеличение частоты преждевременных родов обусловлено в США не только увеличением числа многоплодных беременностей, возраста беременных, но и увеличением частоты показаний к индукции преждевременных родов (R. Roberto, Ch. Lockwood, 1999).
Относительно выживаемости новорожденных известно, что только некоторые новорожденные могут выжить в сроке 22 нед беременности, но не в сроке 20 нед. Выхаживание недоношенных детей гестационного возраста 22 нед возможно только при применении усовершенствованных технологий (R. Roberto, Ch. Lockwood, 1999). Масса тела в 500 г исторически рассматривается как лимит по выживаемости.
Осложнения ПРПО
Интерлейкин-6, а также прокальцитонин в материнской сыворотке повышаются раньше, чем СРБ, и могут быть использованы для ранней диагностики субклинических форм инфекции.
Еще одна проблема лабораторной диагностики обусловлена необходимостью проведения профилактики респираторного дистресс-синдрома (РДС) с применением глюкокортикоидов, так как применение последних может оказать влияние на количество лейкоцитов, по крайней мере, в течение времени созревания легких.
Для матери ПРПО при недоношенной беременности в 30% случаев может осложниться клинически или субклинически выраженным хориоамнионитом, септицемией или эндометритом. К возможным осложнениям дополнительно относят не только ПОНРП, но и нервно-психические расстройства, смерть. Особо подчеркивается, что ПРПО для матери может осложниться в послеродовом периоде эндомиометритом, послеродовым сепсисом (септицемией), послеродовым кровотечением, венозным тромбозом.
Для плода ПРПО при недоношенной беременности может осложниться: 1) проявлениями недоношенности у новорожденного: РДС, некротическим энтероколитом, наличием открытого артериального протока, внутрижелудочковым кровоизлиянием, ретинопатией недоношенных, слуховыми расстройствами, церебральным параличом; 2) маловодием (результат - лицевые аномалии, нарушения членорасположения, гипоплазия легких, задержка роста плода); 3) гипоксией плода вследствие компрессии пуповины, отслойки плаценты; 4) неонатальной заболеваемостью вследствие неправильного членорасположения, маловодия, недоношенности. При ПРПО обнаруживаются врожденные пороки развития плода, с которыми может быть и связан ПРПО.
S. Suzuki и соавт. [34, 35] изучили акушерские и неонатальные исходы преждевременных родов при одноплодной беременности, осложненной ПОНРП, после ПРПО и без ПРПО. Проанализированы 95 случаев при сроке беременности от 22 до 36 нед. В общем число случаев отслойки плаценты при одноплодной беременности с ПРПО составляет 4,7%, отношение шансов (odds ratio - OR) - 6,50 (р<0,01). В данном исследовании из 95 случаев ПОНРП при недоношенной одноплодной беременности в 64 (67,4%) случаях она произошла без ПРПО и в 31 (32,6%) случае - с ПРПО. Частота гистологически подтвержденного хориоамнионита у женщин после ПРПО была значительно выше, чем у пациенток без ПРПО (р=0,02).
E. Reece и соавт. [30] представили обзор исследований, посвященных оценке OR и доверительного интервала (CI, confidence intervals) развития осложнений при трех вариантах ведения ПРПО при доношенной беременности: индукции родов окситоцином, простагландином и применение выжидательной тактики. Так, отношение шансов развития хориоамнионита было выше при индукции родов простагландином по сравнению с их индукцией окситоцином (OR=1,55, CI=1,09-2,21), при индукции родов окситоцином по сравнению с применением выжидательной тактики (OR=0,91, CI=0,51-1,62). Установлен наименьший риск развития хориоамнионита при индукции родов простагландином по сравнению с применением выжидательной тактики (OR=0,68, CI=0,51-0,91). Однако при сравнении индукции родов простагландином и применением выжидательной тактики OR проведения кесарева сечения было 0,95 (CI=0,76-1,20), что больше, чем при индукции родов простагландином в сравнении с окситоцином (OR=0,67, CI=0,34-1,29), но меньше, чем при сравнении индукции родов окситоцином и применением выжидательной тактики (OR=1,24, CI=0,89-1,73).
T. Mohr [28] считает, что основными причинами ПРПО являются: бактериальный вагиноз, многоплодная беременность, многоводие, преждевременные сокращения миометрия, кровотечение в I триместре беременности, никотиновая зависимость, преждевременные роды или ПРПО при недоношенной беременности в анамнезе. ПРПО происходит, если устойчивость амниона к давлению снижается, что может иметь разные причины. Неповрежденный амнион с достаточным количеством амниотической жидкости необходим не только для развития плода (легких, движений), а также защищает плод от восходящей инфекции. Конечно, это может быть следствием механического напряжения мембраны. Например, во время родов, при многоплодной беременности или многоводии. Однако возможной причиной может явиться уменьшение сопротивления амниона. Начиная с 20 нед беременности, уменьшается синтез коллагена (уменьшение коллагена-мРНК) и снижается выработка коллаген-стабилизирующих ферментов, таких как лизилоксидаза. Другим механизмом является увеличение разрушения коллагена конкретными матричными металлопротеиназами (ММП), в основном MMП-1, -8 и -9 (специфические ингибиторы роста ткани). Роды при хориоамнионите приводят к дисбалансу уровня матричных металлопротеиназ. Повышенная способность коллагена к растворению приводит к разрушению амниона и, следовательно, к снижению сопротивления мембраны.
Независимо от срока беременности, синдром амниотической инфекции значительно ухудшает прогноз для новорожденного. Чувствительность лабораторных маркеров (например, интерлейкина-6 и прокальцитонина), которые могут выборочно обнаружить субклинические формы АИС, не до конца изучена.
Одной из основных причин ПРПО является восходящая вагинальная инфекция. Патофизиологически инфекция приводит к усилению производства цитокинов и простагландинов (Е2 и F2) и через каскад - к развитию родовой деятельности. Основными инфекционными агентами при ПРПО T. Mohr [28] называет: Streptococci группы В, E. coli, Fusobacteria, Peptostreptococci, Bacterioides, Ureaplasma urealyticum. Таким образом, в зависимости от срока беременности нужно решить, следует ли продлить беременность, так как существует повышенный риск развития АИС и преждевременных родов.
K. Shimoya и соавт. [33] пришли к выводу, что хориоамнионит снижает риск развития РДС плода, что связано с повышением уровня интерлейкина-6 (ИЛ-6) в плазме крови плода. С другой стороны, назначение глюкокортикоидов напрямую приводит к подавлению концентрации ИЛ-6 и ИЛ-8 в крови плода, что может подавлять ассоциированное с ИЛ-6 созревание легких плода.

V. Phupong и соавт. [26] считают, что в сроке 32-34 нед при родоразрешении необходимо прогнозировать осложнения, связанные не только с недоношенностью (см. таблицу), но и с риском инфекционных осложнений.
При изучении роли инфекционного фактора в генезе преждевременных родов J. Rzanek-Głowacka и соавт. [32] в 1999-2001 гг. провели собственные исследования. Приведены убедительные доказательные сведения о роли бактериального вагиноза в возникновении ПРПО. Авторы пришли к выводу, что число случаев внутриутробной инфекции при беременности составляет от 1 до 10%. Клинически выраженный хориоамнионит осложняет течение от 1 до 5% беременностей, но почти 25% преждевременных родов в значительной степени повышают заболеваемость и смертность новорожденных, а также являются причиной заболеваемости матерей. Очень важно выявить риск развития внутриутробного инфицирования плода от матери и провести своевременную диагностику хориоамнионита у матери. Авторы провели оценку взаимосвязи бактериальной флоры цервикального канала беременной с ПРПО при преждевременных родах ранее 32 нед с клиническими и лабораторными признаками инфекции у матери и наличием бактериальной флоры в крови новорожденных. Обследованы 37 беременных женщин в возрасте от 20 до 43 лет в сроки беременности от 24 до 32 нед. Средняя продолжительность от начала подтекания околоплодных вод до родов составила 11,1±8,63 дня. В результате бактериологического исследования отделяемого из цервикального канала женщин обследуемой группы выявили: Staphylococcusepidermidis - у 27%, кишечная палочка - у 19%, Streptococcus группы B - у 10,8%, Enterococcus faecalis - у 8,1%. В результате бактериологических исследований крови новорожденных выявили: Staphylococcus epidermisis - у 13,5%, Staphylococcushaemolyticus - у 10,8%, Klebsiella pneumoniae - у 10,8%, синегнойная палочка - у 8,1%. В 97,3% случаев у новорожденных выявлены врожденные инфекции в форме пневмонии, подтвержденные рентгенологически. Подтверждение внутриутробной инфекции при гистологическом исследовании плаценты в форме хориоамнионита имело место в 25 (67,5%) случаях. Исследователи пришли к выводу, что при ПРПО у женщин бактериальный вагиноз (БВ) является фактором риска развития внутриутробных инфекций у новорожденных.
Учитывая этот факт, в настоящее время общепризнанной является необходимость санации всех беременных с клиническими проявлениями бактериального вагиноза [2, 4, 36]. Препаратами выбора в этом случае являются метронидазол и клиндамицин.
Центр по контролю и профилактике заболеваний США (Centres for Disease Control and Prevention, 2010) рекомендует для лечения беременных метронидазол в дозах 500 мг 2 раза в сутки или 250 мг 2 раза в сутки на протяжении 7 дней как препарат первой линии. Альтернативой является пероральный прием клиндамицина по 300 мг 2 раза в сутки в течение 7 дней [36]. Европейское общество по лечению заболеваний, передающихся половым путем, кроме вышеуказанных способов приема препаратов рекомендует прием метронидазола однократно в дозе 2 г, а также местное применение метронидазола в форме геля или клиндамицина в виде 2% вагинального крема (5 г на ночь в течение 7 дней) [4].
Российские клинические рекомендации отдают предпочтение местному лечению БВ в первой половине беременности и пероральному применению метронидазола со второй половины беременности [2].
Таким образом, прогнозирование ПРПО рекомендовано до наступления беременности при наличии следующих факторов риска развития преждевременных родов: низкий социально-экономический статус женщин, индекс массы тела менее 19,0, курение, преждевременные роды в анамнезе, истмико-цервикальная недостаточность, аномалии развития матки, акушерские осложнения (гипертензия, кровотечение во время беременности, инфекция, многоводие), инфекция генитального тракта, наследственные генетические расстройства, антифосфолипидный синдром. И если некоторые факторы риска (социально-экономический статус, наследственность, аномалии развития половых органов и т.д.) являются немодифицируемыми, то инфекция, дисгормональные нарушения или приобретенная патология системы гемостаза могут быть прогнозируемы и предотвратимы. Роль инфекции значима более всего как причины преждевременного разрыва плодных оболочек. Профилактика и лечение хронической генитальной инфекции [20] являются залогом профилактики ПРПО.
Читайте также:

