Гемофильная палочка латинское название
Обновлено: 24.04.2024
Для данного исследования лаборатория принимает следующий биоматериал:
- Мазок/отделяемое конъюнктивы глаза (правый)
- Мазок/отделяемое конъюнктивы глаза (левый)
Возможны ограничения в приеме биоматериала. Уточняйте информацию в расписании нужного Вам офиса.
Подготовка к исследованию
Условия подготовки определяются лечащим врачом.
Внимание! Для хранения и транспортировки биологического материала лаборатория CMD предоставляет специальные расходные материалы, которые необходимо получить в ближайшем офисе перед обращением к врачу.
Взятие материала рекомендуется проводить
- до начала антибактериальной терапии или не ранее, чем через две недели после ее окончания;
- мазок/отделяемое конъюнктивы глаз. Выделяемый из глаза материал при помощи зонд-тампона собирают утром после сна до умывания из места наибольшего его скопления на конъюнктиве глаза.
Доставка в лабораторию в день взятия биоматериала при Т=+2+25 °С в коллекторе. Замораживание образцов недопустимо!
Метод исследования
Haemophilus influenzae (или палочка Пфейффера) – возбудитель гемофильной инфекции (Hib-инфекции), которая характеризуется преимущественно поражением респираторного тракта и оболочек мозга. Выделяют 6 серотипов H. influenzae (серотипы a, b, c, d, e, f). Наиболее патогенными свойствами и способностью вызывать тяжелые формы заболевания обладает H. influenzaeтипа b (Hib). Распространение инфекции происходит воздушно-капельным или бытовым путями передачи. К наиболее распространенным формам инфекции относится пневмония, синусит, средний отит, ринофарингит, конъюнктивит. Наиболее часто Hib-инфекции подвержены дети в возрасте 6–48 мес., реже новорожденные и дети старше 5 лет.
Культуральные исследования выполняются с применением высококачественных транспортных и питательных сред ведущих мировых производителей. Идентификацию выделенных микроорганизмов проводят классическим бактериологическим методом с использованием современных тест-систем. На следующем этапе лабораторного исследования определяется чувствительность возбудителя к антимикробным препаратам. Выбор спектра зависит от выявленного возбудителя, интерпретация определения чувствительности соответствует стандартам EUCAST (Европейский комитет по определению чувствительности к антимикробным препаратам (European Committee Antimicrobial Susceptibility Testing)).
Показания к исследованию:
- Обследование лиц с подозрением на Hib-инфекцию (конъюнктивит, пневмония, менингит, септицемия, отит, синусит, гнойный артрит, остеомиелит);
- Обследование контактных лиц;
- Подбор антибактериальной терапии;
- Оценка эффективности антибактериальной терапии.
Результат бактериологического исследования, в случае обнаружения гемофильной палочки (Haemophilus influenzae типа b) предоставляется в качественном формате, содержит антибиотикограмму и заключение.
Интерпретация проводится врачом с учетом клинических проявлений.
Гемофильная палочка, палочка Пфейфера (лат. Haemophilus influenzae ), — грамотрицательная неподвижная палочковидная бактерия семейства Pasteurellaceae. Первоначально описана в 1892 г. немецким бактериологом Рихардом Пфейфером (Пфайффером, нем. Richard Pfeiffer , 1858—1945) как возбудитель инфлюэнцы (гриппа). Первый свободноживущий организм, чей геном был полностью отсеквенирован. Возбудитель т. н. гемофильной инфекции у человека.
Содержание
Биологические свойства
Морфология
Мелкая (0,3—0,5 × 0,2—0,3 мкм) неподвижная коккобацилла, располагается одиночно, попарно и скоплениями, образует капсулу. Жгутиков не имеет, слабо прокрашивается анилиновыми красителями.
Культуральные свойства
Хемоорганогетеротроф, факультативный анаэроб. Образует маленькие, непрозрачные плоские колонии на средах, содержащих прогретую кровь (кровяной агар только с лошадиной или кроличьей кровью, шоколадный агар, Колумбийский агар и среда Левенталя обогащенные гемоглобином), не растёт на простых питательных средах, не содержащих кровь, для жизнедеятельности необходимы факторы X (гем) и V (НАД, зависимость от факторов является систематическим признаком [1] ), сбраживает глюкозу с образованием кислоты. Образует колонии S- и R- типа. Гладкие колонии S- типа образуются H. influenzae типа В, образующих капсулу. Для гемофильных бактерий характерен так называемый феномен кормушки или сателлита, который проявляется в их способности расти на кровяном агаре вокруг колоний стафилококков или других бактерий, продуцирующих НАД или вызывающих гемолиз. Для самих гемофильных палочек, способность вызывать гемолиз не характерна. Мелкие радужные колонии гемофильных бактерий могут быть обнаружены на кровяном агаре только в зоне гемолиза, образуемой другими микроорганизмами, например стафилококками.
Геном
Геном H. influenzae штамма Rd был первым геномом свободноживущего организма, который был полностью секвенирован в 1995 г. и опубликован в журнале Science. Микроб был выбран потому что нобелевский лауреат Хамилтон Отанел Смит долгое время работал с этим микроорганизмом и мог предоставить высококачественные библиотеки клонированной ДНК [2] . Геном представлен кольцевой двуцепочечной молекулой ДНК размером 1830138 п.н. и содержит 1789 гена, из которых 1657 кодируют белки, процент % Г+Ц пар составляет 38 % [3] .
Антигенные свойства
H. influenzae разделяются на 6 серотипов- A, B, C, D, E и F [4] . Штаммы серотипа В вызывают наиболее тяжело протекающие инфекции.
Патология
Первоначально H. influenzae идентифицировали как возбудителя гриппа, после установления вирусной природы гриппа (1933 г.) обнаружилось, что микроб является одним из возбудителей пневмонии [5] , менингита [6] , эпиглоттита [7] , заболеваниям подвержены дети в возрасте до 3 лет [8] , а также взрослые с ослабленным иммунитетом [9] . Ассоциирован с перикардитом, целлюлитом, остеомиелитом, септическим артритом [10] , а также с развитием диабета первого типа [11] . H. influenzae поражает только людей [12] . Капсула является фактором патогенности и защищает микроорганизм от действия иммунной системы человека.
Гемофильная инфекция — острые инфекционные болезни, вызванные палочкой инфлюэнцы, характеризуется преимущественным поражением органов дыхания, центральной нервной системы и развитием гнойных очагов в различных органах.
Содержание
Этиология
Возбудитель — Haemophilus influenzae (палочка инфлюэнцы, палочка Пфайфера) относится к семейству Pasteurellaceae, роду гемофилюсов (который включает 16 видов бактерий).
Представляет собой мелкую грамотрицательную коккобациллу (0,3 мкм в диаметре), для своего роста требует наличия содержащихся в эритроцитах термолабильного фактора V (НАД) и термостабильного фактора X (гемин).
По культуральным свойствам (продукция индола, активность уреазы и др.) разделяется на 7 биотипов (от I до VII). Часть выделенных со слизистых оболочек палочек инфлюэнцы имеет капсулы. Известно 6 антигенно различающихся капсульных типов, обозначаемых от А до F. Наибольшее значение в патологии человека имеет Haemophilus influenzae type b. Данный серотип отличается от других наличием 8 генов, ответственных за образование фимбрий, которые способствуют улучшению адгезивных и пенетрантных свойств. Также, в отличие от других серотипов, гемофилюс инфлюэнцы типа b — единственно способная проникать в кровеносное русло.
Эпидемиология
Источником и резервуаром инфекции является только человек. Путь распространения — воздушно-капельный. Возбудитель локализуется на слизистой оболочке верхних дыхательных путей. H.influenzae можно выделить из носо-глотки 90 % здоровых людей, причем на более вирулентный тип b приходится около 5 % всех выделенных штаммов. Здоровое носительство может продолжаться от нескольких дней до нескольких месяцев. Носительство сохраняется даже при высоком титре специфических антител и даже при назначении высоких доз антибиотиков. Чаще всего заболевают дети в возрасте от 6 мес до 4 лет, реже болеют новорожденные, дети более старшего возраста и взрослые.
До введения обязательной вакцинации против Hib в США (до 1990г), по данным ААР (American Academy of Pediatrics) ежегодно отмечалось около 20.000 случаев заболевания и около 1.000 летальных исходов у детей в результате гемофильной инфекции. Неврологические осложнения отмечались в 25-35 % случаев. В настоящее время в европейских странах регистрируется 26-43 случаев заболеваний на 100.000 детей, смертность составляет 1-3 %, высок уровень неврологических осложнений.
Показатели заболеваемости гемофильной инфекцией типа b в тысячи раз выше у детей восприимчивых возрастов (75-85 % случаев заболеваний — в возрасте до 24 мес, пик — 6-12 мес).
Выделяют следующие группы риска для данного заболевания:
- люди экстремальных возрастов (дети до 2-х лет, пожилые люди);
- дети, посещающие детские дошкольные учреждения. В одном из исследований было показано, что до 50% инвазивных форм можно отнести за счёт посещения детских учреждений;
- дети на грудном вскармливании. Фактор грудного вскармливания является отчасти гипотетическим, так как до конца не ясен механизм воздействия на защиту от гемофильной инфекции. Здесь могут играть роль как питательные, так и иммунные факторы, находящиеся в грудном молоке. После иммунизации женщин полисахаридной вакциной на 36-39 неделях беременности было отмечено 20-кратное возрастание выделения специфических антител с грудным молоком в послеродовом периоде;
- представители неевропейских рас. Этот фактор риска также является достаточно спорным, однако многие исследования заболеваемости показывали, что заболеваемость среди детей неевропейских рас значительно выше;
- лица с низким социально-экономическим статусом. Риск заболевания значительно увеличивается при скученном проживании;
- лица с различными видами иммунодефицита;
- крайне ослабленные и страдающие алкоголизмом;
- больные лимфогранулематозом (болезнь Ходжкина), серповидно-клеточной анемией;
- лица подвергшиеся спленэктомии (удаления селезёнки).
Заболеваемость повышается в конце зимы и весной. За последние годы заметно увеличилась заболеваемость взрослых.
Необходимо отметить, что вариант клинической формы гемофильной инфекции зависит от возраста. Так, согласно зарубежным данным, менингит встречается чаще у детей в возрасте 6-9 месяцев, эпиглоттит встречается чаще у детей старше 2-х лет, целлюлит (воспаление подкожной клетчатки) чаще встречается у детей в годовалом возрасте. Для взрослых и пожилых людей менингит является нехарактерным — чаще встречается пневмония.
Патогенез
Воротами инфекции является слизистая оболочка носоглотки. Механизмом передачи является воздушно-капельный, однако у маленьких детей путь передачи может быть контактным. Возбудитель может длительное время персистировать в области ворот инфекции в виде латентной бессимптомной инфекции. В некоторых случаях, в основном у лиц с ослабленными защитными силами и лиц, входящих в группу риска, латентная форма переходит в манифестную. Риск перехода инаппарантного носительства в манифестную форму усиливается при наличии сопутствующей вирусной инфекции и повышении микробной массы. Необходимо отметить роль вторичных контактов. Данный механизм передачи наиболее актуален для детей в возрасте до двух лет. Следует отличать первичное заболевание, которое возникает вследствие контакта со здоровым носителем и вторичное, которое возникает при контакте с больным в манифестной форме. Инфекция распространяется по окружающим тканям, обусловливая развитие синуситов, отитов, бронхитов, пневмоний, воспаление подкожной жиро-вой клетчатки, или путем гематогенной диссеминации поражает суставы и другие органы, протекая по типу сепсиса. Штаммы гемофильной палочки, не имеющие капсулы, поражают только слизистые оболочки. Системные заболевания вызывают только возбудители, обладающие капсулой, в 95 % случаях это гемофильная палочка типа b. Уникальным свойством бактерий данного типа является их способность проникать в кровеносное русло путем разрывания межклеточных соединений. Также, более выраженная патогенность этих штаммов связана с тем, что капсула способна подавлять фагоцитоз. Возбудитель может в течение нескольких суток персистировать в кровеносном русле бессимптомно до тех пор, пока масса микробных тел не станет критической. Затем бактерия проникает в ЦНС через хороидальные сплетения, вызывая инфильтрацию и гнойное воспаление мягких мозговых оболочек. У перенесших заболевание развивается стойкий иммунитет.
Иммунный отклик организма на данный вид инфекции имеет несколько особенностей. Вследствие подавления фагоцитоза, продукция антител В-лимфоцитами активируется без участия Т-хелперов. Именно поэтому иммунный отклик организма в ответ на инвазию Hib в большинстве случаев недостаточен, отсутствует т. н. бустерный (ударный) отклик при повторной экспозиции антигена гемофильной палочки. Также отмечается крайне слабая Т-независимая продукция специфических антител в возрасте до 18 месяцев. Кроме того, полисахариды являются набором олигосахаридов, каждый из которых способен индуцировать слабый иммунный отклик. Это в свою очередь обусловливает множественность и вариабельность продуцируемых антител в ущерб количественному фактору. Местный иммунитет, представленный секреторными антителами класса IgA изучен недостаточно. Более того, было обнаружено, что капсульные виды H.influenzae выделяют протеазы, инактивирующие антитела. Проведенные исследования местного иммунитета у здоровых носителей показали, что роль местного иммунитета может быть достаточно важной — блокировка пенетрации слизистой оболочки бактериями, предотвращение проникновения микроорганизмов в кровеносное русло. Комплемент при гемофильной инфекции может быть активирован как по классическому (антитело-зависимому) пути, так и по альтернативному пути. Ан-тигены клеточной стенки H.influenzae способны активировать комплемент по альтернативному пути, в то время как комплекс антител и антигенов, способен активировать комплемент по классическому пути.
Симптомы и течение
Длительность инкубационного периода установить трудно, так как заболевание нередко является следствием перехода латентной инфекции в манифестную. Может развиться местный воспалительный процесс слизистой оболочки верхних дыхательных путей или развиваются заболевания, обусловленные гематогенной диссеминацией. Гемофильная палочка типа b является одной из частых причин генерализованной инфекции (бактериемии) у детей, у половины из них развивается гнойный менингит, довольно часто (15-20 %) пневмония и реже другие очаговые поражения. Как правило, гемофильная инфекция протекает остро, но некоторые клинические формы могут принимать затяжное течение.
Гемофильная инфекция может протекать в следующих клинических формах:
- 1. Гнойный менингит.
- 2. Острая пневмония.
- 3. Септицемия.
- 4. Воспаление подкожной клетчатки (целлюлит).
- 5. Эпиглоттит (воспаление надгортанника).
- 6. Гнойный артрит.
- 7. Прочие заболевания (перикардит, синуситы, отит, заболевания дыхательных путей и др.).
По данным Бостонского университета самыми частыми клиническими формами гемофильной инфекции являются менингит, средний отит и пневмония.
Гнойный менингит наблюдается преимущественно у детей от 9 месяцев до 4 лет (для данной возрастной группы это самая частая причина менингитов). Заболевание развивается остро, иногда с симптомов ОРЗ, затем быстро развивается клиническая симптоматика, характерная для бактериальных менингитов. Иногда менингиальный синдром сочетается с другими проявлениями гемофильной инфекции (гнойный артрит, воспаление надгортанника, целлюлиты. Заболевание протекает тяжело и нередко кончается летально (около 10-15 % случаев).
Гемофильная пневмония (по данным Бостонского университета) является второй по частоте среди всех бактериальных пневмоний у детей. Может проявляться как в виде очаговой, так и в виде долевой (крупозной), очень часто (до 70 %) сопровождается гнойным плевритом (у детей), может осложняться гнойным перикардитом, средним отитом. Может принимать затяжное течение. У взрослых, особенно пожилых лиц, гемофильная инфекция может наслаиваться на другие виды инфекции.
Гемофильный сепсис чаще развивается у детей 6-12 мес, предрасположенных к этому заболеванию. Протекает бурно, нередко как молниеносный, с септическим шоком и быстрой гибелью больного.
Воспаление подкожной клетчатки (целлюлит) также развивается у детей до 12 мес, чаще локализуется на лице, реже на конечностях. Начинается нередко с картины ОРЗ (ринофарингит), затем появляется припухлость в области щеки или вокруг глазницы, кожа над припухлостью гиперемирована, с цианотичным оттенком, иногда заболевание сопровождается воспалением средним отитом. Температура тела субфебрильная, симптомы общей интоксикации выражены слабо. У детей старших возрастов воспаление подкожной клетчатки может локализоваться на конечностях.
Воспаление надгортанника (эпиглоттит) является очень тяжелой формой гемофильной инфекции, в большинстве случаев (около 90 %) сопровождается бактериемией. Начинается остро, характеризуется быстрым подъемом температуры тела, выраженной общей интоксикацией и картиной быстро прогрессирующего крупа, который может привести к гибели ребенка от асфиксии (полная непроходимость дыхательных путей или остановка дыхания).
Гнойные артриты являются следствием гематогенного заноса гемофильной палочки, нередко сопровождаются остеомиелитом.
Диагноз, диффренциальный диагноз
При распознавании необходимо учитывать возраст больного, наличие факторов, способствющих инфицированию гемофильной палочкой, характерные клинические проявления (целлюлиты, эпиглоттит и др.). Подтверждением диагноза служит выделение гемофильной палочки в гное, мокроте, ликворе, материале, взятом со слизистых оболочек. Средами выбора для культивирования являются агары, обогащенные кровью (20 %)(желательно наличие эритроцитарных кофакторов X и V). Окраска по Граму также является диагностически важной. Серологическими тестами выбора являются латекс-агглютинация и реакция преципитации. Ценность этих методов особенно велика для диагностики в тех случаях, когда антимикробная терапия была начата до посева культуры. В спинномозговой жидкости (иногда в моче) можно обнаружить капсульный антиген гемофильной палочки с помощью реакции встречного иммунофореза или иммуноферментного метода. Однако факт обнаружение не может однозначно свидетельствовать в пользу диагноза гемофильной инфекции, так как антиген может выявляться при носительстве, при недавней вакцинации полисахаридной вакциной или загрязнении анализа перекрестно-реагирующими фекальными микроорганизмами. В клинически важных случаях проводят тест на антибиотикорезистентность.
Лечение
Без этиотропной терапии некоторые формы гемофильной инфекции (менингит, эпиглоттит) почти всегда заканчиваются смертью больного. Необходимо возможно раньше начать этиотропную терапию. Наиболее эффективным и малотоксичным до 1970 года, когда был обнаружен факт наличия антибиотикорезистенности у H.influenzae, считался ампициллин, однако в последние годы все чаще стали выделяться штаммы гемофильной палочки, резистентные к данному антибиотику. H.influenzae устойчив к пенициллинам, некоторые из штаммов продуцируют пенициллиназу. Ампициллин вводят внутривенно в суточной дозе 200—400 мг/кг/сут детям и 6 г/сут взрослым. В некоторых рекомендациях, в частности в руководстве Американской Педиатрической Академии, предлагается с самого начала применять ампициллин, цефалоспорины в комбинации с левомицетином. Однако, согласно последним исследованиям, проведенным в России (Москве и Санкт-Петербурге и других крупных городах), штаммы гемофильной палочки, циркулирующие в этих областях резистентны практически ко всем классам антимикробных препаратов. В последнее время в отечественных и зарубежных публикациях появились сведения о более высокой, нежели для ампициллина, эффективности таких антибиотиков, как амоксиклав (ко-амоксиклав, бисептол) и азитромицин (сумамед), даже при применении их короткими курсами.
Профилактика и мероприятия в очаге
Здоровым носителям гемофильной палочки типа b и лицам из группы риска, контактирующим с больными гемофильной инфекцией, в течение первой недели после регистрации первого случая заболевания рекомендуется принимать рифампицин внутрь в дозе 10-20 мг/кг/сут (максимум 600 мг/сут) однократно в течение 4 дней.
Специфическая иммунопрофилактика
Позже проводились многочисленные испытания полисахаридных вакцин в Европе и Северной Америке. В частности, клиническое испытание в Великобритании (1991—1993) показало снижение на 87 % заболеваемости менингитом гемофильной этиологии. В Голландии, при проведении аналогичного исследования, было зафиксировано полное отсутствие случаев менингита гемофильной этиологии в течение 2-х лет после начала иммунизации.
В настоящее время обязательная иммунизация против гемофильной инфекции введена в США (1990), Канаде (1990) и ряде других стран. С 2011 года прививка против Hib стала обязательна в России [1] [2] . Вакцинация проводится детям в 3 этапа: в 3, 4,5 и 6 месяцев. В возрасте 18 месяцев — однократная ревакцинация.
Некоторые факты, подтверждающие эффективность вакцинации
По данным, опубликованным рядом авторов (Adams WG et al) в JAMA, результаты таковы:
Снижение числа случаев заболеваний менингитом гемофильной этиологии у детей на 82 % с 1985 по 1991, предотвращение около 10.000-16.000 заболеваний гемофильной инфекцией в 1991 году.
В настоящее время наиболее эффективным считается введение трех доз конъюгированных вакцин — в 2, 4 и 6 месяцев. Вакцины взаимозаменяемы. Рекомендуется также вводить последнюю (ударную) дозу в возрасте 12 месяцев [источник не указан 123 дня] .
Инфекции вызванные Haemophilus influenzae, ducreyi: диагностика, лечение, профилактика
Бактерии рода Haemophilus — маленькие грамотрицательные коккобациллы, рост которых зависит от наличия в среде экзогенных факторов роста X (гемин) и V (никотинамидадениндинуклеотид). Поражают слизистые оболочки организма. Наиболее патогенные виды — Haemophilus influenzae и Н. ducreyi.
Инфекции вызываемые Haemophilus influenzae
Основной фактор патогенности Haemophilus influenzae — антифагоцитарная полисахаридная капсула (шесть разновидностей — от а до f). Кроме того, бактерия способна экспрессировать на своей поверхности липополисахарид и IgA протеазу. У непривитых пациентов вызывает септицемию, менингит и остеомиелит, обычно обусловленных серотипом b.
Клинические признаки инфекции вызванной Haemophilus influenzae. Инфекция обычно возникает в дошкольном возрасте и характеризуется гнойным менингитом, острым эпиглоттитом (воспаление надгортанника), септицемией, целлюлитом подкожно-жировой клетчатки лица и остеомиелитом. Штаммы, не образующие капсулу, считают представителями нормальной микрофлоры носоглотки. Иногда они могут быть причиной развития среднего отита, синусита и инфекций грудной клетки у пациентов с обструк-тивными болезнями лёгких.
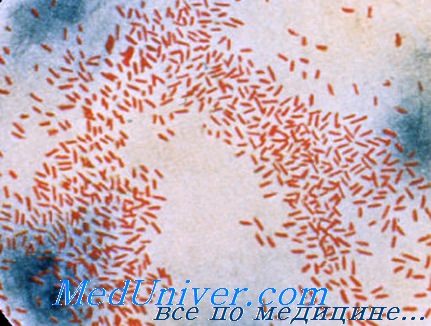
Лабораторная диагностика инфекции вызванной Haemophilus influenzae. Для ранней диагностики менингита используют определение антигенов возбудителя. Выполняют посев спинномозговой жидкости, мокроты, крови или гноя на шоколадный агар и инкубацию в среде с 5% содержанием диоксида углерода. Обнаружение Haemophilus influenzae основано на зависимости их роста от наличия в среде X и V факторов.
Лечение и профилактика инфекции вызванной Haemophilus influenzae. Устойчивость большинства штаммов Н. influenzae к ампициллину обусловлена способностью бактерии вырабатывать b-лактамазу. Для лечения применяют амоксициллин + клавулановую кислоту, кларитромицин, тетрациклин или триметоприм. При тяжёлой инфекции рекомендовано применение устойчивых к b-лактамазе цефалоспоринов.
В настоящее время детскую инфекцию практически удалось победить благодаря белковой конъюгированной вакцине против возбудителей серотипа b. Штаммы Haemophilus, не образующие капсулу, распространены повсеместно, а потому лицам с ослабленным иммунитетом практически невозможно избежать заражения.
Инфекции вызванные Haemophilus ducreyi
Инфекции, вызываемые Haemophilus ducreyi, передаются половым путём и характеризуются развитием болезненных асимметричных мягких генитальных язв (мягкий шанкр). Заболевание сопровождается лимфаденопатией, а нагноение паховых лимфатических узлов приводит к образованию свищей. Инфекция в основном распространена в развивающихся странах и способствует передаче ВИЧ-инфекции.
Для профилактики заболевания применяют эритромицин или амоксициллин + клавулановая кислота. Большое значение имеет своевременное обнаружение и лечение носителей инфекции.
Редактор: Искандер Милевски. Дата обновления публикации: 18.3.2021
Возбудителем гемофильной инфекции является бактерия Haemophilus influenzae (или палочка Пфейффера) из семейства Pasteurellaceae (Hib). Длительное время гемофилы считались возбудителем гриппа, так как эта инфекция наиболее часто протекает в форме ринофарингита или ОРЗ без специфических особенностей, что и обусловило такое название. Бактерия представляет собой мелкую полиморфную палочку, иногда по форме напоминающую коккобациллу. Спор нет, имеет капсулу. Для культивации требует кровь, специальные добавки и витамины. В зависимости от различий химического строения и антигенных свойств капсулы выделяют 6 серотипов H. influenzae (серотипы a, b,c,d,e,f), а также бескапсульные штаммы.
Инфицирование гемофильными палочками редко приводит к заболеванию, однако спектр инфекционных поражений может быть чрезвычайно широк и зависит от серотипа возбудителя. У взрослых H.influenzae вызывает преимущественно очаговую бронхопневмонию, часто сочетающуюся с выраженным трахеобронхитом. Пневмония редко приобретает тяжелое течение, но в отдельных случаях может осложниться экссудативным плевритом, перикардитом, менингитом, артритом и т.п. Гемофилы входят в состав нормальной флоры верхних дыхательных путей, уровень бессимптомного носительства у детей достигает более 40%.
Наиболее патогенными свойствами и способностью вызывать тяжелые формы заболевания обладает H.influenzae тип b (Hib). Ее вирулентные свойства связаны преимущественно с капсульным полисахаридом и продукцией мембранотоксина.
При инвазивных формах заболевания возбудитель выявляется в стерильных жидкостях организма – СМЖ, крови, плевральной жидкости и др. К неинвазивным формам инфекции относится пневмония (без бактериемии), синусит, средний отит, ринофарингит, конъюнктивит. При генерализации инфекционного процесса развиваются инвазивные формы инфекции, наиболее частым проявлением которых является менингит (51–65%), септицемия – 12%, эпиглоттит – 10%, пневмония (с бактериемией) – 8% в структуре инвазивных Hib инфекций.
Наиболее часто Hib-инфекции подвержены дети в возрасте 6–48 мес, реже новорожденные и дети старше 5 лет. Подавляющее число заболевших приходится на возраст от 3 мес до 3 лет.
Факторами риска являются:
- посещение детских организованных коллективов (ясли, детские сады), особенно закрытого типа (дома ребенка, интернаты);
- искусственное вскармливание;
- иммунодефициты (первичные и вторичные, включая ВИЧ-инфекцию);
- хронические заболевания (сердца, легких, сахарный диабет).
Распространение инфекции происходит воздушно-капельным или бытовым путями передачи. В более редких случаях – при родах, от матери с гемофильной колонизацией генитального тракта.
Источником и основным резервуаром инфекции является только человек. В среднем среди здоровых детей бактерионосители составляют 2–5%, однако в окружении больного доля их может возрастать до 30% и выше. Уменьшение частоты носительства способствует снижению уровня заболеваемости. В странах, где введена вакцинация против Hib-инфекции, доля носителей в популяции здоровых детей снизилась до 0,5–1%.
Показания к обследованию
- Исследования по эпидемиологическим показаниям – среди контактных лиц в очаге Hib-инфекции (чаще всего Hib-менингит);
- профилактические исследования – с целью выявления уровня носительства в популяции, особенно в закрытых детских коллективах;
- диагностические исследования – при подозрение на заболевание эпиглоттитом, пневмонией, менингитом, септицемией, отитом, синуситом, гнойным артритом, остеомиелитом.
Материал для исследований
- Мокрота, лаважная жидкость, пунктаты (при подозрении на пневмонию); гнойное отделяемое, пунктаты; (средний отит, синусит); СМЖ, кровь; (менингит, менигоэнцефалит); кровь (септические состояния); пунктаты (гнойный артрит, остеомиелит); секционный материал; мазок из зева (обследование контактных в очаге Hib–менингита и проведение профилактических исследований) – культуральные исследования;
- СМЖ, кровь, пунктаты – обнаружение фрагментов ДНК;
- СМЖ, кровь – обнаружение АГ.
Этиологическая лабораторная диагностика включает микроскопию исследуемого материала, посев материала с дальнейшей культуральной и биохимической идентификацией возбудителя, определением антибиотикочувствительности; обнаружение генетических фрагментов ДНК Hib и АГ Hib в стерильных жидкостях организма.
Дифференциальная диагностика проводится с микробными агентами:
- При эпиглоттите – с возбудителями вызывающими истинный и ложный круп (C.diphtheriae, S.pyogenes, различные вирусы);
- при менингите – с возбудителями, вызывающими гнойный менингит (N.meningitidis, S.pneumoniae, S.aureus и др.);
- при пневмонии – S.pneumoniae, C.pneumoniae, M.pneumoniae, L.pneumophila, S.aureus, семействомEnterobacteriaceae, вирусами гриппа;
- при отите и синусите – S.pneumoniae, Ps.aeruginosa, S.aureus, M.catarrhalis, S.pyogenes, дрожжевые грибки родаCandida;
- при гнойном артрите, остеомиелите – S.aureus, E.coli, анаэробная инфекция.
Сравнительная характеристика методов лабораторной диагностики. Микроскопические исследования используют для выявления гемофильных палочек в разных видах биологического материала: ликворе, крови, пунктатах стерильных локусов, пунктатах нестерильных локусов (мокрота, мазки из зева, придаточных пазух, уха и др.). Микроскопия, как самостоятельное исследование, обычно не проводится, так как имеет малую диагностическую ценность. Микроскопическое исследование может использоваться только для решения вопроса пригодности мокроты или лаважной жидкости для посева (в мазке должно находиться более 25 сегментоядерных лейкоцитов и менее 10 эпителиальных клеток в поле зрения), а также определения микробных ассоциаций.
Для посева с дальнейшей культуральной и биохимической идентификацией возбудителя, определением антибиотикочувствительности используют материалы стерильных локусов (кровь, ликвор, синовиальную, перикардиальную, плевральную жидкости) и различный материал из нестерильных локусов.
Важной проблемой для лечения Hib-инфекции является рост устойчивости β-лактамным антибиотикам, в первую очередь ампициллину, обусловленных продукцией плазмидных β-лактамаз. Кроме того, в мире отмечается увеличение резистентности к гентамицину, эритромицину, левомицетину.
При определении чувствительности к антибиотикам культуры, выделенной из нестерильных локусов, в первую очередь исследуют устойчивость к ампициллину, ампициллину/сульбактаму, ко-тримоксазолу. Желательно провести тест на продукцию β-лактамаз с нитроцефином. В качестве дополнительных препаратов для характеристики штамма в исследование включают цефалоспорины II–III поколения, тетрациклины, макролиды, хлорамфеникол, фторхинолоны.
Штаммы, выделенные из ликвора и крови, исследуют на чувствительность к ампициллину, цефоласпоринам III поколения, карбапенемам, хлорамфениколу, другие препараты (тетрациклины, макролиды, фторхинолоны) добавляются для более полной характеристики культуры.
Обнаружение АГ Hib в стерильных жидкостях организма (ликворе, крови) выполняют при использовании наборов реагентов, основанных на реакции латекс-агглютинации или коагглютинации.
Обнаружение фрагментов ДНК Hib проводят методом ПЦР. Исследование основано на обнаружении специфического фрагмента гена bex A, кодирующего связанный с капсулой белок возбудителя и проводится только с материалом, полученным из стерильных локусов (СМЖ, кровь, пунктаты)
Особенности интерпретации результатов лабораторных исследований. Диагноз Hib-инфекция считается установленным в случае:
Читайте также:

