Гемолитическая анемия при малярии
Обновлено: 24.04.2024
Анемия при малярии. Поражение органов при малярии
Третьим характерным признаком малярии является анемия гипохромного нормоцитарного типа. Анемия носит гемолитический характер, при затяжной малярии наблюдается функциональное угнетение костного мозга. В тяжелых случаях, в частности у беременных, может развиться анемия пернициозного типа. Степень анемии становится особенно очевидной после прекращения лихорадки, так как в периоде приступов процент гемоглобина и количество эритроцитов (а также лейкоцитов) могут увеличиваться за счет сгущения крови. В остром периоде малярии в крови много молодых, незрелых форм эритроцитов: ретикулоцитов (полихроматофилов), нормобластов, а также пойкило- и анизоцитов. В послелнхорадочном периоде увеличивается процент ретикулоцнтов, что свидетельствует об активной деятельности костного мозга.
Помимо трех основных признаков малярии — лихорадки, увеличения печени и селезенки и анемии, для острого периода малярии весьма характерны герпетические высыпания на губах, крыльях носа, реже других частях лица. Постоянны нарушения со стороны нервной системы: вегетативные расстройства, головные боли, бессонница, в тяжелых случаях малярии-поражения периферических нервов. Поражения центральной нервной системы приобретают особое значение при тропической малярии н молниеносном течении трехдневной малярии.
Расстройства сердечно-сосудистой системы носят главным образом функциональный характер. Наиболее резко они выражены во время лихорадочного приступа. Когда наблюдается учащение пульса, в периоде озноба — подъем артериального и особенно венозного давления, увеличение массы циркулирующей крови, в периоде жара и пота — падение артериального давления. Указанные гемодинамические сдвиги обусловлены резким перераспределением крови из депо в периферические сосуды и обратно а сзязи с лихорадкой, нарушениями нервной регуляции кровообращения, а при тяжелом течении малярии с анемией — также изменением сердечной мышцы дистрофического характера.

В связи с указанными гемодинамическими сдвигами в периоде озноба отмечается учащенное мочеиспускание с обильным количеством прозрачной, разведенной мочи. В периоде жара и особенно пота количество мочи становится скудным, в моче может появляться небольшое количество белка, эритроцитов, гиалиновых цилиндров.
При малярии, особенно тропической, нередко возникает острый диффузный нефрит, быстро исчезающий после специфического противомалярийного лечения. Значительно реже наблюдается липоидный и амилоидный нефроз. При злокачественной малярии возможно развитие острого некротического нефроза.
Поражении легких не характерны для малярии. Пневмонии возникают только при тяжелом течении инфекции. При злокачественном течении малярии возможны геморрагически-некротические поражения легких наряду с поражениями других органов гнперергического характера.
В лихорадочном периоде аппетит понижен, нередки извращении вкуса, запоры. Возможно возникновение кишечной колики и профузных поносов, связанных с вегетативно-сосудистыми расстройствами в кишечной стенке, по-видимому, аллергического характера. Тяжелые язвенно-некротические поражения кишечника обусловлены сопутствующей бациллярной или протозойной дизентерией.
В крови, помимо анемии, отмечается лейко- и нейтропения с ядерным сдвигом влево и характерным изменением лейкоцитарного профиля. Лимфоцитоз и моиоцптоз, описываемые как важные признаки малярии, имеют относительный характер. В тяжелых случаях наблюдаются анэозинофилия и моноцитоз. РОЭ повышена.
Информация на сайте подлежит консультации лечащим врачом и не заменяет очной консультации с ним.
См. подробнее в пользовательском соглашении.
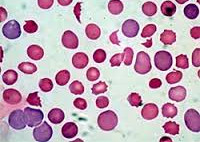
Гемолитическая анемия – патология эритроцитов, отличительным признаком которой является ускоренное разрушение красных кровяных телец с высвобождением повышенного количества непрямого билирубина. Для данной группы заболеваний типично сочетание анемического синдрома, желтухи и увеличения размеров селезенки. В процессе диагностики исследуется общий анализ крови, уровень билирубина, анализ кала и мочи, УЗИ органов брюшной полости; проводится биопсия костного мозга, иммунологические исследования. В качестве методов лечения используется медикаментозная, гемотрансфузионная терапия; при гиперспленизме показана спленэктомия.
МКБ-10


Общие сведения
Гемолитическая анемия (ГА) - малокровие, обусловленное нарушением жизненного цикла эритроцитов, а именно преобладанием процессов их разрушения (эритроцитолиза) над образованием и созреванием (эритропоэзом). Данная группа анемий очень обширна. Их распространенность неодинакова в различных географических широтах и возрастных когортах; в среднем патология встречается у 1% населения. Среди прочих видов анемий на долю гемолитических приходится 11%. Патология характеризуется укорочением жизненного цикла эритроцитов и их распадом (гемолизом) раньше времени (через 14-21 день вместо 100-120 суток в норме). При этом разрушение эритроцитов может происходить непосредственно в сосудистом русле (внутрисосудистый гемолиз) или в селезенке, печени, костном мозге (внесосудистый гемолиз).

Причины
Этиопатогенетическую основу наследственных гемолитических синдромов составляют генетические дефекты мембран эритроцитов, их ферментных систем либо структуры гемоглобина. Данные предпосылки обусловливают морфофункциональную неполноценность эритроцитов и их повышенное разрушение. Гемолиз эритроцитов при приобретенных анемиях наступает под влиянием внутренних факторов или факторов окружающей среды, среди которых:
- Аутоиммунные процессы. Образование антител, агглютинирующих эритроциты, возможно при гемобластозах (остром лейкозе, хроническом лимфолейкозе, лимфогранулематозе), аутоиммунной патологии (СКВ, неспецифическом язвенном колите), инфекционных заболеваниях (инфекционном мононуклеозе, токсоплазмозе, сифилисе, вирусной пневмонии). Развитию иммунных гемолитических анемий могут способствовать посттрансфузионные реакции, профилактическая вакцинация, гемолитическая болезнь плода.
- Токсическое действие на эритроциты. В ряде случаев острому внутрисосудистому гемолизу предшествует отравление мышьяковистыми соединениями, тяжелыми металлами, уксусной кислотой, грибными ядами, алкоголем и др. Вызывать разрушение клеток крови может прием определенных лекарств (противомалярийных препаратов, сульфаниламидов, производных нитрофуранового ряда, анальгетиков).
- Механическое повреждение эритроцитов. Гемолиз эритроцитов может наблюдаться при тяжелых физических нагрузках (длительной ходьбе, беге, лыжном переходе), при ДВС-синдроме, малярии, злокачественной артериальной гипертензии, протезировании клапанов сердца и сосудов, проведении гипербарической оксигенации, сепсисе, обширных ожогах. В этих случаях под действием тех или иных факторов происходит травматизация и разрыв мембран изначально полноценных эритроцитов.

Патогенез
Классификация
В гематологии гемолитические анемии подразделяются на две большие группы: врожденные (наследственные) и приобретенные. Наследственные ГА включают следующие формы:
- эритроцитарные мембранопатии (микросфероцитоз – болезнь Минковского-Шоффара, овалоцитоз, акантоцитоз) – анемии, обусловлены структурными аномалиями мембран эритроцитов
- ферментопении (энзимопении) – анемии, вызванные дефицитом тех или иных ферментов (глюкозо-6-фосфатдегидрогеназы, пируваткиназы и др.)
- гемоглобинопатии- анемии, связанные с качественными нарушениями структуры гемоглобина или изменением соотношения его нормальных форм (талассемия, серповидно-клеточная анемия).
Приобретенные ГА подразделяются на:
- мембранопатии приобретенные (пароксизмальная ночная гемоглобинурия – б-нь Маркиафавы-Микели, шпороклеточная анемия)
- иммунные (ауто- и изоиммунные) – обусловлены воздействием антител
- токсические – анемии, обусловленные воздействием химических веществ, биологических ядов, бактериальных токсинов
- механические - анемии, вызванные механическим повреждением структуры эритроцитов (тромбоцитопеническая пурпура, маршевая гемоглобинурия)
Симптомы
Наследственные мембранопатии, ферментопении и гемоглобинопатии
Наиболее распространенной формой данной группы анемий является микросфероцитоз, или болезнь Минковского-Шоффара. Наследуется по аутосомно-доминантному типу; обычно прослеживается у нескольких представителей семьи. Дефектность эритроцитов обусловлена дефицитом в мембране актомиозиноподобного белка и липидов, что приводит к изменению формы и диаметра эритроцитов, их массивному и преждевременному гемолизу в селезенке. Манифестация микросфероцитарной ГА возможна в любом возрасте (в младенчестве, юношестве, старости), однако обычно проявления возникают у детей старшего возраста и подростков. Тяжесть заболевания варьирует от субклинического течения до тяжелых форм, характеризующихся часто повторяющимися гемолитическими кризами. В момент криза нарастает температура тела, головокружение, слабость; возникают боли в животе и рвота.
Основным признаком микросфероцитарной гемолитической анемии служит желтуха различной степени интенсивности. Вследствие высокого содержания стеркобилина кал становится интенсивно окрашенным в темно-коричневый цвет. У пациентов с болезнь Минковского-Шоффара наблюдается склонность к образованию камней в желчном пузыре, поэтому часто развиваются признаки обострения калькулезного холецистита, возникают приступы желчной колики, а при закупорке холедоха конкрементом - обтурационная желтуха. При микросфероцитозе во всех случаях увеличена селезенка, а у половины пациентов – еще и печень. Кроме наследственной микросфероцитарной анемии, у детей часто встречаются другие врожденные дисплазии: башенный череп, косоглазие, седловидная деформация носа, аномалии прикуса, готическое нёбо, полидактилия или брадидактилия и пр. Пациенты среднего и пожилого возраста страдают трофическими язвами голени, которые возникают в результате гемолиза эритроцитов в капиллярах конечностей и плохо поддаются лечению.
Приобретенные гемолитические анемии
Среди различных приобретенных вариантов чаще других встречаются аутоиммунные анемии. Для них общим пусковым фактором выступает образование антител к антигенам собственных эритроцитов. Гемолиз эритроцитов может носить как внутрисосудистый, так и внутриклеточный характер. Гемолитический криз при аутоиммунной анемии развивается остро и внезапно. Он протекает с лихорадкой, резкой слабостью, головокружением, сердцебиением, одышкой, болями в эпигастрии и пояснице. Иногда острым проявлениям предшествуют предвестники в виде субфебрилитета и артралгий. В период криза стремительно нарастает желтуха, не сопровождающаяся кожным зудом, увеличивается печень и селезенка. При некоторых формах аутоиммунных анемий больные плохо переносят холод; в условиях низких температур у них может развиваться синдром Рейно, крапивница, гемоглобинурия. Вследствие недостаточности кровообращения в мелких сосудах возможны осложнения в виде гангрены пальцев ног и рук.
Осложнения
Каждый вид ГА имеет свои специфические осложнения: например, ЖКБ – при микросфероцитозе, печеночная недостаточность – при токсических формах и т.д. К числу общих осложнений относятся гемолитические кризы, которые могут провоцироваться инфекциями, стрессами, родами у женщин. При остром массивном гемолизе возможно развитие гемолитической комы, характеризующейся коллапсом, спутанным сознанием, олигурией, усилением желтухи. Угрозу жизни больного несут ДВС-синдром, инфаркт селезенки или спонтанный разрыв органа. Неотложной медицинской помощи требуют острая сердечно-сосудистая и почечная недостаточность.
Диагностика
Определение формы ГА на основе анализа причин, симптоматики и объективных данных относится к компетенции гематолога. При первичной беседе выясняется семейный анамнез, частота и тяжесть протекания гемолитических кризов. В процессе осмотра оценивается окраска кожных покровов, склер и видимых слизистых, производится пальпация живота для оценки величины печени и селезенки. Сплено- и гепатомегалия подтверждается при проведении УЗИ печени и селезенки. Лабораторный диагностический комплекс включает:
- Исследование крови. Изменения в гемограмме характеризуются нормо- или гипохромной анемией, лейкопенией, тромбоцитопенией, ретикулоцитозом, ускорением СОЭ. В биохимических пробах крови определяется гипербилирубинемия (увеличение фракции непрямого билирубина), увеличение активности лактатдегидрогеназы. При аутоиммунных анемиях большое диагностическое значение имеет положительная проба Кумбса.
- Анализы мочи и кала. Исследование мочи выявляет протеинурию, уробилинурию, гемосидеринурию, гемоглобинурию. В копрограмме повышено содержание стеркобилина.
- Миелограмму. Для цитологического подтверждения выполняется стернальная пункция. Исследование пунктата костного мозга обнаруживает гиперплазию эритроидного ростка.
В процессе дифференциальной диагностики исключаются гепатиты, цирроз печени, портальная гипертензия, гепатолиенальный синдром, порфирии, гемобластозы. Пациента консультируют гастроэнтеролог, клинический фармаколог, инфекционист и другие специалисты.

Лечение
Различные формы ГА имеют свои особенности и подходы к лечению. При всех вариантах приобретенной гемолитической анемии необходимо позаботиться об устранении влияния гемолизирующих факторов. Во время гемолитических кризов больным необходимы инфузии растворов, плазмы крови; витаминотерапия, по необходимости – гормоно- и антибиотикотерапия. При микросфероцитозе единственно эффективным методом, приводящим к 100 % прекращению гемолиза, является спленэктомия.
При аутоиммунной анемии показана терапия глюкокортикоидными гормонами (преднизолоном), сокращающая или прекращающая гемолиз. В некоторых случаях требуемый эффект достигается назначением иммунодепрессантов (азатиоприна, 6-меркаптопурина, хлорамбуцила), противомалярийных препаратов (хлорохина). При резистентных к медикаментозной терапии формах аутоиммунной анемии выполняется спленэктомия. Лечение гемоглобинурии предполагает переливание отмытых эритроцитов, плазмозаменителей, назначение антикоагулянтов и антиагрегантов. Развитие токсической гемолитической анемии диктует необходимость проведения интенсивной терапии: дезинтоксикации, форсированного диуреза, гемодиализа, по показаниям – введение антидотов.
Прогноз и профилактика
Течение и исход зависят от вида анемии, тяжести протекания кризов, полноты патогенетической терапии. При многих приобретенных вариантах устранение причин и полноценное лечение приводит к полному выздоровлению. Излечения врожденных анемий добиться нельзя, однако возможно достижение длительной ремиссии. При развитии почечной недостаточности и других фатальных осложнений прогноз неблагоприятен. Предупредить развитие ГА позволяет профилактика острых инфекционных заболеваний, интоксикаций, отравлений. Запрещается бесконтрольное самостоятельное использование лекарственных препаратов. Необходимо тщательная подготовка пациентов к гемотрансфузиям, вакцинации с проведением всего комплекса необходимых обследований.
4. Клинические рекомендации по диагностике и лечению аутоиммунных гемолитический анемий/ Цветаева Н.В., Никулина О.Ф. - 2014.
Малярия – трансмиссивная протозойная инфекция, вызываемая патогенными простейшими рода Plasmodium и характеризующаяся приступообразным, рецидивирующим течением. Специфическими симптомами малярии служат повторные приступы лихорадки, гепатоспленомегалия, анемия. В течении лихорадочных приступов у больных малярией четко прослеживаются сменяющие друг друга стадии озноба, жара и пота. Диагноз малярии подтверждается при обнаружении малярийного плазмодия в мазке или толстой капле крови, а также результатами серологической диагностики. Для этиотропной терапии малярии используются специальные противопротозойные препараты (хинин и его аналоги).
Общие сведения
Малярия (перемежающаяся лихорадка, болотная лихорадка) – группа паразитарных заболеваний человека, возбудителями которых выступают различные виды малярийного плазмодия, поражающего преимущественно эритроциты крови и ретикулоэндотелиальную систему. Малярия протекает с лихорадочными пароксизмами, гепатолиенальным и анемическим синдромом. Малярия широко распространена в странах Экваториальной Африки, Юго-Восточной Азии, Океании, Центральной и Южной Америки. Ежегодно в мире регистрируется 350-500 млн. новых инвазий и порядка 1,3-3 млн. летальных исходов от малярии. Высокая заболеваемость малярией в мире объясняется развитием резистентности плазмодиев к специфической терапии, а переносчиков протозойной инфекции – к действию инсектицидов. В связи с увеличением миграционных и туристических потоков завозные случаи малярии все чаще встречаются на территории Европы, в т. ч. в России.

Причины малярии
Малярию вызывают паразитические простейшие, принадлежащие к классу споровиков, роду Plasmodium (малярийные плазмодии). Заболевание человека вызывают 4 вида плазмодиев: P. Vivax (возбудитель трехдневной малярии), P. Malariae (возбудитель четырехдневной малярии), P.falciparum (возбудитель тропической малярии) и P. Ovale (возбудитель овале-малярии, сходной с трехдневной).
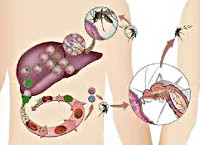
Малярийные плазмодии проходят сложный жизненный цикл, включающий бесполое развитие (шизогонию) в организме промежуточного хозяина - человека и половое развитие (спорогонию) в организме главного хозяина - самок комаров Anopheles. Инфицирование комаров происходит при укусах человека, больного малярией или паразитоносителя. При кровососании в желудок комара попадают мужские и женские половые клетки плазмодиев (микро-и макрогаметоциты); здесь происходит их оплодотворение с образованием зиготы, а затем ооцисты. В результате многократного деления ооциста превращается в инвазионные формы плазмодиев - спорозоиты, которые проникают в слюнные железы комара и могут там находиться в течение 2-х месяцев.
Инфицирование человека происходит при укусе инвазированной самкой комара, со слюной которой в кровь промежуточного хозяина проникают спорозоиты. В организме человека возбудитель малярии проходит тканевую и эритроцитарную фазы своего бесполого развития. Тканевая фаза (экзоэритроцитарная шизогония) протекает в гепатоцитах и тканевых макрофагах, где спорозоиты последовательно трансформируются в тканевые трофозоиты, шизонты и мерозоиты. По окончании этой фазы мерозоиты проникают в эритроциты крови, где протекает эритроцитарная фаза шизогонии. В клетках крови мерозоиты превращается в трофозоиты, а затем в шизонты, из которых в результате деления вновь образуются мерозоиты. В конце такого цикла эритроциты разрушаются, а высвободившиеся мерозоиты внедряются в новые эритроциты, где цикл превращений повторяется вновь. В результате 3-4-х эритроцитарных циклов, образуются гаметоциты – незрелые мужские и женские половые клетки, дальнейшее (половое) развитие которых протекает в организме самки комара Anopheles.
Учитывая особенности развития плазмодия, становится очевидным, что основным путем передачи малярии от человека человеку является трансмиссивный, реализуемый посредством укусов самками комара рода Anopheles. Вместе с тем, возможна трансплацентарная передача инфекции во время беременности, а также парентеральное заражение при переливании донорской крови, взятой от паразитоносителей. В эндемических очагах к малярии в большей степени восприимчивы дети и приезжие. Пик заболеваемости малярией совпадает с сезоном активности комаров и приходится на летне-осеннее время.
Пароксизмальный характер лихорадочных приступов при малярии связан с эритроцитарной фазой развития малярийного плазмодия. Развитие лихорадки совпадает с распадом эритроцитов, высвобождением в кровь мерозоитов и продуктов их обмена. Чужеродные для организма субстанции оказывают общетоксическое воздействие, вызывая пирогенную реакцию, а также гиперплазию лимфоидных и ретикулоэндотелиальных элементов печени и селезенки, приводя к увеличению этих органов. Гемолитическая анемия при малярии является следствием распада эритроцитов.
Симптомы малярии
В течении малярии выделяют инкубационный период, период первичных острых проявлений, вторичный латентный период и период рецидивов. Инкубационный период при трехдневной малярии и овале-малярии длится 1-3 недели, при четырехдневной - 2-5 недель, при тропической - около 2-х недель. Типичными клиническими синдромами для всех форм малярии служат лихорадочный, гепатолиенальный и анемический.
Через 1-2 часа фаза озноба сменяется жаром, что совпадает с повышением температуры тела до 40-41 °С. Возникают гиперемия, гипертермия, сухость кожи, инъекция склер, жажда, увеличение печени и селезенки. Может отмечаться возбуждение, бред, судороги, потеря сознания. На высоком уровне температура может удерживаться до 5-8 и более часов, после чего происходит профузное потоотделение, резкое снижение температуры тела до нормального уровня, что знаменует собой окончание приступа лихорадки при малярии. При трехдневной малярии приступы повторяются каждый 3-й день, при четырехдневной – каждый 4-й день и т. д. К 2-3-й неделе развивается гемолитическая анемия, появляется субиктеричность кожи и склер при нормальной окраске мочи и кала.
Своевременное лечение позволяет остановить развитие малярии после 1-2 приступов. Без специфической терапии продолжительность трехдневной малярии составляет около 2 лет, тропической - около 1 года, овале-малярии - 3-4 года. В этом случае после 10-14 пароксизмов инфекция переходит в латентную стадию, которая может длиться от нескольких недель до 1 года и дольше. Обычно через 2-3 месяца видимого благополучия развиваются ранние рецидивы малярии, которые протекают так же, как острые проявления болезни. Поздние рецидивы возникают через 5-9 месяцев - в этот период приступы имеют более легкое течение.
Осложнения малярии
Тяжелыми, порой жизнеугрожающими осложнениями малярии могут служить малярийная кома, малярийный алгид, разрыв селезенки, отек мозга, ОПН, ДВС-синдром, психические нарушения. Малярийной комой чаще всего осложняется течение тропической малярии. Развитие комы связано с нарушениями микроциркуляции головного мозга в результате образования паразитарных тромбов, состоящих из эритроцитов, зараженных шизонтами. В течении малярийной комы выделяют периоды сомноленции (сонливость, адинамия), сопора (резкая заторможенность, снижение рефлексов) и глубокой комы (отсутствие сознания и рефлексов). Летальный исход при возникновении данного осложнения наступает в 96-98% случаев.
Малярийный алгид сопровождается развитием коллаптоидного состояния с артериальной гипотонией, нитевидным пульсом, гипотермией, снижением сухожильных рефлексов, бледностью кожных покровов, холодным потом. Нередко возникают поносы и явления дегидратации. Признаки разрыва селезенки при малярии возникают спонтанно и включают в себя кинжальную боль в животе с иррадиацией в левое плечо и лопатку, резкую бледность, холодный пот, снижение АД, тахикардию, нитевидный пульс. По данным УЗИ выявляется свободная жидкость в брюшной полости. При отсутствии экстренного оперативного вмешательства быстро наступает смерть от острой кровопотери и гиповолемического шока.
Отек мозга развивается при злокачественной, молниеносной форме трехдневной малярии, чаще у детей-дошкольников и подростков. Возникает на высоте лихорадочного пароксизма и характеризуется сильной головной болью, судорогами с потерей сознания, выделением пены изо рта и скорой гибелью пациента. Развитие острой почечной недостаточности при малярии связано с массивным внутрисосудистым гемолизом эритроцитов, нарушением почечного кровообращения, интенсивной гемоглобинурией. Обычно является исходом гемоглобинурийной лихорадки. Специфическим осложнением тропической малярии выступают психические расстройства, включающие в себя психомоторное возбуждение, бред, галлюцинации и т. д.
Диагностика малярии
Фундамент клинической диагностики малярии составляет триада признаков: приступообразная интермиттирующая лихорадка, повторяющаяся каждые 48 или 72 часов, гепатоспленомегалия, гемолитическая анемия. Одновременно выясняется факт посещения больным эндемичных регионов, перенесенных гемотрансфузий и парентеральных вмешательств в течение последних 2-3-х месяцев.
Специфическим лабораторным методом диагностики малярии служит микроскопия толстой капли крови, позволяющая обнаружить наличие и количество паразитов. Качественную идентификацию вида плазмодия и стадию шизогонии проводят путем исследования на малярийный плазмодий мазка крови. Забор крови лучше производить на высоте лихорадочного приступа. Вспомогательную роль в выявлении малярии играют серологические методы – РИФ, РФА, РНГА. В плане дифференциальной диагностике наибольшее значение имеет исключение у лихорадящего больного бруцеллеза, возвратного тифа, лейшманиоза, сепсиса, туберкулеза, менингоэнцефалита, гемолитической желтухи, цирроза печени, лейкоза и др.
Лечение малярии
Больные с подозрением на малярию госпитализируются в инфекционный стационар с назначением строгого постельного режима, обильного питья, инфузионной терапии, общеукрепляющего и симптоматического лечения. При необходимости больным проводится гемосорбция и гемодиализ.
Первоначально для специфической химиотерапии малярии использовался хинин, выделенный из коры хинного дерева. В настоящее время создано большое количество синтетических препаратов, однако из-за быстрого развития резистентности паразитов к синтетическим лекарствам, хинин до сих пор не утратил своей актуальности. В зависимости от оказываемого действия противомалярийные препараты делятся на тканевые шизонтоциды, воздействующие на тканевые формы малярийного плазмодия (хиноцид, примахин) и гематоциды, воздействующие на эритоцитарные формы возбудителя (хлорохин, пириметамин, мепакрин, хинин и др.). Они назначаются в различных сочетаниях и по определенной схеме в зависимости от формы и тяжести течения малярии. Так, при трехдневной малярии обычно проводится 3-дневный курс лечения хлорохином, затем 10-дневный прием примахина или хиноцида для уничтожения тканевых форм паразита. Возможны и другие схемы противомалярийной терапии.
Прогноз и профилактика малярии
Своевременная и правильная терапия малярии приводит к быстрому купированию клинических проявлений. Летальные исходы при проведении лечения возникают примерно в 1% случаев, как правило, при осложненных формах тропической малярии.
Профилактика малярии проводится в двух направлениях: уничтожение комаров-переносчиков возбудителей и индивидуальная защита. Первое направление включает обработку территорий инсектицидами. Второе - использование средств индивидуальной защиты (кремов, лосьонов, противомоскитных сеток), проведение специфической химиопрофилактики лицам, совершающим поездки в районы, неблагополучные по малярии. С целью раннего выявления больных и паразитоносителей всем пациентам с лихорадкой неясного генеза должна проводиться микроскопия крови на малярию.
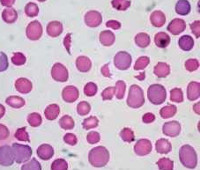
Гемолитические анемии у детей – это группа разных по патогенезу заболеваний, главным признаком которых является уменьшение продолжительности жизни эритроцитов, развитие их гемолиза. Клиническая картина имеет общие симптомы: возникновение желтухи, спленомегалии, реже гепатомегалии, тёмное окрашивание мочи. Для лабораторных исследований характерно снижение гемоглобина, ретикулоцитоз, повышение уровня билирубина (в основном за счет непрямой фракции), повышение ЛДГ, уробилиногена мочи. Метод лечения зависит от этиологии анемии: возможна медикаментозная терапия, проведение гемотрансфузий, спленэктомия при гиперспленизме.
МКБ-10
Общие сведения
Гемолитические анемии – это эритроцитопатии, при которых имеет место стойкое или массированное преобладание разрушения эритроцитов над их образованием. Среди всех анемий у детей встречаются в 11,5% случаев, в 5,3% ‒ от общего числа заболеваний крови. В числе больных незначительно преобладают лица мужского пола. Чаще диагностируются наследственные формы (76,6%) и особенно – наследственная сфероцитарная гемолитическая анемия (56,4%). Некоторые формы связывают с этнической принадлежностью: талассемия характерна для азиатов, жителей Кавказский республик, побережья Средиземного моря; серповидноклеточная анемия – для лиц негроидной расы, дефицит Г-6-ФД – для представителей еврейской национальности. Гемолитическая болезнь плода на территории РФ встречается у 0,6% новорожденных.

Причины
Этиология у наследственных и приобретенных гемолитических анемий различна. При наследственных анемиях патологии в строении эритроцитов запрограммированы на генетическом уровне: известно 16 вариантов с аутосомно-доминантным типом наследования, 29 – с рецессивным, 7 разновидностей – с Х-сцепленным. Все причины, которые приводят к гемолизу, разделяются на внеклеточные и внутриклеточные.
Внеклеточные причины типичны для анемий приобретенного характера. В этом случае эритроциты дефектов не имеют, а разрушаются под воздействием внешних факторов: ретикулоэндотелиальной гиперактивности (гиперспленизм), механических и химических нарушений целостности эритроцитов, иммунологических отклонений (под воздействием антител), паразитарной инвазии, витаминодефицита, некоторых инфекций. Внутриклеточные причины гемолиза – это нарушение структуры и функций эритроцитов, такие как дефекты эритроцитарного метаболизма, строения гемоглобина, мембран клеток.
Патогенез
В патогенезе наследственных гемолитические анемии главную роль играет внесосудистый гемолиз – разрушение эритроцитов происходит в клетках ретикулоэндотелиальной системы. Высвобождаемый гем распадается до несвязанного билирубина. В печени такое количество билирубина не может полностью связаться с глюкуроновой кислотой, развивается гипербилирубинемия. Клинически проявляется нарастанием желтухи, формированием у детей в раннем возрасте камней желчного пузыря, содержащих билирубинат кальция. В кишечнике билирубин метаболизируется в уробилин, избыток которого окрашивает мочу в темный цвет. Гиперактивность селезенки приводит к увеличению ее размеров с развитием гиперспленизма.
Внутрисосудистый гемолиз возникает при приобретенных гемолитических анемиях. Происходит распад эритроцитов в кровотоке, высвободившееся количество гемоглобина не связывается полностью с гаптоглобином в плазме, вследствие чего развивается гемоглобинурия. Избыток гемосидерина, который образуется в селезенке, почках, печени, способствует развитию гемосидероза данных органов и нарушению их функции. Компенсаторное усиление эритропоэза вызывает ретикулоцитоз. Гиперплазия костного мозга ведет к деформации черепа и скелета у детей.
Классификация
Общепринятая классификация гемолитических анемии у детей предложена Идельсоном Л.И. в 1975 году. Согласно ей выделяются две основные группы: наследственные и приобретенные, в каждой из которых обозначаются этиопатогенетические формы. Наследственные анемии классифицируются по локализации генетической аномалии, которая приводит к неполноценности эритроцитов. К ним относятся:
- Мембранопатии. Гемолитические анемии связаны с дефектами белковых и липидных комплексов мембран эритроцитов: врожденная эритропоэтическая порфирия, наследственные эллиптоцитоз и сфероцитоз – болезнь Минковского-Шоффара.
- Ферментопатии. Гемолиз обусловлен дефицитом эритроцитарных ферментов, которые обеспечивают пентозо-фосфатный цикл, гликолиз, синтез АТФ и порфиринов, обмен нуклеотидов и глютатиона.
- Гемоглобинопатии. Патологические состояния, вызванные структурными нарушениями гемоглобина и изменением синтеза его цепей: талассемия, серповидноклеточная анемия, эритропорфирия.
Приобретенные гемолитические анемии связаны с влиянием различных факторов, которые способствуют гемолизу в сосудистом русле и в органах ретикулоэндотелиальной системы. Среди них выделяют:
- Иммунные формы. Причиной гибели эритроцитов является выработка к ним антител. При изоиммунном варианте в организм проникают антиэритроцитарные антитела (гемолитическая болезнь новорожденных) или попадают красные кровяные клетки, к которым у больного есть сенсибилизация (посттрансфузионные анемии). Для гетероиммунных форм характерна фиксация на эритроцитах медикаментозных препаратов (пенициллины, сульфаниламиды, хинидин) или вирусов, что делает их антигеном. Аутоиммунные анемии вызваны образованием антител к собственным нормальным эритроцитам при онкологических заболеваниях, лимфолейкозе, миеломной болезни, системной красной волчанке, а также выработкой тепловых и холодовых антител.
- Механические формы. Гемолиз вызван механическим разрушением эритроцитов. Прямое повреждение возможно искусственными сердечными клапанами, паразитарной инвазией (малярийный плазмодий, токсоплазма), бактериальными токсинами (β-гемолитический стрептококк, менингококк), ядами змей, насекомых. При маршевой гемоглобинурии и анемии спортсменов после длительной интенсивной нагрузки гемолиз происходит в капиллярах нижних конечностей. Гиперспленизм является причиной разрушения нормальных эритроцитов в селезенке.
Симптомы
Клиническая картина, развивающаяся при разных типах гемолиза, имеет общие черты. Для приобретенных гемолитических анемий характерно острое нарастание симптоматики. Большинство наследственных анемий протекает хронически с периодическими гемолитическими кризами. Для развития криза необходимо воздействие триггера: переохлаждения, употребления токсичных препаратов, инфекционного заболевания. Первыми симптомами являются общая слабость, лихорадка, диспепсические расстройства, головная боль. В дальнейшем нарастают признаки билирубиновой интоксикации: иктеричность слизистых оболочек и желтушность кожи; появляются тяжесть, дискомфорт в верхних отделах живота из-за гепато- и спленомегалии, потемнение мочи - от розового до почти черного цвета. На фоне анемизации нарастает бледность с восковидным оттенком, появляются ощущения сердцебиения и перебоев в работе сердца. В тяжелых случаях развивается олигурия (уменьшение количества выделяемой мочи) и анурия, вплоть до шока.
Осложнения
При разных гемолитических анемиях возможны типичные только для них осложнения. Новорожденные с тяжелой гипербилирубинемией, вызванной наследственными формами, угрожаемы по развитию ядерной желтухи. К трем-четырем годам есть риск возникновения холестаза, хронического гепатита, цирроза печени. Большое количество гемотрансфузий у лиц с тяжелым течением способствует гемосидерозу селезенки, костного мозга, печени. Инфицирование парвовирусом В19 больных талассемией, серповидно-клеточной анемией ведет к фатальным последствиям – развитию арегенераторного криза. Для всех гемолитических состояний грозными осложнениями являются диссеминированное внутрисосудистое свертывание, острая сердечная и почечная недостаточность, анемическая кома.
Диагностика
Диагностика гемолитических анемий в педиатрии имеет некоторые особенности. После 12 месяцев в крови ребенка исчезают черты, характерные для неонатального типа кроветворения: макроцитоз, фетальный гемоглобин, пониженная минимальная осмотическая стойкость эритроцитов, нестабильность уровня ретикулоцитов. Поэтому точное типирование гемолитической анемии возможно только после этого возраста. В диагностике принимают участие педиатр и детский гематолог. В план обследования должны быть включены:
- Сбор анамнеза и общий осмотр. Выясняется этническая принадлежность, наличие у родственников гемолитических анемий, желчнокаменной болезни, история беременности и родов матери, группа крови, резус-фактор родителей. Педиатр осматривает ребенка на предмет выявления желтухи, типичной бледности, стигм дизэмбриогенеза; проводит пальпацию живота для выявления гепато-, спленомегалии, аускультацию сердца с целью выслушивания систолического шума на верхушке сердца, учащения сердцебиения.
- Клинические анализы. Общий анализ крови проводится с определением морфологии эритроцитов, лейкоцитов и тромбоцитов. При исследовании выявляются снижение гемоглобина, атипичные формы эритроцитов (при мембранопатиях и гемоглобинопатиях), наличие ретикулоцитов (как признака напряжения эритропоэза), тельца Гейнца-Эрлиха (при дефиците Г6ФД), повышение СОЭ. В общем анализе мочи отмечается повышение уробилина, гемоглобинурия.
- Биохимия крови. Для биохимического анализа типичны гипербилирубинемия, повышение ЛДГ, при внутрисосудистом гемолизе – гипергемоглобинемия, гипогаптоглобинемия. Прямая проба Кумбса (прямой антиглобулиновый тест) положительна при наличии аутоантител к поверхности эритроцитов, характерных для иммунных гемолитических анемий. Но при массивном гемолизе, а также при холодовых и гемолизиновых формах АИГА, вызванных IgА или IgM- аутоантителами, проба может быть отрицательной.
- Инструментальные методы. УЗИ либо КТ органов брюшной полости с высокой точностью определяют увеличения размер печени, селезенки, их структуру, состояние желчевыводящей системы. Трепанобиопсия костного мозга проводится с целью определения типа эритропоэза (нормо-, мегало- или сидеробластный), а также исключения патологии со стороны костного мозга (апластическая анемия, лейкоз, метастатическое поражение при злокачественных образованиях).
Специфические методы исследования. Определение длительности жизни эритроцитов может проводиться методами дифференциальной агглютинации, продукции угарного газа, проточной цитометрией (клеточное биотинилирование и др.), прямыми радиоизотопическими исследованиями. Генетические исследования и определение мутаций уточняют причины наследственного гемолиза.
Лечение
Лечение гемолитической анемии проводится в стационарных условиях, под наблюдением педиатра, гематолога, при переливаниях крови – трансфузиолога. Лечебный подход зависит от тяжести состояния пациента, периода заболевания (гемолитический криз или ремиссия), причины возникновения гемолиза. Методы терапии можно объединить в следующие группы:
- Медикаментозная терапия. Назначается как этиотропно, так и симптоматически. При увеличении селезенки и гепатомегалии применяют глюкокортикоидные гормоны. Аутоиммунные анемии требуют назначения цитостатиков, эритропоэтина. При дефиците фолатов назначают цианокобаламин и фолиевую кислоту. Гемолитический криз требует инфузионной терапии, снятия симптомов интоксикации. Для выведения избытка железа больным проводятся курсы хелаторной терапии (десферал). Во многих случаях с профилактической целью используются желчегонные средства.
- Гемотрансфузии. Переливание компонентов крови проводят в стационарных условиях при выраженной анемии по жизненным показаниям. Трансфузия эритроцитарной массы осуществляется строго по индивидуальному подбору, предпочтительно использовать отмытые и размороженные эритроциты. Длительная гемотрансфузионная терапия может осложниться избыточным отложением железа в тканях.
- Хирургическое лечение. Спленэктомия – хирургическое удаление селезенки – используется при спленомегалии, если лекарственная терапия не имеет эффекта. Метод особенно эффективен при гиперспленизме, когда секвестрация эритроцитов происходит в селезенке. При гемолитических анемиях часто развивается холелитиаз, который требует оперативного удаления желчного пузыря (холецистэктомии) или экстракции конкремента из желчных путей.
Прогноз и профилактика
Прогноз при гемолитических анемиях у детей зависит от этиологического фактора. Приобретенные формы и большинство наследственных имеют благоприятный исход при своевременно начатом лечении и соблюдении мер профилактики. В качестве системы питания используется диета №5 по Певзнеру, предназначенная для снижения нагрузки на билиарный тракт. Необходим охранительный режим: избегание перегрева и переохлаждений; исключение контактов с инфекционными больными; ознакомление со списком препаратов и веществ, которые могут вызвать гемолиз (хинин, сульфаниламиды, левомицетин, аспирин, нитрофураны и прочие); определение показаний и строгих противопоказаний к вакцинации (при дефиците глюкозо-6фосватдегидрогеназы, аутоиммунных анемиях иммунизация запрещена, при сфероцитозе – рекомендована).
3. Классификация и диагностика анемий у детей/ Румянцев А.Г.// Вопросы современной педиатрии. - 2011 - Т.10, №1.
Клиника малярийного приступа. Анемия при малярии
Малярийные приступы обычно начинаются в одно и то же время суток, в утренние часы, что может помогать в дифференциальной диагностике малярии сдругими остролихорадочными заболеваниями, при которых максимальное повышение температуры наблюдается обычно во второй половине дня. У больных тропической малярией в начале болезни часто наблюдается атипичная лихорадка неправильного, послабляющего ремиттирующего типа, что связано с разным временем окончания генерации шизогонии у возбудителя, вследствие чего происходит наслоение приступов друг на друга и изменение характера температуры в течение суток.
При отсутствии этиотропного лечения приступы малярии могут повторяться до 12-14 раз, а затем самостоятельно прекращаться (за исключением случаев тропической малярии); после чего наступает латентный период. Паразитемия в это время уменьшается, но не исчезает. В латентный период, длящийся от нескольких дней до 2-3 мес, у части больных вновь нарастает паразитемия и наступают ранние рецидивы малярии (один или несколько), по клинической картине похожие на первый приступ.
Латентный период при трехдневной и овале-малярии может удлиняться до 6-8 мес и более, после чего вновь повторяются приступы (поздние экзоэритроцитарные рецидивы). При тропической и четырехдневной малярии поздние рецидивы не наблюдаются.
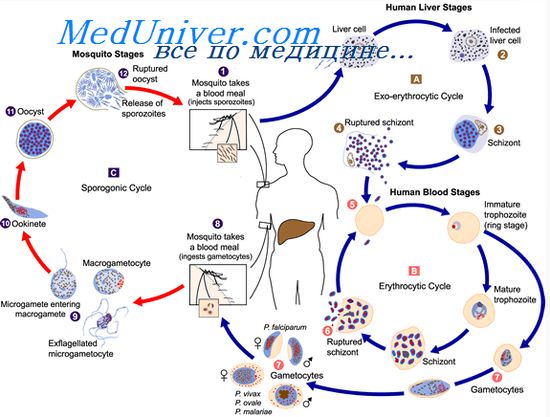
Наиболее выраженные клинические изменения при малярии (особенно при ее рецидивах) наблюдаются со стороны селезенки, печени, ЦНС и крови. Печень и селезенка становятся увеличенными и плотноватыми; больше увеличена селезенка. Функциональное состояние печени существенно не меняется. По современным воззрениям развитие цирроза печени при хронической малярии допускается только в случаях сочетания малярии с одновременным поражением печени другой этиологии - вирусной, алиментарно-токсической и др.
Поражения ЦНС обусловлены интоксикационным синдромом, а при тропической малярии и самим паразитом, тяготеющим к рецепторам эндотелия кровеносных сосудов головного мозга. Уже давно были описаны поражения почек при малярии (Е.М. Тареев, И.М. Мадьяр) в виде острого нефрита или нефротического синдрома. Позднее показано участие в их развитии иммунокомплексных процессов (отложение в почечных клубочках иммуноглобулинов классов М и G) с участием специфических антигенов возбудителя, что приводит иногда к развитию ХПН и необратимой почечной патологии.
Гемолитическая (гипохромная) анемия является обязательным признаком малярии, начиная с ее первых приступов; она усиливается при хронической инфекции. Снижаются количество эритроцитов и содержание гемоглобина. В результате усиления эритропоэза повышается количество ретикулоцитов, появляется полихроматофилия. Снижается количество лейкоцитов с эозино- и нейтропенией, появляется относительный лимфоцитоз, а при выздоровлении - моноцитоз. При злокачественных формах малярии типичны нейтрофильный лейкоцитоз и ускоренная РОЭ.
Биохимические изменения в крови проявляются повышением непрямого билирубина, снижением холестерина, уменьшением альбуминов и увеличением гамма-глобулинов, гиперкалиемией. При малярийном гепатите увеличивается уровень прямого билирубина, повышается активность трансаминаз. При поражениях почек повышаются уровни креатинина и мочевины, появляются в моче белок, эритроциты, зернистые цилиндры.
Информация на сайте подлежит консультации лечащим врачом и не заменяет очной консультации с ним.
См. подробнее в пользовательском соглашении.
Читайте также:

