Гемолиз эритроцитов при малярии
Обновлено: 24.04.2024
Трансфузионная гемолитическая реакция (ТГР) — гемолиз эритроцитов реципиента или донора (редко), возникающий при переливании крови и её компонентов. Реакции могут быть иммунной или неиммунной природы.
Этиология и патогенез • Иммунные реакции при несовместимости по системе АВ0 • Деструкция донорских эритроцитов реципиентными несовместимыми изоантителами • Изосенсибилизация, вызванная повторными трансфузиями • Изосенсибилизация, возникшая при предыдущих беременностях.
Клиническая картина • Немедленные (внутрисосудистые) ТГР •• Тревожное состояние, беспокойство, чувство страха •• Гиперемия кожи •• Болевой синдром — боли в животе, груди •• Сердечно-сосудистый синдром — тахикардия, артериальная гипотензия •• Респираторный синдром — одышка, бронхоспазм •• Лихорадка, озноб • При одновременном введении компонентов крови и средств для наркоза клиническая картина ТГР стёрта • ТГР замедленного типа (внесосудистые) развиваются через 2–14 дней •• Лихорадка •• Анемия •• Синдром желтухи.
Лабораторные исследования • ОАК — анемия, ретикулоцитоз • Биохимический анализ крови — повышение содержания непрямого билирубина, азота, мочевины, креатинина, снижение концентрации гаптоглобина • Положительный прямой антиглобулиновый тест (тест Кумбса) • В моче — гемоглобинурия.
Дифференциальная диагностика • Аутоиммунные заболевания • Гемоглобинопатии, ферментативные дефекты эритроцитов • Гемолитические анемии (приобретённые, врождённые).
ЛЕЧЕНИЕ
Тактика ведения • Немедленное прекращение трансфузии при появлении первых признаков реакции • Лечение трансфузионной реакции в условиях реанимационного отделения • Контроль жизненно важных функций • Поддержание диуреза в объёме 100 мл/ч в течение 6–8 ч • Контроль гемостаза, коагулограммы — ранняя диагностика ДВС • Поддержание систолического АД выше 100 мм рт.ст.
Лекарственная терапия • 0, 9% р-р натрия хлорида в/в капельно при скорости введения 150–300 мл/ч • При синдроме дыхательных нарушений — увлажнённый кислород, эпинефрин • ГК (преднизолон, гидрокортизон) • Антигистаминные препараты • При артериальной гипотензии и нарушении почечного кровотока — допамин • При ДВС — гепарин • Мочегонные средства (например, фуросемид, этакриновая кислота). Некоторые клиницисты рекомендуют внутривенную инфузию маннитола: сначала 20 г (например, 100 мл 20% р-ра), затем со скоростью 10–15 мл/мин до 200 г (1 000 мл).
Осложнения • Почечная недостаточность • Правожелудочковая недостаточность.
Течение и прогноз • Обычно ТГР протекает остро и при адекватном и своевременном лечении прогностически благоприятна • Прогноз для жизни отягощает присоединение почечной недостаточности, ДВС • Тяжёлое течение — редко. Смертность при тяжёлом течении (редко) составляет 50%.
Возрастные особенности. В раннем детском и пожилом возрасте ТГР протекают гораздо тяжелее.
Профилактика • Сбор анамнеза о предшествующих трансфузиях и реакциях при них; аллергологический анамнез • Назначение гемотрансфузий по строгим показаниям • Двукратная оценка групповой, резус- и биологической совместимости переливаемой крови и крови реципиента • Проверка документации и этикеток на пакете (флаконе) с препаратом • Наблюдение за состоянием пациента во время трансфузии (измерение АД, пульса, диуреза при возможности).
Сокращение. ТГР — трансфузионная гемолитическая реакция.
МКБ-10 • T80.3 Реакция на AB0-несовместимость • T80.4 Реакция на Rh-несовместимость
Примечание. Гаптоглобин — гликопротеид сыворотки крови, взаимодействующий с Hb (при гемолизе) с образованием комплексного соединения, обладающего пероксидазной активностью и разрушаемого клетками ретикулоэндотелиальной системы с высвобождением молекулярного железа.
Код вставки на сайт
Трансфузионная гемолитическая реакция (ТГР) — гемолиз эритроцитов реципиента или донора (редко), возникающий при переливании крови и её компонентов. Реакции могут быть иммунной или неиммунной природы.
Этиология и патогенез • Иммунные реакции при несовместимости по системе АВ0 • Деструкция донорских эритроцитов реципиентными несовместимыми изоантителами • Изосенсибилизация, вызванная повторными трансфузиями • Изосенсибилизация, возникшая при предыдущих беременностях.
Клиническая картина • Немедленные (внутрисосудистые) ТГР •• Тревожное состояние, беспокойство, чувство страха •• Гиперемия кожи •• Болевой синдром — боли в животе, груди •• Сердечно-сосудистый синдром — тахикардия, артериальная гипотензия •• Респираторный синдром — одышка, бронхоспазм •• Лихорадка, озноб • При одновременном введении компонентов крови и средств для наркоза клиническая картина ТГР стёрта • ТГР замедленного типа (внесосудистые) развиваются через 2–14 дней •• Лихорадка •• Анемия •• Синдром желтухи.
Лабораторные исследования • ОАК — анемия, ретикулоцитоз • Биохимический анализ крови — повышение содержания непрямого билирубина, азота, мочевины, креатинина, снижение концентрации гаптоглобина • Положительный прямой антиглобулиновый тест (тест Кумбса) • В моче — гемоглобинурия.
Дифференциальная диагностика • Аутоиммунные заболевания • Гемоглобинопатии, ферментативные дефекты эритроцитов • Гемолитические анемии (приобретённые, врождённые).
ЛЕЧЕНИЕ
Тактика ведения • Немедленное прекращение трансфузии при появлении первых признаков реакции • Лечение трансфузионной реакции в условиях реанимационного отделения • Контроль жизненно важных функций • Поддержание диуреза в объёме 100 мл/ч в течение 6–8 ч • Контроль гемостаза, коагулограммы — ранняя диагностика ДВС • Поддержание систолического АД выше 100 мм рт.ст.
Лекарственная терапия • 0, 9% р-р натрия хлорида в/в капельно при скорости введения 150–300 мл/ч • При синдроме дыхательных нарушений — увлажнённый кислород, эпинефрин • ГК (преднизолон, гидрокортизон) • Антигистаминные препараты • При артериальной гипотензии и нарушении почечного кровотока — допамин • При ДВС — гепарин • Мочегонные средства (например, фуросемид, этакриновая кислота). Некоторые клиницисты рекомендуют внутривенную инфузию маннитола: сначала 20 г (например, 100 мл 20% р-ра), затем со скоростью 10–15 мл/мин до 200 г (1 000 мл).
Осложнения • Почечная недостаточность • Правожелудочковая недостаточность.
Течение и прогноз • Обычно ТГР протекает остро и при адекватном и своевременном лечении прогностически благоприятна • Прогноз для жизни отягощает присоединение почечной недостаточности, ДВС • Тяжёлое течение — редко. Смертность при тяжёлом течении (редко) составляет 50%.
Возрастные особенности. В раннем детском и пожилом возрасте ТГР протекают гораздо тяжелее.
Профилактика • Сбор анамнеза о предшествующих трансфузиях и реакциях при них; аллергологический анамнез • Назначение гемотрансфузий по строгим показаниям • Двукратная оценка групповой, резус- и биологической совместимости переливаемой крови и крови реципиента • Проверка документации и этикеток на пакете (флаконе) с препаратом • Наблюдение за состоянием пациента во время трансфузии (измерение АД, пульса, диуреза при возможности).
Сокращение. ТГР — трансфузионная гемолитическая реакция.
МКБ-10 • T80.3 Реакция на AB0-несовместимость • T80.4 Реакция на Rh-несовместимость
Примечание. Гаптоглобин — гликопротеид сыворотки крови, взаимодействующий с Hb (при гемолизе) с образованием комплексного соединения, обладающего пероксидазной активностью и разрушаемого клетками ретикулоэндотелиальной системы с высвобождением молекулярного железа.
Гемолиз при малярии. Лихорадка Оройя. Осложнения гемолиза.
Гемолиз на почве действия простых гемолизинов или прямого распада эритроцитов.
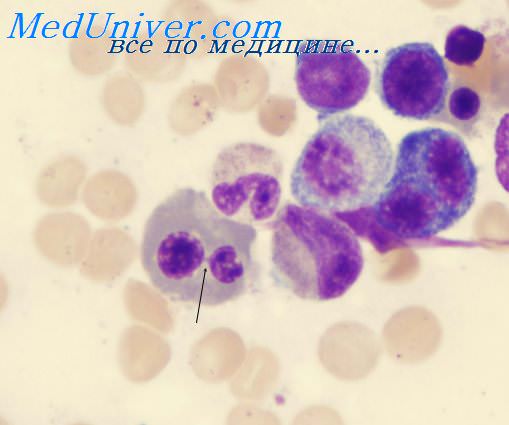
Малярия: при неясных гемолитических анемиях надо вспомнить о малярии как причинном факторе. Типичной клинической картины малярии, особенно лихорадочных приступов, может не быть. Вопрос решает нахождение в эритроцитах плазмодиев малярии. Наблюдаются повышения гемслиза в виде кризов. Резкое усиление гемолитических процессов с гемоглобинурией после лечения малярии препаратами хинина хорошо известно под названием черноводной лихорадки (гемоглобинурийная лихорадка).
Лихорадка Оройя (Oroya), обусловленная Bartonella bacilliformis; наблюдается преимущественно в Перу. Дает высокую смертность.
Бактериальные токсины при септических процессах: часто вызывают тяжелые гемолитические анемии; значительное гемолитическое действие могут оказывать при общих инфекциях особенно гемолитические стрептококки, стафилококки и коли-бациллы. При затяжном септическом эндокардите анемия также может иметь гемолитический характер.
Особенно опасна гемолитическая анемия при газовой гангрен е; она макроцитарная и может вести к гемоглобинурии.
Интоксикации химическими веществами, например, такими, как бензол, толуол, свинец, фенилгидразин, мышьяковистый водород, пирогаллол, метилхлорид, ди нитробензол, толуилендиамин, ди нитротолуол, фенилгидроксиламин, анилин, хлорноватокислыи калий, сульфаниламиды, змеиный яд. В зависимости от степени интоксикации симптомы наступают остро или постепенно. Гемоглобинурия наблюдается только в тяжелых случаях.
После массивных гемоглобинурий часто наступает анурия с последующей уремией, частично в результате закупорки отводящих канальцев почек гемоглобиновыми цилиндрами, а частично в результате интерстициального нефритического процесса. Почти всегда имеется повышение остаточного азота.
Желтуха сильнее выражена только в начале заболевания и через несколько дней постепенно исчезает.
Картина крови в тяжелых случаях может быть очень характерной в результате появления теней эритроцитов. Через несколько дней после падения гемоглобина появляется ретикулоцитоз.
Как особо характерную разновидность гемолитических анемий на почве интоксикаций химическими веществами следует подчеркнуть анемию с внутренними тельцами Эрлиха — Гейнца (Ehrlich — Heinz). Она развивается особенно часто после фенилгидразина и дериватов нитробензола, а со времени введения сульфаниламидной терапии — после некоторых препаратов (стрептоцид, сульфидин и т. д.). При массивной их дозировке в большом проценте случаев в эритроцитах находят до 300°/00так называемых телец Эрлиха— Гейнца (выявляются по методу окраски ретикулоцитов)). Клинически на первом плане — цианоз, очевидно, вследствие образования метгемоглобина. Однако химическое определение метгемоглобина из-за его летучести затруднено. Гемоглобину рия наблюдается только в очень тяжелых случаях.
Появление внутренних телец обычно предшествует развитию анемии, что может иметь важное диагностическое значение. В этих случаях позже также наступает ретикулоцитоз. В дифференциально-диагностическом отношении очень доказательно нахождение внутренних телец, что говорит о прямом повреждении эритроцитов упомянутыми веществами. В редких случаях эти тельца наблюдаются также при атрофии селезенки или после спленэктомий (Rohr). Но при этом всегда находят также тельца Жоллй.
Описано также спонтанное образование телец Эрлиха — Гейнца у маленьких детей (Willi, Gasser и Каrrеr).
При выявлении в сыворотке метгемоглобина надо помнить, что он не всегда является результатом экзогенного повреждения, но что в редких случаях наблюдаются также и семейные метгемоглобинемии.
Фавизм: в Сардинии, Сицилии и Южной Италии гемолитическая анемия может вызываться употреблением в пищу особого вида бобов — vicia faba. Клинические симптомы соответствуют анемии Ледерер — Брилля.
Гемолиз при тяжелых общих заболеваниях (рак, саркома, лейкозы, лимфогранулематоз, дермоидные кисты) обусловливается эндогенными токсическими продуктами обмена веществ, связанными с основным заболеванием. То же можно сказать о гемолитических анемиях беременных.
Информация на сайте подлежит консультации лечащим врачом и не заменяет очной консультации с ним.
См. подробнее в пользовательском соглашении.
Тяжесть течения P.falciparum-малярии. Клинические особенности P.falciparum-малярии
С первых дней болезни на фоне лихорадки (обычно ремиттирующего, субконтинуального или неправильного типов) больные отмечают сильную головную боль, головокружение, разлитые миалгии и артралгии, резкую слабость При высокой температуре тела наблюдаются тошнота, повторная рвота, артериальная гипотензия, тахикардия и тахипноэ Характерным признаком болезни являются боли в мезогастрии, учащение стула, при этом, в отличие от острых кишечных инфекций, каловые массы обычно не имеют патологических примесей.
У ряда больных в начальный период болезни наблюдаются кашель, признаки бронхоспазма, аллергическая экзантема.
Увеличение печени и селезенки выявляется позднее, чем при других видах инфекции, — на 7-10-й день болезни, что затрудняет раннюю диагностику. Анемия развивается рано и быстро прогрессирует, сопровождаясь желтушностью южных покровов.
Частыми проявлениями Р. falciparum-малярии являются олигурия, альбуминурия, микрогематурия и цилиндрурия, которые обычно купируются этиотропными средствами. У многих больных определяется клинико-биохимический комплекс симптомов острого гепатита.
В случае несвоевременной диагностики и неадекватной терапии у неиммунных лиц в течение первых 5-7 дней болезни часто развиваются шок, малярийная кома, острая почечная недостаточность, острый массивный гемолиз, гемоглобинурия, геморрагический синдром и другие тяжелые осложнения.
Коматозная Р. falciparum-малярия характеризуется стадийным развитием клинической картины. Вначале больные отмечают интенсивную и усиливающуюся головную боль, головокружение, повторную рвоту. Наблюдаются вялость, выраженная психическая истощаемость и сонливость больного (стадия сомноленции). Спустя несколько часов может развиться сопорозная стадия, в которой сознание больных может быть спутанным, возникают судороги, отмечаются оживление рефлексов и появление патологических рефлексов, явления менингизма.
При отсутствии терапии развивается глубокая кома с арефлексией, артериальной гипотензией, прогрессирующей одышкой, парезом сфинктеров Прогноз в таких случаях часто неблагоприятный, но адекватная терапия в период сомноленции и сопора может обеспечить выздоровление большей части больных.
Острая почечная недостаточность при Р. falciparum-малярия обычно развивается в конце 1-й или в начале 2-й недели болезни и характеризуется прогрессирующей олигурией и анурией, азотемией, гиперкалиемией. В моче обнаруживаются высокое содержание белка, эритроциты, лейкоциты, гиалиновые и зернистые цилиндры. Острая почечная недостаточность часто сочетается с другими видами осложнений. Своевременная этиотропная терапия обеспечивает хороший купирующий эффект.
Тяжелым осложнением P. falciparum-малярии является гемоглобинурия, возникающая как в результате острого внутрисосудистого гемолиза вследствие массивной инвазии, так и (наиболее часто) в результате использования хинина, примахина, сульфаниламидных препаратов у лиц с дефицитом Г-6-ФДГ. В зависимости от степени гемолиза у больных остро повышается температура тела, возникают боли в поясничной области, олиго- и анурия с отделением скудной мочи почти черного цвета (за счет оксигемоглобина в свежей моче) или цвета красного вина (за счет метгемоглобина в постоявшей моче).
При отстаивании моча разделяется на два слоя: верхний — прозрачный, темно-вишневого цвета и нижний — мутный, с большим количеством детрита. Отмечается быстрое развитие и прогрессирование желтухи и анемии. В дальнейшем может развиться острая почечная недостаточность с неблагоприятным прогнозом. Как правило, гемоглобинурия развивается при массивной паразитемии, однако ввиду первоочередного разрушения инвазированных эритроцитов в препаратах толстой капли и мазках крови паразиты могут обнаруживаться с трудом, что усложняет распознавание болезни и может приводить к диагностическим ошибкам.
Информация на сайте подлежит консультации лечащим врачом и не заменяет очной консультации с ним.
См. подробнее в пользовательском соглашении.
Под названием гемолитические анемии объединяется группа приобретенных и наследственных заболеваний, характеризующихся повышением внутриклеточным или внутрисосудистым разрушением эритроцитов.
Аутоиммунные гемолитические анемии включают формы заболевания, связанные с образованием антител к собственным антигенам эритроцитов.
В общей группе гемолитических анемий чаще встречаются аутоиммунные гемолитические анемии. Частота их составляет 1 случай на 75 000-80 000 населения.
Что провоцирует / Причины Аутоиммунной гемолитической анемии:
Иммунные гемолитические анемии могут возникать под влиянием антиэритроцитарных изо- и аутоантител и, соответственно, подразделяются на изоиммунные и аутоиммунные.
К изоиммунным относятся гемолитические анемии новорожденных, обусловленные несовместимостью по системам АВО и резус между матерью и плодом, посттрансфузионные гемолитические анемии.
При аутоиммунных гемолитических анемиях происходит срыв иммунологической толерантности к неизмененным антигенам собственных эритроцитов, иногда - к антигенам, имеющим сходные с эритроцитами детерминанты. Антитела к подобным антигенам способны вступать во взаимодействие и с неизмененными антигенами собственных эритроцитов. Неполные тепловые агглютинины являются наиболее частой разновидностью антител, способных вызывать развитие аутоиммунных гемолитических анемий. Эти антитела относятся к IgG, редко - к IgM, IgA.
Иммунные гемолитические анемии подразделяются на изоиммунные и аутоиммунные. Серологический принцип дифференциации аутоиммунных гемолитических анемий позволяет выделить формы, обусловленные неполными тепловыми агглютининами, тепловыми гемолизинами, холодовыми агглютининами, двухфазными холодовыми гемолизинами (типа Доната - Ландштейнера) и эритроопсонинами. Некоторые авторы выделяют форму гемолитической анемии с антителами против антигена нормобластов костного мозга.
По клиническому течению выделяют острые и хронические варианты.
Различают симптоматические и идиопатические аутоиммунные гемолитические анемии. Симптоматические аутоиммунные анемии возникают на фоне различных заболеваний, сопровождающихся нарушениями в иммунокомпетентной системе. Наиболее часто они встречаются при хроническом лимфолейкозе, лимфогранулематозе, остром лейкозе, системной красной волчанке, ревматоидном артрите, хронических гепатитах и циррозах печени. В тех случаях, когда появление аутоантител не удается связать с каким-либо патологическим процессом, говорят об идиопатической аутоиммунной гемолитической анемии, которая составляет около 50 % всех аутоиммунных анемий.
Образование аутоантител происходит в результате нарушения в системе иммунокомпетентных клеток, которые воспринимают эритроцитарный антиген как чужеродный и начинают вырабатывать к нему антитела. После фиксации аутоантител на эритроцитах последние захватываются клетками ретикулогистиоцитарной системы, где подвергаются агглютинации и распаду. Гемолиз эритроциов происходит главным образом в селезенке, печени, костном мозге. Аутоантитела к эритроцитам принадлежат к различным типам.
По серологическому принципу аутоиммунные гемолитические анемии делятся на несколько форм:
- анемии с неполными тепловыми агглютининами
- анемии с тепловыми гемолизинами
- анемии с полными холодовыми агглютининами
- анемии с двухфазными гемолизинами
- анемии с агглютининами против нормобластов костного мозга
Каждая из этих форм имеет некоторые особенности в клинической картине, течении и серологической диагностике. Наиболее часто встречаются анемии с неполными тепловыми агглютининами, составляющие 70 - 80 % всех аутоиммунных гемолитических анемий.
Патогенез (что происходит?) во время Аутоиммунной гемолитической анемии:
Сущность аутоиммунных процессов состоит в том, что в результате ослабления Т-супрессорной системы иммунитета, контролирующей аутоагрессию, происходит активация В-системы иммунитета, синтезирующей при этом антитела против неизмененных антигенов различных органов. В реализации аутоагрессии принимают участие также Т-лимфоциты-киллеры. Антитела - это иммуноглобулины (Ig), принадлежащие чаще всего к классу G, реже - М и А; они специфичны и направлены против определенного антигена. К IgM относятся, в частности, холодовые антитела и двухфазные гемолизины. Эритроцит, несущий на себе антитела, фагоцитируется макрофагами и в них разрушается; возможен лизис эритроцитов с участием комплемента. Антитела класса IgM могут вызвать агглютинацию эритроцитов непосредственно в кровеносном русле, а антитела класса IgG способны разрушать эритроцит только в макрофагах селезенки. Во всех случаях гемолиз эритроцитов происходит тем интенсивнее, чем больше на их поверхности находится антител. Описана гемолитическая анемия с антителами к спектрину.
Симптомы Аутоиммунной гемолитической анемии:
При остром начале аутоиммунных гемолитических анемий у больных появляются быстро нарастающая слабость, одышка и сердцебиение, боли в области сердца, иногда в пояснице, повышение температуры тела и рвота, интенсивная желтуха. При хроническом течении процесса отмечают относительно удовлетворительное самочувствие больных даже при глубокой анемии, нередко выраженную желтуху, в большинстве случаев увеличение селезенки, иногда и печени, чередование периодов обострения и ремиссии.
Анемия носит нормохромный, иногда гиперхромный характер, при гемолитических кризах обычно отмечается выраженный или умеренный ретикулоцитоз. В периферической крови обнаруживается макроцитоз и микросфероцитоз эритроцитов, возможно появление нормобластов. СОЭ в большинстве случаев увеличена. Содержание лейкоцитов при хронической форме бывает нормальным, при острой - встречается лейкоцитоз, достигающий иногда высоких цифр со значительным сдвигом лейкоцитарной формулы влево. Количество тромбоцитов обычно нормальное.
При синдроме Фишера - Ивенса аутоиммунная гемолитическая анемия сочетается с аутоиммунной тромбоцитопенией. В костном мозге эритропозз усилен, редко выявляются мегалобласты. У большинства больных снижена осмотическая резистентность эритроцитов, что обусловлено значительным числом микросфероцитов в периферической крови. Содержание билирубина увеличено за счет свободной фракции, повышено и содержание стеркобилина в кале.
Неполные тепловые агглютинины обнаруживаются с помощью прямой пробы Кумбса с поливалентной антиглобулиновой сывороткой. При положительном тесте с помощью антисывороток к IgG, IgM и т. д. уточняется, к какому классу иммуноглобулинов относятся выявляемые антитела. Если на поверхности эритроцитов менее 500 фиксированных молекул IgG, проба Кумбса отрицательна. Подобное явление наблюдается обычно у больных с хронической формой аутоиммунной гемолитической анемии или перенесших острый гемолиз. Кумбс-негативными оказываются и случаи, когда на эритроцитах фиксированы антитела, принадлежащие к IgA или IgM (в отношении которых поливалентная антиглобулиновая сыворотка менее активна).
Примерно в 50% случаев идиопатических аутоиммунных гемолитических анемий одновременно с появлением иммуноглобулинов, фиксированных на поверхности эритроцитов, выявляются антитела к собственным лимфоцитам.
Гемолитическая анемия, обусловленная Холодовыми агглютининами (холодовая гемагглютининовая болезнь) имеет хроническое течение. Она развивается при резком повышении титра Холодовых гемагглютининов. Различают идиопатические и симптоматические формы заболевания. Ведущим симптомом болезни является чрезмерно повышенная чувствительность к холоду, которая проявляется в виде посинения и побеления пальцев рук и ног, ушей, кончика носа. Расстройства периферического кровообращения приводят к развитию синдрома Рейно, тромбофлебитов, тромбозов и трофических изменений вплоть до акрогангрены, иногда холодовой крапивницы. Возникновение вазомоторных нарушений связано с образованием при охлаждении крупных внутрисосудистых конгломератов из агглютинированных эритроцитов с последующим спазмом сосудистой стенки. Эти изменения сочетаются с усиленным преимущественно внутриклеточным гемолизом. У части больных встречается увеличение печени и селезенки. Наблюдаются умеренно выраженная нормохромная или гиперхромная анемия, ретикулоцитоз, нормальное количество лейкоцитов и тромбоцитов, увеличение СОЭ, незначительное повышение уровня свободной фракции билирубина, высокий титр полных Холодовых агглютининов (выявляемый методом агглютинации в солевой среде), иногда признаки гемоглобинурии. Характерной является агглютинация эритроцитов in vitro, возникающая при комнатной температуре и исчезающая при подогревании. При невозможности выполнения иммунологических тестов диагностическое значение приобретает провокационная проба с охлаждением (в сыворотке крови, полученной от перетянутого жгутом пальца после опускания его в ледяную воду, определяется повышенное содержание свободного гемоглобина).
При холодовой гемагглютининовой болезни в отличие от пароксизмальной холодовой гемоглобинурии гемолитический криз и вазомоторные нарушения возникают только от переохлаждения тела и гемоглобинурия, начавшаяся в условиях холода, прекращается с переходом больного в теплое помещение.
Симптомокомплекс, свойственный холодовой гемагтлютининовой болезни, может возникнуть на фоне различных острых инфекций и некоторых форм гемобластозов. При идиопатических формах заболевания полного выздоровления не наблюдается, при симптоматических прогноз зависит главным образом от тяжести основного процесса.
Пароксизмальная холодовая гемоглобинурия относится к числу редких форм гемолитических анемий. Ею заболевают люди обоего пола, чаще дети.
У больных с пароксизмальной холодовой гемоглобинурией после пребывания на холоде могут появиться общее недомогание, головная боль, ломота в теле и другие неприятные ощущения. Вслед за этим начинается озноб, повышается температура, отмечается тошнота и рвота. Моча приобретает черную окраску. Одновременно иногда выявляются желтушность, увеличение селезенки и вазомоторные нарушения. На фоне гемолитического криза у больных обнаруживают умеренную анемию, ретикулоцитоз, повышение содержания свободной фракции билирубина, гемосидеринурию и протеинурию.
Окончательный диагноз пароксизмальной холодовой гемоглобинурии устанавливают на основании обнаруженных двухфазных гемолизинов по методу Доната - Ландштейнера. Для нее не характерна аутоагглютинация эритроцитов, постоянно наблюдающаяся при холодовой гемагтлютинацией ной болезни.
Гемолитическая анемия, обусловленная эритроопсонинами. Существование аутоопсонинов к клеткам крови является общепризнанным. При приобретенной идиопатической гемолитической анемии, циррозе печени, гипопластической анемии с гемолитическим компонентом и лейкозах обнаружен феномен аутоэритрофагоцитоза.
Приобретенная идиопатическая гемолитическая анемия, сопровождающаяся положительным феноменом аутоэритрофагоцитоза, имеет хроническое течение. Периоды ремиссии, длящиеся иногда значительное время, сменяются гемолитическим кризом, характеризующимся иктеричностью видимых слизистых оболочек, потемнением мочи, анемией, ретикулоцитозом и повышением непрямой фракции билирубина, иногда увеличением селезенки и печени.
При идиопатических и симптоматических гемолитических анемиях выявление аутоэритрофагоцитоза при отсутствии данных, указывающих на наличие других форм аутоиммунных гемолитических анемий, дает основание отнести их к гемолитической анемии, обусловленной эритроопсонинами. Диагностическая проба аутоэритрофагоцитоза проводится в прямом и непрямом вариантах.
Иммуногемолитические анемии, обусловленные применением лекарств. Различные лечебные препараты (хинин, допегит, сульфаниламиды, тетрациклин, цепорин и др.), способные вызывать гемолиз, образуют комплексы со специфическими гетероантителами, затем оседают на эритроциты и присоединяют к себе комплемент, что приводит к нарушению мембраны эритроцитов. Такой механизм медикаментозно обусловленных гемолитических анемий подтверждается обнаружением на эритроцитах больных комплемента при отсутствии на них иммуноглобулинов. Анемии характеризуются острым началом с признаками внутрисосудистого гемолиза (гемоглобинурия, ретикулоцитоз, повышение содержания свободной фракции билирубина, усиление эритропоэза). На фоне гемолитического криза иногда развивается острая почечная недостаточность.
Несколько по-иному протекают гемолитические анемии, развивающиеся при назначении пенициллина и метилдофа. Введение за сутки 15 000 и более ЕД пенициллина может привести к развитию гемолитической анемии, характеризующейся внутриклеточным гипергемолизом. Наряду с общими клинико-лабораторными признаками гемолитического синдрома обнаруживается также положительная прямая проба Кумбса (выявляемые антитела относятся к IgG). Пенициллин, связываясь с антигеном мембраны эритроцитов, образует комплекс, против которого в организме вырабатываются антитела.
При длительном применении метилдофа у части больных возникает гемолитический синдром, имеющий черты идиопатической формы аутоиммунных гемолитических анемий. Выявляемые антитела идентичны с тепловыми агглютининами и относятся к IgG.
Гемолитическая анемия, обусловленная механическими факторами, связана с разрушением эритроцитов при их прохождении через измененные сосуды или через искусственные клапаны. Эндотелий сосудов изменяется при васкулитах, злокачественной артериальной гипертензии; при этом адгезия и агрегация тромбоцитов активированы, как и система свертывания крови и образования тромбина. Развиваются распространенный стаз крови и тромбоз мелких кровеносных сосудов (ДВС-синдром) с травматизацией эритроцитов, в результате чего они фрагментируются; в мазке крови находят многочисленные фрагменты эритроцитов (шистоциты). Разрушаются эритроциты также при их прохождении через искусственные клапаны (чаще - при многоклапанной коррекции); описана гемолитическая анемия на фоне сенильного кальцинированного аортального клапана. Диагноз базируется на признаках анемии, повышении концентрации свободного билирубина в сыворотке крови, наличии шистоцитов в мазке периферической крови и симптоматике основного заболевания, ставшего причиной механического гемолиза.
Реже встречается в клинической практике гемолитическая анемия, обусловленная воздействием свинца, при отравлении кислотами, ядами змей или дефицитом витамина Е, а также внутриклеточными паразитами. Гемолитическая анемия развивается, например, после укуса змеи, случайного или намеренного (суицид) приема уксусной кислоты, при контакте с парами свинца, на фоне малярии. Анемия носит нормоцитарный, нормохромный, регенераторный характер; в сыворотке крови повышено содержание свободной фракции билирубина и железа.
Гемолитико-уремический синдром (болезнь Мошковича, синдром Гассера) может осложнять течение аутоиммунных гемолитических анемий. Заболевание аутоиммунной природы характеризуется гемолитической анемией, тромбоцитопенией, поражением почек. Отмечаются диссеминированное поражение сосудов и капилляров с вовлечением практически всех органов и систем, выраженные изменения со стороны коагулограммы, характерные для ДВС-синдрома.
Диагностика Аутоиммунной гемолитической анемии:
Диагноз аутоиммунной гемолитической анемии ставят на основании наличия клинико-гематологических признаков гемолиза и выявления на поверхности эритроцитов аутоантител с помощью пробы Кумбса (положительная почти в 60% аутоиммунного гемолиза). Дифференцируют заболевание от наследственного микросфероцитоза, гемолитических анемий, связанных с дефицитом ферментов.
В крови - нормохромная или умеренно гиперхромная анемия различной выраженности, ретикулоцитоз, нормобласты. В ряде случаев в мазках крови обнаруживаются микросфероциты. Количество лейкоцитов может повышаться при гемолитическом кризе. Число тромбоцитов, как правило, в пределах нормы, но может встречаться тромбоцитопения. СОЭ значительно увеличена. В костном мозге наблюдается выраженная гиперплазия эритроидного ростка. Содержание билирубина в крови, как правило, повышено за счет непрямого.
Лечение Аутоиммунной гемолитической анемии:
При острых формах приобретенных аутоиммунных гемолитических анемиях назначают преднизолон в суточной дозе 60-80 мг. При неэффективности она может быть увеличена до 150 мг и больше. Суточная доза препарата делится на 3 части в соотношении 3:2:1. По мере стихания гемолитического криза доза преднизолона постепенно снижается (по 2,5-5 мг в день) до половины исходной. Дальнейшее снижение дозы препарата во избежание рецидивирования гемолитического криза осуществляют по 2,5 мг в течение 4-5 дней, затем еще в меньших дозах и с большими интервалами до полной отмены препарата. При хронической аутоиммунной гемолитической анемии достаточно назначить 20-25 мг преднизолона, а по мере улучшения общего состояния больного и показателей эритропоэза переводить на поддерживающую дозу (5-10 мг). При холодовой гемагглютининовой болезни показана аналогичная терапия преднизолоном.
Спленэктомия при аутоиммунной гемолитической анемии, связанных с тепловыми агглютининами и аутоэритроопсонинами, может быть рекомендована лишь больным, у которых кортикостероидная терапия сопровождается непродолжительными ремиссиями (до 6-7 мес.) или имеется резистентность к ней. У больных гемолитической анемией, обусловленной гемолизинами, спленэктомия не предотвращает гемолитические кризы. Однако они наблюдаются реже, чем до операции, и легче купируются с помощью кортикостероидных гормонов.
При рефрактерных аутоиммунных гемолитических анемиях в сочетании с преднизолоном могут быть использованы иммунодепрессаты (6-меркаптопурин, имуран, хлорбутин, метотрексат, циклофосфамид и др.).
В стадии глубокого гемолитического криза применяют переливания эритроцитной массы, подобранной с помощью непрямой пробы Кумбса; для снижения выраженной эндогенной интоксикации назначают гемодез, полидез и другие дезинтоксикационные средства.
Лечение гемолитико-уремического синдрома, который может осложнять течение аутоиммунных гемолитических анемий, включает кортикостероидные гормоны, свежезамороженную плазму, плазмаферез, гемодиализ, трансфузии отмытых или криоконсервированных эритроцитов. Несмотря на использование комплекса современных терапевтических средств, прогноз часто неблагоприятный.
К каким докторам следует обращаться если у Вас Аутоиммунная гемолитическая анемия:
Вас что-то беспокоит? Вы хотите узнать более детальную информацию о Аутоиммунной гемолитической анемии, ее причинах, симптомах, методах лечения и профилактики, ходе течения болезни и соблюдении диеты после нее? Или же Вам необходим осмотр? Вы можете записаться на прием к доктору .
Малярия (от лат. mala aria - плохой воздух) - острое или хроническое рецидивирующее инфекционное заболевание, имеющее различные клинические формы в зависимости от срока созревания возбудителя; характеризуется лихорадочными пароксизмами, гипохромной анемией, увеличением селезенки и печени.
Этиология и патогенез
Заболевание вызывается несколькими видами простейших рода Plasmodium (впервые плазмодий малярии был обнаружен в эритроцитах А. Лавераном в 1880 г.). Попав в кровь при укусе комара, плазмодии проделывают сложный цикл развития, паразитируют в эритроцитах человека, размножаясь бесполым путем, который называют шизогонией. Шизонты паразита накапливают в цитоплазме частицы темно-бурого пигмента - гемоме-ланина. При гемолизе паразиты и гемомеланин высвобождаются из эритроцита, причем пигмент фагоцитируется клетками макрофагальной системы, а шизонты вновь внедряются в эритроциты. В связи с этим развиваются надпеченочная (гемолитическая) анемия, гемомеланоз и гемосидероз элементов ретикуло-эндотелиальной системы, завершающийся склерозом. В периоды гемолитических кризов появляются острые сосудистые расстройства (стаз, диапедезные кровоизлияния). В связи с персистирую-щей антигенемией при малярии в крови появляются токсические иммунные комплексы. С их воздействием связано поражение микроциркуля-торного русла (повышение проницаемости, геморрагии), а также развитие гломерулонефрита.
Патологическая анатомия
В связи с существованием нескольких видов малярийного плазмодия, различающихся по срокам их созревания, выделяют трехдневную, четырехдневную и тропическую формы малярии. При трехдневной малярии, наиболее частой, в связи с разрушением эритроцитов развивается анемия, тяжесть которой усугубляется свойством плазмодиев трехдневной малярии поселяться в молодых эритроцитах - ретикулоцитах. Высвобождающиеся при распаде эритроцитов продукты, особенно гемомеланин, захватываются клетками макрофагальной системы, что приводит к увеличению селезенки и печени, гиперплазии костного мозга. Органы, загруженные пигментом, приобретают темно-серую, а иногда черную окраску. Селезенка увеличивается особенно быстро, вначале в результате полнокровия, а затем - гиперплазии клеток, фагоцитирующих пигмент. Пульпа ее становится темной, почти черной. В острой стадии малярии селезенка мягкая, полнокровная, в хронической - плотная вследствие развивающегося склероза; масса ее достигает 3-5 кг
Симптомы
При хронической малярии отмечаются огрубение стромы печени и разрастание в ней соединительной ткани. Костный мозг плоских и трубчатых костей имеет темно-серую окраску, отмечается гиперплазия его клеток и отложение в них пигмента. Встречаются участки аплазии костного мозга. Гемомеланоз органов гистиоцитарно-макрофагальной системы сочетается с их гемосидерозом. Развивается надпеченочная (гемолитическая) желтуха. Патологическая анатомия четырехдневной малярии подобна таковой при трехдневной малярии. При тропической малярии изменения, с одной стороны, имеют много общего с описанными при трехдневной форме, с другой - отличаются некоторыми особенностями. Они объясняются тем, что эритроциты, содержащие дозревающие шизонты тропической малярии, скапливаются в терминальных участках кровяного русла, что ведет к развитию паразитарных стазов. В местах скопления дозревающих шизонтов в период деления их на мерозоиты происходит фагоцитоз неитрофилами и макрофагами как зараженных эритроцитов и незрелых шизонтов, так и продуктов распада и пигмента, появляющихся после деления плазмодиев. С паразитарными стазами связаны опасные для жизни изменения головного мозга, которые определяют развитие малярийной комы. Кора и другие участки серого вещества головного мозга имеют в таких случаях темную коричнево-серую (дымчатую) окраску. В белом веществе встречаются многочисленные точечные кровоизлияния, которые окружают сосуды, заполненные агглютинированными эритроцитами с паразитами в цитоплазме или гиалиновыми тромбами. Вокруг таких сосудов, помимо кровоизлияний, появляются очаги некроза мозговой ткани. На границе некроза и кровоизлияния через 2 сут от начала комы находят реактивное разрастание клеток глии, что ведет к формированию своеобразных узелков - так называемых гранулем Дюрка.
Прогноз
Осложнением острой малярии может быть гломерулонефрит, хронической - истощение, амилоидоз.
Смерть наблюдается обычно при тропической малярии, осложненной комой.
Читайте также:

