Геморрагический шок в инфекции
Обновлено: 18.04.2024
Тактика ведения больного с геморрагическим шоком.
У больных с кровопотерей более 40-50% ОЦК крововосполнение необходимо проводить одновременно с ингаляцией 100% кислорода через маску наркозного аппарата. Необходимо быть готовым к проведен по интубации трахеи и ИВЛ.
Кровопотерю восполняют в две или три вены, струйно, растворами кристаллоидов, коллоидов и эритроцитарной массой или плазмой общим объем, в 2-2,5 раза превышающем объем кровопотери. Соотношение кристаллоидов, коллоидов и эритроцитарной массы должно быть 1:1:2.
Одновременно с восполнением кровопотери внутривенно инфузируют растворы адреномиметиков (допамин, добутамин, норадренашн) в дозе, определяемой ответной реакцией сердечно-сосудистой системы. При отсутствии допамина или в случае резистентности к проводимой терапии используют капельное введение адреналина.
На фоне восполнения ОЦК и введения адреномиметиков при стабилизации систолического" артериального давления на уровне 90 мм рт. ст. целесообразно введение вазодилятаторов (нгпроглицерин, дроперидол) с тем, чтобы снять избыточный артериолоспазм.
Для профилактики синдрома ДВС назначают антиагрегантную (трентал по 100 мг, растворенный в 200 мл изотонического раствора хлорида натрия, вводимый в течение 1,5-2 часов 2-3 раза в сутки), антикоагулянтную (гепарин по 2500 - 5000 Ед. через 4-6 часов) и антипротеиназную терапию (контрикал 10000-150000 Ед/сут.).
При восстановлении ОЦК и стабилизации гемодинамических показателей до среднефизиологического уровня при сохраняющейся анурии или олигурии рекомендуется назначение салуретиков (лазикс в дозе 100-200 мг).
При необходимости проводится коррекция уровня электролитов и КОС крови, антигипоксантная и антиоксидантная терапия.
Некоторые авторы выделяют 5-й тип кровопотери - кровопотеря более 60% ОЦК, при которой клиника геморрагического шока не успевает развиться. Такая кровопотеря протекает по типу первичного геморрагического коллапса с быстрым наступлением терминального состояния и остановкой сердца. Для этого состояния характерно быстрое снижение АД и МОК с потерей сознания, снижение коронарного кровотока с ишемией миокарда и развитие фибрилляции или асистолии желудочков сердца. Фибрилляция или асистолия желудочков сердца наступает на фоне кровотечения или в ближайшие несколько минут после его остановки. Летальный исход можно предупредить путем немедленной попытки добиться максимально возможной централизации кровообращения. Для этого могут быть использованы следующие приемы.
1. Пережатие кулаком аорты (через брюшную стенку) в абдоминальном ее отделе.
2. Внутривенное (внутрисердечнои) введение адреналина (возможно одновременно с норадреналином или мезатоном) в дозе 0,1 мг/сек и более, с последующим постепенным снижением дозы адреналина на фоне крововосполнештя.
3. Внутриартериальное (через бедренную артерию) нагнетание крови в центральном направлении.
Такая централизация кровообращения позволяет на какое-то время сохранить кровоснабжение головного мозга и сердца на критическом уровне, произвести остановку кровотечения и восполнить кровопотерю.
Больные с явными признаками продолжающегося кровотечения и нестабильными показателями гемодинамики направляются в операционную где неотложные диагностические и лечебные мероприятия совмещаются с предоперационной подготовкой.
Наличие клиники постгеморрагической анемии без явных признаков продолжающегося кровотечения служит основанием для госпитализации пациента в ОРИТ, где осуществляются диагностические мероприятия по установлению источника кровотечения, оценке гемостаза и другие лечебно-диагностические процедуры.
При подозрении на желудочно-кишечное кровотечение необходимо выполнение фиброгастродуоденоскопии, во время которой определяют наличие крови в просвете ЖКТ, источник кровотечения, его локализацию, размеры повреждения ЖКТ, состояние гемостаза. К признакам продолжающегося желудочно-кишечного кровотечения и неустойчивого гемостаза относят артериальное (пульсирующее) кровотечение, подтекание венозной крови, свежий сгусток, тромб красного цвета, тромб в состоянии ретракции, гематома вокруг источника кровотечения.
При кровотечении из расширенных вен пищевода, обусловленного портальной гипертензией, в желудок вводят и устанавливают зонд Блекмора-Сентаккена. Внутривенно вводят 20 Ед питуитрина, с последующими инъекциями препарата по 5 Ед через 4-6 часов (суточная доза 30 Ед). Целесообразно применение в течение 5 дней октреатида в дозе 25 мкг/ч (профилактика стрессорных эрозий слизистой ЖКТ).
В зависимости от результатов диагностической эндоскопии используют различные методы остановки кровотечения.
Неэффективность общих и местных гемостатических мероприятий диктует необходимость оперативного вмешательства.
При выборе инфузионных средств необходимо помнить, что кристаллоидные растворы не столь значительно увеличивают ОЦК по сравнению с коллоидами. Инфузия 1000 мл раствора Рингера увеличивает ОЦК на 300 мл, тогда как вливание 100 мл 25% раствора альбумина увеличивает ОЦК на 450 мл.
Использование растворов глюкозы при острой массивной кровопотере несколько ограничено, так как метаболизм глюкозы приводит к образованию свободной воды, которая быстро покидает внутрисосудистое пространство, и только 10 мл из каждых 100 мл раствора глюкозы остаются в сосудистом русле.
Растворы гидрооксиэтилкрахмала (HAES-steril 6% и 10%) по своему действию подобны альбумину. HAES-steril вводится в дозе не более 20 мл/кг в сутки. Волемический эффект препарата сохраняется в течение 24 часов. Использование HAES-steril сопровождается удлинением времени кровотечения, снижением уровня плазменных факторов свертывания (особенно VIII фактора), удлинением АЧТВ.
Гипертонический (7,5%) раствор хлорида натрия, используемый в дозе 3-4 мл/кг, увеличивает ОЦК вследствие быстрого перехода жидкости из интерстициального пространства в кровеносное русло. 250 мл 7,5% раствора хлорида натрия увеличивают внутрисосудистый объем прибизительно на 1000 мл.
Критериями адекватности проводимой инфузионной терапии являются нормализация уровеня ЦВД и диуреза 30 мл/ч и более.
Информация на сайте подлежит консультации лечащим врачом и не заменяет очной консультации с ним.
См. подробнее в пользовательском соглашении.

В происхождении геморрагического шока важно исключить медленную потерю крови даже значительного объема. Установлено, что нарушения гемодинамики при постепенной потере до 1,5 л не приводят к серьезным последствиям. Это связано с включением механизмов компенсации.
В условиях внезапного кровотечения незамещенный объем в 0,5 л сопровождается острой тканевой кислородной недостаточностью (гипоксией).
Чаще всего кровопотеря наблюдается при травмах, оперативных вмешательствах, в акушерской практике при родовой деятельности у женщин.
От каких механизмов зависит тяжесть шока?
В развитии патогенеза компенсации кровопотери имеют значение:
- состояние нервной регуляции сосудистого тонуса;
- способность сердца работать в условиях гипоксии;
- свертываемость крови;
- условия окружающей среды по дополнительному обеспечению кислородом;
- уровень иммунитета.
Ясно, что у человека с хроническими заболеваниями шансов перенести массивную кровопотерю значительно меньше, чем у ранее здорового. Работа военных медиков в условиях афганской войны показала, насколько тяжелой оказывается умеренная кровопотеря для здоровых бойцов в условиях высокогорья, где насыщенность воздуха кислородом снижена.

Быстрая транспортировка раненых с помощью БТР-ов и вертолетов спасла немало солдат
У человека в среднем циркулирует постоянно около 5л крови по артериальным и венозным сосудам. При этом 75% находится в венозной системе. Поэтому от быстроты адаптации именно вен зависит последующая реакция.
Во время систолического сокращения выталкиваемый объем крови недостаточен для тканей и внутренних органов, он питает только коронарные артерии. В ответ включается эндокринная защита в виде повышенной секреции адренокортикотропного и антидиуретического гормонов, альдостерона, ренина. Это позволяет задержать жидкость в организме, прекратить мочевыделительную функцию почек.
Одновременно повышается концентрация натрия, хлоридов, но теряется калий.
Повышенный синтез катехоламинов сопровождается спазмом сосудов на периферии, растет сосудистое сопротивление.
Сердце пытается компенсировать необходимый выброс учащением сокращений (тахикардией), но их не хватает. Потери калия снижают сократительную способность миокарда, формируется сердечная недостаточность. Артериальное давление резко падает.
Восполнение объема циркулирующей крови способно предотвратить общие нарушения микроциркуляции. От скорости и полноты оказания мероприятий неотложного значения зависит жизнь пациента.
Причины
Причиной геморрагического шока является острое кровотечение.
Травматический болевой шок не всегда сопровождается значительной кровопотерей. Для него более характерна распространенная поверхность поражения (обширные ожоги, сочетанные переломы, раздавливание тканей). Но сочетание с неостановленным кровотечением усугубляет действие поражающих факторов, утяжеляет клиническое течение.

У беременных женщин важна срочная диагностика причины шока
Геморрагический шок в акушерстве случается в ходе тяжелых родов, во время беременности, в послеродовом периоде. Массивную кровопотерю вызывают:
- разрывы матки и родовых путей;
- предлежание плаценты;
- при нормальном положении плаценты возможна ее досрочная отслойка;
- прерывание беременности;
- гипотония матки после родов.
В таких случаях часто кровотечения сочетаются с другой патологией (травмы в ходе родовой деятельности, гестоз, сопутствующие хронические заболевания женщины).
Клинические проявления
Клиника геморрагического шока определяется степенью нарушенной микроциркуляции, выраженностью сердечной и сосудистой недостаточности. В зависимости от этапа развития патологических изменений принято различать стадии геморрагического шока:
Это уменьшение объема циркулирующей крови в результате кровопотери. Быстрая остановка кровотечения и гемотрансфузия способствуют снижению летальности, которая все равно остается очень высокой.
2. Что такое необратимый геморрагический шок?
В 1940 году Уиггерс (C.J. Wiggers) продемонстрировал, что геморрагический шок вызывает такие изменения в организме, которые не устраняются простым возмещением кровопотери. Восемьдесят процентов животных, у которых был вызван тяжелый геморрагический шок, погибли в течение 24 часов, несмотря на реинфузию им выпущенной крови.
"Необратимый шок" обусловлен продолжающейся потерей плазмы в результате ее утечки из сосудистого русла между эндотелиальными клетками и развитием изотонического отека скелетных мышц. Уиггерс доказал, что эти потери можно компенсировать дополнительной инфузией солевых изотопических растворов.
3. Какова классификация геморрагического шока?
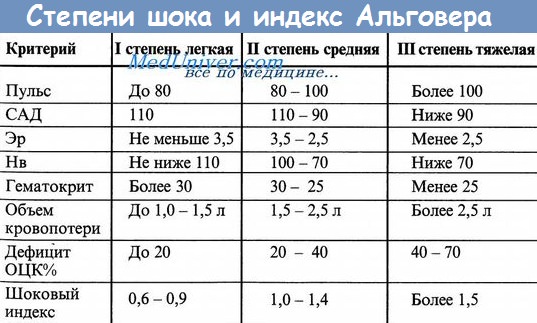
Первый класс кровопотери: объем циркулирующей крови (ОЦК) снижается на 15%; клинические симптомы кровопотери практически отсутствуют; иногда наблюдается тахикардия.
Второй класс кровопотери: ОЦК снижается на 15-30% (750-1500 мл у больного весом 70 кг); развивается тахикардия, тахипноэ, снижается систолическое давление.
Третий класс кровопотери: ОЦК снижается на 30-40% (приблизительно 2000 мл для взрослых); развивается тахикардия, тахипноэ, угнетение сознания, гипотензия, уменьшается количество мочи.
Четвертый класс кровопотери: ОЦК уменьшается более чем па 40%, что сразу представляет опасность для жизни; развивается резкая тахикардия, значительное снижение систолического давления вплоть до исчезновения пульса на периферических артериях, прекращается фильтрация мочи почками, кожные покровы становятся холодными и бледными.

4. Чему равен в норме ОЦК?
В норме ОЦК составляет 7% веса тела взрослых, что приблизительно составляет 70 мл/кг. У детей ОЦК составляет 9% веса тела или 90 мл/кг.
5. Какие механизмы ведут к гипотензии?
Около 70% ОЦК приходится на венозную систему и обеспечивает преднагрузку сердцу. Уменьшение объема венозной крови приводит к снижению наполнения сердца. Согласно закону Старлинга, чем больше растягивается сердечная мышца, тем выше сократительная способность сердца. С другой стороны, снижение наполнения сердца приводит к ослаблению сокращения, уменьшению ударного объема и сердечного выброса.
Кроме того, стойкий геморрагический шок ведет к деполяризации мембран в скелетных мышцах, что способствует перемещению воды из внеклеточного пространства внутрь клетки. Это перемещение вызывает дальнейшее снижение ОЦК.
6. Как организм компенсирует снижение ОЦК?
Резкое снижение давления в крупных сосудах приводит к возбуждению симпатической нервной системы и освобождению эндогенных катехоламинов. Эта реакция в сочетании с угнетением вагусного центра в стволе мозга (рефлекс Марея (Marey)) вызывает вазоконстрикцию, тахикардию, повышение силы сердечных сокращений.
Сосуды по-разному воспринимают стимулы к вазоконстрикции (принципы демократии при этом не учитываются); самую высокую способность к вазокопстрикции проявляют кожные, брыжеечные и почечные сосуды. Снижение почечного кровотока ведет к освобождению ренина, который способствует превращению ангиотензина-1 в ангиотензин-2.
Ангиотензин-2 является потенциальным вазоконстриктором и также стимулирует освобождение альдостерона и антидиуретического гормона гипофиза. При этом усиливается реабсорбция натрия и воды в почечных канальцах, что, в свою очередь, увеличивает объем циркулирующей жидкости.
7. Меняется ли с возрастом способность к компенсации снижения ОЦК?
К сожалению, да. Пожилой возраст — серьезное испытание. Сердечный выброс можно повысить, увеличивая число сердечных сокращений до величины в 200 ударов/минуту минус возраст (максимальное количество сердечных сокращений = 220 - возраст). У младенцев же ударный объем относительно стабильный, и сердечный выброс у них повышается только за счет увеличения числа сердечных сокращений.
8. Как реагируют клетки на геморрагический шок?
При неадекватном кровоснабжении и оксигенации клетки неспособны осуществлять нормальный аэробный метаболизм, что приводит к образованию молочной кислоты и развитию метаболического ацидоза. Снижается образование аденозин-трифосфата (АТФ), и клетка не может поддерживать поляризованность мембраны.
Первым тому свидетельством становится набухание эндоплазматического ретикулума, затем повреждаются митохондрий, выбрасываются лизосомальпые ферменты и внутрь клетки поступают натрий и вода. Депонирование воды в клетках увеличивает дефицит межклеточной жидкости и объема циркулирующей в сосудах крови.
9. Каковы клинические симптомы геморрагического шока?
Частый пульс и низкое систолическое давление. При инвазивном мониторинге выявляется снижение диуреза, центрального венозного давления, давления заклинивания в легочных капиллярах, сердечного выброса и насыщения кислородом смешанной крови.
10. Можно ли исключить геморрагический шок, если гематокрит в норме?
Нет. Концентрация эритроцитов снижается только после инфузии экзогенной жидкости или после перемещения интерстициальной жидкости в кровяное русло. Если не проводить инфузионную терапию, то второе обычно происходит через 24 часа после развития шока.
11. Чем геморрагический шок отличается от других видов шока?
Кардиогенный констриктивный шок (в результате тампонады сердца или напряженного пневмоторакса) характеризуется повышением центрального венозного давления и уравниванием давлений в правых и левых отделах сердца. Нейрогенный шок напоминает геморрагический, поскольку в основе его лежит снижение объема циркулирующей жидкости за счет депонирования крови в венах и снижения тонуса артерий ниже уровня повреждения спинного мозга.
Септический шок может развиться у травматологических больных, которые обратились за медицинской помощью с опозданием. Первыми симптомами септического шока являются лихорадка, теплые розовые кожные покровы и повышенный сердечный выброс.
12. Что такое тахикардия?
Тахикардией считается количество сердечных сокращений >160 ударов в минуту у детей первых дух лет жизни, > 140 ударов в минуту у детей дошкольного возраста и > 100 ударов в минуту у взрослых. Будьте внимательны, больной может принимать препараты, урежающие сердечный ритм (например, b-блокаторы).
13. Где может “потеряться” кровь при кровопотере?
В отличие от явной потери крови при наружных повреждениях, кровь может скапливаться в брюшной и грудной полостях, забрюшинном пространстве (после перелома костей таза) и бедрах. Эта скрытая потеря крови может перевести геморрагический шок в необратимую стадию и привести к летальному исходу.
14. Каковы первостепенные лечебные мероприятия при геморрагическом шоке?
Остановить кровотечение и восполнить объем циркулирующей жидкости. В первую очередь нужно поставить широкопросветный периферический внутривенный катетер (14G или 16G). Закон Пуазейля гласит, что сопротивление жидкости пропорционально четвертой степени радиуса просвета катетера. Если периферическую вену катетеризировать не удается, нужно катетеризировать центральную вену (бедренную, подключичную или внутреннюю яремную). У детей хорошо себя зарекомендовали внутрикостные катетеры, введенные в большеберцовую кость.
15. В каком количестве и какой тип жидкости нужно назначить в первую очередь?
Взрослым нужно быстро перелить 1-2 литра подогретого Рингер-лактата. Маленьким детям инфузию проводят из расчета 20 мл/кг веса.
16. Нужно ли применять коллоидные растворы для лечения геморрагического шока?
Споры относительно преимуществ кристаллоидных и коллоидных растворов (растворы альбумина или декстранов) при лечении геморрагического шока продолжаются. Мета-анализ многочисленных проспективных клинических исследований указывает па снижение летальности у травматологических больных при восстановлении объема циркулирующей жидкости кристаллоидными растворами в отличие от коллоидных растворов.
Как ни странно, эти исследования не выявили между реанимацией кристаллоидными либо коллоидными растворами никаких различий во влиянии на развитие отека легких, необходимость гемотрансфузии или продолжительность госпитализации.
17. В каких случаях необходимо сразу провести гемотрансфузию?
В критических ситуациях проводится трансфузия эритроцитарной массы первой группы резус-отрицателыюй без перекрестного совмещения (резус-ноложительную кровь можно использовать у мужчин, которым ранее гемотрапсфузии не проводились; женщинам всегда переливают резус-отрицательиую кровь во избежание сенсибилизации, которая может осложнить будущие беременности).
18. Каковы физиологические осложнения гемотрансфузии?
Наиболее распространенным осложнением является гипотермия, вызванная переливанием холодной крови. Эта проблема может быть устранена, если контейнер крови поместить в быстросогревающую систему. Замещение кровопотери только эритроцитарной массой и кристаллоидными растворами может привести к разбавлению факторов свертывания. В этих случаях необходимо дополнительное переливание свежезамороженной плазмы.
При переливании донорской крови, содержащей цитрат, требуется дополнительное введение кальция (после трансфузии каждых четырех доз крови вводят 250 мг глюконата кальция). Существуют доказательства того, что долго хранящаяся кровь содержит продукты распада жиров, которые способствуют развитию воспаления с повреждением тканей и последующей полиорганной недостаточностью. Медиатором процесса являются нейтрофилы.
Кроме того, во время гемотрапсфузии существует риск заражения гепатитами В и С, ВИЧ-инфекцией и вирусом Т-клеточной лимфомы человека.

ДДК — диастолическое давление крови; ЛКД — легочно-капиллярное давление;
МСВ - минутный сердечный выброс; САД - среднее артериальное давление; СДК — систолическое давление крови;
СЛАД — среднее легочное артериальное давление.
Ударный объем сердца можно определить по МСВ и ЧСС; резистентность — из относительного изменения давления с каждой стороны круга кровообращения.
b СЛАД = [2 (легочное СДК) + легочное ДДК] / 3.
19. Существует ли альтернатива переливанию донорской крови?
С экономической точки зрения достаточно выгодна аутотрансфузия крови, полученной при эвакуации гемоторакса через торакостомический дренаж. Кровь собирают, фильтруют, смешивают с антикоагулянтами (цитратом) и возвращают больному. Иногда используются аппараты для сбора крови во время операции и последующей ее реинфузии. Однако количество крови, пригодной к реинфузии, ограничено.
В настоящее время нельзя купить настоящий заменитель крови, однако несколько таких препаратов находятся на стадии апробации Управления по контролю за качеством пищевых продуктов и лекарственных средств (FDA). Эти кровезаменители содержат различные виды очищенного гемоглобина (без эритроцитов), молекулы которого химически связаны, что задерживает его выделение с мочой. Действие кровезаменителей напоминает нативный гемоглобин, но период их полувыведения достаточно короткий.
Кровезаменители не нужно совмещать с кровью больного; они не содержат инфекционных возбудителей и гораздо дольше могут храниться при комнатной температуре.
20. Почему геморрагический шок вызывает нарушение функции внутренних органов?
Тяжелый геморрагический шок запускает мощную воспалительную реакцию, которую иногда не удается остановить даже соответствующими реанимационными мероприятиями. Во время вьетнамской войны раненым оказывалась своевременная медицинская помощь. Тем не менее у лиц, перенесших геморрагический шок, позднее развивалась легочная недостаточность или респираторный дистресс-синдром взрослых (РДСВ).
Больных с РДСВ можно перевести па искусственную вентиляцию легких, но в дальнейшем они погибнут от сочетанной недостаточности печени, почек, сердца и костного мозга (т.е. тяжелой нолиоргапной недостаточности). Полиорганная недостаточность остается ведущей причиной поздней посттравматической летальности. Помимо нарушения синтеза АТФ, при шоке освобождаются фактор активации тромбоцитов, интерлейкин-8 и метаболиты арахидоновой кислоты, которые способствуют адгезии нейтрофилов к эндотелиальным клеткам и освобождению цитотоксичных медиаторов.
Происходит повреждение внутренних органов. Мезентериальное кровяное русло является очагом синтеза нровоспалительных веществ (кишечник — двигатель полиорганной недостаточности). Помимо непосредственной активации нейтрофилов, в мезентериальных сосудах происходит освобождение нровоспалительных веществ в лимфатическую систему, что также способствует активации нейтрофилов и повреждению легких.
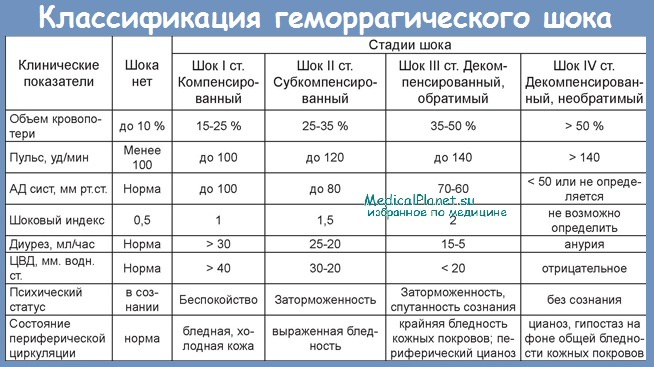
Учебное видео - шоковый индекс Альговера, степени кровопотери и анемии
Редактор: Искандер Милевски. Дата обновления публикации: 18.3.2021
Геморрагический шок (ГШ) — это критическое состояние организма, связанное с острой кровопотерей, в результате чего возникает кризис макро-и микроциркуляции, синдром полиорганной и полисистемной недостаточности. С патофизиологической точки зрения — это кризис микроциркуляции, его неспособность обеспечить адекватный тканевой обмен, удовлетворить потребность тканей в кислороде, энергетических продуктах, удалить токсичные продукты обмена.
Тяжесть и скорость нарушений при ГШ зависит от длительности артериальной гипотонии, восходящего состояния органов и систем. При восходящей гиповолемии кратковременная гипоксия в родах ведет к шоку, так как является пусковым механизмом нарушения гемостаза.
Клиника геморрагического шока
Геморрагический шок проявляется слабостью, головокружением, тошнотой, сухостью во рту, потемнением в глазах, при увеличении кровопотери — потерей сознания. В связи с компенсаторным перераспределением крови ее количество уменьшается в мышцах, коже проявляется бледностью кожных покровов с серым оттенком конечности холодные, влажные. Уменьшение почечного кровотока проявляется снижением диуреза, в последующем с нарушением микроциркуляции в почках, с развитием ишемии, гипоксии, некроза канальцев. При увеличении объема кровопотери нарастают симптомы дыхательной недостаточности: одышка, нарушение ритма дыхания, возбуждение, периферийное цианоз.
Выделяют четыре степени тяжести геморрагического шока:
- I степень тяжести отмечается при дефиците ОЦК 15%. Общее состояние удовлетворительное, кожные покровы бледного цвета, незначительное тахикардия (до 80-90 уд / мин) АД в пределах 100 мм рт.ст., гемоглобин 90г / л, центральное венозное давление в норме.
- II степень тяжести — дефицит ОЦК до 30%. Общее состояние средней тяжести, жалобы на слабость, головокружение, потемнение в глазах, тошноту, кожа бледная, холодная. Артериальное давление 80-90 мм рт.ст., центральное венозное давление ниже 60 мм вод.ст., тахикардия до 100-120 уд / мин, диурез снижен, гемоглобин 80г / л и ниже.
- III степень тяжести имеет место при дефиците ОЦК 30-40%. Общее состояние тяжелое. Наблюдается резкая заторможенность, головокружение, кожные покровы бледного цвета, акроцианоз, артериальное давление ниже 60-70 мм рт.ст., ЦВД падает (20-30 мм вод.ст. и ниже). Наблюдается гипотермия, частый пульс (130-140 уд / мин), олигурия.
- IV степень тяжести наблюдается при дефиците ОЦК более 40%. Состояние очень тяжелое, сознание отсутствует. Артериальное давление и центральное венозное давление не определяется, пульс отмечается только на сонных артериях. Дыхание поверхностное, учащенное, с патологическим ритмом, отмечается подвижное возбуждения, гипорефлексия, анурия.
Лечение геморрагического шока
Устранение причины кровотечения — главный момент лечения геморрагического шока. Выбор метода остановки кровотечения зависит от ее причины. При лечении большое значение имеет скорость компенсации кровопотери и своевременное хирургическое лечение. При II степени тяжести геморрагический шок является абсолютным показанием к оперативной остановке кровотечения.
Инфузионная терапия при геморрагическом шоке должна проводиться в 2-3 вены: при АД в пределах 40-50 мм рт.ст. объемная скорость инфузии должна быть 300 мл / мин при АД 70-80 мм рт.ст. — 150-200 мл / мин при стабилизации АД до 100-110 мм рт.ст. инфузия проводится капельно под контролем АД и почасового диуреза.
Соотношение коллоидов и кристаллоидов должно быть 2:1. В инфузионную терапию включаются: реополиглюкин, волекам, эритромасса, нативная или свежезамороженная плазма (5-6 флаконов), альбумин, раствор Рингера-Локка, глюкоза, панангин, преднизолон, коргликон, для коррекции метаболического ацидоза — 4% раствор гидрокарбоната натрия, трисамин. При гипотензивном синдроме — введение дофамина или допамина. Объем инфузии должен превышать предполагаемую кровопотерю на 60-80%, одновременно проводится гемотрансфузия в объеме не более 75% кровопотери при ее одномоментном замещении, затем отсроченная гемотрансфузия в меньших дозах.
Для ликвидации вазоспазма после устранения кровотечения и ликвидации дефицита ОЦК применяют ганглиоблокаторы с препаратами, которые улучшают реологические свойства крови (реополиглюкин, трентал, компламин, курантил). Необходимо применять глюкокортикоиды в больших дозах (30-50мг/кг гидрокортизона или 10-30мг/кг преднизолона), мочегонные средства, искусственную вентиляцию легких.
Для лечения ДВС-синдрома при ГШ применяют свежезамороженную плазму, ингибиторы протеаз — контрикал (трасилол) по 60-80000 ОД, гордокс по 500-600000 ОД. Дицинон, этамзилат, андроксон снижают ломкость капилляров, усиливают функциональную активность тромбоцитов. Применяют сердечные гликозиды, иммунокорректоры, витамины, по показаниям — антибактериальную терапию, анаболики (неробол, ретаболил), эссенциале.
Летальность при геморрагическом шоке зависит от времени устранения кровотечения, объема кровопотери и проведения мероприятий интенсивной терапии. В настоящее время она составляет около 15% от всех случаев.
Большое значение после интенсивной терапии имеет реабилитационная терапия, лечебная гимнастика.
Геморрагический шок является опасным для жизни осложнением массивного кровотечения и может развиваться после больших хирургических операций. Главным фактором предупреждения геморрагического шока является адекватное восполнение кровопотери и своевременная остановка кровотечения.
Причиной геморрагического шока является острая кровопотеря любого генеза, в частности, травма, операция, повреждение органов и тканей патологическим процессом. Наиболее часто встречаются кровотечения из желудочно-кишечного тракта (в 85% язвенной этиологии) и акушерско-гинекологические кровотечения.
В чистом виде массивная кровопотеря и геморрагический шок наблюдаются относительно редко, чаще сопутствуют или являются компонентом травматического, септического или других видов шока как проявление тяжелых циркуляторных расгройств.
Патогенез геморрагического шока
У молодых здоровых людей кровопотеря 500-750 мл или до 10% ОЦК не вызывает значительных гемодинамических изменений.
Остро возникший дефицит ОЦК (более 20-25%) ведет к уменьшению венозного возврата и, как следствие, снижению сердечного выброса и артериального давления. В ответ на артериальную гипотензию барорецепторы высокого давления дуги аорты вызывают активацию симпато-адреналовой системы с выбросом в кровь катехоламинов (концентрация адреналина может увеличивается в 2 раза, норадреналина - в 6 раз). Адреналин, воздействуя на Р-адренорецепторы, вызывает тахикардию, спазм артерий и вен, содержащих 70% ОЦК. Спазм сосудов кожи, подкожной клетчатки, желудочно-кишечного тракта может обеспечить поступление в сосудистое русло до 500-600 мл крови. Норадреналин, влияя на а-адренорецепторы, вызывает спазм мелких сосудов - артериол и венул, определяющих ОПСС. Вследствие гипердинамии сердца, генерализации вазоспазма и повышения ОПСС, перераспределения крови обеспечивается сердечный выброс, необходимый для поддержания нормального кровообращения головного мозга и сердца.

1. Спазм сосудов почек на фоне гиповолемии и артериальной гипотензии снижает перфузию последних и клинически проявляется олигурией.
2. Спазм сосудов кожи и нарушение микроциркуляции клинически проявляется бледностью кожных покровов и мраморным рисунком кожи.
3. Вазоспазм в бассейне ЖКТ вызывает некроз слизистой оболочки желудка и двенадцатиперстной кишки с образованием так называемых "стрессорных" язв.
4. Констрикция сосудов кожи, подкожной клетчатки, мышц обусловливает развитие тканевой гипоксии, приводящей к накоплению недоокисленных метаболитов, ацидозу и повреждению клеточных мембран эндотелия. Нарушение проницаемости эндотелия, повышение гидростатического давления способствуют переходу жидкой части крови в интерстиций и формированию агрегатов эритроцитов (сладж-синдром), что предрасполагает к развитию в дальнейшем синдрома ДВС.
5. Образующиеся в сосудах микроэмболы, включающие тромбоциты и лейкоциты, с током крови попадают в малый круг кровообращения, вызыват микротромбоз спазмированных сосудов легких, нарушение вен-тиляционно-перфузионных соотношений, что является предпосылкой к развитию респираторного дистресс-синдрома.
6. Нарушение микроциркуляции, вызванное гиперкатехолемией, помимо изменения реологии крови, приводит к ее скоплению в капиллярах и выключению значительного количества жидкости из кровотока, в результате чего развивается феномен патологического депонирования ("секвестрации"). Основу "секвестрированной" крови составляют агрегаты клеток, капли жира, активные полипептиды, кислые метаболиты и другие продукты клеточной деструкции. Образно говоря, такое "кровяное озеро" быстро превращается в болото, так как стаз и ацидоз подготавливают почву для внутрисосудистой коагуляции - синдрома ДВС.
Диагностика геморрагической гиповолемии, как правило, не вызывает затруднений. При осмотре у больных отмечается разной степени выраженности бледность кожных покровов и слизистых оболочек, частый малый пульс, уменьшение кровонаполнения подкожной венозной сети, сосудов склер, снижение артериального давления. Определенные трудности возникают при определении объема кровопотери и степени шока в случае развития картины гиповолемии без артериальной гипотензии.
Информация на сайте подлежит консультации лечащим врачом и не заменяет очной консультации с ним.
См. подробнее в пользовательском соглашении.
Читайте также:

