Герпесвирусная инфекция ассоциированная с цитомегаловирусом
Обновлено: 23.04.2024
1. Институт полиомиелита и вирусных энцефалитов им. М.П. Чумакова РАМН;
2. Инфекционная клиническая больница №1, Москва
Менингоэнцефалит, ассоциированный с цитомегаловирусом, вирусом простого герпеса и вирусом варицелла-зостер
Журнал: Журнал неврологии и психиатрии им. С.С. Корсакова. 2011;111(7): 66‑70
Деконенко Е.П., Рудомётов Ю.П., Русанова С.А., Соколова М.В., Белялетдинова И.Х. Менингоэнцефалит, ассоциированный с цитомегаловирусом, вирусом простого герпеса и вирусом варицелла-зостер. Журнал неврологии и психиатрии им. С.С. Корсакова. 2011;111(7):66‑70.
Dekonenko EP, Rudometov IuP, Rusanova SA, Sokolova MV, Belialetdinova IKh. Meningoencephalitis associated with cytomegalovirus, Herpes simplex and Varicella-zoster virus infections. Zhurnal Nevrologii i Psikhiatrii imeni S.S. Korsakova. 2011;111(7):66‑70. (In Russ.).
1. Институт полиомиелита и вирусных энцефалитов им. М.П. Чумакова РАМН;
2. Инфекционная клиническая больница №1, Москва
1. Институт полиомиелита и вирусных энцефалитов им. М.П. Чумакова РАМН;
2. Инфекционная клиническая больница №1, Москва
Герпетический энцефалит (ГЭ), причиной которого служит вирус простого герпеса 1-го типа (ВПГ-1), является одним из тяжелых и распространенных вирусных поражений нервной системы [1, 11]. Кроме ВПГ-1, другие вирусы семейства герпеса также могут вызывать энцефалиты. Значительно реже причиной нейроинфекций бывает сочетанное поражение двумя вирусами. В литературе представлены немногочисленные случаи энцефалитов и менингитов, вызванные коинфекцией вирусных возбудителей: ВПГ-1 и цитомегаловируса (ЦМВ) [10, 20], ВПГ-1 и кори [5] и др. [6]. В настоящей работе приводится описание редкого случая заболевания у иммунокомпетентной пациентки, при котором после инфекции, ассоциированной с ЦМВ и ВПГ-1, развился эпизод с активацией вируса варицелла-зостер (ВВЗ).
Пациентка З., 16 лет, ученица 10 класса, заболела остро 25.07.08 с появления высокой температуры тела и головной боли. Вечером 26.07.08 развился эпизод бреда и галлюцинаций. Утром 27.07.08 - приступ генерализованных тонико-клонических судорог, который стал причиной госпитализации. За неделю до заболевания был эпизод ОРЗ с кашлем, но без температурной реакции.
При поступлении в больницу состояние тяжелое. Сознание спутанное, дезориентированна, сопротивлялась осмотру, была агрессивной, двигательное беспокойство, нецеленаправленные движения конечностями. На словесные команды не реагировала. Речь в виде отдельных слов и нечленораздельных звуков. Глаза открыты, движения глазных яблок содружественные, но хаотичные, взор стойко не фиксировала. Нарушений черепных нервов и двигательных функций нет. Умеренная ригидность мышц шеи. При люмбальной пункции: цереброспинальная жидкость (ЦСЖ) бесцветная, прозрачная, цитоз 162/3 (68% нейтрофилов), белок и глюкоза в пределах нормы. Микроскопия и посев ликвора возбудителей не обнаружили.
Острое начало заболевания с высокой лихорадкой, нарушением сознания, расстройствами психики, судорогами, признаками воспаления в ЦСЖ заставляли предполагать инфекционное поражение ЦНС. Один из возможных диагнозов - герпетический энцефалит. Как рекомендуется в таких случаях [17], с первого дня госпитализации больной назначен ацикловир в дозе 1,5 г/сут внутривенно. Также пациентка получала цефтриаксон 4,0 г/сут, дексаметазон 12-16 мг/сут, дезинтоксикационную терапию, симптоматические и противосудорожные препараты.

На 14-й день болезни (08.08.08) была проведена компьютерная томография (КТ) головного мозга. В правой височной области, островке и подлежащих отделах головного мозга выявлен очаг пониженной плотности неправильной формы, вероятно, воспалительного характера (рис. 1). Рисунок 1. КТ больной З. на 14-й день болезни. Очаг пониженной плотности в правой височной области и островке.
Результаты КТ свидетельствовали в пользу диагноза герпетического энцефалита, для которого характерны очаги пониженной плотности височной локализации [8, 14, 15]. В течение следующей недели у больной сохранялись высокая температура и спутанность сознания, повторялись эпизоды психических нарушений, галлюцинаций, в связи с чем были увеличены дозы противосудорожных и седативных препаратов. Периоды психического возбуждения сменялись эпизодами сонливости и заторможенности. Со стороны внутренних органов (дыхания и сердечной деятельности) отклонений не наблюдалось.
Повторное исследование ЦСЖ на 19-й день болезни (13.08.08) показало уменьшение цитоза (123/3, 87% лимфоцитов, белок 0,495 г/л). Положительная динамика была отмечена в неврологическом статусе: ясное сознание, отсутствие менингеальных знаков и двигательных нарушений. Выявлялись осиплость голоса вследствие пареза левой половины гортани, симптомы орального автоматизма, патологические стопные знаки. При общении с больной - снижение памяти при сохранной ориентировке в собственной личности.
В восстановительном периоде у больной длительно сохранялась субфебрильная температура (воспалительные изменения в моче), были назначены цефазолин 2,0 г/сут и короткий курс преднизолона. Из других отклонений отмечена аменорея. Осмотр гинеколога патологии не выявил. Аменорея расценена как результат постинфекционного осложнения.
Рентгенография органов грудной клетки и придаточных пазух носа: без патологии. Осмотр окулиста: миопия обоих глаз слабой степени. ЭКГ в динамике: полувертикальная ось сердца, синусовая тахикардия. Электроэнцефалография (ЭЭГ) в дебюте болезни: дезорганизация корковых ритмов, умеренная эпилептическая активность преимущественно в центрально-теменно-височных областях левого полушария. В динамике болезни на ЭЭГ сохранялись умеренные изменения биоэлектрической активности головного мозга. Биохимические анализы крови в пределах нормы. Кровь на RW и ВИЧ-инфекцию отрицательна.
На 34-й день болезни (28.08.08) магнитно-резонансная томография (МРТ) головного мозга выявила в височной доле, островке, наружных отделах подкорковых структур, медиальных отделах лобной доли, частично теменной доли и зрительном бугре правого полушария диффузную зону измененного сигнала, гиперинтенсивного в режимах Т2 и T2 diff и гипоинтенсивного в режиме Т1; признаки объемного воздействия в виде слабой визуализации субарахноидального пространства височной доли и нижнего рога правого бокового желудочка; слева в медиальных отделах височной доли и островке выявлялась небольшая зона аналогично измененного MP-сигнала. Заключение: картина соответствует воспалительным изменениям в обоих полушариях головного мозга (рис. 2). Рисунок 2. МРТ больной З. на 34-й день болезни, аксиальное (а) и сагиттальное (б) изображения. Описание в тексте.
Пациентка была проконсультирована специалистом центра патологии речи. Заключение: модально-неспецифические нарушения памяти; эмоционально-личностные нарушения; грубое нарушение протекания нейродинамических процессов.
Анализ ЦСЖ на 40-й день болезни (03.09.08): бесцветная, прозрачная, белок - 0,33 г/л, цитоз - 38/3. Общий анализ крови при выписке: гемоглобин - 107 г/л, эритроциты - 3,99·10 12 /л, лейкоциты - 5,4·10 9 /л, СОЭ - 18 мм/час. Общий анализ мочи при выписке: относительная плотность - 1022, реакция кислая, белка, сахара нет, лейкоциты - 4 в поле зрения. Анализ мочи по Нечипоренко: без патологии. На фоне улучшения больная в удовлетворительном состоянии 09.09.08 была выписана под наблюдение поликлиники по месту жительства.

Консультация психиатра: продуктивной психопатологии не обнаружено, последствия перенесенной нейроинфекции. При ЭЭГ 16.09.08 отмечалось снижение амплитуды биоэлектрической активности мозга по сравнению с предшествующими записями: доминировала низкоамплитудная активность 10-15 мкВ с пикообразными и заостренными волнами. Анализ ЦСЖ 17.09.08: бесцветная, прозрачная, белок - 0,7 г/л, цитоз - 91/3 (90 лимфоцитов, 1 нейтрофильный лейкоцит). Исследование антител к ВВЗ 18.09.08 (57-й день болезни) выявило повышение титров IgM в сыворотке крови при отсутствии их в ЦСЖ (см. таблицу). Общие анализы крови и мочи, биохимический анализ крови при поступлении в стационар - без патологии.
В качестве противовирусной терапии больной был проведен курс валтрекса по 0,5 г 3 раза в день в течение 2 нед. Из других препаратов назначены депакин-хроно 150 мг 2 раза в сутки, сибазон 2,5 мг 2 раза в сутки, глиатилин 400 мг 3 раза в сутки. На фоне терапии состояние пациентки улучшилось, стала спокойной, общительной, хотя и с элементами эйфории. Высыпания затянулись, оставив пигментацию. В неврологическом статусе ухудшений не отмечалось.
30.09.08 пациенка была консультирована нейропсихологом, отмечены нарушения нейродинамического и регуляторного аспектов психической деятельности, неспецифические нарушения памяти и эмоциональной сферы, свидетельствующие о дисфункции базальных отделов лобно-височной коры, патологии конвекситальных отделов височных и затылочных зон коры больших полушарий.
Глазное дно не изменено. ЭКГ: нормальное положение ЭОС, синусовая тахикардия. В остальном без особенностей. Выписана 01.10.08 в удовлетворительном состоянии под наблюдение невролога по месту жительства. Рекомендовано продолжить прием глиатилина по 400 мг 3 раза в сутки, сибазона по 2,5 мг 2 раза в сутки, депакина по 150 мг 2 раза в сутки.
На МРТ от 28.11.08 отмечена положительная динамика по сравнению с предшествующим исследованием (от 28.08.08) в виде уменьшения измененного МР-сигнала в правом полушарии большого мозга и отсутствия признаков объемного воздействия.
Пациентка находилась под нашим наблюдением с дебюта заболевания. При последнем осмотре 08.11.10 активно жалоб не предъявляет. Неврологически: мелкоразмашистый нистагм вправо, легкая девиация языка. Анизорефлексия сухожильных рефлексов на фоне их оживления: на руках выше слева, на ногах - выше справа. В пробе Ромберга покачивание. Эмоциональная лабильность. Работает и успешно учится на 2-м курсе вечернего института.

При МРТ-исследовании от 08.11.10 сохраняются поствоспалительные изменения в обоих полушариях большого мозга (рис. 3). Рисунок 3. МРТ пациентки З., аксиальное изображение.
Окончательный диагноз: острый менингоэнцефалит, ассоциированный с ЦМВ, ВПГ-1 и ВВЗ, тяжелая форма.
Представлен редкий случай острого тяжелого менингоэнцефалита у 16-летней девушки, вызванный ЦМВ и ВПГ-1 и осложнившийся реактивацией латентной варицелла-зостерной инфекции. В доступной нам литературе мы не встретили подобного описания острого менингоэнцефалита, ассоциированного с последовательной инфекцией тремя вирусами герпеса.
В настоящее время большинство нейроинфекций диагностируется с применением метода ПЦР, имеющего большие преимущества - быстрота, экономичность, возможность одновременного обследования большого числа пациентов. Однако он не лишен недостатков, поскольку может быть псевдонегативным в первые 3-4 дня болезни и чувствительность его существенно снижается после 10-20-го дня болезни. В последнее время появляются публикации, указывающие на его недостаточную чувствительность и рекомендующие применение испытанных тестов с определением антител в ЦСЖ [3, 7].
Так, канадские исследователи проанализировали 12-летнюю статистику (1994-2005) частоты клинических, лабораторных и инструментальных данных, эффективности терапии и исходов ГЭ на примере больницы Торонто [7]. ГЭ был диагностирован у 16 пациентов. У 12 (75%) больных в ЦСЖ был обнаружен вирус герпеса методом ПЦР, из них у 2 анализ был отрицательным в 1-й день, но положительным на 3-7-й день госпитализации. У 4 больных с отрицательными результатами ПЦР получено более чем 4-кратное нарастание титра противовирусных антител в периоде выздоровления. У 4 (25%) пациентов с положительной ПЦР в ЦСЖ не было увеличения титров антител. У 5 больных имели место ложноположительные результаты ПЦР в ЦСЖ, из них у 4 серологические анализы были отрицательными. Авторы публикации считают, что метод диагностики ГЭ с помощью исследования антител в ЦСЖ используется незаслуженно редко.
Ряд исследователей считают целесообразным использовать метод ПЦР параллельно с серологическим исследованием крови и ЦСЖ, поскольку: 1) ДНК вируса определяется преимущественно в первые 10-14 дней болезни, а больной может поступать и исследоваться в более поздние сроки; 2) метод ПЦР может быть псевдонегативным или псевдопозитивным, и параллельное исследование антител повышает результативность исследования [16].
Следующий вывод - возможность вирусных осложнений в восстановительный период после перенесенного энцефалита в стадии ранней реконвалесценции. Реактивация латентной ВВЗ могла быть пропущена, если сыпь была бы менее манифестной или отсутствовала, что нередко бывает при реактивации ВВЗ [9].
Нейтрофильный состав ЦСЖ, который определялся у нашей больной при первом ее исследовании (68% нейтрофилов), может быть при вирусных поражениях ЦНС в дебюте заболевания (ВПГ-1, ЦМВ). Мы наблюдали нейтрофильный состав ЦСЖ у 4% больных с герпетическим энцефалитом [2].
Хотя течение энцефалита у нашей больной было тяжелым, его исход можно считать достаточно благополучным, несмотря на двустороннее поражение головного мозга, которое протекает, как правило, с более тяжелыми последствиями. Больная полностью сохранила познавательные способности и после заболевания поступила в институт, где успешно учится. Вероятно, сказался положительный эффект рано начатого и полноценного лечения ацикловиром.
Инфекции вызванные цитомегаловирусом: диагностика, лечение, профилактика
Вирусы герпеса — большие, покрытые оболочкой, двунитевые ДНК-вирусы (120—200 нм). Геном содержит 120—240 тыс. пар нуклеотидов, кодирующих более 35 белков. Оболочка состоит из гликопротеинов и Fc-рецепторов. Инфекция персистирует у человека на протяжении всей жизни, переходя в латентную форму после острой стадии и периодически рецидивируя (особенно при снижении иммунитета у человека).
Классификация герпес-вирусов
Все вирусы герпеса разделяют на:
• а-герпес-вирусы — быстрорастущие цитолитические вирусы, вызывающие латентную инфекцию и поражающие нейроны (вирусы простого и опоясывающего герпеса);
• бета-герпес-вирусы — медленно растущие вирусы, вызывающие латентные инфекции секреторных желёз и почек (цитомегаловирус);
• у-герпес-вирусы — вирусы, вызывающие латентный инфекционный процесс в лимфоидной ткани (вирус Эпштейна—Барр).
Недавно обнаруженные вирусы герпеса человека типа 6 и 7 (ВГЧ-6 и ВГЧ-7) относят к у-герпес-вирусам, так как они вызывают латентные инфекции лимфатических узлов и имеют генетические сходства именно с этой группой вирусов герпеса. ВГЧ-8, ассоциированный с саркомой Капоши, сходен с вирусом Эпштейна—Барр. Все вирусы герпеса, за исключением вируса простого герпеса типа 1 и 2, различны по антигенной структуре.
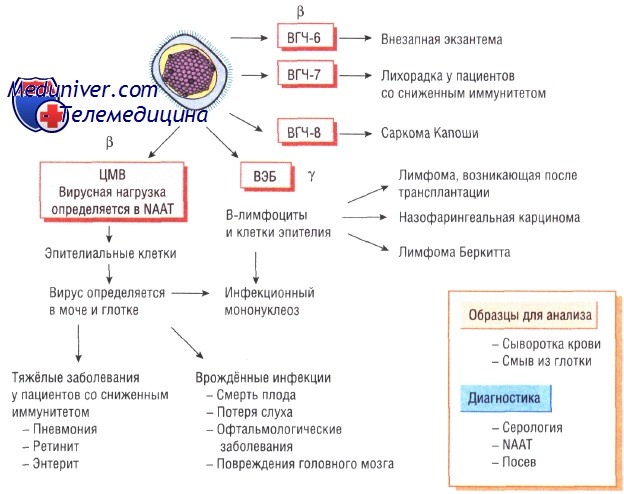
Инфекции вызванные цитомегаловирусом
По своей структуре цитомегаловирус похож на все остальные вирусы герпеса. Обычно он персистирует в организме на протяжении всей жизни. Его обнаруживают в моче и слюне человека. Примерно 50% населения Великобритании инфицированы ВГЧ-5.
Эпидемиология и патогенез цитомегаловирусной инфекции. Механизм передачи инфекции — вертикальный или контактный (от человека к человеку). Чем ниже социально-экономические условия, тем раньше происходит инфицирование. Возможен вертикальный механизм передачи инфекции. Кроме того, заражение может произойти при переливании крови или пересадке органов; в этом случае инфекции свойственно очень тяжёлое течение.
Клинические признаки инфекции вызванной цитомегаловирусом. Врождённая инфекция обычно протекает в тяжёлой форме. В начальном периоде выраженные симптомы заболевания отсутствуют. В дальнейшем возникает прогрессирующая глухота, задержка развития. При заражении после рождения заболевание протекает в лёгкой форме. У пациентов со сниженным иммунитетом (ВИЧ-инфекция, состояние после трансплантации органов) может развиться тяжёлая пневмония, ретинит, поражение кишечника, причём вирусная инфекция может быть приобретённой (от пересаженного органа) или собственной (латентная форма).
Диагностика инфекции вызванной цитомегаловирусом. Врождённую инфекцию диагностируют при проведении анализа мочи через 3 нед после рождения. У взрослых цитомегаловирус может быть культивирован либо определён молекулярно-генетическим методом в образцах мочи и крови. Исследование вирусной нагрузки имеет большое значение для диагностики тяжёлого течения инфекции и назначения своевременного лечения.
Лечение и профилактика инфекции вызванной цитомегаловирусом. При тяжёлой инфекции, угрожающей жизни пациента, а также при риске потери зрения лечение проводят ганцикловиром в комплексе с иммуноглобулином (при развитии пневмонии). Эфир ганцикловира, валганцикловир принимают внутрь, назначают в начале лечения и в качестве поддерживающей терапии. Ещё более токсичные альтернативные препараты (фоскарнет и цидофовир) ингибируют цепочечную ДНК-полимеразу. Важная мера профилактики заболевания — тщательный подбор донорских органов для пересадки и крови для переливания.
Редактор: Искандер Милевски. Дата обновления публикации: 18.3.2021
Клиника и диагностика поражений вирусом простого герпеса при иммунодефиците
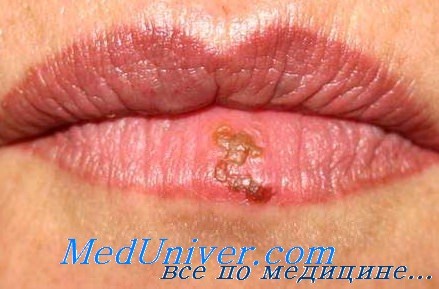
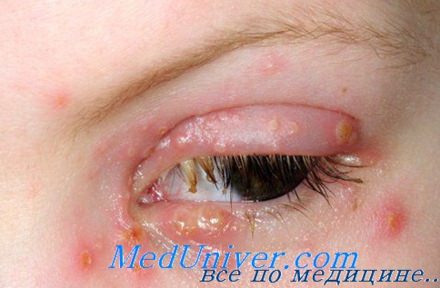
Поражение лица и ротоглотки наиболее типично для реактивации герпесвирусной инфекции. Морфология герпетических высыпаний зависит от типа пораженной эпителиальной ткани. На красной кайме губ и коже лица первичными элементами являются мелкие везикулы, которые возникают последовательно, имеют тенденцию к быстрому слиянию и формированию крупного вялого пузыря. Эти элементы умеренно болезненны, типично ощущение жжения.
После отторжения некротизированного эпителия обнажаются эрозированные кровоточащие поверхности, по краям которых появляются новые мелкие везикулы, и элемент начинает расти от центральной части к периферии.
Суперинфицирование элементов часто приводит к возникновению глубоких некрозов, заживающих с формированием рубца. Поражение лица вирусом герпеса следует дифференцировать от поражения зигомицетами (Absidia, Rhisopus, Mucor) и Aspergillus, которые вызывают тяжелые некрозы тканей лица, расплавление хрящей и костей лицевого скелета с быстрым обезображиванием внешнего облика пациента.
На слизистой оболочке рта наиболее типичным является возникновение нескольких одинаковых поверхностных некротических элементов диаметром 1—3 мм, которые затем углубляются и увеличиваются в размерах, часто сливаются. В самых тяжелых случаях значительная площадь полости рта поражена крайне болезненными глубокими некрозами серого цвета с кровоточащими участками эрозий.
В прошлом, до введения всеобщей профилактики ацикловиром, у больных после ТКМ герпетические поражения ротоглотки нередко становились причиной обструкции верхних дыхательных путей, в связи с чем возникала необходимость в протективной интубации трахеи.
Процесс заживления глубоких некрозов часто проходит стадию отторжения фибриновых пленок с обнажением ригидных сосудов десен, что может быть чревато значительной кровопотерей, особенно у детей младшего возраста. Мы наблюдали кровотечения из язв на деснах в объеме до 400 мл в сутки. Кроме того, заживление язв нередко сопровождается обильной саливацией: потерей до 700—900 мл слюны в сутки, что может стать причиной обезвоживания у детей.
Знание закономерностей развития герпетического стоматита позволяет сделать вывод, что при нейтропении лечение его нельзя ограничивать ацикловиром: необходимо назначать препараты, активные в отношении стрептококков, анаэробов, грамотрицательной флоры и грибов. Монотерапии, отвечающей таким требованиям, не существует, поэтому при фебрильной нейтропении, сопровождающейся стоматитом, мы наряду с ацикловиром всегда используем бета-лактам с расширенным спектром антианаэробной активности (пиперациллин/тазобактам, имипенем, амоксициллин/клавуланат) либо к другим бета-лактамам добавляем метронидазол.
Часто драматического улучшения удается добиться при использовании клиндамицина или пенициллина. Кроме того, мы рекомендуем и сами всегда используем системную противогрибковую терапию.
Поражение вирусом простого герпеса пищевода
При распространении инфекции из полости ротоглотки поражается верхний сегмент пищевода. Другой путь — контаминация инфицированной герпес-вирусом слюной эрозированного (в результате желудочно-пищеводного рефлюкса или рвоты) пищевода. В этом случае поражается нижний сегмент пищевода. Клиническая картина среднего и дистального эзофагита очень типична: больные жалуются на ощущение кома за грудиной, сильное жжение и боли, которые значительно усиливаются после глотания и рвоты.
Следует отметить, что последняя локализация — одно из самых опасных проявлений герпесвирусной инфекции, поскольку именно дистальный эзофагит служит воротами для развития инвазивных бактериальных и грибковых инфекций. По морфологической картине (язвенно-некротические элементы, захватывающие все слои пищевода) отличить герпетическое поражение от цитомегаловирусного, бактериального или грибкового не представляется возможным. Без проведения биопсии установить точный микробиологический диагноз невозможно.
Если принято решение выполнить эзофагоскопию и биопсию, то для диагностики герпес-вирусного поражения необходимо получить биоптат эпителия края язвы, а для диагностики ЦМВ-поражения — ее дна. Это связано с тем, что герпес-вирус поражает эпителий, а цитомегаловирус — строму.
При герпетическом эзофагите, как и при герпетическом стоматите, особенно больным с фебрильной нейтропенией, наряду с ацикловиром всегда следует назначать антимикотик системного действия (амфотерицин В внутривенно в дозе 0,3—0,5 мг/кг в сутки, флюконазол внутривенно или внутрь, возможно вориконазол и итраконазол) и системные антибиотики, обладающие антианаэробной активностью.
Важную роль играют антацидная и антирефлюксная (ранитидин или омепразол, дофаминовые антагонисты) терапия и адекватное обезболивание наркотиками.
Поражение бронхиального дерева и легких вирусом простого герпеса
Чаще всего герпетический трахеобронхит развивается у иммунокомпрометированных больных с герпетическим эзофагитом, которые интубированы и находятся на искусственной вентиляции легких. Наблюдаются также фокальные герпетические пневмонии. Диффузные пневмонии с развитием дыхательной недостаточности, напротив, являются следствием диссеминированной герпетической инфекции у больных с глубоким дефицитом клеточного или гуморального иммунитета.
Поражение вирусом простого герпеса центральной нервной системы
Герпетический энцефалит — очень редкое проявление реактивации герпесвирусной инфекции у онкогематологических больных. Он не отличается от энцефалита у иммунокомпетентного хозяина, т. е. характеризуется энцефалитическим синдромом и признаками воспаления и некроза на компьютерных и ядерно-магнитных томограммах. Поражение спинного мозга вирусом герпеса является казуистикой. Описаны случаи восходящего поперечного миелита.
Диагностика поражений вируса простого герпеса
Известно несколько методов быстрой и специфической диагностики герпесвирусной инфекции. Классическим методом является выделение вируса, основанное на его цитопатическом действии на чувствительные культуры клеток млекопитающих. Этот метод достаточно быстрый (90 % позитивных результатов в первые 3 дня, 100% —в первые 7 дней культивирования) и весьма специфичный.
Существует более быстрый метод (комбинация иммуноферментного и культурального методов), которым выявляют наличие вирусных антигенов в чувствительной клеточной культуре, зараженной исследуемым материалом. Этот метод аналогичен описанному ранее методу shell vial для ЦМВ и позволяет получить результаты в течение суток.
Следует отметить, что, как и при ЦМВ-инфекции, серологические данные (наличие специфического IgM или повышение титра IgG) и выделение вируса простого герпеса со слюной не несут полезной оперативной информации. Особенно важно это при диагностике герпесвирусного энцефалита. Нам доводилось наблюдать неадекватную интерпретацию серологических тестов у больных с энцефалитическим синдромом и необоснованное назначение ацикловира в высоких дозах. Единственным надежным методом диагностики является проведение биопсии ткани головного мозга и вирусологического исследования.
Редактор: Искандер Милевски. Дата обновления публикации: 18.3.2021
Цитомегаловирусная инфекция (ЦМВ-инфекция) у гематологических больных
Среди вирусных инфекций, поражающих больных с нарушениями иммунитета, герпетическим вирусам принадлежит особая роль. С одной стороны, вирусы этой группы часто вызывают тяжелые органные поражения, напрямую угрожающие жизни больного, а с другой — разработанные методы вирусологического мониторинга, профилактической и упреждающей терапии позволяют свести этот риск к минимуму.
В статьях на нашем сайте рассмотрены особенности эпидемиологии и клинической картины инфекций, вызываемых лишь несколькими герпес-вирусами, наиболее часто встречающихся у гематоонкологических больных, а также изложены рациональные подходы к диагностике и лечению этих заболеваний.
Цитомегаловирус (ЦМВ) — один из самых частых вирусных спутников человека. В развитых странах 50—80 % населения в возрасте до 50 лет переносят инаппарантную инфекцию и являются серопозитивными по ЦМВ, в то время как в странах с низким или средним социально-экономическим развитием практически 100 % населения к 30 годам являются серопозитивными. Такая же закономерность наблюдается в различных в отношении материальной обеспеченности слоях населения: при высоком материальном достатке и часто соответствующем ему более высоком культурном уровне средний возраст первичной ЦМВ-контаминации, регистрируемой по сероконверсии, значительно выше, чем при среднем и низком достатке.
Причина этого феномена кроется, по всей вероятности, в менее строгих гигиенических правилах и традициях (например, облизывание матерями детских сосок, пользование одной и той же посудой и столовыми приборами и т. д.).

Главными эффекторами антицитомегаловирусного иммунитета являются вирусспецифические цитотоксические лимфоциты, в то время как все типы антител в лучшем случае играют вспомогательную роль. Отсюда очевидно, что наиболее уязвимой группой в отношении развития тяжелой первичной инфекции или клинически значимой реактивации являются больные с врожденным либо приобретенным (в том числе ятрогенным) дефицитом клеточного иммунитета.
Кроме факта наличия клеточного иммунодефицита, важный фактор риска — его длительность. Классической демонстрацией данного положения является различие в частоте реактивации ЦМВ и развития ЦМВ-синдрома и ЦМВ-пневмонии у реципиентов при трансплантации аллогенного и аутологичного костного мозга. При одинаковой исходной степени иммуносупрессии, но несоизмеримо более короткой ее продолжительности ЦМВ-пневмония, которая развивалась у 30—40 % реципиентов после аллогенной трансплантации костного мозга (ТКМ) до разработки упреждающего или профилактического лечения ганцикловиром, является казуистикой (не более 0,5 %) после аутологичной трансплантации.
Группы риска в отношении развития тяжелой ЦМВ-инфекции:
1) перинатально инфицированные новорожденные (особенно недоношенные);
2) дети с тяжелыми комбинированными врожденными иммунодефицитами;
3) больные СПИДом;
4) реципиенты аллогенной трансплантации гемо-поэтических стволовых клеток;
5) реципиенты солидных органов.
В отношении больных, которым проводят стандартную химиотерапию по поводу лейкозов, лимфом или солидных опухолей, статистики, оценивающей частоту развития ЦМВ-ассоциированных клинических синдромов, не существует, хотя описаны как отдельные случаи, так и небольшие серии тяжелых проявлений ЦМВ-инфекции в данных группах.
Справедливо считать, что развитие клинически значимых симптомов ЦМВ-инфекции теоретически возможно у любого больного после цитотоксической иммуносупрессивной терапии, однако большинство таких больных составляют реципиенты аллогенной ТКМ. Наличие современных специфичных и чувствительных методов быстрой диагностики делают абсолютно неприемлемой эмпирическую терапию не только потому, что такое лечение достаточно дорого и токсично, но и потому, что цена ошибки и соответственно неадекватного лечения при постановке диагноза только по клиническим симптомам слишком велика. Так, на основании клинической картины очень трудно отличить ЦМВ-пневмонию от пневмоцистоза или лучевого пневмонита, а затяжной ЦМВ-гепатит — от хронического гепатолиенального кандидоза.
Как отмечалось, подавляющее большинство взрослых больных и значительный процент детей в нашей стране ЦМВ-серопозитивны, поэтому наблюдать в гематологическом стационаре первичную ЦМВ-инфекцию приходится нечасто. Непосредственная передача ЦМВ от одного больного к другому маловероятна, если больные не вступают в контакт более близкий, чем это предписано больничным режимом. В зависимости от серологического статуса, степени и длительности иммуносупрессии проявления ЦМВ-инфекции у гематологических больных могут быть различными.
Редактор: Искандер Милевски. Дата обновления публикации: 18.3.2021
Читайте также:

