Гомеопатией можно вылечить цитомегаловирус
Обновлено: 19.04.2024
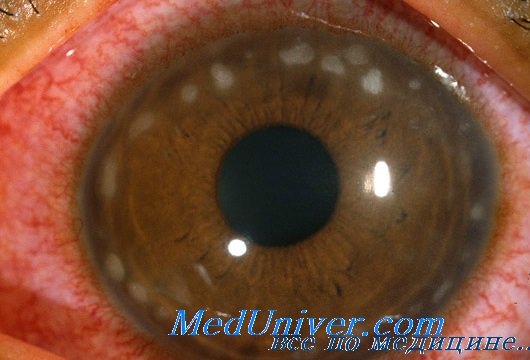
Поражение глаз при цитомегаловирусной инфекции (ЦМВ)
Цитомегаловирус человека является членом семейства герпесвирусов, содержит ДНК, покрыт липидсодержащей оболочкой, размножается медленно внутриклеточно. При этом пораженные клетки увеличиваются в размерах и содержат крупные внутриядерные включения, что отразилось в названии вируса. От других герпесвирусов отличается сравнительно низкой вирулентностью, резким подавлением клеточного иммунитета, меньшей чувствительностью к аналогам нуклеозидов. Культивируется только в культуре человеческих фибробластов, давая цитопатический эффект лишь через 30—50 дней. Известно три его штамма: Davis, AD-169, Kerr.
Источником ЦМВ инфекции являются люди, зараженные цитоме-галовирусом, количество которых в возрасте после 50 лет составляет более 75-90%. Цитомегаловирус содержится в грудном молоке, слюне, крови, фекалиях, моче, семенной жидкости, в секрете шейки матки. Заражение происходит внутриутробно в 0,3-2,4% случаев, в родовом канале, при грудном вскармливании, через слюну, контактным путем, в том числе половым, при переливании крови, пересадке органов.
Цитомегаловирус проникает в организм трансплацентарно, через слизистые оболочки или поврежденную кожу. В здоровом организме он персистирует пожизненно в виде латентной бессимптомной инфекции, лишь изредка возникает мононуклеоз-ная форма заболевания. При заражении же лица с ослабленным Т-клеточным иммунитетом или его ослаблении у зараженного происходит реактивация вируса с появлением клинически выраженных форм болезни. Иммунодефицит развивается при СПИДе, у реципиентов аллотрансплантатов, больных, принимающих иммунодепрессанты и цитостатики, и в других случаях.
Цитомегаловирусная инфекция у лиц с иммунодефицитом начинается с продолжительной лихорадки, слабости, анорексии, ночных потов, миалгии, артралгии. Часто развивается пневмония, гепатит, поражается желудочно-кишечный тракт с возникновением язв в пищеводе, желудке, тонкой и толстой кишке, ретинит. Развивается лейкопения с появлением атипичных мононуклеаров, тромбоцитопения, нарушаются функции печени.
Частота хориоретинита у новорожденных с генерализованной цитомегаловирусной инфекцией может достигать 30%. Врожденная ЦМВ-инфекция может быть асимптомной или же проявляться различными поражениями глаз: дакриоциститом, дактриоаденитом, конъюнктивитом, помутнением роговицы, кератомаляцией, склеритом, катарактой, хориоретинитом, периваскулярным экссудатом сетчатки, ретинальными кровоизлияниями, атрофией зрительного нерва, врожденными дефектами зрительного нерва, а в некоторых случаях и полной гибелью глаза.
Развивающиеся при ретините атрофия и рубцевание сетчатой оболочки могут привести к ее отслойке, вызывая внезапную и полную потерю зрения. Цитомегаловирусный ретинит часто является проявлением генерализованной формы инфекции и требует полного обследования больного с определением наличия вирусемии методом ПЦР. Цитомегаловирус может обнаруживаться в слезной жидкости у больных хориоретинитом.
Редактор: Искандер Милевски. Дата обновления публикации: 18.3.2021
Одной из актуальных проблем современной медицины является высокая инфицированность населения одним из представителей оппортунистических возбудителей — вирусом Эпштейна–Барр (ВЭБ).
Одной из актуальных проблем современной медицины является высокая инфицированность населения одним из представителей оппортунистических возбудителей — вирусом Эпштейна–Барр (ВЭБ). Практикующие врачи в своей повседневной практике чаще сталкиваются с клинически манифестными формами первичной Эпштейна–Барр-вирусной инфекции (ЭБВИ) в виде острой, как правило, не верифицированной респираторной инфекцией (более 40% случаев) или инфекционным мононуклеозом (около 18% всех заболеваний) [1, 2]. В большинстве случаев эти заболевания протекают доброкачественно и заканчиваются выздоровлением, но с пожизненной персистенцией ВЭБ в организме переболевшего [1, 3–5].
Однако в 10–25% случаев первичное инфицирование ВЭБ, протекающее бессимптомно, и острая ЭБВИ могут иметь неблагоприятные последствия [6–9] с формированием лимфопролиферативных и онкологических заболеваний, синдрома хронической усталости, ВЭБ-ассоциированного гемофагоцитарного синдрома и др. [7, 9, 11–14].
До настоящего времени нет четких критериев, позволяющих прогнозировать исход первичного инфицирования ВЭБ. Перед врачом, к которому обращается пациент с острой ЭБВИ, всегда встает вопрос: что предпринять в каждом конкретном случае, чтобы максимально снизить риск развития хронической ЭБВИ и ВЭБ-ассоциированных патологических состояний Этот вопрос не праздный, и ответить на него действительно очень трудно, т. к. до сих пор нет четкой патогенетически обоснованной схемы лечения больных, а имеющиеся рекомендации часто противоречат друг другу.
По мнению многих исследователей, лечение ЭБВИ-мононуклеоза (ЭБВИМ) не требует назначения специфической терапии [15–17]. Лечение больных, как правило, проводится в амбулаторных условиях, изоляция пациента не требуется. Показаниями к госпитализации следует считать длительную лихорадку, выраженный синдром тонзиллита и/или синдром ангины, полилимфаденопатию, желтуху, анемию, обструкцию дыхательных путей, боли в животе и развитие осложнений (хирургических, неврологических, гематологических, со стороны сердечно-сосудистой и дыхательной системы, синдром Рейе).
При легком и среднетяжелом течении ЭБВ ИМ больным целесообразно рекомендовать палатный или общий режим с возвращением к обычной деятельности на адекватном для каждого конкретного больного физическом и энергетическом уровне. Проведенное многоцентровое исследование показало, что необоснованно рекомендуемый строгий постельный режим удлиняет период выздоровления и сопровождается длительным астеническим синдромом, требующим нередко медикаментозного лечения [18].
При легком течении ЭБВ ИМ лечение больных ограничивается поддерживающей терапией, включающей адекватную гидратацию, полоскание ротоглотки раствором антисептиков (с добавлением 2% раствора лидокаина (ксилокаина) при выраженном дискомфорте в глотке), нестероидные противовоспалительные препараты, такие как парацетамол (Ацетаминофен, Тайленол). По мнению ряда авторов назначение блокаторов Н2 рецепторов, витаминов, гепатопротекторов и местная обработка миндалин различными антисептиками являются малоэффективными и необоснованными способами лечения [19, 20]. Из экзотических методов лечения следует упомянуть рекомендуемое Ф. Г. Боковым и соавт. (2006) применение мегадоз бифидобактерий при лечении больных острым мононуклеозом [21].
Мнения о целесообразности назначения антибактериальных препаратов при лечении ЭБВИМ весьма противоречивы. По мнению Gershburg E. (2005) тонзиллит при ИМ часто асептический и назначение антибактериальной терапии не оправдано. Также нет смысла в применении антибактериальных средств при катаральной ангине [4]. Показанием для назначения антибактериальных препаратов является присоединение вторичной бактериальной инфекции (развитие у больного лакунарной или некротической ангины, таких осложнений, как пневмония, плеврит и др.), о чем свидетельствуют сохраняющиеся более трех суток выраженные воспалительные изменения показателей крови и фебрильная лихорадка. Выбор препарата зависит от чувствительности микрофлоры на миндалинах больного к антибиотикам и возможных побочных реакций со стороны органов и систем.
По данным H. Fota-Markowcka et al. (2002) у больных чаще выделяют гемофильную палочку, стафилококк и пиогенный стрептококк, реже — грибы рода Candida [22], поэтому следует признать обоснованным назначение этим больным препаратов из группы цефалоспоринов 2–3 поколения, линкосамидов, макролидов и противогрибковых средств (флуконазол) в терапевтических дозах на 5–7 дней (реже — 10 дней) [4]. Некоторые авторы при наличии некротической ангины и гнилостном запахе изо рта, вызванных, вероятно, ассоциированной анаэробной флорой, рекомендуют использовать метронидазол по 0,75 г/сут, разделенных на 3 приема, в течение 7–10 дней.
Противопоказаны препараты из группы аминопенициллинов (ампициллин, амоксициллин (Флемоксин Солютаб, Хиконцил), амоксициллин с клавуланатом (Амоксиклав, Моксиклав, Аугментин)) из-за возможности развития аллергической реакции в виде экзантемы. Появление сыпи на аминопенициллины не является IgE-зависимой реакцией, поэтому применение блокаторов Н1 гистаминовых рецепторов не имеет ни профилактического, ни лечебного эффекта [19].
По мнению ряда авторов до настоящего времени сохраняется эмпирический подход к назначению глюкокортикостероидов больным с ЭБВИ [23]. Глюкокортикостероиды (преднизолон, преднизон (Делтазон, Метикортен, Оразон, Ликвид Пред), Солу Кортеф (гидрокортизон), дексаметазон) рекомендуются больным с тяжелым течением ЭБВИМ, с обструкцией дыхательных путей, неврологическими и гематологическими осложнениями (тяжелая тромбоцитопения, гемолитическая анемия) [4, 24]. Суточная доза преднизолона составляет 60–80 мг в течение 3–5 дней (реже 7 дней) с последующей быстрой отменой препарата. Одинаковой точки зрения на назначение этим больным глюкокортикостероидов при развитии миокардита, перикардита и поражениях ЦНС нет.
При тяжелом течении ЭБВИМ показана внутривенная дезинтоксикационная терапия, при разрыве селезенки — хирургическое лечение.
Наиболее дискуссионным остается вопрос о назначении противовирусной терапии больным с ЭБВИ. В настоящее время известен большой перечень препаратов, являющихся ингибиторами ВЭБ репликации в культуре клеток [4, 25–27].
I. Подавляющие активность ДНК-полимеразы ВЭБ:
- ациклические аналоги нуклеозидов (ацикловир, ганцикловир, пенцикловир, валацикловир, валганцикловир, фамцикловир);
- ациклические аналоги нуклеотидов (цидофовир, адефовир);
- аналоги пирофосфатов (Фоскарнет (фоскавир), фосфоноацетиловая кислота);
- 4 оксо-дигидрохинолины (возможно).
II. Различные соединения, не ингибирующие вирусной ДНК-полимеразы (механизм изучается): марибавир, бета-L-5 урацил йододиоксолан, индолокарбазол.
Однако проведенный метаанализ пяти рандомизированных контролируемых испытаний с участием 339 больных ЭБВИМ, принимавших ацикловир (Зовиракс), показал неэффективность препарата [28, 29].
Одна из возможных причин кроется в цикле развития ВЭБ, в котором ДНК вируса имеет линейную либо циркулярную (эписома) структуру и размножается в ядре клетки хозяина. Активная репликация вируса происходит при продуктивной (литической) стадии инфекционного процесса (ДНК ВЭБ линейной формы). При острой ЭБВИ и активации хронической ЭБВИ происходит цитолитический цикл развития вируса, при котором он запускает экспрессию собственных ранних антигенов и активирует некоторые гены клеток макроорганизма, продукты которых участвуют в репликации ВЭБ. При латентной ЭБВИ ДНК вируса имеет вид эписомы (круговой суперспиральный геном), находящейся в ядре. Циркулярный геном ДНК ВЭБ характерен для CD21+ лимфоцитов, в которых даже при первичном инфицировании вирусом практически не наблюдается литической стадии инфекционного процесса, а ДНК воспроизводится в виде эписомы синхронно с клеточным делением инфицированных клеток. Гибель пораженных ВЭБ В лимфоцитов связана не с опосредованным вирусом цитолизом, а с действием цитотоксических лимфоцитов [4].
При назначении противовирусных препаратов при ЭБВИ врач должен помнить, что их клиническая эффективность зависит от правильной трактовки клинических проявлений болезни, стадии инфекционного процесса и цикла развития вируса на этой стадии. Однако не менее важным является и тот факт, что большинство симптомов ЭБВИ связаны не с прямым цитопатическим действием вируса в инфицированных тканях, а с опосредованным иммунопатологическим ответом ВЭБ-инфицированных В лимфоцитов, циркулирующих в крови и находящихся в клетках пораженных органов. Именно поэтому аналоги нуклеозидов (ацикловир, ганцикловир и др.) и ингибиторы полимеразы (Фоскарнет), подавляющие репликацию ВЭБ и уменьшающие содержание вируса в слюне (но не санирующие ее полностью [4], не оказывают клинического эффекта на тяжесть и продолжительность симптомов ЭБВИМ.
Показаниями для лечения ЭБВИМ противовирусными препаратами являются: тяжелое, осложненное течение болезни, необходимость профилактики ВЭБ-ассоциированной В-клеточной лимфопролиферации у иммунокомпрометированных пациентов, ВЭБ-ассоциированная лейкоплакия. Bannett N. J., Domachowske J. (2010) рекомендуют применять ацикловир (Зовиракс) внутрь в дозе 800 мг внутрь 5 раз в сутки в течение 10 дней (или 10 мг/кг каждые 8 часов в течение 7–10 дней). При поражениях нервной системы предпочтителен внутривенный способ введения препарата в дозе 30 мг/кг/сут 3 раза в сутки в течение 7–10 дней.
По мнению E. Gershburg, J. S. Pagano (2005), если под действием каких-либо факторов (например, иммуномодуляторов, при ВЭБ-ассоциированных злокачественных опухолях — применение лучевой терапии, гемцитабина, доксорубицина, аргинина бутирата и др.) удается перевести ДНК ВЭБ из эписомы в активную репликативную форму, т. е. активировать литический цикл вируса, то в этом случае можно ожидать клинический эффект от противовирусной терапии.
В комплексной терапии рекомендуется внутривенное введение иммуноглобулинов (Гаммар-П, Полигам, Сандоглобулин, Альфаглобин и др.) 400 мг/кг/сут, № 4–5.
В последние годы все чаще для лечения ЭБВИ стали применять рекомбинантные альфа-интерфероны (Интрон А, Роферон-А, Реаферон-ЕС) по 1 млн ME в/м в течение 5–7 дней или через день; при хронической активной ЭБВИ — 3 млн ME в/м 3 раза в неделю, курс 12–36 недель.
Медикаментозная коррекция астенического синдрома при хронической ЭБВИ включает назначение адаптогенов, высоких доз витаминов группы В, ноотропных препаратов, антидепрессантов, психостимуляторов, препаратов с прохолинергическим механизмом действия и корректоров клеточного метаболизма [30–32].
Залогом успешного лечения больного с ЭБВИ являются комплексная терапия и строго индивидуальная тактика ведения как в стационаре, так и во время диспансерного наблюдения.
Литература
И. В. Шестакова, доктор медицинских наук, доцент
Н. Д. Ющук, доктор медицинских наук, профессор, академик РАМН
МГМСУ, Москва
В последнее десятилетие характер серьезной медико-социальной проблемы приобрели оппортунистические инфекции вследствие их широкого распространения и крайне неблагоприятного влияния на уровень общего и репродуктивного здоровья населения [1,2,6,7]. Результаты проведенных исследований свидетельствуют о росте ЦМВ-инфекции при патологии генитального тракта у женщин [5,7]. Генерализованная форма цитомегаловирусной инфекции у женщин может проявляться в виде воспаления и эрозии шейки матки, внутреннего слоя матки, влагалища и яичников, а у мужчин генерализованная форма цитомегаловирусной инфекции поражает яички, околоушные железы, вызывает воспаление мочеиспускательного канала и неприятные ощущения при мочеиспускании. Так, цитомегалические клетки были выявлены, в соскобах шейки матки, цервикального канала, эндометрия, что свидетельствует о возможности ЦМВ вызывать эрозии шейки матки, цервициты, эндометриты. Гигантские ядерные включения обнаруживались и при исследовании кондилом [1,7]. Наиболее часто ЦМВИ органов малого таза возникает на фоне иммуносупрессии, выражающейся в дисбалансе регуляции иммунной системы, в том числе цитокиновой [3,4,5,7]. Способность вируса реплицироваться в клетках иммунной системы и индуцировать ее недостаточность является фоном для развития рецидивирующих бактериальных, грибковых и вирусных заболеваний.
Эффективное лечение цитомегалии сопряжено с определенными трудностями в выборе медикаментов. В арсенале врачей сегодня имеется несколько терапевтических средств - противовирусные препараты и человеческие иммуноглобулины [6,7]. До настоящего времени для лечения ЦМВИ наиболее широко использовались ацикловир и ганцикловир[2,6]. Высоким профилем безопасности обладает ацикловир, однако его действие на ЦМВ в 100 раз ниже, чем на ВПГ1/2 типа. Ганцикловир - характеризуется большей активностью против ЦМВ (в 50 раз), но выраженным токсическим эффектом [2,5]. В экспериментальных исследованиях доказано, что ганцикловир может угнетать сперматогенез и не исключается его канцерогенное воздействие на организм[9]. Во многих медицинских центрах мира проводиться пассивная иммунопрофилактика ЦМВИ с помощью иммуноглобулинов. При этом имеется достаточное количество работ, в которых дискутируется эффективность профилактического назначения иммуноглобулина у разных групп больных[2].
Все вышеперечисленное определяет необходимость поиска новых безопасных высокоэффективных препаратов обладающих противовирусным и иммуномодулирующим действием. Именно поэтому представляет интерес отечественный противовирусный препарат растительного происхождения Панавир, эффективный в отношении инфекций вызываемых разными ДНК- и РНК- содержащими вирусами (ЦМВ, ВПГ, ВПЧ). Руководствуясь инструкцией препарат может назначаться врачом при цитомегаловирусной инфекции, в том числе у пациенток с привычным невынашиванием беременности. Может применяться у женщин с хронической вирусной инфекцией и интерферонодефицитным состоянием на этапе подготовки к беременности. Характерными особенностями противовирусной активности Панавира является ингибирование синтеза вирусных белков, повышение жизнеспособности клеток, а так же индуцирование продукции IFN-a и IFN-y лейкоцитами.
Целью исследования явилось определение эффективности ректальных суппозиторий Панавир в лечении пациентов с ЦМВИ органов малого таза.
Материалы и методы
Под наблюдением находилось 30 больных с реактивацией ЦМВИ в органах малого таза, в возрасте от 20 до 40 лет. Диагностику ЦМВИ проводили при помощи исследования соскобов из уретры, вагины и цервикального канала с выявлением ДНК ЦМВ методом ампфликации нуклеиновых кислот ПЦР. Интерфероновый статус определяли в крови больных полученной из кубитальной вены. Забор материала для лабораторных исследований проводился до и через месяц после окончания лечения. Изучение эффективности, переносимости препарата проводилось на основании изучения: динамики показателей интерферонового статуса, отсутствия ДНК вируса цитомегалии в соскобах из урогенитального тракта после лечения и длительности ремиссии.
Панавир назначали, по 1 суппозиторию ректально на ночь. Процедура повторялась через день, 5 свечей на курс.
Результаты
При исследовании соскобов из урогенитального тракта при помощи ПЦР и ПЦР real time у всех больных выделены ДНК ЦМВ в клинически значимом титре, что свидетельствовало реактивации инфекции в нижних отделах органов малого таза.
При оценке показателей интерферонового статуса до лечения выявлены нарушения у всех 30 больных с цитомегаловирусной инфекцией органов малого таза.
Динамика показателей интерферонового статуса после терапии больных суппозиториями панавир
| Показатели (Ме/мл) | До лечения (п=30) | После лечения (п=30) | Контрольная группа |
| сывороточный IFN | 16,8±3,1* | 6 ±2,0** | 4,8 ±0,5 |
| Продукция FN-a | 24,2 ±2,6* | 67,6 ±4,6** | 89 ±1,5 |
| Продукция IFN-y | 12,4 ±2,7* | 27,3 ± 2,66** | 32,4 ±5,9 |
Частота выделения ДНК ЦМВ из эпителия урогенитального тракта после терапии больных суппозиториями панавир
| Срок лечения | Число больных | ЦМВ не выявлен | ЦМВ выявлен |
| До лечения | 30 | 0 | 30 |
| После лечения | 30 | 27 | 3 |
Через месяц после терапии суппозиториями панавир ДНК ЦМВ в соскобах из урогенитального тракта не обнаруживалась у 27 пациентов из 30.
При наблюдении за больными в период 60 дней после проведенного лечения ремиссия наблюдалась у 29 пациентов.
Выводы:
Литература
1. Прозоровский СВ., Тартаковский И.С. Возбудители оппортунистических инфекций - роль в инфекционной патологии человека и методы лабораторной диагностики. Клин. лаб. диаг. 1998; 2: 24, 33-5.
2. Чешек Н.И. Методическое пособие для врачей. Цитомегаловирусная инфекция. Эпидемиология, клиника, диагностика, лечение и профилактика. М, 2001, 3-5.
3. Белокрицкая Т.Е., Витковский Ю.А., Пономарева Ю.Н. Роль цитокинов в патогенезе нарушений иммунитета и гемостаза у больных с тяжелыми дисплазиями и раком шейки матки. Вопр. онкол. 2003; 49 (1): 51-4.
4. Краснопольский В. И., Радзинский В.Е., Буянова С.Н. Патология влагалища и шейки матки. М.: Медицина, 1997.
5. Козлова В.И., Пухнер А.Ф. Вирусные, хламидийные и микоплазменные заболевания гениталий. М., 1997; с. 536.
6.0shiro ВТ. Cytomegalovirus Infection in Pregnancy. In Protocols for Infectious Diseases in Obstetrics and Gynecology, 2nd ed. Mead PB, Hager WD, Faro S, eds.: BlackwellScience, 2000; 157-70.
7. Sweet RL, Gibbbs RS (eds.). Infectious Diseases of the Female Genital Tract, 3d ed.: Williams and Wilkins, 2005; 469-79.
Лечение цитомегаловирусной инфекции - препараты
Подход к лечению ЦМВ-инфекции существенно отличается у реципиентов после аллогенной трансплантации костного мозга (ТКМ) и у больных, подвергающихся химиотерапии (в том числе высокодозной после трансплантации аутологичных стволовых клеток). Больным первой группы необходимо упреждающее лечение, поскольку, несмотря на наличие препаратов, эффективно ингибирующих репликацию вируса, лечение уже развившихся висцеральных поражений эффективно не более чем в половине случаев.
Больным, получающим стандартную химиотерапию, специфическое лечение проводят только при установленном или высоковероятном висцеральном поражении.
Методы контроля ЦМВ-инфекции у реципиентов аллогенного костного мозга зависят от ЦМВ-статуса пары донор — реципиент. При серонегативности как донора, так и реципиента самым надежным способом профилактики ЦМВ-инфекции является использование для трансфузий препаратов крови от серонегативных доноров или лейкодеплеция с помощью фильтров последнего поколения, предназначенных для фильтрации в банках крови. При любом другом сочетании ЦМВ-статусов главные инструменты контроля — еженедельный мониторинг ЦМВ-виремии (методом ПЦР или выявлением антигенемии рр65) и упреждающее лечение ганцикловиром при позитивном результате.
Для начала терапии больных высокого риска (реципиенты неродственной или неполностью совместимой трансплантации, лечение РТПХ антитимоцитарным глобулином) достаточно однократного позитивного анализа. В то же время у больных низкого риска при невысокой вирусной нагрузке назначение специфической терапии можно отложить до повторного позитивного анализа, выполненного с интервалом 3— 5 дней. Этот подход проверен многими исследователями, в том числе нами. Доказано, что такой подход эффективнее и дешевле, чем профилактическое использование высоких доз иммуноглобулина и ацикловира, которое было популярно в конце 80-х — начале 90-х годов.

Ганцикловир (1,3-дигидрокси-пропоксиметил-гуанин) сам по себе не является активным противовирусным агентом, необходимо его фосфорилирование вирусной тимидинкиназой. В форме трифосфата ганцикловир ингибирует вирусную ДНК-полимеразу. Сродство ганцикловира к тимидинкиназам человека значительно меньше, поэтому его токсичность для человеческих клеток относительно невелика.
Доза ганцикловира для курса индукции составляет 10 мг/кг в сутки на два введения. Курс индукции продолжается 2—3 нед, после чего назначают поддерживающую дозу — 5 мг/кг в сутки на одно введение ежедневно или 5—6 раз в неделю. Длительность курса поддерживающей терапии определяют индивидуально. При упреждающем лечении реактивации ЦМВ после аллогенной ТКМ при достижении негативной реакции на антигене-мию или виремию поддерживающее лечение можно не проводить, в то время как при органном поражении (пневмония, ЦМВ-колит) лечение должно быть продолжено до купирования симптомов и негативизации результатов вирусологических исследований, а при ЦМВ-ретините терапия может быть пожизненной.
При длительном профилактическом или упреждающем применении ганцикловира в раннем посттрансплантационном периоде высока частота поздних ЦМВ-пневмоний. Таким пациентам необходимо продолжать мониторинг ЦМВ-виремии или антигенемии и после 100-го дня после трансплантации [11]. Примерно у 20 % больных, леченных ганцикловиром в указанной дозе, развивается гранулоцитопения менее 1000 в 1 м\ во всех случаях обратимая (быстрее под влиянием G-CSF), с медианой длительности 12 дней. Резистентность ЦМВ к ганцикловиру является редкостью.
Отличным от ганцикловира по механизму действия (прямое ингибирование ДНК-полимеразы) является натрия фосфоноформат (фоскарнет, фоскавир), который может быть эффективен при резистентности данного штамма вируса к ганцикловиру. Индукционная доза натрия фосфоноформата 90 мг/кг каждые 12 ч. Продолжительность курса лечения составляет 14 дней, затем проводят поддерживающую терапию в половинной дозе. Побочными реакциями являются нарушение функции почек, гипомагнезиемия, гипокальциемия и изъязвление слизистых оболочек наружных половых органов.
Необходимо отметить коммерчески доступный специфический антицитомегаловирусный иммуноглобулин. Убедительных доказательств его эффективности в лечении вызванных ЦМВ болезней нет. С учетом его дороговизны, а также наличия препаратов, оказывающих специфическое противовирусное действие, дальнейшее применение этого препарата вряд ли оправдано.
Редактор: Искандер Милевски. Дата обновления публикации: 18.3.2021
ЦМВИ у детей. Что делать если у ребенка обнаружили цитомегаловирусную инфекцию?
Цитомегаловирусная инфекция (ЦМВИ) во многом остается "темной лошадкой" для современных инфекционистов. Обладателям вируса-возбудителя в теории может быть кто угодно, но далеко не каждый об этом догадывается. Дело обстоит таким образом, во-первых, потому что довольно часто носительство бывает бессимптомным, во-вторых, в связи с тем что возможности передачи вируса весьма широкие. Возбудитель ЦМВИ попадает в организм через плаценту, вертикально (когда плод проходит через родовые пути), при грудном вскармливании с молоком, при переливании крови и в процессе полового контакта. В отношении детей большую роль играют первые три способа передачи вируса.
Цитомегаловирус в организме может вести себя по-разному, собственно, именно это во многом затрудняет его диагностику. Как уже говорилось выше, он может вообще никак себя не проявлять, но лишь при одном условии - прочной и хорошо функционирующей иммунной системе, которая активное размножение вируса в клетках организма может подавить. Однако в условиях иммунодефицита этот вирус становится по-настоящему опасен. Поэтому от него страдают помимо больных СПИДом и людей пожилого возраста еще и дети.
ЦМВИ выявляется особенно часто у детей до двух лет - это период становления иммунитета ребенка. Его иммунная система не в столько в дефиците, сколько супрессирована, то есть в некоторой степени подавлена, особенно на первых месяцах жизни. Таким образом природа защищает новорожденного от чрезмерно сильных реакций иммунитета на огромное множество чужеродных агентов. После года та защита, которую малыш получал с молоком матери, начинает исчезать, а свои противовирусные частицы вырабатываться в должной мере пока не могут. В связи с этим дети нередко страдают от ЦМВИ.

Проявления ЦМВИ достаточно широко варьируют, так как вирус способен проникать практически во все клетки организма и вызывать цитопатический эффект. Проще говоря, клетки меняются и утрачивают способность нормально функционировать. Что говорит о врожденной ЦМВИ, которую ребенок получил либо через плаценту еще в утробе, либо в процессе родов?
1. У таких детей имеется желтушность кожных покров и склер глаз. Печень значительно увеличена, так как цитомегаловирус имеет склонность поселяться сразу в клетки этого органа.
2. Из-за нарушения работы печени страдает и свертываемость крови, на основании этого дети с ЦМВИ страдают от повышенной кровоточивости (на коже появляются синячки, сыпь, плохо заживает пупочная ранка, кровь может появиться в стуле).
3. Также значительно увеличивается селезенка.
4. Помимо этого есть ряд других признаков: страдают легкие (вплоть до развития пневмонии), нарушена центральная нервная система (менингит, энцефалит, гидроцефалия характеризуются судорогами, повышенной возбудимостью). Изменено состояние органов ЖКТ, что характеризуется колитами, энтеритами, недостаточностью поджелудочной железы. Вирус не обходит стороной и почки, приводя к развитию нефрита.
К сожалению, выхаживать таких новорожденных чрезвычайно трудно, ведь на фоне такого "букета" к ослабленному организму присоединяются другие инфекционные заболевания. Поэтому тяжело текущие ЦМВИ часто заканчиваются гибелью новорожденного еще в первые недели его жизни, либо вовсе приводят к выкидышу, если женщина заразилась на ранних сроках беременности.
К счастью, такое тяжелое течение заболевания бывает далеко не у всех новорожденных (всего у 10 %), так что причина тяжести ЦМВИ в этом случае во многом остается загадкой. Те же дети, которые относительно легко переживают инфекцию, нередко впервые сталкиваются с ней через месяц-два после рождения. И в этом случае симптомы могут быть самыми разными. Обычно снижается слух или зрение, нарушается работа нервной системы, страдает физическое развитие. Вот с такими проблемами родители приходят к педиатру, и установить истинную причину - ЦМВИ удается не всегда.
Стоит помнить о и передаче вируса ребенку с материнским молоком. Когда инфицирование происходит таким путем, у ребенка часто возникает пневмония, которая лечению антибактериальными препаратами не поддается.

Дети старшего возраста и подростки с ЦМВИ сталкиваются еще реже в силу прочности их иммунной системы. Но если вирус все же активизировался, то проявляет он себя обычно снижением работоспособности, болью в суставах, лихорадкой и головными болями. Вывод таков, что по одним признакам установить наличие ЦМВ невозможно, всегда требуется лабораторное подтверждение. Оно заключается в поиске специфических антител, которые наш организм вырабатывает в ответ на наличие конкретных вирусных частиц. Есть специфические антитела - есть и вирус. Что же делать, если у ребенка обнаружили ЦМВИ?
1. Обнаружение ЦМВИ возможно еще в процессе беременности, посредством УЗИ, ведь вирус может приводить к формированию множественных видимых пороков у плода. Поскольку такие дети в будущем практически не жизнеспособны, беременность предлагается прервать.
2. В том случае, когда ЦМВИ выявляется у ребенка через некоторое время после рождения (не в первые дни), тактика врача будет зависеть от течения инфекционного процесса. Есть конкретные лекарственные средства, которые назначают для подавления ЦМВ - Ганцикловир, Фоскарнет. Однако принимать решение об их применении самостоятельно нельзя, так как эти лекарственные средства обладают рядом очень серьезных побочных эффектов. Они негативно сказываются на состоянии крови и токсичны для почек. В связи с этим их применяют только при острой необходимости, когда цитомегаловирус выходит из-под контроля. Новый препарат Цитотект, тоже подходит для лечения ЦМВИ, но вводится он также исключительно по назначению специалиста.
3. Нужно добиваться, чтобы признаки ЦМВИ не появлялись у ребенка. А для этого очень важно укреплять его иммунитет, который самостоятельно способен подавлять вирус и не давать ему негативно влиять на здоровье малыша. Есть множество природных иммуностимуляторов, которые разрешено давать детям (настойка эхинацеи, элеутерококка), Иммунал, Иммудон и другие средства, которые можно использовать курсами после консультации у педиатра с целью улучшения работы иммунной системы. Не последнюю роль играет питание. Не забывайте, что оно должно привносить в организм нужное количество белков, углеводов и жиров, микроэлементов, витаминов. Следите за тем, чтобы ребенок соблюдал режим, не переутомлялся, регулярно бывал на свежем воздухе и физически был активен.
- Вернуться в оглавление раздела "Микробиология"
Информация на сайте подлежит консультации лечащим врачом и не заменяет очной консультации с ним.
См. подробнее в пользовательском соглашении.
Читайте также:

