Грибково-вирусные инфекции в гинекологии
Обновлено: 19.04.2024
Среди половых заболеваний грибковые инфекции становятся все более распространенными. В настоящее время считаются основным этиологическим фактором таких патологий Candida albicans и другие виды рода Candida, реже встречаются плесневые грибы и Geotrichum.
Важную роль в распространении генитального микоза играют факторы окружающей среды:
- индустриализация;
- урбанизация;
- пренебрежение гигиеной;
- синтетическое белье;
- близкие контакты в бассейне, на пляжах и т.д.;
- сексуальные контакты с многочисленными партнерами.
Также влияние оказывают различные внешние факторы — антибиотики, стероиды, цитостатики и иммунодепрессанты, и внутренние — нарушение иммунных механизмов, генетическая предрасположенность, злокачественные опухоли, диабет, атопический диатез.
Развитие полового микоза зависит от количества клеток атакующего гриба и его вирулентности, то есть способности размножаться и прилипать к эпителию и продуцируемым протеолитическим ферментам, фосфолипазе и токсическим метаболитам. Также важна способность преодолевать сапрофитную бактериальную флору благодаря грибковым β-лактамным антибиотикам, которые являются производными фуцидиновой кислоты и стрептомицина.
Грибковые инфекции у женщин: грибковый вульвовагинит
В настоящее время считается что грибковый вульвовагинит является причиной воспаления этого органа в 40%. Патология относится к наиболее часто диагностируемым микозам от возраста новорожденного до поздней старости. Инфекция может затрагивать только влагалище, но в большинстве случаев протекает вместе с вульвитом.
У новорожденных болезнь начинается с перинатальной инфекции, поражающей половые органы и рот. В дальнейшие периоды развития ребенка, вплоть до полового созревания, болезнь имеет характер острого воспаления, реже хронического, а у девочек после 10–12 лет напоминает микоз у женщин. У детей наиболее распространенным возбудителем является Candida albicans.
У женщин грибковый вульвовагинит имеет следующие формы, связанные с различными патогенами. К ним относятся:
- пенициллез;
- аспергиллез;
- кандидоз;
- геотрихоз.
Пенициллез, аспергиллез и геотрихоз имеют меньшее клиническое значение, и поэтому их описание было опущено. Тем более что в клиническом течении этих инфекций имеется много схожих симптомов, и различить патологии можно только с помощью детального микологического исследования.
Поэтому в статье более подробно обсуждаются инфекции вульвы и влагалища, вызванные дрожжеподобными грибами (вульвовагинит Candida mycetica). С медицинской точки зрения, в настоящее время считаются патогенными по крайней мере 12 видов грибов Candida.

Вульвовагинит
Среди дрожжеподобных грибов, обнаруженных во влагалище, наиболее распространенным патогеном является C. albicans (около 70%). Другие виды также являются потенциальной причиной вульвовагинита: C. glabrata, C. krusei, C. kefyr (C. pseudotropicalis), C. parapsilosis, C. tropicalis, C. stelatoidea, C. guilliermondi, C. zeylanoides, C. famata, C. incospicua, C. lusitaniae, C. macedoninsis, C. rugosa, C. viswanathii.
Вульвовагинальный кандидоз часто встречается у беременных. Болезнь диагностируется примерно у 10% женщин в первом триместре и 23-55% во время третьего триместра беременности. Вульвовагинальные грибковые инфекции чаще встречаются (до 90%) у беременных женщин, которые были носителями C. albicans.
Также увеличивает риск развития вульвовагинального кандидоза диабет. Рецидивирующая генитальная молочница часто может быть первым важным симптомом этого заболевания. Вагинальные заболевания распространены у девочек с диабетом, и 2/3 из них имеют одинаковую бактериальную флору в области вульвы и заднего прохода.
У многих женщин генитальная молочница развивается при приеме антибиотиков, особенно обладающих широким спектром активности.
Развитию кандидоза способствует использование иммунодепрессантов, в основном, у людей с неэффективной иммунной системой. Прежде всего опасно нарушение клеточного иммунитета, которое касается как CD4, CD8, так и медиаторов их активности, то есть лимфокинов и интерлейкинов.
Большинство ученых в настоящее время указывают на повышенный риск развития вульвовагинального кандидоза у женщин, использующих гормональную контрацепцию.
Начало вульвовагинального кандидоза обычно бывает внезапным. Первые симптомы обычно появляются перед менструацией. Их интенсивность может варьироваться — от легкой до очень тяжелой формы. При острой инфекции возникают зуд, жжение и болезненность вульвы, особенно во время и после полового акта, а также жжение вокруг заднего прохода и болезненное мочеиспускание.
- отек и покраснение стенок влагалища с эпителиальными трещинами;
- пятна или папулы на поверхности слизистой оболочки вульвы, влагалища и влагалищного отдела шейки матки;
- диффузные или единичные эрозии в своде влагалища;
- папулезные гнойничковые воспаления ануса,
- изменение цвета кожи на половых губах, внутренних поверхностях бедер и промежности;
- густые белые или кремовые выделения, иногда прозрачные, водянистые выделения.
При хронических инфекциях вульвы и влагалища дрожжевые выделения из влагалища разной степени выраженности возникают периодически. Иногда возникает зуд и жжение вульвы или влагалища, особенно до или после менструации. Физикальное обследование указывает на наличие обильного, плотного, белого, гнойного или сыроподобного отделяемого.
Примерно у 30% женщин вульвовагинальный кандидоз может протекать бессимптомно, иногда единственным симптомом является слабый зуд, ощущаемый некоторыми пациентками перед менструацией.
Заболевание может быть спорадической инфекцией, оно также может быть рецидивирующим.
Осложнения кандидоза вульвы и влагалища:
- воспаление влагалищной части матки (cervitis Candida mycetica);
- проктит (proctitis Кандида mycetica);
- опрелости в промежности (опрелости Кандида mycetica perinei);
- кандидоз мочевыделительной системы;
- изменения и гиперплазия вульвы и шейки матки, напоминающие бородавки.
Дифференциальный диагноз в первую очередь касается бактериального воспаления — трихомониаза, гонореи и хламидийной инфекции, а также постменопаузального вагинита и выделений из влагалища, вызванных инородными телами, химическими раздражителями.
Диагноз кандидоз половых органов устанавливается на основании анализов (преимущественно микологических) и после исключения других причин вульвовагинита. Диагноз, основанный только на клинических признаках заболевания, неверен.
Микологическая диагностика состоит из изучения выделений в 10%-ном растворе гидроксида калия (KOH), окрашивания мазка с использованием метода Грама и PAS и на культуре (агаровая среда Сабуро, агаровая среда Никерсона-Манковского, рисовый агар, солод, кофейный агар, рисовый агар с добавлением твина 80), а также выполнение теста на миколин.
Лечение состоит из применения противогрибковых средств. Терапия может быть местной, общей или комбинированной — общей и местной.
Актуальные методы лечения включают применение противогрибковых препаратов в различных формах: таблетки, диски, тампоны, гель и кремы. Хорошие результаты дает натамицин (пимафуцин) 1 раз в сутки влагалищная свеч а и 100 мг в течение 3 или 6 дней. Более эффективны производные азола 1-го и 3-го поколения.

Противогрибковые свечи
Первое поколение включает в себя:
- клотримазол (1%, 2%, 5% вагинальный крем, вагинальные таблетки 100 мг, 200 мг, 300 мг, 500 мг);
- миконазол (вагинальный гель, шарики 100 мг, 200 мг, 400 мг и 1,2 нитрата миконазола);
- эконазол (1% крем, вагинальные шарики 50 мг и 150 мг);
- изоконазол (300 мг свечи);
- бутоконазол (2% вагинальный крем).
Представители третьего поколения:
- итраконазол (влагалищные шарики 80 мг);
- тирозол 3 (шарики по 80 мг),
- тирозол (0,4% и 0,8% влагалищный крем).
Продолжительность лечения производными азола варьируется от двухнедельного лечения до одного приема.
Общее лечение включает использование азольных производных второго и третьего поколений. Производным второго поколения является кетоконазол, вводимый в дозе 400 мг в течение 7-14 дней.
Производные третьего поколения — итраконазол и флуконазол. Итраконазол, доступный в настоящее время под названием Орунгал, рекомендуется в дозе 200 мг в течение 3 дней или 100 мг в течение 4-8 дней. Прием Орунгала 200 мг один раз в месяц в течение полугода защищает от рецидивов. Флуконазол (Дифлюкан) назначается в разовой дозе 150 мг.
Итраконазол и флуконазол не следует применять беременным и кормящим женщинам.
При комбинированном общем и местном лечении пероральные противогрибковые препараты вводят локально и одновременно принимают внутрь.
В случае рецидивирующей вульвовагиновой молочницы необходимо устранить предрасполагающие факторы. Некоторые специалисты рекомендуют одновременное лечение половых партнеров и пероральное применение антимикотиков у пациентов для предотвращения желудочно-кишечной реинфекции у пациентов.
Грибковые половые инфекции у мужчин: дрожжевая инфекция головки и крайней плоти (баланит, микотический баланопостит)
Генитальный микоз у мужчин обычно проявляется в виде воспаления головки (баланит) или воспаления головки и крайней плоти (баланопостит). Реже поражаются мочеиспускательный канал и верхние отделы мочевыводящих путей, предстательная железа, семенные пузырьки и придатки яичка.
Возбудителем заболевания чаще всего является дрожжеподобный гриб C. albicans , иногда C. tropicalis или другие виды рода Candida.

Дрожжеподобный гриб C. albicans
Грибы поражают в основном людей, страдающих ожирением, пожилых мужчин и людей с диабетом и фимозом. Предрасполагающими факторами являются:
- влажная среда внутри мешка крайней плоти;
- отсутствие личной гигиены;
- недостаточное высыхание головки и крайней плоти после мытья;
- дрожжевой вульвовагинит у половых партнеров.
Морфотическая картина изменений очень разнообразна, поэтому часто используется классификация, учитывающая множественность и различную степень изменений, а также различную интенсивность воспалительного процесса.
I Простая, неосложненная форма
- эритематозно-эрозивная разновидность (varietas erythematous — erosiva);
- эритематозно-эрозивная разновидность с белым налетом (varietas pseudo membranacea);
- гирлянда (varietas gyrata);
- герпетиформный вид (varietas herpetiformis).
- Подострая (subacuta): папулопустулярная (папулопустулезная).
- Хроническая: эритематозная эксфолиативный вид (erythematosquamosa).
II Сложная форма с одновременным поражением мочеиспускательного канала, верхних отделов мочевыводящих путей, предстательной железы, семенных пузырьков, придатка яичка, кожи половых органов и перигенитальной области.
Дрожжевые инфекции мужских мочеполовых органов обычно возникают в области головки и крайней плоти, гораздо реже при уретрите. Молочница уретры имеет признаки хронического или подострого вида. Симптомы заболевания включают в себя наличие в целом скудных, менее обильных, слизистых, белых и иногда желтых выделений, а также покраснение и отек наружной уретры.
Дифференциальный диагноз должен учитывать:
- неспецифическое воспаление головки;
- воспаление эпителиальных клеток;
- кольцевое эрозивное воспаление;
- псориаз;
- эритроплазию.
Диагноз может быть установлен только на основании микологического и микроскопического исследования.
Лечение должно основываться прежде всего на тщательных гигиенических процедурах с очисткой и сушкой области крайней плоти. Рекомендуются кремы , содержащие нистатин (100 000 МЕ в 1 г среды), амфотерицин В (фунгизон), натамицин (пимафуцин).

Лечение грибковых половых инфекций у мужчин
В рефрактерных случаях или при сложных формах с осложнениями следует начинать комбинированную терапию, как при дрожжевой инфекции вульвы и влагалища, с предпочтением в общей терапии производных азола третьего поколения и при длительном применении. Эффективен Итраконазол в дозе 100 мг в сутки в течение 4-6 дней до 12 недель.
При кандидозе уретры назначается местное лечение амфотерицином В в виде 1-процентной инстилляции в количестве 4-6 процедур.
Любые генитальные поражения воспалительного, острого или хронического характера всегда должны диагностироваться на наличие грибковой инфекции. Желательно, чтобы для установления правильного диагноза было проведено микологическое обследование. Обнаружение патогенного гриба позволит использовать правильную терапию и эффективное лечение заболевания.
Большое значение имеет определение предрасполагающих факторов и их устранение, особенно в случаях повторного течения. Также важны профилактические действия.
Что такое вагинальный кандидоз (молочница)? Причины возникновения, диагностику и методы лечения разберем в статье доктора Соснина А. С., гинеколога со стажем в 15 лет.
Над статьей доктора Соснина А. С. работали литературный редактор Вера Васина , научный редактор Сергей Федосов и шеф-редактор Лада Родчанина

Определение болезни. Причины заболевания
Вагинальный кандидоз (кандидозный вагинит) — поражение слизистой оболочки влагалища дрожжеподобными грибами рода Candida. В быту эту болезнь называют молочницей .
Краткое содержание статьи — в видео:
Candida — это условно-патогенные микроорганизмы, факультативные анаэробы (организмы, способные жить как в присутствии кислорода, так и без него). Они обладают тропизмом — направлением роста на клетки богатые гликогеном, в частности клетки слизистой оболочки влагалища. Самый распространённый вид возбудителя, который встречается в 70—90 % случаев, — Candida albicans.
В последние годы растёт заболеваемость кандидозом, вызванным другими представителями рода Candida. Наиболее часто выявляются:
- С. glabrata (15 %);
- C. dubliniensis (6 %);
- C. tropicalis (3—5 %);
- C. parapsilosis (3 %);
- C. krucei (1—3 %).
Распространение новых видов микроорганизмов связано в первую очередь с бесконтрольным самолечением пациенток, приводящем к возрастающей устойчивости грибов к препаратам [3] [4] .
Частота кандидозного вагинита среди инфекционных заболеваний влагалища и вульвы составляет 30—45 %. Патология занимает второе место среди всех инфекционных заболеваний влагалища и является крайне распространённым поводом для обращения женщин за медицинской помощью. По данным J. S. Bingham (1999):
- к 25 годам около 50 % женщин репродуктивного возраста сталкивались с хотя бы одним диагностированным врачом эпизодом вагинального кандидоза;
- к началу периода менопаузы — около 75 % [17] .
Кандидозный вагинит редко наблюдается в постменопаузе, за исключением тех пациенток, которые получают гормональную заместительную терапию.
Предрасполагающими факторами заболевания являются:
- Механические — ношение синтетического белья, первый половой контакт, травматическое повреждение тканей влагалища, длительное применение внутриматочной спирали.
- Физиологические — беременность, менструация.
- Эндокринные — гипотиреоз, сахарный диабет.
- Иммунодефицитные состояния.
- Ятрогенные (приём антибиотиков, кортикостероидов, иммуносупрессоров, лучевая терапия, химиотерапия, онкологические заболевания, оральные контрацептивы).
- Прочие (авитаминоз, аллергические заболевания, хронические патологии гениталий и желудочно-кишечного тракта).
Заболевание, как правило, не передаётся половым путём, но установлено, что оно связано с характером половых контактов: анально-вагинальным и орогенитальным. Также не исключается вероятность развития кандидозного баланопостита у половых партнёров пациенток с вагинальным кандидозом.
При обнаружении схожих симптомов проконсультируйтесь у врача. Не занимайтесь самолечением - это опасно для вашего здоровья!
Симптомы вагинального кандидоза
Основные симптомы при вагинальном кандидозе:
- жжение и зуд в области влагалища и вульвы;
- творожистые выделения из влагалища;
- расстройства мочеиспускания;
- боль при половом акте.
Зуд может усиливаться после водных процедур, полового акта, ночью во время сна и в период менструации [1] .
В целом симптомы вагинального кандидоза нарастают перед менструацией. При беременности проявление болезни также усугубляется, это связано со снижением иммунитета у беременных женщин.
Объективные признаки вагинального кандидоза:
- отёк и гипермия слизистой оболочки влагалища и наружных половых органов;
- белые или зеленовато-белые наложения на стенках влагалища;
- покраснение слизистой влагалища.
При осложнённом кандидозе на коже наружных половых органов появляются везикулы — пузырьки, возвышающиеся над уровнем кожи или слизистой и заполненные прозрачным или мутным содержимым, которые могут вскрываться и образовывать эрозии. При вагинальном кандидозе также могут наблюдаться трещины слизистой вульвы, задней спайки и перианальной области [2] .
Патогенез вагинального кандидоза
Грибы рода Candida относятся к условно-патогенной микрофлоре, которая присутствует как в окружающей среде, так и на поверхности кожных покровов и слизистых оболочках здорового человека (в полости рта, кишечнике, влагалище). При снижении защитных сил организма возможно повышение адгезивных свойств (способности прилипать) грибов с прикреплением их к клеткам эпителия влагалища, колонизацией слизистой оболочки и развитием воспалительной реакции [7] .
Вагинальный кандидоз зачастую затрагивает только поверхностные слои эпителия влагалища без проникновения возбудителя в более глубокие слои слизистой оболочки. Однако в редких случаях эпителиальный барьер преодолевается и происходит инвазия в подлежащую ткань с последующей гематогенной диссеминацией (распространением возбудителя инфекции из первичного очага заболевания по всему органу или организму посредством кровотока) [8] [9] .
Основные этапы патогенеза:
- Адгезия (прилипание) грибов на слизистой и колонизация.
- Инвазия (проникновение) в эпителий.
- Преодоление эпителиального барьера.
- Проникновение в соединительную ткань.
- Преодоление защитных механизмов ткани.
- Попадание в сосуды.
- Гематогенная диссеминация.
При вагинальном кандидозе воспаление происходит в верхних слоях эпителия влагалища. Причина состоит в том, что поддерживается динамическое равновесие между грибом, который не может проникнуть в более глубокие слои, и организмом, который сдерживает его распространение. Соответственно инфекция может долго развиваться в одном месте, проявляясь творожистыми выделениями из влагалища. Обострение заболевания происходит при сдвиге равновесия между развитием грибов и защитными силами организма.
Классификация и стадии развития вагинального кандидоза
Согласно национальным клиническим рекомендациям [18] , выделяют две формы вагинального кандидоза:
- острую — до трёх обострений в год;
- хроническую (рецидивирующую) — не менее четырёх обострений в год.
По классификации, предложенной D.A. Eschenbach, вагинальный кандидоз подразделяют на два типа:
У женщин различают три формы заболевания:
- вагинит (воспаление влагалища); (воспаление влагалища и вульвы); (воспаление шейки матки).
У мужчин выделяют:
- баланит (воспаление головки полового члена);
- баланопостит (воспаление крайней плоти и головки полового члена); (воспаление мочеиспускательного канала).
Для острой формы вагинального кандидоза характерны выраженные симптомы: обильные выделения из влагалища, жжение и зуд во влагалище и наружных половых органах. На фоне таких симптомов нередко снижается трудоспособность пациентки и развиваются неврозы. Острая форма вагинального кандидоза встречается наиболее часто и формируется в результате увеличения количества грибов рода Candida во влагалище на фоне снижения иммунитета пациентки.
Рецидивирующий вагинальный кандидоз — встречается у 10—15 % женщин репродуктивного возраста и проявляется четырьмя и более обострениями за год [11] .
Неосложнённая форма заболевания предполагает впервые выявленный или возникающий менее четырёх раз в год вагинальный кандидоз с умеренными проявлениями вагинита у пациенток без сопутствующих факторов риска (сахарный диабет, приём глюкокортикоидов, цитостатиков и др.).
При осложнённом вагинальном кандидозе наблюдаются яркие объективные симптомы: покраснение, отёк, образование язв, трещин слизистых оболочек и кожи перианальной области. Также характерны рецидивы четыре и более раз в год. Заболевание часто возникает на фоне сахарного диабета, ВИЧ-инфекции, терапии глюкокортикоидами и цитостатиками. Возбудителем заболевания в данном случае являются как C. albicans, так и другие грибы рода Candida.
Осложнения вагинального кандидоза
К осложнениям вагинального кандидоза у женщин относятся:
- стеноз влагалища;
- воспалительные патологии органов малого таза — сальпингит, оофорит и другие;
- заболевания мочевыделительной системы — цистит, уретрит[2] .
Стеноз влагалища развивается при воспалении стенок влагалища. При этом просвет влагалища сужается, а стенки влагалища становятся плохо растяжимы. Пациентки испытывают боль при половом акте.
Сальпингит — инфекционно-воспалительное заболевание фаллопиевой (маточной) трубы. Возникает при переходе инфекции восходящим путем из влагалища, не исключен также и гематогенный путь передачи. Сальпингит чаще всего протекает в сочетании с оофоритом — воспалением яичника. Поражение может быть как односторонним, так и двусторонним. Пациентки испытывают боль в области придатков, внизу живота слева или справа, повышается температура тела, возникает общее недомогание, слабость, а иногда и тошнота со рвотой. При несвоевременном лечении данного осложнения высок риск бесплодия, наступления внематочной беременности, возникновения спаечного процесса, приводящего к оперативному вмешательству, инфицированию органов брюшины и малого таза. Сальпингит особенно опасен в случаях, когда с кандидозом сочетаются другие инфекции [1] .
Уретрит — воспаление слизистой мочеиспускательного канала. Проявляется болезненным мочеиспусканием, чувством жжения в области уретры, выделением с мочой крови или гноя, дискомфортом при соприкосновении с бельём, слипанием краёв уретры, покраснением области вокруг мочеиспускательного канала.
Цистит — воспаление мочевого пузыря. Патология возникает при попадании возбудителя восходящим путём через уретру в мочевой пузырь. Симптомы цистита схожи с симптомами уретрита, однако есть некоторые отличия: частые позывы к мочеиспусканию при небольшом количестве мочи, чувство неполного опорожнения мочевого пузыря, боль, резь в конце мочеиспускания, помутнение мочи, повышение температуры тела, боли внизу живота.
На фоне вагинального кандидоза возрастает частота осложнений при беременности, а также увеличивается риск инфицирования плода.
Кандидоз плода может вызвать его внутриутробную гибель или приводить к преждевременным родам. После родов у женщин возможно развитие кандидозного эндометрита — воспалительного процесса в тканях, выстилающих внутреннюю полость матки.
Диагностика вагинального кандидоза
Диагностика вагинального кандидоза основывается на характерных жалобах пациентки, данных анамнеза, клинических проявлениях, выявленных при гинекологическом осмотре. В зеркалах видна гиперемия, отёк слизистой, белые налёты на стенках влагалища.
Независимо от этих признаков, подтверждение диагноза должно основываться на лабораторных данных:
- Микроскопия мазков вагинального отделяемого — позволяет выявить споры и мицелий гриба.
- Культуральный метод — посев влагалищного содержимого на искусственные питательные среды. Метод определяет количество, видовую принадлежность, чувствительность к противогрибковым препаратам, а также характер и степень заселения другими микроорганизмами. Культуральный метод дополняет микроскопию.
- Серологическая диагностика (РСК). Определяет антитела против антигенов грибов рода Candida. Такая диагностика имеет значение при генерализации процесса.
- Молекулярно-биологические методы. Направлены на обнаружение специфических фрагментов ДНК Candida spp. Применяют метод полимеразной цепной реакции (ПЦР).
- Иммунофлюоресцентная диагностика (Candida Sure Test) проводится в случае рецидивирующего течения вагинального кандидоза [15] .
К дополнительным методам диагностики относятся: изучение микробиоценоза кишечника, обследование на инфекции, передаваемые половым путём, внутривенный тест на толерантность к глюкозе [16] .
Дифференциальную диагностику проводят со следующими заболеваниями:
- генитальным герпесом; ;
- аэробным вагинитом;
- кожными заболеваниями (экземой, красным плоским лишаём, склеродермией, болезнью Бехчета и др.).
Лечение вагинального кандидоза
Показаниями к назначению терапии вагинального кандидоза являются жалобы пациентки, клинические проявления и лабораторное подтверждение наличия грибов рода Candida. Лечение не требуется при обнаружении грибов без каких-либо клинических проявлений (кандидозоносительство). Это правило обусловлено тем, что грибы рода Candida могут содержаться в небольшом количестве во влагалище и являются частью нормальной микрофлоры, если их количество не превышает пороговое значение 10 4 .
Механизм действия противогрибковых препаратов — нарушение синтеза эргостерола (вещества в составе клеточных мембран грибов), что приводит к образованию дефектов в мембране микроорганизма. В зависимости от дозы антимикотики проявляют фунгистатическое (замедление роста) или фунгицидное (полное уничтожение) действие [15] .
Существуют различные группы препаратов для лечения вагинального кандидоза:
- антибиотики (пимафуцин, амфотерицин В, нистатин, леворин);
- имидазолы (клотримазол, сертаконазол, кетоконазол, гино-певарил, миконазол);
- триазолы (итраконазол, флуконазол);
- комбинированные препараты ("Тержинан", "Полижинакс", "Пимафукорт", "Клион Д", "Макмирор комплекс");
- препараты разных групп (флуцитозин, гризеофульвин, дафнеджин, нитрофунгин, йодат поливинилпирролидон).
Лечение подбирается гинекологом индивидуально для каждой пациентки, учитывая клиническую картину, форму заболевания и степень выраженности симптомов. Но важно отметить, что при лечении молочницы при беременности флуконазол противопоказан, так как он может негативно повлиять на развитие плода [19] [20] .
При лечении острых форм вагинального кандидоза назначают местное лечение. Препарат не всасывается в системный кровоток, а действует в области влагалища и слизистой. Примеры схем лечения:
-
150 мг в виде вагинальных свечей один раз в сутки в течение трёх дней; один аппликатор крема на ночь вагинально в течение трёх дней; одна свеча на ночь один раз в сутки в течение восьми дней; одна таблетка на ночь в течение 10 дней.
При хроническом кандидозе наряду с местным лечением применяют системные антимикотики:
-
150 мг один раз внутрь; 200 мг внутрь два раза с интервалом 12 часов в течение одного дня или 200 мг в сутки в течение трёх дней.
При рецидивирующей форме заболевания (более четырёх эпизодов в год) применяют схему:
-
150 мг внутрь три раза с интервалом 72 часа в 1,4 и 7 день лечения.
Для купирования рецидивов препарат применяют в дозировке 150 мг один раз в неделю в течение шести месяцев.
В последние годы всё больше исследуется способность C. albicans формировать биоплёнки — вещества на поверхности колонии микроорганизмов, которые служат барьером для проникновения лекарственных средств и обеспечивают выживание. Основным полисахаридом, определяющим развитие резистентности к антибиотикам, является глюкан. Его рассматривают как одну из причин формирования резистентности к антимикотическим препаратам. Этим объясняется отсутствие эффекта при лечении у некоторых больных. Таким пациенткам можно порекомендовать препарат фентиконазол 600 мг в сутки с интервалом в три дня. Лекарство отличается от других способностью преодолевать биоплёнки, тем самым повышая эффективность лечения при резистентности к другим препаратам.
Прогноз. Профилактика
При своевременном обращении пациентки к врачу, лабораторном обследовании и отсутствии самолечения прогноз благоприятный. Самолечение опасно из-за риска рецидива заболевания, его хронизации и возникновения резистентности к препарату, неверно выбранному пациенткой или при неадекватной дозе.
Чтобы повысить эффективность терапии пациентки должны следовать схеме лечения, индивидуально назначенной гинекологом. Во время лечения и диспансерного наблюдения необходимо соблюдать половой покой или применять барьерные методы контрацепции. Повторно обратиться к врачу для контроля анализов следует через 7-10 дней [12] .
Что такое цервицит? Причины возникновения, диагностику и методы лечения разберем в статье доктора Батаршиной О. И., гинеколога со стажем в 18 лет.
Над статьей доктора Батаршиной О. И. работали литературный редактор Маргарита Тихонова , научный редактор Сергей Федосов и шеф-редактор Лада Родчанина

Определение болезни. Причины заболевания
Цервицит — это воспалительное заболевание шейки матки, которое развивается под влиянием различных агентов (как инфекционных, так и неинфекционных) [2] .
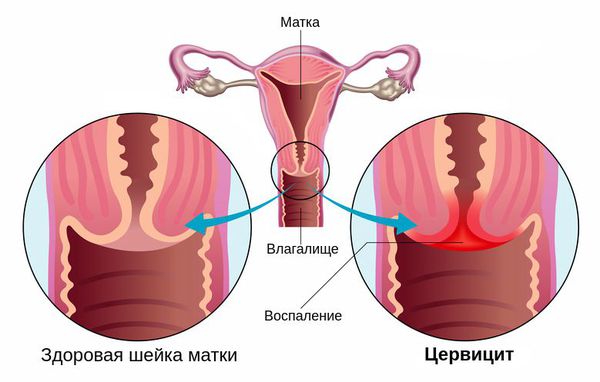
Распространённость цервицита у женщин достигает 10-45 %. Наиболее часто его вызывают возбудители, передаваемые половым путём, такие как гонокок, хламидия, трихомонада, вирус герпеса, бледная трепонема и др. [7] [8] [11] . Также причиной возникновения цервицита являются различные заболевания, аллергические реакции на противозачаточные спермициды, латекс в составе презервативов или продукты женской гигиены, такие как мыла, гели для душа или дезодоранты.
Длительный и вялотекущий дисбиоз влагалища (бактериальный вагиноз) также рассматривается как одна из возможных причин цервицита, поскольку на фоне изменения уровня кислотности влагалища меняется и соотношение видов влагалищной микрофлоры.
В зоне риска по возникновению цервицита находятся женщины, которые:
Также доказано, что фоном для развития воспаления шейки матки и его хронизации является местный иммунодефицит, связанный с нарушением защитной функции слизистой оболочки.
При обнаружении схожих симптомов проконсультируйтесь у врача. Не занимайтесь самолечением - это опасно для вашего здоровья!
Симптомы цервицита
Возможно как симптомное, так и бессимптомное течение заболевания [31] .
При бессимптомном процессе диагноз "цервицит" может быть поставлен:
- при неудовлетворительных результатах мазков — повышенном уровне лейкоцитов (клеток крови, отвечающих за иммунный ответ на внедрение инфекционных агентов);
- на основан ии визуального осмотра шейки матки врачом-гинекологом — покраснения и отёка шейки матки.
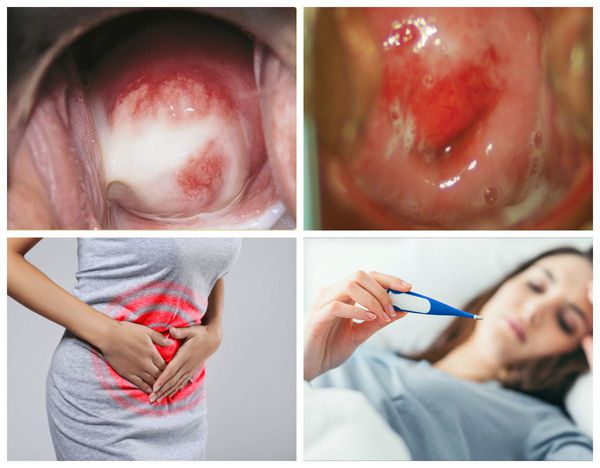
При симптомном течении заболевания женщину могут беспокоить:
- сероватые или бледно-жёлтые выделения из влагалища;
- аномальные кровянистые выделения во время или после полового контакта, а также в перерывах между менструациями [31] ;
- боль во время секса;
- затруднённое, болезненное или частое мочеиспускание;
- тазовая боль или, в редких случаях, лихорадка.
Патогенез цервицита
Когда речь идет о патогенезе цервицита, прежде всего необходимо обозначить понятия, о которых пойдёт речь.
Шейка матки представляет собой гладкомышечный орган длиной 2-3 см, образованный соединительной тканью. Основная функция данной части матки — барьерная. Она реализуется за счёт секрета (выделений) слизистой , которая препятствует попаданию патогенных возбудителей в матку, маточные трубы и малый таз. В состав секрета входят как иммуноглобулины всех классов ( IgG, IgM, IgA и др. ), так и вещества, обладающие высокой расщепляющей и бактерицидной активностью.
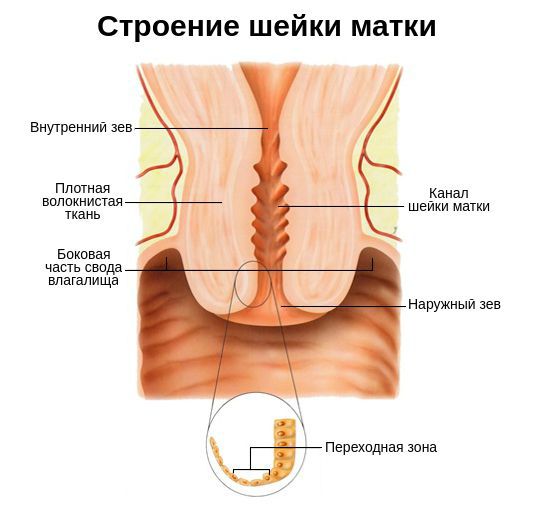
Также шейку матки защищает микрофлора влагалища . Она состоит из анаэробных и аэробных бактерий, причём первых в десять раз больше, чем вторых. Такое соотношение создаёт определённый уровень кислотности слизистой, который не позволяет патогенным микроорганизмам внедряться в полость матки [8] .
Циклическое воздействие половых гормонов на женский организм позволяет сохранять микрофлору влагалища в норме, тем самым защищать шейку матки:
- в первой фазе менструального цикла под воздействием эстрогенов синтезируется гликоген, стимулируется выработка слизистого секрета, выполняющего барьерную функцию [4][17][27] ;
- во второй фазе цикла под воздействием прогестерона происходит подкисление среды влагалища и размножение лактобактерий.
При снижении барьерных свойств микрофлоры влагалища и слизистой шейки матки в организм женщины проникают различные патогенные возбудители, которые приводят к развитию цервицита. Их активному проникновению и распространению в полости малого таза способствуют сперматозоиды в качестве клеток-переносчиков инфекционных агентов, а также трихомонады и установка внутриматочной спирали на фоне воспалительного процесса.
Острый цервицит
Чаще возникает при поражении шейки матки специфическими возбудителями (например, гонококком), а также после искусственного прерывания беременности, в осложнённом послеродовом периоде (возбудителями чаще становятся стафилококковая и стрептококковая инфекции) и при вирусном поражении шейки матки. На ранней стадии заболевания возникают:
- полнокровие сосудов;
- повышение уровня лейкоцитов (лейкоцитарная инфильтрация);
- просачивание крови сквозь стенки сосудов в зону воспаления (экссудация);
- дистрофические изменения с вакуолизацией цитоплазмы и ядер клеток.
В результате дистрофических изменений клеток на поверхности слизистой оболочки шейки матки появляется гнойный и серозно-гнойный экссудат — сероватые или бледно-жёлтые выделения.
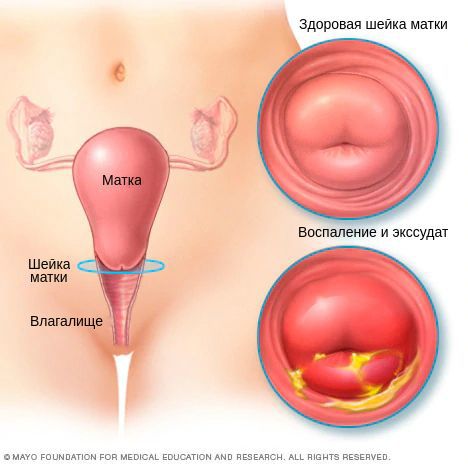
Хронический цервицит
При проникновении возбудителей в межклеточное пространство крипт шейки матки (небольших трубчатых углублений), труднодоступных для лечения, возникает хронический цервицит. Причиной хронизации заболевания нередко является поражение шейки матки хламидийной инфекцией. В 24-40 % случаев хронический цервицит возникает на фоне длительного и вялотекущего бактериального вагиноза. При осмотре гинекологом шейка матки выглядит покрасневшей, отёчной, легко травмируется. Микроскопически наблюдается инфильтрация подэпителиальной ткани лимфоцитами, плазмоцитами, полнокровие сосудов. Наряду с дистрофическими процессами в ткани преобладают процессы непрямого деления клеток, разрастания ткани и замещения одного вида клеток другим. Часто при хроническом цервиците нарушаются процессы ороговения клеток, что проявляется уплотнением тканей и изменением процесса гликогенизации клеток [6] [11] .
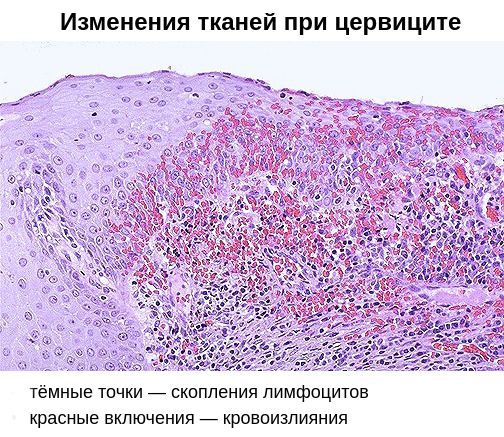
Помимо специфического возбудителя, немалую роль в возникновении хронического цервицита играет вторичный иммунодефицит. Он заключается в неполноценности клеточного и гуморального иммунитета. На клеточном уровне снижается количество Т- и В-лимфоцитов, а также нарушается фагоцитарная активности клеток, позволяющая им поглощать и переваривать патогенные микроорганизмы. В результате возбудители остаются в организме, снижается содержание антител IgG и IgM, увеличивается выработка антител IgA, что ведёт к изменению качества цервикальной слизи.
Послеродовой цервицит
Отдельно такую форму не выделяют, цервицит после родов ничем не отличается от обычного. Разница может быть лишь в лечении: не все антибиотики можно принимать при грудном вскармливании.
Классификация и стадии развития цервицита
Классификация цервицита зависит от типа возбудителей, локализации и давности патологических процессов. Так, в зависимости от типа возбудителя цервициты подразделяют на инфекционные и неинфекционные. Инфекционные цервициты бывают:
- гонококковыми;
- хламидийными;
- трихомонадными;
- кандидозными;
- вирусными.
Неинфекционные цервициты рассматриваются и классифицируется в зависимости от причины, вызвавшей воспаление. Они бывают аллергическими, атрофическими (сенильными) и др. [8] .
Кроме того, по локализации цервицит подразделяют на:
- экзоцервицит — протекает преимущественно на поверхности шейки матки;
- эндоцервицит — в основном затрагивает эпителий канала шейки матки (цервикальный канал).
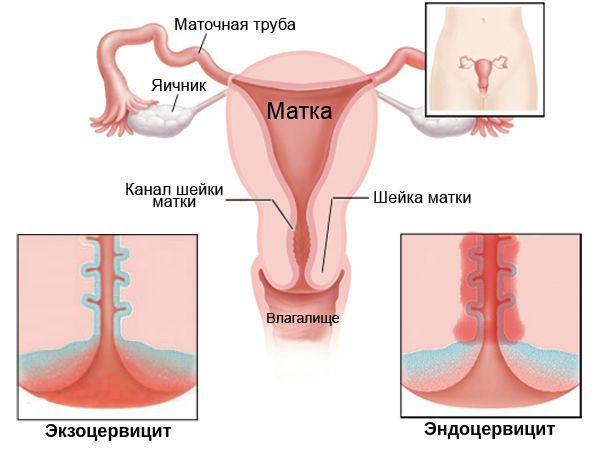
По длительности протекания процесса цервицит может быть:
- острым — процесс воспаления длится не более шести недель;
- хроническим — болезнь протекает с периодическими ремиссиями и обострениями.
Осложнения цервицита
Выявление причины цервицита имеет важное значение, поскольку при наличии инфекционного агента возбудитель способен распространяться за пределы шейк и матки и вызывать эндометрит , а также воспаление в теле матки, маточных трубах и малом тазе. В ряде случаев это приводит к бесплодию или препятствует вынашиванию плода [25] [27] .
Цервицит и беременность
Если беременность возникла на фоне цервицита, возбудитель заболевания может привести к преждевременному прерыванию беременности в связи с проникновением инфекции в водную оболочку, обращённую к плоду, затем в хорион (плаценту), околоплодные воды и сам плод.
При инфицировании ребёнка на ранних сроках беременности могут сформироваться врождённые пороки развития, возникает риск первичной плацентарной недостаточности и внутриутробной гибели плода. При позднем инфицировании наблюдаются следующие осложнения беременности:
- внутриутробная задержка развития плода;
- вторичная плацентарная недостаточность (часто на фоне плацентита — воспаления плаценты);
- локальные и генерализованные (распространённые) инфекционные поражения плода.
Генерализованные формы внутриутробной инфекции чаще развиваются в первом триместре беременности, так как плод ещё не может препятствовать распространению воспалительного процесса. В третьем триместре воспалительные изменения вызывают сужение или обтурацию (закрытие просвета) каналов и отверстий, что ведёт к аномальному развитию уже сформировавшегося органа — псевдоуродствам ( гидроцефалии , гидронефрозу и др.) [29] .
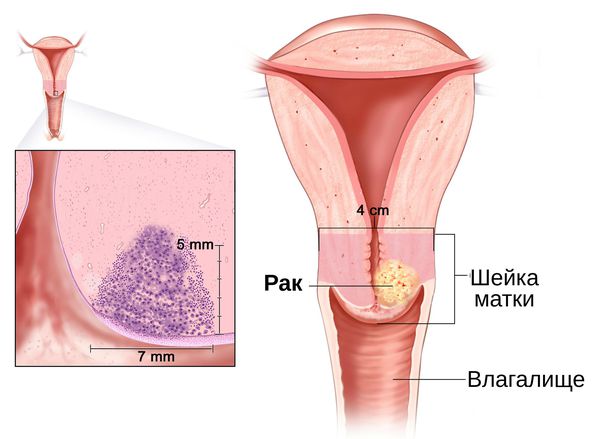
Длительное воспаление шейки матки становится фоном для развития злокачественных процессов . Это связано с нарушением регенерации слизистой оболочки шейки матки, которое наблюдается при хроническом цервиците. Наиболее значимыми факторами, влияющими на регенерацию, являются вирусы и хламидии [10] . Учёные доказали, что формирование рака шейки матки происходит только на фоне сохранившейся в криптах вирусной инфекции, которая активируется более чем через год после первичного обнаружения возбудителя [30] .
Диагностика цервицита
Диагностическими критериями цервицита при осмотре в зеркалах являются:
- покраснение слизистой, отёк;
- обильные выделения грязно-серого или зеленоватого цвета;
- творожистое отделяемое (при грибковом поражении шейки матки и влагалища).
При микроскопическом исследовании наблюдается увеличение количества лейкоцитов, также можно обнаружить возбудителей трихомониаза и гонореи.
Однозначными признаками цервицита при вульвоцервикоскопии служат:
- фолликулярный кольпит, "лунный ландшафт" — для хламидиоза;
- очаговый кольпит — для трихомониаза;
- диффузный кольпит — для неспецифической бактериальной инфекции;
- симптом "манной крупы" — для герпетической инфекции [17] .
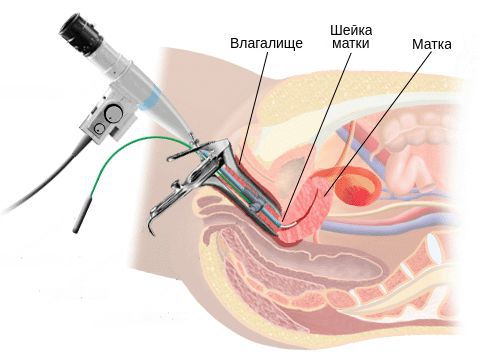
Бактериологическое исследование с поверхности шейки матки и заднего свода влагалища позволяет оценить не только соотношение лактофлоры, создающей нормальную кислотность влагалища, но и выявить рост условно-патогенных возбудител ей, таких как кишечные палочки, стрептококки, стафилококки, анаэробные кокки и др. Причём клинически значимым является рост микроорганизмов в колич естве более чем 10 4 КОЕ/мл.
ПЦР-диагностика позволяет обнаружить специфических возбудителей, вызвавших воспалительный процесс, таких как микоплаз мы, уреаплазмы, гарднереллы, хламидии, вирус герпеса и др. [31] . Для этого исследования врач-гинеколог должен взять мазок из шейки матки.
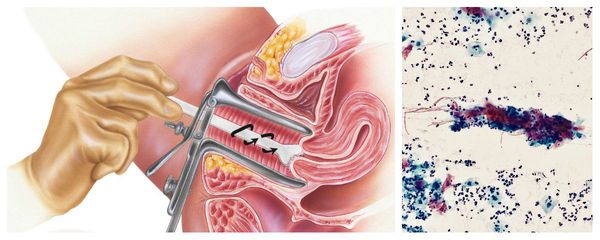
Цитологическое исследование клеточного материала позволяет оценить структуру клеток, характер и уровень их повреждения, а также эффективность лечения в динамике. При длительно текущем воспалении шейки матки в цитограмме преобладают гистиоциты, плазмациты, фибробласты и лимфоидные элементы. При продуктивном воспалении (защитной реакции организма) преобладают клеточные инфильтраты — макрофагальные, г игантоклеточные, плазмоклеточные, лимфоцитарно-моноцитарные. В 40 % случаев цитологическая диагностика позволяет выявить возбудителя заболевания (хламидии, кандиды, трихомонады, цитомегаловирус), более чем в 50 % случаев диагностируется папилломавирус и вирус простого герпеса.
При ультразвуковом исследовании признаками эндоцервицита являются увеличение толщины М-эхо шейки матки более 4 мм и реактивный отёк подэпителиальных о тделов УЗИ. рекомендуется выполнять на 5-7 день менструального цикла.
Следует помнить, что обследование гинекологом и взятие мазков проводятся перед началом менструации или через несколько дней после её окончания: оптимальный срок — пятый день, когда нет мажущих кровянистых выделений. Накануне и в день процедуры не следует использовать вагинальные свечи, тампоны, мази, средства интимной гигиены, поскольку это может стать причиной получения недостоверных данных. Кроме того, необходимо отказаться от спринцевания и воздержаться от половых контактов в течение одного-двух дней до сдачи анализа.
Лечение цервицита
Препараты для лечения цервицита
Определяющим звеном при выборе тактики лечения является природа возбудителя цервицита: вирусные воспаления шейки матки предполагают использование противовирусных препаратов, бактериальные воспаления — приём антибактериальных средств. При этом важно учитывать чувствительность выявленных инфекционных агентов к антибиотикам [1] [2] [3] .
Главной проблемой лечения цервицита шейки матки являются наличие нескольких возбудителей (микст-инфекции) и устойчивость возбудителей к антибактериальным препаратам. В таких случаях необходимо прибегнуть к приёму комбинации антибиотиков. Конкретные препараты назначает врач.
Иногда антибиотикотерапия сопровождается назначением фитопрепаратов, биологически активных добавок. Также рекомендуются общеукрепляющие физические нагрузки, нормализация режима труда и отдыха [9] [24] .
Помимо лечения пациентки параллельно в обязательном порядке проводится лечение её полового партнёра. Во время терапии необходимо пользоваться барьерной контрацепцией.
Нормали зация микробиоценоза влагалища с помощью пробиотиков [15] в сочетании с иммунокоррекцией (с учётом данных иммунограммы) [5] [16] [19] также целесообразны, поскольку изменённый уровень кислотности среды и возникающий дефицит иммунных факторов способствуют частым рецидивам воспалительного процесса [40] [43] [44] .
Физиотерапия
Кроме того, в ряде случаев назначается физиолечение:
- ДМВ-терапия — лечение дециметровыми волнами частотой от 300 МГц до 3 ГГц, проводится каждый день, предполагает 10-15 процедур продолжительностью 10 минут;
- магнитотерапия — воздействие магнитного поля низкой или высокой частоты, проводится каждый день, предполагает 10-20 процедур продолжительностью 10-20 минут;
- диадинамотерапия — лечение высокочастотным электрическим током, проводится каждый день до появления ощущения болезненной вибрации, предполагает 12-15 процедур;
- СМТ-терапия — лечение низкочастотным электрическим током, проводится каждый день, предполагает 12-15 процедур;
- электрофорез с солями магния — воздействует на область малого таза, проводится каждый день, предполагает 10-15 процедур продолжительностью 20 минут;
- дарсонвализация и лазеротерапия с использованием влагалищных датчиков — проводятся каждый день, предполагает 10-12 процедур [32] .
Деструктивные методы лечения цервицита
Цервицит — это воспалительный процесс, поэтому его лечат медикаментозно. Физические или химические методы применяются при атипии в клетках, покрывающих шейку матки или выстилающих цервикальный канал. Прижигание кислотами, жидким азотом, лазерная вапоризация, аргоноплазменная абляция, электрохирургическая эксцизия для лечения цервицита не используются .
Прогноз. Профилактика
Прогноз заболевания при своевременно начатом лечении благоприятный. При бессимптомном цервиците и отсутствии инфекций, передаваемых половым путём, у пациенток остаётся риск появления выраженных клинических признаков заболевания [30] .
Помимо основного лечения назначаются консультации других специалистов для коррекции различных нарушений (нейроэндокринных, гормональных, иммунных), выявления соматических заболеваний и факторов риска. Это позволит предотвратить повторное развитие цервицита [28] .
С целью профилактики воспаления шейки матки рекомендуется:
- один раз в шесть месяцев посещать гинеколога;
- использовать барьерные средства контрацепции;
- не допускать хронизации заболеваний мочеполовой системы.
Клиника.
1. Первичный генитальный герпес у лиц, не имевших контакта с ВПГ, характеризуется генитальными и экстра генитальными поражениями. Чаще всего процесс протекает на больших и малых половых губах, слизистой влагалища и шейки матки, в области балано-препуционной бороздки, крайней плоти, слизистой головки полового члена и мочеиспускательного канала. После скрытого периода, длящегося от 1 до 5 дней, появляются боль, зуд в местах поражения, выделения. У 60% больных наблюдается повышение температуры, головные и мышечные боли, в 23% случаев - увеличение паховых и бедренных лимфоузлов. На пораженных участках возникают мелкие, 1-3 мм в диаметре серозные пузырьки, сидящие на гиперемированном основании. Вначале прозрачное, содержимое пузырьков становится мутным, гноевидным. Вскрываются пузырьки с образованием ярко-красной эрозии, покрываясь тонкой корочкой, которая по мере эпителизации отпадает. Заживление происходит без рубцов, но остается временная гиперемия или пигментация. Средняя продолжительность местных проявлений 10-12 дней.
Поражение мочеиспускательного канала начинается внезапно с выделения слизи в виде "утренней капли", почти бесцветной. Больные жалуются на расстройство мочеиспускания, боли, чувство жара, иногда зуда или жжения в области наружных гениталий. Через 1-2 недели симптомы исчезают, но у большинства больных возникают рецидивы болезни с интервалами от нескольких недель до нескольких лет.
2. Вторичный генитальный герпес протекает легче, и выздоровление наступает быстрее. Высыпанных элементов мало. Рецидивы при ВПГ-2 проявляются раньше и чаще, чем при ВПГ-1.
Анализ сывороток различных групп населения показал очень высокое содержание антител против ВПГ-2 у пациентов с инвазивной карциномой шейки матки (в 83% случаев, против 20% в контрольной). Врачи должны более тщательно обследовать больных с герпетической инфекцией гениталий, как на вирусное, так и злокачественное заболевание шейки матки.
Вторичный генитальный герпес способствует возникновению рака головки полового члена.
Лечение: зависит от формы и периода заболевания.
При первичном генитальном герпесе местно 5% мазь или крем ацикловир, таблетки ацикловир по 200 мг 5 раз в день в течение 5 дней или внутривенное введение ацикловира 5мг/кг каждые 8 часов в течение 5 дней, бонофтоновая, теброфеновая или оксолиновая мази 6 раз в сутки в течение 15-20 дней, иммуностимуляторы.
При поражении уретры - введение каплями раствора интерферона.
При эрозиях - примочки или суппозитории с интерфероном, виферон.
При рецидивирующем генитальном герпесе:
- эпизодическое лечение каждого обострения: наружно 5% крем ацикловир 5 раз в день в течение 10 дней, иммуностимуляторы,
- при 6 и более обострений в год - продолжительная терапия ацикловиром по 200 мг 4-5 раз в день в течение 3 месяцев, иммуностимуляторы.
Генерализованный герпес новорожденных.
1. Неонатальная герпетическая инфекция у детей почти всегда связана с ВПГ-1, который поражает ротовую полость и лицо. Передача возбудителя чаще всего происходит при родах во время прохождения через родовые пути. Большинство женщин, родивших зараженных детей, не имеют в анамнезе герпетических заболеваний. В клинической картине преобладают явления энцефалита (лихорадка, вялость, снижение аппетита, судороги), характерно поражение кожи и внутренних органов (печени, легких, надпочечников),
Профилактика заключается в 100% обследовании супругов и беременных женщин для выявления антител к вирусам герпеса. При явных клинических проявлениях генитального герпеса у беременной - рождение ребенка кесаревым сечением.
Прогноз - сомнительный, смертность достигает 90%.
2. Трансплацентарно или путем восходящей инфекции, особенно после преждевременного разрыва оболочек, а также путем передачи вирусов со спермой через инфицированную яйцеклетку, развивается внутриутробное инфицирование, на 50% обусловленное ВПГ-2. Наибольшее число заболеваний у новорожденных встречается при первичной инфекции у матери на поздних сроках беременности. Это может привести к молниеносной диссеминирующей инфекции плода и послужить причиной нарушения органогенеза и возникновения уродств или обусловливает самопроизвольное преждевременное прерывание беременности, мертворождение и раннюю детскую смертность. Дети могут рождаться с недоразвитостью головного мозга, гепатитом, желтухой, менингитом, отложением кальция в головном мозге, поражением глаз, зрительного нерва, клеток крови, надпочечников и др. Такие дети, как правило, нежизнеспособны.
ВИРУС ГЕРПЕСА ЗОСТЕР
1. Ветряная оспа - развивается при отсутствии предшествующего иммунитета. Возбудитель передается воздушно-капельным путем. Чаще болеют дети. После исчезновения клинических проявлений вирус в организме сохраняется пожизненно.
2. При резком снижении защитных сил организма вирус персистирует, что манифестно проявляется в виде клиники ветряной оспы (у лиц, уже переболевших ей). Затем наступает (атентный период, характеризующийся развитием вирусов в ганглиях периферической нервной системы, и развивается клиника, широко известная под названием опоясывающий лишай. Появляется сильное чувство жжения, стреляющие боли, покалывания. Боли часто симулируют клинику стенокардии, аппендицита и др. Вскоре на отечном гиперемированном основании развиваются многочисленные пузырьки с серозным содержимым. Высыпания локализуются по ходу нервов (чаще межреберных и тройничных). Присоединяются резкие, жгучие боли такой интенсивности, что больные кричат, вынуждены искать положение тела, при котором боли менее сильные. Пузырьки сливаются в буллы, появляются очаги некроза. Длительность заболевания 3-4 недели, после чего сыпь исчезает, боль может оставаться несколько месяцев или лет.
Больных с опоясывающим герпесом нужно наиболее тщательно обследовать на выявление онкологических заболеваний.
Лечение: местно в остром периоде жидкий анальгин и флуцинар; мази госсипол, теброфеновая, Ацикловир по 800 мг 5 раз в день в течение 7-10 дней и иммунокорректоры. После однократно перенесенного заболевание не повторяется.
ВИРУС ЭПШТЕЙНА-БАРРА
С этим вирусом связано развитие инфекционного мононуклеоза. Заболевание часто дает малигнизацию в лимфому Беркита, тесно связан и с возникновением лимфогранулематоза. Встречается больше в странах Африки и Азии, поражая детей 2-15 лет. Процесс протекает в верхней челюсти, яичниках, орбитах глаз, почках, селезенке, периферических лимфоузлах. Лечение по схеме полихимиотерапии агрессивных лимфом.
ВИРУС ЦИТОМЕГАЛИИ
Цитомегаловирус человека (Сytomegalovirus hominis, Вирус Герпеса Человека 5 типа).
Краткое название: ЦМВ, ВГЧ-5, CMV, HHV-5.
Классификация:
Семейство: Герпесвирусы
Подсемейство: бета-герпесвирусы.
ЦитоМегалоВирус (ЦМВ) был открыт ученой Маргарет Гледис Смит в 1956 году. Этот вирус наиболее распространенный среди людей представитель группы герпес - вирусов. Внешний ЦМВ сходен с вирусами простого герпеса, вызывающими генитальный герпес и герпес губ. Большинство взрослых и значительное количество детей инфицировано этим вирусом. Статистика свидетельствует, что половина жителей села и до 90% городского населения возрасте до 40 лет инфицированы цитомегаловирусом. После инфицирования вирус долгие годы может бессимптомно находиться в организме, не вызывая каких-либо заболеваний. У большинства людей с "нормальным" иммунитетом вирус до конца жизни никак не проявляет себя.
Наибольшую опасность ЦМВ - инфекция представляет для людей с иммунодефицитами, развившимися вследствие лучевой или химиотерапии при онкологических заболеваниях, при приеме в значительных дозах кортикостероидов , иммуносупрессивной терапии при пересадке органов, ВИЧ - инфекции, а также если ЦМВ заражается новорожденный. У этой группы людей цитомегаловирус может вызвать пневмонию, поражения головного мозга печени, сердца и сетчатки глаза.
Как происходит заражение:
Вирус попадает из внешней среды со слюной больного собеседника, с мужским семенем, выделениями из влагалища и шейки матки, с мочой, с кровью, со слезной жидкостью, с грудным молоком (наиболее распространенный в мире способ передачи).
Пути передачи:
1. Контактный и половой:
- - Контакт с новорожденными, включая ежедневный уход за ними (дети инфицированные в родах, в течении первых 5 лет жизни выделяют из организма вирус);
- - Половой путь (раннее начало половой жизни, множество половых партнеров, гомосексуальные связи, перенесенные ранее венерические болезни)
2. Внутрибольничное заражение
- - При пересадке органов от лиц, инфицированных ЦМВ.
- - При переливании крови и препаратов крови от лица, инфицированного ЦМВ. (В Российской Федерации продукты из крови и цельная кровь на наличие ЦМВ не проверяются).
Вирус попадает в организм человека и проникает в кровь. Но не дремлет страж нашего здоровья - иммунная система, она убивает вирус в крови, "загоняя" его в железы, вырабатывающие слюну /слюнные железы/ и ткань почки, где вирус переходит в неактивное состояние и на протяжении многих недель, месяцев или лет "спит". "Спящий" вирус иммунная система распознать не может.
При нарушениях иммунитета происходит реактивация: цитомегаловирус разрушает структуры человеческой клетки, вызывая образование комочков из ядер, митохондрий, эндоплазматической сети, аппарата Гольджи, лизосом - известных Вам по школьному курсу биологии. После подобных разрушений клетка, как тонущий корабль, наполняется подзавязку жидкостью и сильно разбухает. Инфекционный процесс характеризуется поражением слюнных желез с образованием в тканях гигантских клеток с внутриядерными включениями, ассоциирован с ВИЧ. Для передачи возбудителя требуется длительный и тесный контакт.
Основной путь передачи - половой. Вирус обнаруживается в слюне, моче, крови, грудном молоке, сперме (очень много). Выделяется со слюной до 4 недель, с мочой - до 2-х лет.
Заболевание протекает бессимптомно или с небольшой клиникой. При внутриутробном заражении дети рождаются с недоразвитым головным мозгом, с массивными отложениями кальция в нем, водянкой головного мозга, гепатитом, желтухой, увеличением печени и селезенки, пневмонией, пороками сердца, поражением миокарда, паховой грыжей, врожденными уродствами и др.
Лечение: ацикловир внутривенно 5 мг/кг веса (10 мг/кг) 3 раза в день в течение 10 дней в сочетании с иммуностимулирующей терапией.
ВИЧ (Вирус Иммунодефицита Человека) - это вирус, который передается от человека к человеку определенными путями и вызывает нарушение функций или разрушение иммунной системы организма человека.
ВИЧ-инфекция возникает при проникновении в организм человека вируса иммунодефицита.
СПИД (AIDS) - это сокращение от Синдром Приобретенного Иммунного Дефицита. Это последняя (терминальная) стадия ВИЧ - инфекции.
Что делает вич в организме человека?
ВИЧ - это необычный вирус, потому что человек может быть инфицирован много лет и казаться при этом абсолютно здоровым. Но вирус постепенно размножается внутри организма и в конце концов уничтожает возможность организма бороться против инфекций и болезней, убивая клетки крови, которые являются частью иммунной (защитной) системы организма.
Если человек инфицирован, это еще не значит, что у него сразу разовьется СПИД. Вирус может находиться в организме десять и более лет, прежде чем человек почувствует какие-либо симптомы заболевания. В течение этого периода человек может выглядеть и чувствовать себя абсолютно здоровым, но при этом может передать этот вирус другим. Таким образом:
- можно получить ВИЧ, даже не подозревая этого;
- можно передать ВИЧ другим, не зная об этом.
Через некоторое время после попадания ВИЧ в организм у людей появляется состояние, напоминающее грипп, но через несколько дней оно проходит. Обычно никто не связывает эти проявления с ВИЧ - инфекцией.
Что происходит с человеком, больным спидом?
У человека появляются серьезные проблемы со здоровьем: могут развиться пневмония, рак, различные формы лихорадки, другие серьезные заболевания, многие из которых никогда не возникают у людей с не разрушенной иммунной системой. Эта стадия заболевания называется СПИД. В это время человек может резко потерять вес на 10% и более, иметь длительное время (более одного месяца) постоянно повышенную температуру тела, сильное ночное потоотделение, хроническую усталость, увеличение лимфатических узлов, постоянный кашель и длительный жидкий стул. После этого наступает момент, когда сопротивляемость организма окончательно потеряна, а болезни настолько обостряются, что человек умирает.
Можно ли вылечить СПИД?
В настоящее время нет лекарства, способного уничтожить ВИЧ в организме человека и нет вакцины, способной предотвратить заражение. Но существуют препараты, которые при правильном подборе и применении могут поддержать здоровье и замедлить развитие СПИДа на длительное время. Благодаря этим лекарствам человек может полноценно жить. Успехи генотерапии вселяют надежду, что в ближайшем будущем возможно появление способа лечения, основанного на методе редакции генома (CRISPR-Cas), позволяющего внести в копию гена CCR5 инфицированного ВИЧ человека делецию 36 нуклеотидов. Известно, что люди, имеющие такую мутантную версию этого гена (CCR5-delta36) маловосприимчивы или совсем невосприимчивы к вирусу ВИЧ. Большинство природных носителей этой мутации (делеции) - выходцы из северных стран Европы (Норвегии, Финляндии) и северных регионов европейской части России.
Как передается ВИЧ?
Исследование показало, что ВИЧ содержится в различных биологических жидкостях организма человека, но в различных количествах. В концентрации, достаточной для заражения, вирус содержится в крови, сперме, влагалищном секрете, материнском молоке. Пути заражения ВИЧ -инфекцией различны, но, чтобы заражение произошло, необходимо:
- попадание ВИЧ в кровь здорового человека;
- количество ВИЧ должно быть достаточным для заражения.
Поэтому вирус иммунодефицита может попасть в организм человека только тремя путями:
(I) При незащищенном половом контакте с ВИЧ - инфицированным или больным СПИДом.
Большинство случаев передачи ВИЧ - инфекции происходит при половых контактах. Чем с большим количеством людей человек вступает в половые отношения без использования презерватива, тем выше вероятность того, что он в конце концов окажется с партнером - носителем ВИЧ. В то же время может быть достаточно только одного полового контакта с носителем вируса, чтобы заразиться ВИЧ - инфекцией. Во время полового акта ВИЧ может передаваться от мужчины к женщин, от женщины к мужчине, от мужчины к мужчине и от женщины к женщине.
(II) При попадании крови ВИЧ - инфицированного или больного СПИДом в организм здорового человека.
Это может произойти при переливании крови или ее продуктов от ВИЧ - инфицированных доноров или при использовании нестерильного, необработанного медицинского инструментария, содержащего частицы крови инфицированных. Но сейчас шансы заразиться таким способом очень малы. Продукты крови, которые используются для лечения людей, исследуются на содержание вируса, применяются одноразовые медицинские инструменты. Этот путь передачи ВИЧ распространен среди лиц, употребляющих наркотики внутривенно, так как часто группа потребителей наркотиков имеет общие шприц и иглу, которые никак не обрабатывается.
(III) От ВИЧ - инфицированного или больного СПИДом матери - ребенку.
Это тоже может произойти во время беременности (когда ВИЧ проникает через плаценту к плоду), в процессе родов (когда во время прохождения ребенка через родовые пути матери ВИЧ вместе с кровью может попасть в организм новорожденного через легко ранимую кожу) и при грудном вскармливании ребенка (когда ВИЧ из молока матери через микротравмы во рту попадает в кровь).
ВИЧ - инфекция не передается в быту. Невозможно заразиться, пользуясь с ВИЧ - инфицированными общей посудой, туалетом, плавая с ними в одном бассейне, здороваясь и обнимаясь. ВИЧ не переносится насекомыми.
Никто не застрахован от заражения ВИЧ. Любой человек, мужчина или женщин, в любом возрасте, вне зависимости от места проживания и религиозных убеждений может заразиться. Чтобы не пребывать в неведении, необходимо переодически сдавать анализ на ВИЧ. Особенно это касается тех, кто имел за последнее время случайные связи, с незащищенными половыми контактами, подвергался операциям или переливанию крови, делал инъекции, лечил зубы, проходил инструментальное исследование или вмешательство у гинеколога или уролога, напрямую контактировал с кровью других людей. Анализ крови на ВИЧ обычно делается быстро, анонимно, недорого. Помните, что раннее обнаружение ВИЧ-инфекции и своевременно начатое лечение позволяют прожить инфицированному человеку как минимум 20 лет с момента постановки диагноза. Это тот срок, который позволит медицинской науке найти окончательное решение вопроса ВИЧ-инфекции.
Читайте также:

