Грибковые и паразитарные заболевания кишечника
Обновлено: 05.05.2024
Для цитирования: Лапина Т.Л., Ивашкин В.Т. Грибковая инфекция в патологии желудочно-кишечного тракта. РМЖ. 2001;1:32.
Значение грибковой инфекции в гастроэнтерологии или переоценивается, или наоборот, не находит должной оценки. Часто имеет место явная гипердиагностика. Например, на основании наличия грибов Candida в посеве мазка со слизистой ротовой полости у человека без признаков стоматита, или в анализе кала “на дисбактериоз” больного с синдромом раздраженной кишки устанавливается диагноз кандидоза или даже “системного микоза”. При этом совершенно не учитывается, что грибок является комменсалом человека и широко распространен в окружающей среде (как например, Candida, Aspergillus). Поэтому выделение, скажем, представителей Candida с поверхности кожи, полости рта, из мокроты, мочи и кала должно быть интерпретировано с осторожностью.
Всегда нужно учитывать, что многие грибы не проявляют патогенные свойства, если организм хозяина не ослаблен. Нарушения анатомических, физиологических и иммунологических механизмов защиты организма создают условия для развития инфекционного процесса, вызванного его собственной в обычных условиях непатогенной микрофлорой или сапрофитными микроорганизмами из окружающей среды.
К условиям развития оппортунистической инфекции относятся: лечение кортикостероидами, иммунодепрессантами, антиметаболитами, антибиотиками; СПИД и другие иммунодефицитные состояния; серьезные метаболические расстройства (например, при сахарном диабете, почечной недостаточности); новообразования и противоопухолевая терапия. Грибковое поражение, в том числе и желудочно-кишечного тракта, развивающееся на фоне тяжелого заболевания, должно быть вовремя распознано и адекватно пролечено, так как эта инфекция может оказать отрицательное влияние на прогноз основного заболевания. Правильно распознанное грибковое поражение желудочно-кишечного тракта часто обеспечивает основной диагноз. Так, кандидоз ротовой полости и пищевода - одна из “визитных карточек” СПИДа. Одним из важных гастроэнтерологических аспектов рассматриваемой проблемы является также и то, что грибковая инфекция может явиться осложнением энтерального и особенно парентерального питания.
Клиническая картина
Наиболее часто у больных с подавленным иммунитетом отмечается инфекция Candida albicans, реже – другими представителями рода Сandida.
Для кандидозного стоматита характерен белый налет, слегка возвышающийся над слизистой оболочкой ротовой полости и напоминающий свернувшееся молоко или творог. При снятии налета обнажается гиперемированная поверхность, которая может слегка кровоточить (псевдомембранозная форма). При атрофической форме очаги поражения имеют вид эритемы. Симптомы включают в себя сухость, жжение, частое снижение вкусовой чувствительности. Кандидозный стоматит широко распространен среди больных СПИДом (один из наиболее частых вариантов манифестации заболевания), а также при применении антибиотиков, кортикостероидов и противоопухолевых средств.
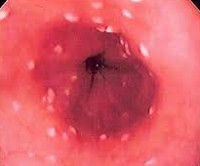
Грибковые эзофагиты - чаще всего кандидозные. Они развиваются при иммунодефицитных состояниях, антиботикотерапи, часто у больных сахарным диабетом (высокая концентрация глюкозы в слюне благоприятна для роста грибов), у лиц старческого возраста или с нарушенным трофологическим статусом. Грибковые эзофагиты встречаются и при ахалазии кардии, других двигательных нарушениях, например в рамках склеродермии, и при стенозах пищевода. Клинически грибковые эзофагиты проявляются дисфагией и одинофагией (болезненное глотание). В тяжелых случаях специфический эзофагит может осложняться кровотечением, перфорацией, стриктурой пищевода или развитием кандидомикозного сепсиса. При эндоскопическом исследовании определяются желто-белые рельефные наложения на гиперемированной слизистой оболочке пищевода. Рентгенологическое исследование может выявить множественные дефекты наполнения различных размеров. Диагноз подтверждается при микроскопическом исследовании мазков, полученных при эзофагоскопии.
Жалобы на дисфагию и дискомфорт за грудиной у больного СПИДом служат основанием для широкого дифференциального диагноза, так как поражение пищевода у этих больных может быть вызвано и вирусами (простого герпеса, цитомегаловирусом), и развитием саркомы Капоши, и другими причинами. Однако диагностику кандидозного эзофагита нельзя назвать сложной. Наличие грибкового стоматита у ВИЧ-инфицированного больного с дисфагией, скорее всего, укажет на правильную этиологию эзофагита, а эндоскопия с микробиологическим или гистологическим исследованием однозначно устанавливает диагноз в 95,5% случаев (I. McGowan, I.V.D. Weller, 1998).
При подавлении иммунной системы и общем ослаблении организма возможно развитие грибкового гастрита, наиболее частым возбудителем которого являются представители рода Candida, Histoplasma, Mucor.
Кандидоз с поражением тонкой и толстой кишки, как причина диареи - не столь частое явление, как это может показаться на первый взгляд. Диарея - один из наиболее частых симптомов иммунодефицитных состояний, причем не только инфекционные агенты становятся ее причиной. Однако роль грибковой инфекции (в том числе Candida), как причины диареи, невелика. Так, при СПИДе возбудителями инфекционного процесса в тонкой и толстой кишке, сопровождающегося диареей, являются, в первую очередь, простейшие - Cryptosporidium, Microsporidium (Enterocytozoon beineusi), Isospora belli, Giardia lamblia. Из вирусов, связанных при СПИДе с развитием диарейного синдрома, следует назвать цитомегаловирус и вирус простого герпеса, а из бактерий – выделить Salmonella, Shigella, Campylobacter spp.
Важно обратить внимание на хорошо дифференцированную нозологическую единицу - псевдомембранозный колит. Это острое воспалительное заболевание кишечника, ассоциированное с антибиотикотерапией. Его клиническая картина варьирует от кратковременной диареи до тяжелой формы с лихорадкой, дегидратацией и осложнениями. Описаны случаи этого заболевания при уремии, после цитостатической терапии. При колоноскопии на слизистой оболочке обнаруживаются фибриноидные наложения, из-за которых заболевание и получило свое название. Несмотря на поверхностное сходство с кандидозом (начало заболевания провоцируется антибиотиками, на слизистой оболочке выявляются наложения белого цвета), псевдомембранозный колит не имеет никакого отношения к этой грибковой инфекции. Возбудитель колита, ассоциированного с антибиотиками (синоним псевдомембранозного колита), установлен. Это Clostridium difficile - грамположительный анаэроб. Антибиотикотерапия, подавляя собственную микрофлору, создает условия для размножения С. difficile и проявления ее патогенных свойств. Диагноз устанавливается на основании выявления возбудителя в кале или путем обнаружения токсина С. difficile. Это отступление, посвященное псевдомебранозному колиту, еще раз подчеркивает необходимость адекватной оценки клинической картины, данных инструментального обследования и лабораторных тестов. Диагноз грибковой инфекции, в том числе кандидоза, должен опираться на возможно более полную информацию.
Диагностика
Наиболее частые грибковые поражение желудочно-кишечного тракта – кандидоз ротовой полости и пищевода – имеют достаточно характерные признаки. Для правильного диагноза получение культуры возбудителя должно быть подтверждено характерными клиническими симптомами, исключением другой этиологии, а также гистологическими признаками тканевой инвазии. В случае системного кандидоза диагноз помогает поставить посев гриба из крови, спинномозговой жидкости или из тканей, например, биоптата печени, что позволит прояснить клинические признаки - септицемию, менингит или поражение печени.
Гораздо меньшее значение в гастроэнтерологии имеют Cryptococcus и Histoplasma. Как правило, вовлечение в патологический процесс при этих грибковых инфекциях органов желудочно-кишечного тракта и печени наступает у больных с иммунодефицитом при диссеминированной форме заболевания. Histoplasma capsulatum при гематогенном распространении из легких поражает печень и селезенку с явлениями гепато- и спленомегалии, а поражение желудочно-кишечного тракта сопровождается изъязвлением (особенно часто ротовой полости). При СПИДе Cryptococcus neoformans и Histoplasma spp. при диссеминированных криптококкозе и гистоплазмозе поражают печень по типу гранулематозного гепатита. Клинически и биохимически при этом имеет место синдром холестаза. Для установления точного диагноза необходима биопсия печени, при которой будет доказана грибковая тканевая инвазия.
Лечение
Современные противогрибковые средства представляют собой весьма внушительный арсенал.
Флуконазол (водорастворимый триазол) высокоселективно ингибирует грибковый цитохром P450, блокирует синтез стеролов в клетках гриба. На сегодняшний день существует отечественный флуконазол - Флюкостат. Он почти полностью всасывается в желудочно-кишечном тракте, что позволяет быстро достичь адекватных концентраций в сыворотке. Его применяют при кандидозах и криптококкозе. При СПИДе для лечения криптококкоза после предварительного курса амфотерицином В (без фторцитозина или в сочетании с ним, что предпочтительнее) флуконазол назначают по 200 мг в сутки.
Кетоконазол (производное имидазола) обладает широким спектром противогрибковой активности, однако в отличие от флуконазола может вызвать временную блокаду синтеза тестостерона и кортизола.
Фторцитозин включается в клетки гриба, где превращается в 5-фторурацил и ингибирует тимидилатсинтетазу. Обычно препарат используют для лечения кандидоза, криптококкоза, хромомикоза.
Амфотерицин В воздействует на стеролы грибковой мембраны, нарушает ее барьерные функции, что приводит к лизису грибов. Показанием к его назначению являются системные микозы - кандидамикоз, аспергиллез, гистоплазмоз и другие.
С учетом тяжести заболеваний, на фоне которых возможны оппортунистические инфекции, противогрибковая терапия часто требует комбинирования препаратов, повторных курсов или поддерживающего лечения. В качестве примера возможные варианты лечения кандидозного поражения желудочно-кишечного тракта у больных СПИДом представлены в таблице.
Флуконазол –
Флюкостат (торговое название)
(ЛЭНСФарм)
Микозы желудочно-кишечного тракта — патологические состояния, развившиеся вследствие поражения пищеварительных органов дрожжеподобными, плесневыми, диморфными грибами. Проявляются изменением вкуса, появлением налетов на видимых слизистых, диспепсией, жидким стулом, болевыми ощущениями разной локализации. Диагностируются с помощью эзофагогастродуоденоскопии, колоноскопии, электрогастрографии, микробиологического исследования биоптата, ИФА, РИФ, ПЦР. Для лечения используют антимикотики, пробиотики, иммуномодуляторы в сочетании с комплексной терапией основного заболевания, осложнившегося грибковой инфекций.
МКБ-10
Общие сведения

Причины микозов желудочно-кишечного тракта
Возбудителями микотической инфекции органов ЖКТ становятся плесневые, дрожжеподобные, диморфные грибы, в большинстве случаев являющиеся естественными комменсалами человеческого организма. 9 из 10 микозов пищеварительного тракта провоцируется Candida albicans — условно-патогенным микроорганизмом, который высеивается у 65-70% населения. Микотический процесс также может развиться в результате размножения так называемых кандид non-albicans (С. guilliermondii, С. kefyr, С. krusei, С. tropicalis и др.). Некандидозные формы микотических желудочно-кишечных болезней, вызванные возбудителями бластомикоза, гистоплазмоза, кокцидиомикоза, криптококкоза, паракокцидиомикоза, споротрихоза, возникают при диссеминации грибов из очагов на коже, в респираторном тракте, других органах. Аспергиллез пищеварительных органов, интестинальный зигомикоз диагностируются редко, обычно – при наличии тяжелой сопутствующей патологии.
Манифестации микозов часто предшествуют другие патологические состояния, способствующие патологической активации условно-патогенной флоры за счет снижения местной защитной реакции слизистой ЖКТ, угнетения иммунных сил организма. Специалисты в сфере гастроэнтерологии и микологии выделяют следующие предпосылки к развитию желудочно-кишечного микотического заболевания:
- Физиологическая иммунная недостаточность. Естественное снижение иммунитета наблюдается у беременных, связано с необходимостью поддержания гестации. Незрелость иммунной системы характерна для новорожденных, риск инфицирования возрастает при недоношенности и наличии генитального кандидоза у матери. В пожилом возрасте отмечается инволютивное угасание защитных сил.
- Патологический иммунодефицит. Несостоятельность иммунной системы лежит в основе ВИЧ-инфекции и ее клинически выраженной формы — СПИД. Нарушения иммунитета отмечаются при дисплазии тимуса, других первичных иммунодефицитах, онкогематологических и лимфопролиферативных болезнях (лейкозах, лимфогранулематозе, неходжкинских лимфомах), сахарном диабете, голодании.
- Ятрогенные факторы. Иммунная функция угнетается при использовании кортикостероидов, цитостатиков, других химиопрепаратов у пациентов, перенесших трансплантацию органа, принимающих лечение по поводу онкопатологии, ревматоидного артрита, СКВ, гломерулонефрита, других системных болезней. Развитию микозов способствует антибактериальная терапия.
- Повреждения слизистой оболочки ЖКТ. Инвазии грибов более подвержены больные, страдающие атрофическим гастритом, ахалазией кардии, бульбитом, гастроэзофагеальной рефлюксной болезнью, дисбиозом, болезнью Крона, другой желудочно-кишечной патологией. Инфицирование облегчается при ожогах, травматизации эпителия зубными протезами, твердой пищей, интубационной трубкой.
Патогенез
Механизм развития микозов желудочно-кишечного тракта основан на нарушении баланса между реактивностью организма и факторами патогенности грибов — протеолитическими ферментами инвазии (коагулазой, каталазой, козеиназой, фосфолипазой), фибриллярными белковыми комплексами, эндотоксинами. При иммунодефиците уменьшается активность интраэпителиальных лимфоцитов, В-клеток кишечника, снижается цитотоксичность Т-клеточных элементов, нарушается секреция интерферона, фагоцитоз. В результате возбудители микозов быстро обсеменяют эпителий, легко проникают через собственную пластинку слизистой, агрегируются в пейеровых бляшках.
При травмах, химических ожогах, заболеваниях пищеварительных органов, изменениях кислотности и ферментативного состава желудочного, кишечного соков ситуация усугубляется наличием участков пораженной слизистой, замедленной регенерацией эпителиальных клеток, нарушением защитной функции естественных секретов. У пациентов, принимающих антибиотики, дополнительным патогенетическим фактором становится гибель облигатных микроорганизмов (кишечной палочки, аэробных лактобацилл, анаэробных бифидобактерий), которые являются естественными антагонистами грибов и сдерживают их неконтролируемое размножение.
Классификация
При систематизации форм микотической инфекции ЖКТ учитывают вид возбудителя, локализацию и распространенность патологического процесса. С учетом этиологии различают кандидоз, являющийся самым частым видом микозов, и редкие формы грибкового поражения (аспергиллез, криптококкоз, зигомицетоз и др.). При поражении одного отдела пищеварительного тракта говорят о фокальном микозе, при массивном распространении инфекции — об инвазивном диффузном, при отсутствии признаков инвазии — о микотическом дисбиозе. Наиболее часто используют классификацию микозов по локализации поражения, в соответствии с которой выделяют:
- Орофарингеальные поражения. В структуре микотических инфекций ЖКТ занимают первое место. Обычно встречаются у новорожденных и пациентов с иммунодефицитными состояниями (СПИД, гемобластозы).
- Микотический эзофагит. Диагностируется у 1-7% больных. Чаще развивается при сниженном иммунитете. Может протекать как в поверхностной, так и в эрозивной форме с повышенной кровоточивостью.
- Микотические поражения желудка. Составляют до 5,2% микозов ЖКТ. Выявляются при гастродуоденальных язвах, хронических гастритах. В ряде случаев определяются ассоциации грибов и хеликобактера.
- Микозы кишечника. Обычно возникают на фоне микотического поражения верхних отделов пищеварительного тракта. Как правило, диагностируются у больных, получающих массивную антибиотикотерапию.
- Микотическая инфекция гепатобилиарной системы. Осложняет дискинезию желчных путей, холестаз, холецистолитиаз, лямблиоз. Диагностируется редко, в том числе из-за низкой настороженности.
Симптомы микозов ЖКТ
Клиническая картина заболевания различна в зависимости от распространенности поражения. При орофарингеальной локализации микоза у пациента возникают боли во время приема пищи, неприятный привкус во рту, на слизистой оболочке щек и языка появляются белые налеты. Поражение пищевода и желудка характеризуется болью при глотании, дисфагией, изжогой, отрыжкой, тошнотой и рвотой, дискомфортом в эпигастральной области, снижением аппетита. При прогрессировании заболевания в процесс вовлекаются нижележащие отделы желудочно-кишечного тракта, что клинически проявляется диареей с примесями слизи и крови, болезненностью в левой подвздошной области. Возможны нарушения общего состояния: субфебрильная температура тела, слабость, снижение трудоспособности, резкое уменьшение веса.
Осложнения
Вследствие проникновения микроорганизмов из пищеварительного тракта в забрюшинную клетчатку могут возникать гнойно-воспалительные процессы — парапроктит, паранефрит, межкишечные или поддиафрагмальные абсцессы. У пациентов со сниженной реактивностью организма имеется склонность к генерализации микозов с развитием септицемии, приводящей к распространению грибков на другие органы. Наиболее опасно микотическое поражение гепатобилиарной системы, которое может вызывать желтуху и печеночную недостаточность. При тяжелом течении заболевания формируются некрозы стенки кишечника, иногда – с перфорацией. Возможны профузные желудочно-кишечные кровотечения, пенетрация язв в соседние органы.
Диагностика
Постановка диагноза микозов желудочно-кишечного тракта затруднена из-за полиморфности и неспецифичности клинической картины заболевания, которая сходна с проявлениями других патологий пищеварительной системы. Для диагностики грибкового поражения требуется комплексное обследование пациента. Наиболее информативными являются следующие методы:
В клиническом анализе крови наблюдаются неспецифические признаки воспалительного процесса: повышение СОЭ, незначительный лейкоцитоз, может выявляться снижение уровня эритроцитов и гемоглобина, что обусловлено кровотечениями. Для исследования структуры всех слоев стенки пищеварительного тракта выполняется эндоскопическая ультрасонография. Дифференциальная диагностика осуществляется с воспалительными заболеваниями кишечника (терминальным илеитом, неспецифическим язвенным колитом), злокачественными новообразованиями, псевдомембранозным энтероколитом, желудочно-кишечным туберкулезом. Помимо осмотра гастроэнтеролога пациенту могут потребоваться консультации инфекциониста, онколога, фтизиатра.
Лечение микозов ЖКТ
Основными задачами являются терапия расстройства, вызвавшего активацию микотической флоры, и этиопатогенетическое воздействие на возбудителя грибковой инфекции. Лечение болезней пищеварительного тракта, иммунодефицитных и других патологических состояний проводят по протоколам соответствующих заболеваний. Для подавления грибкового процесса используют:
- Антимикотики. По результатам наблюдений, наиболее эффективной является терапия триазолами. Средства этой группы угнетают систему цитохрома P-450 и синтез эргостерола клеточных мембран, нарушая рост и репликацию кандид и криптококков. В качестве альтернативы с учетом особенностей возбудителя могут применяться полиены, аллиламины, эхинокандины.
- Пробиотики. Препараты, в которых содержатся непатогенные и нетоксигенные микроорганизмы, позволяют восполнить естественную микрофлору кишечника, нормализовать ее состав после проведенной антибактериальной терапии. Апатогенные бактерии стимулируют кишечный иммунитет, оказывают антагонистический эффект по отношению к грибам, нарушают их адгезию к слизистым.
При отсутствии противопоказаний проводится неспецифическая иммунотерапия стимуляторами естественного иммунитета (высокополимерные полисахаридные комплексы, регенеранты, производные пиримидина), Т- и В-лимфоцитов (полипептидные экстракты вилочковой железы, культур клеток костного мозга, селезенки). Возможно дополнительное использование растительных иммуномодуляторов, витаминно-минеральных комплексов.
Прогноз и профилактика
Исход болезни зависит от степени повреждения пищеварительных органов, состояния иммунной системы пациента, своевременности диагностики и терапии. Прогноз сомнительный при генерализации процесса и наличии тяжелых сопутствующих заболеваний. Для предупреждения развития микозов необходимо не допускать неоправданного применения антибактериальных средств, назначать профилактические курсы противогрибковых препаратов при длительном лечении цитостатиками, кортикостероидами, другими медикаментами с иммунодепрессорным эффектом, осуществлять диспансерное наблюдение за пациентами с иммунодефицитом.
2. Грибковые поражения желудочно-кишечного тракта/ Омаров Т.Р., Омарова Л.А.// Русский медицинский журнал – 2016 - №11.
3. Микозы пищеварительного тракта (обзор)/ Лесовой В.С., Липницкий А.В., Очкурова О.М.// Проблемы медицинской микологии – 2004 – Т.6, №2.
Кандидоз кишечника – инфекционное поражение пищеварительного тракта, вызванное собственной грибковой флорой пациента (Candida spp.) на фоне значительного ослабления иммунитета. Клинические проявления кандидоза кишечника варьируют в зависимости от формы заболевания: разжижение стула, повышенный метеоризм, неопределенные боли в животе, язвенный колит и грибковый сепсис. Диагноз ставится на основании эндоскопического исследования, гистологического и культурального анализа биоптатов, кала. Лечение включает три основных направления: назначение антимикотиков, нормализацию микрофлоры кишечника и коррекцию иммунного статуса пациента.

Общие сведения
Кандидоз кишечника – грибковое поражение слизистой оболочки пищеварительного тракта. Является актуальной проблемой современности, так как диагностика и определение критериев данного заболевания представляют сложность для многих клиницистов. Связано это с повсеместной распространенностью грибов рода Candida, в том числе и в организме здоровых людей (носительство грибов рода Candida в кишечнике присуще 80% населения). Инвазивный кандидоз кишечника практически никогда не встречается у людей с нормально функционирующим иммунитетом, почти всегда это оппортунистическая инфекция, связанная с иммунным дисбалансом организма.
Кроме того, для многих специалистов бывает достаточно сложно дифференцировать транзиторное кандидоносительство и неинвазивный кандидоз кишечника (именно он составляет подавляющее большинство всех клинических случаев кандидоза пищеварительной системы). Разграничить два этих состояния возможно только при наличии современного диагностического оборудования. Для установления правильного диагноза необходимо наличие трех диагностических критериев: выявление одного или нескольких факторов риска, эндоскопические признаки кандидоза кишечника, положительный результат культурального исследования. Таким образом, тактика назначения антимикотиков при первом обнаружении в посевах грибов рода Candida, без дальнейшего обследования, является ошибочной.

Причины кандидоза кишечника
Специалисты в области гастроэнтерологии выделяют две патогенетические формы кандидоза кишечника – инвазивную и неинвазивную. В клинической практике чаще встречается неинвазивный кандидоз кишечника на фоне дисбактериоза и смешанной кишечной инфекции (грибково-бактериальной, грибково-протозойной и др.). Висцеральная форма развивается на фоне выраженной нейтропении (практически полное отсутствие нейтрофильных лейкоцитов) и поздних стадий СПИДа.
Факторы риска
Для формирования кандидоза кишечника необходимо наличие хотя бы одного из предрасполагающих факторов:
- физиологического снижения иммунитета (период новорожденности или пожилой возраст, сильный стресс, беременность);
- врожденного иммунодефицита (синдром Di George, Nezelof и др.);
- онкопатологии, особенно в период полихимиотерапии;
- аутоиммунных и аллергических заболеваний (усугубляет угнетение иммунитета лечение кортикостероидными гормонами);
- приема иммунодепрессантов после трансплантации органов;
- тяжелых эндокринных заболеваний, соматической патологии, требующей интенсивной терапии;
- длительного лечения антибактериальными препаратами резервного ряда;
- синдрома первичного иммунодефицита;
- выраженного дисбаланса питательных веществ в рационе (особенно недостатка белка и витаминов).
В клинической практике чаще встречается кандидоз кишечника, обусловленный сочетанием нескольких из перечисленных факторов.
Патогенез
При неинвазивной форме грибы рода Candida начинают неконтролируемо размножаться в просвете кишки, не проникая в толщу ее слизистой. При этом выделяются специфические грибковые токсины, образуются ядовитые продукты ферментации, оказывающие раздражающее действие на слизистую оболочку кишечника. Перечисленные токсические агенты провоцируют дальнейшее усугубление дисбиоза, формирование микотической аллергии, вторичного иммунодефицита.
Патогенез инвазивного кандидоза кишечника иной. При условии ослабления местного и общего иммунитета грибы рода Candida интимно прикрепляются к эпителию кишечника (они имеют тропность к плоскому многослойному эпителию), затем внедряются в его толщу, трансформируясь в нитчатую форму. При наличии выраженной супрессии клеточного иммунитета Candida проникают в кровоток и распространяются по организму, вызывая висцеральный кандидоз (поражение печени, поджелудочной железы).
Симптомы кандидоза кишечника
Кандидоз кишечника встречается в трех основных клинических формах: инвазивный диффузный, инвазивный фокальный и неинвазивный. Критериями диагностики инвазивного диффузного кандидоза кишечника являются тяжелое состояние пациента на фоне выраженной интоксикации, повышение температуры тела, сильная боль в животе, диарея, примесь крови в стуле, системные проявления микоза (поражение печени, поджелудочной железы, селезенки, желчного пузыря и др.). Если эта форма кандидоза кишечника является случайной находкой во время обследования по поводу других заболеваний, в первую очередь следует думать о дебюте СПИДа или сахарного диабета. Инвазивный диффузный кандидоз кишечника не характерен для людей с нормально функционирующей системой иммунитета.
Инвазивный фокальный кандидоз кишечника может осложнять течение язвенной болезни двенадцатиперстной кишки, неспецифического язвенного колита. Заподозрить данную форму кандидоза можно у пациентов с упорным и затяжным течением фонового заболевания, не поддающегося стандартной терапии. Для этого варианта микоза характерна локальная инвазия нитчатой формы Candida в местах нарушенной эпителизации (на дне язв кишечника). При этом в окружающих тканях, других отделах кишки друзы грибов не выявляются. Клиническая картина соответствует основному заболеванию, а псевдомицелий обнаруживается случайно при гистологическом исследовании биоптатов.
Неинвазивный кандидоз кишечника является наиболее распространенной формой данного заболевания. Эта патология не ассоциируется с проникновением грибов в толщу кишечной стенки, а связана с массивным размножением Candida в просвете кишки. При этом выделяется огромное количество токсичных метаболитов, которые оказывают как местное, так и общее резорбтивное действие. Сегодня установлено, что неинвазивный кандидоз составляет примерно треть всех случаев дисбиоза кишечника. Клинически неинвазивный кандидоз кишечника протекает на фоне удовлетворительного состояния пациента, сопровождается умеренными явлениями интоксикации, дискомфортом в животе, метеоризмом, неустойчивым стулом. Часто у таких больных обостряются различные аллергические заболевания. Эту форму кандидоза зачастую путают с синдромом раздраженного кишечника.
Диагностика
Диагностика кандидоза кишечника затрудняется отсутствием типичных клинических признаков, а также достаточно специфичных и чувствительных методов выявления грибов рода Candida в образцах тканей и кале. В общем анализе крови при тяжелых формах заболевания определяется уменьшение количества лейкоцитов, лимфоцитов, эритроцитов. Обязательна консультация врача-эндоскописта для выбора оптимального метода исследования кишечника. Во время эндоскопии обычно обнаруживают неспецифические признаки поражения слизистой, поэтому решающее значение в постановке диагноза имеет эндоскопическая биопсия и морфологическое исследование биоптатов.
Трудности диагностики заключаются в том, что псевдомицелий грибов можно выявить не во всех пробах материала, поэтому достаточно часто встречаются ложноотрицательные результаты. Визуально при диффузном инвазивном кандидозе кишечника определяются признаки язвенно-некротического поражения слизистой, а при неинвазивном – катаральное воспаление. Диагностическим критерием инвазивного кандидоза кишечника служит наличие кандидозного псевдомицелия в биоптатах и отпечатках слизистой оболочки кишки.
Всем пациентам с грибковым поражением кишечника обязательно проводится анализ кала на дисбактериоз, бактериологическое исследование кала. Чаще всего эти анализы выявляют смешанную флору: не только грибы рода Candida, но и кишечную палочку, клебсиеллы, стафилококки и др. Выявление более 1000 колониеобразующих единиц на грамм патологического материала свидетельствует в пользу кандидоза кишечника и исключает носительство грибковой флоры. Основной задачей культурального исследования является установление вида возбудителя, определение чувствительности выделенной микрофлоры к антимикотикам.
Лечение кандидоза кишечника
Консультация гастроэнтеролога при кандидозе кишечника позволяет выявить факторы риска данного заболевания, определить объем необходимых исследований. Так как кандидоз кишечника не имеет специфических клинических признаков, заподозрить эту патологию бывает достаточно сложно. При наличии лабораторных свидетельств кандидоза кишечника выбор тактики лечения зависит от клинического варианта, наличия сопутствующей патологии, переносимости антимикотических препаратов. Обязательными звеньями лечебного процесса при кандидозе кишечника являются: коррекция фонового заболевания, приведшего к снижению иммунитета и активации грибковой флоры; назначение целевого противогрибкового средства; модуляция иммунитета.
Пациенты с диффузной инвазивной формой кандидоза кишечника госпитализируются в стационар. Препаратами выбора для инвазивных микозов являются азольные антимикотики (кетоконазол, флуконазол, итраконазол и пр.), которые активно всасываются из кишечника и оказывают системное действие. Начинают лечение обычно с введения амфотерицина В, затем переходят на терапию флуконазолом.
Для эрадикации грибковой флоры при неинвазивных формах кандидоза кишечника используют противогрибковые препараты нерезорбтивного действия – они плохо всасываются слизистой оболочкой кишки и оказывают сильное местное действие. Нерезорбтивные полиеновые антимикотики имеют ряд преимуществ – у них практически нет побочных действий, они не угнетают нормальную микрофлору кишечника, не вызывают привыкания. К полиеновым препаратам относят натамицин, нистатин. Так как в патогенезе неинвазивного кандидоза имеют значение состояние дисбиоза и смешанная флора, обязательно назначают противомикробные препараты, эубиотики. В качестве симптоматического лечения применяют пищеварительные ферменты, сорбенты, спазмолитики и анальгетики.
Прогноз и профилактика
При диффузной инвазивной форме кандидоза кишечника прогноз серьезный, так как она может приводить к генерализации процесса. Прогноз при инвазивном кандидозе кишечника значительно отягощается наличием тяжелых фоновых заболеваний. При остальных вариантах заболевания прогноз благоприятный при своевременном начале лечения.
Профилактика кандидоза кишечника заключается в устранении предрасполагающих к этой патологии факторов; лечении заболеваний пищеварительного тракта, приводящих к дисбиозу. Для поддержания нормальной микрофлоры кишечника следует разнообразно питаться, ограничивая содержание простых углеводов, употреблять достаточное количество клетчатки. Пациенты, входящие в группу риска по развитию кандидоза органов ЖКТ (ВИЧ, тяжелая эндокринная патология, полихимиотерапия, лечение кортикостероидными гормонами и пр.), требуют пристального внимания и регулярного обследования.
На рубеже XIX-XX вв. уже были описаны почти все основные микозы человека и их возбудители. Имена Вирхова, Груби, Ремарка, Шенлейна, а затем Сабуро тесно связаны с историей становления медицинской микологии. В связи с широким применением антибиотиков, вто
На рубеже XIX-XX вв. уже были описаны почти все основные микозы человека и их возбудители. Имена Вирхова, Груби, Ремарка, Шенлейна, а затем Сабуро тесно связаны с историей становления медицинской микологии. В связи с широким применением антибиотиков, вторая половина XX в. сопровождалась значительным ростом заболеваемости микозами, которые в настоящее время поражают от 5 до 20% взрослого населения (А. Ю. Сергеев, Ю. В. Сергеев, 2003). Среди всех микотических поражений организма человека на втором месте после онихомикоза стоит кандидамикоз слизистых оболочек, до 40% случаев которого, в свою очередь, составляет орофарингеальный микоз (В. Я. Кунельская, 1989).
Значительно реже — в 5-6% случаев — наблюдается микоз глотки, вызванный микроорганизмом бактериальной природы Leptotrix buccalis и грибами Aspergillus, Penicillium, Mucor и др. В ряде случаев поражение глотки обусловлено двумя и более видами грибов — Pharingomycosis mixta.
Практически все эти виды грибов являются сапрофитами, условно-патогенной микрофлорой, активизируются и становятся возбудителями заболевания при нарушении реактивности организма (И. В. Чумичева, 2003).
Развитие фарингомикоза провоцирует сахарный диабет, системные заболевания крови и желудочно-кишечного тракта, особенно дисбактериоз кишечника. Дефицит бифидобактерий и других молочно-кислых бактерий приводит к нарушению синтеза витаминов группы В и к беспрепятственному заселению грибками не только кишечника, но и других соприкасающихся с внешней средой полостей организма (полости носа, рта, уха). Кроме того, отрицательное влияние оказывают злокачественные новообразования, при которых нарушается баланс витаминов, углеводный и белковый обмен, страдает общая, в том числе антимикотическая, резистентность организма. Особенно часто отмечаются микозы у больных СПИДом, 10% которых умирают от грибковых инфекций. Нередко фарингомикоз глотки и полости рта развивается при длительном и неправильном применении топических глюкокортикостероидов при бронхиальной астме.
В формировании патогенетических механизмов грибкового поражения глотки на первое место выступает перестройка иммунной реактивности — накопление и циркуляция в крови грибковых антител, которые обусловливают реакции немедленного и замедленного типа. Имеет значение и изменение клеточного иммунитета. Немаловажное звено в патогенезе фарингомикоза — специфическая и неспецифическая сенсибилизация и аллергия. Определенную роль здесь играет и травматическое повреждение слизистой оболочки глотки — как фактор, предрасполагающий к развитию грибкового процесса.
Микотические очаги в глотке обычно локализуются на небных миндалинах, дужках, небной занавеске, задней стенке, языке. Тканевые реакции выражаются атипической гиперплазией эпителия, образованием гранулем, иногда имеющих псевдотуберкулезный характер, а также в некротических изменениях различной степени выраженности. Гиперплазия эпителия в форме гиперкератоза особенно выражена в криптах миндалин на фоне воспалительного процесса в строме и может принимать форму папилломатоза. В тканях слизистой оболочки глотки, языка и строме миндалин определяются грибковые элементы, располагающиеся субэпителиально.
Микроскопия нативного препарата — наиболее простой и надежный способ диагностики микозов, позволяющий не только установить наличие гриба в исследуемом материале, но и отличить сапрофитию от грибкового заболевания. При сапрофитии в препаратах встречаются лишь единичные непочкующиеся клетки, а при микозе в каждом препарате постоянно определяются все элементы грибов: и мицелий, и бластоспоры.
Забор материала из глотки для исследования на грибы производят ушным пинцетом, ушными щипцами Гартмана или ушной ложкой Фолькмана. Недопустимо для этой цели использовать ватный тампон, поскольку основная часть липкого патологического содержимого остается на тампоне, в связи с чем при микроскопическом исследовании или посеве возможен ложноотрицательный результат. Собранный материал осторожно наносят на стерильное предметное стекло. Материал нельзя растирать по стеклу, так как при этом могут быть повреждены нежные элементы гриба, что также снижает достоверность результатов микроскопии. Выполняют микроскопию неокрашенного и окрашенного по Романовскому-Гимзе нативного препарата, посев патологического отделяемого, полученного при соскобе с миндалин или задней стенки глотки, на элективную питательную среду Сабуро с последующим пересевом культур грибов на среду Чанека для идентификации возбудителя. При выделении культуры Candida нередко требуется количественная оценка. В случае актиномикоза при микроскопии находят значительное разрастание грануляционной ткани с актиномицетами.
Иммунологическая диагностика основана на обнаружении антигенов возбудителя в крови. Серологическая диагностика — разновидность иммунологической диагностики, позволяющая обнаружить в крови антитела к компонентам клетки возбудителя. Особенностью иммунологических методов диагностики является то, что серийные наборы антител или антигенных диагностикумов разработаны только для нескольких, наиболее распространенных возбудителей (кандидоза, криптококкоза, аспергиллеза; диформных грибов). К недостаткам методов иммунодиагностики относят недостаточную чувствительность и специфичность. Однако с помощью иммунодиагностики удается, в частности, прослеживать эффективность лечения по снижению титров (А. Ю. Сергеев, Ю. В. Сергеев, 2003).
Микотическое поражение глотки бывает острым, при этом оно, как правило, сопровождается распространенным поражением слизистой полости рта и глотки, и хроническим, при котором поражение нередко является ограниченным в пределах небных миндалин (тонзилломикоз) или задней стенки глотки (фарингомикоз), — различают рецидивирующую и персистирующую формы хронического фарингомикоза. По клинико-морфологической картине фарингомикозы делятся на псевдомембранозные, которые встречаются чаще всего при данной локализации; эритематозные (атрофические), гиперпластические (гипертрофические, или кандидозная лейкоплакия); эрозивно-язвенные встречаются редко (А. Ю. Сергеев, Ю. В. Сергеев, 2003).
Клиническая картина фарингомикоза разнообразна и определяется не столько разновидностью гриба, вызвавшего заболевание, сколько общей и антимикотической активностью организма. Клиника кандидоза, пенициллиоза и аспергиллеза практически идентична (М. Р. Богомильский, В. Р. Чистякова, 2001). Заболевание характеризуется болями в горле, подъемом температуры, гиперемией слизистой оболочки, появлением вначале мелких белых налетов, а затем и обширных некрозов эпителия, возникающих под влиянием поражения его грибами, стойко сохраняющимися при лечении традиционными консервативными методами. На слизистой оболочке видны множественные серовато-белые налеты неправильной формы, располагающиеся на миндалинах, дужках, небе, а также в других местах и снимающиеся с трудом; после их удаления остается эрозированная поверхность. При хронической форме типичные жалобы появляются с характерной цикличностью, через две-три недели. При поверхностном микозе определяется нерезко выраженная гиперемия слизистой оболочки с небольшими участками полупрозрачных или плотных пикообразных налетов сероватого или белого цвета, чаще имеющих творожистый, комковатый характер. Налеты снимаются легко, обнажая гладкую гиперемированную слизистую оболочку. В ряде случаев налеты могут сливаться и уплотняться. После их удаления обнажается слизистая оболочка, кровоточащая при малейшем повреждении, что очень напоминает поражение глотки при дифтерии. При язвенно-пленчатом поражении процесс, как правило, локализуется на инфильтрированных, бугристых миндалинах и распространяется на прилежащие образования. Язвы с неровными краями покрыты белым, легко снимающимся налетом. Регионарные лимфатические узлы (за- и подчелюстные) увеличиваются незначительно и мало болезненны (И. В. Чумичева, 2003).
Нередко такие поражения обнаруживаются не только в глотке, но и в других отделах дыхательного и пищеварительного трактов, что значительно ухудшает состояние больного. Исключительно тяжелым течением, сходным по симптоматике с сепсисом, отличается поражение грибками внутренних органов (В. Я. Кунельская, 1989).
Лептотрихоз глотки выражается образованием шиповидных, остроконечных, очень плотных выростов (стебельчатых пленок в виде шипов) серого или желтовато-серого цвета на поверхности неизмененной слизистой оболочки небных, язычной, глоточной миндалин, боковых валиков и гранул задней стенки глотки, а также на небных дужках. Эти выросты являются следствием ороговения плоского эпителия, отрываются с трудом, по частям и содержат клетки Leptotrix buccalis. Заболевание часто бессимптомное и длительное, иногда больные жалуются на ощущение инородного тела в глотке. Воспалительные изменения слизистой оболочки и лихорадка отсутствуют. Течение болезни упорное (В. Я. Кунельская, 1989).
Актиномикоз характеризуется образованием плотных бугристых инфильтратов темно-красного цвета (специфическая инфекционная гранулема), медленно растущих (иногда процесс проявляется в виде острой флегмоны), располагающихся чаще в области полости рта и шеи, реже в области языка, миндалин, носа и гортани. Со временем происходит нагноение опухоли, образуются абсцессы. В процесс вовлекаются окружающие ткани подбородочной области и щеки, затем опухоль может самостоятельно вскрыться с образованием свища. В содержимом можно найти желто-зеленые друзы гриба. Вследствие воспалительного отека жевательных мышц появляется их тризм; регионарная лимфаденопатия нехарактерна (М. Р. Богомильский, В. Р. Чистякова, 2001).
Кандидомикоз глотки следует отличать от дифтерии, фузоспирохетоза и поражения глотки при заболеваниях крови (В. Я. Кунельская, 1989).
Комплексный метод лечения тонзилло- и фарингомикоза включает три основополагающих принципа.
- Общее и местное использование современных противогрибковых препаратов (при этом отменяют ранее применявшиеся антибиотики).
- Восстановление нарушенного микробиоценоза кишечника.
В коррекции изменений микробиоценоза кишечника, в свою очередь, имеют значение три фактора:- нормализация химических процессов в кишечнике и борьба с условно-патогенной флорой с помощью диеты (продукты с бактерицидным действием), антибактериальные средства, интестопан, мексаформ;
- прием бактериальных препаратов, содержащих живые культуры (бифидумбактерин, колибактерин, лактобактерин);
- повышение неспецифических защитных реакций организма, способствующих формированию здоровой микрофлоры; для этого в комплексной терапии кандидоза от трех недель до трех месяцев используют эубиотики (аципол, бактисубтил, хилак-форте, линекс).
В большинстве случаев лечение фарингомикоза начинают с назначения местной терапии, а затем, при необходимости, подключают системную терапию производными азолов: флуконазол (дифлюкан, микосист, флюкостат, флюмикон) по 100 мг/сут, кетоконазол (низорал) по 200 мг/сут, а также итраконазол по 100 мг/сут и др. При этом системные препараты принимают в течение одной—трех недель от одного до трех курсов (L. L. Patton et al., 2001). Антимикотическое действие этих препаратов основано на нарушении синтеза эргостерина (микостатическое) или связывании его (микоцидное) с эргостерином — основным компонентом клеточных мембран грибов.
Препараты для местной этиотропной терапии делятся на антисептики и антимикотики. Продолжительность лечения острых форм местными антимикотиками составляет обычно две-три недели, антисептиками — несколько больше. Лечение проводят до полного исчезновения клинических проявлений, а затем продолжают еще в течение недели (H.-J. Tietz, 2002).
Антисептики с противогрибковым действием обычно назначают в форме смазываний и полосканий. Смазывания проводят 1-2% водными растворами бриллиантового зеленого или метиленового синего, нанося их на предварительно высушенную поверхность слизистой. Эти препараты широко распространены и доступны, однако по эффективности уступают антимикотикам, к ним быстро развивается устойчивость, а непрерывное их использование ведет к раздражению слизистой. Более эффективен разведенный в два-три раза раствор Люголя, 10—15% раствор буры в глицерине. Полоскания растворами марганцево-кислого калия (1:5000), 1% борной кислоты проводят два-три раза в день или после каждого приема пищи (М. Р. Богомильский, В. Р. Чистякова, 2001). Местные антисептики рекомендуется чередовать каждую неделю. Более эффективны современные антисептики — 0,12% хлоргексидина биглюконата или 0,1% раствора гексетидина, который выпускается также в виде аэрозоля. Для полосканий необходимо 10—15 мл любого из этих растворов, процедуру выполняют на протяжении 30—60 с после приема пищи дважды в день. Аэрозоль распыляют в течение 1-2 с. В отличие от полосканий с антимикотиками, растворы антисептиков нельзя глотать.
Антимикотики — полиеновые антибиотики (нистатин, леворин, амфотерицин, натамицин и др.) и имидазольные производные (флуконазол, кетоконазол, клотримазол) — назначают в виде растворов, аэрозолей, капель, обычных и жевательных таблеток. Необходимо объяснить больному, что любой препарат для местного лечения должен как можно дольше оставаться в полости рта. Таблетки нистатина следует разжевывать и долго держать кашицу во рту. При быстром проглатывании они не оказывают никакого действия на микотический процесс в глотке, так как не всасываются через кишечную стенку.
При распространенном кандидозе глотки не рекомендуют проведение оперативных вмешательств на лимфатическом глоточном кольце, промывание лакун миндалин, УВЧ- и СВЧ-терапию, паровые ингаляции, компрессы на шею, а также использование антибиотиков пенициллинового и тетрациклинового ряда (М. Р. Богомильский, В. Р. Чистякова, 2001). При лептотрихозе производят удаление, крио- или лазеродеструкцию патологических структур лишь на небных миндалинах. В случае актиномикоза назначают комплексное лечение: антибактериальную и противогрибковую терапию, йодистые препараты внутрь, широкое вскрытие, дренирование и промывание антисептиками воспалительных инфильтратов, иммунотерапию (инъекции актинолизата). В тяжелых случаях проводят рентгенотерапию.
Выработаны следующие рекомендации по профилактике орофарингеального кандидоза.
Длительность курсов антибиотикотерапии должна быть достаточной для эрадикации бактериального возбудителя, но не более. Не следует профилактически назначать антибиотики, в частности при респираторных вирусных инфекциях. При назначении повторных курсов антибиотикотерапии показано обязательное проведение сопутствующей противогрибковой терапии.
Необходим контроль за состоянием слизистой оболочки ротоглотки при лечении местными и системными кортикостероидами; при лечении бронхиальной астмы применяются небулайзеры.
Следует тщательно после каждого приема пищи полоскать рот кипяченой водой, 2-3% раствором питьевой соды, слабым раствором марганцево-кислого калия, а также чистить зубы пастами, содержащими противомикробные добавки.
Необходимо своевременно проводить лечение кариеса, периодонтита, хронического тонзиллита и других заболеваний полости рта и глотки (А. Ю. Сергеев, Ю. В. Сергеев, 2003).
По вопросам литературы обращайтесь в редакцию
И. И. Акулич, кандидат медицинских наук
А. С. Лопатин, доктор медицинских наук, профессор
ЦКБ МЦ УД Президента РФ, МоскваКак происходит заражение?
До попадания в организм человека, гельминты и простейшие проходят цикл развития в других средах или живых организмах.
- В почве при определённых условиях температуры и влажности сохраняются яйца и личинки аскарид, стронгилоид, анкилостом Человек заражается при попадании зараженной почвы через грязные руки, воду, непромытые фрукты и овощи, непосредственно с землёй.
- В живых организмах проходят циклы развития следующие гельминты: описторхи (кошачья двуустка), клонорхи, трихинеллы, токсокары, эхинококки, свиной и бычий цепень. До достижения зрелости, чтобы паразитировать в человеке, возможна смена одного или двух промежуточных хозяев. Это моллюски, ракообразные, рыба, насекомые. Употребление термически недостаточно обработанной рыбы и мяса, сырой воды приводит к заражению.
Ещё один путь заражения - при непосредственном контакте людей через рукопожатия, общие предметы гигиены и быта или путем самозаражения. Речь идёт о контагиозных гельминтах: энтеробиоз, стронгилоидоз, цистицеркоз, лямблиоз.
Как можно заподозрить паразитарное заболевание?
Проявления могут быть разнообразными, течение от легкого до тяжёлого. Редко возникают типичные признаки, выдающие конкретного возбудителя. Зачастую признаков нет, или они маскируются под другие заболевания, или исчезают по мере окончания одного цикла развития паразита и начала другого. Например, личинки аскарид сначала попадают в лёгкие человека, где дозревают и мигрируют в кишечник. Ребёнка может беспокоить недолгий кашель (похоже на простуду), не настораживающий родителя.
Тем не менее, обычно выделяют острую и хроническую фазы течения паразитарного заболевания.
Острые проявления возникают вследствие общего воздействия на организм:
- Влияния токсинов – повышение температуры до 37 – 37,5 градусов, слабость, головные боли, снижение настроения и работоспособности, нарушения сна;
- Аллергических реакций – кожный зуд, крапивница, бронхоспазм, одышка, реже отёк Квинке;
- Активации иммунной системы– боли в мышцах и суставах; увеличение лимфоузлов, печени и селезенки
- Механического воздействия – если посмотреть под микроскопом, у каждого гельминта можно увидеть приспособления для закрепления в организме, травмирующие слизистую: зубья, крючья, присоски. В результате возникают боли в животе, частый стул, диспепсия.
Хроническая фаза характеризуется поражением определённых органов и систем. Чаще всего страдает кишечник, длительное механическое воздействие приводит к его воспалению, нарушениям всасывания и переваривания пищи. Развивается анемия, недостаток витаминов и микроэлементов, а у маленьких детей отмечается задержка роста и набора веса. Могут поражаться желчный пузырь и желчевыводящие пути (лямблиоз); сердечно-сосудистая система, лёгкие, нервная система (чаще трихинеллез); лёгкие и печень (эхинококкоз) и так далее. При длительном течении подавляется иммунитет и присоединяются вторичные инфекции.
Если Вы обнаружили любой из перечисленных признаков, сдайте клинический анализ крови с лейкоцитарной формулой. Повышение эозинофилов до 7-10% и более станет ещё одним подозрительным критерием.
Как выявить паразитарное заболевание?
-
, предпочтительнее обогащающий метод – PARASEP Определяет яйца всех видов гельминтов и простейших, обитающих в кишечнике
Следует обратить внимание на следующие моменты:
На что нужно обратить внимание?
- Наличие проявлений и одновременное обнаружение IgG могут свидетельствовать о хронической фазе гельминтоза
- В сомнительных случаях рекомендовано повторное исследование IgG через 2 недели. Нарастание уровня антител в 2 раза и более говорит об активности гельминта
- При трихинеллезе, эхинококкозе, цистицеркозе определение антител – единственный возможный метод лабораторной диагностики, поскольку человек – промежуточный хозяин для данных гельминтов.
Читайте также:

