Грибковые и протозойные инфекции
Обновлено: 18.04.2024
Иммунный ответ при грибковых инфекциях. Иммунитет и грибы. Гуморальные реакции иммунитета при грибковых инфекциях. Клеточный иммунитет при грибковых инфекциях.
Грибковые клетки и их продукты — сильные иммуногены. Их распознавание иммунной системой проявляется в виде клеточных и гуморальных реакций. Многие грибковые Аг проявляют сенсибилизирующее действие, поэтому аллергический компонент — важное звено патогенеза микозов. Однако при микозах сенсибилизация не строго специфична, не отражает уровня иммунного реагирования и нередко не имеет прогностическое значение. Патогенные грибы содержат большой набор Аг.
Гуморальные реакции иммунитета при грибковых инфекциях
Большинство грибковых поражений сопровождается образованием высоких титров AT. Вид AT и нарастание концентрации отражают статус и прогрессирование инфекции. При микозах образуются высокие титры AT классов IgM, IgG и IgA; при сенсибилизирующем действии грибковых Аг дополнительно образуются IgE. Значение цитотоксического действия AT в комплементзависимом цитолизе невелика, так как комплемент непосредственно действует на грибковую клетку, активирующую его по классическому и альтернативному пути. Сложность антигенной структуры возбудителей микозов приводит к появлению значительного пула AT, не участвующих напрямую в уничтожении возбудителя и не проявляющих строгой видоспецифичности.
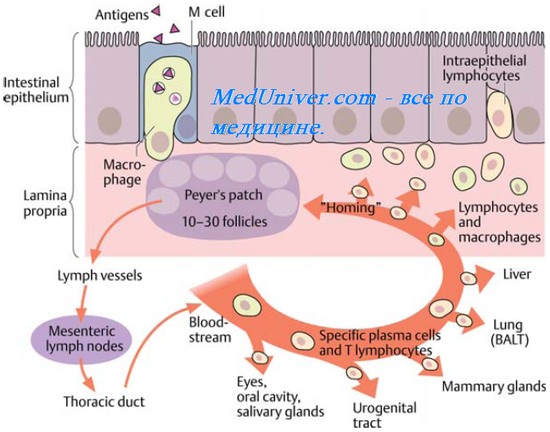
Клеточный иммунитет при грибковых инфекциях
Клеточные реакции играют основную роль в элиминации патогенных грибов. Исключая поверхностные микозы (где нет контакта между Аг и иммунокомпетентными клетками), у заражённых лиц развивается реакция ГЗТ, обнаруживаемая уже через 10-14 сут.
Предполагается, что основная роль в формировании резистентности принадлежит именно клеточным реакциям, но клинических данных, подтверждающих это положение, нет. В эксперименте показана важная роль ЦТЛ, так как их перенос сингенным реципиентам (клетки или организмы с идентичным набором Аг МНС) приводит к состоянию резистентности; участие Т-хелперов реализуется в активации клеток макрофагально-моноцитарной системы и полиморфноядерных клеток (при респираторных микозах) и стимуляции их фагоцитарной активности.
В ряде случаев иммунные реакции не только не препятствуют, но и способствуют развитию патологических реакций (гиперчувствительность, аутоиммунные поражения), что приводит к хроническому, рецидивирующему течению многих микозов.
Информация на сайте подлежит консультации лечащим врачом и не заменяет очной консультации с ним.
См. подробнее в пользовательском соглашении.
Туберкулез и сифилис ЦНС. Грибковые, протозойные инфекции ЦНС
Mycobacterium tuberculosis и Treponema pallidum являются основными причинами инфекций ЦНС.
М. tuberculosis (возбудитель туберкулеза) может инфицировать ЦНС и вызывать менингит, туберкулезные абсцессы или широко распространенный милиарный туберкулез головного и спинного мозга. Эти серьезные заболевания требуют соответствующих антибиотиков.
Сифилитический менингит и нейросифилис — проявления инфекции, вызванной Т. pallidum во время вторичного и третичного сифилиса. Нейросифилис часто сопровождается изменениями интеллекта и может принимать другие формы ментальной болезни. Во время третичного сифилиса в ЦНС могут формироваться сифилитические гуммы (области фокальной дегенерации мозговой ткани, подобно абсцессам). После диагностирования все стадии сифилиса должны быть пролечены пенициллином; после лечения пенициллином даже гуммы редуцируют.
Грибковые инфекции ЦНС
Различные грибы могут вызвать менингит и/или фокальные повреждения в головном и спинном мозге, особенно у пациентов с иммунодефицитом (например, у людей со СПИДом или у больных, получающих противоопухолевые или иммуносупрессивные средства). К таким грибам относятся С. immitis и Histoplasma capsulatum. Эти организмы напоминают М. tuberculosis, которые попадают в организм человека воздушным путем, в результате заболевание обычно поражает легкие, но может вовлекаться и ЦНС. СМЖ содержит комплементфиксированное антитело в 95% случаев концидиоидомикоза; обнаружение таких антител обусловливает начальную антимикотическую терапию. С. immitis можно обнаружить при микроскопическом исследовании СМЖ приблизительно в 50% случаев. Сопутствующие антитела менее часты при гистоплазмозе, этот диагноз зависит от выделения Н. capsulatum в культуре.
Лечение и концидиоидомикоза, и гистоплазмоза — сложный процесс, который базируется на амфотерицине В.
Протозойные инфекции ЦНС
Малярия ЦНС. Церебральная малярия, возникающая из-за инфицирования Plasmodium falciparum, — наиболее серьезная и частая инфекция ЦНС. Каждый год регистрируют около 2 млн летальных исходов в результате малярии, из которых 0,5 млн приходится на детей с церебральной малярией в Африке. Показатель смертности от этого заболевания составляет 20%, несмотря на эффективное общее лечение, которое включает хинин (или хинидин) или производные алкалоида полыни артемизина.
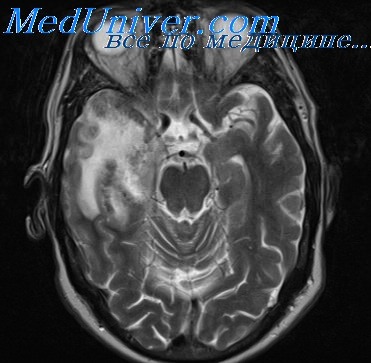
Токсоплазмоз ЦНС. Инфекции, вызванные Toxoplasma gondii, могут встречаться у пациентов с иммуносупрессией. Если иммуносупрессия не связана со СПИДом, то лишь 2-5% инфекций ЦНС обусловлено этим возбудителем, но у пациентов со СПИДом частота повышается до 25-80%. При этих состояниях часто присутствуют повреждения мозга, которые лучше выявляются с помощью МРТ. В зависимости от локализации повреждений могут быть мышечная слабость, гемипарезы и конвульсии.
Средствами выбора для лечения токсоплазмоза являются пириметамин плюс сульфонамид. Однако из-за антифолатного действия пириметамина может возникнуть депрессия костного мозга. Антифолат триметоприм при этой болезни имеет небольшое значение. Можно применять антибиотикмакролид кларитромицин.
Протозойные, паразитарные инфекции ЦНС у детей: причины, диагностика, лечение
За исключением токсоплазмоза и, в определенной степени, нейроцистицеркоза, протозойное и паразитарное поражение ликвора в развитых странах встречается редко. Малярия, однако, имеет повышенное значение из-за частых путешествий в зараженные страны и не всегда проводимой или неэффективной профилактике. В таблице ниже перечислены основные клинические особенности и доступное лечение некоторых протозойных и паразитарных заболеваний.

а) Малярия нервной системы у детей. По оценкам, не менее миллиона детей умирает от малярии только в Африке (Snow et al., 2005), и основной причиной смерти является поражение головного мозга, с пиком малярии мозга среди детей в возрасте между двумя и шестью годами. Малярию вызывают четыре разновидности рода Plasmodium-. Р. vivax, Р. falciparum, Р. malariae и Р. ovale, и тяжелым осложнением инвазии Р. falciparum является малярия мозга.
У детей данная патология определяется тремя критериями: расстройства сознания с неспособностью локализовать боль (по шкале комы Блантайра
Отличительными признаками при гистологическом исследовании являются капиллярный и венозный застой в мозге с эритроцитами, содержащими и не содержащими паразитов (MacPherson et al., 1985). Самым ранним признаком обычно является лихорадка, следующая за признаками расстройства дыхания (вторичным по отношению к метаболическому ацидозу и/или анемии), судороги и сниженный уровень сознания. Характерны двигательные расстройства и патологическая поза.
Типичные при любой форме малярии припадки могут быть генерализованными или очаговыми. Некоторые могут быть субклиническими. Они связаны с худшим исходом, особенно при продолжительности. Эпилептический статус возникает в 10-20% случаев. Гипогликемия отмечается у 30% пациентов и имеет тяжелое прогностическое значение (Molyneux et al., 1989).
Повышенное ВЧД наблюдается у большинства детей (Newton et al., 1991) с малярией мозга и считается связанным с повышением объема циркулирующей крови в мозге. Среди детей со значительно повышенным ВЧД имеется наибольший уровень смертности и более частое появление долговременных последствий.
В целом диагноз определяется анамнезом, клиническим исследованием и исследованием толстого и тонкого мазка крови. Результаты исследования ликвора обычно ничем не примечательны, а при наличии плеоцитоза более вероятным диагнозом становится менингит или энцефалит. Лечение необходимо начинать без определенных доказательств в сомнительных случаях у любых пациентов, которые в последние три месяца подвергались укусам или в течение последнего года получали профилактическое лечение (Newton и Warrell, 1998). Парентеральное назначение алкалоидов хины (хинин или хинидин в США) — основной метод лечения.
Все шире используются дериваты артемизинина (артесунат и артеметер); несмотря на более быстрое очищение крови от паразитов, они не продемонстрировали преимуществ по снижению летальных исходов по сравнению с алкалоидами хины. Их преимущество заключается в возможности ректального применения, хотя из-за обнаруженной при испытаниях на животных нейротоксичности их применение остается ограниченным. Рекомендуемая поддерживающая терапия включает жаропонижающие средства, мероприятия для устранения гиповолемии, антиконвульсанты для контроля за припадками, осмотические средства (например, маннитол) для снижения ВЧД, глюкозу при гипогликемии и переливание крови при определенных значениях анемии и, возможно, высокой периферической паразитемии (>10% пораженных эритроцитов).
В прошлом настоятельно рекомендовали применение кортикостероидов, но из-за отсутствия определенной патофизиологической основы они больше не используются. Другие вспомогательные средства, такие как десферриоксамин, малярийный гипериммунный глобулин, анти-TNFa и пентоксифиллин не показали очевидного преимущества, а некоторые из них наносили вред, поэтому до дальнейшего изучения они не должны использоваться (Warrell, 1999). Средний показатель смертности от церебральной малярии варьирует между 15% и 20% (Marsh et al., 1995, Idro и et al., 2005) с наличием остаточной инвалидности у 10-15% выживших. Некоторые последствия носят транзиторный характер, например атаксия, другие частично улучшаются через несколько месяцев (двигательные нарушения, такие как гемипарез и корковая слепота), но отдельные остаются, создавая проблемы (например, припадки). Кроме того, у многих выживших имеются незначительные когнитивные расстройства (Kihara et al., 2006).
б) Приобретенный токсоплазмоз. Инфекция Т. gondii обычно имеет легкое или бессимптомное течение, но в иммунодефицитном организме может поражать ЦНС и вызвать менингоэнцефалит, у новорожденных — энцефалит и хориоретинит, вследствие трансплацентарного инфицирования, хориоретинит в качестве первичной инфекции или внутричерепные новообразования у пациентов с ослабленным иммунитетом.

MPT: интрамуральные узелки одиночного цистицеркоза (слева, стрелка)
и множественные нейроцистицеркозные очаги (справа).
в) Нейроцистицеркоз. Нейроцистицеркоз (НЦЦ) наиболее распространенное гельминтозное заболевание ЦНС и основная проблема здравоохранения во многих развивающихся странах. Болезнь развивается в результате плохой санитарии, когда человек становится промежуточным хозяином в жизненном цикле Taenia solium, проглатывая яйца солитера. Инвазия инкапсулированной формой Т. solium может затем развиваться в пределах паренхимы мозга, базилярной цистерны или редко в спинном мозге, вызывая воспаление, отек и остаточную кальцификацию. Нейроцистицеркоз (НЦЦ) обычно проявляется у детей, когда цисты начинают отмирать и провоцировать воспаление. Среди признаков заболевания отмечают длительные очаговые/генерализованные припадки или иногда признаки повышенного внутричерепного давления, вторичного по отношению к цистицеркозному энцефалиту или гидроцефалии, вызванных кистевидными цистицерками в базилярной цистерне или желудочковой системе.
Диагностическим критерием служит выявление при сканировании мозга одиночного кольцевидного поражения с окружающим отеком или при обнаружении множественных поражений, некоторые из которых кальцифицированны. На МРТ можно обнаружить головку червя. Дифференциальная диагностика одиночных поражений от других единичных гранулем, таких как туберкулема, без биопсии затруднительна. Полезным может быть определение сывороточных антител против цистицерка, хотя в эндемичных районах исследование может привести к высокому уровню ложно-положительных результатов. Del Brutto et al. (2001) разработали набор диагностических критериев для помощи в установлении НЦЦ. Лечение альбендазолом (15 мг/кг/сут. в течение 8 дней) доказало свою эффективность, с добавлением стероидов в тяжелых случаях инвазии или при развитии побочных эффектов от лечения. Поскольку большинство пациентов обращается за медицинской помощью в результате отмирания цист, лечение уже не рекомендовалось; однако недавние исследования показали, что при использовании альбендазола уменьшается долговременный риск развития припадков (Garcia et al., 2004).
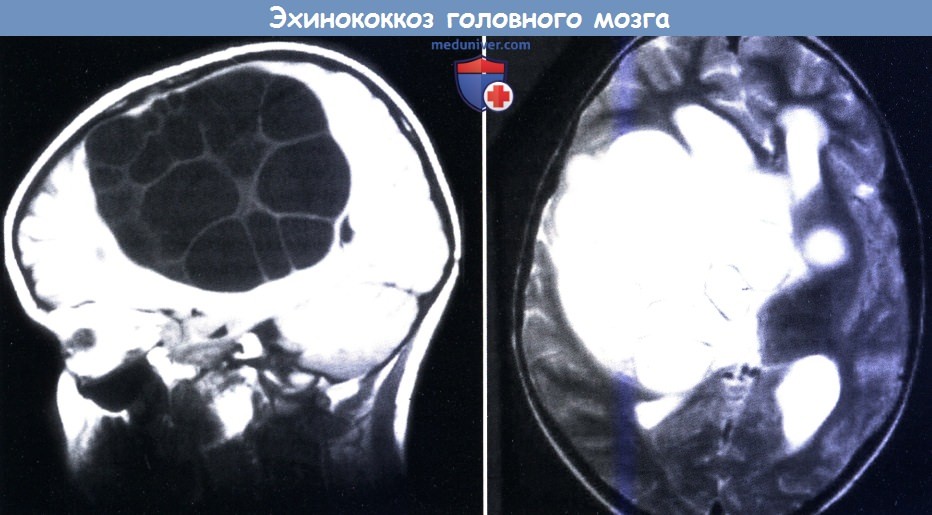
Гидатидный эхинококкоз. МРТ в Т1-режиме (слева) и Т2 (справа):
множественные кистозные повреждения после Echinococcus granulosus.
г) Эхинококкоз нервной системы. Инвазия человека солитером собаки, Echinococcus, называемая также эхинококкозом и распространенная в странах, где разводят овец. Человек заражается при заглатывании яиц, выделяемых собаками (окончательный хозяин). Echinococcus granulosus вызывает кистозный эхинококкоз, и в основном вызывает кисты в печени и легких, хотя в 5% случаев кисты развиваются и в ЦНС. Поскольку пузыри растут медленно, зачастую они остаются бессимптомными до тех пор, пока не достигнут значительных размеров. Клинические проявления в основном связаны с признаками и симптомами внутричерепной гипертензии, тогда как очаговый неврологический дефицит возникает редко.
На КТ и МРТ определяются округлые или овальные кисты с ровными контурами и содержимым, имеющим плотность ликвора. Может выявляться смещение срединных структур и желудочковая деформация (Tuzun et al., 2002). В диагностике можно использовать ИФА или РИГА (непрямая гемагглютинация) с эхинококковым антигеном. Предпочтительным лечением является осторожное хирургическое удаление, чтобы предотвратить разрыв стенки кисты. При больших повреждениях предопреционное лечение альбендазолом, видимо, улучшает исход (Altinors et al., 2000).
д) Эозинофильный менингит. Наиболее частой причиной эозинофильного менингита рассматривают паразитарное или протозойное заболевание; однако высокая доля эозинофилов (>4%) может также наблюдаться в случаях инфекционного или постинфекционного менингита, вторичного по отношению к грибковой, риккетсиозной, микоплазмозной или трепонемной инфекции, подострому склерозирующему панэнцефалиту и лимфоцитарному хориоменингиту. Эозинофилия в ликворе может также быть связана с неинфекционными расстройствами, такими как болезнь Ходжкина, рассеянный склероз, лейкемия, субарахноидальное кровоизлияние и реакция на интратекальное введение антибиотиков (Weller, 1993).
Что такое вагинальный кандидоз (молочница)? Причины возникновения, диагностику и методы лечения разберем в статье доктора Соснина А. С., гинеколога со стажем в 15 лет.
Над статьей доктора Соснина А. С. работали литературный редактор Вера Васина , научный редактор Сергей Федосов и шеф-редактор Лада Родчанина

Определение болезни. Причины заболевания
Вагинальный кандидоз (кандидозный вагинит) — поражение слизистой оболочки влагалища дрожжеподобными грибами рода Candida. В быту эту болезнь называют молочницей .
Краткое содержание статьи — в видео:
Candida — это условно-патогенные микроорганизмы, факультативные анаэробы (организмы, способные жить как в присутствии кислорода, так и без него). Они обладают тропизмом — направлением роста на клетки богатые гликогеном, в частности клетки слизистой оболочки влагалища. Самый распространённый вид возбудителя, который встречается в 70—90 % случаев, — Candida albicans.
В последние годы растёт заболеваемость кандидозом, вызванным другими представителями рода Candida. Наиболее часто выявляются:
- С. glabrata (15 %);
- C. dubliniensis (6 %);
- C. tropicalis (3—5 %);
- C. parapsilosis (3 %);
- C. krucei (1—3 %).
Распространение новых видов микроорганизмов связано в первую очередь с бесконтрольным самолечением пациенток, приводящем к возрастающей устойчивости грибов к препаратам [3] [4] .
Частота кандидозного вагинита среди инфекционных заболеваний влагалища и вульвы составляет 30—45 %. Патология занимает второе место среди всех инфекционных заболеваний влагалища и является крайне распространённым поводом для обращения женщин за медицинской помощью. По данным J. S. Bingham (1999):
- к 25 годам около 50 % женщин репродуктивного возраста сталкивались с хотя бы одним диагностированным врачом эпизодом вагинального кандидоза;
- к началу периода менопаузы — около 75 % [17] .
Кандидозный вагинит редко наблюдается в постменопаузе, за исключением тех пациенток, которые получают гормональную заместительную терапию.
Предрасполагающими факторами заболевания являются:
- Механические — ношение синтетического белья, первый половой контакт, травматическое повреждение тканей влагалища, длительное применение внутриматочной спирали.
- Физиологические — беременность, менструация.
- Эндокринные — гипотиреоз, сахарный диабет.
- Иммунодефицитные состояния.
- Ятрогенные (приём антибиотиков, кортикостероидов, иммуносупрессоров, лучевая терапия, химиотерапия, онкологические заболевания, оральные контрацептивы).
- Прочие (авитаминоз, аллергические заболевания, хронические патологии гениталий и желудочно-кишечного тракта).
Заболевание, как правило, не передаётся половым путём, но установлено, что оно связано с характером половых контактов: анально-вагинальным и орогенитальным. Также не исключается вероятность развития кандидозного баланопостита у половых партнёров пациенток с вагинальным кандидозом.
При обнаружении схожих симптомов проконсультируйтесь у врача. Не занимайтесь самолечением - это опасно для вашего здоровья!
Симптомы вагинального кандидоза
Основные симптомы при вагинальном кандидозе:
- жжение и зуд в области влагалища и вульвы;
- творожистые выделения из влагалища;
- расстройства мочеиспускания;
- боль при половом акте.
Зуд может усиливаться после водных процедур, полового акта, ночью во время сна и в период менструации [1] .
В целом симптомы вагинального кандидоза нарастают перед менструацией. При беременности проявление болезни также усугубляется, это связано со снижением иммунитета у беременных женщин.
Объективные признаки вагинального кандидоза:
- отёк и гипермия слизистой оболочки влагалища и наружных половых органов;
- белые или зеленовато-белые наложения на стенках влагалища;
- покраснение слизистой влагалища.
При осложнённом кандидозе на коже наружных половых органов появляются везикулы — пузырьки, возвышающиеся над уровнем кожи или слизистой и заполненные прозрачным или мутным содержимым, которые могут вскрываться и образовывать эрозии. При вагинальном кандидозе также могут наблюдаться трещины слизистой вульвы, задней спайки и перианальной области [2] .
Патогенез вагинального кандидоза
Грибы рода Candida относятся к условно-патогенной микрофлоре, которая присутствует как в окружающей среде, так и на поверхности кожных покровов и слизистых оболочках здорового человека (в полости рта, кишечнике, влагалище). При снижении защитных сил организма возможно повышение адгезивных свойств (способности прилипать) грибов с прикреплением их к клеткам эпителия влагалища, колонизацией слизистой оболочки и развитием воспалительной реакции [7] .
Вагинальный кандидоз зачастую затрагивает только поверхностные слои эпителия влагалища без проникновения возбудителя в более глубокие слои слизистой оболочки. Однако в редких случаях эпителиальный барьер преодолевается и происходит инвазия в подлежащую ткань с последующей гематогенной диссеминацией (распространением возбудителя инфекции из первичного очага заболевания по всему органу или организму посредством кровотока) [8] [9] .
Основные этапы патогенеза:
- Адгезия (прилипание) грибов на слизистой и колонизация.
- Инвазия (проникновение) в эпителий.
- Преодоление эпителиального барьера.
- Проникновение в соединительную ткань.
- Преодоление защитных механизмов ткани.
- Попадание в сосуды.
- Гематогенная диссеминация.
При вагинальном кандидозе воспаление происходит в верхних слоях эпителия влагалища. Причина состоит в том, что поддерживается динамическое равновесие между грибом, который не может проникнуть в более глубокие слои, и организмом, который сдерживает его распространение. Соответственно инфекция может долго развиваться в одном месте, проявляясь творожистыми выделениями из влагалища. Обострение заболевания происходит при сдвиге равновесия между развитием грибов и защитными силами организма.
Классификация и стадии развития вагинального кандидоза
Согласно национальным клиническим рекомендациям [18] , выделяют две формы вагинального кандидоза:
- острую — до трёх обострений в год;
- хроническую (рецидивирующую) — не менее четырёх обострений в год.
По классификации, предложенной D.A. Eschenbach, вагинальный кандидоз подразделяют на два типа:
У женщин различают три формы заболевания:
- вагинит (воспаление влагалища); (воспаление влагалища и вульвы); (воспаление шейки матки).
У мужчин выделяют:
- баланит (воспаление головки полового члена);
- баланопостит (воспаление крайней плоти и головки полового члена); (воспаление мочеиспускательного канала).
Для острой формы вагинального кандидоза характерны выраженные симптомы: обильные выделения из влагалища, жжение и зуд во влагалище и наружных половых органах. На фоне таких симптомов нередко снижается трудоспособность пациентки и развиваются неврозы. Острая форма вагинального кандидоза встречается наиболее часто и формируется в результате увеличения количества грибов рода Candida во влагалище на фоне снижения иммунитета пациентки.
Рецидивирующий вагинальный кандидоз — встречается у 10—15 % женщин репродуктивного возраста и проявляется четырьмя и более обострениями за год [11] .
Неосложнённая форма заболевания предполагает впервые выявленный или возникающий менее четырёх раз в год вагинальный кандидоз с умеренными проявлениями вагинита у пациенток без сопутствующих факторов риска (сахарный диабет, приём глюкокортикоидов, цитостатиков и др.).
При осложнённом вагинальном кандидозе наблюдаются яркие объективные симптомы: покраснение, отёк, образование язв, трещин слизистых оболочек и кожи перианальной области. Также характерны рецидивы четыре и более раз в год. Заболевание часто возникает на фоне сахарного диабета, ВИЧ-инфекции, терапии глюкокортикоидами и цитостатиками. Возбудителем заболевания в данном случае являются как C. albicans, так и другие грибы рода Candida.
Осложнения вагинального кандидоза
К осложнениям вагинального кандидоза у женщин относятся:
- стеноз влагалища;
- воспалительные патологии органов малого таза — сальпингит, оофорит и другие;
- заболевания мочевыделительной системы — цистит, уретрит[2] .
Стеноз влагалища развивается при воспалении стенок влагалища. При этом просвет влагалища сужается, а стенки влагалища становятся плохо растяжимы. Пациентки испытывают боль при половом акте.
Сальпингит — инфекционно-воспалительное заболевание фаллопиевой (маточной) трубы. Возникает при переходе инфекции восходящим путем из влагалища, не исключен также и гематогенный путь передачи. Сальпингит чаще всего протекает в сочетании с оофоритом — воспалением яичника. Поражение может быть как односторонним, так и двусторонним. Пациентки испытывают боль в области придатков, внизу живота слева или справа, повышается температура тела, возникает общее недомогание, слабость, а иногда и тошнота со рвотой. При несвоевременном лечении данного осложнения высок риск бесплодия, наступления внематочной беременности, возникновения спаечного процесса, приводящего к оперативному вмешательству, инфицированию органов брюшины и малого таза. Сальпингит особенно опасен в случаях, когда с кандидозом сочетаются другие инфекции [1] .
Уретрит — воспаление слизистой мочеиспускательного канала. Проявляется болезненным мочеиспусканием, чувством жжения в области уретры, выделением с мочой крови или гноя, дискомфортом при соприкосновении с бельём, слипанием краёв уретры, покраснением области вокруг мочеиспускательного канала.
Цистит — воспаление мочевого пузыря. Патология возникает при попадании возбудителя восходящим путём через уретру в мочевой пузырь. Симптомы цистита схожи с симптомами уретрита, однако есть некоторые отличия: частые позывы к мочеиспусканию при небольшом количестве мочи, чувство неполного опорожнения мочевого пузыря, боль, резь в конце мочеиспускания, помутнение мочи, повышение температуры тела, боли внизу живота.
На фоне вагинального кандидоза возрастает частота осложнений при беременности, а также увеличивается риск инфицирования плода.
Кандидоз плода может вызвать его внутриутробную гибель или приводить к преждевременным родам. После родов у женщин возможно развитие кандидозного эндометрита — воспалительного процесса в тканях, выстилающих внутреннюю полость матки.
Диагностика вагинального кандидоза
Диагностика вагинального кандидоза основывается на характерных жалобах пациентки, данных анамнеза, клинических проявлениях, выявленных при гинекологическом осмотре. В зеркалах видна гиперемия, отёк слизистой, белые налёты на стенках влагалища.
Независимо от этих признаков, подтверждение диагноза должно основываться на лабораторных данных:
- Микроскопия мазков вагинального отделяемого — позволяет выявить споры и мицелий гриба.
- Культуральный метод — посев влагалищного содержимого на искусственные питательные среды. Метод определяет количество, видовую принадлежность, чувствительность к противогрибковым препаратам, а также характер и степень заселения другими микроорганизмами. Культуральный метод дополняет микроскопию.
- Серологическая диагностика (РСК). Определяет антитела против антигенов грибов рода Candida. Такая диагностика имеет значение при генерализации процесса.
- Молекулярно-биологические методы. Направлены на обнаружение специфических фрагментов ДНК Candida spp. Применяют метод полимеразной цепной реакции (ПЦР).
- Иммунофлюоресцентная диагностика (Candida Sure Test) проводится в случае рецидивирующего течения вагинального кандидоза [15] .
К дополнительным методам диагностики относятся: изучение микробиоценоза кишечника, обследование на инфекции, передаваемые половым путём, внутривенный тест на толерантность к глюкозе [16] .
Дифференциальную диагностику проводят со следующими заболеваниями:
- генитальным герпесом; ;
- аэробным вагинитом;
- кожными заболеваниями (экземой, красным плоским лишаём, склеродермией, болезнью Бехчета и др.).
Лечение вагинального кандидоза
Показаниями к назначению терапии вагинального кандидоза являются жалобы пациентки, клинические проявления и лабораторное подтверждение наличия грибов рода Candida. Лечение не требуется при обнаружении грибов без каких-либо клинических проявлений (кандидозоносительство). Это правило обусловлено тем, что грибы рода Candida могут содержаться в небольшом количестве во влагалище и являются частью нормальной микрофлоры, если их количество не превышает пороговое значение 10 4 .
Механизм действия противогрибковых препаратов — нарушение синтеза эргостерола (вещества в составе клеточных мембран грибов), что приводит к образованию дефектов в мембране микроорганизма. В зависимости от дозы антимикотики проявляют фунгистатическое (замедление роста) или фунгицидное (полное уничтожение) действие [15] .
Существуют различные группы препаратов для лечения вагинального кандидоза:
- антибиотики (пимафуцин, амфотерицин В, нистатин, леворин);
- имидазолы (клотримазол, сертаконазол, кетоконазол, гино-певарил, миконазол);
- триазолы (итраконазол, флуконазол);
- комбинированные препараты ("Тержинан", "Полижинакс", "Пимафукорт", "Клион Д", "Макмирор комплекс");
- препараты разных групп (флуцитозин, гризеофульвин, дафнеджин, нитрофунгин, йодат поливинилпирролидон).
Лечение подбирается гинекологом индивидуально для каждой пациентки, учитывая клиническую картину, форму заболевания и степень выраженности симптомов. Но важно отметить, что при лечении молочницы при беременности флуконазол противопоказан, так как он может негативно повлиять на развитие плода [19] [20] .
При лечении острых форм вагинального кандидоза назначают местное лечение. Препарат не всасывается в системный кровоток, а действует в области влагалища и слизистой. Примеры схем лечения:
-
150 мг в виде вагинальных свечей один раз в сутки в течение трёх дней; один аппликатор крема на ночь вагинально в течение трёх дней; одна свеча на ночь один раз в сутки в течение восьми дней; одна таблетка на ночь в течение 10 дней.
При хроническом кандидозе наряду с местным лечением применяют системные антимикотики:
-
150 мг один раз внутрь; 200 мг внутрь два раза с интервалом 12 часов в течение одного дня или 200 мг в сутки в течение трёх дней.
При рецидивирующей форме заболевания (более четырёх эпизодов в год) применяют схему:
-
150 мг внутрь три раза с интервалом 72 часа в 1,4 и 7 день лечения.
Для купирования рецидивов препарат применяют в дозировке 150 мг один раз в неделю в течение шести месяцев.
В последние годы всё больше исследуется способность C. albicans формировать биоплёнки — вещества на поверхности колонии микроорганизмов, которые служат барьером для проникновения лекарственных средств и обеспечивают выживание. Основным полисахаридом, определяющим развитие резистентности к антибиотикам, является глюкан. Его рассматривают как одну из причин формирования резистентности к антимикотическим препаратам. Этим объясняется отсутствие эффекта при лечении у некоторых больных. Таким пациенткам можно порекомендовать препарат фентиконазол 600 мг в сутки с интервалом в три дня. Лекарство отличается от других способностью преодолевать биоплёнки, тем самым повышая эффективность лечения при резистентности к другим препаратам.
Прогноз. Профилактика
При своевременном обращении пациентки к врачу, лабораторном обследовании и отсутствии самолечения прогноз благоприятный. Самолечение опасно из-за риска рецидива заболевания, его хронизации и возникновения резистентности к препарату, неверно выбранному пациенткой или при неадекватной дозе.
Чтобы повысить эффективность терапии пациентки должны следовать схеме лечения, индивидуально назначенной гинекологом. Во время лечения и диспансерного наблюдения необходимо соблюдать половой покой или применять барьерные методы контрацепции. Повторно обратиться к врачу для контроля анализов следует через 7-10 дней [12] .

Протозойные заболевания или протозоозы - это заболевания, вызванные простейшими микроорганизмами. Такие инфекции могут быть системными (поражать весь организм) и кишечными (поражают желудочно-кишечный тракт).
К системным протозоозам относятся малярия, бабезиоз, лейшманиоз, токсоплазмоз, трипаносомоз.
В этой статье мы поговорим о простейших, которые поражают желудочно-кишечный тракт и вызывают кишечные инфекции.
Кишечные простейшие передаются фекально-оральным путем. Встречаются простейшие, а соответственно и инфекции, вызванные ими, по всеми миру, но наиболее широко распространены в областях с плохими санитарно-гигиеническими условиями и контролем за состоянием воды. Токсоплазмоз, кстати, тоже передается орально-фекальным путем, но при этом не поражает ЖКТ (подробнее по ссылке). Некоторые простейшие могут распространяться половым путем, например при орально-анальных контактах. Несколько разновидностей простейших вызывают тяжелые инфекции у пациентов с ВИЧ-инфекцией в продвинутой стадии.
Наиболее важными кишечными протозойными патогенами являются лямблии и амебы, криптоспоридии, бластоцисты и др.
Многие патогенные и непатогенные микроорганизмы могут находиться в кишечнике в одно и то же время. При этом инфекции, вызванные кишечными простейшими, в большинстве случаев характеризуются либо бессимптомным течением, либо стертой клинической симптоматикой. Настороженность по поводу паразитарных заболеваний имеет место при хронических диареях, кожных высыпаниях неясной этиологии, в некоторых случаях при длительно сохраняющейся эозинофилии в крови.
Постановка диагноза основывается на сборе эпидемиологического анамнеза, на выявлении симптомов и физикального обследования, а также на результатах лабораторного исследования кала на простейшие, а при наличии возможностей - на антигены возбудителей (криптопроридии, амебы, лямблии) или выявление генетического материала простейших с помощью молекулярно-генетических методов.
Микроскопический анализ кала является скрининговым методом диагностики, но может потребовать повторных исследований, методов концентрации и специальных окрашиваний. Наиболее информативным в этом плане может быть анализ трехдневного кала с применением специальных методов обогащения, с интервалом в две недели при первом отрицательном результате. Два последовательных отрицательных результата исследования кала на я/гельминтов и простейшие с интервалом в 14 дней позволяют исключить паразитарную (и глистную) инвазию, и дообследоваться в другом направлении.
Entamoeba histolytica/E. dispar .
Кишечный амебиаз распространен повсеместно, преимущественно в Центральной Америке, западной Южной Америке, Западной и Южной Африке и на индийском субконтиненте. В развитых странах большинство случаев происходит среди недавних иммигрантов и туристов, вернувшихся из эндемичных областей. Амебиаз является третьей по распространенности причиной смерти от паразитозов после малярии и шистосомоза.
Разновидностей амеб множество, но наиболее часто выявляются E.histolytica и E. dispar. Принято считать, что E.dispar непатогенна, но при ее выявлении в совокупности с клинической картиной заболевания, необходимость лечения рассматривается индивидуально.
Человек инфицируется при заглатывании цист с пищей или водой, или при оральных сексуальных контактах. После попадания в организм человека из цисты выходит трофозоит, который по мере продвижения по кишечнику может либо проникать в ткани кишечника, либо выводиться с калом (как в виде цист, так и в виде трофозоитов). Для заражения опасны только цисты.
В 90% случаев течение болезни бессимптомное. Если все же есть клиническая картина, то она может варьировать от легкой диареи до тяжелой дизентерии (боль в животе, диарея с кровью и слизью, снижение веса, повышение Т тела) и даже вызывать опасные осложнения: перфорацию кишечника, кишечные кровотечения и др. К факторам риска тяжелого течения относятся молодой возраст, беременность, лечение кортикостероидами, злокачественные новообразования, недоедание и алкоголизм, а также ВИЧ-инфекция.
Амебная инфекция может стать хронической и проявляться в виде диареи с болью в животе, слизью, метеоризмом, потерей веса. Могут обнаруживаться безболезненные, пальпируемые скопления - амебомы - по ходу толстого кишечника.
При внекишечном амебиазе наиболее часто поражается печень (абсцесс печени). Симптомы включают боль или дискомфорт в области печени, иррадиирующие в правое плечо, неустойчивую лихорадку, потливость, озноб, тошноту, рвоту, слабость и потерю веса. Абсцесс может перфорировать в поддиафрагмальное пространство, правую плевральную полость, правое легкое, перикард.
Основным методом диагностики, помимо общеклинических исследований (при которых можно обнаружить лейкоцитоз, эозинофилию, повышение СОЭ, повышение уровня трансаминаз печени и др.) является микроскопия кала. При этом 3х-кратное исследование повышает чувствительность до 95%. Чувствительностью до 100% обладают иммунохроматографические методы, основанные на выявлении антигена амеб в кале, кроме того они позволяют дифференцировать E.dispar и E.Histolytica. Так же могут использоваться молекулярно-генетические методы - ПЦР, и серологические методы - определение наличия антител к амебам, но серологические данные нельзя интерпретировать отдельно от других.
Из инструментального обследования информативным может быть колоноскопия, при которой выявляются характерные изъязвления стенки кишечника, а дальше проводится биопсия и гистологическое исследование материала, где могут быть выявлены трофозоиты амеб.
При подозрении на внекишечный амебиаз используют Р-графию органов грудной клетки, УЗИ органов брюшной полости, КТ с контрастированием или МРТ.
Лечение проводится только после лабораторного подтверждения диагноза. И оно включает в себя несколько схем последовательно применяемых противомикробных препаратов (действующих как на ткани кишечника, так и в просвете кишечника), в зависимости от тяжести заболевания, формы (кишечная или внекишечная), индивидуальной непереносимости препаратов и другого-другого-другого.
Лямблиоз не менее широко распространен - лямблии наиболее часто обнаруживаются при исследовании кала. Пути передачи те же, инфицирование происходит при проглатывании цист. После попадания в организм из цист выходит трофозоит, который паразитирует в тканях тонкой кишки, дозревает, а затем выводится в окружающую среду с калом в виде цист.
Характер клинических проявлений у человека, вероятно, зависит от ряда факторов, включая вирулентность изолята, паразитарную нагрузку и иммунный ответ хозяина. Половина переносит без симптомов, 15 процентов выделяют цисты без симптомов (бессимптомная инфекция встречается как у детей, так и у взрослых, а бессимптомное выделение кист может длиться шесть месяцев и более), 35-45% отмечают клинические симптомы острой или хронической инфекции.
Острый лямблиоз: диарея, недомогание, стеаторея, спазмы в животе и вздутие, метеоризм, тошнота, снижение веса, рвота, лихорадка, запор, крапивница. Симптомы обычно развиваются после инкубационного периода от 7 до 14 дней. Возникновение острых желудочно-кишечных симптомов в течение одной недели после контакта вряд ли может быть связано с инфекцией Giardia . Симптомы могут длиться от двух до четырех недель.
Симптомы хронического лямблиоза могут включать: жидкий стул, но обычно не диарея, стеаторея, потеря веса (от 10 до 20 процентов веса тела), мальабсорбция, задержка роста, недомогание, усталость, депрессия, спазмы в животе, метеоризм, отрыжка. Проявления могут усиливаться и уменьшаться в течение многих месяцев.
Нарушение всасывания может быть причиной значительной потери веса, которая может возникнуть при лямблиозе. Даже в случаях бессимптомной инфекции может возникнуть нарушение всасывания жиров, сахаров, углеводов и витаминов. Это может привести к гипоальбуминемии и дефициту витаминов A, B12 и фолиевой кислоты. Приобретенная непереносимость лактозы встречается примерно у 40 процентов пациентов - клинически это проявляется обострением кишечных симптомов после употребления молочных продуктов. Восстановление может занять много недель даже после избавления от паразита.
Осложнения: мальабсорбция, потеря веса, у путешественников длительная диарея, у детей может привести к задержке роста. Редко - сыпь, крапивница, афтозные язвы и реактивный артрит или синовит, холецистит, холангит или гранулематозный гепатит. При этом лямблиоз не ассоциирован со смертностью даже у иммунокомпрометированных лиц.
Диагностика основана на обнаружении простейших (трофозоитов или цист) при микроскопии кала, на выявлении антигена лямблий в кале иммунохроматографическими методами, обнаружении генетического материала методом ПЦР. При подозрении на лямблиоз и получении 5 негативных результата исследования кала необходимо рассмотреть возможность исследования дуоденального содержимого. Стоит помнить, что на обнаружение паразита могут влиять прием антибактериальных, антацидных препаратов, а также обследования с использованием контрастных веществ.
Лечение проводится только при лабораторном подтверждении диагноза и при наличии клинических проявлений заболевания, лечение бессимптомных носителей осуществляется в случае, если они контактируют с беременными, с больными муковисцидозом, если это дети, посещающие ДДО или работники пищевой промышленности.
Спорообразующие простейшие (Cryptosporidium parvum, Isospora belli, Cyclospora cayetanensis, Mycrosporidia)
Жизненный цикл для всех спорообразующих простейших одинаков и начинается после проглатывания спор, из которых в тонком кишечнике высвобождаются спорозоиты и начинают активно размножаться в энтероцитах, а затем способствуют развитию новых спор, выделяющихся с калом после гибели энтероцитов. При паразитировании данных микроорганизмов значительно страдает архитектоника ворсинок, что нарушает всасывание.
Из всех спорообразующих наиболее изучены криптоспоридии - о них и пойдет речь.
Путь передачи - фекально-оральный, инфицирование при проглатывании цист с водой, пищей, от человека к человеку, от животных к человеку. Факторами риска тяжелого течения могут быть ВИЧ-инфекция, трансплантация органов, дефицит IgA, гипогаммаглобулинемия и прием иммунодепрессантов.
В 30% случаев встречается бессимптомное течение. У пациентов, у которых развиваются симптомы, инкубационный период обычно составляет от 7 до 10 дней (от 2 до 28 дней). Диарея, связанная с криптоспоридиозом, может быть острой или хронической, кратковременной, прерывистой или непрерывной, скудной или обильной, с водянистым стулом до 25 л/день. Часто пациенты отмечают недомогание, тошноту и анорексию, спастические боли в животе и субфебрильную температуру. У иммунокомпетентных людей болезнь обычно проходит без лечения в течение 10–14 дней, хотя может сохраняться дольше или рецидивировать после первоначального улучшения. У людей с ослабленным иммунитетом криптоспоридиоз может стать хроническим изнурительным заболеванием с постоянной диареей и значительным истощением. Наиболее подвержены риску люди, живущие с ВИЧ, не принимающие антиретровирусную терапию и имеющие низкий уровень СД4+ менее 100-50кл/мкл.
Диагностика основана на выявлении микроорганизмов при микроскопии кала, выявлении их генетического материала методом ПЦР, обнаружение антигенов криптоспоридий в фекалиях, гистологическом исследовании биоптатов слизистой оболочки кишечника.
Если пациент с иммунодефицитом, то лечение может вызвать некоторые трудности - чаще это длительная, комбинированная терапия, которая может не дать желаемых результатов. При наличии ВИЧ-инфекции у пациента следует незамедлительно начать антиретровирусную терапию, в некоторых случаев этого бывает достаточно, но все же иногда необходимо добавить и противопаразитарные препараты.
У иммунокомпетентных лиц лечение криптоспоридиоза не требуется, если только клинические проявления не длятся более двух недель.
Распространен повсеместно. Фекально-оральный путь передачи. У людей паразитирует в толстом кишечнике, чаще встречается у пациентов с ВИЧ-инфекцией. Патогенез развития заболевания изучен не до конца. Вопрос о том, действительно ли этот паразит является патогеном для человека, остается спорным. Выделение этого паразита с диареей у пациентов с трансплантацией почек и другими иммунодефицитами коррелирует, но практически не связано со смертностью. У людей с ВИЧ-инфекцией и бластоцистозом симптомы исчезают самопроизвольно или подтверждается другая их этиология.
Клинические проявления при бластоцистозе могут включать: диарею, тошноту, анорексию, спазмы в животе, вздутие живота, метеоризм, крапивницу и усталость. Обычно описывается водянистая диарея (может быть острой или хронической). Лихорадка обычно отсутствует.
Диагностика - микроскопия и ПЦР-исследование кала, а также культуральные методы.
Пациенты с обнаруженными бластоцистами в кале и без клинических проявлений не нуждаются в лечении. Если все же есть клинические проявления, то необходимо исключить другую их этиологию, и только в случае исключения другой этиологии рассматривается вопрос о лечение.
Балантидиаз человека наиболее распространен в тропических и субтропических регионах и развивающихся странах. Путь передачи фекально-оральный, при заглатывании цист при употреблении зараженной пищи или воды. Источником инфекции являются свиньи. Эксцистация происходит в тонкой кишке, паразит колонизирует подвздошную и толстую кишки, могут проникать в ткани, цисты формируются в просвете кишечника и выделяются с калом.
Большинство случаев протекает бессимптомно. Риск развития симптомов увеличивается при сопутствующей инфекционной патологии. Симптомы могут включать тошноту, рвоту, потерю веса, боль в животе и заметную диарею с примесью крови. Фульминантное течение заболевания с перфорацией кишечника возникает редко.
Диагноз инфекции B. coli устанавливается путем обнаружения трофозоитов или цист при исследовании кала или соскобах слизистой оболочки, полученных при колоноскопии или ректороманоскопии.
Оптимальный подход к лечению балантидиаза неясен. В целом, лечение целесообразно при симптоматическом течении инфекции. Если симптомы не исчезают после проведенной терапии, необходимо повторить исследование кала для исключения другой этиологии.
Ранее считалась комменсалом. Путь передачи фекально-оральный, инфекция ассоциирована с энтеробиозом.
Инфекция может быть симптоматической или бессимптомной. Общие симптомы включают боль в животе, острую и рецидивирующую диарею, тошноту, рвоту, метеоризм. D. fragilis может проявляться периферической эозинофилией и/или эозинофильным колитом. Диарея обычно длится 1-2 недели, тогда как боль в животе может сохраняться в течение 1-2 месяцев. Из-за очень высокой связи с острицами у некоторых пациентов также может проявляться анальный зуд, инфекции нижних мочевыводящих путей.
Диагноз ставится путем обнаружения трофозоитов при микроскопии образцов стула или с помощью молекулярно-генетических методов.
У бессимптомного человека обычно не требует лечения, но инфекции, вызванные D. fragilis, следует лечить, если организм обнаруживается как единственный патоген в образцах стула пациентов с абдоминальной болью или диареей более 1 недели.
Несколько непатогенных простейших обитают в кишечном тракте и могут быть идентифицированы в образцах стула, отправленных в клиническую лабораторию для исследования яиц и паразитов. Поскольку диагностическая лаборатория может сообщить об этих непатогенных паразитах, важно уметь различать организмы, требующие лечения, и организмы, которые этого не требуют.
Непатогенные простейшие можно разделить на две группы: амебы и жгутиковые.
Читайте также:

