Губчатый энцефалит животных это
Обновлено: 22.04.2024
BSE эпизоотической повлияло на Великобританию , и в меньшей степени , несколько других стран, в период между 1986 и 2000 - х годов, инфицировано более 190000 животных, не считая тех, кто не был бы поставлен диагноз. Это коровье бешенство уходит корнями в использование для кормления крупного рогатого скота муки , получаемой из неизрасходованных частей туш крупного рогатого скота и туш животных. Эпидемия приняла особый оборот, когда в начале 1996 года ученые осознали, что болезнь может передаваться людям через употребление мясных продуктов. В 2016 году болезнь унесла жизни 231 человека, страдающего симптомами, похожими на болезнь Крейтцфельдта-Якоба, болезнь, похожую на BSE.
После официального заявления правительства Соединенного Королевства от 21 марта 1996 года о передаче болезни крупного рогатого скота людям средства массовой информации быстро охватили это дело и передали его широкой общественности, что породило беспрецедентный кризис. Этот кризис был как этическим, так как осознание потребителями определенных общепринятых практик селекции, которые до тех пор игнорировались ими, например, использование животной муки в пищу, и экономического из-за последовавшего за этим падения потребления говядины и стоимости выращивания приняты различные меры.
В настоящее время лекарства от этой болезни нет, и ее можно остановить только профилактическими мерами .

Резюме
Эпидемиология
Заболевание впервые было выявлено в Великобритании в 1986 году .
Симптомы
ГЭКРС поражает головной и спинной мозг крупного рогатого скота. Он вызывает повреждение мозга, характеризующееся губчатыми изменениями, видимыми под оптическим микроскопом, соответствующими вакуолизированным нейронам. Происходит более или менее важная потеря нейронов и умножение астроцитов , клеток мозга с иммунной функцией. Патогены группируются вместе, образуя характерные амилоидные бляшки , хотя и в меньшей степени, чем при других трансмиссивных губчатых энцефалопатиях. Внешние симптомы обычно появляются через 4–5 лет после заражения и всегда у животных старше 2 лет (обычно от 3 до 7 лет). Первоначально они проявляются в изменении поведения животного, которое иногда может пинаться, проявлять опасения и повышенную чувствительность к внешним раздражителям (шум, прикосновение, ослепление) и изолироваться от остального стада. У пораженного животного обычно наблюдается снижение надоев молока и веса, при этом его аппетит не снижается. Курс может длиться от недели до года, при этом разные фазы заболевания имеют разную продолжительность от одного животного к другому. На завершающем этапе эволюции у животного наблюдаются настоящие нарушения опорно-двигательного аппарата. Он часто теряет равновесие, иногда не может встать. С физиологической точки зрения наблюдается тахикардия и отсутствие лихорадки. Однако появление этих симптомов не может быть уверенным в обнаружении случая BSE. Это связано с тем, что опорно-двигательные расстройства, такие как травяная тетания , распространены у крупного рогатого скота, и поэтому диагностика заболевания затруднена.
Нетрадиционный возбудитель
Обсуждается реальная природа возбудителя инфекции. Теория, в настоящее время широко принятая научным сообществом, - это теория приона , белка, который в случае болезни принимает аномальную конформацию, которая может передаваться другим здоровым прионным белкам. Альтернативной теорией является вирусный агент, который легче объяснил бы способность агента генерировать несколько штаммов. [исх. требуется] Прион ( PRoteinasceous Infectious ONly ) представляет собой сиалогликопротеин из 253 аминокислот. Сиалогликопротеины участвуют в адгезии клеток . Это так называемая устойчивая форма этого белка, которая вызывает заболевание. Эта форма отличается от нормальной формы только своей конформацией, что делает ее особенно гидрофобной , что объясняет образование агрегатов, устойчивых к протеазам, и накопление инфекционного белка в клетке. Модифицированный белок проникает в клетку посредством эндоцитоза или через специфический рецептор нормального приона, белок LRP ( белок рецептора ламинина ), который, по-видимому, вмешивается в процесс, поскольку его концентрация увеличивается с загрязнением. Как только аномальный белок попадает в клетку, он превращает нормальные прионы в устойчивые. Поскольку протеазы больше не могут их разрушать, эти белки накапливаются и в конечном итоге вызывают гибель нейрона и, таким образом, образование амилоидных бляшек . Поскольку прион является белком, он не имеет собственного метаболизма и поэтому устойчив к замораживанию, высыханию и нагреванию при обычных температурах приготовления, даже тех, которые используются для пастеризации и стерилизации . Действительно, для разрушения прион необходимо нагреть до температуры 133 ° C в течение 20 минут при давлении 3 бара.
Истоки эпидемии

На самом деле неизвестно, как появился возбудитель BSE. Преобладают две гипотезы.
Первый - это межвидовое заражение от родственной болезни - скрейпи овец . Эта возможность была экспериментально доказана, но клинические и невропатологические расстройства в этих двух случаях различаются. Это наблюдение привело ко второй гипотезе, согласно которой заболевание будет эндемичным для крупного рогатого скота и будет очень мало распространено до того, как оно было распространено в середине 1980-х годов. В ветеринарном журнале за 1883 год описан случай скрепи у крупного рогатого скота. аргумент, используемый защитниками этой теории, хотя этот случай мог соответствовать совершенно другому неврологическому заболеванию.
Регулярно обсуждаются другие более или менее достоверные или обсуждаемые теории. Так :
Возможно, мы никогда не узнаем наверняка, как и когда именно появился патоген, ответственный за заболевание, но, что касается его циркуляции, переработка туш животных рендерерами, кажется, находится под вопросом. Части костей и мяса, не употребляемые в пищу людьми ; мертвые животные, собранные на ферме при оказании услуг, составляют основные отходы мясной промышленности; они отделяются от жира путем варки, а затем превращаются в муку. До появления BSE животная мука широко использовалась для кормления крупного рогатого скота и других животных, поскольку она энергетична, богата минералами и белками и хорошо усваивается жвачими животными. Поэтому они широко использовались при разведении крупного рогатого скота, особенно молочных коров . Это потребление скотом животной муки, полученной из кальцинированных тканей крупного рогатого скота или овцы (в зависимости от принятой гипотезы), такой как головной и спинной мозг , и загрязненной агентом BSE, что, вероятно, является причиной начала эпидемии.
Первоначально эта мука стерилизовалась при высоких температурах, и стадия экстракции жира органическими растворителями позволяла, даже если никто не подозревал об этом, уничтожить любые патогенные прионы. Но в 1981 году были снижены температуры стерилизации и исключен этап экстракции жирным растворителем. Это упрощение протокола было направлено на повышение рентабельности сектора, с одной стороны, за счет лучшего сохранения белков, содержащихся в муке, с другой стороны, за счет сокращения закупок растворителей и энергии, затраты на которые значительно выросли после два нефтяных кризиса на 1973 и 1979 . Кроме того, авария, связанная с обращением с растворителем на одном из основных английских заводов по производству муки для животных, привела к усилению мер безопасности, стоимость которых была высокой, что также способствовало изменению практики, которое, по всей видимости, вызвало эпидемию . Затем прион можно было распространить в муке для животных в больших масштабах через корм для животных, а зараженные и забитые животные, в свою очередь, были переведены на муку, что усугубило это явление.
Также подозревается путь заражения от матери к детенышу. Это может составлять до 10% загрязнений.
Случай NAIF и сохранение эпидемии BSE
Чтобы объяснить эти случаи и тихое преследование зоонозов, несмотря на драконовские меры (много раз после запрета на еду для животных во Франции в 1990 году и многочисленных мер контроля), ищется возможный третий путь заражения, но он еще не найден. Среди редких заслуживающих доверия гипотез можно выделить:
Передача инфекции
В людях
Существует форма подострых трансмиссивных губчатых энцефалопатий (TSE) , специфичные для человека , известным как болезнь Крейтцфельда-Якоб (БАЯ) , который является дегенерацией из центральной нервной системы , характеризуемой наращивание в прионе . Инкубационный период исчисляется годами или даже десятилетиями до появления нарушений баланса и чувствительности , за которыми следует слабоумие . Примерно через год результат является систематическим летальным исходом. Это заболевание имеет несколько причин: большинство случаев считается спорадическим, поскольку происхождение неизвестно. Существует также наследственная передача (10% случаев) и ятрогенные инфекции ( т.е. из-за оперативного процесса), связанные с использованием гормона (как в случае с гормоном роста во Франции ) или трансплантатов церебральных тканей ( твердой мозговой оболочки ) из трупы пациентов или при использовании плохо обеззараженных хирургических инструментов (электродов).
По оценкам, в 2016 году от этой болезни погиб 231 человек, в том числе 178 в Великобритании , 27 во Франции , 5 в Испании , 4 в Ирландии и США , 3 в Нидерландах и Италии, 2 в Португалии и Канаде, и по одному в Японии , Тайване и Саудовской Аравии . Мы действительно не знаем, сколько жертв в конечном итоге заболеет этой болезнью, потому что инкубационный период у людей варьируется и плохо изучен.
Другим домашним животным

Когда болезнь впервые появилась, ее часто приписывали овцам из-за ее сходства со скрепи. Сегодня эта гипотеза потеряла часть своего авторитета. Однако, если точное происхождение заболевания неизвестно, остается уверенным, что оно имеет сильную склонность преодолевать видовой барьер. С мая 1990 года эпидемия распространилась на кошачьих после смерти домашней кошки, ставшей жертвой болезни, вероятно, зараженной пищей, причем корм для кошек очень часто готовили из коровьих субпродуктов. BSE заразил антилоп и других диких жвачных животных в британских зоопарках, а также ряд плотоядных животных: львов , тигров , пум , гепардов . Он также легко передается на другие виды диких полорогих , таких как зубр . Мы смогли экспериментально наблюдать возможную передачу вируса другим млекопитающим , включая мышей , свиней и некоторых обезьян , однако с использованием очень инвазивных методов (инъекции в мозг).
Французское агентство по безопасности пищевых продуктов ( AFSSA ) , опубликованное в марте 2005 года мнение окончательно подтвердив риск BSE в мелких жвачных животных ( козы и овцы ). У этих двух видов риск передачи вируса человеку может быть выше, потому что, помимо мяса, может быть заражено молоко. Afssa считает принятые меры предосторожности недостаточными; молоко из подозреваемых стад не проверяется, и исследуется только часть трупов подозреваемых животных .
С другой стороны, определенное количество видов кажется нечувствительным к болезни. Это особенно верно в отношении птиц , которые не страдают от TSE, вероятно, из-за их короткой продолжительности жизни. Собаку , то кролик , то лошадь и рыба не страдают от этого типа неврологических заболеваний.
Последствия и кризис
Передаваемая средствами массовой информации информация о рисках для здоровья человека, связанных с этим заболеванием, приводит к быстрому падению потребления мяса, что является причиной серьезных экономических трудностей в мясной отрасли. Помимо падения потребления, игроки этого сектора несут расходы, связанные с искоренением болезни. Таким образом, животноводы понесли большие потери из-за систематического забоя своих стад, а бойням и предприятиям вторичной переработки пришлось адаптироваться к новому законодательству.
Болезнь Крейтцфельдта-Якоба — редко встречающееся дегенеративное заболевание головного мозга, связанное с накоплением в нейронах патологического белка приона. Клинически болезнь Крейтцфельдта-Якоба проявляется слабоумием, пирамидными и экстрапирамидными нарушениями, миоклониями, симптомами поражения мозжечка и нарушением зрения. Диагноз болезни Крейтцфельдта-Якоба основывается на совокупности клинических симптомов, данных ЭЭГ, анализа цереброспинальной жидкости, МРТ и ПЭТ головного мозга, а также морфологического исследования образца тканей мозга, полученного в результате биопсии или посмертно. Эффективное лечение болезни Крейтцфельдта-Якоба пока не найдено. Заболевание имеет 100% летальный исход.
МКБ-10
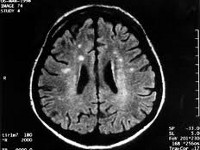
Общие сведения

Причины
Установлено, что болезнь Крейтцфельдта-Якоба имеет инфекционный характер. Заражение может произойти при пересадке зараженных прионами тканей, через нейрохирургический инструмент и препараты крови, при введении некоторых гормональных препаратов (человеческого гонадотропина для лечения бесплодия и соматотропина для терапии гипопитуитаризма). Болезнь Крейтцфельдта-Якоба новой формы может развиваться после употребления в пищу мяса заболевших животных (коровы) или носителей инфекции (овец и коз).
В результате ряда исследований стало известно, что болезнь Крейтцфельдта-Якоба связана с проникновением в организм инфекционного белка — приона. В норме в клетках головного мозга человека содержится здоровый прион, имеющий несколько другое строение. Инфекционный прион, попадая в организм человека не разрушается, а с током крови поступает в головной мозг и откладывается на поверхности нейронов. Его взаимодействие с нормальными прионами мозговой клетки приводит к тому, что они изменяют свою структуру, постепенно трансформируясь в патогенную, подобную инфекционному приону, форму. Патогенные прионы образуют бляшки и приводят к гибели нейрона.
Болезнь Крейтцфельдта-Якоба имеет достаточно длительный инкубационный период, связанный с временем, необходимым для проникновения инфекционных прионов в мозговую ткань и патогенной трансформации здоровых прионов. Длительность инкубационного периода напрямую зависит от способа заражения. При инфицировании тканей головного мозга зараженным хирургическим инструментом болезнь Крейтцфельдта-Якоба развивается через 15-20 месяцев. При инфицировании через имплантированные в околомозговые структуры ткани (например, твердую мозговую оболочку, роговицу глаза) инкубационный период может длиться до 5,5 лет. При внутримышечном введении инфицированных лекарственных препаратов (например, гонадотропина, соматотропина, содержащих бычий тромбин гемостатиков) болезнь Крейтцфельдта-Якоба начинает проявляться спустя 12,5 лет.
Отмечаются также наследственные формы болезни Крейтцфельдта-Якоба, связанные с генетическими нарушениями, приводящими к образованию патологических прионов.
Классификация
Практическая неврология классифицирует болезнь Крейтцфельдта-Якоба с учетом ее клинической формы. В соответствии с этим выделяют: подострую спонгиоформную энцефалопатию, отличающуюся быстрым течением и диффузным поражением мозговой коры; классическую (дискинетическую) форму, представляющую собой сочетание пирамидных и экстрапирамидных симптомов со слабоумием (деменцией); промежуточную форму болезни Крейтцфельдта — Якоба, характеризующуюся преобладанием мозжечковых и подкорковых расстройств; амиотрофическую форму, двигательные и речевые расстройства при которой напоминают клинику бокового амиотрофического склероза.
Симптомы болезни Крейтцфельдта-Якоба
В большинстве случаев болезнь Крейтцфельдта-Якоба характеризуется постепенным развитием, однако возможно подострое или острое начало. Примерно в 30% случаев болезнь Крейтцфельдта-Якоба начинается с продромальных симптомов: раздражительности, рассеянности, головных болей, нарушений сна, головокружения, ухудшения памяти, снижения зрения, безынициативности, снижения либидо, изменения поведенческих реакций. Возможно эпизодическое возникновение эйфории и/или беспричинного страха, отрывистые бредовые или галлюцинаторные переживания. Из неврологических нарушений в продромальном периоде наблюдаются: шаткость во время ходьбы, парестезии, расстройство высших функций коры головного мозга (алексия, акалькулия и пр.). Описаны несколько случаев, когда болезнь Крейтцфельдта-Якоба дебютировала с появления корковой слепоты.
В стадии развернутых клинических проявлений болезнь Крейтцфельдта-Якоба характеризуется прогрессирующим спастическим параличем (параплегией или гемиплегией), атаксией, эпилептическими припадками. Возникают экстрапирамидные нарушения: мышечная ригидность, атетоз, тремор. Практически у всех больных наблюдаются миоклонии — быстрые неритмичные сокращения отдельных мышц. Чаще всего отмечается миоклонус губы и века. Наблюдаются вторично генерализованные миоклонические приступы. Появляется и нарастает ярко выраженная деменция, сопровождающаяся нарушениями речи вплоть до ее полного распада. Новый вариант болезни Крейтцфельдта-Якоба отличается преобладанием психиатрической симптоматики и расстройств чувствительности. В 100% случаев он сопровождается мозжечковыми нарушениями, в то время как при спорадической болезни Крейтцфельдта-Якоба расстройства функции мозжечка наблюдаются лишь в 40% случаев.
В терминальной стадии болезнь Крейтцфельдта-Якоба характеризуется глубокой деменцией. Пациенты не контактны, находятся в состоянии прострации, утрачен контроль над функцией тазовых органов. Наблюдаются гиперкинезы, выраженные мышечные атрофии, нарушения глотания, пролежни. Возможна гипертермия и эпилептические приступы. Смерть наступает в коматозном состоянии на фоне децеребрационной ригидности и выраженной кахексии.
Диагностика
Клиническая диагностика заболевания основана на сочетании прогрессирующей в течение 2-х лет деменции, пирамидных и экстрапирамидных расстройств, миоклоний, мозжечковых расстройств и нарушений зрения. Для уточнения диагноза невролог назначает инструментальные методы обследования: электроэнцефалографию (ЭЭГ), ПЭТ и МРТ головного мозга, люмбальную пункцию. В сомнительных случаях для установления диагноза болезнь Крейтцфельдта-Якоба производят стереотаксическую биопсию головного мозга.
На ЭЭГ на фоне сниженной биоэлектрической активности у большинства больных наблюдаются периодические или псевдопериодические острые волны. Отмечается билатеральная, фокальная или генерализованная миоклоническая активность, которая в начальной стадии определяется у половины больных, а в терминальной стадии выявляется в 100% случаев спорадической болезни Крейтцфельдта-Якоба. Новый вариант заболевания часто протекает без существенных изменений ЭЭГ-паттерна.
Люмбальная пункция в обязательном порядке проводится пациентам с подозрением на болезнь Крейтцфельдта-Якоба. Она позволяет оценить давление ликвора и произвести исследование цереброспинальной жидкости. Отсутствие патологических изменений ликвора позволяет дифференцировать болезнь Крейтцфельдта-Якоба от многих других заболеваний ЦНС.
Наиболее достоверным методом диагностики является морфологическое исследование образцов мозговой ткани, которые могут быть получены прижизненно путем биопсии или при аутопсии после смерти пациента. Применение иммуноцитохимического метода позволяет обнаружить в исследуемом материале отложения патологического белка — приона.
Дифференциальная диагностика
Дифференциальную диагностику болезни Крейтцфельдта-Якоба необходимо проводить с лобно-височной деменцией, герпевирусным энцефалитом, болезнью Альцгеймера, мультиинфарктной деменцией (слабоумием, развивающимся после повторных ишемических и геморрагических инсультов), хроническим менингитом, арахноидитом, нормотензивной гидроцефалией, энцефалопатией Хашимото, сопровождающей некоторые случаи аутоиммунного тиреоидита, и др.
Лечение болезни Крейтцфельдта-Якоба
В современной медицине подходы к лечению болезни Крейтцфельдта-Якоба находятся в стадии активной разработки. Общепринятые противовирусные препараты, а также пассивная иммунизация и вакцинация людей и животных выявились неэффективными. Отмечено, что блокирующее действие на синтез патологических прионов в инфицированных нейронах оказывает Брефелдин А, а блокаторы кальциевых каналов продлевают жизнь инфицированных клеток. Обычно пациенты, имеющие болезнь Крейтцфельдта-Якоба, получают симптоматическое лечение. Оно направлено на купирование миоклонических приступов и экстрапирамидных нарушений, в связи с чем применяются антиэпилептические и противопаркинсонические лекарственные средства.
Прогноз болезни Крейтцфельдта-Якоба
Болезнь Крейтцфельдта-Якоба является фатальным заболеванием. Продолжительность жизни большинства больных не превышает 1 год с момента начала клинических проявлений; а средняя длительность составляет 8 месяцев. Лишь 5-10% заболевших живут в течение 2 и более лет. Наследственная болезнь Крейтцфельдта-Якоба в среднем длится около 26 месяцев.

Прионные болезни - группа нейродегенеративных заболеваний человека и животных, этиологически связанных с особым инфекционным белком - прионом. Эти заболевания характеризуются тяжелым прогрессирующим течением и неизбежным смертельным исходом.
А теперь немного истории.
Впервые термин "спонгиозная (губкообразная, губчатая) энцефалопатия" был применен в 1957 году исландским ученым Б. Сигурдссоном при описании заболеваний овец на острове Исландия, которые отличались от всех известных заболеваний четырьмя признаками: необычно продолжительным (до нескольких лет) инкубационным периодом; медленно прогрессирующим (месяцы и годы) характером течения; необычностью поражения органов и тканей; неизбежным смертельным исходом. Б. Сигурдссон объединил такие заболевания под общим названием "медленные инфекции".
Три года спустя впервые было описано куру - неизвестное ранее заболевание, встречающееся у дикарей с привычками ритуального каннибализма на острове Новая Гвинея, проявляющееся нарушением координации движений и дрожанием. Клиническая и патологоанатомическая симптоматика куру у людей была сходна с таковой при болезни овец, известной с 1700 года - скрепи. В 1966 году Гайдушеком на обезьянах (шимпанзе) была доказана инфекционная природа куру. В 1967 году исследователями были опубликовали данные, согласно которым в мозге зараженных вирусом куру шимпанзе были обнаружены: "губчатость" серого вещества головного мозга, увеличение числа вспомогательных клеток (астроглии), гибель нейронов в ряде отделов мозга.Эти морфологические признаки (с определенными вариациями) характерны для всех прионных болезней человека и животных.
В дальнейшем губкообразная энцефалопатия была обнаружена у людей, страдающих болезнью Крейтцфельда-Якоба, синдромом Герстманна-Штреусслера, фатальной семейной бессонницей. В конце прошлого столетия эксперты ВОЗ прогнозировали возможность значительной эпидемии нового варианта болезни Крейтцфельда-Якоба в ближайшие 10 лет. Но в последние 5 лет, к счастью, наметилась явная тенденция к снижению прироста заболевания.
Большую загадку и, соответственно, интерес представляет тот факт, что некоторые варианты прионных болезней могут иметь инфекционную природу (например, вызываются пересадкой твердой мозговой оболочки или применением экстрактов тканей, содержащих гормон роста и гонадотропин), другие - имеют наследственный характер, а третьи никак не связаны ни с наследственностью, ни с инфекционной передачей.
Во всех случаях виновником заболеваний является собственный дефектный белок - прионный белок, который превращается в инфекционный аналог - прион. Прион как бы "заставляет" окружающие его нормальные молекулы прионного белка принимать патологическую форму, и этот процесс носит характер цепной реакции. По меткому выражению профессора Стэнли Прузинера, "доктор Джекил превращается в мистера Хайда". Дефектный прионный белок обладает аномальными свойствами, он контагиозен и фатален для любых близлежащих нейронов.
Профессор С. Прузинер получил в 1997 году Нобелевскую премию по физиологии и медицине за доказательство существования нового биологического инфекционного агента - приона, не содержащего ДНК или РНК, способного переносить информацию и преодолевать видовой барьер.
В настоящее время унифицированы диагностические критерии прионных болезней, ведется работа по их выявлению и изучению. Достижения молекулярной биологии последних лет дают надежду глубже понять причину болезни и механизмы патологической трансформации прионного белка и, главное, - найти эффективные средства для лечения этих смертельных заболеваний. Предварительные результаты экспериментальных исследований на клеточных культурах весьма обнадеживающи, и не исключено, что некоторые "антиприонные" соединения могут в ближайшие 5 лет стать объектом первых клинических испытаний.
Клещевой энцефалит – инфекционное заболевание, в основе которого лежит повреждение головного и спинного мозга флавивирусом, передающимся человеку при укусах иксодовых клещей. В зависимости от формы болезни его проявлениями являются лихорадка, головная боль, судороги, рвота, нарушение координации движений, боли по ходу нервов, вялые парезы и параличи. Диагноз подтверждается с помощью ПЦР крови и спинномозговой жидкости. Лечение на ранних сроках заболевания заключается в назначении иммуноглобулина против клещевого энцефалита, противовирусных препаратов. На поздних сроках возможно только предотвращение жизнеугрожающих состояний и симптоматическое лечение.
МКБ-10
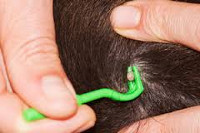
Общие сведения
Клещевой энцефалит (весенне-летний клещевой менингоэнцефалит) представляет собой вирусное заболевание (вирусный энцефалит), которое передается человеку через укусы иксодовых клещей, характеризуется поражением головного и спинного мозга. Основной зоной его распространения является Сибирь, Дальний Восток, Китай, Монголия. Однако вспышки заболевания также наблюдаются в лесных районах стран Восточной Европы и Скандинавского полуострова.
Клещевой энцефалит относится к так называемым трансмиссивным инфекциям, то есть тем, которые передаются человеку через кровососущих насекомых. Каждый год на территории Российской Федерации регистрируется примерно 5—6 тыс. случаев данного инфекционного заболевания.

Причины клещевого энцефалита
Возбудителем заболевания является вирус из рода флавивирусов (Flavivirus). На снимках с электронного микроскопа он представляет собой частицы в виде шара с мелкими выступами на поверхности, размером 40—50 нм. Такой маленький размер (в 2 раза меньше вируса гриппа и в 3—4 раза меньше вируса кори) позволяет возбудителю легко проникать через все защитные барьеры иммунной системы.
Особенностями вируса клещевого энцефалита является слабая устойчивость к действию высоких температур, дезинфицирующих средств и ультрафиолетового излучения. Так, при кипячении он погибает через 2 минуты и не может сохраняться в окружающей среде в жаркую солнечную погоду. Однако при низких температурах он способен долго поддерживать жизнеспособность. В зараженных молочных продуктах флавивирус не теряет своих свойств в течение 2 месяцев.
В природе вирус клещевого энцефалита, как и следует из названия заболевания, находится в организме иксодовых клещей. Кроме человека, вирус может поражать диких и домашних животных, в том числе коров и коз. Поэтому заражение может происходить как напрямую – при укусе человека клещом или случайном раздавливании насекомого при попытках его извлечь, так и при употреблении молока и молочных продуктов, не прошедших термическую обработку и полученных от больных животных. Чем дольше клещ находится на коже человека, тем выше риск развития заболевания.
Самое большое число случаев заболевания регистрируется в конце весны и начале осени, это связано с увеличением числа клещей в это время. Заразиться вирусом клещевого энцефалита можно во время прогулок по лесу, парку, посещении мест отдыха на природе.
Классификация клещевого энцефалита
В зависимости от того, какие признаки заболевания выражены сильнее всего, клещевой энцефалит может протекать в 3 формах:
- лихорадочной (при преобладании лихорадки), развивается у 50% больных
- менингеальной (при поражении оболочек головного и спинного мозга), характерна для 30% зараженных
- очаговой (при вовлечении в процесс вещества мозга с развитием очаговой неврологической симптоматики), отмечается у 20% заболевших.
Симптомы клещевого энцефалита
Скрытый, или инкубационный период заболевания длится примерно 1—2 недели. Но могут встречаться как молниеносные, когда от момента заражения до первых признаков проходит 24 часа, так и затяжные формы заболевания, с длительностью инкубационного периода до 1 месяца.
Во время скрытого периода вирусные частицы усиленно размножаются в месте внедрения (кожная рана или стенка кишечника), затем попадают в кровь и с ней разносятся по всему организму. Именно этот момент знаменует появление первых клинических симптомов. Второй пик размножения флавивируса происходит уже во внутренних органах (ЦНС, почках, лимфатических узлах, печени).
Все формы клещевого энцефалита (лихорадочная, менингеальная, очаговая) имеют общие начальные признаки. Заболевание начинается остро, во многих случаях больной может четко указать даже час, когда его состояние резко ухудшилось. Первые симптомы напоминают проявления гриппа: озноб, ломота в мышцах, артралгии, головная боль, слабость, вялость, может наблюдаться рвота и судороги на фоне резкого подъема температуры тела (характерно для детей). При осмотре обращают на себя внимание покраснение кожи лица, шеи вплоть до ключиц, белки глаз с расширенными кровеносными сосудами. Последующее течение заболевания напрямую зависит от той формы, в которой оно будет протекать у конкретного больного.
Лихорадочная форма
Клещевой энцефалит в этой форме протекает с преобладанием лихорадочного состояния, которое может длиться от 2 до 10 дней. В большинстве случае он носит волновой характер, то есть, после первого подъема температуры и последующего стихания клинических проявлений, болезнь как будто возвращается вновь и следует новый приступ лихорадки, длящийся несколько дней. Примерно через 10 дней температура тела приходит в норму, общее состояние больного улучшается. Однако слабость, отсутствие аппетита, приступы сердцебиения, потливость могут наблюдаться еще в течение 1 месяцев после лабораторного выздоровления (по результатам анализов крови и спинномозговой жидкости).
Менингеальная форма
Эта форма характеризуется появлением на 3—4 день заболевания признаков менингита - поражения оболочек спинного и головного мозга. Проявляется следующими симптомами: сильнейшей головной болью, которую не облегчают обезболивающие средства; рвотой, повышенной чувствительностью кожных покровов, когда даже прикосновение одежды к телу вызывает болевые ощущения; ригидностью (сильным напряжением) затылочных мышц, что приводит к непроизвольному запрокидыванию головы назад; симптомом Кернига – невозможностью произвольно разогнуть в колене ногу, согнутую под прямым углов в коленном и тазобедренном суставе в положении лежа на спине; верхним и нижним симптомами Брудзинского – при попытке врача наклонить голову больного вперед (подбородком к груди) и при надавливании на лобок, происходит рефлекторное сгибание ног в коленных и тазобедренных суставах.
Все эти проявления болезни объединяются понятием менингеальный синдром и означают то, что вирус клещевого энцефалита достиг оболочек спинного и головного мозга. Лихорадка и менингеальные симптомы продолжаются примерно 2 недели. После нормализации температуры у больных длительное время (до 2 месяцев) сохраняется астения (слабость, вялость), плохая переносимость яркого света, громких звуков, подавленное настроение.
Очаговая форма
Относится к самым тяжелым и наиболее неблагоприятным по прогнозу формам клещевого энцефалита. В ее основе лежит проникновение возбудителя в вещество головного и спинного мозга. Характеризуется резким повышением температуры тела до 40°C и выше, отмечается вялость, сонливое состояние (гиперсомния), рвота, судороги, озноб.
Наблюдаются симптомы поражения вещества головного мозга с возникновением галлюцинаций, расстройств сознания, бреда, нарушения восприятия времени и пространства. При вовлечении в процесс ствола мозга, в котором располагаются центры, отвечающие за обеспечение жизненно важных функций, могут наблюдаться нарушения дыхания и сердечной деятельности. При попадании вируса в ткань мозжечка развивается нарушение чувства равновесия, дрожь в руках и ногах. При поражении спинного мозга наступают вялые (с пониженным мышечным тонусом) парезы и параличи мышц шеи, плеч, верхней части груди и надлопаточной области. При проникновении вируса в корешки спинного мозга возникает радикулит - боль по ходу нерва, нарушение произвольных движений, функций внутренних органов, появление расстройств кожной чувствительности в тех отделах, за которые отвечает пораженный корешок.
Очаговая форма клещевого энцефалита может носить двухволновой характер (двухволновый вирусный менингоэнцефалит), когда первый приступ болезни похож на обычную лихорадочную форму, а через несколько дней после нормализации температуры тела резко возникают симптомы повреждения вещества головного и спинного мозга.
Особой формой клещевого энцефалита является прогредиентная, которая может развиться после любой другой формы заболевания. Она характеризуется развитием стойких нарушений функций головного и спинного мозга спустя несколько месяцев или даже лет после острого периода болезни.
Диагностика клещевого энцефалита
В установке точного диагноза важную роль играют: клинические проявления; эпидемиологические данные; лабораторные исследования.
Клинические проявления. Это те характеристики заболевания, которые описывает врач невролог, обследуя больного. К клиническим проявлениям относятся жалобы пациента, содержащие особенности начала заболевания, последовательность возникновения тех или иных симптомов; объективный осмотр, который выявляет признаки поражения органов и систем.
Эпидемиологические данные. Это сведения о месте проживания пациента, его профессиональной деятельности, употребления в пищу тех или иных продуктов, сезона, в который возникло заболевание, факта укуса клеща и попыток самостоятельно извлечь его из кожи. Эти данные помогают сузить круг предполагаемых заболеваний.
Лабораторные исследования. Для подтверждения причины заболевания используют обнаружение частиц вируса клещевого энцефалита в крови и спинномозговой жидкости с помощью ПЦР (полимеразной цепной реакции). Кроме того, могут быть использованы серологические методы с определением титра антител в парных сыворотках больного, взятых с интервалом в 2 недели. При этом учитывается не только уровень титра антител в одной пробе, но и его нарастание или уменьшение в зависимости от времени прошедшего от начала заболевания.
Лечение клещевого энцефалита
Лечение производится исключительно в стационаре. Поскольку человек является тупиковым звеном в распространении флавивируса, то больной клещевым энцефалитом не заразен и не представляет опасности для окружающих, поэтому все лечебные мероприятия проводятся не в инфекционном отделении, а в неврологии.
Лечение включает специфическую (направленную на возбудителя), патогенетическую (блокирующую механизмы развития заболевания) и симптоматическую терапию. Больному назначается строгий постельный режим. Схема специфического лечения зависит от времени, прошедшего с момента появления первых симптомов. В самом начале заболевания (первая неделя) высокую эффективность показало назначение больным противоклещевого иммуноглобулина. Его вводят в течение 3 дней. Также при ранней диагностике хорошие результаты дает применение противовирусных препаратов: рибонуклеазы, рибавирина, интерферона, экстракт побегов картофеля.
Все эти препараты неэффективны на поздних стадиях заболевания, когда вирус уже поразил центральную нервную систему. В этом случае лечение направлено не на борьбу с возбудителем болезни, а на патологические механизмы, угрожающие жизни пациента. Для этого используют подачу кислорода через маску, ИВЛ при нарушении дыхания, мочегонные средства для снижения внутричерепного давления, препараты, увеличивающие устойчивость мозга к кислородному голоданию, нейролептики.
Прогноз и профилактика клещевого энцефалита
Прогноз при клещевом энцефалите зависит от степени поражения нервной системы. При лихорадочной форме, как правило, все больные полностью выздоравливают. При менингеальной форме также прогноз благоприятный, однако в некоторых случаях могут наблюдаться стойкие осложнения со стороны ЦНС в виде хронических головных болей, развития мигрени. Очаговая форма клещевого энцефалита является самой неблагоприятной по прогнозу. Смертность может достигать 30 человек на 100 заболевших. Осложнениями этой формы является возникновение стойких параличей, судорожного синдрома, снижение умственных способностей.
Профилактика клещевого энцефалита делится на 2 направления: организационные мероприятия и вакцинация. Организационные мероприятия заключаются в обучении жителей эндемичных регионов (мест распространения заболевания) соблюдению правил посещения лесных зон и мест отдыха на природе в период активности клещей: одевание одежды, закрывающей большую часть тела (с длинными рукавами и штанинами, панамы или кепки на голову); тщательный осмотр одежды и тела на предмет выявления живых клещей; немедленное обращение за медицинской помощью в случае обнаружения присосавшегося насекомого; предупреждение о недопустимости самостоятельного удаления прицепившегося клеща с кожи; нанесение репеллентов на одежду перед прогулкой; обязательное кипячение молока, покупка молочных продуктов только у официальных производителей.
Вакцинация включает в себя: пассивную иммунизацию – введение иммуноглобулина пациентам, не прививавшимся ранее от клещевого энцефалита (в случае укуса клеща) и активную иммунизацию – проведение прививок жителям района распространения заболевания за 1 месяц до сезона активности клещей.
Читайте также:

