Хеликобактер и кровоточивость десен
Обновлено: 08.05.2024
Маев И.В., Айвазова Р.А., Самсонов А.А., Андреев Н.Г.
Кафедра пропедевтики внутренних болезней и гастроэнтерологии ГОУ ВПО “Московский государственный медико-стоматологический университет” Минздравсоцразвития РФ, Москва
Инфекция Helicobacter pylori ассоциирована с самыми распространенными заболеваниями желудка и двенадцатиперстной кишки (язвенной болезнью, хроническим гастритом, раком желудка). Средой обитания бактерии является желудок и двенадцатиперстная кишка. Полость рта считается вторичным резервуаром H. pylori. Инфекция хорошо поддается лечению с помощью комплекса антибиотиков (эрадикационная терапия), однако риск рецидивов и побочных эффектов данного лечения достаточно велик. В данной статье обсуждаются вопросы сочетанной с хеликобактериозом патологии полости рта, пародонта, побочных эффектов эрадикационной терапии, ее переносимости. Предлагаются пути оптимизации лечения хеликобактерной инфекции с применением препаратов, способствующих восстановлению микроэкологии как желудочно-кишечного тракта в целом, так и полости рта в частности.
В настоящее время антихеликобактерная терапия считается основным стандартом лечения язвенной болезни (ЯБ), ассоциированной с Helicobacter pylori, что отражено в международных (I, II, III, IV Маастрихтские соглашения) и российских рекомендациях по лечению гастроэнтерологических больных.
Достоверно известно, что проблема хеликобактериоза касается не только патологии желудочно-кишечного тракта (ЖКТ), но и смежных областей, в частности стоматологии, т. к. многие авторы рассматривают полость рта как возможный источник инфицирования H. pylori и рецидивирования
ЯБ [1]. Активно обсуждается вопрос и об участии полости рта в реинфицировании организма H. pylori. Ряд российских и зарубежных ученых в своих работах отмечают высокую вероятность рецидива ЯБ и хронического гастрита, ассоциированных с H. pylori, из-за неполноценной эрадикационной терапии (ЭТ) в результате неэффективности некоторых хеликобактерных средств, недостаточности сроков лечения, сохранения резервуаров инфекции, в т. ч. в полости рта пациентов [2, 3].
В последние годы обсемененность полости рта H. pylori стали учитывать и как фактор, оказывающий влияние на развитие и течение стоматологических заболеваний [4]. Обсуждается возможность выделения такого термина, как H. pylori-ассоциированные заболевания пародонта [5]. В связи
с этим встает вопрос и об ЭТ как о базисной терапии лечения заболеваний пародонта и гастродуоденальной зоны у больных ЯБ двенадцатиперстной кишки (ДПК), ассоциированной с H. pylori.
Эрадикация (уничтожение) H. pylori с помощью адекватных комбинаций антибактериальных средств
способствует регрессу воспалительнодистрофических изменений слизистой оболочки желудка и ДПК; восстановлению защитных свойств слизистой оболочки гастродуоденальной зоны; существенному снижению частоты рецидивов ЯБ (с 60–70 до 1–3 % в течение двух лет наблюдений), а следовательно, и ее осложнений; профилактике развития мальтомы и рака желудка.
При наличии H. pylori-ассоциированной патологии ЖКТ целью лечения является решение следующих задач:
• устранение в кратчайший срок симптомов болезни;
• уничтожение H. pylori в гастродуоденальной слизистой оболочке;
• купирование активного воспаления в слизистой оболочке желудка и ДПК;
• обеспечение заживления язв и эрозий;
• предупреждение развития обострений и осложнений, включая лимфому и рак желудка.
По числу препаратов, входящих в схему эрадикации, выделяют:
• трехкомпонентную схему (два антимикробных препарата + антисекреторный);
• четырехкомпонентную схему – квадротерапию (три антимикробных препарата + антисекреторный).
Использование эффективных антисекреторных средств больными ЯБ имеет огромную клиническую значимость, поскольку это приводит к сокращению сроков рубцевания язвы, избавлению от болей и симптомов язвенной диспепсии, значительно снижает риск развития осложнений и, что особенно важно, достоверно и существенно повышает длительность ремиссии заболевания, снижает частоту ее рецидивов, а следовательно, снижает частоту рецидивов болезней пародонта.
В настоящее время наиболее оптимальными эрадикационными комплексами признаны схемы, включающие ингибитор протонной помпы (ИПП) и 2 или 3 антимикробных препарата (выбор тройной или квадросхем лечения зависит от чувствительности H. pylori в конкретном регионе к кларитромицину).
Десятилетие потребовалось для отработки наиболее эффективных схем лечения. Бесконтрольное назначение антибиотиков с целью достижения эрадикации в 1990-х гг. привело к лавинообразному нарастанию первичной и вторичной резистентности H. pylori с последующим снижением эффективности терапии. Иллюстрацией этого факта служит резистентность к производным нитроимидазола, которые используются в большинстве эрадикационных схем. Многоцентровое европейское исследование по изучению чувствительности к метронидазолу in vitro показало, что около 27,5 % (от 7 до 49 %) протестированных штаммов были резистентными.
В нашей стране к 2003 г. число штаммов H. pylori, резистентных к метронидазолу, достигло 55,5 %. Опасной можно назвать тенденцию к росту полирезистентных штаммов – 11,1 % [6]. Очевидно, проблему резистентности можно решить, лишь строго регламентируя подходы к режимам эрадикации.
Резкое увеличение во всем мире числа штаммов H. pylori, устойчивых к нитроимидазолам, сделало актуальным поиск более действенных режимов эрадикации микроорганизма. В связи с этим наиболее эффективной в регионах с низкой резистентностью H. pylori к кларитромицину остается схема на основе комбинации ИПП, макролидного антибиотика (кларитромицина) и амоксициллина (тройная терапия первой линии).
Если чувствительность к антибактериальным препаратам у конкретного индивидуума до назначения лечения не определялась, а резистентность к кларитромицину в данном регионе превышает 15–20 %, тройную терапию назначать не следует: рекомендуется сразу назначать квадротерапию. Квадротерапия существует в двух вариантах: классической (ИПП + висмут + тетрациклин + метронидазол) и модифицированной терапии первой линии, в состав которой помимо ИПП, амоксициллина и кларитромицина включается третий антимикробный компонент – препарат висмута. Классическая квадротерапия с препаратом висмута в качестве терапии первой линии приводит к эрадикации в 93,3 % случаев [7]. Примечательно, что подобные высокие показатели эрадикации (93,7 %) регистрируются при включении препарата висмута в состав обычной схемы тройной терапии с амоксициллином и кларитромицином [8]. Вместе с тем последняя комбинация предпочтительнее, поскольку позволяет преодолевать резистентность H. pylori к кларитромицину, самому эффективному
компоненту ЭТ, и легче переносится. Амоксициллин нарушает синтез гликопротеидов в стенке бактерий и обладает бактерицидным эффектом в отношении H. pylori, который существенно возрастает в нейтральной среде, препарат ингибирует транспептидазу, нарушает синтез пептидогликана (опорного белка клеточной стенки) в период деления и роста, вызывает лизис микроорганизмов. Резистентность H. pylori к амоксициллину развивается крайне редко. В стоматологической практике амоксициллин эффективно применяют в лечении периимплантационных
инфекционных осложнений, остро и хронически протекающих периодонтитов, денто-альвеолярных абсцессов и других гнойно-воспалительных процессов в челюстно-лицевой области.
Амоксициллин является одним из препаратов первого выбора при системной антибиотикотерапии заболеваний пародонта, может использоваться профилактически перед обширными хирургическими вмешательствами [9]. В многочисленных работах показана эффективность применения схем, включающих макролиды с целью эрадикации H. pylori. Макролиды демонстрируют максимальный бактерицидный эффект в отношении H. pylori среди всех антибиотиков, применяемых в схемах. Этот эффект является дозозависимым и реализуется при применении кларитромицина в дозе 1000 мг/сут [10]. В схемах эрадикации использовались различные антибиотики группы макролидов (кларитромицин, азитромицин, рокситромицин). Тем не менее лишь кларитромицин благодаря своим фармакокинетическим и фармакодинамическим особенностям присутствует в рекомендациях
Маастрихт-II, -III и -IV.
В России в эрадикационных схемах хорошо зарекомендовал себя кларитромицин. По мнению ведущих специалистов, макролидные антибиотики, в частности кларитромицин, являются наиболее перспективной группой антибиотиков в лечении одонтогенной инфекции, в т. ч. и у больных, имеющих изменения со стороны иммунной системы, что позволяет широко использовать их в лечении заболеваний пародонта [11–14].
Важной проблемой при антихеликобактерной терапии являются ее побочные эффекты, а также переносимость и безопасность массивной антибиотикотерапии в целом, на фоне которой могут возникать аллергические, токсические и дисбиотические изменения в организме [15]. Частота побочных эффектов при использовании различных схем тройной терапии весьма вариабельна и составляет, по данным зарубежных авторов, от 20 до 59 % [16].
Каждый из антибиотиков сам по себе имеет немало побочных эффектов. Так, при приеме кларитромицина возможны умеренные диспепсические расстройства – чаще диарея, изменение вкуса, глоссит и др. Спектр подобных проявлений у амоксициллина еще более выражен, с акцентом на аллергические реакции вплоть до анафилактического шока и отека Квинке. Как указывалось, третьим антибактериальным средством, используемым в схемах эрадикационной терапии, является коллоидный субстрат висмута. Это соединение обладает выраженными цитопротекторным, противовоспалительным и бактерицидным действием в отношении H. pylori, однако и оно не лишено побочных эффектов [17]. К ним можно отнести появление головной боли, аллергических реакций; кроме того, при применении препарата из-за образования в кишечнике сульфида висмута кал способен приобретать черную окраску, что в сочетании с диареей может имитировать признаки желудочно-кишечного кровотечения [18].
По нашим данным, побочные реакции развиваются среди 11,7 % пациентов, получающих ЭТ. Клинические наблюдения за состоянием ЖКТ и полости рта основывались на данных сравнительного анализа результатов применения одно- и двухнедельных схем ЭТ первой линии по Маастрихт-III. Первая группа получала терапию по следующей схеме: рабепразол 20 мг 2 раза в сутки + кларитромицин 500 мг 2 раза в сутки + амоксициллин 1000 мг 2 раза в сутки курсом 7 дней. Вторая
группа получала идентичную терапию, но в течение 14 дней. Результаты ЭТ были следующими: 83,4 % эрадикации у больных первой группы и 96,7 % – у второй, что свидетельствует о бóльшей эффективности терапии, пролонгированной до двух недель.
В целом у 7 (11,7 %) больных первой и второй групп, соответственно 3 и 4 (10,0 и 13,3 %) пациентов, на фоне ЭТ отмечены вновь появившиеся симптомы диспепсии как следствие применения ее компонентов. Это были явления умеренного чувства горечи во рту по утрам как при 7-дневном, так и
при 14-дневном курсах (по 2 случая) и 3 случая неустойчивого стула (диареи) у одного больного на фоне недельного лечения и у двух пациентов при проведении двухнедельной эрадикационной терапии. Следует отметить, что все указанные побочные эффекты антихеликобактерной терапии не повлекли отмены лечения, успешно купировались приемом смектита диоктаэдрического по 1 пакету через 1,5 часа после еды и на ночь и не возобновлялись после окончания курсов эрадикации H. pylori. К моменту контроля эрадикации (6-я неделя) все указанные явления исчезли.
В целом наш многолетний опыт применения кларитромицина и амоксициллина свидетельствует о хорошей переносимости данных лекарственных препаратов как при 7-дневной, так и при 14-дневной эрадикационной терапии, позволяющей проводить полноценное лечение практически 100 % нуждающихся в ней больных без каких-либо серьезных последствий.
Использование рабепразола при лечении ЯБ в качестве базисного препарата терапии первой линии по Маастрихт-III в режимах 7- и 14-дневной терапии имело ряд преимуществ перед антисекреторными препаратами предыдущих поколений, что было обусловлено более сильным, быстрым, продолжительным и достаточно предсказуемым антисекреторным действием. Препараты этой
группы не имели побочных эффектов, при их использовании резистентности и синдрома отмены не отмечено.
Второй общепризнанной проблемой при антибиотикотерапии является развитие дисбиозов полости рта и ЖКТ. Известно, что нерациональная антибиотикотерапия, неблагоприятная экологическая обстановка, возрастание стрессовых воздействий создают условия для повсеместного распространения дисбиоза ЖКТ, активизации хронических бактериальных инфекций, аллергизации организма взрослых и детей. Было доказано существенное влияние дисбиоза и иммунодефицита на длительность и тяжесть острых, а также хронических заболеваний полости рта, затруднение и повышение стоимости их диагностики и лечения [19].
Традиционное комплексное лечение заболеваний пародонта включает применение общих и местных антисептических, антимикробных, антибактериальных препаратов широкого спектра действия. В большинство схем лечения входят антисептические средства, содержащие хлоргексидин, оказывающий бактериостатическое действие. Известно, что применение данного антисептика в течение 2 недель приводит к нарушению состава микробной флоры полости рта, увеличению частоты выделения и количества дрожжеподобных грибов кандида, что можно трактовать как субклиническую стадию дисбиоза.
По мнению ряда ведущих ученых, заболевания пародонта на фоне дисбиотического сдвига ЖКТ и полости рта имеют следующие особенности [20]:
• более раннюю, чем среди лиц без фоновой патологии, генерализацию патологического процесса;
• более выраженные признаки воспаления в тканях пародонта, нередко сопровождающиеся выделением гноя из пародонтальных карманов;
• рецидивирующий характер течения пародонтита у пациентов с сочетанной патологией ЖКТ и полости рта;
• резистентность к традиционной терапии;
• нестойкость ремиссии заболевания. Таким образом, развитие дисбиоза в полости рта является наиболее мощным фактором, способствующим развитию и поддержанию болезней пародонта.
Являясь вторичной патологией, дисбиоз полости рта усугубляет тяжесть и ухудшает прогноз течения основного процесса, а успешное устранение дисбиотических нарушений улучшает результаты
лечения первичного заболевания.
Современные подходы к лечению хронических заболеваний полости рта учитывают комплексное применение этиотропной, патогенетической и симптоматической терапии. При коррекции дисбиотических нарушений в состав комплексного лечения следует включать препараты, способствующие восстановлению микроэкологии и нормализации системы местного иммунитета.
Использование микробных биопрепаратов, действующим началом которых является нормальная микрофлора с высокими антагонистическими и ферментативными свойствами, является перспективным направлением в лечении заболеваний пародонта. В зависимости от составляющих компонентов их подразделяют на вакцины, биологически активные добавки, эубиотики, про- и пребиотики.
Наиболее перспективной группой лекарственных средств, механизм действия которых направлен на восстановление колонизационной резистентности в целом, можно считать иммуномодуляторы бактериального происхождения. Лизаты микроорганизмов, являясь представителем указанного класса препаратов, представляют собой поливалентный антигенный комплекс, спектр которого соответствует видовому представительству традиционных возбудителей инфекционных процессов в полости рта, повышают фагоцитарную активность макрофагов, увеличивает содержания лизоцима и интерферона, стимулируют продукцию секреторного иммуноглобулина A иммунокомпетентными клетками, подавляют синтез микробных гидролаз; угнетают образование сенсибилизированных антител.
Лизаты микроорганизмов хорошо совмещаются с лекарственными средствами различных групп и могут быть включены в состав комплексного лечения [21, 22].
Для восстановления микрофлоры кишечника применяют бифидосодержащие лечебно-диетические продукты питания. Наиболее популярными и массовыми в настоящее время во всем мире являются йогурты, в состав которых входят молочнокислые бактерии разных видов [23].
Эубиотики – это бактерийные препараты, действующим началом которых являются живые лиофильно высушенные культуры микроорганизмов – представителей нормальной микрофлоры. Ведущие российские ученые доказали, что применение эубиотиков достоверно улучшает клиническое состояние пародонта, способствуя исчезновению отека, гиперемии слизистой оболочки десны, уменьшению кровоточивости десен, снижению концентрации патогенных и условнопатогенных видов микроорганизмов (стафилококков, протея, гемолитического стрептококка), восстановлению
лактофлоры [24].
Пробиотики – ферменты, подавляющие рост патогенных микроорганизмов. Пробиотики являются активаторами роста нормальной микрофлоры [25].
При заболеваниях слизистой оболочки полости рта также широко используются пребиотики, препараты лактулозы, которые не перевариваются в кишечнике и стимулируют рост нормальной флоры.
Некоторые ученые при лечении дисбиозов основную ставку делают на фаготерапию, предварительно определив чувствительность к фагам, которые являются естественными рычагами регуляции численности популяции микроорганизмов, биологическими ограничителями. Бактериофаги обладают высокой специфичностью к патогенным микроорганизмам, селективно лизируют только специфические бактерии; в отсутствие “хозяина” выводятся из организма и являются индифферентными по отношению к нему, а также обладают более высокой избирательностью действия, чем антибиотики.
Таким образом, комплексный индивидуальный подход, внимательное наблюдение за пациентами с патологией полости рта, сочетанной с хеликобактериозом, оптимальная антихеликобактерная терапия, при которой из большой палитры выбирают средства, улучшающие ее переносимость и положительно влияющие на состоянии как ЖКТ в целом, так и полости рта в частности, и пародонта могут существенно облегчить переносимость лечения и в целом улучшить показатели ЭТ.
Литература
Об авторах / Для корреспонденции
Информацию из данного раздела нельзя использовать для самодиагностики и самолечения. В случае боли или иного обострения заболевания диагностические исследования должен назначать только лечащий врач. Для постановки диагноза и правильного назначения лечения следует обращаться к Вашему лечащему врачу.
Хеликобактериоз: причины появления, симптомы, диагностика и способы лечения.
Определение
Хеликобактериоз – инфекционное заболевание, поражающее пилорический отдел желудка, или привратник, и двенадцатиперстную кишку. Его возбудителем является уникальная патогенная микроаэрофильная грамотрицательная бактерия хеликобактер пилори (H. pylori). Свое название бактерия получила за счет отдела желудка, в котором она обитает – пилорического.
В результате микроорганизм еще сильнее колонизирует слизистую оболочку, формирует ее повышенную восприимчивость к соляной кислоте и провоцирует воспаление, приводящее к развитию язвенных дефектов.
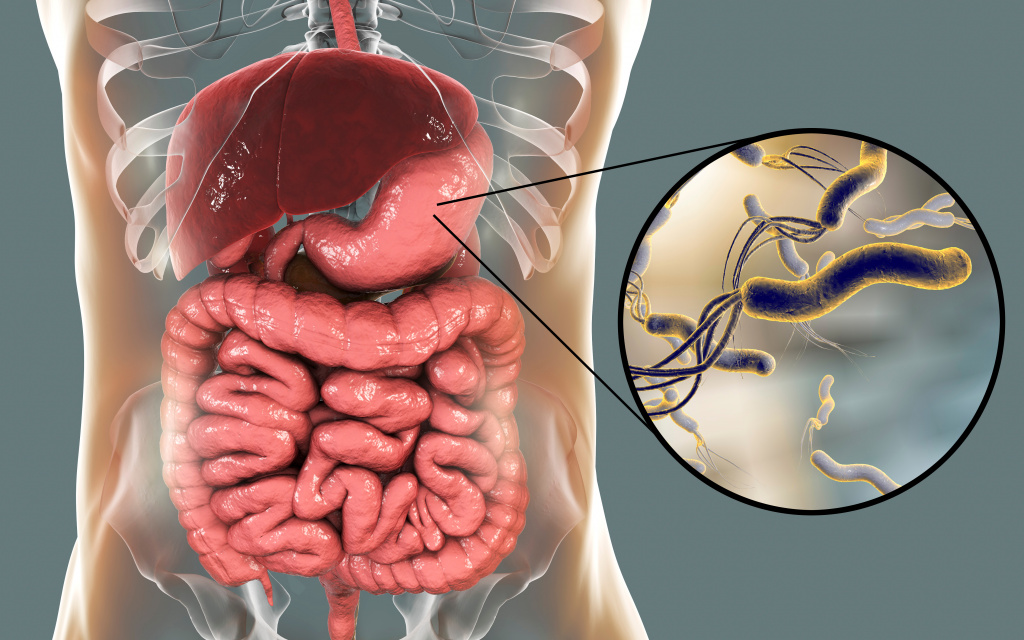
Хеликобактер пилори – спиралевидная бактерия длиной 3,5 и шириной 0,5 микрон. Она имеет жгутики, с помощью которых свободно перемещается по стенке желудка либо надежно на ней закрепляется. Бактерия H. pylori очень изменчива, ее штаммы (разновидности) отличаются друг от друга способностью прикрепляться к слизистой оболочке желудка, вызывать воспалительный процесс и обладают разной степенью патогенности.

Хеликобактер пилори, колонизирующая слизистую оболочку желудка, — частая причина ее воспалительных изменений, она признана этиологическим фактором гастрита, а сам гастрит — инфекционным заболеванием. В зависимости от состояния защитных факторов желудка возникший инфекционный процесс может протекать латентно или с выраженной клинической симптоматикой воспаления. Согласно современным представлениям, H. pylori вызывает хронический гастрит у всех зараженных лиц. Это может привести к язвенной болезни, атрофическому гастриту, аденокарциноме желудка или низкодифференцируемой лимфоме желудка. H. pylori относится к канцерогенам первого порядка.
Результаты многочисленных исследований дают основание предполагать возможную патогенетическую или опосредованную роль инфекции H. pylori в развитии и/или течении заболеваний, не относящихся к пищеварению: кардио-, цереброваскулярных, аутоиммунных заболеваний, заболеваний крови, кожи, нервной системы и многих других.
Патоген отличается относительной устойчивостью к окружающей среде: при кипячении хеликобактерии гибнут практически мгновенно, при обработке дезинфицирующими составами — в течение нескольких минут.
Причины появления хеликобактериоза
Заразиться бактерией можно при контакте с загрязненной водой или продуктами питания. Инфицирование возможно во время проведения эндоскопии и при использовании других плохо стерилизованных медицинских инструментов, которые имели прямой контакт со слизистой желудка пациента.
Бытовой способ передачи (например, через поцелуи, личные вещи и проч.) также возможен, о чем свидетельствует выделение бактерии из слюны и зубного налета.
Распространенность инфекции варьируется в зависимости от географического региона, возраста пациента, его этнической принадлежности и социально-экономического статуса. По данным Департамента здравоохранения г. Москвы (2019), распространенность этой инфекции в Москве составляет 60,7–88%, в Санкт-Петербурге - 63,6%, в Восточной Сибири достигает 90%.
Классификация заболеваний
Заболевания, связанные с H. pylori:
- гастрит,
- дуоденит,
- гастродуоденит,
- эзофагит,
- язвенная болезнь желудка,
- язвенная болезнь двенадцатиперстной кишки,
- железодефицитная анемия неясного генеза,
- рак желудка,
- рак двенадцатиперстной кишки.
Основной жалобой, с которой больные с признаками Helicobacter-инфекции обращаются к врачу, являются желудочные боли. Локализация симптома может меняться и переходить в область расположения двенадцатиперстной кишки.
Боли бывают острыми, ноющими, тупыми, возникают в верхних отделах живота слева и по центру в околопупочной области. Дискомфорт может возникать при длительном голодании, натощак или через определенное время после приема пищи.
Симптоматика хеликобактериоза зависит от клинической формы заболевания и может включать:
- чувство тяжести в животе после еды;
- нарушение аппетита, связанное с внезапными приступами тошноты (если слизистая желудка сильно травмирована);
- беспричинная рвота на фоне нормальной температуры тела;
- изжога (жгучие ощущения в пищеводе и даже гортани) и отрыжка с неприятным кислым или горьким привкусом;
- хронические запоры (отсутствие дефекации в течение трех суток и более);
- разжижение каловых масс, появление пенистой или водянистой консистенции;
- кишечные спазмы и вздутие живота.
- снижение аппетита до полного его отсутствия;
- тошнота может сменяться рвотой со сгустками крови;
- резкое снижение массы тела, не являющееся нормой;
- сухость во рту и привкус металла;
- появление белого налета на языке;
- неприятный запах изо рта при отсутствии кариеса;
- заеды в уголках рта;
- кровоточивость десен.
Диагностика хеликобактериоза
Долгое время хеликобактериоз может никак себя не проявлять, при этом провоцируя развитие язвы, аденокарциномы или мальтомы желудка. В особой зоне риска люди, чьи родственники имеют эти заболевания в анамнезе.
Диагностика может быть инвазивной (эндоскопия с последующей биопсией желудочных тканей) и неинвазивной (лабораторные исследования).
Согласно международным рекомендациям, методами выбора для диагностики бактерии и оценки эффективности лечения H. pylori служат дыхательный̆ тест с мочевиной, меченной 13С и определение специфических антигенов H. pylori в кале иммунохроматографическим методом.
Синонимы: Дыхательный тест с 13С-меченной мочевиной. 13 UBT; 13C-UBT. Краткая характеристика 13С-уреазного дыхательного теста Дыхательный тест в текущей модификации предназначен для лиц старше 12 лет. 13С-уреазный дыхательный тест относится к неинвазивным безопасным методам исследования.
Информацию из данного раздела нельзя использовать для самодиагностики и самолечения. В случае боли или иного обострения заболевания диагностические исследования должен назначать только лечащий врач. Для постановки диагноза и правильного назначения лечения следует обращаться к Вашему лечащему врачу.
Кровоточивость десен: причины появления, при каких заболеваниях возникает, диагностика и способы лечения.
Определение
Кровоточивость десен появляется во время чистки зубов или пережевывания твердой пищи, например, яблок или сырой моркови. Следует помнить, что в некоторых случаях это состояние может быть симптомом таких серьезных заболеваний полости рта как гингивит и пародонтит.
Кроме того, к настоящему моменту накоплено большое количество данных, доказывающих взаимосвязь сахарного диабета и сердечно-сосудистых патологий с воспалением пародонта (тканей, окружающих зубы).
Разновидности кровоточивости десен
По частоте проявлений кровоточивость десен может быть хронической, то есть возникающей регулярно, или носить ситуативный характер – как правило, в ответ на травму десны.
Возможные причины кровоточивости десен
Причины появления кровоточивости десен можно разделить на две основные группы:
- Патологии ротовой полости.
- Патологии систем организма.
- Гингивит. Для этого заболевания характерно развитие воспаления слизистой оболочке десен. Симптомами данного состояния являются покраснение либо синюшность десен, их отек и кровоточивость. В запущенных случаях проявления заболевания мешают приему пищи и беспокоят даже во сне.
- Пародонтит – заболевание, требующее обязательного обращения к стоматологу. Характеризуется выраженной кровоточивостью десен, шаткостью зубов, шейки которых оголяются, в результате чего зубы выпадают. Пародонтит нередко сопровождается сильным воспалением вплоть до выделения гноя из кармана, образующегося между зубом и десной.
- Зубной камень представляет собой затвердевшие остатки пищи и продукты жизнедеятельности бактерий полости рта. Он травмирует десны, что ведет к их кровоточивости. Различают поддесневые камни (внешне незаметные) и наддесневые (видны невооруженным глазом).
- неприятные и болезненные ощущения при прикосновении (надавливании на десны, чистке зубов);
- неприятный запах изо рта;
- повышенное слюноотделение, не связанное с другими заболеваниями полости рта или органов желудочно-кишечного тракта;
- зубной налет и камни;
- изменение внешнего вида десен (набухание, появление красноты или синюшности);
- изменение внешнего вида зубов (оголение шейки, изменение цвета вследствие отложения зубного камня).
Наиболее часто встречающиеся патологии организма, ведущие к кровоточивости десен
Авитаминоз. Всем известное заболевание цинга связано с недостаточным поступлением в организм витамина С, это проявляется повышенной кровоточивостью десен, нарушением синтеза коллагена, в результате чего соединительная ткань не может полностью осуществлять свои функции.
Причиной кровоточивости десен может стать недостаточное поступление в организм витамина А (ретинола), рибофлавина и пиридоксина (В2 и В6), кальциферола (витамина Д, в частности, его разновидности – витамина Д3), токоферола (витамина Е), никотиновой кислоты (витамина РР) и витамина К. Последний не только влияет на структуру тканей, но и участвует в процессах свертывания крови.
Гормональная перестройка организма, возникающая в период беременности и полового созревания подростков, может также сопровождаться кровоточивостью десен.
При сахарном диабете поражаются мелкие сосуды всего организме, в том числе и ротовой полости, сетчатки глаза и т.д.
Для гепатитов различной этиологии также характерно развитие кровоточивости десен, поскольку в печени синтезируется много факторов свертывания крови. С учетом того, что свертывающая система крови человека работает по принципу каскада, недостаток хотя бы одного элемента ведет к нарушению гемостаза. Для гепатитов характерен смешанный тип нарушения свертывания, обусловленный и нехваткой многих витаминов в результате нарушения их всасывания, и снижением уровня тромбоцитов, и поражением печени как источника факторов свертывания.
Лейкозы, а также заболевания крови различного характера, ведущие к снижению количества тромбоцитов, или наоборот, повышающие вязкость крови, могут проявляться повышенной кровоточивостью десен. При этих заболеваниях обращает на себя внимание бледность кожи и видимых слизистых оболочек, появление кровотечений различных локализаций, синяков, повышенная утомляемость, слабость; возможна ночная потливость, лихорадка, не обусловленная какими-либо другими причинами.
К каким врачам обращаться при кровоточивости десен
Если врачу не удается найти первопричину кровоточивости, необходима консультация терапевта , эндокринолога или гастроэнтеролога .
Диагностика и обследования при кровоточивости десен
При подозрении на сахарный диабет как причину кровоточивости десен необходимо назначают глюкозотолерантный тест, определение гликированного гемоглобина в крови, определение уровня глюкозы в крови натощак и в течение дня.
Синонимы: Анализ крови на ГТТ; Пероральный глюкозотолерантный тест (ПГТТ); Тест на толерантность к глюкозе; Проба с 75 граммами глюкозы. Glucose Tolerance Test (GTT); Oral Glucose Tolerance Test (ОGTT). Краткое описание исследования «Глюкозотолерантный тест с определением гл.
Инфекция Helicobacterpylori является одной из наиболее распространенных в мире. К ассоциированным с Helicobacterpylori болезням относят хронический гастрит, язвенную болезнь желудка и двенадцатиперстной кишки. Полость рта - это вторичный резервуар и дополнительный источник реинфицирования организма Helicobacterpylori. Цель исследования: изучение особенностей клинического течения заболеваний слизистой оболочки полости рта, ассоциированных с Helicobacterpylori, до и после эрадикации. В ходе выполнения работы было проведено комплексное стоматологическое обследование 108 пациентов в возрасте от 18 до 55 лет. Всем больным с заболеваниями слизистой оболочки полости рта, ассоциированными с Helicobacterpylori, было рекомендовано комплексное, индивидуализированное, этиопатогенетическое, обоснованное, последовательное, динамичное, симптоматическое лечение, состоящее из общего и местного. Было выявлено, что Helicobacterpylori способствует увеличению степени тяжести заболевания слизистой оболочки полости рта. Лечение заболеваний слизистой оболочки полости рта, ассоциированных с Helicobacterpylori, необходимо проводить совместно с гастроэнтерологом, неврологом (психологом, психотерапевтом) с согласованием схем местного и общего лечения.

1. Арутюнов С.Д. Особенности состояния тканей пародонта у больных язвенной болезнью двенадцатиперстной кишки, ассоциированной Helicobacterpylori / С.Д. Арутюнов, И.В. Маев, Н.В. Романенко // Пародонтология. – 2005. – № 3. – С. 30-33.
3. Исаков В.А. Диагностика и лечение инфекции, вызванной Helicobacterpylori: IV Маастрихтское соглашение // Новые рекомендации по диагностике и лечению инфекции H.pylori – Маастрихт IV (Флоренция). – 2012. – Вып.2. – С.4-23. – (BestClinicalPractice).
4. Терапевтическая стоматология / Боровский Е.В. [и др.]. – М.: Медицинское информационное агентство, 2006. – 840 с.
5. Diagnosis and epidemiology of Helicobacter pylori infection / X. Calvet, M.J. RamírezLázaro, P. Lehours, F. Mégraud // Helicobacter. – 2013. – № 18. – Р. 5-11.
6. Graham D.Y. Compilobacter pylori and peptic ulcer disease // Gastroenterolgy. – 1998. – Vol. 96 (Suppl). – P. 615-625.
К ассоциированным с H. pylori болезням относят хронический гастрит, язвенную болезнь желудка и двенадцатиперстной кишки. Так, Н. pylori определяется у 95% больных с язвенной болезнью 12-перстной кишки, у 70-80% больных с язвенной болезнью желудка, у 50% больных с неязвенной диспепсией. Признана важная роль этого микроорганизма в развитии MALT-лимфомы и аденокарциномы желудка [3; 5].Выявлено присутствие Н. pylori в слюне, мягком зубном налете, зубной бляшке, гнойном содержимом пародонтальных карманов, на зубных ортопедических конструкциях [1]. Таким образом, полость рта - это вторичный резервуар и дополнительный источник реинфицирования организма H. pylori.
В современной литературе мало данных о проявлении геликобактериоза на слизистой оболочке полости рта, систематике этих проявлений, зависимости течения инфекции Н. pylori в желудочно-кишечном тракте и слизистой оболочке полости рта.
Изучение особенностей клинического течения заболеваний слизистой оболочки полости рта, ассоциированных с H. pylori, до и после эрадикации.
Материал и методы
В зависимости от степени обсемененности слизистой оболочки желудка H. pylori и наличия заболеваний слизистой оболочки полости рта пациенты были разделены на группы:
- 1-я группа – 27 человек, у которых было диагностировано наличие заболеваний слизистой оболочки полости рта, ассоциированных с H. pylori. Наличие в желудке H. pylori было выявлено гистологическим методом, уреазным дыхательным методом (Хелик-скан). Степень обсемененности слизистой оболочки желудка – слабая (+), до 20 микробных тел в поле зрения, при увеличении микроскопа х 630 (критерии Л.И. Аруина, 1995);
- 2-я группа – 29 человек, у которых было диагностировано наличие заболеваний слизистой оболочки полости рта, ассоциированных H. pylori. Наличие в желудке H. pyloriбыло выявлено гистологическим методом, уреазным дыхательным методом (Хелик-скан). Степень обсемененности слизистой оболочки желудка – средняя (++), до 50 микробных тел в поле зрения, при увеличении микроскопа х 630 (критерии Л.И. Аруина, 1995);
- 3-я группа - 24 человека, у которых было диагностировано наличие заболеваний слизистой оболочки полости рта, ассоциированных с H. pylori. Наличие в желудке H. pylori было выявлено гистологическим методом, уреазным дыхательным методом (Хелик-скан). Степень обсемененности слизистой оболочки желудка – высокая (+++), более 50 микробных тел в поле зрения, при увеличении микроскопа х 630 (критерии Л.И. Аруина, 1995);
- группу сравнения (4-я группа обследования) составили 28 человек, имеющие заболевания слизистой оболочки полости рта, без диагностированной сопутствующей общесоматической патологии. Отсутствие в желудке H. pylori было подтверждено уреазным дыхательным методом (Хелик-скан).
Диагностика H. pylori в желудке проводилась троекратно: до лечения (первичная диагностика) – всем пациентам, участвующим в исследовании; через 1 месяц после окончания курса выбранной схемы лечения (контроль эффективности выбранной схемы лечения); через 6 месяцев после проведенного лечения (оценка отдаленных результатов выбранной схемы лечения).
Уровень гигиены полости рта изучали с помощью упрощенного индекса гигиены ИГР-У (J.C. Green, J.R. Vermillion, 1964).Для исследования состояния тканей пародонта использовали папиллярно-маргинально-альвеолярный (РМА) индекс, модифицированный C.Parma в 1960 году.
Определение кислотности смешанной слюны осуществлялось дважды: до лечения и сразу после завершения назначенной схемы лечения, рН определяли потенциометрическим методом с помощью портативного рН-метра Марк-901. Забор слюны проводился с целью изучения состояния местного иммунитета полости рта, определяли количество сывороточных иммуноглобулинов А, G, M (IgA, IgG, IgM), секреторного иммуноглобулина А (sIgA), активность лизоцима в смешанной слюне (Liz), с подсчетом коэффициента сбалансированности факторов местного иммунитета (Ксб) у пациентов до лечения и после лечения по выбранным схемам.
Состояние слизистой желудка и двенадцатиперстной кишки оценивали по результатам заключения эзофагогастродуоденоскопии с исследованием биоптата на наличие H. pylori. Заключение о степени обсемененности желудка H. pylori было сделано с помощью гистологического метода диагностики.Уреазный дыхательный тест,из неинвазивных методов диагностики H. pylori в желудке, пациентам проводили с помощью комбинированного устройства ХЕЛИК-скан. Обследование проводилось всем пациентам, в утренние часы, натощак, троекратно: до лечения, через 1 месяц после лечения, через 6 месяцев после лечения.
Всем больным с заболеваниями слизистой оболочки полости рта, ассоциированными с H. pylori, было рекомендовано комплексное, индивидуализированное, этиопатогенетическое, обоснованное, последовательное, динамичное, симптоматическое лечение, состоящее из общего и местного.
Упациентов 1-й группы выявились такие заболевания слизистой оболочки полости рта, как десквамативный глоссит, рецидивирующий афтозный стоматит легкой степени тяжести (1-2 афты), гиперплазия грибовидных сосочков.

Рис.1. Заболевания слизистой оболочки полости рта у пациентов 1-й группы (слабая степень обсемененности желудка H. pylori)
У пациентов 2-й группы наблюдались такие заболевания слизистой оболочки полости рта, как десквамативный глоссит, рецидивирующий афтозный стоматит легкой и средне-тяжелой степени тяжести (3 афты), типичная и экссудативно-гиперемическая формы красного плоского лишая, ксеростомия.

Рис.2. Заболевания слизистой оболочки полости рта у пациентов 2-й группы (средняя степень обсемененности желудка H. pylori)
У пациентов 3-й группы регистрировались такие заболевания слизистой оболочки полости рта, как десквамативный глоссит, рецидивирующий афтозный стоматит средне-тяжелой и тяжелой (множественные афты) степени тяжести, эрозивно-язвенная и буллезная формы красного плоского лишая, плоская и веррукозная формы лейкоплакии, ксеростомия, хронический атрофический кандидоз.

Рис.3. Заболевания слизистой оболочки полости рта у пациентов 3-й группы (высокая степень обсемененности желудка H. pylori)
При оценке интенсивности кариеса зубов у пациентов с заболеваниями слизистой оболочки полости рта, ассоциированных с H. pylori, среднее значение индекса КПУ высокое, распространенность кариеса 100%, в отличие от группы сравнения.
Среднее значение упрощенного индекса гигиены ИГР-У (J.C. Green, J.R. Vermillion, 1964), папилярно-маргинально-альвеолярного (РМА) индекса, модифицированного C.Parma, у пациентов с заболеваниями слизистой оболочки полости рта, ассоциированных с H. pylori, выше, чем в группе сравнения, что свидетельствует о плохой гигиене полости рта и необходимости обязательного и срочного проведения профессиональной гигиены полости рта, включающей щадящее удаление зубных отложений, обучение рациональной гигиене полости рта, подбор средств индивидуальной гигиены, контролируемую чистку зубов.
Особенности клинического течения рецидивирующего афтозного стоматита при обсемененности желудка H. pylori следующие: большее количество афт, удлиняется период их заживления с 7-10 дней до 2-3 недель, увеличивается диаметр афты.
Гиперплазия грибовидных сосочков диаметром 0,5-0,8 см, при обсемененности желудка H. pylori, сочетается с беловатым или беловато-сероватым плотным налетом на языке, указывая на гиповитаминоз витаминов группы В и нарушения процессов всасываемости витаминов в тонком кишечнике.
Основным этиологическим фактором, как известно, при красном плоском лишае является неврогенный, в анамнезе у большинства таких больных можно выявить сильный стресс, который спровоцировал рецидив заболевания.Эти пациенты страдают выраженной канцерофобией, плаксивы, раздражительны, насторожены. Однако красный плоский лишай встречается и при различной степени обсемененности желудка H. pylori, проявляясь в различных формах: типичной, экссудативно-гиперемической, эрозивно-язвенной, буллезной. При этом более выражен сосудистый рисунок слизистой оболочки полости рта, гиперемия, отек. Эрозии полигональной формы занимают обширную площадь, покрыты фибринозным налетом, кровоточат при легком прикосновении. Эпителизация эрозий при высокой обсемененности желудка H. pylori длительная, от 3-4 недель. Необходимо совместное составление схемы общего и местного лечения гастроэнтеролога, стоматолога и невролога (психолога, психиатра), для воздействия на этиопатогенез (стресс) и усугубляющий фактор течения заболевания (обсемененность полости рта и желудка H. pylori).
Хронический атрофический кандидоз при обсемененности желудка H. pylori характеризуется более выраженной гиперемией, сухостью в полости рта, галитозом, отпечатками зубов на боковой поверхности и кончике языка, долго незаживающими (от 7 до 23 дней) трещинами в уголках губ, покрытыми тонкими и мягкими чешуйками перламутрового цвета.
Таким образом, в результате обследования пациентов с заболеваниями слизистой оболочки полости рта, мы выявили, что H. pylori способствует увеличению степени тяжести заболевания слизистой оболочки полости рта.
Заболевания слизистой оболочки полости рта, ассоциированные с H. Pylori, имеют следующие закономерности: более длительный период заживления, более выраженное воспаление, больший по площади очаг поражения, частые рецидивы заболеваний. Высокий уровень КПУ, 100% распространенность кариеса зубов, низкий уровень гигиены полости рта способствуют поддержанию воспаления,изменению микробного ландшафта и кислотно-щелочного баланса полости рта.
Лечение заболеваний слизистой оболочки полости рта, ассоциированных с H. pylori, необходимо проводить совместно с гастроэнтерологом, неврологом (психологом, психотерапевтом) с согласованием схем местного и общего лечения.
Рецензент:
Читайте также:

