Хеликобактер пилори во рту и влагалище
Обновлено: 25.04.2024
Одной из закономерностей, характерных для нормальной микрофлоры желудочно-кишечного тракта, является определенная качественная и количественная специфичность ее в различных отделах пищеварительного тракта, обусловленная морфологическими и функциональными особенностями соответствующих отделов. Общепризнанной в последние десятилетия являлась этиологическая роль Хеликобактер пилори (Helicobacter pylori) в развитии воспалительных заболеваний желудка и 12-перстной кишки (хронического гастрита, язвенной болезни, рака желудка). Попробуем разобраться, так ли это в действительности.
Состав микрофлоры ЖКТ
Полость рта – входные ворота для микроорганизмов. Оптимальные и стабильные условия для жизнедеятельности микроорганизмов в полости рта (температура, влажность, питание и др.) приводят к тому, что качественный состав микрофлоры чрезвычайно разнообразен и постоянен. Общее количество микроорганизмов в 1 мл слюны примерно находится на таком же уровне, как в дистальных отделах толстой кишки и составляет 10^7 и 10^8, но отличается видовой специфичностью. Среди бактерий доминируют стрептококки, составляющие 30-60%.
Содержимое желудка у 10% здоровых людей стерильно благодаря бактериостатическому и бактерицидному действию соляной кислоты и лизоциму, при сохраненной желудочной секреции, не превышает 10^3 микроорганизмов в 1 мл желудочного сока и преобладают анаэробные микроорганизмы.
По данным Drazer B.A. et al, 1969, Bauchop N.,1971, Browning et al., 1974 и др., у здоровых лиц в слизистой оболочке желудка и желудочном соке наблюдаются: бактериоиды, лактобактерии, энтеробактерии, вейлонелла, стрептококки, стафилококки, микрококки, нейссерии, кампилобактер и др., всего более 14-22 видов бактерий. Среди микрофлоры преобладают стафилококки и стрептококки, грамотрицательные бактерии.
Исследования последних лет по данным разных авторов показал, что у здоровых людей выделяется от 6 – 85% хеликобактер пилори и в 46% определяются антитела к хеликобактеру, у некоторых людей в желудке вместе с хеликобактером определяются кандиды. Основная масса бактерий обитает в пилорическом (выходном) отделе желудка, у здоровых лиц выделяются в 44,4% случаев Н.pylori., в 55,5% — стрептококки, в 61.1% — стафилококки, в 50% молочнокислые лактобациллы, в 22,2% грибы рода Candida и др. Из биоптатов слизистой желудка разных отделов желудка обнаружены Н.pylori — в 33,3%, стафилококки -в 61,1%, стрептококки и лактобациллы встретились в 44,4% случаев и в 27,7% — грибы рода Candida и др. микроорганизмы. Представляется чрезвычайно интересным сочетанность выявления микроорганизмов в слизистой оболочке различных отделов желудка.
Такое разнообразие представителей микрофлоры желудка составляет микроэкологию желудка у здорового человека и нарушение ее приводит к проявлением патогенных свойств микроорганизмов, относящихся к условно-патогенной микрофлоре (H.pylori, стафилококки, стрептококки, Candida, коринобактерии и другие) и находящихся в избыточном количестве в желудке, наряду с другими причинными факторами, может способствовать или поддерживать патологические процессы в желудке.
К вопросу о Хеликобактер пилори
Высока распространенность хеликобактериоза, составляющая две трети населения Земного шара, в Азии и Африке -100% населения (Av.J.Gastroenterol.1999), но риск развития язвы составляет 1% в год или 10% за всю жизнь. Тотальное уничтожение НР (Хеликобактер пилори ) в Германии и Англии не выявило связи между наличием НР и раком желудка. В Японии, несмотря на уничтожение НР, рак желудка лидирует среди причин смерти (Kurihara,1998). По-видимому, Helicobacter pylori не может рассматриваться как единственный этиологический фактор хронического гастрита и язвенной болезни. Следует говорить о нарушении в целом микроэкологии желудка, состоящей из различных представителей условно-патогенной и облигатной флоры.
Концепция первичной ответственности НР при язвенной болезни дефекта при сохранении НР на слизистой желудка не отвечает особенностям заболевания, таким как цикличность течения, различные ритмы рецидивирования, успешное рубцевание язвенного, рецидивы язвы при отсутствии НР, высокая степень заживления язв на плацебо (30%). НР – реальность, которая сосуществует с человеком на протяжении тысячелетий и не может не иметь полезных свойств и является компонентом микрофлоры желудка.
Некоторые эпидемиологи и гастроэнтерологи считают, что лечение хеликобактер пилори и другой микрофлоры желудка ведет к резкому нарастанию изжоги, на 8% в год увеличивается частота рака пищевода. Недавние исследования показали, что хеликобактер пилори увеличивает синтез гормонов лептина, снижающего аппетит и грелина, вызывающего голод. После лечения – уничтожения микрофлоры желудка — пациенты набирают массу тела и повышается уровень холестерина в крови, возможной причиной которых может быть нарушения микроэкологии желудочно-кишечного тракта.
В настоящее время известно, что причинами нарушений микрофлоры желудка могут быть препараты, которые применяются при заболеваниях желудка и 12-перстной кишки – это антисекреторные препараты и антациды, которые уменьшают кислотность желудочного сока, защищают слизистую желудка. Возникает дисбактериоз желудка, когда условно-патогенная флора становится патогенной (может вызвать повреждения слизистой желудка – гастрит, язву). Доказано, что прием антацидов приводит к повышенному росту энтеробактера, хеликобактер пилори, стафиолококка, пропионобактерий и др.
При эрадикационной терапии легко развивается резистентность к препаратам. По мнению Директора Германского Национального центра по изучению НР, доктора Kist, в настоящее время 50% больных имеют штаммы НР, устойчивые к антибиотикам. Таким образом, язвенную болезнь необходимо лечить всеми известными способами, не забывая о микроэкологии желудка, которая является отделом желудочно-кишечного тракта.
В настоящее время в диагностике нарушения микробиоценоза желудка предпочтение отдано роли хеликобактер пилори, определению кандид.
Диагностика инфекции Хеликобактер пилори
- Инвазивные методы диагностики — исследование в биоптатах слизистой оболочки желудка, полученных при эндоскопическом исследовании, с помощью гистологии, бактериологии или быстрого уреазного теста (Хелпил=тест).
- Неинвазивные методы диагностики — уреазные дыхательные тесты (с мочевиной, меченной С13, или мочевины). Следует отметить,что уреазной активностью обладают все штаммы хеликобактера, а также стафилоккоки, стрептококки, микрококки, кандиды, псевдомонады и другие представители условно-патогенной флоры желудка.
- Количественный ИФА концентрации антигена H.pylori в кале – высокоэффективный метод для первичной диагностики и контроля эрадикационной терапии.
- Иммунологические методы:
- иммуноблот для определения в крови Ig G / Ig A-антител против различных антигенов Helicоbacter pylori, обладающих патогенностью – Cag A и Vac A белки (используется редко),
- серологический метод — ИФА содержания антител против Н.pylori в сыворотке крови Ig G и Ig A (высоко специфичный метод диагностики и контроля лечения),
- серологический метод – ИФА содержания антихеликобактерных антител в слюне (чувствительность и специфичность уступают исследованию антител в сыворотке крови),
- экспресс-тест на основе иммунопреципитации и иммунохроматографии капиллярной крови пациента (не применяется у детей, при контроле лечения в виду низкой чувствительности).
Наличие инфицирования хеликобактер пилори должно быть доказано двумя методами. Диагностики хеликобактерной инфекции, разработанные в настоящее время, отражают нарушение микроэкологии желудка в целом и требуют новых подходов к профилактике и лечению этих нарушений.
Лечение Хеликобактер пилори
Эрадикационная терапия
Эволюция применяемых методик диагностики и лечения хеликобактериоза желудка за последние 10 – 12 лет, использование различных схем лечения с увеличение компонентов эрадикационной терапии, количества и доз антимикробных средств, продолжительности лечения, убедительно демонстрирует недостаточность положительных результатов.
В России отмечаются наиболее низкие показатели эффективности эрадикационной терапии хеликобактера, что возможно связано с со следующими факторами:
- высокой степенью обсемененности слизистой оболочки желудка,
- мутацией микроорганизмов,
- резистентностью хеликобактер пилори к используемым антибактериальным средствам,
- генетическим полиморфизмом генов цитохрома Р-4590, снижающих эффективность антисекреторных препаратов (ИПП),
- иммуногенетическими особенности макроорганизма,
- низкой комплаентности (приверженности) пациентов к лечению,
- развитием побочных эффектов.
Фитотерапия
Принципы коррекции нарушений микроэкологии желудка включают в себя применение антибактериальных препаратов пре- и пробиотиков, фитопрепараты.
Исходя из принципов коррекции микроэкологии желудочно-кишечного тракта, изложенных ранее, возможно использование уже описанных препаратов фитотерапии и лекарственных средств. В добавление к вышеизложенному можно добавить известный опыт американских ученых, которые показали, что прием имбиря активно угнетает рост условно-патогенной флоры желудка и, в том числе, НР. Солодка, издавна использовалась при лечении язв желудочно-кишечного тракта. Исследования, проведенные в институте медицинской микробиологии и вирусологии в Германии, показали, что экстракт солодки уничтожает штамм НР, устойчивый к кларитромицину — одному их трех компонентов антихеликобактерной терапии (Fukai T, et al.,2003). Исследования показали, что антихеликобактерными свойствами обладает большое число растений: лук, чеснок, тмин, берберин, куркума и др.
Нами проведены исследования, целью которых явилась оценка эффективности применения фитотерапевтических сборов и бактериальных пробиотиков в лечении и профилактике язвенной болезни, ассоциированной с хеликобактерной инфекцией. Приводим растительные сборы, разработанные фитотерапевтом Михальченко С.И.
Состав: Сабельник болотный, бадан, кубышка, душица, зверобой продырявленный, кровохлебка обыкновенная, лист и почки березы, корни лабазника, калган, золотарник обыкновенный, исланский мох.
Состав: калган (корни), кровохлебка (корни), зверобой продырявленный, пастушья сумка (трава), ромашка(соцветия), пустырник (трава, исланский мох (слоевище), кипрей узколистный, кубышка, почки тополя, золотарник обыкновенный (трава), кора дуба.
Применение: 1 десертную ложку сбора залить 500 мл кипятка, настоять ночь в фарфоровой посуде или термосе, процедить.
Прием: по 150 мл 3 раза в день за 30 минут до еды. 10 дней пить, 2 дня перерыв, лечебная порция сбора 200-400 г. Курс лечения 1-3 месяца.
Лечение фитотерапевтическими сборами сочеталось с разработанными нами прерывистыми курсами бактериальных пробиотиков не более 10 дней. Исследования показали, что применение фитотерапии и пробиотиков в лечении язвенной болезни обладает антихеликобактерной направленностью, точнее восстановлением нарушений микроэкологии желудка и соответственно улучшает течение язвенной болезни.
Информацию из данного раздела нельзя использовать для самодиагностики и самолечения. В случае боли или иного обострения заболевания диагностические исследования должен назначать только лечащий врач. Для постановки диагноза и правильного назначения лечения следует обращаться к Вашему лечащему врачу.
Хеликобактериоз: причины появления, симптомы, диагностика и способы лечения.
Определение
Хеликобактериоз – инфекционное заболевание, поражающее пилорический отдел желудка, или привратник, и двенадцатиперстную кишку. Его возбудителем является уникальная патогенная микроаэрофильная грамотрицательная бактерия хеликобактер пилори (H. pylori). Свое название бактерия получила за счет отдела желудка, в котором она обитает – пилорического.
В результате микроорганизм еще сильнее колонизирует слизистую оболочку, формирует ее повышенную восприимчивость к соляной кислоте и провоцирует воспаление, приводящее к развитию язвенных дефектов.
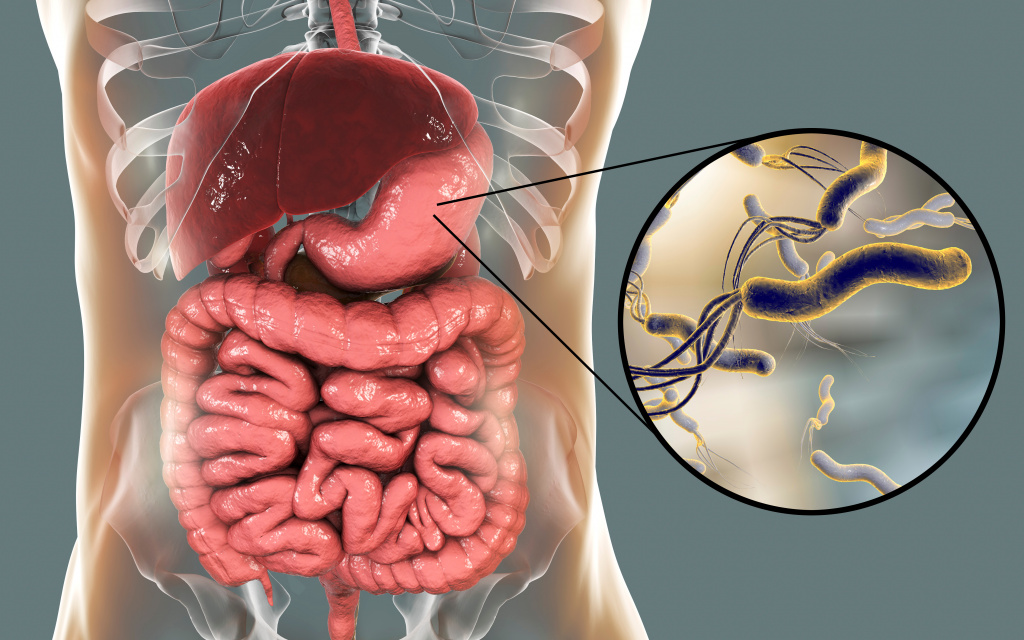
Хеликобактер пилори – спиралевидная бактерия длиной 3,5 и шириной 0,5 микрон. Она имеет жгутики, с помощью которых свободно перемещается по стенке желудка либо надежно на ней закрепляется. Бактерия H. pylori очень изменчива, ее штаммы (разновидности) отличаются друг от друга способностью прикрепляться к слизистой оболочке желудка, вызывать воспалительный процесс и обладают разной степенью патогенности.

Хеликобактер пилори, колонизирующая слизистую оболочку желудка, — частая причина ее воспалительных изменений, она признана этиологическим фактором гастрита, а сам гастрит — инфекционным заболеванием. В зависимости от состояния защитных факторов желудка возникший инфекционный процесс может протекать латентно или с выраженной клинической симптоматикой воспаления. Согласно современным представлениям, H. pylori вызывает хронический гастрит у всех зараженных лиц. Это может привести к язвенной болезни, атрофическому гастриту, аденокарциноме желудка или низкодифференцируемой лимфоме желудка. H. pylori относится к канцерогенам первого порядка.
Результаты многочисленных исследований дают основание предполагать возможную патогенетическую или опосредованную роль инфекции H. pylori в развитии и/или течении заболеваний, не относящихся к пищеварению: кардио-, цереброваскулярных, аутоиммунных заболеваний, заболеваний крови, кожи, нервной системы и многих других.
Патоген отличается относительной устойчивостью к окружающей среде: при кипячении хеликобактерии гибнут практически мгновенно, при обработке дезинфицирующими составами — в течение нескольких минут.
Причины появления хеликобактериоза
Заразиться бактерией можно при контакте с загрязненной водой или продуктами питания. Инфицирование возможно во время проведения эндоскопии и при использовании других плохо стерилизованных медицинских инструментов, которые имели прямой контакт со слизистой желудка пациента.
Бытовой способ передачи (например, через поцелуи, личные вещи и проч.) также возможен, о чем свидетельствует выделение бактерии из слюны и зубного налета.
Распространенность инфекции варьируется в зависимости от географического региона, возраста пациента, его этнической принадлежности и социально-экономического статуса. По данным Департамента здравоохранения г. Москвы (2019), распространенность этой инфекции в Москве составляет 60,7–88%, в Санкт-Петербурге - 63,6%, в Восточной Сибири достигает 90%.
Классификация заболеваний
Заболевания, связанные с H. pylori:
- гастрит,
- дуоденит,
- гастродуоденит,
- эзофагит,
- язвенная болезнь желудка,
- язвенная болезнь двенадцатиперстной кишки,
- железодефицитная анемия неясного генеза,
- рак желудка,
- рак двенадцатиперстной кишки.
Основной жалобой, с которой больные с признаками Helicobacter-инфекции обращаются к врачу, являются желудочные боли. Локализация симптома может меняться и переходить в область расположения двенадцатиперстной кишки.
Боли бывают острыми, ноющими, тупыми, возникают в верхних отделах живота слева и по центру в околопупочной области. Дискомфорт может возникать при длительном голодании, натощак или через определенное время после приема пищи.
Симптоматика хеликобактериоза зависит от клинической формы заболевания и может включать:
- чувство тяжести в животе после еды;
- нарушение аппетита, связанное с внезапными приступами тошноты (если слизистая желудка сильно травмирована);
- беспричинная рвота на фоне нормальной температуры тела;
- изжога (жгучие ощущения в пищеводе и даже гортани) и отрыжка с неприятным кислым или горьким привкусом;
- хронические запоры (отсутствие дефекации в течение трех суток и более);
- разжижение каловых масс, появление пенистой или водянистой консистенции;
- кишечные спазмы и вздутие живота.
- снижение аппетита до полного его отсутствия;
- тошнота может сменяться рвотой со сгустками крови;
- резкое снижение массы тела, не являющееся нормой;
- сухость во рту и привкус металла;
- появление белого налета на языке;
- неприятный запах изо рта при отсутствии кариеса;
- заеды в уголках рта;
- кровоточивость десен.
Диагностика хеликобактериоза
Долгое время хеликобактериоз может никак себя не проявлять, при этом провоцируя развитие язвы, аденокарциномы или мальтомы желудка. В особой зоне риска люди, чьи родственники имеют эти заболевания в анамнезе.
Диагностика может быть инвазивной (эндоскопия с последующей биопсией желудочных тканей) и неинвазивной (лабораторные исследования).
Согласно международным рекомендациям, методами выбора для диагностики бактерии и оценки эффективности лечения H. pylori служат дыхательный̆ тест с мочевиной, меченной 13С и определение специфических антигенов H. pylori в кале иммунохроматографическим методом.
Синонимы: Дыхательный тест с 13С-меченной мочевиной. 13 UBT; 13C-UBT. Краткая характеристика 13С-уреазного дыхательного теста Дыхательный тест в текущей модификации предназначен для лиц старше 12 лет. 13С-уреазный дыхательный тест относится к неинвазивным безопасным методам исследования.
Оксана Михайловна Драпкина, профессор, доктор медицинских наук:
– Сейчас мы передаем слово профессору Юрию Павловичу Успенскому. Юрий Павлович расскажет о хеликобактер пилори и о грибах рода Candida, что их объединяет у гастроэнтерологического больного.
Юрий Павлович Успенский, профессор, доктор медицинских наук:
– Дорогие коллеги, мы с вами прекрасно знаем, что благодаря эпохальному открытию колоссальной роли пилорического хеликобактера в развитии хронического гастрита, язвенной болезни, рака желудка, уже к концу 90-х годов стало очевидным, что количество вновь выявленных случаев язвенной болезни уменьшается, что даже дало возможность гастроэнтерологам заявить о том, что XX век – это век уходящей язвенной болезни, а XXI – это век рождающейся гастроэзофагеальной рефлюксной болезни.
Однако, к сожалению, тенденции последнего времени оказались не столь оптимистичны и основные проблемы связаны все-таки с уменьшающейся эффективностью эрадикационной терапии. Причины этого лежат в плоскости возрастающей резистентности хеликобактер пилори к антибактериальным препаратам, которые входят в состав схем традиционной эрадикационной терапии.
Так один из патриархов, профессор Мегро (F.Megraud), отметил, что резистентность к кларитромицину, согласно молекулярно-генетическим методам, в Европе достигает 46%. Что же происходит при этом? При этом происходит драматическое снижение эффективности эрадикационной терапии, которая не превышает 18%. Что касается Российской Федерации, то диапазон вариаций резистентности к кларитромицину весьма широк. Почему-то в нашем северо-западном регионе наиболее высока резистентность к кларитромицину в Санкт-Петербурге. Причем это были абсолютно независимые исследования: педиатрический анклав профессора Корниенко Е.А., наши исследования доктора Барышниковой Н.В., исследования института Пастера. Причем были разные методы, и все они дали крайне высокие (более 30%) цифры резистентности к кларитромицину.
Коллеги, говоря о новых антибактериальных препаратах как варианте преодоления резистентности к антибиотикам, повышения эффективности эрадикационной терапии, хотелось бы сказать, что все-таки этот путь достаточно опасный, а может быть, даже и тупиковый, потому что тем самым мы способствуем воспитанию полирезистентных штаммов к антибиотикам хеликобактер пилори.
И на самом деле неконтролируемое потребление антибиотиков, это глобальная проблема человечества. Не столь давно, 18 ноября 2012 года, состоялся Европейский день осведомленности о проблеме резистентности и потребления антибиотиков, когда была предложена мировая стратегия борьбы с распространением резистентных форм микроорганизмов.
Непосредственное влияние препаратов висмута на хеликобактер пилори было продемонстрировано в виде целого ряда грамотно организованных исследований, и связаны были эти действия с блокированием адгезии хеликобактера с прямым ингибированием энзимов и уреазы этого микроорганизма.
Кроме того, в последние годы утвердилась концепция активно разрабатываемой школы профессора Кононова в Омске о том, что даже в случае успешно проведенной эрадикационной терапии формируется воспалительный инфильтрат (из-за продукции цитокинов, из-за продукции активных форм кислорода), и он сохраняется достаточно долго – от 1 до 12 месяцев. Поэтому и в этой связи включение препаратов висмута в комплекс эрадикационной терапии является оправданным с клинической точки зрения, потому что при этом происходит подавление ассоциированного воспаления из-за уменьшения продукции цитокинов, увеличения продукции цитопротективных простагландинов, и, соответственно, увеличение эпидермального фактора роста.
Какая же висмутсодержащая схема эрадикации является предпочтительной? Право на существование имеет и та схема, о которой мы сейчас говорили, когда висмут добавляется к стандартной терапии, и 10-дневная схема, о которой говорила Татьяна Львовна (висмут, метронидазол, тетрациклин и ингибитор протонного насоса). Все они обеспечивают достаточно высокий и эффективный уровень эрадикации.
А какая же связь между пилорическим хеликобактером и грибами рода Candida? Согласно нашим исследованиям, оказалось, что у одних и тех же больных экспрессируются гены, которые кодируют как факторы патогенности хеликобактер пилори, так и факторы адгезии и инвазии грибов рода Candida. А грибы рода Candida albicans действительно обладают факторами вирулентности, факторами адгезии, инвазии. Связь между концентрацией грибов рода Candida в толстой кишке и степенью обсемененности хеликобактер пилори антрального отдела желудка достаточно четко выражена и была продемонстрирована еще 10 лет назад в работах М.М. Захарченко.
Что происходит под влиянием антибактериальной терапии с грибами рода Candida? Их популяция неуклонно растет как следствие прямого стимулирующего действия (есть данные, что больные с кандидемией, то есть с кандидосепсисом, получали 4 и более антибиотиков), а также вследствие ингибирующего влияния на бактерии-антагонисты грибов рода Candida.
Что же такое грибы рода Candida? Посмотрите, вот эти данные показывают, что, оказывается, это транзиторные микроорганизмы, они обнаруживаются и в мороженом, и в других кисломолочных и молочных продуктах. То есть, на первый взгляд, нет ничего страшного в их присутствии, они транзитом проходят через организм человека. Но так происходит лишь тогда, когда иммунологическая реактивность макроорганизма достаточно высока. А если она низка, если это человек, страдающий иммунодефицитом, получающий гормональную терапию, если это ослабленный больной, тогда реален риск инвазии грибов рода Candida в слизистой оболочке, развития кандидоза пищевода, толстой кишки, транслокации микроба через кишечную стенку вплоть до развития кандидемии и кандидосепсиса.
В ряде случаев при пониженной иммунной резистентности макроорганизма инвазивный кандидоз не развивается, но возможно развитие неинвазивного кандидоза, когда увеличивается концентрация грибов рода Candida в просвете кишечника. Но и при этом ситуация далека от благополучной, потому что в этих условиях имеет место сенсибилизация, интоксикация организма, формирование вторичного иммунодефицита и присоединение микст-инфекции. Потому что грибы рода Candida обладают целым рядом ферментных, полисахаридных и иных факторов агрессии и патогенности.
Критерием диагностики неинвазивного кандидоза кишечника и повышенной пролиферации грибов рода Candida является снижение числа нормобиоты ниже 100 миллионов колониеобразующих единиц на грамм фекалий и рост грибов рода Candida ssp. при посеве кала выше 1000 колониеобразующих единиц на грамм фекалий.
Наличие тесной патогенетической взаимосвязи между грибами и хеликобактером подтверждает то, что в 98% образцов грибов рода Candida, выделенных из слизистой, детектируется хеликобактер пилори. И в большинстве образцов содержится ген острова патогенности cag A.
В другой работе показано, что также из грибов, выделенных из ротовой полости, идентифицируется присутствие генов хеликобактер пилори и почти в 100% случаев наблюдается гомологичность между генами грибов и генами контрольной популяции хеликобактера.
Согласно отечественной работе у детей с HP-ассоциированным гастродуоденитом с возрастом увеличивается число высокопатогенных штаммов микроорганизма хеликобактер пилори. Но при этом имеется сопряженность роста таких штаммов с увеличением гена sap2. Это ген, который кодирует синтез фактора вирулентности грибов рода Candida с 41,2% до 100% у детей, достигших 17-18 лет.
Таким образом, в последние годы сформировалась концепция, что дрожжеподобные микромицеты являются естественным биологическим резервуаром для грибов рода Candida. То есть что же при этом происходит? Татьяна Львовна уже говорила сегодня о стратегиях выживания пилорического хеликобактера. Но они не ограничиваются одной лишь уреазной активностью. Дело в том, что хеликобактер – это вообще весьма уязвимый организм, крайне чувствительный и к температурным условиям, и к пищевым, и желчным детергентам. Поэтому для своего выживания он способен пенетрировать капсулу и клеточную стенку гриба рода Candida, адгезировать плазменную мембрану гриба с образованием вакуоли и располагаться внутри этого организма, приобретая устойчивость к изменяющимся условиям среды, в том числе температурным, пищевым и желчным детергентам.
Вот и очень интересная работа, которая была выполнена 10 лет назад. Она показывает, что взаимоотношения между грибами и хеликобактером являются, по сути, эквипотенциальными. Их такая комбинация увеличивает и вирулентность грибов рода Candida. А проведенная эрадикационная терапия, даже в случае своей успешности, достоверно уменьшает частоту выявления хеликобактера в желудке, но увеличивает частоту выявления грибов рода Candida.
Что же делать в этой ситуации? По всей видимости, необходим поиск инновационных подходов к диагностике коррекции кандидозы такого рода пациентов. И сложность заключается в том, что среди традиционно принятого в гастроэнтерологии методов лечения, методы, направленные на предотвращение экспансии Candida spp., по сути, отсутствуют. Равно как и отсутствует антикандидозная активность у всех антибактериальных средств, входящих в состав классической эрадикационной терапии. А между тем такие пути необходимо искать, потому что грибы, как мы уже с вами говорили, способны помимо кишечника заселять другие анатомические и экологические ниши организма и в полной мере проявлять свои патогенные свойства.
К путям минимизации риска развития и прогрессирования кандидоза органов пищеварения при использовании эрадикационной терапии можно отнести исключение из эрадикационного комплекса антибиотика с потенциально высокой резистентностью к ним и включение в терапию первой линии препаратов висмута. Кроме того, у ряда пациентов требуется дополнительное назначение нерезорбцируемых антимикотических препаратов.
Пока же позвольте сделать заключение о том, что кандидоз органов пищеварения – это междисциплинарная проблема и для ее решения нужна интеграция усилий гастроэнтерологической и микологической службы. Высокое представительство грибов рода Candida в составе желудочно-кишечной микрофлоры связано с плотностью бактериального обсеменения и вирулентностью микроорганизма в хеликобактер пилори. Перспективным же путем повышения эффективности и безопасности эрадикационной терапии, а также элиминации грибов рода Candida и профилактики прогрессирования кандидоза органов пищеварения является дополнительное включение в схемы эрадикационной терапии тем контингентам пациентов, о которых мы с вами выше говорили, препаратов висмута и нерезорбцируемых антимикотиков.
Еще не так давно считалось, что гастрит вызывают неправильное питание, еда всухомятку, стрессы и отсутствие горячего супа на обед. Потом ученые обнаружили связь этой болезни с бактерией хеликобактер пилори — и с тех пор подход к лечению заболеваний ЖКТ кардинально изменился.
Можно ли заразиться через посуду в ресторане, вызывает ли хеликобактер рак и нужно ли избавляться от бактерии, которая живет в организме 80% белорусов, рассказал врач-гастроэнтеролог с 40-летним опытом работы Георгий Матвеевич Усов.

Георгий Усов,
врач-гастроэнтеролог высшей категории
Минского клинического консультативно-диагностического центра,
кандидат медицинских наук
— Что такое хеликобактер? Это патогенная бактерия или условно-патогенная?
— Хеликобактер пилори (Helicobacter pylori) — бактерия, которая была открыта австралийскими учеными Робином Уорреном и Барри Маршаллом. За это открытие в 2005 году они получили Нобелевскую премию.
Хеликобактер — патогенная бактерия. Наличие ее в организме человека приводит к поражению слизистой оболочки желудка и двенадцатиперстной кишки и развитию таких заболеваний, как хронический гастрит, язва желудка и двенадцатиперстной кишки, рак желудка, мальтома желудка.
Сегодня хеликобактер — самая распространенная хроническая инфекция в мире.
— Какие факторы в таком случае провоцируют развитие гастрита, язвы, рака? И могут ли эти болезни возникнуть без участия хеликобактера?
— При наличии хеликобактера у всех людей выявляется какое-либо заболевание желудка. Выявление конкретного заболевания зависит от штамма хеликобактера. Штаммы H. руlori, имеющие в своем составе определенные генотипы, предрасполагают к развитию язвенной болезни и рака желудка. И если язвой желудка и двенадцатиперстной кишки или онкологическими заболеваниями заболевают не все инфицированные люди, то гастритом — все.

Верно и то, что данные болезни могут возникать и без хеликобактер пилори.
- Кроме гастритов, связанных с хеликобактером, имеются гастриты, связанные с забросом содержимого двенадцатиперстной кишки в желудок, так называемые рефлюксные (химические) гастриты, гастриты, связанные с образованием антител к слизистой оболочке желудка (аутоиммунные гастриты).
- Причиной язв может быть прием нестероидных противовоспалительных препаратов, ацетилсалициловой кислоты, изредка нервные факторы, погрешности в еде.
- Причиной раковых заболеваний могут быть погрешности в питании, канцерогенные вещества, поступающие в пищу, курение, наследственная предрасположенность и др.
— Как передается эта бактерия человеку? Можно ли заразиться от животных? А в ресторане через посуду?
— Путь передачи хеликобактера контактно-бытовой. Бактерия передается:
- через недостаточно чистую посуду, когда люди едят из одной тарелки или пьют из одной чашки, едят пищу друг у друга;
- в семье, когда родители пробуют пищу перед тем, как дать ее ребенку, или облизывают соску малыша;
- в случае использования людьми одной зубной щетки;
- через губную помаду;
- при отсутствии мытья рук после туалета и перед едой;
- через сексуальные поцелуи.
Хеликобактер также выявлен у кошек и собак, вследствие чего существует возможность заражения человека от них. Что касается ресторана, то, если грязная посуда плохо обрабатывается, появляется высокая возможность заражения хеликобактером.
— Какой процент людей в Беларуси живет с хеликобактером? Почему этот показатель выше, чем в Западной Европе и США?
— Качественных эпидемиологических исследований по распространению хеликобактера среди населения Беларуси не проводилось. Проводились лишь относительно небольшие исследования среди населения отдельных областей и отдельных групп населения.
Считается, что распространенность хеликобактера среди белорусов составляет около 70-80%.
Среди населения РФ по ряду исследований в отдельных российских регионах распространенность составляет от 65 до 90%. Данный показатель выше, чем в Западной Европе и США, в связи с недостаточно качественным соблюдением гигиены в нашей стране.

— Какие симптомы должны заставить человека сдать анализ на хеликобактер? Какие из них неочевидные, не связанные напрямую с ЖКТ?
— Диспепсические расстройства (боли, жжение в эпигастральной области — верхних отделах живота, тошнота, плохой аппетит, тяжесть в эпигастральной области, рвота и т. д.) требуют обследования на хеликобактер.
В некоторых случаях хеликобактер может быть причиной также:
- железодефицитной анемии;
- халитоза (плохого запаха изо рта);
- крапивницы.
Однако следует помнить, что данные заболевания могут возникать и по множеству других причин.
— Какие анализы на выявление хеликобактер существуют? Какие из них самые объективные?
— Существует несколько разновидностей анализов.
- Гистологическое исследование биопсийного материала из слизистой желудка, причем следует исследовать слизистую как антрального отдела, так и тела желудка.
- Быстрый уреазный тест. Тест выполняется в момент гастроскопии. Биопсия слизистой берется из полости желудка, помещается в среду, содержащую мочевину и такой индикатор, как феноловый красный. Уреазы преобразуют мочевину в аммиак, вследствие чего повышается рН среды, и желтый цвет образца (отрицательный) меняется на красный (положительный).
- С13-уреазный дыхательный тест на немецкой аппаратуре, достоверность которого более 92%.
- Российская модификация дыхательного теста — хелик-тест, достоверность которого, по данным ряда российских авторов, составляет от 30 до 80%.
- Определение антител к хеликобактеру IgM и IgG в крови.
- Исследование антигенов хеликобактера в кале.

Самыми объективными из анализов являются гистологический тест, С13-уреазный дыхательный тест на аппаратуре немецкой фирмы FAN, исследование антигенов хеликобактера в кале и быстрый уреазный тест. Исследование крови на антитела к хеликобактер пилори приемлемо при первичном исследовании до лечения хеликобактера. В то же время для контрольного исследования оно не годится, так как антитела к хеликобактеру остаются повышенными в течение нескольких лет в крови после излечения от хеликобактера, давая ложноположительный результат.
Хелик-тест из-за низкой достоверности нигде в мире, кроме нескольких стран СНГ, не применяется.
— Что делать, если анализ положительный? Влияет ли, например, количественное значение антител в крови на степень опасности бактерии для здоровья?
— При положительном анализе на хеликобактер решается вопрос о проведении антихеликобактерной терапии. На степень опасности для здоровья количественное значение хеликобактера существенного значения не имеет, ибо высокая обсемененность хеликобактером в ряде случаев в наших исследованиях приводила к значительно меньшим изменениям слизистой оболочки, чем низкая, или существенно не отличалась. Причина — в индивидуальной резистентности (восприимчивости) организма к хеликобактеру.
При незначительных превышениях IgA желательно провести другой метод исследования хеликобактера, например С13-уреазный дыхательный тест или исследование кала на антигены хеликобактера, чтобы подтвердить или опровергнуть положительный результат.

— Всегда ли положительный анализ говорит о необходимости лечения? В каких случаях хеликобактер не лечат?
— Раньше считалось, что лечение хеликобактера следует проводить, только если имеются клинические проявления заболевания. Сейчас в связи с выявлением существенной роли хеликобактера в развитии рака желудка лечение рекомендуют проводить всем больным с хеликобактерной инфекцией.
В некоторых странах, в частности, Японии, лечение хеликобактера проводится всем больным бесплатно. При этом тем людям, которые отказываются лечиться от хеликобактера, при развитии у них рака желудка не оплачивают страховку.
У лиц с язвами желудка и двенадцатиперстной кишки санация хеликобактера приводит к уменьшению появления новых язв в три раза.
Лечение хеликобактера НЕ проводят:
- больным с аллергией и/или непереносимостью препаратов, предназначенных для лечения хеликобактера;
- тем, у кого все схемы лечения оказались неэффективными;
- отказывающимся от лечения пациентам.
На мой взгляд, больным с хроническим гастритом, у которых имеются лишь незначительные изменения слизистой оболочки желудка, от лечения можно временно воздержаться.
Лечение детей не проводят: существует большая вероятность повторного заражения из-за нахождения в детском коллективе и развития ряда побочных реакций, особенно при повторном лечении. Для детей желательно выделение отдельной посуды и соблюдение правил личной гигиены.

— Какое лечение назначается?
— Излечиться от хеликобактера полностью возможно только при назначении антибиотиков и блокаторов протоновой помпы (антисекреторных лекарственных средств — прим. ред.), усиливающих эффект антибиотиков, в ряде случаев в сочетании с препаратами висмута.
В последнее время выявлено бактерицидное действие некоторых пробиотиков в отношении хеликобактера.
Например, существует препарат, содержащий инактивированные бактерии пробиотического штамма Lactobacillus reuteri. Однако подобные препараты полностью от хеликобактера не излечивают.
— Должны ли параллельно лечиться домашние? Может ли такое быть, что у одного из членов семьи есть хеликобактер, а у остальных — нет?
— Да, лечение взрослых членов семьи при наличии у них хеликобактера должно проводиться, детям из-за указанных выше причин — нет. При этом наличие хеликобактера у всех членов одной семьи необязательно. Это зависит от индивидуальной резистентности организма к бактерии. В исследованиях и клинической практике неоднократно были случаи, когда хеликобактер не обнаруживался у отдельных членов семьи. Поэтому лечению всегда должны предшествовать анализы.
Читайте также:

