Хламидийный уретрит у мужчин лечение препараты
Обновлено: 24.04.2024
Уретрит представляет собой воспалительное заболевание мочеиспускательного канала, которое может иметь как инфекционный, так и неинфекционный характер.
Чаще всего причиной уретрита являются передающиеся половым путём бактерии: гонококки, хламидии, микоплазмы и др., реже - вирусы и простейшие (трихомонады). Наиболее авторитетными и регулярно обновляющимися клиническими рекомендациями по диагностике и лечению инфекций урогенитального тракта сегодня являются рекомендации Центра Контроля Заболеваемости (CDC - Centres for Disease Control) [1] и Европейской Ассоциации урологов [2]. Данная статья представляет собой попытку обобщения основных положений этих рекомендаций касательно одного из наиболее распространённых заболеваний среди инфекций, передающихся половым путем - негонококкового уретрита.
Негонококковый уретрит (НГУ) считается полиэтиологичным заболеванием и может быть вызван различными возбудителями. Из года в год имеет место рост заболеваемости негонококковыми уретритами. С 1972 года этот показатель превосходит заболеваемость гонореей.
Наиболее часто выявляемым и потенциально опасным этиотропным агентом является хламидия (Chamydia trachomatis), являющаяся причиной негонококкового уретрита у 15-55 % больных. Немаловажным представляется и тот факт, что хламидии одновременно выявляются у 30-45 % больных гонореей. По современным эпидемиологическим данным, у молодых людей заболеваемость инфекциями, вызванными Chamydia trachomatis, каждый год увеличивается на 5 % [3].
Другими причинами негонококкового уретрита могут быть Ureaplasma urealyticum, Mycoplasma genitalium, Trichomonas vaginalis, вирус простого герпеса и аденовирус. Немаловажно, однако, что вызывать воспаление мочеиспускательного канала может и банальная флора, в частности, кишечная палочка (Esherichia coli). У 20-30 % больных причину негонококкового уретрита установить не удаётся. У большинства из них не представляется возможным убедительно доказать, что негонококковый уретрит был вызван микоплазмой, трихомонадами, вирусом простого герпеса, аденовирусом или другими микроорганизмами.
Инкубационный период при негонококковом уретрите составляет 1-5 недель с момента полового контакта, однако, зачастую имеет место и более продолжительный инкубационный период. Хламидийный уретрит может осложниться эпидидимитом, простатитом и синдромом Рейтера (сочетание уретрита с коньюнктивитом и артритом).
Воспаление мочеиспускательного канала у мужчин бывает бессимптомным, но все-таки чаще сопровождается характерными проявлениями: гнойными или слизисто-гнойными выделениями, резью или болью при мочеиспускании и повышенной чув ствительностью наружного отверстия мочеиспускательного канала.
Учитывая, что у больного негонококковым уретритом с большой долей вероятности причиной может являться микроорганизм, передающийся половым путем, важен сбор анамнеза интимной жизни за последние 2 месяца (количество половых партнерш, незащищённые барьерными методами оральные, генитальные и анальные контакты).
Лабораторным подтверждением диагноза "уретрит" является наличие при исследовании мазка по Граму > 5 полиморфноядерных лейкоцитов в п/зр (х 1000) и/или выявление более 10 лейкоцитов при исследовании осадка (х 400) первой порции мочи. Мазок из уретры с окраской по Граму позволяет не только документировать наличие воспалительного процесса, но и, при выявлении внутриклеточных грамотрицательных диплококков, с 99 % специфичностью и 95 % чувствительностью диагностировать уретрит гонококковой природы.
Культуральные методы идентификации возбудителей негонококковых уретритов (посев на среды куриных эмбрионов - для диагностики Chlamydia trachomatis, Mycoplasma IST тест - на Ureaplasma urealyticum и Mycoplasma hominis) обладают высокой специфичностью и позволяют определять чувствительность выявленного микроорганизма к антибиотикам. Чувствительность культуральных методов, однако, не очень высока и составляет 40-85 %. На сегодняшний день разработаны и используются высокочувствительные некультуральные методы диагностики основных возбудителей НГУ (Chamydia trachomatis, Mycoplasma genitalium, Ureaplasma urealyticum и Trichomonas vaginalis), такие как метод полимеразной цепной реакции (ПЦР), лигазной цепной реакции. В связи с высокой чувствительностью этих тестов, составляющей 70-95 %, для ПЦР может использоваться не мазок, а моча пациента. Эти методы заслуженно получают всё большее распространение в клинической практике в силу их информативности и возможности быстрого получения результата теста (обычно, через 24-36 часов).
Основными способами профилактики НГУ являются: ограничение/прекращение беспорядочных половых связей, а также использование барьерных методов контрацепции (презервативов) при генитальных, оральных и прочих интимных контактах.
Принципы лечения больного негонококковым уретритом следующие:
1. Назначение больному антибиотика.
2. Одновременное лечение полового партнера/половых партнеров, с которыми был контакт за последние 2 месяца.
3. Воздержание от интимной близости в течение 7 дней терапии.
Антибиотикотерапия назначается эмпирически исходя из известной чувствительности Chlamydia trachomatis, Mycoplasma genitalium и Ureaplasma urealyticum - микроорганизмов, наиболее часто вызывающих НГУ. Лечение должно проводиться таблетированными антибактериальными препаратами. Наиболее эффективными лекарственными средствами в отношении перечисленных выше возбудителей являются препараты группы тетрациклинов и макролидов. Инъекционная терапия при негонококковых уретритах нецелесообразна, а проведение каких либо инстилляций в уретру (как при негонококковых, так и при гонококковых уретритах) даже противопоказано в связи с доказанной опасностью хронизации воспалительного процесса.
В соответствии с современными международными клиническими рекомендациями [1, 2] препаратами выбора для лечения НГУ являются:
Доксициклин по 100 мг 2 раза в сутки 7 дней или азитромицин 1 г однократно.
В качестве альтернативных представлены следующие схемы лечения:
При трихомонадном уретрите рекомендуется назначение внутрь:
Поскольку у ряда больных этиотропный агент НГУ установить не удаётся, признаки воспаления после первичной терапии могут выявляться у 20-40 % пациентов, что обычно требует проведения дополнительного лечения альтернативными антибактериальными препаратами.
Следует отметить, что современные клинические рекомендации по лечению больных НГУ не лишены недостатков. Основным из них является тот факт, что за исключением случаев трихомонадной инфекции, выбор препарата для эмпирической терапии НГУ не зависит от выявляемого возбудителя и, главным образом, основывается на его активности в отношении Chlamydia trachomatis.
Доксициклин и азитромицин стали препаратами первой линии, поскольку мета-анализ, опубликованный в 2002 году [4], показал сходную и достаточно высокую их эффективность при лечении больных с хламидийной инфекцией. Отметим, однако, что данный мета-анализ обобщает результаты применения рассматриваемых препаратов в лечении хламидиоза не только у мужчин с НГУ, но и у женщин с цервицитами. Данный факт делает не вполне корректной экстраполяцию его результатов на когорту мужчин с НГУ.
В связи с этим, для сравнительной оценки доксициклина и азитромицина в лечении исключительно хламидийных НГУ у мужчин, а также с целью обновления данных по клинической и микробиологической эффективности рекомендуемых режимов антибиотикотерапии, в 2008 году российскими исследователями был проведён ещё один мета-анализ [5]. Для включения в мета-анализ отбирали только проспективные рандомизированные контролируемые клинические исследования (РКИ), сравнивающие эффективность и безопасность доксициклина 100 мг, применяемого в течение 7 дней, и азитромицина, назначаемого однократно в дозе 1,0 г у мужчин с НГУ. Отбирали исследования, в которые включались только мужчины, или исследования, из которых можно вычленить данные, касающиеся мужчин.
Из 160 оригинальных печатных работ по рассматриваемой теме (статьи в журналах, абстракты конференций, записи библиографических баз данных) было найдено 17 публикаций, описывающих потенциально подходящие для включения в мета-анализ исследования. Однако только восемь из этих работ являлись проспективными рандомизированными исследованиями и полностью соответствовали критериям включения в мета-анализ.
В результате мета-анализа было установлено, что у пациентов, получавших доксициклин, достоверно чаще отмечалась эрадикация C. trachomatis на 4-й неделе терапии по сравнению с пациентами, получающими азитромицин (100 и 92,5 % соответственно). Отношение шансов, рассчитанных по методу Peto для этого показателя, составило 0,15 (CI: 0,04, 0,69, p = 0,009) (рисунок).
Рисунок. Отношение шансов по показателю эрадикации C. trachomatis на 4-й неделе терапии
По другим параметрам эффективности и безопасности, таким как эрадикация возбудителя на 2-й неделе терапии, выздоровление (клиническая эффективность на 2-й неделе), стойкий клинический ответ (эффективность на 4-й неделе), количество нежелательных реакций, статистически достоверных различий выявлено не было.
Очевидно, что появление новых антибактериальных средств расширяет возможности врача при подборе оптимальной антимикробной терапии. Так произошло при появлении азитромицина в качестве средства для лечения хламидиоза. С другой стороны, как показало рассматриваемое исследование, доксициклин, относительно недорогой и достаточно давно используемый для лечения хламидийных НГУ препарат, имеет все основания считаться препаратом выбора, поскольку имеет преимущества перед азитромицином по показателю эрадикации C. trachomatis на 4-й неделе с начала терапии.
Необходимо отметить, что в настоящее время на фармакологическом рынке существуют разные лекарственные формы доксициклина, содержащие разные соли этого антибиотика. Установлено, что на безопасность применения доксициклина влияют два основных фактора - лекарственная форма и особенности его химического строения. Лекарственные формы по степени повышения безопасности можно расположить следующим образом: капсулы - таблетки - растворимые таблетки; соли соответственно гидрохлорид - гиклат - карегинат - моногидрат [6]. В отличие от применявшейся ранее соли гидрохлорида, доксициклин в виде моногидрата не оказывает повреждающего воздействия на слизистую оболочку пищевода и существенно реже вызывает диспепсические расстройства (тошноту, рвоту, горечь во рту, изжогу, боль в эпигастрии и т. д.). Более того, доксициклина моногидрат в форме диспергируемых таблеток (Юнидокс Солютаб) имеет более высокую, чем у капсул, биодоступность действующего вещества (абсолютная биодоступность достигает 95 %).
Весьма значимой и актуальной является проблема оптимальной антибиотикотерапии нехламидийных НГУ. Наиболее часто при нехламидийных НГУ выявляются Mycoplasma genitalium (у 23,8 % пациентов) и U. urealyticum (у 18,8 %). И если НГУ, вызванные U. urealyticum, очень хорошо поддаются терапии препаратами первой линии (доксициклином и азитромицином), то в случае инфицирования M. genitalium результаты лечения указанными препаратами являются далеко не такими однозначными. Так, к примеру, в одном из недавно (2006 г.) проведённых исследований неэффективность лечения при стандартном однодозном приёме азитромицина в дозировке 1 г достигала 28 % [8]. Эффективность терапии фторхинолонами уретритов, вызванных M. genitalium, низкая, а данные по тетрациклинам противоречивые.
Возможные пути повышения эффективности терапии заболеваний, обусловленных M. genitalium, представляются в использовании более длительных схем назначения азитромицина (5 дневный курс: 0,5-0,25-0,25-0,25-0,25), применении более активных в отношении данного микроорганизма макролидов (например, джозамицина) или использовании антибактериальных препаратов других групп (фторхинолоны IV поколения) [9].
Пока идёт накопление информации о роли и особенностях (чувствительность к антимикробным препаратам, методы культивирования и т. д.) разных микоплазм в развитии инфекций репродуктивных органов у мужчин, основным критерием выбора антимикробных препаратов должны быть результаты клинических исследований.
В настоящее время в России проводится открытое многоцентровое несравнительное исследование по оценке эффективности и безопасности джозамицина (Вильпрафена ® ) в лечении НГУ у мужчин и цервицитов у женщин, вызванных M. genitalium. Препарат назначается в режиме 500 мг 3 раза в день, 10 дней. Оценка микробиологической эффективности (отделяемого уретры и первой порции утренней мочи) выполняется посредством двух методов амплификации нуклеиновых кислот - ПЦР и NASBA. Первые результаты исследования, опубликованные в конце 2008 г., свидетельствуют о высокой эффективности джозамицина в лечении мужчин с НГУ, вызванными M. genitalium: элиминация возбудителя была достигнута у 95 % пациентов [10].
Представляется очевидным, что для выработки оптимальной антимикробной терапии уретритов, вызванных микоплазмами, потребуется дальнейшее накопление и анализ данных по клинической эффективности разных схем терапии. В настоящее время это направление исследований является весьма актуальным.
Заключение
Негонококковый уретрит - весьма распространённое заболевание, в подавляющем большинстве случаев вызываемое возбудителями, передающимися половым путем. В основе оптимальной терапии больных НГУ лежит точная этиологическая диагностика, а также рациональная антибиотикотерапия пациентов и их половых партнеров с учётом установленной на сегодняшний день чувствительности возбудителей к антибактериальным препаратам.
Данные наиболее актуального на сегодняшний день мета-анализа свидетельствуют о том, что доксициклин является наиболее эффективным и безопасным препаратом для лечения НГУ у мужчин, вызванного Clamydia trachomatis. При этом важно отметить, что с точки зрения переностимости и удобства приёма предпочтение стоит отдавать доксициклину в виде соли моногидрата (Юнидокс Солютаб). Весьма актуальной представляется сегодня проблема определения оптимальных схем лечения НГу, вызванных Mycoplasma genitalium, поскольку традиционно применяющиеся противохламидийные режимы терапии, в частности однократный приём азитромицина в дозе 1 г, в отношении данного возбудителя оказываются недостаточно эффективными. Джозамицин имеет высокую активность in vitro в отношении различных видов микоплазм, а результаты современных клинических исследований свидетельствуют о высокой эффективности этого макролида при НГУ, вызванном Mycoplasma genitalium у мужчин. Представляется перспективным дальнейшее накопление клинических данных по возможностям терапии джозамицином в рамках более крупных сравнительных рандомизированных исследований, что позволит определить место этого препарата в терапии больных НГУ.
Главенствующая роль антибактериальной терапии в лечении урогенитальных инфекций, в том числе наиболее распространенной хламидийной, ни у кого не вызывает сомнения. Вместе с тем в настоящее время при диагностике и лечении урогенитальной инфекции растет
На современном этапе в медицинскую практику дерматовенеролога все активнее вводятся стандарты для диагностики и терапии различных заболеваний. Это касается и урогенитальных инфекций. Согласно методическим рекомендациям (2003 г.) полное излечивание и исчезновение симптомов обычно наблюдается после назначения следующих рекомендуемых схем лечения: азитромицин 1 г перорально в однократной дозе или доксициклин 100 мг перорально 2 раза в день, в течение 7 дней. Альтернативными препаратами считают: эритромицин 500 мг 4 раза в сутки или офлоксацин 300 мг внутрь 2 раза в сутки в течение 7 дней, а также джозамицин в дозе 500 мг 2 раза в сутки в течение 7–10 дней [2].
Между тем в литературе все чаще стали появляться данные о фактах отсутствия положительного эффекта при адекватной антибиотикотерапии [3, 4]. В то же время, как справедливо подчеркивают исследователи, данные о структуре антибиотикорезистентности различаются в зависимости от географического района выделения штаммов возбудителей и меняются с течением времени [5]. В этой связи при проведении рациональной антибиотикотерапии инфекций необходимо учитывать уровень антибиотикорезистентности патогенов в данном регионе. Возможно, поэтому сведения об эффективности применения этиотропной терапии урогенитальных инфекций хотя и многочисленны, но весьма противоречивы [6].
Учитывая спектр антибактериальной активности азитромицина и джозамицина, их фармакокинетические свойства, способность активизировать фагоцитоз, мы поставили перед собой задачу изучить их эффективность: клиническую, бактериологическую и иммунологическую.
Критериями эффективности считали: клинические данные, микробиологические по результатам прямого иммунофлюоресцентного анализа (ПИФ) и полимеразной цепной реакции (ПЦР) через 1 и 3 месяца после лечения, иммунологических данных (критериальные показатели иммунного статуса человека через 1 месяц после лечения), по данным катамнеза в течение 1 года после терапии. В процессе наблюдения нами были отслежены на фоне применения разных схем терапии побочные эффекты, представленные в табл. 1.
Как следует из табл. 1, наиболее частыми побочными реакциями в обеих группах были диспепсические явления, присоединение кандидоза наблюдалось во второй группе обследованных, получавших джозамицин.
Клиническую эффективность оценивали в баллах:
3 балла — полное клиническое выздоровление (исчезновение всех исходных симптомов болезни);
2 балла — улучшение состояния, неполное исчезновение признаков заболевания;
1 балл — улучшение общего состояния, но без изменений клинических симптомов;
0 баллов — ухудшение состояния.
Во второй группе больных, получавших джозамицин, по уровню субтипов ИЛ-12 выявлены закономерности, подобные вышеописанным в первой группе. Вместе с тем при оценке иммунного статуса больных этой группы установлено, что не происходит их нормализации, более того, по ряду показателей выявлено отсутствие динамики или усугубление дисбаланса функциональной активности иммуноцитов (табл. 2).
Полученные результаты исследования иммунного статуса у больных второй группы позволяют считать, что джозамицин супрессирующе влияет на Т-клеточный иммунитет за счет активации их готовности к апоптозу. Выявленные изменения, по-видимому, могут быть причиной как рецидива заболевания, так и развития осложнений и поэтому являются основанием включения иммунокорригирующих препаратов с преимущественным воздействием на фагоцитарное звено в комплекс лечения больных хламидийным хроническим уретритом при использовании джозамицина.
Итак, проведенные исследования показали хорошую клиническую и бактериологическую эффективность использованных препаратов при лечении хламидийных хронических уретритов у мужчин. Вместе с тем результаты иммунологического аспекта терапии этими препаратами являются основанием к дифференцированному подходу при назначении лечения больным УГИ, обусловленной C. trachomatis.
При использовании джозамицина одновременно рекомендуется подключение иммунокорригирующих препаратов, с преимущественным воздействием на фагоцитарное звено, что связано с выявленным его супрессирующим действием, в отличие от Сумамеда, на Т-клеточный иммунитет за счет активации неготовности к апоптозу.
Литература
Иммунологический мониторинг для прогнозирования течения патологического процесса, обусловленного хламидийной инфекцией: Метод. рекомендации № 2000/21. Екатеринбург. 2000. 13 с.
Борисенко К. К. Современные итоги и некоторые проблемы лечения урогенитального хламидиоза / К. К. Борисенко, М. Б. Алиев. Современные направления в диагностике и лечении урогенитального хламидиоза. Новосибирск, 1998. С. 3–4.
Чеботарев В. В. Урогенитальный хламидиоз: современные проблемы диагностики, патогенеза, лечения / Журнал дерматовенерологии, косметологии. 1997. № 2. с. 5–11.
Черненькая Т. В. Чувствительность энтеробактерий к беталактамным антибиотикам // Антибиотики и химиотерапия. 2000. № 4. С. 28–29.
Урологические инфекции (хламидии, микоплазмы, уреаплазмы). Клиника, диагностика, лечение: Метод. пособие / В. В. Делекторский, Г. И. Яшкова, Е. К. Назарова, И. Н. Лупан. М.: ДЕТСТОМ-1. 2000. 28 с.
Ильин И. И. Размышления о лечении урогенитального хламидиоза / И. И. Ильин, Ю. И. Ковалев, О. В. Лысенко // Вестник дерматологии и венерологии. 1994. № 1. С. 30–33.
Скрипкин Ю. К. Лечение джозамицином (вильпрофеном) больных урогенитальным хламидиозом (Ю. К. Скрипкин, М. Г. Пашинян) // Вестник дерматологии и венерологии. 2000. № 3. С. 49–50.
Соловьев А. М. Почему азитромицин считается препаратом выбора для лечения урогенитальной хламидийной инфекции? / А. М. Соловьев, О. Л. Поздняков, А. В. Терещенко // Русский медицинский журнал. 2006. Т. 14. № 15 (267). С. 1160–1163.
А. Д. Юцковский, доктор медицинских наук, профессор
И. А. Юцковская
Е. В. Маркелова
Владивостокский государственный медицинский университет, Владивосток
В течение последних лет в Российской Федерации заболеваемость урогенитальной хламидийной инфекцией вышла на первое место среди всех бактериальных инфекций, передаваемых половым путем (ИППП), и уступает по частоте только трихомониазу. Такая же картина в ст
В течение последних лет в Российской Федерации заболеваемость урогенитальной хламидийной инфекцией вышла на первое место среди всех бактериальных инфекций, передаваемых половым путем (ИППП), и уступает по частоте только трихомониазу. Такая же картина в странах Северной Америки и Европы, где урогенитальный хламидиоз уже много лет является самым распространенным бактериальным ИППП. Хотя доля Clamidia trachomatis (C. trachomatis) как этиологического агента в общей структуре уретритов у мужчин не превышает 50%, именно этот возбудитель остается главной причиной таких уретритов.
Классификация хламидийных инфекций. В принятой в большинстве стран мира международной классификации болезней Х пересмотра (МКБ-Х) урогенитальные хламидийные инфекции подразделяются:
1. На хламидийную инфекцию нижних отделов (неосложненную):
2. Инфекцию верхних отделов мочеполового тракта (осложненную):
Кроме этого, в МКБ-Х выделяют хламидийную инфекцию аноректальной области, хламидийные фарингиты, а также хламидийную инфекцию других локализаций.
Эта классификация более удобна для статистических отчетов, где требуется четкая рубрификация всех болезней. Специалисты нередко в клинической практике видоизменяют МКБ с целью большей адаптации ее для своей работы. Так, для назначения адекватной терапии хламидийных инфекций важно понять, какая из 3 форм урогенитального хламидиоза имеется у больного:
Клинические проявления хламидийной инфекции. Чаще всего у мужчин на практике встречается хламидийная инфекция нижних отделов урогенитального тракта — уретриты.
Уретриты, вызванные С. trachomatis, проявляются обычно скудной клинической симптоматикой, хотя могут сопровождаться и признаками острого воспаления, сходными с гонореей. Нередко инфицирование нижних отделов урогенитального тракта у мужчин хламидиями может протекать без какой-либо клинической симптоматики.
Наиболее частые проявления хламидийной инфекции нижних отделов урогенитального тракта у мужчин — это наличие слизисто-гнойных или слизистых необильных выделений из уретры, дизурии (зуда, жжения, болезненности при мочеиспускании), дискомфорт, зуд, жжение в области уретры. При клиническом обследовании у таких пациентов можно выявить гиперемию и отечность слизистой оболочки наружного отверстия мочеиспускательного канала, инфильтрацию стенок уретры, повышенный лейкоцитоз в материале из уретры.
Успешное излечение хламидийной инфекции во многом зависит от выбора правильной тактики терапии, поскольку ошибки на самом начальном этапе болезни, будь то диагностические ошибки или неадекватный выбор антибиотиков, могут привести к тому, что от инфекции избавиться не удастся, что грозит больному серьезными осложнениями.
К наиболее тяжелым осложнениям хламидийной инфекции относят: эпидидимиты, воспалительные заболевания органов малого таза (ВЗОМТ), бесплодие у лиц обоего пола, болезнь Рейтера, перигепатит, пельвиоперитонит, патологию плода и послеродовую патологию у матери, а также некоторые другие состояния. Их развитие может быть связано не только с хламидиями, но и с другими возбудителями, однако хламидии остаются наиболее частой причиной указанных осложнений.
Уникальность азитромицина базируется на его исключительной фармакокинетике. Азитромицин устойчив в кислой среде, благодаря чему хорошо всасывается после приема внутрь (Feise EF et al, 1990). Одновременный прием с пищей уменьшает всасывание на 50%, поэтому препарат принимают за 1 ч до или через 2 ч после еды. Этого недостатка лишена таблетированная форма препарата, которая может приниматься независимо от приема пищи.
После приема внутрь 500 мг азитромицина биодоступность препарата составляет 37%, а максимальная концентрация в плазме (0,4 мг/л) достигается через 2–3 часа, затем она плавно снижается к 24 ч, в последующие сроки препарат в крови не определяется (Комаров Р.В. с соавт, 2001). Этого недостаточно для достижения терапевтического эффекта при лечении инфекций, сопровождающихся бактериемией. Однако липофильность молекулы азитромицина обеспечивает, помимо высокого уровня всасывания в кишечнике, еще и отличное проникновение препарата в ткани. Быстрое проникновение азитромицина из крови в ткани обеспечивается также низким уровнем связывания азитромицина с белками крови, что дает возможность достигнуть быстрого терапевтического эффекта при инфекциях, поражающих клетки и ткани (Foulds G et al, 1990).
Эффективность антибиотиков обычно оценивается путем сравнения активности в условиях in vitro (это показатель минимальной подавляемой концентрации (МПК) и концентрации препарата в сыворотке крови. Эти сравнения могут приводить к ошибочным представлениям о реальной эффективности антибиотика. Для ее оценки необходимо принимать во внимание еще и концентрацию препарата в тканях и месте воспаления. Именно эти показатели азитромицина обеспечивают ему превосходство. В различных тканях концентрации азитромицина в десятки раз превышают концентрации в сыворотке крови (рис. 1).
В эксперименте и исследованиях на животных было показано, что клинический и бактериологический эффекты макролидных антибиотков прямо зависят от времени превышения их концентраций над значениями МПК90 возбудителей, причем условием положительного эффекта является превышение концентрациями МПК в течение как минимум 40% интервала дозирования. Учитывая, что, по данным Комарова Р.В. и соавт. (2001), через 3 дня после приема концентрации азитромицина в секрете/ткани предстательной железы в 16,8 раза превышали значения МПК и, принимая это значение времени за 40%, можно прогнозировать сохранение эффекта азитромицина в течение как минимум 7 дней после однократного приема.
Для антибактериальных препаратов важен не только уровень накопления в тканях, но и соотношение тканевых концентраций и значений МПК для возбудителей инфекций. Так, концентрации азитромицина в секрете и ткани предстательной железы, представленные выше (рис. 1), превышали МПК90 для хламидий во все сроки наблюдения, вплоть до 2-х недель (в исследовании LeBell M. et al (1996)).
Полученные данные подтверждают возможность однократного применения азитромицина при неосложненной хламидийной инфекции, когда необходимо 7-дневное воздействие на микроорганизм, перекрывающее 2 жизненных цикла хламидий, а также его назначения короткими курсами с длительными интервалами между ними при осложненном и персистирующем хламидиозе.
Накопление препарата в макрофагах и полиморфноядерных лейкоцитах и транспортировка его с ними к месту воспаления дополняют нацеленное действие азитромицина в очаге инфекции. Показано, что концентрация препарата в месте воспаления в значительной степени превышает его концентрацию в здоровой ткани (Pukander J, 1990).
Способность азитромицина к проникновению внутрь клеток обеспечивает активное воздействие на внутриклеточные микроорганизмы, к которым относится С. trachomatis. При заболеваниях, вызываемых внутриклеточными патогенами, эффект лечения и скорость элиминации возбудителя из организма зависят от уровня концентраций антибиотика внутри клеток (полиморфноядерные лейкоциты, макрофаги, клетки эпителия). Среди всех антибиотиков макролиды характеризуются наибольшей способностью концентрироваться внутри клетки. Азитромицин при этом особенно привлекателен, поскольку соотношение концентраций антибиотика внутри клетки и в экстрацеллюлярном пространстве составляет для него 40 и более. По этому показателю азитромицин превосходит не только эритромицин, но и другие полусинтетические макролиды (Фомина И.П. с соавт., 1996).
В эксперименте установлено, что азитромицин накапливается в лейкоцитах с последующим медленным высвобождением. При этом соотношение внутри-/внеклеточных концентраций в полиморфноядерных лейкоцитах и макрофагах in vitro после 2 ч инкубации с антибиотиком составляет 79, превышая соответствующие показатели для эритромицина в 4–5 раз. Внутриклеточная концентрация азитромицина обнаруживается в течение 24 ч и более. Установлено также, что предварительная обработка клеток азитромицином не влияет на захватывающую, переваривающую и киллерную функции фагоцитов (McDonald P. J. et al, 1991). К дополнительным важным свойствам азитромицина, способствующим быстрой реализации терапевтического эффекта, даже при коротких схемах применения относится концентрация антибиотика в фибробластах, превращающихся в своеобразный резервуар, из которого препарат высвобождается в очаге инфекции (Glodue R. P. et al, 1990).
Еще одна важная особенность азитромицина — продолжительный период полувыведения — 68 ч, который приводит к тому, что высокие уровни концентрации в месте инфекции, сохраняющиеся в течение продолжительного периода времени (до 10 дней), обеспечивают постоянное активное воздействие на патогенные микроорганизмы (Andriole V. T., 1990, Retsema J., et al, 1990). Сокращение времени приема антибиотика при сохранении терапевтической эффективности очень важный принцип при амбулаторном лечении пациента. По данным различных авторов, только 65% больных полностью выполняют предписания врача. Почти половина лиц, получающих лечение как половые партнеры инфицированных пациентов, полноценно не выполняют режим терапии. По данным Grob P. R., 1992, в течение первых 3–5 дней лечения неисполнительность отмечается приблизительно в половине случаев, на 6–7 день ее уровень возрастает до 71–81%. По этим причинам предпочтение отдается сегодня схемам лечения, предусматривающим однократный или по крайней мере не очень частый прием лекарств. Длительный период полувыведения азитромицина из организма, сохранение эффективных концентраций в очаге инфекции в течение 4–5 дней после прекращения лечения позволяют проводить укороченные курсы терапии, которые соответствуют по эффективности 10-дневным курсам лечения традиционными антибиотиками (Фомина И.П. с соавт., 1996). Азитромицин остается единственным на сегодня антибиотиком однократного приема для лечения неосложненной хламидийной инфекции. Еще в 1993 г. Lister P. J. et al показали, что однократный прием 1,0 грамма азитромицина не уступает по эффективности 7-дневному курсу доксициклина. Большое удобство применения азитромицина для больных и возможность контроля за приемом однократной дозы со стороны медицинского персонала позволяют обеспечить практически 100%-ное соблюдение режима лечения (Petitta ABS et al, 1999).
Азитромицин метаболизируется в печени, причем 50% выделяется с желчью в неизмененном виде, около 6% выводится с мочой.
При приеме азитромицина могут наблюдаться побочные эффекты со стороны желудочно-кишечного тракта (тошнота, рвота, диарея) и печени (повышение активности трансаминаз, холестаз, желтуха), а также аллергические реакции.
Механизм действия азитромицина, как и других макролидов, обусловлен влиянием на функцию бактериальных рибосом. Препарат связывается с 50S субъединицей рибосом рибосомы и таким образом подавляет биосинтез белков микроорганизма, оказывая бактериостатическое действие. Бактерицидное действие препарата начинается в концентрациях, превышающих МПК в несколько раз.
Азитромицин при уретритах нехламидийной этиологии. Азитромицин проявляет высокую активность не только в отношении хламидии, но и других инфекций, которые могут передаваться при сексуальных контактах: Ureaplasma urealyticum, Mycoplasma genitalium, Neisseria gonorrhoeae и Haemophilus ducreyi. Mycoplasma hominis в большинстве случаев резистентна к азитромицину.
Азитромицин активен также и в отношении грамположительной (St. aureus, St. epidermidis, включая штаммы, продуцирующие бета-лактамазы, различных видов стрептококков, за исключением штаммов, резистентных к макролидам, и энтерококков) и грамотрицательной флоры (Haemophilus influenzae, Moraxella catarrhallis и др). Эти микроорганизмы также могут быть обнаружены в мочеполовых путях, но их роль в возникновении уретрита не доказана.
Рекомендации по применению азитромицина при хламидийной инфекции. Для лечения больных хламидийной инфекцией нижних отделов урогенитального тракта все вышеназванные руководства в качестве метода выбора рекомендуют однократный прием азитромицина в дозе 1,0 грамм, за 1 ч до еды или через 2 ч после, если препарат используется в капсулах, или независимо от приема пищи при приеме таблеток. Другим препаратом выбора является доксициклин, который назначают по 100 мг 2 раза в сутки в течение 7 дней. К недостаткам азитромицина в сравнении с доксициклином можно было бы отнести более высокую стоимость азитромицина. Однако согласно результатам фармакоэкономических исследований, проведенных CDC, более высокая стоимость азитромицина в сравнении с доксициклином компенсируется снижением затрат, связанных с лечением ВЗОМТ, эктопической беременности и бесплодия, возникающими из-за неадекватной терапии, связанной с несоблюдением назначенной схемы лечения, что значительно чаще встречается при назначении доксициклина.
К преимуществам азитромицина перед доксициклином, помимо более высокой комплаентности лечения, относятся лучшая переносимость, а также возможность применения у подростков.
Заключение. Таким образом, уникальные фармакокинетические характеристики азитромицина — продолжительный период полувыведения, высокий уровень всасывания и устойчивость в кислой среде, способность этого антибиотика транспортироваться лейкоцитами к месту воспаления, высокая и продолжительная концентрация в тканях, возможность проникновения внутрь клетки, а также простые схемы применения, высокая клиническая эффективность и комплаентность лечения, низкая токсичность сохраняют позицию азитромицина как основного препарата при лечении хламидийных уретритов у мужчин и другой патологии, связанной с хламидийной инфекцией.
Гомберг М. А., доктор медицинских наук
Соловьев А. М., кандидат медицинских наук
МГМСУ, Москва
Урогенитальная хламидийная инфекция, по данным ВОЗ, является одной из самых распространенных инфекций, передаваемых половым путем. Особенности клинического течения (скудная симптоматика или ее полное отсутствие как у мужчин
Урогенитальная хламидийная инфекция, по данным ВОЗ, является одной из самых распространенных инфекций, передаваемых половым путем. Особенности клинического течения (скудная симптоматика или ее полное отсутствие как у мужчин, так и у женщин) и трудности лабораторной диагностики приводят к тому, что инфицированные лица обращаются к специалистам несвоевременно. Это затрудняет лечение и увеличивает риск развития осложнений.
Профессор А. Л. Машкиллейсон еще в 80-х гг. прошлого века указывал на необходимость выбора терапевтической тактики с учетом клинической формы хламидиоза. Это положение не потеряло своей актуальности до сегодняшнего дня. Современная классификация урогенитального хламидиоза, согласно МКБ-Х, подразумевает деление на хламидийную инфекцию нижних отделов (неосложненную) и инфекцию верхних отделов мочеполового тракта (осложненную). Терапевтический подход к лечению каждой из этих форм различается.
- наличие инфекции в организме (в течение многих месяцев и даже лет);
- многократное неэффективное лечение различными антибиотиками;
- иммунологические нарушения;
- высокие титры сывороточных и местно-секретируемых противохламидийных антител (в особенности IgA);
- возможное отсутствие хламидийной инфекции у половых партнеров больных хламидиозом, несмотря на половые контакты без использования презерватива.
Таким образом, терапевтические подходы к лечению урогенитального хламидиоза можно разделить на три основные группы:
1) лечение больных с хламидийной инфекцией нижних отделов урогенитального тракта;
2) лечение больных с хламидийной инфекцией верхних отделов урогенитального тракта;
3) лечение больных персистирующим и рецидивирующим урогенитальным хламидиозом.
Во всех этих изданиях для антибактериальной терапии хламидийной инфекции рекомендуются антибиотики следующих фармакологических групп: тетрациклины, макролиды и фторхинолоны. Ниже мы постараемся пояснить различия в терапевтических подходах к лечению различных форм урогенитальной хламидийной инфекции.
Лечение больных хламидийной инфекцией нижних отделов урогенитального тракта
При лечении этой формы инфекции, как правило, достаточно одной лишь антибактериальной терапии и нет необходимости в дополнительных терапевтических мероприятиях.
Антибиотики тетрациклинового ряда
Препараты тетрациклинового ряда — это основные лекарственные средства, применяемые для лечения больных хламидиозом. Согласно всем упоминавшимся выше рекомендациям, для лечения больных урогенитальным хламидиозом препаратом выбора является доксициклин. Он назначается в дозе 100 мг два раза в сутки не менее семи дней. Первая доза составляет 200 мг. Преимущество использования доксициклина в его достаточно высокой эффективности (по данным литературы, 95—100%) и относительно небольшой стоимости лечения. У больных хламидиозом можно использовать другие препараты этой группы: тетрациклин (препарат рекомендуется ФР в качестве альтернативного) — по 500 мг четыре раза в сутки 7—10 дней, метациклин — по 300 мг четыре раза в сутки 7—10 дней.
У доксициклина, по сравнению с тетрациклином, выше биодоступность, он имеет более длительный период полувыведения и лучше переносится. Кроме того, при использовании доксициклина, и в этом его отличие от других тетрациклинов, нет необходимости соблюдать диету, назначаемую из-за связывания тетрациклинов с ионами Са. Следует помнить, что все препараты тетрациклинового ряда противопоказаны при почечной недостаточности, беременности и для лечения детей до восьми лет. Наиболее частыми побочными эффектами при приеме лекарственных средств тетрациклинового ряда являются тошнота, рвота, диарея, аллергические реакции. В период лечения препаратами этой группы больным необходимо избегать инсоляции из-за возможности фотосенсибилизации.
Макролиды
К числу наиболее активных противохламидийных препаратов принадлежат макролиды. К препаратам выбора при лечении хламидиоза относят азитромицин. Высокая терапевтическая концентрация азитромицина в тканях достигается после однократного приема стандартной дозы антибиотика и сохраняется в местах воспаления не менее семи суток. ФР и другие руководства рекомендуют для лечения больных хламидиозом нижних отделов мочеполового тракта однократный прием 1,0 г азитромицина за 1 ч до еды или через 2 ч после.
В качестве альтернативных препаратов в ФР представлены: спирамицин который назначается по 3 млн МЕ три раза в сутки в течение 10 дней; рокситромицин — по 150 мг два раза в сутки 10 дней; эритромицин — по 500 мг четыре раза в сутки 10 дней. Также при лечении больных хламидийной инфекцией используют другие препараты группы макролидов: джозамицин — по 500 мг два раза в сутки 10 дней, кларитромицин — по 250 мг два раза в сутки 10 дней, мидекамицин — по 400 мг три раза в сутки 10 дней. Преимуществами всех современных макролидных антибиотиков перед эритромицином являются улучшенная фармакокинетика, хорошая переносимость и меньшая кратность приема.
При приеме макролидов могут наблюдаться побочные эффекты со стороны желудочно-кишечного тракта (тошнота, рвота, диарея) и печени (повышение активности трансаминаз, холестаз, желтуха). Разумеется, возможны и аллергические реакции.
Фторхинолоны
Следующую группу препаратов, обладающих противохламидийной активностью, составляют фторхинолоны. Препаратам той группы свойственна различная, в том числе и достаточно высокая, чтобы излечивать эту инфекцию, активность in vitro в отношении Chlamydia trachomatis. Однако единственным препаратом данной группы, который современные руководства рекомендуют для лечения хламидиоза, да и то в качестве альтернативного, является офлоксацин. Его назначают по 400 мг два раза в день в течение 10 дней. Преимуществом офлоксацина перед другими фторхинолонами можно считать его практически 100-процентную биодоступность.
Из других препаратов этой группы применяют пефлоксацин — по 400 мг два раза в сутки 10 дней и ломефлоксацин — по 400 мг один-два раза в сутки 10 дней.
Такие ограничения в использовании фторхинолонов для лечения хламидийной инфекции связаны с тем, что в сравнении с антибиотиками других вышеперечисленных групп после подобной терапии слишком высок процент рецидивов.
Показанием к использованию фторхинолонов при хламидиозе может быть смешанная гонорейно-хламидийная инфекция или сочетание Chlamydia trachomatis с другими микроорганизмами, демонстрирующими чувствительность к этим антибиотикам (требующая терапии сопутствующая кокковая или палочковая флора).
Группа фторхинолонов является сегодня одним из наиболее активно развивающихся классов противомикробных препаратов. Появляются все новые и новые поколения фторхинолонов. Хинолоны последних поколений (III и IV) превосходят предшествующие препараты этой группы по активности в отношении хламидий и кратности применения.
Препараты из группы фторхинолонов противопоказаны беременным и детям до 12 лет, больным с нарушением функции печени и почек. Из побочных реакций после приема фторхинолонов могут наблюдаться диспептические расстройства, тошнота, рвота, головокружение, аллергические реакции, тендиниты. Для всех препаратов этой группы, за исключением моксифлоксацина, характерен фотосенсибилизирующий эффект, о чем необходимо напоминать больному.
Лечение хламидиоза у беременных и новорожденных
В огромном числе наблюдений, проводившихся за почти 50 лет существования эритромицина, показана его безопасность, благодаря чему этот антибиотик можно считать едва ли не единственным лекарственным средством, разрешенным к применению у беременных и новорожденных.
По всем существующим сегодня рекомендациям, включая рекомендации ФР, беременным женщинам эритромицин назначают по 500 мг четыре раза в сутки 7 дней или по 250 мг четыре раза в сутки 14 дней. Для детей до 8 лет (с массой тела до 45 кг) разовая доза составляет 50 мг на 1 кг массы тела, кратность — каждые 6 ч в течение 10—14 дней. Детям старше 8 лет назначают такой же курс эритромицина, как и взрослым.
Достаточно высокой терапевтической эффективностью и лучшей, чем у эритромицина, переносимостью обладает еще один давно известный представитель макролидов — спирамицин. Его назначают по 3 млн МЕ три раза в сутки 7—10 дней.
Лечение больных с хламидийной инфекцией верхних отделов урогенитального тракта
При лечении больных с данной клинической формой хламидийной инфекции используют все перечисленные выше антибиотики, но менее продолжительными курсами (до трех недель), чем при неосложненных формах заболевания. Более удобен в этих случаях азитромицин, который ФР рекомендует назначать курсами: три курса по 1 г один раз в неделю.
В многоцентровом исследовании, проведенном в различных регионах России (г. Екатеринбург, Ставрополь и Москва), была показана высокая эффективность такой схемы применения азитромицина при осложненных формах хламидиоза (применялся препарат сумамед фирмы ПЛИВА, Хорватия), что и позволило внести соответствующие дополнения в рекомендации.
Лечение больных с осложненной формой хламидийной инфекции должно быть комплексным, поскольку процесс связан не только с наличием инфекции, но и с теми неблагоприятными последствиями, которые она вызывает при длительном течении болезни. Поэтому для достижения клинического излечения назначение антибактериальных препаратов в таких случаях должно сочетаться с комплексом противовоспалительных, симптоматических и физиотерапевтических мероприятий, выбор которых зависит от характера патологии.
Лечение больных с персистирующим и рецидивирующим урогенитальным хламидиозом
Персистенция хламидий требует особого подхода к больному. Применения одних антибиотиков при этой форме инфекции, как правило, недостаточно, поскольку все эффективные в отношении хламидий антибиотики обладают бактериостатическим действием и способны оказывать эффект только в процессе осуществления жизненного цикла хламидий. Поскольку при персистенции данный жизненный цикл приостанавливается на неопределенное время, использование антибиотиков в этот период не способно привести к гибели микроорганизмов, остановившихся в своем развитии. Однако лечить данную инфекцию необходимо, так как сохранение хламидий в организме может сопровождаться иммунными нарушениями, что ведет к различным осложнениям, в частности бесплодию.
При лечении таких состояний обычно рекомендуют сочетанную терапию антибиотиками и иммунокорректорами. Были предложения назначать антибиотики в различных сочетаниях длительными курсами. Последний подход имеет существенные отрицательные стороны: длительный прием антибиотиков неблагоприятно воздействует на работу всех систем организма: желудочно-кишечный тракт (нарушая работу печени и микроэкологию кишечника), нервную, мочевыделительную, иммунную (угнетая иммунитет и аллергизируя организм больного) системы. Кроме того, при персистирующей инфекции антибиотики в качестве монотерапии вообще могут быть неэффективны, исходя из особых биологических свойств возбудителя, о чем уже говорилось выше.
Наши исследования показали, что примерно у 75% больных персистирующим хламидиозом встречаются различные нарушения иммунного статуса. Они выражаются, в первую очередь, в изменении числа CD4+ и CD8+ Т-клеток и нарушении их соотношения примерно у 50% больных. По сравнению с контрольной группой, у больных наблюдается статистически достоверное снижение относительных и абсолютных показателей естественных киллеров (CD16+) (что очень важно с точки зрения продукции интерферона), HLA DR-клеток, В-клеток (CD72+ и CD21+).
Наши наблюдения, основанные на лечении более 1000 больных персистирующим хламидиозом, показывают, что наиболее оптимальна в этих случаях комбинированная терапия, основанная на сочетании антибиотиков и иммунных препаратов. При антибиотикотерапии используют стандартные для осложненной инфекции курсы и дозировки перечисленных выше антибиотиков. Но начинать лечение желательно с курса иммунотерапии. Из иммунных препаратов наибольшей эффективности можно добиться, применяя полиоксидоний и a-интерферон. На основании собственных исследований мы предлагаем следующие варианты предшествующей назначению антибиотиков иммунотерапии:
- полиоксидоний назначается по 6 мг в/м один раз в сутки; первые две инъекции ежедневно, затем три инъекции через день, остальные два раза в неделю, всего на курс 10 инъекций. После четвертой инъекции начинают курс антибактериальной терапии;
- интерферон альфа-2b назначается в виде ректальных суппозиториев двумя 5-ти дневными циклами с интервалом в две недели между ними в суммарной дозе 10 млн МЕ на курс. После окончания иммунотерапии проводится курс антибактериальной терапии. Причем оптимальным в этой ситуации оказался курс азитромицина по схеме лечения осложненных форм (по 1,0 г на 1-й, 7-й и 14-й дни).
Указанные подходы позволяют повысить эффективность лечения персистирующей и рецидивирующей хламидийной инфекции до 90%.
В ближайшие две недели после окончания лечения следует использовать метод выделения хламидий в культуре клеток, потому что только он дает возможность определить наличие в организме пациента жизнеспособных форм хламидий. Положительный результат остальных методов, включая полимеразую цепную реакцию (ПЦР) или прямую иммунофлюоресценцию (ПИФ), не обязательно говорит о том, что лечение было неэффективным, а может рассматриваться лишь как свидетельство того, что не произошла полная элиминация хламидий или их фрагментов. Следовательно, эти методы позволяют судить об эффективности проведенного лечения не ранее чем через 30 дней после окончания антибиотикотерапии.
Таким образом, соблюдение определенных правил ведения больных с урогенитальным хламидиозом позволяет добиваться полного излечения даже в тех ситуациях, когда хламидии сохраняются у пациента в течение продолжительного времени, а сам инфекционный агент оказывается устойчив к обычной антибактериальной терапии.
М. А. Гомберг, доктор медицинских наук
А. М. Соловьев, кандидат медицинских наук
ЦНИКВИ, МГМСУ, г. Москва
Что такое уретрит? Причины возникновения, диагностику и методы лечения разберем в статье доктора Барашиков Д. В., уролога со стажем в 20 лет.
Над статьей доктора Барашиков Д. В. работали литературный редактор Юлия Липовская , научный редактор Сергей Федосов и шеф-редактор Лада Родчанина

Определение болезни. Причины заболевания
Уретрит (urethritis, греч. urethra — мочеиспускательный канал, -itis — воспалительный ответ) — воспалительный процесс в стенке мочеиспускательного канала [1] .
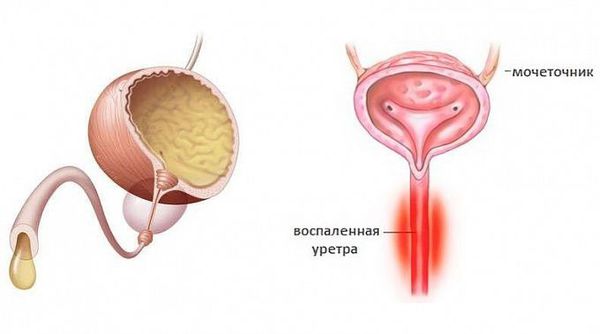
Уретриты могут иметь гонорейную природу и негонорейную. Негонококковый уретрит является распространенным заболеванием — ежегодно во всём мире регистрируют около 50 млн. случаев. По статистике в США и Великобритании заболеваемость негонококковым уретритом значительно превышает заболеваемость гонококковым уретритом, одна из причин — лабораторные анализы стали лучше выявлять заболевание [1] . Среди самых распространённых причин возникновения негонококковых уретритов называют хламидийную инфекцию.
Болезнь протекает в острой и хронической форме. Установлено, что острый уретрит чаще вызван сочетанием бактерий Chlamydia trachomatis и Ureaplasma urealyticum (у 45,4 % пациентов), подострый — Chlamydia trachomatis (у 66,7 %) [2] .
Наиболее частый путь передачи — половой, реже воспалительный процесс инициируется условно-патогенной флорой. Уретрит может быть вызван бактериями, грибками или вирусами (например, вирусом герпеса).
Причины уретрита
Гораздо реже уретрит инициируется сопутствующими заболеваниями, воздействием агрессивных веществ (спермицидных лубрикантов, спиртосодержащих растворов) или травмами.
Предрасполагающими факторами для развития уретрита могут служить:
- переохлаждение;
- травма (микротравма во время полового акта) половых органов;
- сопутствующие заболевания (сахарный диабет, мочекаменная болезнь, аутоимунные заболевания, дисбиоз влагалища);
- снижение общего иммунитета, изменение гормонального статуса (менопауза);
- оперативные вмешательства и манипуляции (например цистоскопия — эндоскопическое исследование мочевого пузыря, катетеризация, бужирование уретры);
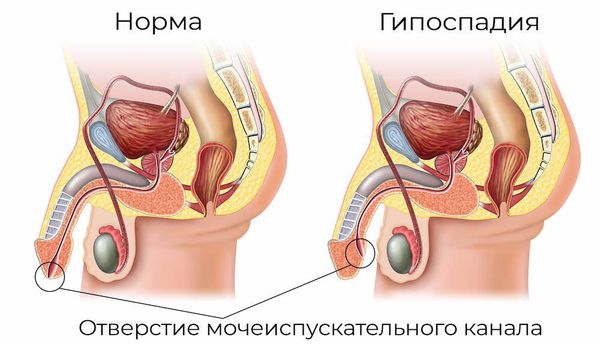
- аномалии развития половых органов: гипоспадия — это генетическое нарушение, при которой наружное отверстие уретры располагается в нетипичном месте (передней стенке влагалища или на теле полового члена);
- несоблюдение личной гигиены;
- употребление в больших количествах острого, кислого, солёного и алкоголя;
- малоподвижный образ жизни, сидячая работа.
При обнаружении схожих симптомов проконсультируйтесь у врача. Не занимайтесь самолечением - это опасно для вашего здоровья!
Симптомы уретрита
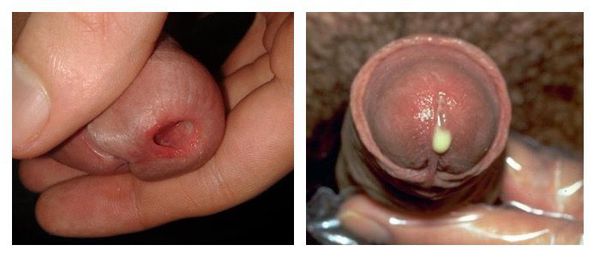
Выраженность клинических симптомов зависит от стадии воспалительного процесса. Как правило, в острую стадию имеются жжение, "резь" или зуд в начале мочеиспускания, выделения из наружного отверстия мочеиспускательного канала.
При визуальном осмотре выявляют гиперемию, отёк слизистой оболочки в области наружного отверстия мочеиспускательного канала, обильное слизистое или гнойное отделяемое, при пальпации мочеиспускательного канала наблюдаются болезненные ощущения [3] . В дальнейшем гиперемия, отёк и выделения из уретры уменьшаются, становятся незначительным, либо прекращаются. При сохранении симптомов заболевание переходит в хроническую форму спустя два месяца.
Уретрит у мужчин
У мужчин клиническая картина ярко выражена, нередко сочетается с затруднением мочеиспускания.
Уретрит у женщин
У женщин заболевание чаще всего проявляется симптомами острого цистита: частыми, болезненными мочеиспусканиями и болью внизу живота. Женщины более часто страдают клинически выраженными симптомами уретрита по сравнению с мужчинами, что связано с анатомическими особенностями строения мочеполовой системы — короткая уретра (около 1 см) и близкое расположение анального отверстия. Учитывая строение уретры, уретрит у женщин чаще приводит к развитию восходящей инфекции и может стать причиной бесплодия.
У достаточно большого количества пациентов уретрит изначально протекает со стёртыми проявлениями (торпидная или вялотекущая форма). Пациенты предъявляют жалобы лишь на скудное отделяемое из уретры по утрам на нижнем белье. В некоторых случаях возможно "склеивание" и незначительная гиперемия наружного отверстия уретры, разбрызгивание мочи при мочеиспускании. Цвет и прозрачность мочи обычно не меняется.
При торпидных уретритах воспалительный синдром достаточно часто не ограничивается передней уретрой, а распространяется на задний отдел, предстательную железу и шейку мочевого пузыря.
Тотальный уретрит характеризуется частыми, императивными позывами к мочеиспусканию, болью внизу живота и промежности. Нередко имеется примесь крови в моче, либо примесь гнойного отделяемого. Воспалительная реакция в остром периоде длится от нескольких дней до трёх недель.
Патогенез уретрита
У мужчин микрофлора уретры остается постоянной на протяжении всей жизни. Её представляют стафилококки, дифтероиды, диплококки, палочки и анаэробы (пептококки, бактероиды, энтеробактерии и клостридии). Микроорганизмы заселяют лишь первые несколько сантиметров мочеиспускательного канала — на остальном протяжении он почти стерилен. Реакция в канале нейтрально-щелочная.
В норме у женщин микрофлора уретры представлена теми же бактериями, что у мужчин, но в большем количестве. В небольшом количестве в уретре присутствуют лактобацилы и кишечная палочка. Бактерии свободно размножаются, не вызывая при этом воспаления. В медицине этот процесс называется колонизацией.
От первоночальной колонизации уретры зависит устойчивость слизистой к воспалительным процессам. Если баланс микрофлоры нарушен, она может стать одной из факторов развития уретрита или привести к хроническому течению болезни [15] .
Различные инфекционные агенты, попадая на слизистую оболочку мочеиспускательного канала, адгезируются (сцепляются с поверхностью) и вызывают локальную воспалительную реакцию, либо персистируют (присутствуют в неактивном состоянии) в ней продолжительное время без клинических признаков уретрита.
Классификация и стадии развития уретрита
Уретрит подразделяется по своей этиологии на:
- Гоноррейный уретрит.
- Негоноррейный:
- инфекционный, в том числе бактериальный уретрит (бактериальный-патогенная и условно-патогенная флора, например хламидийный уретрит, а также вирусный, спирохетный, кандидомикотический уретрит, амебный, микоплазменный, трихомонадный уретрит);
- неинфекционный (посттравматический, аллергический, аутоимунный) [4] .
По Международной классификации болезней МКБ-10 к уретриту и уретральному синдрому также относятся:
- уретральный абсцесс (абсцесс железы Купера, железы Литтре);
- неспецифический уретрит (негонококковый, невенерический);
- другие уретриты (уретральный меатит, язва наружного отверстия уретры, постменопаузальный уретрит).
Классификация по локализации воспалительного процесса достаточно условная.
По глубине (степени) поражения выделяют следующие виды уретритов (преимущественно у мужчин):
- передний уретрит (передняя уретра, висячий отдел);
- задний уретрит (простатический отдел уретры);
- тотальный уретрит (поражение уретры на всем протяжении).
По клиническому течению выделяют уретриты:
- острый;
- хронический;
- торпидный.
Осложнения уретрита
При отсутствии адекватной терапии активный процесс переходит в хроническую форму с периодическими эпизодами обострения. Это, в свою очередь, может привести к рубцовой деформации (стриктуре) уретры на любых уровнях, к развитию баланопостита (воспаление головки полового члена), простатита, везикулита, орхоэпидидимита (воспаления яичка с придатком) и воспалительных заболеваний верхних мочевыводящих путей (пиелонефрита) [5] . В случае развития пиелонефрита к симптомам может присоединиться гипертермия (повышение температуры тела), озноб, усиление боли и общая слабость.
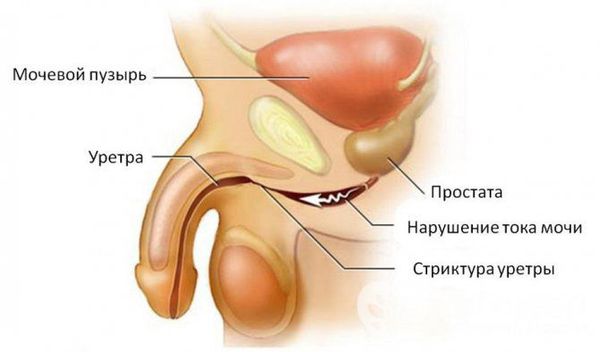
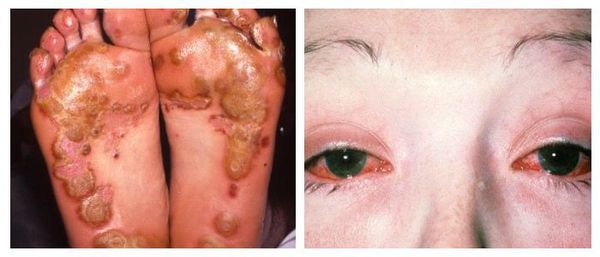
Наиболее тяжёлым осложнением уретрита, вызванного хламидийной инфекцией, является синдром Рейтера — реактивный артрит (или негнойное воспаление суставов) в сочетании с конъюнктивитом (воспалительным процессом конъюнктивы, тонкой прозрачной ткани, выстилающей внутреннюю поверхность века и видимую часть склеры) [6] .
Диагностика уретрита
Рекомендации Центра Контроля Заболеваемости (CDC) и Европейской Ассоциации урологов на сегодняшний день являются наиболее авторитетными и регулярно обновляющимися клиническими рекомендациями по диагностике и лечению инфекций урогенитального тракта [7] [8] .
Симптомы уретрита могут быть схожими с симптомами других заболеваний мочеполовой системы, поэтому очень важно провести дифференциальную диагностику. В этом помогает правильно и тщательно собранный анамнез, жалобы пациента, лабораторная и инструментальная диагностика [3] .
Первоначально проводится стандартный осмотр и сбор анамнеза. Во время беседы врач должен выяснить, что именно беспокоит пациента, когда возникли первые симптомы, был ли в недавнем времени незащищенный половой акт, назначалось ли ранее лечение по поводу ИППП, имеются ли хронические заболевания.
После этого проводится гинекологический осмотр у женщин для исключения воспалительных заболеваний половой сферы, при отсутствии последних — обследование у уролога. Врач оценивает состояния мочеиспускательного канала, выявляет наличие выделений (гнойных или слизистых). Параллельно осматривается кожный покров промежности и наружные половые органы на наличие гиперемии (покраснения), налёта и высыпаний. Всем пациенткам для подтверждения диагноза дистопии наружного отверстия уретры выполняется пальцевое исследование влагалища. Оно позволяет выявить уретро-гименальные спайки, приводящие к интравагинальному смещению и зиянию наружного отверстия уретры при половом акте, что способствует повторному инфицированию нижних мочевыводящих путей и механической травме наружного отверстия уретры [9] .
После осмотра и у мужчин, и у женщин производится забор мазков из уретры для микроскопии и бактериологического исследования с целью выявления возбудителя болезни [10] . Также исследуют общий анализ мочи, а также анализ мочи по Нечипоренко на наличие лейкоцитов, бактерий и кристаллов солей.
Проведение 3-х стаканной пробы мочи позволяет косвенно определить уровень распространенности воспалительного процесса. Оценивается количество лейкоцитов в поле зрения:
- в первой порции — соответствует уретриту;
- во второй порции — циститу, простатиту (у мужчин);
- в третьей порции — воспалению верхних мочевыводящих путей (пиелонефрит).
Бактериологическое исследование (посев) отделяемого из уретры позволяет выявить патогенную и условно-патогенную микрофлору, ее титр (концентрацию) и чувствительность к антибиотикам. Диагностически значимым титром у женщин является 10х4, у мужчин — 10х3 КОЕ/мл.
Серологический метод – определение антител (иммуноглобулинов класса G, M и А) в венозной крови пациента к наиболее распространенным возбудителям уретрита. Используется как вспомогательный метод.
ПЦР – методика исследования отделяемого из уретры, крови или мочи, а также иных биологических жидкостей посредством полимеразной цепной реакции, с целью обнаружения в них определенных возбудителей.
Приемуществом метода является высокая чувствительность. Вероятность ложноотрицательного ответа ничтожно мала, а вероятность ложноположительного ответа составляет менее 1 %.
Существуют специально разработанные диагностические комплексы [11] . К ним относятся исследования "Андрофлор" у мужчин и "Фемофлор" у женщин, которые включают в себя наиболее полную и комплексную этиологическую диагностику острых и хронических заболеваний и оценку микробиоценоза урогенитального тракта.
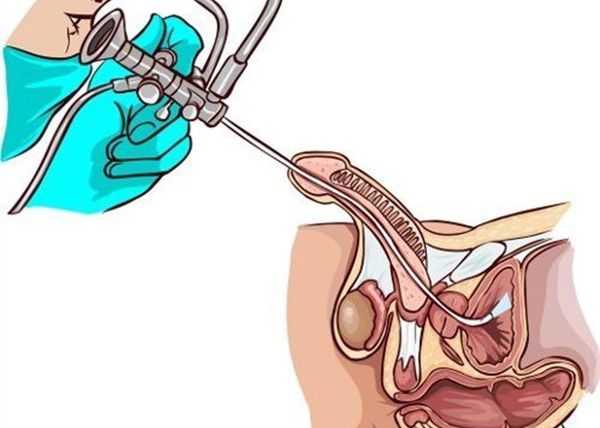
Наряду с лабораторными исследованиями, немаловажную роль играет проведение специфических исследований, таких как уретроцистоскопия или уретрография. В первом случае в мочеиспускательный канал вводят цистоскоп, с помощью которого визуализируют слизистую оболочку уретры, мочевого пузыря. При уретрографии диагностика проводится с использованием рентгеноконтрастного вещества и выполнения серии снимков для оценки проходимости и наличия патологических процессов в уретре.
Для исключения органических изменений и дифференциальной диагностики с другими заболеваниями, выполняется ультразвуковое исследование органов малого таза и верхних мочевых путей (мочевого пузыря, матки, придатков, простаты и семенных пузырьков, почек).
Лечение уретрита
В случае обнаружения у себя симптомов уретрита, необходимо обратиться к квалифицированному специалисту: урологу, гинекологу либо дерматовенерологу.
Чем лечить уретрит
Лечение уретрита — медикаментозное. Терапия зависит от типа уретрита и направлена на устранение его причины. При гоноррейном уретрите необходима консультация дерматовенеролога с последующей антибактериальной терапией и контролем излеченности пациента и его полового партнера.
Основные препараты для лечения уретрита — это антибиотики. Лечение мужчин, ведущих половую жизнь, как правило, включает в себя инъекции цефтриаксона для лечения гонореи и пероральный приём азитромицина для лечения хламидиоза. Если обследование исключает гонорею и хламидиоз, то может применяться антибиотик триметоприм или фторхинолон (например, ципрофлоксацин). У женщин лечение такое же, как и лечение цистита. Для лечения инфекции, вызванной вирусом простого герпеса, могут потребоваться противовирусные препараты.
При негоноррейных бактериальных и грибковых уретритах основным методом является назначение антибактериальной и антимикотической терапии после верификации диагноза и определения чувствительности микрофлоры к антибиотикам (мазок, ПЦР диагностика, исключение гинекологических заболеваний и других воспалительных процессов, имеющих сходную клиническую картину).
В некоторых случаях возможно назначение эмпирической терапии, основанной на опыте лечения и частоте выявляемости возбудителя, обычно при недостатке точных данных. Сначала назначается препарат, а в дальнейшем врач оценивает, насколько он эффективен.
Параллельно базовой терапии пациенту назначают препараты, стимулирующие общий и местный иммунный ответ. Также применяют препараты для стимуляции местного иммунитета и профиллактики рецидивов. Доказана высокая эффективность препарата Уро-Ваксом при негонококковых бактериальных уретритах, вызванных E. coli.
Для купирования внезапных и непреодолимых позывов к мочеиспусканию применяют ингибиторы М-холинорецепторов (солифенацин), селективные агонисты бета3-адренорецепторов (мирабегрон) и блокаторы альфа-адренорецепторов (тамсулозин). Механизм действия данных препаратов направлен на расслабление гладкомышечных клеток (снятие спазма) в строме простаты, шейке и мышечной оболочке мочевого пузыря.
Дополнительным методом является физиотерапия, действие которой направлено на уменьшение воспалительного, болевого синдрома, улучшение микроциркуляции в тканях [12] .
Физиотерапия при уретрите
В современных рекомендациях Европейской ассоциации урологов и публикациях в качественных научных журналах физиотерапия для лечения уретртита не упоминается. Это говорит о том, что эффективность физиопроцедур не доказана и их можно использовать только в дополнение к основному лечению.
Фитотерапия при уретрите
Фитотерапия может облегчить симптомы уретрита на этапе диагностики и в комплексе с верно подобранным антибиотиком. Однако нет убедительных доказательств о её влиянии на уропатогены в отличие от антибактериальных препаратов, которые являются основой лечения. В рекомендации Европейской ассоциации урологов фитотерапия не входит.
Прогноз. Профилактика
Своевременное лечение бактериального уретрита и соблюдение рекомендаций гарантирует полное выздоровление. После санированного (пролеченного) бактериального уретрита возможно реинфицирование (повторное заражение) при незащищенных половых актах с инфицированным партнером. Поэтому при уретритах, вызванных ИППП, для профилактики рецидивов лечение обязательно должен проходить и половой партнёр.
Учитывая распространенность и многогранность клинической картины уретрита, а также риск развития осложнений, для профилактики рекомендуется придерживаться определенных правил поведения:
- Барьерный метод контрацепции с непостоянным половым партнером (при выявлении патогенной микрофлоры рекомендуется обследование полового партнёра).
- Соблюдение личной гигиены: для женщин — вытирать интимную зону, начиная спереди и по направлению назад. Использование мыла может привести к дисбалансу полезных бактерий, что может вызвать присоединение инфекции. Мужчинам во время принятия душа необходимо сдвигать крайнюю плоть и тщательно обрабатывать головку полового члена.
- Адекватная физическая активность, укрепление иммунитета.
- Правильное питание.
- Своевременное лечение сопутствующих заболеваний, регулярные осмотры специалистов (1-2 раза в год у гинеколога или уролога).
- При появлении даже незначительных симптомов необходимо обратиться к урологу либо гинекологу. Перед этим важно исключить самостоятельный прием препаратов, так как это сгладит клиническую картину и затруднит диагностику [12] .
Читайте также:

