Холера туберкулез рахит альбинизм дифтерия
Обновлено: 16.04.2024
Информацию из данного раздела нельзя использовать для самодиагностики и самолечения. В случае боли или иного обострения заболевания диагностические исследования должен назначать только лечащий врач. Для постановки диагноза и правильного назначения лечения следует обращаться к Вашему лечащему врачу.
Туберкулез легких: причины появления, симптомы, диагностика и способы лечения.
Определение
Туберкулез – инфекционное заболевание, передающееся воздушно-капельным путем. Его возбудителем является бактерия Mycobacterium tuberculosis. Заразиться может каждый, но особенно восприимчивы к туберкулезу дети ввиду недостаточно сформированного иммунитета.
Заболевание излечимо, но лечение занимает длительное время. Огромное значение имеет ранняя диагностика туберкулеза - чем скорее он будет выявлен, тем меньше осложнений вызовет.
Причины появления туберкулеза
Туберкулез передается воздушно-капельным и воздушно-пылевым путями. Микобактерии находятся в мельчайших каплях, которые больной туберкулезом выделяет при разговоре, кашле, чихании и т.д.
Количество людей, инфицированных бактериями туберкулеза, составляет примерно 25–30%. Но заболевает только каждый десятый из них.
Выделяет микобактерии не каждый больной туберкулезом, а только тот, у кого происходит распад легочной ткани и бактериовыделение (в просторечии – открытая форма туберкулеза). Получить дозу микобактерий можно, даже не контактируя непосредственно с больным человеком, так как они способны оседать на частичках пыли и оставаться на ней при благоприятных условиях до 18 дней.
Дети чрезвычайно восприимчивы к инфекциям, а отсутствие прививок приводит к тому, что, встретив туберкулезную палочку, организм не распознает ее как чужеродный агент и не выделяет антитела для борьбы с инфекцией, а вместо этого дает бактериям возможность беспрепятственно проникнуть в легкие.
Среди взрослого населения в группу риска по заражению туберкулезом входят:
- пожилые люди,
- лица, страдающие хроническими заболеваниями (такими, как сахарный диабет, аутоиммунные заболевания),
- люди с онкологическими заболеваниями,
- люди, принимающие иммуносупрессивные препараты,
- пациенты, перенесшие тяжелые операции,
- курильщики.
- Первичный туберкулезный комплекс. Возникает при первичном заражении туберкулезом и встречается, как правило, среди детей. Протекает без выраженных симптомов, рентгенологически напоминает пневмонию, поэтому диагностика затруднена, не заразен. Небольшой очаг в большинстве случаев закрывается капсулой, и болезнь дальше не развивается.
- Туберкулез внутригрудных лимфатических узлов. Характеризуется распространением туберкулезных очагов в обоих легких и поражением лимфоузлов.
- Диссеминированный туберкулез легких. По всей поверхности легких образуются крошечные воспалительные бугорки. Может быть острым или хроническим, протекает тяжело (с лихорадкой, интоксикацией) и волнообразно.
- Очаговый туберкулез легких. В легком образуется от одного до нескольких воспалительных очагов не более 1 см в диаметре. Может протекать бессимптомно или с невысокой температурой, недомоганием.
- Инфильтративный туберкулез легких. Является одним из осложнений очагового туберкулеза. Протекает тяжело, с длительной лихорадкой, потерей веса, кашлем, может наблюдаться кровохарканье.
- Казеозная пневмония. Тяжелая форма легочного туберкулеза, развивается остро, с тяжелой интоксикацией, лихорадкой. Характеризуется массивным воспалением и затем распадом легочной ткани с образованием полостей в легком. Чаще всего возникает у больных с ослабленным иммунитетом.
- Туберкулема легких. В ткани легкого образуется инкапсулированный очаг более 1 см в диаметре, внутри которого происходит распад легочной ткани.
- Кавернозный туберкулез легких. Тяжелая форма туберкулеза, при которой происходит деструкция легочной ткани и образуются большие каверны (полости) в легком. Возникает как осложнение других форм туберкулеза.
- Фиброзно-кавернозный туберкулез легких. Является завершающим этапом кавернозного туберкулеза, когда окончательно формируется полость в легком.
- Цирротический туберкулез легких. Последняя стадия туберкулеза легких, характеризуется замещением легочной ткани на рубцовую. Встречается в 0,1-8% случаев, в основном у нелеченых или неправильно леченых пациентов. Для формирования данной формы требуются годы болезни.
- Туберкулезный плеврит. Воспалительный процесс поражает оболочку легких – плевру. Может развиться как осложнение туберкулеза легких или как самостоятельное заболевание, особенно у молодых людей.
- Туберкулез бронхов, трахеи, верхних дыхательных путей.
- Туберкулез органов дыхания, комбинированный с профессиональными пылевыми заболеваниями легких.
- с выделением микобактерий туберкулеза (МБТ+);
- без выделения микобактерий туберкулеза (МБТ–).
- Выраженная слабость, утомляемость, хроническая усталость.
- Бессонница, ночные кошмары.
- Снижение аппетита и потеря массы тела.
- Ночная потливость (она может быть настолько сильной, что больному приходится менять постельное белье).
- Повышение температуры тела, в основном до субфебрильных значений, то есть не выше 37,5°С. Температура держится постоянно и сопровождается ознобом.
- Кашель. Сначала больных беспокоит сухой кашель, но по мере прогрессирования заболевания появляется мокрота.
- Кровохарканье. Характерно для более поздних стадий туберкулеза.
- Боль в грудной клетке. Возникающая при кашле боль свидетельствует о вовлечении плевры в патологический процесс.
- Сильная одышка.
-
Клинический анализ крови с развернутой лейкоцитарной формулой (с целью выявления воспалительного процесса).
Синонимы: Общий анализ крови, ОАК. Full blood count, FBC, Complete blood count (CBC) with differential white blood cell count (CBC with diff), Hemogram. Краткое описание исследования Клинический анализ крови: общий анализ, лейкоформула, СОЭ См. также: Общий анализ – см. тест № 5, Лейкоцит.
Синонимы: Общий белок сыворотки крови; Общий сывороточный белок. Total Protein; Serum Тotal Protein; Total Serum Protein; TProt; ТР. Краткая характеристика определяемого вещества Общий белок Сыворотка крови (плазма крови, лишенная фибриногена) содержит множество белков, выполняющих разнообразны.
Тест предназначен для скрининговой оценки состава и количественного соотношения фракций белка сыворотки крови методом электрофореза. Синонимы: Электрофорез белков сыворотки. SPEP. Краткая характеристика белковых фракций сыворотки крови Общий белок сыворотки крови состоит из смеси белков с ра.
С-реактивный белок – белок острой фазы, чувствительный индикатор повреждения тканей при воспалении, некрозе, травме. Синонимы: Анализ крови на СРБ; С-реактивный белок сыворотки крови. C-reactive Protein (CRP), quantitative; C-reactive protein test; CRP test. Краткое описание опред.
Аланинаминотрансфераза − внутриклеточный фермент, участвующий в метаболизме аминокислот. Тест используют в диагностике поражений печени, сердечной и скелетных мышц. Синонимы: Глутамат-пируват-трансаминаза; Глутамат-пируват-трансаминаза в сыворотке; СГПТ. Alanine aminotransferase; S.
Синонимы: Глутамино-щавелевоуксусная трансаминаза; Глутамат-оксалоацетат-трансаминаза сыворотки крови (СГОТ); L-аспартат 2-оксоглутарат аминотрансфераза; ГЩТ. Aspartateaminotransferase; Serum Glutamicoxaloacetic Transaminase; SGOT; GOT. Краткая характеристика определяемого вещества АсАТ .
Синонимы: Анализ крови на ЛДГ; Лактатдегидрогеназа; L-лактат; НАД+Оксидоредуктаза; Дегидрогеназа молочной кислоты. Lactate dehydrogenase, Total; Lactic dehydrogenase; LDH; LD. Краткая характеристика определяемого вещества Лактатдегидрогеназа ЛДГ – цитоплазматический.
Синонимы: Анализ крови на креатинин; Сывороточный креатинин; Креатинин сыворотки, оценка СКФ. Сreat; Сre; Blood Creatinine; Serum Creatinine; Serum Creat. Краткая характеристика определяемого вещества Креатинин Креатинин – низкомолекулярное азотсодержащее вещество, продукт метаболизма креа.
Синонимы: Анализ крови на электролиты; Электролиты в сыворотке крови. Electrolyte Panel; Serum electrolyte test; Sodium, Potassium, Chloride; Na/K/Cl. Краткая характеристика определяемых веществ (Калий, Натрий, Хлор) Калий (К+) Основной внутриклеточный катион. Кал.
Общий кальций – основной компонент костной ткани и важнейший биогенный элемент, обладающий важными структурными, метаболическими и регуляторными функциями в организме. Синонимы: Анализ крови на общий кальций; Общий кальций в сыворотке. Total blood calcium; Total calcium; Bl.
Определение ДНК возбудителей туберкулеза: комплекса микобактерий: M. tuberculosis, M. bovis, M. bovis BCG, M. microti, M. africanum в мокроте, смывах с бронхов, лаважной жидкости методом полимеразной цепной реакции (ПЦР) с детекцией в режиме «реального времени. Туберкулёз (от лат. tubercul.
Рентгенологическое исследование структуры легких с целью диагностики различных патологий.
Исследование, позволяющее получить данные о состоянии органов грудной клетки и средостения.
Диагностический тест с постановкой внутрикожной пробы для всех возрастных групп с целью диагностики туберкулезной инфекции.
Туберкулез – инфекционное хроническое заболевание, вызываемое микобактериями туберкулеза (Mycobacterium tuberculosis complex). Активный туберкулез развивается приблизительно у 10% людей, инфицированных M. tuberculosis. В остальных случаях благодаря иммунной системе происходит элиминация возбуд.
Лечение туберкулеза легких
Успех лечения во многом зависит от ранней диагностики заболевания. Терапия туберкулеза длительная и составляет от 4 месяцев до нескольких лет.
Самостоятельное прекращение приема лекарств, пропуск или уменьшение дозировки могут вызвать резистентность, то есть устойчивость микобактерий к антибиотикам.
Во время лечения необходимо отказаться от курения и употребления алкоголя.
Терапия туберкулеза подразумевает комбинацию нескольких антибактериальных препаратов. В основном все лекарства принимают в таблетированной форме, однако в начале заболевания или при тяжелом течении требуется их внутривенное введение.
Лечение туберкулеза осуществляется как дома, так и в специализированном стационаре. Госпитализация показана при первичном обнаружении туберкулеза, для лечения тяжелых форм туберкулеза и для хирургического лечения туберкулеза легких.
Во время терапии туберкулеза очень важно полноценно питаться, получая с пищей необходимое количество калорий, витаминов и питательных веществ.
Калорийность пищи должна быть на 10% выше, чем при обычном образе жизни. Молочные продукты, нежирное мясо, рыба, орехи богаты белком, который необходим для укрепления иммунитета. Обязательно нужно включать в меню овощи, зелень, цельнозерновые продукты. Следует избегать фастфуда, жирной, копченой пищи, сахара и сладких газированных напитков.
К неспецифическим осложнениям, характерным для многих легочных заболеваний, врачи относят кровохарканье, легочное кровотечение, спонтанный пневмоторакс. Спонтанный пневмоторакс – это попадание воздуха в плевральную полость вследствие повреждения ткани легкого. Наличие воздуха в плевральной полости сдавливает легкие и мешает нормальному процессу дыхания. Описаны случаи, когда к пневмотораксу приводит образование бронхоплевральных свищей.
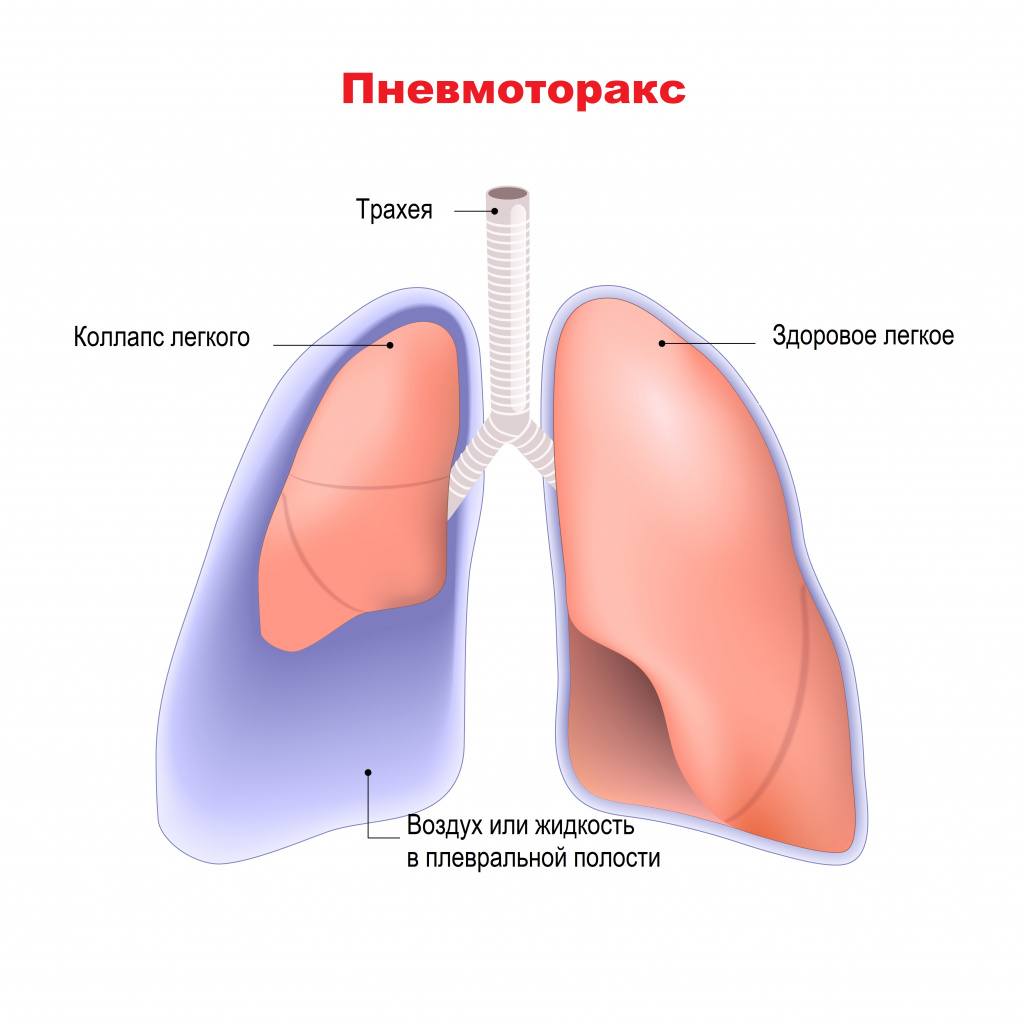
К редким, но грозным осложнениям относятся: ателектаз (спадение части легкого, которая перестает участвовать в газообмене и процессе дыхания), абсцесс легкого (образование гнойника в ткани легкого), амилоидоз внутренних органов (в результате длительного воспалительного процесса происходит нарушение белкового обмена, в органах начинает откладываться белок-амилоид, вследствие чего нарушается их нормальная работа), хроническая легочная недостаточность.
К специфическим осложнениям, характерным для туберкулеза легких, относятся: туберкулез бронхов, трахеи, гортани, корня языка; туберкулезный плеврит; туберкулезная эмпиема – скопление гноя в плевральной полости.
Профилактика туберкулеза легких
К специфической профилактике относится вакцинация.
Вакцину вводят внутрикожно, после чего формируется местный туберкулезный процесс, неопасный для общего здоровья. Впоследствии организм вырабатывает специфический иммунитет против микобактерий. Это значит, что привитой ребенок с хорошим поствакцинальным иммунитетом при встрече с микобактериями либо не инфицируется, либо переносит инфекцию в легкой форме.
Иммунитет, приобретенный после прививки БЦЖ, сохраняется в среднем 5 лет. Повторные вакцинации проводят в 7 и 14 лет.
Профилактика туберкулеза у взрослых включает ежегодную диспансеризацию с выполнением флюорографии легких.
- Карачунский М.А. Дифференциальная диагностика туберкулеза легких // Пульмонология и аллергология. – Т.1. – 2005. С. 6–9.
- Клинические рекомендации «Туберкулез у взрослых. Разраб.: Российское Общество Фтизиатров, Ассоциация фтизиатров. – 2022.
- Клинические рекомендации «Туберкулез у детей. Разраб.: Российское Общество Фтизиатров. – 2020.
Информацию из данного раздела нельзя использовать для самодиагностики и самолечения. В случае боли или иного обострения заболевания диагностические исследования должен назначать только лечащий врач. Для постановки диагноза и правильного назначения лечения следует обращаться к Вашему лечащему врачу.

Задание 7 № 6
Определите происхождение болезней, приведённых в списке. Запишите номер каждой из болезней в списке в соответствующую ячейку таблицы. В ячейках таблицы может быть записано несколько номеров.
Список болезней человека:
1) ветряная оспа
2) синдром Дауна
3) инфаркт миокарда
Передается по наследству: синдром Дауна. Инфекционные заболевания: ветряная оспа, дизентерия, малярия. Неинфекционное: инфаркт миокарда.
Ответ: наследственное — 2, инфекционное — 145, неинфекционное — 3.

Задание 7 № 945
Определите происхождение болезней, приведённых в списке. Запишите номер каждой из болезней в списке в соответствующую ячейку таблицы. В ячейках таблицы может быть записано несколько номеров.
Список болезней человека:
| Глистные инвазии | Вирусная инфекция | Неинфекционное заболевание |
Глистная инвазия – это большая группа болезней, связанная с проникновением паразитических червей в организм человека.
Неинфекционные заболевания — известные также как хронические болезни, не передаются от человека человеку. Они имеют длительную продолжительность и, как правило, медленно прогрессируют.
Вирусные инфекции – большая группа заболеваний, причиной которых служит вирус.
Ответ: Глистные инвазии — 13, вирусная инфекция — 4, неинфекционное заболевание — 25.

Задание 7 № 946
Определите происхождение болезней, приведённых в списке. Запишите номер каждой из болезней в списке в соответствующую ячейку таблицы. В ячейках таблицы может быть записано несколько номеров.
Список болезней человека:
Инфекционные заболевания — группа заболеваний, вызываемых проникновением в организм патогенных (болезнетворных) микроорганизмов, вирусов.
Неинфекционные заболевания — известные также как хронические болезни, не передаются от человека человеку. Они имеют длительную продолжительность и, как правило, медленно прогрессируют.
Ответ: Бактериологические — 13, вирусные — 4, неинфекционное заболевание — 25.

Задание 7 № 947
Определите происхождение болезней, приведённых в списке. Запишите номер каждой из болезней в списке в соответствующую ячейку таблицы. В ячейках таблицы может быть записано несколько номеров.
Список болезней человека:
5) куриная слепота
Инфекционные заболевания — группа заболеваний, вызываемых проникновением в организм патогенных (болезнетворных) микроорганизмов, вирусов.
Неинфекционные заболевания — известные также как хронические болезни, не передаются от человека человеку. Они имеют длительную продолжительность и, как правило, медленно прогрессируют.
Наследственные заболевания – это болезни, появление и развитие которых связано со сложными нарушениями в наследственном аппарате клеток, передаваемых через гаметы (репродуктивные клетки). Обусловлено возникновение таких недугов нарушениями в процессах хранения, реализации и передачи генетической информации.
Что такое рахит? Причины возникновения, диагностику и методы лечения разберем в статье доктора Федотовой Натальи Николаевны, педиатра со стажем в 11 лет.
Над статьей доктора Федотовой Натальи Николаевны работали литературный редактор Вера Васина , научный редактор Наталья Бычкова и шеф-редактор Маргарита Тихонова

Определение болезни. Причины заболевания
Рахит (Rickets) — это заболевание, которое возникает при нарушениях обмена фосфора и кальция, из-за чего растущая костная ткань не минерализируется [6] . Болезнью страдают только дети, преимущественно грудного и раннего возраста.
К рахиту приводит дефицит витамина D, а именно его активных метаболитов — кальцитриола и кальцидиола. При заболевании повышается нервная возбудимость, деформируются кости и снижается мышечный тонус [13] [14] [15] [16] [17] .
![Рахит [18]](https://probolezny.ru/media/bolezny/rahit/rahit-18_s.jpg)
Распространённость рахита
Рахит встречается во всём мире, но чаще всего его выявляют у народов Крайнего Севера. В этих районах не хватает солнечного света, а 90 % образующегося в организме витамина D вырабатывается в коже под влиянием ультрафиолета. По последним данным, частота рахита в России колеблется от 54 до 66 %, но преобладают лёгкие и стёртые формы [13] .
Причины и факторы риска рахита
Выделяют первичный и вторичный рахит. Разница между ними — в причинах заболевания, которые, в свою очередь, связаны с возрастом ребёнка.
Причины первичного витамин D-дефицитного рахита:
- Ребёнок мало времени проводит на свежем воздухе, ему не хватает солнечного света. Постоянное пребывание в помещении — это важный фактор развития рахита.
- Пищевые факторы:
- питание неадаптированными молочными смесями, в которые в том числе не добавлен витамин D;
- длительное исключительно молочное вскармливание (женским или коровьим молоком), введение прикорма позднее 6-месячного возраста;
- применение только вегетарианского прикорма: овощей, фруктов, злаков, бобовых [1] .
К предрасполагающим причинам относятся факторы, связанные с беременностью и родами:
- возраст матери младше 17 и старше 35 лет [13] ; ;
- плацентарная недостаточность;
- несбалансированное питание беременной, недостаток двигательной активности и свежего воздуха;
- недоношенность (преждевременные роды);
- большая масса плода при рождении (более 4 кг);
- низкая масса тела при рождении (менее 1,5 кг).
Причины вторичного витамин D-дефицитного и минералдефицитного рахита:
- Синдром мальабсорбции — нарушенное всасывание питательных веществ в тонком кишечнике; синдром мальдигестии — недостаточность пищеварения (глютеновая энтеропатия, муковисцидоз и другие заболевания) [15] .
- Повышенная проницаемость кишечной стенки и хронические неспецифические воспалительные заболевания кишечника (болезнь Крона, неспецифический язвенный колит).
- Лактазная недостаточность — в организме отсутствует, недостаточно вырабатывается или слабо активен фермент лактаза, расщепляющий молочный сахар (лактозу).
- Тяжёлые и длительно текущие энтериты с выраженным дисбактериозом и диареей.
- Гипофосфатемия как генетическая патология, наследуемая по Х-сцепленному доминантному типу.
- Хронические болезни печени и почек: хронический гепатит, в том числе аутоиммунный; первичный склерозирующий холангит; наследственное заболевание печени, обусловленное недостаточностью a-1-антитрипсина; нефрогенные остеопатии — аномалии развития почек (поликистоз, гипоплазия почек), интерстициальный нефрит, тубулопатии.
- Медикаментозные факторы:
- приём противосудорожных средств (Фенобарбитала и Дифенина) от полугода;
- длительное применение диуретиков (зависит от частоты приёма и дозы; но обычно с ними назначаются витамин D и микроэлементы);
- внутривенное питание более пяти дней.
- Экологические факторы:
- повышенное содержание в почве, воде и пище тяжёлых металлов: стронция, свинца, цинка;
- избыток фосфора в продуктах питания;
- недостаток кальция в почве и воде и, соответственно, в овощах.
Также к развитию рахита предрасполагают:
- недостаточная двигательная активность ребёнка (тугое пеленание, отсутствие гимнастики);
- нарушения обмена веществ;
- полигиповитаминозы (дефицит многих витаминов);
- хронические инфекции.
При обнаружении схожих симптомов проконсультируйтесь у врача. Не занимайтесь самолечением - это опасно для вашего здоровья!
Симптомы рахита
Клинические проявления рахита зависят от периода его развития. Выделяют начальный период, период разгара, выздоровления и остаточных явлений.
Начальный период
Симптомы заболевания отчётливо видны в 3–4-месячном возрасте, но первые признаки проявляются уже в 1–1,5 месяца. К таким проявлениям относятся:
- повышенная нервная возбудимость: ребёнок становится беспокойным, пугливым, раздражительным, излишне чувствительным к внешним факторам; у него нарушается сон, он часто вздрагивает, особенно при засыпании, громком звуке или внезапной вспышке света;
- снижение аппетита;
- сильная потливость, особенно во сне и при кормлении; пот приобретает кислый запах, становится липким;
- облысение затылка (из-за повышенной потливости головки, беспокойства и трения о постель или шапочку);
- резкий запах мочи;
- сниженный тонус мышц; .
Начальный период рахита длится от 1,5 недель до месяца.
Период разгара
Далее наступает период разгара, во время которого возникают изменения со стороны скелета:

![Костные утолщения запястий при рахите [19]](https://probolezny.ru/media/bolezny/rahit/kostnye-utolsheniya-zapyastiy-pri-rahite-19_s.jpg)
Период выздоровления
Исчезают признаки активного рахита, такие как потливость, повышенная нервная возбудимость, сниженный мышечный тонус, размягчение костей и др. Обычно этот период наступает после лечения, но может возникать и спонтанно.
Период остаточных явлений
Патогенез рахита
Витамин D поступает в организм с едой и пищевыми добавками, а также образуется в коже под воздействием солнечного света. Чтобы поступивший из пищи витамин D стал активным, ему предстоит пройти две последовательные реакции окисления:
- первая реакция протекает в печени, в результате образуется кальцидиол;
- вторая реакция проходит в почках и завершается выработкой активной формы — кальцитриола.
Кальцитриол контролирует обмен кальция в организме. При низкой концентрации ионов кальция он способствует его мобилизации из костной ткани. Также кальцитриол повышает содержание кальция и фосфора во внеклеточной жидкости, что укрепляет растущие кости.
В метаболизме витамина D важная роль принадлежит паратгормону — гормону паращитовидной железы. При дефиците витамина D развивается гипокальциемия, из-за чего избыточно вырабатывается паратгормон, что ведёт к потере фосфора и снижает отложение кальция в костях.
На начальной стадии рахита снижается концентрация кальция в сыворотке крови. При этом активируется паратгормон, что возвращает уровень кальция в норму, но содержание фосфора остаётся низким. Щелочная фосфатаза просачивается во внеклеточную жидкость, её концентрация повышается от умеренной до очень высокой [2] . Щелочная фосфатаза вырабатывается остеобластами — сверхактивными клетками костной ткани, играющими важную роль в её формировании и обновлении. Чем выше их активность, тем больше концентрация щелочной фосфатазы в крови, поэтому её уровень высок после переломов.
Классификация и стадии развития рахита
В клинической педиатрии многие годы используется классификация рахита, принятая на VI Всесоюзном съезде детских врачей в 1947 году по предложению педиатра С. О. Дулицкого. В ней предусмотрено уточнение периода болезни, её течения и степени тяжести [15] .
По периоду заболевания различают начальный период, период разгара, выздоровления и остаточных явлений.
По характеру течения выделяют:
По тяжести течения рахита выделяют:
Осложнения рахита
У детей, страдающих рахитом, может возникнуть спазмофилия — состояние, при котором появляются судороги и другие признаки повышенной нервно-мышечной возбудимости.
Для спазмофилии характерны:
- лицевой феномен Хвостека — мышцы лица сокращаются в ответ на удар молоточком в области перед ухом, где проходит лицевой нерв ;
- симптом Эрба — мышцы сокращаются при воздействии электрического тока силой менее 5 мА.
Смазмофилия возникает из-за снижения уровня ионов кальция в крови менее 1,0 ммоль/л (общего кальция ниже 1,8 ммоль/л) на фоне увеличения pH крови и других тканей организма.
Спазмофилию могут провоцировать острые респираторные вирусные инфекции, гипервентиляция лёгких, нервно-психическое возбуждение, рвота, терапия витамином D одновременно с ультрафиолетовым облучением (УФО) [13] .
Диагностика рахита
Для диагностики рахита врач собирает анамнез (историю болезни), осматривает ребёнка и назначает лабораторно-инструментальные исследования.
Лабораторная диагностика:
- анализ крови на содержание кальция — на начальной стадии рахита его уровень снижен (2,0 ммоль/л), но на момент постановки диагноза часто повышается до нормы (2,2 – 2,7 ммоль/л), что связано с активной секрецией гормонов паращитовидной железы;
- определение уровня фосфора в сыворотке крови — обычно его уровень ниже возрастной нормы (1,5 – 1,8 ммоль/л);
- исследование концентрации в крови щелочной фосфатазы — обычно её содержится примерно в два раза больше, чем в норме (более 400 ЕД/л);
- исследование содержания в крови паратгормона — обычно также повышено;
- определение уровня метаболита витамина D (кальцитриола) в крови — может быть нормальным или повышенным из-за активной работы паращитовидной железы.
![Снимок коленного сустава при рахите [20]](https://probolezny.ru/media/bolezny/rahit/snimok-kolennogo-sustava-pri-rahite-20_s.jpg)
Перечисленные исследования позволяют как уточнить диагноз, так и контролировать эффективность лечения [16] .
Дифференциальная диагностика
Рахит следует отличать от следующих заболеваний:
- Гипофосфатазия — редкое генетическое врождённое заболевание, при котором нарушается минерализация костей скелета и зубов, возникают системные осложнения: проблемы с дыханием, судороги, слабость мышц, боль в костях и кальциноз почек.
- Синдром Янсена — редкая аутосомно-доминантная форма нарушения развития костей, для которой характерно поражение метафизов и непропорционально низкий рост.
- Гипофосфатемический рахит, устойчивый к витамину D, — наследственная группа заболеваний, при которых из организма избыточно выводится фосфор. Болезнь может развиться из-за поломок в различных генах, которые регулируют обмен фосфора. В результате нарушается минерализация костной ткани и не хватает энергии мышцам, так как молекула АТФ (аккумулятор энергии в организме) включает фосфор. Когда ребёнок начинает ходить, под тяжестью собственного тела у него появляются рахитические деформации ног.
- Дефицит кальция — признаки нехватки кальция и витамина D одинаковы. Отличить состояния можно, сдав анализ крови.
- Дефицит фосфора — может развиться у недоношенных детей, находящихся на грудном вскармливании и не получающих минеральных добавок. Симптомы также схожи с дефицитом витамина D, поэтому такое состояние можно ошибочно принять за рахит.
Лечение рахита
Для лечения и профилактики назначают витамин D: минимум 1000 МЕ в сутки для детей грудного возраста, 1500 – 2000 МЕ — детям от года до трёх лет. Используются капли — Аквадетрим, Вигантол, ДеТриФерол. Аквадетрим также есть в таблетках. Препараты применяют ежедневно в течение нескольких месяцев, пока концентрация щелочной фосфатазы не приблизится к норме.
Также рекомендуется регулярно гулять на свежем воздухе, проводить общий массаж и заниматься лечебной гимнастикой. В первый год жизни ребёнка следует кормить грудью или адаптированной смесью и своевременно вводить прикормы [5] . Остаточные явления рахита устраняются с помощью лечебной физкультуры и массажа.
Ребёнку, страдающему рахитом, обязательно проводится санация очагов инфекции (например, носоглотки, кишечника, мочевыводящей системы). Детям с перинатальным поражением центральной нервной системы, т .е. возникшим во время беременности и родов, нужно своевременно проходить неврологическое лечение и реабилитацию.
Повышенная чувствительность и передозировка витамином D может привести к повышенному уровню кальция в крови и моче. При этих состояниях нарушается сердечный ритм, появляется тошнота, рвота, головная боль, слабость, раздражительность, снижается вес, усиливается жажда, учащается мочеиспускание, образуются почечные камни, повышается уровень кальция в почках и мягких тканях, возникает почечная недостаточность, анорексия, гипертония, запор или жидкий стул.
При хронической передозировке витамином D возникает деминерализация костей, кальций откладывается в почках, сосудах, сердце, лёгких, кишечнике и нарушается работа органов [6] . Развивается полиурия и полидипсия — обильное выделение мочи и очень сильная жажда. Повышенная концентрация кальция в крови и моче способствует нефрокалькулёзу и нефрокальцинозу. Всё это может привести к смерти пациента, поэтому принимать витамин D нужно под контролем врача и с наблюдением за лабораторными показателями [17] .
Прогноз. Профилактика
Дети с витамин D-дефицитным рахитом, как правило, хорошо реагируют на адекватное лечение препаратами витамина D. Однако как во время выздоровления, так и в период остаточных явлений, у них могут сохраняться, а иногда даже усиливаться кариес, деформация грудной клетки и костей таза, нарушение осанки и искривление ног.
У женщин, перенёсших в детстве рахит, может развиться поясничный лордоз — искривление поясничного отдела позвоночника, при котором этот отдел как бы уходит вперёд, к животу. Из-за этого могут быть сужены размеры входа и выхода из малого таза, что осложняет вынашивание плода и роды, часто требуется операция кесарева сечения [15] .
Профилактика рахита
Профилактику рахита нужно начинать ещё до рождения ребёнка. Пища беременной женщины должна содержать достаточно калорий, белков, жиров, углеводов, минеральных солей и витаминов. Обязательны прогулки на свежем воздухе и здоровый образ жизни. Специфическая профилактика в этом периоде заключается в приёме витамина D. Учитывая, что в России часто встречается его дефицит, всем женщинам, готовящимся к зачатию, желательно получать витамин D в профилактических дозах (не менее 600–800 МЕ витамина D в сутки). При наступлении беременности дозу увеличивают до 800–1200 МЕ в сутки.
Постнатальная профилактика рахита начинается сразу после рождения ребёнка. Предпочтительнее естественное вскармливание, но важно своевременно ввести прикорм. Также нужно заниматься гимнастикой, принимать воздушные ванны, проводить массаж, водные процедуры, гулять на свежем воздухе и поддерживать положительный эмоциональный тонус ребёнка.
Специфическая профилактика рахита заключается в приёме витамина D [15] . Искусственные заменители грудного молока, хотя и обогащены им (в среднем 40–45 МЕ на 100 мл), суточную потребность не покрывают. Шестимесячный ребёнок, находящийся на искусственном вскармливании, получает не более 15–20 % необходимого витамина D. Относительно низкая его усвояемость приводит к тому, что это количество оказывается ниже ещё в два раза. Даже самые лучшие смеси не способны обеспечить ребёнка достаточным количеством этого витамина.
Согласно международным рекомендациям, чтобы предотвратить рахит, нужен ультрафиолетовый свет или 10 мкг (400 МЕ) препарата витамина D ежедневно и нормальное поступление кальция и фосфора [11] [12] . В день достаточно 20 минут ультрафиолетового облучения, попадающего на лицо светлокожего ребёнка, и на несколько минут больше для детей с повышенной пигментацией.
В руководстве по клинической практике Эндокринного общества США сказано, что детям первого года жизни в сутки требуется принимать 400–1000 МЕ витамина D, а детям от года — 600–1000 МЕ [9] . Европейское общество детской гастроэнтерологии, гепатологии и питания также рекомендует приём витамина D по 400 МЕ/сутки детям первого года жизни [10] .
Отечественные рекомендации отличаются из-за климатических особенностей. Профилактические дозы витамина D составляют:
- детям 1–12 месяцев — 1000 МЕ/сутки без перерыва на летние месяцы (не требует пересчёта у детей на смешанном и искусственном вскармливании);
- детям 1–3 лет — 1500 МЕ/сутки без перерыва на летние месяцы;
- детям 3–18 лет —1000 МЕ/сутки без перерыва на летние месяцы.
- беременным женщинам — 2000 МЕ на весь период беременности [14] .
Для Европейского севера России рекомендованы следующие дозы в зависимости от возраста ребёнка:
- 1–6 месяцев (вне зависимости от вида вскармливания) – 1000 МЕ/сутки;
- 6–12 месяцев – 1500 МЕ/сутки;
- 1–3 года – 1500 МЕ/сутки;
- дети старше 3 лет – 1500 МЕ/сутки.
Информацию из данного раздела нельзя использовать для самодиагностики и самолечения. В случае боли или иного обострения заболевания диагностические исследования должен назначать только лечащий врач. Для постановки диагноза и правильного назначения лечения следует обращаться к Вашему лечащему врачу.
Альбинизм: причины появления, симптомы, диагностика и способы лечения.
Определение
Альбинизм (от лат. albus — белый) рассматривается как наследственное заболевание и характеризуется врожденным частичным или полным отсутствием в организме пигмента меланина. Таким образом, кожа, волосы и радужная оболочка глаз выглядят обесцвеченными, бледными или имеют более светлый оттенок, чем должны были быть в норме.

Аномалия встречается примерно у 1 из 10-20 тысяч человек на земном шаре и не зависит от этнической принадлежности и пола.
Причины появления альбинизма
Цвет кожи детерминирован генетически. Наличие альбинизма говорит о мутации генов (на настоящий момент описаны 19 генов, отвечающих за появление альбинизма), ответственных за цвет кожи, волос и радужной оболочки глаз. Эти мутации приводят к недостаточной активности фермента тирозиназы, благодаря которой синтезируется аминокислота тирозин, являющаяся основным регулятором производства пигмента меланин – так схематично и очень упрощенно выглядит меланогенез.
Заболевание передается по аутосомно-рецессивному (то есть оба родителя должны являться носителями рецессивного гена) и Х-сцепленному (только в случае с геном GRP143) типам наследования.
Классификация заболевания
Ранее случаи альбинизма разделяли только по внешним (фенотипическим) проявлениям – полный и неполный.
К первому относились все типы альбинизма с выраженными нарушениями пигментации глаз, кожи и ее придатков. К неполным формам – глазные типы заболевания, когда отмечался недостаток пигментации радужной оболочки, а также те разновидности патологии, которые приводили к пятнистости кожи.
В настоящее время принята классификация, основанная на генетических аспектах:
Глазокожный альбинизм тип 1А – полное отсутствие пигмента меланина в организме.
Глазокожный альбинизм тип 1В – при этом типе синтезируется дефектный фермент тирозиназа, поэтому синтез меланина возможен, но с имеет разную степень выраженности.
Температурно-чувствительный глазокожный альбинизм – активность синтеза пигмента зависит от температуры тела. Для него характерно падение активности фермента тирозиназы, если температура тела более 37̊С. При этом типе альбинизма преобладают поражения глаз, поскольку их температура всегда выше 37̊С.
Глазокожный альбинизм тип 2 – активность фермента тирозиназы, нормальная, но нарушен транспорт тирозина, в результате чего меланин не синтезируется.
Глазокожный альбинизм тип 3 – встречается только у африканцев, формируется коричневая окраска кожного покрова.
Глазной альбинизм рецессивный и связанный с Х-хромосомой – синтез пигмента частично нарушен.
Аутосомно-рецессивный глазной альбинизм – данный тип не удалось связать с какими-либо генетическими нарушениями.
Кроме изолированных глазного и глазокожного типов существуют редкие наследственные синдромы альбинизма, которые связаны с системными поражениями. К ним относятся синдром Германски-Пудлака и синдром Чедиака-Хигаси, встречающиеся, к счастью, крайне редко.
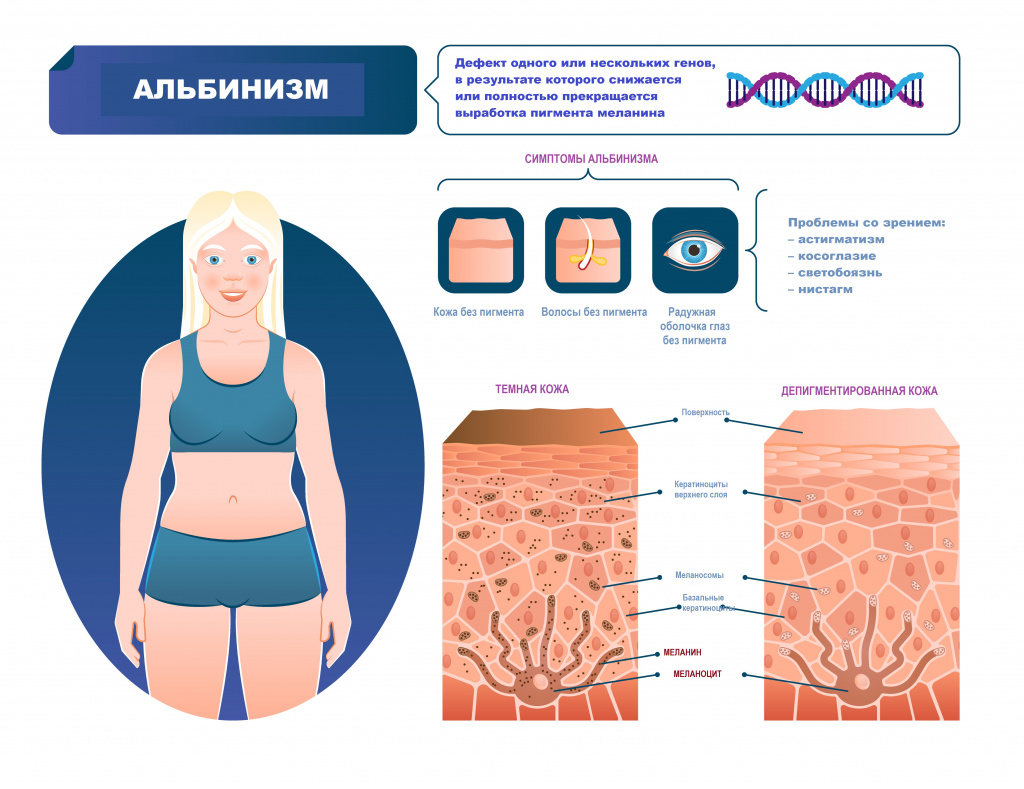
Симптомы альбинизма
Признаки альбинизма, как правило, очевидны, однако могут быть выражены слабо (это зависит от типа альбинизма и дефектного гена). При видимых нарушениях обесцвечены и кожа, и волосы, и радужная оболочка глаз. Один из важных симптомов альбинизма – зрительные нарушения:
- нистагм – быстрые, непроизвольные возвратно-поступательные движения глаз;
- косоглазие – неспособность обоих глаз оставаться направленными в одну и ту же точку или двигаться в унисон;
- экстремальная близорукость или дальнозоркость;
- светобоязнь – чувствительность к свету, иногда переходящая в дневную слепоту;
- астигматизм – аномальная кривизна передней поверхности глаза или внутренней части глаза, вызывающая снижение зрительной функции.
Диагноз ставится сразу после рождения ребенка. Врач-педиатр оценивает состояние пигментации кожи и волос, а офтальмолог – наличие той или иной зрительной патологии.
Подтвердить диагноз альбинизма может врач-генетик, проведя секвенирование генов. Очень важно выявить наследственный характер патологии и собрать анамнез.
Редким и дорогостоящим методом, но позволяющим уточнить прогноз заболевания, является определение тирозиназной активности в тканях (например, в волосяных фолликулах).
Чем лучше сохранена активность тирозиназы в тканях, тем ниже выраженность других симптомов альбинизма.
К каким врачам обращаться
Диагностикой альбинизма занимается врач дерматолог, но первым обнаруживает признаки альбинизма педиатр . При наличии патологии зрения необходима консультация офтальмолога.
Лечение альбинизма
На сегодняшний день специфического лечения альбинизма не существует, поэтому усилия врачей направлены на коррекцию остроты зрения больных и профилактику злокачественных патологий кожи.
- Из-за отсутствия меланина, выполняющего защитную функцию, люди с альбинизмом имеют высокий риск рака кожи.
- Со стороны органов зрения: снижение остроты зрения, отслойка сетчатки.
Специфической профилактики не разработано, есть только профилактические мероприятия, позволяющие улучшить качество жизни больного. Пациентам с альбинизмом рекомендовано защищать глаза от солнечного света солнцезащитными очками. Не рекомендуется находиться на ярком солнце и в любом случае следует защищать кожу специальными солнцезащитными средствами с высоким SPF.
Важно регулярно проходить осмотры дерматолога и офтальмолога для снижения риска развития осложнений.
- Кадышев В.В., Ряжская СА., Халанская О.В. и др. Клинико-генетические аспекты альбинизма // Клиническая офтальмология. – 2021;21(3). – С. 175-180. DOI: 10.32364/2311-7729-2021-21-3-175-180
- Бутов Ю. С. Дерматовенерология. Национальное руководство. Краткое издание / под ред. Ю. С. Бутова, Ю. К. Скрипкина, О. Л. Иванова. – М.: ГЭОТАР-Медиа, 2020. – 896 с.
- Лоскутов И. А. Симптомы и синдромы в офтальмологии / Лоскутов И. А., Беликова Е. И., Корнеева А. В. – М.: ГЭОТАР-Медиа, 2021. – 256 с.
Информацию из данного раздела нельзя использовать для самодиагностики и самолечения. В случае боли или иного обострения заболевания диагностические исследования должен назначать только лечащий врач. Для постановки диагноза и правильного назначения лечения следует обращаться к Вашему лечащему врачу.

Дифтерия - это острое инфекционное заболевание, опасное для жизни. Наиболее восприимчивы к нему дети в возрасте 3–7 лет, в последние годы увеличилась заболеваемость подростков и взрослых.
Дифтерия – это острое инфекционное заболевание, опасное для жизни. Оно протекает в виде острого воспаления верхних дыхательных путей, преимущественно глотки (примерно 90% случаев), носа, кожи в местах ее повреждения, глаз или половых органов.
Основную угрозу, однако, представляет не воспаление, а отравление токсином, который вырабатывает бактерия – возбудитель заболевания, при этом преимущественно поражаются сердечно-сосудистая и нервная системы.
Возбудитель дифтерии и пути заражения
Возбудителем дифтерии являются Corynebacterium diphteriae – грамположительные бактерии в виде палочек с характерными колбовидными утолщениями на концах, которые в мазках располагаются попарно, под углом в виде римской цифры V по отношению друг к другу. Дифтерийные палочки в процессе жизнедеятельности выделяют дифтерийный токсин, фермент нейраминидазу и другие биохимически активные соединения.
Синтез дифтерийного токсина микробными клетками контролируется специальным геном tox. Бактерии могут терять его в процессе жизнедеятельности, утрачивая вместе с ним и свою способность вырабатывать токсин (токсигенность). И, наоборот, изначально нетоксигенные штаммы могут приобретать патогенные свойства, к счастью, это случается крайне редко.
Заболевание передается воздушно-капельным путем от больных дифтерией или от здоровых носителей инфекции, значительно реже – через предметы обихода.
Группа риска
Наиболее восприимчивы к заражению дифтерией дети в возрасте 3–7 лет, но в последние годы увеличилась заболеваемость подростков и взрослых.
Источником инфекции являются больные люди или здоровые носители токсигенных бактерий. Наиболее заразны страдающие дифтерией зева, носа и гортани, так как они активно выделяют возбудителей заболевания с выдыхаемым воздухом. Больные дифтерией глаз, кожи могут распространять инфекцию контактным путем (руки, предметы быта). Здоровые носители бактерий гораздо менее заразны, но отсутствие у них каких-либо внешних признаков их состояния не позволяет контролировать распространение ими инфекции, ведь выявить их можно только случайно в ходе массовых диспансерных обследований. В результате большинство случаев заражения дифтерией обусловлено контактом со здоровыми носителями дифтерийной палочки.
Инкубационный период (время от момента заражения до появления первых признаков заболевания) составляет 2–10 дней.
Дифтерийный токсин
Токсин, вырабатываемый дифтерийной палочкой, состоит из нескольких компонентов. Один из них – фермент гиалуронидаза разрушает гиалуроновую кислоту капилляров и увеличивает их проницаемость, что приводит к выходу из сосудов и пропитыванию окружающих тканей плазмой крови с отложением белка фибриногена. Второй компонент – некротоксин разрушает клетки эпителия с выделением из них фермента тромбокиназы. Тромбокиназа способствует превращению фибриногена в фибрин и образованию на поверхности тканей фибринной пленки. При действии дифтерийного токсина на небные миндалины, которые покрыты несколькими слоями эпителиальных клеток, формируется фибиринная пленка, проникающая вглубь эпителия миндалин и плотно спаянная с ним.
Третий (основной) компонент – собственно токсин способен блокировать процессы клеточного дыхания и синтеза белковых молекул. Наиболее чувствительными к его действию являются капилляры, клетки миокарда и нервные клетки. В результате развивается дистрофия миокарда и инфекционно-токсический миокардит, повреждение капилляров приводит к инфекционно-токсическому шоку, повреждение шванновских клеток (вспомогательные клетки нервной ткани) приводит к демиелинизации нервных волокон (разрушение электроизолирующего слоя миелина с нарушением проведения нервных импульсов по нервным волокнам). Кроме того, дифтерийный токсин вызывает общую интоксикацию организма.
Симптомы и течение
Дифтерия зева обычно начинается с небольшого повышения температуры, незначительной болезненности при глотании, покраснения и отечности миндалин, формированию на них специфического пленчатого налета, увеличения передних верхних шейных лимфатических узлов. Цвет пленок – обычно белый в первые 2–3 дня заболевания, но потом приобретает серый или желтовато-серый цвет. Примерно через неделю заболевание, или заканчивается выздоровлением (легкая форма, как правило, у привитых от дифтерии), или переходит в более тяжелую токсическую форму, обусловленную системным действием дифтерийного токсина.
Токсическая форма дифтерии всегда протекает очень тяжело. Она характеризуется очень высокой температурой тела (39,5-41,0°С), сильными головными болями, сонливостью, апатией. Кожа становится бледной, во рту отмечается сухость, у детей возможна многократная рвота и боль в животе. Отек миндалин становится резко выраженным, может приводить к полному закрытию входа в глотку, распространяется на мягкое и твердое небо, часто также на носоглотку, дыхание затрудняется, голос часто становится гнусавым. Налет распространяется на все ткани ротоглотки. Классическим признаком токсической формы дифтерии зева является отек подкожной клетчатки в области шеи, а иногда и грудной клетки, в результате чего кожа приобретает студнеобразную консистенцию. Передние верхние шейные лимфатические узлы значительно увеличены и болезненны.
Дифтерия носа протекает на фоне нормальной или слегка повышенной температуры тела, интоксикация отсутствует. Из носовых ходов видно серозно-гнойное или кровянисто-гнойное отделяемое. На крыльях носа, щеках, лбу и подбородке появляются участки мокнутия, а затем сухие корочки. Внутри носа видны пленчатые налеты. Патологический процесс может также поражать придаточные пазухи носа. При токсической форме наблюдается отек подкожной клетчатки щек и шеи.
Дифтерия глаза протекает как банальный конъюнктивит и характеризуется умеренной гиперемией и отеком конъюнктивы века, небольшим количеством серозно-гнойного отделяемого из конъюнктивального мешка (катаральная форма). Пленчатая форма проявляется выраженным отеком век, наличием на их конъюнктиве трудно снимаемых пленок серовато-белого цвета. Токсическая форма также сопровождается отеком клетчатки вокруг глазницы.
Дифтерия кожи приводитк длительному не заживлению любых повреждений кожи, гиперемии, на коже присутствует грязно-серый налет, отмечается плотная инфильтрация окружающей кожи.
Диагностика
Диагностику дифтерии проводят на основании данных осмотра больного и результатов анализов. При осмотре за диагноз дифтерия говорят следующие признаки: наличие характерных пленок, а также затруднение дыхания и свистящий шум на вдохе, не характерные для ангины, лающий кашель. Диагноз дифтерии по характерным клиническим признакам при заболевании, протекающем в легкой форме, поставить сложнее.
Общий анализ крови – признаки острого воспалительного процесса.
Исследования мазка под микроскопом (бактериоскопия) – выявление имеющих характерный вид бактерий Corynebacterium diphteriae.
Бактериологическое исследование – посев биологического материала на специальную питательную среду и культивирование колоний микроорганизмов.
Определение уровня (титра) антитоксических антител (высокий титр – 0,05 МЕ/мл и выше позволяет исключить дифтерию).
Серологическое исследование – определение специфических антител в сыворотке крови с помощью методов РПГА, ИФА и др.
Дифтерию зева нужно дифференцировать от острого тонзиллита (фолликулярная и лакунарная формы), ангины Симановского-Венсана (грибковое поражение), сифилитической ангины, ложнопленочной ангины при инфекционном мононуклеозе, паратонзиллярным абсцессом, эпидемическим паротитом, лейкозом. У детей необходимо отвести диагноз ложного крупа.
Лечение
Всех заболевших дифтерией, вне зависимости от тяжести состояния, необходимо госпитализировать в инфекционную больницу.
Лечение состоит в следующем:
Диета – витаминизированная, калорийная, прошедшая тщательную кулинарную обработку еда.
Этиотропная терапия (то есть направленная на устранение причины заболевания) – введение противодифтерийной сыворотки (ПДС), доза и количество раз введения зависят от тяжести и формы заболевания. При легкой форме ПДС вводится однократно внутримышечно в дозе 20–40 тыс. МЕ, при среднетяжелой форме – 50–80 тыс. МЕ однократно или, при необходимости, повторно в той же дозе через 24 часа. При лечении тяжелой формы заболевания суммарная доза увеличивается до 90–120 тыс. МЕ или даже до 150 тыс. МЕ (инфекционно-токсический шок, ДВС-синдром). При этом 2/3 дозы вводится сразу, и в течение первых суток госпитализации должно быть введено 3/4 суммарной дозы.
Антибиотики: при легких формах – эритромицин, рифампицин внутрь, при среднетяжелых и тяжелых формах – инъекционное введение пенициллинов или цефалоспоринов. Продолжительность курса – 10–14 дней. Антибиотики не влияют на дифтерийный токсин, но уменьшают количество бактерий, его вырабатывающих.
Местное лечение – полоскания и орошения дезинфицирующими растворами.
Дезинтоксикационная терапия – глюкозо-солевыми растворами с учетом суточной потребности в жидкости и ее потерь (среднетяжелая и тяжелая форма).
Глюкокортикостероиды – при среднетяжелой и тяжелой формах.
Лечение бактерионосителей проводят антибиотиками: тетрациклины (дети старше 9 лет), эритромицин, цефалоспорины на фоне общеукрепляющей терапии и устранения хронических очагов инфекции.
Осложнения
Среди наиболее серьезных осложненийдифтерии на сердечно-сосудистую систему можно выделить миокардиты, нарушения сердечного ритма.
Неврологические осложнения дифтерии обусловлены поражением различных черепных и периферических нервов и проявляются параличом аккомодации, косоглазием, парезами конечностей, а в более тяжелых случаях параличом дыхательных мышц и мышц диафрагмы.
Вторичными осложнениями дифтерии являются такие тяжелые патологические состояния как острые нарушения мозгового кровообращения (тромбозы, эмболия), метаболическая энцефалопатия, отек головного мозга, токсические поражения почек, дифтерийный гепатит, а также инфекционно-токсический шок и ДВС-синдром (синдром дессиминированного внутрисосудистого свертывания – тяжелое нарушение системы свертывания крови). Токсическая форма дифтерии может приводить к острой почечной, сердечно-сосудистой, дыхательной или полиорганнной недостаточности.
Неспецифическими осложнениями дифтерии являются паратонзиллярный абсцесс, отит, пневмония.
Вакцинация
Вакцинация от дифтерии проводится анатоксином, то есть инактивированным токсином. В ответ на его введение в организме образуются антитела не к Corynebacterium diphteriae, а к дифтерийному токсину.
Согласно российскому прививочному календарю, вакцинация детей в возрасте до года проводится в 3, 4–5 и 6 месяцев. Первая ревакцинация проводится в 18 месяцев, вторая – в 7 лет, третья – в 14. Взрослые должны ревакцинироваться от столбняка и дифтерии каждые 10 лет.
Читайте также:

