Хронический цервицит ассоциированный с уреаплазменной инфекцией
Обновлено: 23.04.2024
В настоящее время в отечественной и зарубежной литературе отмечается повышение внимания практикующих врачей и ученых к вопросам патологии шейки матки в связи с высокой актуальностью и социальной значимостью данной проблемы.
В настоящее время в отечественной и зарубежной литературе отмечается повышение внимания практикующих врачей и ученых к вопросам патологии шейки матки в связи с высокой актуальностью и социальной значимостью данной проблемы. Поскольку слизистая оболочка шейки матки является пограничным барьером между верхним этажом генитального тракта и внешней средой, она постоянно подвергается воздействию повреждающих факторов, среди которых наиболее агрессивное влияние оказывают различные инфекции, передаваемые половым путем (А. И. Новиков, А. В. Кононов, И. Г. Ваганова, 2002).

По данным разных авторов, в настоящее время отмечена высокая частота колонизации мочеполовых органов уреаплазмами: у мужчин — 25%, у женщин — до 80%, частота бессимптомного носительства — до 45,8%. Широкое распространение уреа- и микоплазм, частое их выявление при различных заболеваниях урогенитального тракта, бессимптомное носительство, недостаточное количество знаний в отношении эпидемиологии, неоднозначное мнение ученых о степени значимости данных микроорганизмов в генезе патологических состояний урогенитального тракта — все это поддерживает интерес исследователей к данной проблеме.
Так, в популяции уреаплазмы выявляются у 5–15% населения мира. По данным статистики, уреаплазмами инфицировано 174 млн человек (ВОЗ, 1999; Donovan B. Lancet, 2004). Согласно данным собственных исследований на базе научно-поликлинического отделения НЦАГиП, у пациенток репродуктивного возраста частота встречаемости уреаплазм составляет 22,3%. При этом в качестве моноинфекции уреаплазмоз отмечен в 37,5% случаев, при смешанном инфицировании — в 62,5% (В. Н. Прилепская, О. В. Быковская, 2003).
Уреаплазмы относятся к классу Mollicutes, в который входят также микоплазмы, ахолеплазмы, спироплазмы, анаэроплазмы. В настоящее время считают, что имеется два самостоятельных вида уреаплазм: Ureaplasma parvum и Ureaplasma urealyticum — их клиническая значимость находится в стадии изучения.
Важной для клинической практики морфологической особенностью уреаплазм является их выраженный тропизм к эпителиальным клеткам, а именно к слизистым оболочкам урогенитального тракта, и способность длительно персистировать в эпителиальных клетках. Учитывая тот факт, что первичным очагом поражения являются нижние отделы мочеполовых путей, в них, и в частности в шейке матки, развиваются под влиянием уреаплазм различные патологические процессы.
В структуре патологических изменений шейки матки, обусловленных или ассоциированных с уреаплазмами, ведущее место занимают воспалительные процессы (экзо- и эндоцервициты) — 92,2%. Среди них преобладают эндоцервициты — 46,6%, на втором месте — сочетанные воспалительные процессы (экзо- и эндоцервициты) — 26,6%. Важно отметить, что высокая частота (10–15%) эктопий шейки матки у девушек-подростков и молодых женщин, по-видимому, является предрасполагающим фоном для развития воспаления. Так, нами отмечено развитие воспалительных изменений шейки матки на фоне эктопии в 30% случаев. Вероятно, инфицирование уреаплазмами нарушает процесс замещения цилиндрического эпителия на многослойный плоский при эктопии шейки матки и способствует развитию различных патологических ее состояний.
Для воспалительных процессов уреаплазменной этиологии характерна длительная персистенция, часто — латентное бессимптомное развитие, в результате — поздняя диагностика, хроническое рецидивирующее течение. Клинические проявления могут быть более выражены в пред- и постменструальном периодах. У девочек течение уреаплазмоза бывает более выражено: в виде острых и подострых форм вульвовагинита с частым вовлечением в воспалительный процесс шейки матки и уретры.
Основными жалобами при уреаплазмозе являются: зуд, жжение в области наружных половых органов, белесоватые слизисто-гнойные выделения из влагалища, дизурические расстройства (дискомфорт при мочеиспускании, рези, боли или учащение мочеиспускания, ощущение переполненности мочевого пузыря). Для урогенитального уреаплазмоза вообще характерно частое поражение мочевыделительной системы, причем воспалительный процесс нередко начинается именно с уретральных симптомов и соответствующих жалоб, что требует особого внимания клиницистов [1, 2, 5].
Цервициты при уреаплазмозе не имеют каких-либо патогномоничных кольпоскопических особенностей. Кольпоскопическая картина характеризуется повышенным количеством секрета, гиперемией наружного покрова шейки матки и области входа в цервикальный канал, отечностью слизистой оболочки с неравномерным ее окрашиванием при пробе Шиллера, с характерной крапчатостью за счет чередования мелкоточечных йоднегативных и йодпозитивных участков.
Как правило, при уреаплазмозе цитограммы подтверждают преимущественно воспалительный характер изменений эпителия шейки матки. Согласно классификации по Папаниколау, в большинстве случаев цитограммы при уреаплазменной инфекции относятся к 2-му и 3-му классу. При этом важной особенностью цитологической характеристики шейки матки является преобладание в мазках, взятых с экзо- и эндоцервикса дистрофических изменений в клетках многослойного плоского и цилиндрического эпителия, высокая частота обнаружения клеток с псевдодискариозом, большое количество лимфоцитов, гистиоцитов.
Особое значение имеет и требует соответствующего внимания клиницистов высокая частота выявления аномальных кольпоскопических картин на фоне воспалительных изменений шейки матки, особенно при хронической уреаплазменной инфекции (табл. 1).
На основании приведенных данных можно предположить, что хроническое течение воспалительного процесса шейки матки при уреаплазмозе способствует избыточной пролиферации эпителиальных клеток и развитию полипов цервикального канала, а также, возможно, является одной из причин возникновения лейкоплакии шейки матки и фактором, усугубляющим клинику папилломавирусной инфекции.
При подозрении на наличие уреаплазмоза обследованию подлежат:
- женщины с воспалительными процессами гениталий и их половые партнеры;
- пациентки с хроническими, рецидивирующими воспалительными процессами органов системы мочевыделения;
- женщины с отягощенным акушерско-гинекологическим анамнезом;
- беременные женщины (в любом сроке беременности, по показаниям);
- пациентки с бесплодием.
Как известно, абсолютная патогенность генитальных уреа- и микоплазм (кроме Mycoplasma genitalium) не доказана до настоящего времени. Уреаплазмы скорее относят к условно-патогенным микроорганизмам, однако известно, что различные воспалительные заболевания урогенитального тракта уреаплазменной этиологии могут возникать (и в литературе описан целый ряд нозологий) в результате активации размножения уреаплазм при ослаблении или изменении иммунного и гормонального статуса, присоединении других инфекций, стрессах, изменении гомеостаза, переохлаждении и т. д. Тактика ведения больных зависит от данных комплексного обследования, которое, помимо общеклинических и гинекологического анализов, должно включать лабораторные методы исследования (бактериоскопия, полимеразная цепная реакция, культуральное исследование), при подозрении на наличие патологии шейки матки — расширенную кольпоскопию, цитологическое исследование мазков-отпечатков с экзо- и эндоцервикса и/или биопсию шейки матки с последующим гистологическим исследованием биоптатов.
По общепринятому мнению, уреаплазмы могут считаться этиологическим фактором развития воспалительного процесса при обнаружении их в большом количестве, т. е. при высоком уровне обсемененности. В связи с этим важное практическое значение имеет культуральный метод исследования. Культуральное исследование позволяет провести идентификацию возбудителя, определить его количество в исследуемом материале и оценить чувствительность выделенных штаммов возбудителя к антимикробным препаратам, следовательно, метод помогает сформировать дальнейшую тактику ведения пациента.
Критериями назначения этиотропной терапии при воспалительных заболеваниях уреаплазменной этиологии являются:
- клинические и лабораторные признаки воспалительного процесса органов мочеполовой системы;
- результаты комплексного микробиологического обследования с количественным обнаружением уреаплазм в титрах более 104 КОЕ/мл при культуральном исследовании;
- предстоящие оперативные или другие инвазивные процедуры на органах мочеполовой системы;
- бесплодие (когда исключены другие причины);
- отягощенный акушерско-гинекологический анамнез, осложненное течение беременности.
Основными принципами лечения являются следующие.
Терапия должна проводиться обоим половым партнерам во избежание реинфекции; на весь период лечения и до получения после лечения отрицательных контрольных результатов у обоих половых партнеров целесообразно рекомендовать применение барьерных методов контрацепции (презерватив).
Лечение патологии шейки матки в сочетании с уреаплазменной инфекцией или вследствие ее должно быть двухэтапным. Первый этап заключается в этиотропной терапии и включает в себя использование антибактериальных препаратов, ферментов, антимикотиков (для профилактики кандидоза). В частности, из комплексных ферментных препаратов целесообразно применение Вобэнзима за 5 дней до начала антибактериальной терапии и в течение всего курса антибиотиков по 3–5 драже за 30 мин до еды.
В таблице 2 приведены основные группы препаратов, применяемых для лечения уреаплазмоза, а именно тетрациклины, макролиды, фторхинолоны, аминогликозиды, азалиды. Как известно, уреаплазмы резистентны к антибактериальным препаратам (пенициллин и его производные, цефалоспорины и др.), подавляющим синтез клеточной стенки ввиду отсутствия таковой.
По мнению большинства авторов и как подтверждает собственный опыт, эффективность антибактериальной терапии существенно выше при ее назначении с учетом чувствительности выделенных штаммов уреаплазм к антибиотикам, т. е. при индивидуальном подходе в лечении пациенток.
Длительность лечения подбирается врачом индивидуально в зависимости от тяжести воспалительного процесса и длительности инфицирования.
Хотелось бы отметить, что в настоящее время максимальная чувствительность уреаплазм определена к приведенным выше антибактериальным препаратам: доксициклину (97,2%), джозамицину (96,7%), что подтверждено результатами исследований разных авторов в нашей стране и за рубежом.
Доксициклин является одним из препаратов, назначение которых предпочтительно при уреаплазмозе (Федеральное руководство для врачей по использованию лекарственных средств, 1998). Доксициклин используется в виде двух солей. В капсулированных формах применяется доксициклина гидрохлорид. Рядом исследователей отмечено выраженное воздействие доксициклина гидрохлорида на слизистую желудочно-кишечного тракта, в частности возникновение в более чем 40% случаев повреждения тканей с последующим развитием язв пищевода [4, 6, 9]. В последнее время предложена новая форма известного препарата — моногидрат доксициклина (Юнидокс Солютаб). Доксициклина моногидрат имеет целый ряд преимуществ. Во-первых, данная форма препарата отличается более высокой биодоступностью, сравнимой с внутривенным введением. Во-вторых, запатентованная лекарственная форма Солютаб позволяет пациенту выбрать предпочтительный для себя режим приема препарата, таблетку можно проглотить целиком, разжевать или растворить — в любом случае гарантировано равномерное высвобождение микрочастиц лекарственного вещества.
В-третьих, это важно подчеркнуть, для данной формы доксициклина характерен минимальный риск возникновения нежелательных влияний на слизистую оболочку желудочно-кишечного тракта по сравнению с другими лекарственными формами препарата.
Джозамицин (Вильпрафен) является среди антибактериальных препаратов группы макролидов препаратом выбора в силу ряда причин. Прежде всего это обусловлено, по данным ряда авторов за последние годы, чувствительностью уреаплазм к антибиотикам. Для джозамицина характерна высокая активность по отношению к внутриклеточным микроорганизмам, таким как уреаплазмы, микоплазмы, хламидии, легионеллы, чем объясняется его высокая клиническая эффективность при урогенитальных моно- и микст-инфекциях (особенно при сочетании с хламидиями). Подобно другим препаратам группы макролидов, джозамицин оказывает бактериостатическое действие, а в больших дозах становится бактерицидным. В отличие от других макролидов, в последние годы не наблюдался рост устойчивости уреаплазм к джозамицину. В России и за рубежом джозамицин в течение многих лет применяется во время беременности, при этом не было отмечено каких-либо неблагоприятных последствий для плода. Препарат разрешен к применению во II и III триместрах беременности. Применение джозамицина для лечения урогенитальных инфекций рекомендовано в информационном письме Российского общества акушеров-гинекологов (В. Н. Серов, 2005). Для данного препарата характерна редкость развития побочных эффектов, хорошая переносимость пациентами с патологией желудочно-кишечного тракта, что имеет существенное значение при назначении лечения больным с сопутствующими заболеваниями данной локализации.
При хроническом рецидивирующем течении воспалительного процесса уреаплазменной этиологии, неудачных предшествующих курсах антибактериальной терапии, при хронических воспалительных процессах смешанной этиологии в результате снижения общего и местного иммунитета, иммунологической реактивности происходит нарушение репаративной регенерации тканей. В таких ситуациях применение препаратов, модулирующих реакции общего и местного иммунитета у больных с хроническим воспалением слизистых оболочек, позволяет добиться возможности корригирующего влияния на регенераторный процесс. Назначение иммуномодулирующих препаратов целесообразно осуществлять с учетом данных интерферонового статуса с подбором по чувствительности интерферонпродуцирующих клеток пациента к иммуномодулирующим препаратам. В настоящее время на отечественном фармацевтическом рынке представлен широкий спектр иммуномодулирующих препаратов: Иммуномакс, Циклоферон, Ликопид, Неовир, Галавит, Панавир, Имунофан, Ридостин, Гепон и др. Местно применяются иммуномодулирующие препараты в виде суппозиториев (Кипферон, Виферон, Генферон, Галавит), дозы и схемы применения которых подбираются врачом индивидуально.
При уреаплазмозе во время беременности в I триместре при наличии показаний возможно применение терапии иммуноглобулинами для внутривенного введения, хороший терапевтический эффект дает использование озонотерапии. Во II и III триместрах из антибактериальных препаратов применяются джозамицин (Вильпрафен), эритромицин, спирамицин (Ровамицин) по стандартным схемам.
После завершения рекомендованного курса лечения контроль излеченности проводится обоим половым партнерам через 14–21 день после окончания терапии, далее — в течение трех менструальных циклов через 2–3 дня после менструации. При этом критериями излеченности уреаплазменной инфекции являются отрицательный результат бактериологического исследования на уреаплазмы и отсутствие клинических проявлений воспалительного процесса. В случае выявления после лечения уреаплазм в количестве менее чем 10 4 КОЕ/мл (носительство уреаплазм) и отсутствия клинических симптомов дальнейшее лечение не требуется.
Второй этап лечения патологии шейки матки в сочетании с уреаплазменной инфекцией или вследствие ее предусматривает локальное воздействие на шейку матки и определяется характером патологического процесса (раздельное диагностическое выскабливание — при полипах цервикального канала, лазерокоагуляция шейки матки, криодеструкция, радиоволновая хирургия — по показаниям с учетом данных гистологического исследования биоптатов).
Дальнейшее наблюдение пациенток после комплексного лечения осуществляется в соответствии с определенной международными критериями тактикой ведения больных с патологией шейки матки: в течение 1 года после применения деструктивных методов лечения — контрольное обследование состояния шейки матки (расширенная кольпоскопия, цитологическое исследование) 1 раз в 6 мес; в последующем — профилактический осмотр 1 раз в год (расширенная кольпоскопия, тест Папаниколау).
Литература
В. Н. Прилепская, доктор медицинских наук, профессор
О. В. Быковская, кандидат медицинских наук
НЦАГиП Росмедтехнологии, Москва
Что такое цервицит? Причины возникновения, диагностику и методы лечения разберем в статье доктора Батаршиной О. И., гинеколога со стажем в 18 лет.
Над статьей доктора Батаршиной О. И. работали литературный редактор Маргарита Тихонова , научный редактор Сергей Федосов и шеф-редактор Лада Родчанина

Определение болезни. Причины заболевания
Цервицит — это воспалительное заболевание шейки матки, которое развивается под влиянием различных агентов (как инфекционных, так и неинфекционных) [2] .
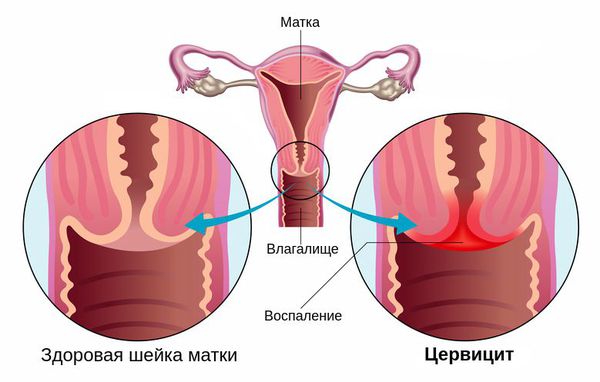
Распространённость цервицита у женщин достигает 10-45 %. Наиболее часто его вызывают возбудители, передаваемые половым путём, такие как гонокок, хламидия, трихомонада, вирус герпеса, бледная трепонема и др. [7] [8] [11] . Также причиной возникновения цервицита являются различные заболевания, аллергические реакции на противозачаточные спермициды, латекс в составе презервативов или продукты женской гигиены, такие как мыла, гели для душа или дезодоранты.
Длительный и вялотекущий дисбиоз влагалища (бактериальный вагиноз) также рассматривается как одна из возможных причин цервицита, поскольку на фоне изменения уровня кислотности влагалища меняется и соотношение видов влагалищной микрофлоры.
В зоне риска по возникновению цервицита находятся женщины, которые:
Также доказано, что фоном для развития воспаления шейки матки и его хронизации является местный иммунодефицит, связанный с нарушением защитной функции слизистой оболочки.
При обнаружении схожих симптомов проконсультируйтесь у врача. Не занимайтесь самолечением - это опасно для вашего здоровья!
Симптомы цервицита
Возможно как симптомное, так и бессимптомное течение заболевания [31] .
При бессимптомном процессе диагноз "цервицит" может быть поставлен:
- при неудовлетворительных результатах мазков — повышенном уровне лейкоцитов (клеток крови, отвечающих за иммунный ответ на внедрение инфекционных агентов);
- на основан ии визуального осмотра шейки матки врачом-гинекологом — покраснения и отёка шейки матки.
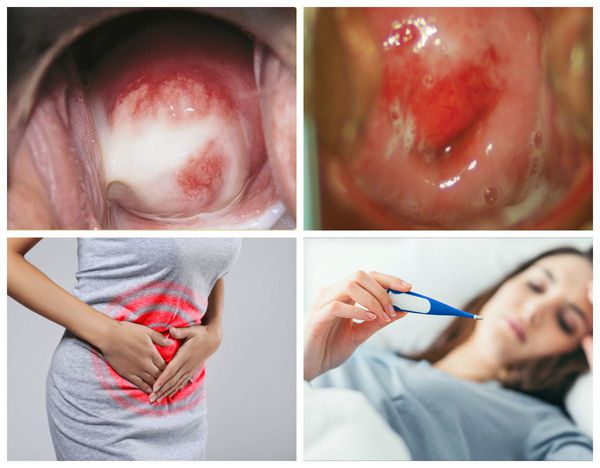
При симптомном течении заболевания женщину могут беспокоить:
- сероватые или бледно-жёлтые выделения из влагалища;
- аномальные кровянистые выделения во время или после полового контакта, а также в перерывах между менструациями [31] ;
- боль во время секса;
- затруднённое, болезненное или частое мочеиспускание;
- тазовая боль или, в редких случаях, лихорадка.
Патогенез цервицита
Когда речь идет о патогенезе цервицита, прежде всего необходимо обозначить понятия, о которых пойдёт речь.
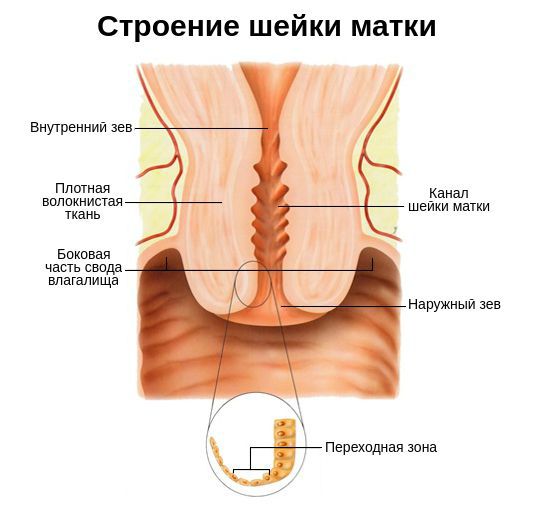
Шейка матки представляет собой гладкомышечный орган длиной 2-3 см, образованный соединительной тканью. Основная функция данной части матки — барьерная. Она реализуется за счёт секрета (выделений) слизистой , которая препятствует попаданию патогенных возбудителей в матку, маточные трубы и малый таз. В состав секрета входят как иммуноглобулины всех классов ( IgG, IgM, IgA и др. ), так и вещества, обладающие высокой расщепляющей и бактерицидной активностью.
Также шейку матки защищает микрофлора влагалища . Она состоит из анаэробных и аэробных бактерий, причём первых в десять раз больше, чем вторых. Такое соотношение создаёт определённый уровень кислотности слизистой, который не позволяет патогенным микроорганизмам внедряться в полость матки [8] .
Циклическое воздействие половых гормонов на женский организм позволяет сохранять микрофлору влагалища в норме, тем самым защищать шейку матки:
- в первой фазе менструального цикла под воздействием эстрогенов синтезируется гликоген, стимулируется выработка слизистого секрета, выполняющего барьерную функцию [4][17][27] ;
- во второй фазе цикла под воздействием прогестерона происходит подкисление среды влагалища и размножение лактобактерий.
При снижении барьерных свойств микрофлоры влагалища и слизистой шейки матки в организм женщины проникают различные патогенные возбудители, которые приводят к развитию цервицита. Их активному проникновению и распространению в полости малого таза способствуют сперматозоиды в качестве клеток-переносчиков инфекционных агентов, а также трихомонады и установка внутриматочной спирали на фоне воспалительного процесса.
Острый цервицит
Чаще возникает при поражении шейки матки специфическими возбудителями (например, гонококком), а также после искусственного прерывания беременности, в осложнённом послеродовом периоде (возбудителями чаще становятся стафилококковая и стрептококковая инфекции) и при вирусном поражении шейки матки. На ранней стадии заболевания возникают:
- полнокровие сосудов;
- повышение уровня лейкоцитов (лейкоцитарная инфильтрация);
- просачивание крови сквозь стенки сосудов в зону воспаления (экссудация);
- дистрофические изменения с вакуолизацией цитоплазмы и ядер клеток.
В результате дистрофических изменений клеток на поверхности слизистой оболочки шейки матки появляется гнойный и серозно-гнойный экссудат — сероватые или бледно-жёлтые выделения.
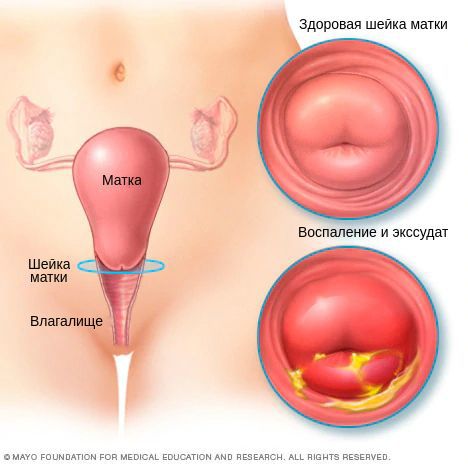
Хронический цервицит
При проникновении возбудителей в межклеточное пространство крипт шейки матки (небольших трубчатых углублений), труднодоступных для лечения, возникает хронический цервицит. Причиной хронизации заболевания нередко является поражение шейки матки хламидийной инфекцией. В 24-40 % случаев хронический цервицит возникает на фоне длительного и вялотекущего бактериального вагиноза. При осмотре гинекологом шейка матки выглядит покрасневшей, отёчной, легко травмируется. Микроскопически наблюдается инфильтрация подэпителиальной ткани лимфоцитами, плазмоцитами, полнокровие сосудов. Наряду с дистрофическими процессами в ткани преобладают процессы непрямого деления клеток, разрастания ткани и замещения одного вида клеток другим. Часто при хроническом цервиците нарушаются процессы ороговения клеток, что проявляется уплотнением тканей и изменением процесса гликогенизации клеток [6] [11] .
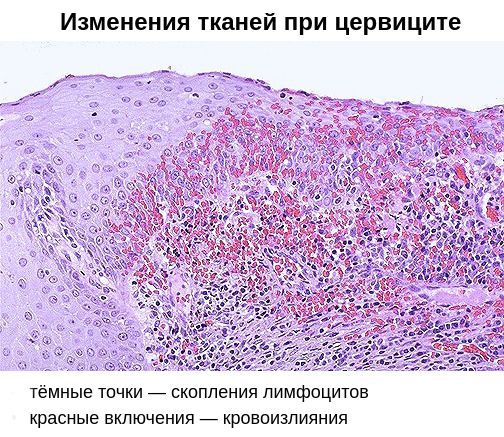
Помимо специфического возбудителя, немалую роль в возникновении хронического цервицита играет вторичный иммунодефицит. Он заключается в неполноценности клеточного и гуморального иммунитета. На клеточном уровне снижается количество Т- и В-лимфоцитов, а также нарушается фагоцитарная активности клеток, позволяющая им поглощать и переваривать патогенные микроорганизмы. В результате возбудители остаются в организме, снижается содержание антител IgG и IgM, увеличивается выработка антител IgA, что ведёт к изменению качества цервикальной слизи.
Послеродовой цервицит
Отдельно такую форму не выделяют, цервицит после родов ничем не отличается от обычного. Разница может быть лишь в лечении: не все антибиотики можно принимать при грудном вскармливании.
Классификация и стадии развития цервицита
Классификация цервицита зависит от типа возбудителей, локализации и давности патологических процессов. Так, в зависимости от типа возбудителя цервициты подразделяют на инфекционные и неинфекционные. Инфекционные цервициты бывают:
- гонококковыми;
- хламидийными;
- трихомонадными;
- кандидозными;
- вирусными.
Неинфекционные цервициты рассматриваются и классифицируется в зависимости от причины, вызвавшей воспаление. Они бывают аллергическими, атрофическими (сенильными) и др. [8] .
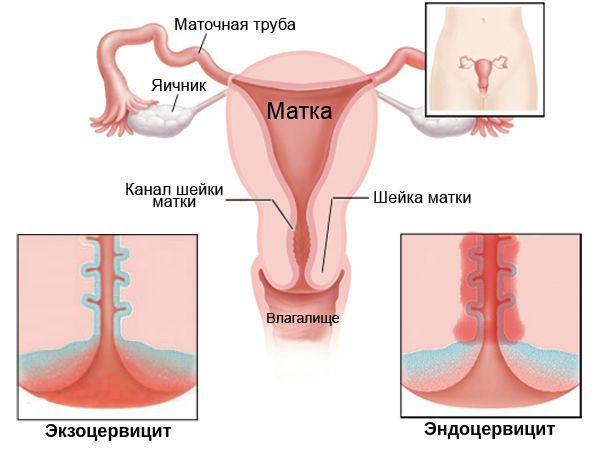
Кроме того, по локализации цервицит подразделяют на:
- экзоцервицит — протекает преимущественно на поверхности шейки матки;
- эндоцервицит — в основном затрагивает эпителий канала шейки матки (цервикальный канал).
По длительности протекания процесса цервицит может быть:
- острым — процесс воспаления длится не более шести недель;
- хроническим — болезнь протекает с периодическими ремиссиями и обострениями.
Осложнения цервицита
Выявление причины цервицита имеет важное значение, поскольку при наличии инфекционного агента возбудитель способен распространяться за пределы шейк и матки и вызывать эндометрит , а также воспаление в теле матки, маточных трубах и малом тазе. В ряде случаев это приводит к бесплодию или препятствует вынашиванию плода [25] [27] .
Цервицит и беременность
Если беременность возникла на фоне цервицита, возбудитель заболевания может привести к преждевременному прерыванию беременности в связи с проникновением инфекции в водную оболочку, обращённую к плоду, затем в хорион (плаценту), околоплодные воды и сам плод.
При инфицировании ребёнка на ранних сроках беременности могут сформироваться врождённые пороки развития, возникает риск первичной плацентарной недостаточности и внутриутробной гибели плода. При позднем инфицировании наблюдаются следующие осложнения беременности:
- внутриутробная задержка развития плода;
- вторичная плацентарная недостаточность (часто на фоне плацентита — воспаления плаценты);
- локальные и генерализованные (распространённые) инфекционные поражения плода.
Генерализованные формы внутриутробной инфекции чаще развиваются в первом триместре беременности, так как плод ещё не может препятствовать распространению воспалительного процесса. В третьем триместре воспалительные изменения вызывают сужение или обтурацию (закрытие просвета) каналов и отверстий, что ведёт к аномальному развитию уже сформировавшегося органа — псевдоуродствам ( гидроцефалии , гидронефрозу и др.) [29] .
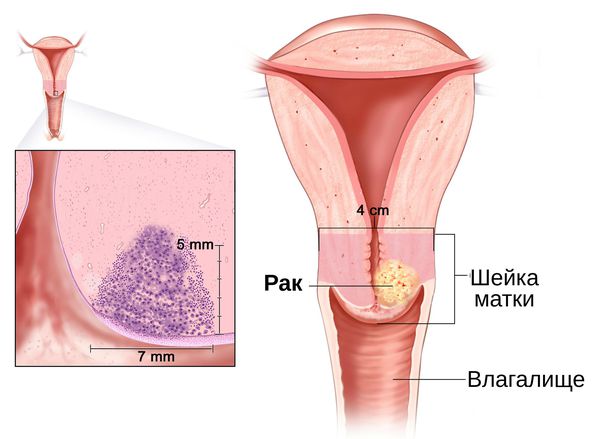
Длительное воспаление шейки матки становится фоном для развития злокачественных процессов . Это связано с нарушением регенерации слизистой оболочки шейки матки, которое наблюдается при хроническом цервиците. Наиболее значимыми факторами, влияющими на регенерацию, являются вирусы и хламидии [10] . Учёные доказали, что формирование рака шейки матки происходит только на фоне сохранившейся в криптах вирусной инфекции, которая активируется более чем через год после первичного обнаружения возбудителя [30] .
Диагностика цервицита
Диагностическими критериями цервицита при осмотре в зеркалах являются:
- покраснение слизистой, отёк;
- обильные выделения грязно-серого или зеленоватого цвета;
- творожистое отделяемое (при грибковом поражении шейки матки и влагалища).
При микроскопическом исследовании наблюдается увеличение количества лейкоцитов, также можно обнаружить возбудителей трихомониаза и гонореи.
Однозначными признаками цервицита при вульвоцервикоскопии служат:
- фолликулярный кольпит, "лунный ландшафт" — для хламидиоза;
- очаговый кольпит — для трихомониаза;
- диффузный кольпит — для неспецифической бактериальной инфекции;
- симптом "манной крупы" — для герпетической инфекции [17] .
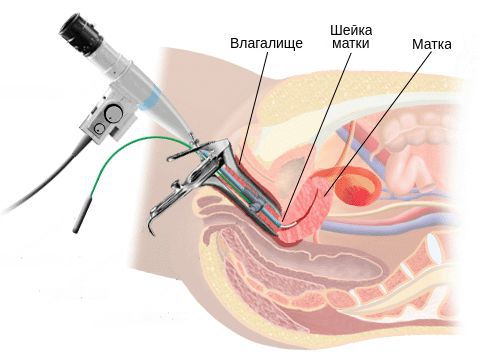
Бактериологическое исследование с поверхности шейки матки и заднего свода влагалища позволяет оценить не только соотношение лактофлоры, создающей нормальную кислотность влагалища, но и выявить рост условно-патогенных возбудител ей, таких как кишечные палочки, стрептококки, стафилококки, анаэробные кокки и др. Причём клинически значимым является рост микроорганизмов в колич естве более чем 10 4 КОЕ/мл.
ПЦР-диагностика позволяет обнаружить специфических возбудителей, вызвавших воспалительный процесс, таких как микоплаз мы, уреаплазмы, гарднереллы, хламидии, вирус герпеса и др. [31] . Для этого исследования врач-гинеколог должен взять мазок из шейки матки.
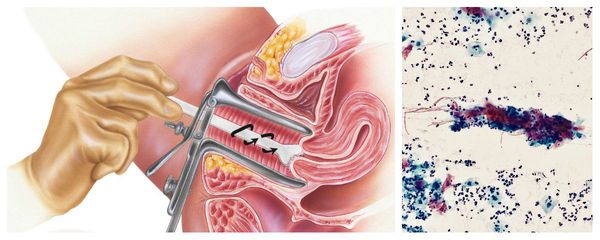
Цитологическое исследование клеточного материала позволяет оценить структуру клеток, характер и уровень их повреждения, а также эффективность лечения в динамике. При длительно текущем воспалении шейки матки в цитограмме преобладают гистиоциты, плазмациты, фибробласты и лимфоидные элементы. При продуктивном воспалении (защитной реакции организма) преобладают клеточные инфильтраты — макрофагальные, г игантоклеточные, плазмоклеточные, лимфоцитарно-моноцитарные. В 40 % случаев цитологическая диагностика позволяет выявить возбудителя заболевания (хламидии, кандиды, трихомонады, цитомегаловирус), более чем в 50 % случаев диагностируется папилломавирус и вирус простого герпеса.
При ультразвуковом исследовании признаками эндоцервицита являются увеличение толщины М-эхо шейки матки более 4 мм и реактивный отёк подэпителиальных о тделов УЗИ. рекомендуется выполнять на 5-7 день менструального цикла.
Следует помнить, что обследование гинекологом и взятие мазков проводятся перед началом менструации или через несколько дней после её окончания: оптимальный срок — пятый день, когда нет мажущих кровянистых выделений. Накануне и в день процедуры не следует использовать вагинальные свечи, тампоны, мази, средства интимной гигиены, поскольку это может стать причиной получения недостоверных данных. Кроме того, необходимо отказаться от спринцевания и воздержаться от половых контактов в течение одного-двух дней до сдачи анализа.
Лечение цервицита
Препараты для лечения цервицита
Определяющим звеном при выборе тактики лечения является природа возбудителя цервицита: вирусные воспаления шейки матки предполагают использование противовирусных препаратов, бактериальные воспаления — приём антибактериальных средств. При этом важно учитывать чувствительность выявленных инфекционных агентов к антибиотикам [1] [2] [3] .
Главной проблемой лечения цервицита шейки матки являются наличие нескольких возбудителей (микст-инфекции) и устойчивость возбудителей к антибактериальным препаратам. В таких случаях необходимо прибегнуть к приёму комбинации антибиотиков. Конкретные препараты назначает врач.
Иногда антибиотикотерапия сопровождается назначением фитопрепаратов, биологически активных добавок. Также рекомендуются общеукрепляющие физические нагрузки, нормализация режима труда и отдыха [9] [24] .
Помимо лечения пациентки параллельно в обязательном порядке проводится лечение её полового партнёра. Во время терапии необходимо пользоваться барьерной контрацепцией.
Нормали зация микробиоценоза влагалища с помощью пробиотиков [15] в сочетании с иммунокоррекцией (с учётом данных иммунограммы) [5] [16] [19] также целесообразны, поскольку изменённый уровень кислотности среды и возникающий дефицит иммунных факторов способствуют частым рецидивам воспалительного процесса [40] [43] [44] .
Физиотерапия
Кроме того, в ряде случаев назначается физиолечение:
- ДМВ-терапия — лечение дециметровыми волнами частотой от 300 МГц до 3 ГГц, проводится каждый день, предполагает 10-15 процедур продолжительностью 10 минут;
- магнитотерапия — воздействие магнитного поля низкой или высокой частоты, проводится каждый день, предполагает 10-20 процедур продолжительностью 10-20 минут;
- диадинамотерапия — лечение высокочастотным электрическим током, проводится каждый день до появления ощущения болезненной вибрации, предполагает 12-15 процедур;
- СМТ-терапия — лечение низкочастотным электрическим током, проводится каждый день, предполагает 12-15 процедур;
- электрофорез с солями магния — воздействует на область малого таза, проводится каждый день, предполагает 10-15 процедур продолжительностью 20 минут;
- дарсонвализация и лазеротерапия с использованием влагалищных датчиков — проводятся каждый день, предполагает 10-12 процедур [32] .
Деструктивные методы лечения цервицита
Цервицит — это воспалительный процесс, поэтому его лечат медикаментозно. Физические или химические методы применяются при атипии в клетках, покрывающих шейку матки или выстилающих цервикальный канал. Прижигание кислотами, жидким азотом, лазерная вапоризация, аргоноплазменная абляция, электрохирургическая эксцизия для лечения цервицита не используются .
Прогноз. Профилактика
Прогноз заболевания при своевременно начатом лечении благоприятный. При бессимптомном цервиците и отсутствии инфекций, передаваемых половым путём, у пациенток остаётся риск появления выраженных клинических признаков заболевания [30] .
Помимо основного лечения назначаются консультации других специалистов для коррекции различных нарушений (нейроэндокринных, гормональных, иммунных), выявления соматических заболеваний и факторов риска. Это позволит предотвратить повторное развитие цервицита [28] .
С целью профилактики воспаления шейки матки рекомендуется:
- один раз в шесть месяцев посещать гинеколога;
- использовать барьерные средства контрацепции;
- не допускать хронизации заболеваний мочеполовой системы.
Что такое дисплазия шейки матки? Причины возникновения, диагностику и методы лечения разберем в статье доктора Игнатенко Татьяны Алексеевны, гинеколога со стажем в 14 лет.
Над статьей доктора Игнатенко Татьяны Алексеевны работали литературный редактор Елена Бережная , научный редактор Сергей Федосов

Определение болезни. Причины заболевания
Дисплазия шейки матки, или цервикальная интраэпителиальная неоплазия (ЦИН), или Cervical Intraepithelial neoplasia (CIN) — это патологический процесс, при котором в толще клеток, покрывающих шейку матки, появляются клетки с различной степенью атипии (неправильного строения, размера, формы).
Причины дисплазии шейки матки
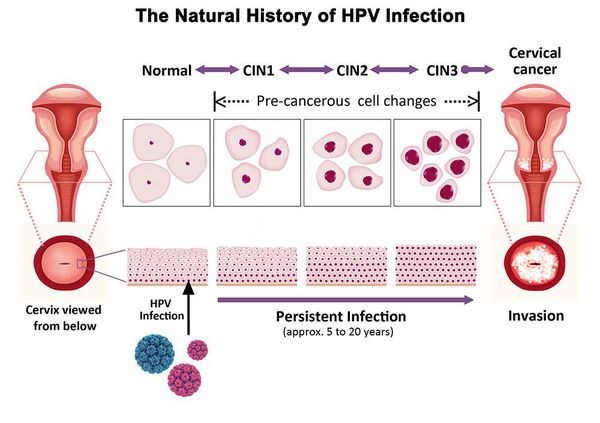
Папилломавирусная инфекция (ВПЧ) — основная причина дисплазии и рака шейки матки. К болезни приводит длительное персистирование именно ВПЧ высокого канцерогенного риска. У женщин с риском развития цервикальной неоплазии распространенность онкогенных типов ВПЧ чрезвычайно велика. ВПЧ становится причиной CIN 2-3 и рака шейки матки в 91,8% и 94,5% случаев соответственно. [1]
К факторам риска дисплазии шейки матки относится длительный приём контрацептивов и курение. Выявлена связь между пассивным курением среди некурящих и повышенным риском возникновения CIN 1. [3]
Другие факторы риска — раннее начало половой жизни, большое число и частая смена половых партнеров, употребление алкоголя, сопутствующие половые инфекции, много беременностей и родов. Риск цервикальной CIN 2 особенно высок у женщин, которые до этого имели опыт пересадки органов, у них выявлена ВИЧ-инфекция или они принимают иммунодепрессанты. [2]
При обнаружении схожих симптомов проконсультируйтесь у врача. Не занимайтесь самолечением - это опасно для вашего здоровья!
Симптомы дисплазии шейки матки
Дисплазия шейки матки, как правило, имеет бессимптомное течение, поэтому пациентки не предъявляют никаких специфических жалоб.
Патогенез дисплазии шейки матки
Критический фактор развития цервикальной интраэпителиальной неоплазии — инфицирование вирусом папилломы человека. Во многих случаях цервикальная интраэпителиальная неоплазия легкой степени отражает временную реакцию организма на папиломавирусную инфекцию и без лечения исчезает в течение полугода-года наблюдения. При цервикальной интраэпителиальной неоплазии умеренной и тяжелой степени высока вероятность встраивания вируса папилломы человека в клеточный геном. Инфицированные клетки начинают продуцировать вирусные белки E6 и Е7, которые продлевают жизнь клетки, сохраняя ее способность к неограниченному делению. Неизбежно формирующиеся на этом фоне мутации клеток ведут к формированию предрака (дисплазии) и рака шейки матки, влагалища и вульвы.
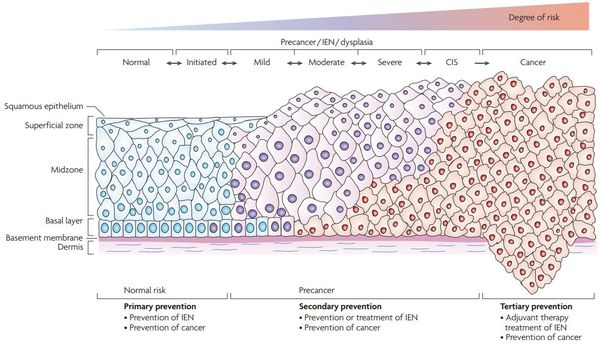
Онкогенные белки ВПЧ (Е6, Е7) взаимодействуют с регуляторными белками клеток шейки матки, приводя к повышению активности онкомаркера p16INK4A, что свидетельствует о неконтролируемом размножении клеток шейки матки. Таким образом, сверхэкспрессия p16INK4A, определяемая в материале шейки матки, который получают при биопсии, является биомаркером интеграции вируса папилломы человека высокого риска в геном и трансформации эпителиальных клеток под действием вируса, что делает эту информацию полезной при оценке прогноза развития предраковых и злокачественных поражений, связанных с инфицированием генитального тракта вирусом папилломы человека. [5]
Классификация и стадии развития дисплазии шейки матки
Для постановки цитологического диагноза (по результатам цитологического исследования соскобов шейки матки и цервикального канала с окрашиванием по Папаниколау (Рар-тест) или жидкостной цитологии) используется классификация Бетесда (The Bethesda System, 2014), основанная на термине SIL (Squamous Intraepithelial Lesion) – плоскоклеточное интраэпителиальное поражение. [10]
Выделяют три вида результатов соскобов с поверхности шейки матки (экзоцервикса):
Классификация Папаниколау
- 1-й класс — нормальная цитологическая картина (отрицательный результат);
- 2-й класс — изменение морфологии клеток, которое обусловлено воспалением во влагалище и (или) шейке матки;
- 3-й класс — единичные клетки с аномалией ядер и цитоплазмы (подозрение на злокачественное новообразование);
- 4-й класс — отдельные клетки с явными признаками озлокачествления;
- 5-й класс — много типично раковых клеток (злокачественное новообразование).
Существуют также гистологические классификации для оценки материала, полученного при биопсии.
По классификации R. M. Richart (1968) в зависимости от глубины поражения поверхностного клеточного слоя выделяют три степени дисплазии шейки матки:
- ЦИН 1 (дисплазия слабой степени) — признаки папилломавирусной инфекции (койлоцитоз и дискератоз). Поражение до 1/3 толщины клеточного пласта;
- ЦИН 2 (дисплазия средней степени) — поражена 1/2 толщины клеточного слоя;
- ЦИН 3 (дисплазия тяжелой степени) — поражение более 2/3 клеточного слоя. [8]
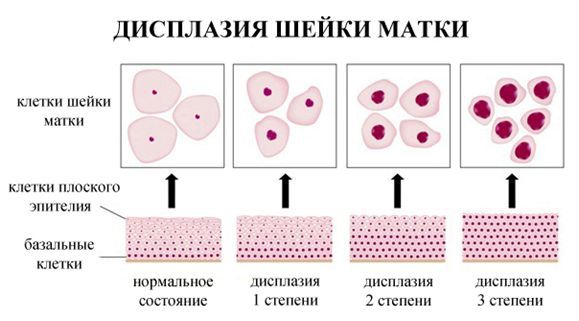
В приведенной ниже таблице даны соотношения классификаций предраковых поражений шейки матки. [9]
| Система Папаниколау | Описательная система ВОЗ | CIN | Терминологи- ческая система Бетесда (ТСБ) |
|---|---|---|---|
| Класс 1 (норма) | Отсутствие злокачественных клеток | Отсутствие неопластических изменений | Норма |
| Класс 2 (метаплазия эпителия, воспалительный тип) | Атипия, связанная с воспалением | Реактивные изменения клеток ASC: ASC - US, ASC - H | |
| Класс 3 ("дискариоз") | Слабая дисплазия | CIN 1 койлоцитоз | LSIL |
| Умеренная дисплазия | CIN 2 | HSIL | |
| Тяжелая дисплазия | CIN 3 | ||
| Класс 4 (клетки, подозрительные на рак или карцинома in situ | Карцинома in situ | ||
| Класс 5 (рак) | Инвазивная карцинома | Карцинома | Карцинома |
Осложнения дисплазии шейки матки
Последствия дисплазии шейки матки
Основное и самое опасное осложнение цервикальной интраэпителиальной неоплазии заключается в развитии рака шейки матки, любой случай развития которого — результат упущенных возможностей диагностики и лечения дисплазии шейки матки. [7]
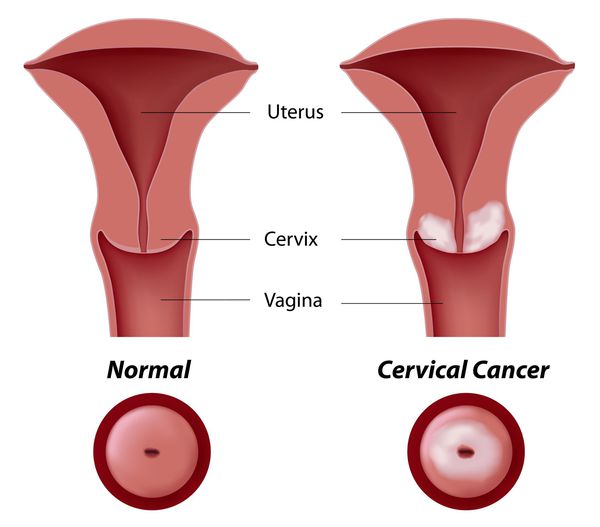
Проводились длительные, систематические исследования риска рака шейки матки у женщин с диагнозом цервикальной интраэпителиальной неоплазии 3 степени (CIN3) по сравнению с женщинами, у которых были нормальные цитологические результаты. Согласно полученным данным, долгосрочный относительный риск развития рака шейки матки зависит от различных гистологических типов CIN3 и выше всего он для аденокарциномы in situ. Даже через 25 и более лет после конизации (хирургического иссечения патологических тканей шейки матки) риск злокачественного перерождения клеток был значительным. [4]
Диагностика дисплазии шейки матки
Для ранней диагностики предраковых поражений шейки матки во многих странах мира существует система цервикального скрининга.
Методы диагностики дисплазии шейки матки
В России система цервикального скрининга включает последовательность действий:
- Цитологическое исследование: РАР-тест;
- ВПЧ-тестирование: в США и странах Евросоюза ВПЧ-тест применяется для первичного скрининга рака шейки матки (РШМ). В России его использование вариативно: при первичном скрининге в сочетании с РАР-тестом, в качестве самостоятельного теста, при ведении пациенток с неясными результатами РАР-теста (ASCUS) и для наблюдения паценток после лечения HSIL;
- Кольпоскопия: показаниями к исследованию являются положительные результаты РАР-теста (класс 2-5). Метод основан на осмотре шейки матки при помощи увеличивающих оптических систем и проведения диагностических проб с растворами уксусной кислоты и йода (Люголя). С помощью кольпоскопии определяют локализацию поражения, его размер, выбирают участок для проведения биопсии, определяют тактику лечения.
При кольпоскопии должна быть тщательно оценена зона трансформации (переходная зона стыка двух видов покровного эпителия шейки матки).
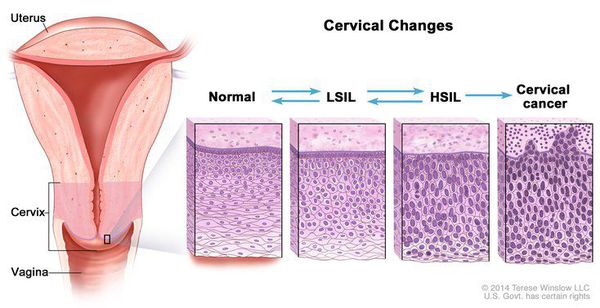
Влагалищная часть шейки матки (экзоцервикс) покрыта многослойным плоским эпителием. В канале шейки матки (цервикальном канале, эндоцервиксе) — цилиндрический эпителий. Место перехода цилиндрического эпителия цервикального канала в многослойный плоский эпителий поверхности шейки матки носит название зоны трансформации. Эта область имеет большое клиническое значение, поскольку именно в ней возникает более 80% случаев дисплазии и рака шейки матки.
Лечение дисплазии шейки матки
Динамическому наблюдению подлежат молодые пациентки (до 35 лет) с LSIL (ВПЧ, ЦИН 1, ЦИН 2, если при биопсии не обнаружен белок р16, являющийся признаком проникновения ВПЧ высокого риска в геном и трансформации опухолевых клеток под действием вируса). Наблюдать возможно пациенток только с 1 и 2 кольпоскопическим типом зоны трансформации.
Контрольные осмотры, цитологическое и ВПЧ-тестирование показаны через 6 и 12 месяцев после первичного обнаружения патологии.
Хирургическое лечение дисплазии
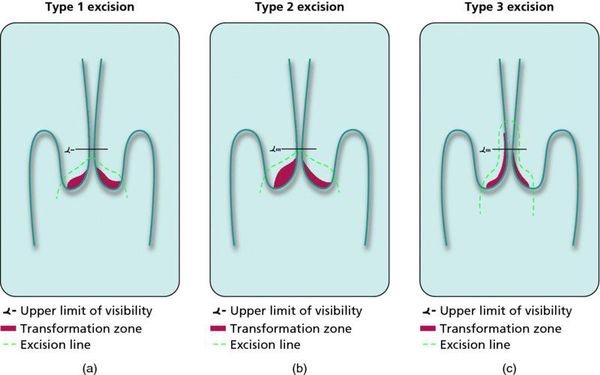
Немаловажно, что при выявлении по кольпоскопии 3 типа зоны трансформации на фоне положительного РАР-теста гинеколог обязан провести выскабливание слизистой канала шейки матки и/или широкую эксцизионную биопсию (конизацию шейки матки) для исключения опухолевого процесса, потенциально располагающегося вне зоны кольпоскопического обзора. Немаловажно наблюдение после операции через 6 и 12 месяцев с выполнением цитологического соскоба и ВПЧ-теста.
Следует отметить, что процедура хирургического иссечения патологических тканей на шейке матки увеличивает риск преждевременных родов. А сама по себе цервикальная интраэпителиальная неоплазия первой степени на течении беременности и родов никак не отражается и зачастую опасности не представляет. [12]
Средний возраст женщин, когда может потребоваться хирургическая коррекция цервикальной внутриэпителиальной неоплазии — около 30 лет. Хирургическое лечение нередко ассоциировано с неблагоприятным течением последующей беременности. Частота и тяжесть неблагоприятных осложнений возрастают с увеличением глубины иссекаемых тканей. [13]
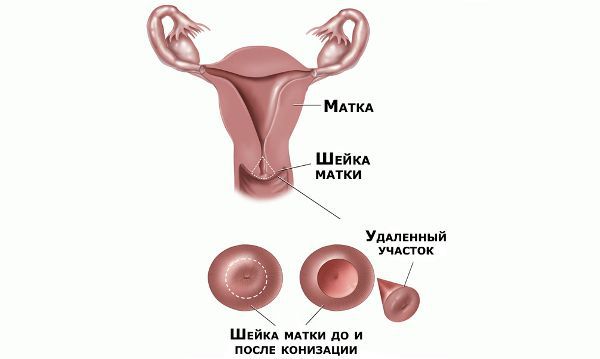
Реабилитация после хирургического лечения
В течение месяца после операции следует воздержаться от спринцеваний, половых контактов и не пользоваться тампонами. На 2–3 недели исключают тяжёлые физические нагрузки и тепловые процедуры. Незначительные сукровичные выделения, усиливающиеся иногда до менструальноподобных, в течение 10–20 дней после операции — это нормальное явление.
При реабилитации после хирургического лечения шейки матки эффективны препараты, содержащие антисептик и стимулятор регенерации эпителия.
После лечения возможен рецидив, поэтому необходимо пожизненное наблюдение: цитологический мазок через 6 и 12 месяцев после операции, затем раз в год в течение 10 лет, далее раз в 3 года.
Планировать беременность после операции на шейке матки можно не ранее, чем через 3–6 месяцев. Эти сроки будут зависеть от глубины эксцизии или конизации и длины шейки матки [9] .
Лечение дисплазии при беременности
В большинстве случаев лечение должно быть отложено на послеродовый период. При беременности на фоне дисплазии шейки матки каждые три месяца проводится кольпоскопический и цитологический контроль. При выявлении рака шейки матки пациентку консультирует онкогинеколог. Доктор подбирает тактику лечения, может потребоваться прервать беременность по онкологическим показаниям [9] .
Прогноз. Профилактика
Дополнительными факторами риска прогрессирования ПВИ с формированием предраковой патологии являются:
- курение;
- длительное использование гормональных контрацептивов;
- многократные травматичные роды;
- ВИЧ-инфекция.
- У пациенток с ЦИН часто обнаруживают вирус простого герпеса 2 типа, цитомегаловирусную инфекцию, хламидийную урогенитальную инфекцию, бактериальный вагиноз, ассоциированный с резким снижением или отсутствием вагинальной лактофлоры, повышенным ростом во влагалище Gardnerella vaginalis и Atopobium vaginae, повышение концентрации в бакпосеве грибов рода Candida, Mycoplasma hominis.
Устранение и профилактика данных факторов способны снизить вероятность развития предраковой патологии шейки матки.
Рак шейки матки поражает преимущественно женщин репродуктивного возраста. Скрининг является важной стратегией вторичной профилактики. Длительный процесс канцерогенной трансформации от появления в организме вируса папилломы человека (ВПЧ) до инвазивного рака дает широкие возможности для выявления заболевания на стадии, когда лечение высокоэффективно. Подходящими скрининговыми тестами в мире признаны цитологическое исследование, визуальный осмотр после применения уксусной кислоты и тесты на выявление ВПЧ. Всемирная организация здравоохранения рекомендует проводить скрининг женщин по крайней мере один раз в жизни в возрасте от 30 до 49 лет. [14]
Согласно приказу Министерства здравоохранения РФ от 03.02.2015. N36ан "Об утверждении порядка проведения диспансеризации определенных групп взрослого населения", осмотр со взятием мазка (соскоба) с поверхности шейки матки и цервикального канала на цитологическое исследование производится 1 раза в 3 года для женщин в возрасте от 21 года до 69 лет включительно.
Что такое уреаплазмоз? Причины возникновения, диагностику и методы лечения разберем в статье доктора Ковалык Владимира Павловича, уролога со стажем в 27 лет.
Над статьей доктора Ковалык Владимира Павловича работали литературный редактор Елена Бережная , научный редактор Сергей Федосов

Определение болезни. Причины заболевания
Уреаплазмоз — группа воспалительных и дисбиотических заболеваний, ассоциированных с уреаплазмами (Ureaplasma species). С 1995 г. различают два вида уреаплазм: Ureaplasma urealyticum и Ureaplasma parvum. Геном U.urealyticum значительно больше U.parvum. В настоящее время невозможно утверждать, что какой-либо из видов является явным патогеном или наоборот — сапрофитом.
Уреаплазмы — условно-патогенные микроорганизмы, которые часто обнаруживаются на слизистых оболочках мочеполовых органов, верхних дыхательных путей и в рото-носоглотке.
В 2021 году профессиональные российские сообщества перестали разрабатывать официальные клинические рекомендации по ведению больных с Ureaplasma spp. и Mycoplasma hominis. Согласно позиции Международного союза по борьбе с инфекциями, передаваемыми половым путём, активное выявление этих микроорганизмов и лечение приносит больше вреда, чем пользы, так как из-за него устойчивость к антибиотикам развивается у действительно опасных инфекций. Поэтому антибиотики при выявлении этих бактерий нужно применять только при наличии симптомов.
Впервые уреаплазмы были выделены в США от темнокожего больного негонококковым уретритом в 1954 г. [1]
Первое попадание уреаплазм в мужскую уретру, как правило, вызывает уретрит — воспаление мочеиспускательного канала. Имеются данные о том, что у женщин уреаплазмы ассоциированы с острыми воспалительными заболеваниями органов малого таза (ВЗОМТ), а также с бактериальным вагинозом. Доказана роль уреаплазм в возникновении бронхолегочных заболеваний у новорожденных (бронхит, пневмония) и послеродового хорионамнионита. [2]
Роль уреаплазм в патологии человека до конца не установлена. Продолжается изучение патогенетической связи этих микроорганизмов с широким спектром заболеваний из разных сфер:
- заболевания мочеполовых органов у мужчин: бесплодие, простатит, везикулит, эпидидимоорхит; [3]
- урогенитальная патология у женщин: ВЗОМТ, бесплодие, воспаление бульбовагинальной железы;
- патология новорождённых. Существуют данные о том, что наличие уреаплазм приводит к низкому весу новорождённого и снижению балла по шкале Апгар;
- патология рожениц: преждевременные роды, преждевременный разрыв околоплодного пузыря, привычный выкидыш, замершая беременность и т. д.; , цистит. Уреаплазмы выявляли в удалённых из почек конкрементах в биоптатах мочевого пузыря, а эксперименты по инфицированию мышей приводили к появлению у них уратных камней в почках.
Уреаплазмы зачастую входят в состав нормальной микрофлоры уретры и влагалища. Частота выявления уреаплазм составляет в среднем 40% в мочеполовых органах у женщин и 5-15% у мужчин. При этом U.parvum обнаруживается значительно чаще, чем U.urealyticum (38% против 9%). [4]
Как передаётся уреаплазма
Уреаплазмы распространяются посредством сексуальных контактов. Чем больше сексуальных партнёров в течение жизни, тем чаще колонизация уреаплазмами влагалища или уретры. Уреаплазмы передаются новорождённым при прохождении через родовой канал. При этом происходит колонизация слизистой вульвы и влагалища у девочек и носоглотки у обоих полов. Частота выявления уреаплазм у новорожденных может достигать 30% и выше, снижаясь до нескольких процентов к первому году жизни. [5]
В последующем рост частоты колонизации уреаплазмами начинается с момента начала половой жизни (в 14-18 лет).
При обнаружении схожих симптомов проконсультируйтесь у врача. Не занимайтесь самолечением - это опасно для вашего здоровья!
Симптомы уреаплазмоза
Симптоматика различается в зависимости от возникшего заболевания.
Уреаплазмоз у мужчин
У мужчин может возникать уретрит, который проявляется скудными выделениями и жжением в мочеиспускательном канале, учащенным мочеиспусканием. Без лечения уретрит склонен к саморазрешению: симптомы затихают, пациент успокаивается. Перенесённый уретрит увеличивает вероятность возникновения в будущем воспаления предстательной железы — простатита. Кроме того, осложнениями уретрита могут быть эпидидимоорхит — воспаление яичка и его придатка, везикулит — семенного пузырька и, редко, куперит — бульбоуретральной железы.
Уреаплозмоз у женщин
У женщин под влиянием уреаплазм может развиваться сальпингоофорит, эндометрит и вагиноз.
Острый сальпингоофорит, эндометрит могут проявляться тянущими болями внизу живота, лихорадкой, слабостью и выделениями из вагины. Воспалительные заболевания тазовых органов у женщин — закономерное следствие бактериального вагиноза, наблюдаемого при выявлении уреаплазм. Симптомы заболевания могут быстро усугубляться, нередко требуется госпитализация в гинекологический стационар.
Помимо воспалительных заболеваний уреаплазмы, помимо многих других микроорганизмов, ассоциированы с бактериальным вагинозом.
Бактериальный вагиноз, как правило, сопровождается выделениями с неприятным запахом, который к тому же усиливается во время близости.
Заболевание предрасполагает к акушерско-гинекологическим осложнениям: преждевременным родам, рождению с низким весом.
Автор статьи разделяет взгляды мировых экспертов в области урогенитальной патологии (Jenny Marazzo, Jorma Paavonen, Sharon Hillier, Gilbert Donders) на отсутствие связи уреаплазм с возникновением цервицита и вагинита. [6] [7] [8]
Здесь необходимо заметить, что российский гайдлайн призывает проводить лечение цервицита и вагинита, базируясь на этиологической роли уреаплазм при этих заболеваниях, что, конечно же, является ошибкой. [17]
Уреаплазмоз у детей
У девочек в большинстве случаев уреаплазмы не вызывают каких-либо заболеваний, наблюдается здоровое носительство. Изредка развивается воспаление вульвыи/или влагалища. У новорождённых девочек и мальчиков повышен риск развития бронхолёгочной дисплазии.
Патогенез уреаплазмоза
Уреаплазмы — условно-патогенные микроорганизмы, т. е. их болезнетворные свойства реализуются только при особых условиях: высокая концентрация на слизистой, иммуносупрессия и другие.
Уреаплазмы прикрепляются к поверхности слизистой оболочки с помощью цитоадгезиновых протеинов. Кроме уретрального эпителия уреаплазмы способны прикрепляться к эритроцитам и сперматозоидам.
Одним из основных факторов патогенности являются ферменты фосфолипаза А и С, под влиянием которых в организме вырабатывается простагландин — фактор, запускающий сокращения непроизвольных мышц, следовательно, возможны преждевременные роды. Воспалительная реакция сопровождается выработкой провоспалительных цитокинов — IL 6, 8, 10.
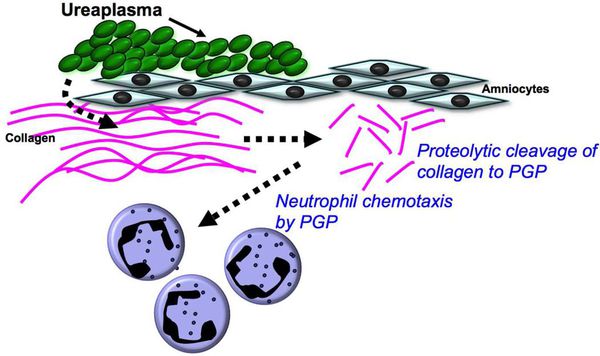
Уреаплазмы обладают IgA-протеазной активностью, разрушая местный защитный фактор слизистой оболочки иммуноглобулин А. [9]
Воспалительный процесс в мочеиспускательном канале развивается при большой концентрации уреаплазм. Так показано, что 10 3 КОЕ/мл и выше ассоциировано с выявлением 12 и более лейкоцитов на мл в уретральном содержимом. [10]
Особые факторы патогенеза реализуются при возникновении бактериального вагиноза. При этом ослабевают факторы местного иммунитета слизистой, благодаря чему такие пациентки более подвержены инфицированию инфекциями, передаваемыми половым путём (в т. ч. ВИЧ). Кислотность вагинального содержимого (рН в норме 3,5-4,5) снижается до нейтральной среды (рН 6,5-7 и выше). Таким образом, ослабевает естественный защитный барьер против болезнетворных микроорганизмов.
Классификация и стадии развития уреаплазмоза
По длительности протекания различают острый и хронический уретрит. Острый уретрит — до 2 месяцев, хронический — более 2 месяцев. В последнем случае различают рецидивирующий и персистирующий уретрит.
Хроническим рецидивирующим уретритом считается заболевание, при котором лейкоциты в уретре к концу лечения пришли в норму, а через 3 месяца — вновь наблюдался их подъём свыше 5 в поле зрения (при увеличении х1000). Хронический персистирующий уретрит — когда повышенное содержание лейкоцитов наблюдалось к концу лечения и через 3 месяца. [11]
ВЗОМТ подразумевает вовлечение в процесс маточных труб, яичника и их связок. Воспаление придатков может быть одно- и двухсторонним, острым или хроническим. Основные симптомы: боль внизу живота, в пояснице, выделения из половых органов, температура 38˚С и выше. [12]
Осложнения уреаплазмоза
У мужчин осложнениями уретрита являются баланопостит — воспаление головки и крайней плоти полового члена. Также возможны простатит, реже — эпидидимоорхит и шеечный цистит. При этом уреаплазмы не рассматриваются в качестве самостоятельного агента, вызывающего воспаление предстательной железы. Вероятно, эта цепь осложнений возникает посредством заднего уретрита и реализуется с помощью уретропростатического рефлюкса, т. е. заброса содержимого задней уретры в ацинусы простаты и семявыносящие протоки. [13]
У женщин ВЗОМТ может осложняться тубоовариальным абсцессом, изредка возникают перитонит и сепсис. В отдалённые сроки возможны серьёзные осложнения, имеющие социальные последствия: хроническая тазовая боль, внематочная беременность и бесплодие.
Маловероятно, что только лишь наличие уреаплазм в биоценозе влагалища приведёт к таким осложнениям. Свой патогенный потенциал эти микроорганизмы реализуют совместно с другими микроорганизмами, приводящими к дисбиотическим изменениям — бактериальному вагинозу. [14]
Диагностика уреаплазмоза
Показанием для назначения исследований для выявления уреаплазм являются клинические и/или лабораторные признаки воспалительного процесса: уретрит, ВЗОМТ. Не следует проводить рутинные исследования всем пациентам, в т.ч. без признаков какого-либо заболевания.
Для выявления уреаплазм используются только прямые методы выявления: бактериологический и молекулярно-генетический. Определение антител: IgG, IgA, IgM неинформативно. Материалом для исследования могут служить отделяемое мочеполовых органов, моча, вагинальный секрет и др.
Прямая иммунофлюоресценция (ПИФ) и иммунофлюоресцентный анализ (ИФА) менее информативны при уреаплазмозе, чем молекулярно-генетические и бактериологические исследования. Их применяют только при отсутствии последних.
Бактериальный вагиноз верифицируют с помощью критериев Амсела:
При наличии любых 3-х из 4-х критериев диагноз является установленным. Тем не менее, ввиду трудоёмкости выполнения, невозможности измерения рН оценка критериев Амсела затруднена.
Лечение уреаплазмоза
Лечение уреаплазмоза показано только в тех случаях, когда в результате обследования выявлена очевидная связь уреаплазм с воспалительным процессом. В случае здорового носительства уреаплазм лечение не показано. Порочной является практика назначения терапии всем лицам, у которых выявлены уреаплазмы.
Лечение показано донорам спермы и при бесплодии, когда других его причин не выявлено.
Недавние бактериологические исследования показали высокую активность в отношении уреаплазм Доксициклина, Джозамицина и ряда других антимикробных препаратов.
Схема лечения уреаплазмоза
Согласно клиническим рекомендациям Российского общества дерматовенерологов при неосложнённом заболевании — уретрит — проводят 10-дневные курсы лечения уреаплазмоза:
- Доксициклин моногидрат 100 мг по 1 таб. 2 раза в день;
- или Джозамицин 500 мг по 1 таб. 3 раза в день.
При персистенции воспалительного процесса курс лечения уреаплазмоза может быть продлён до 14 дней. [17]
При выявлении бактериального вагиноза назначают вагинальные препараты:
- Метронидазол вагинальный гель0,75% на ночь 5 г в течение 5 дней;
- или Клиндамицин крем 2% на ночь в течение 7 дней. [18]
Особенности лечения уреаплазмоза при беременности
При беременности по назначению врача можно применять препараты из группы макролидов и азалидов (Джозамицин, Азитромицин).
Прогноз. Профилактика
Ограничение числа сексуальных партнёров, применение барьерных методов контрацепции уменьшают колонизацию уреаплазм. В тех случаях, когда уже имеется носительство уреаплазм, необходимо профилактическое обследование и консультация у профильных специалистов перед:
Читайте также:

