Хронический тонзиллит дисбактериоз кишечника
Обновлено: 23.04.2024
Кафедра оториноларингологии, кафедра клинической фармакологии, бактериологии, аллергологии и иммунологии Ставропольской государственной медицинской академии
Кафедра оториноларингологии, кафедра клинической фармакологии, бактериологии, аллергологии и иммунологии Ставропольской государственной медицинской академии
Кафедра оториноларингологии, кафедра клинической фармакологии, бактериологии, аллергологии и иммунологии Ставропольской государственной медицинской академии
Кафедра оториноларингологии, кафедра клинической фармакологии, бактериологии, аллергологии и иммунологии Ставропольской государственной медицинской академии
Кафедра оториноларингологии, кафедра клинической фармакологии, бактериологии, аллергологии и иммунологии Ставропольской государственной медицинской академии
Микрофлора небных миндалин при хроническом тонзиллите
Кафедра оториноларингологии, кафедра клинической фармакологии, бактериологии, аллергологии и иммунологии Ставропольской государственной медицинской академии
Цель исследования - разработка стандартных подходов к фармакотерапии обострений хронического тонзиллита (ХТ) на основании данных о региональной специфике микробного пейзажа миндалин. Методы исследования: бактериологические исследования мазков со слизистой оболочки глотки у 668 пациентов с разными формами ХТ. В половине случаев ХТ определен Streptococcus pyogenes, в 24,5% - Mycoplasma pneumoniae. Наличие сопутствующей патологии респираторного и пищеварительного трактов у пациентов увеличивает вероятность идентификации энтеробактерий, энтерококков и стафилококков в ассоциации со стрептококками и микоплазмами. Для обоснованного выбора тактики антибиотикотерапии рекомендовано оценивать отягощающий анамнез и проводить бактериологическую диагностику с выделением и определением чувствительности к противомикробным средствам всех возможных патогенов.
Кафедра оториноларингологии, кафедра клинической фармакологии, бактериологии, аллергологии и иммунологии Ставропольской государственной медицинской академии
Кафедра оториноларингологии, кафедра клинической фармакологии, бактериологии, аллергологии и иммунологии Ставропольской государственной медицинской академии
Кафедра оториноларингологии, кафедра клинической фармакологии, бактериологии, аллергологии и иммунологии Ставропольской государственной медицинской академии
Кафедра оториноларингологии, кафедра клинической фармакологии, бактериологии, аллергологии и иммунологии Ставропольской государственной медицинской академии
Кафедра оториноларингологии, кафедра клинической фармакологии, бактериологии, аллергологии и иммунологии Ставропольской государственной медицинской академии
Хронический тонзиллит (ХТ) — инфекционно-аллергическое заболевание всего организма с наибольшими проявлениями патологического процесса в лимфоидном аппарате глотки. Выраженность проявлений ХТ обусловлена множественными факторами: индивидуальной реактивностью организма, вирулентностью возбудителей, особенностями окружающей среды, длительностью заболевания и т.д.
Одним из основных факторов, определяющих характер клинических проявлений ХТ, являются микробный пейзаж небных миндалин и вирулентность инфекции. Единого мнения о составе микрофлоры в лакунах небных миндалин в настоящее время нет. Это обусловлено, по-видимому, в первую очередь региональными особенностями микрофлоры, поражающей верхние отделы респираторного тракта, способами ее забора и использованием различных методов исследования патологического содержимого небных миндалин.
Исследования, проведенные в различных регионах России [1—3], подтверждают ведущую роль β-гемолитического стрептококка группы А (БТСА) в этиологии ХТ. Вместе с тем при хронической форме патологии в качестве сопутствующей микрофлоры выявляются различные виды сапрофитных и условно-патогенных микроорганизмов.
Разнообразие микрофлоры в лакунах миндалин у больных, страдающих ХТ в различных климатогеографических регионах, затрудняет выработку стандартных подходов к лечению этого весьма распространенного заболевания.
Цель исследования — разработка стандартных подходов к фармакотерапии ХТ на основании данных о региональной специфике микробного пейзажа миндалин.
Материал и методы
Результаты и обсуждение
Бактериологический диагноз был подтвержден у 425 (63,6%) обследованных. У остальных пациентов обострение процесса, видимо, было связано с вирусной инфекцией. Стрептококковый процесс выявлен у 53% пациентов, причем в подавляющем большинстве случаев выделен ЮГСА, а на долю пневмококка пришлось лишь 7,8% случаев обострений. В 24,5% выделены Mycoplasma pneumoniae. Необходимо отметить, что у 98 (23,1%) пациентов были идентифицированы ассоциации микроорганизмов: в ассоциациях с микоплазмами и стрептококками присутствовали Staphylococcusaureus (26,8% всех случаев ХТ), Enterococcus faecalis (3,5%) и представители Enterobacteriaceae spp. (15,3%).
В зависимости от стадии и выраженности воспалительного процесса в лимфаденоидном аппарате глотки заметно менялся и состав микрофлоры в небных миндалинах. Так, в стадии ремиссии ХТ при стихании воспалительного процесса БГСА составляли 27%, а преобладали микоплазмы, энтеробактерии и стафилококки. При катаральной, фолликулярной и лакунарной ангине удельный вес БГСА заметно повышался и достигал 65% при формировании паратонзиллярного абсцесса. Необходимо отметить, что в ранее проведенном исследовании выявлена корреляция частоты персистенции в миндалинах Mycoplasma pneumoniae с частотой обострений у больных с ХТ [3]. Энтерококки и различные виды энтеробактерий выявлялись только у пациентов с сопутствующей патологией желудочно-кишечного тракта (гастроэзофагеальная рефлюксная болезнь, язвенная болезнь).
При оценке чувствительности микроорганизмов к противомикробным средствам установлено, что БГСА в 100% случаев чувствительны к β-лактамным антибиотикам (пенициллин, амоксициллин и др.), левофлоксацину. Резистентными к эритромицину оказалось 12,4%, а к левомицетину — 38% штаммов БГСА. 33% штаммов Mycoplasma pneumoniae оказались резистентными к эритромицину, по 19,4% — к азитромицину и кларитромицину, 8,3% — к тетрациклинам, 16,3% — к офлоксацину/левофлоксацину и всего 5,6% — к ципрофлоксацину. Все штаммы Staphylococcusaureus оказались β-лактамо-продуцирующими, а резистентных к оксациллину, а значит и ко всем β-лактамным антибиотикам, выделено 7,6%.
Таким образом, основными возбудителями обострений при ХТ остаются БГСА, которые выявляются у большинства пациентов, причем с увеличением тяжести процесса доля стрептококков только увеличивается. Частое выявление стафилококков, продуцирующих β-лактамазы, заставляют рассматривать в качестве стартовой терапии назначение защищенных аминопенициллинов. Заметную роль в формировании воспалительного процесса, по-видимому, играет Mycoplasma pneumoniae, а у пациентов с сопутствующей патологией желудочно-кишечного тракта — энтерококки, энтеробактерии. Различный уровень резистентности микроорганизмов позволяет рекомендовать проведение бактериологической диагностики отделяемого из лакун миндалин перед выбором рациональной тактики антибактериальной терапии.
По результатам бактериологической диагностики выбор терапии рекомендуется строить на основании выявленного характера микроорганизмов и уровня их резистентности к противомикробным препаратам. В частности, стрептококковый процесс требует 10-дневной терапии феноксиметилпеницилином или амоксициллином. В случае выявления ассоциации стрептококков со стафилококками, энтерококками или энтеробактериями стартовым следует рассматривать амоксициллин/клавуланат. При микоплазмозах рекомендуется использовать макролидные антибиотики либо фторхинолоны.
Выводы
1. В обязательный перечень диагностических процедур у больных с ХТ следует включать бактериологическое исследование с выявлением всех возможных возбудителей обострений (включая стрептококки, микоплазмы).
2. Выбор тактики антибиотикотерапии (амоксициллин либо амоксициллин/клавуланат, макролиды или фторхинолоны), рекомендованной стандартами, должен строиться с учетом индивидуального микробного пейзажа в каждом случае ХТ.
СОСТОЯНИЕ МИКРОФЛОРЫ КИШЕЧНИКА У БОЛЬНЫХ ХРОНИЧЕСКИМ ТОНЗИЛЛИТОМ ПРИ КОМПЛЕКСНОЙ ЭТИОТРОПНОЙ ТЕРАПИИ

"Любой эпизод острого заболевания и обострение хронического инфекционного процесса приводит к сдвигу в эндобиоценозе. Немаловажным фактором воздействия на микробиоценоз являются антимикробные препараты, однако, при остром и хроническом тонзиллите, острых респираторных инфекциях и других заболеваниях верхних дыхательных путей врачи не придают значения этим изменениям".
ПРОБИОТИКИ И ХРОНИЧЕСКИЙ ТОНЗИЛЛИТ
Примечание редактора

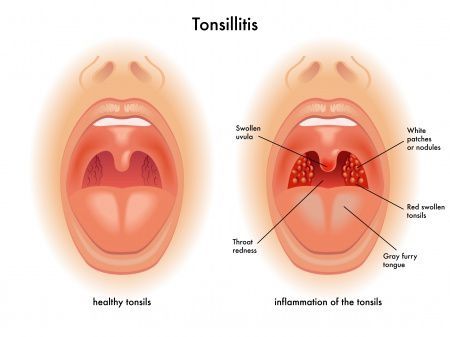
Хронический тонзиллит — длительное воспаление глоточной и нёбных миндалин (от лат. tonsollitae — миндалевидные железы). Развивается после перенесённой ангины и других инфекционных болезней, сопровождающихся воспалением слизистой оболочки зёва (скарлатина, корь, дифтерия), или без предшествующего острого заболевания.
Для простой формы хронического тонзиллита характерны только местные симптомы (боль в горле и др.), если к ним присоединяются общие явления (стойкий шейный лимфаденит, повышенная температура тела, изменения со стороны сердца и т.д.), такая форма называется токсико-аллергической.
Хронический тонзиллит может быть вызван различными инфекциями. Среди патогенов при хроническом тонзиллите наиболее часто обнаруживают стафилококки, стрептококки, пневмококки, гемофильную палочку, моракселлу, аденовирусы, вирус Эпштейна — Барр (ВЭБ), вирусы Коксаки, вирус герпеса, различные анаэробы, микоплазмы, хламидии, грибы.
ВАЖНОЕ ЗАМЕЧАНИЕ К ИССЛЕДОВАНИЮ!
Стоит отметить, что приведенное ниже исследование, в части касаемой применения пробиотиков, привязано к использованию коммерческого препарата Линекс. Проведение исследований под конкретный препарат - это общепринятая и вполне оправданная практика. Если посмотреть результаты запросов по данной теме, то можно увидеть, что не только производители Линекса заинтересованы в продвижении своей продукции микробиологического производства. Таким примером являются, например, рекомендации по использованию пробиотического препарата Бифидум БАГ при профилактике и лечении тонзиллита .
Однако с учетом того, что капсулированная форма Линекса, использованная в исследовании, состоит из таких видов пробиотических микроорганизмов, как Lactobacillus acidophilus, Bifidobacterium infantis, Enterococcus faecium, то опираясь на результаты работы можно предположить, что эффективность пробиотикотерапии можно повысить. Это следует из того, что жидкая форма пробиотиков (в отличие от капсулированной) помимо толстого кишечника активно воздействует и на тонкий кишечник, где происходят все значимые биохимические и микробные процессы (т онкий кишечник отдельно (!) упоминается в исследовании).
Кроме того, в работе особо отмечается прогрессивное снижение общего количества микроорганизмов в тонкой кишке на фоне терапии основного заболевания, преимущественно за счет уменьшения численности Lactobacillus, Bifidobacterium и Propinibacterium freudenreichii . Пробиотические культуры классических (молочных) пропионовоксилых бактерий (ПКБ) P. freudenreichii в описанном исследовании 2016 года не использовались. И здесь стоит отметить, что б иоконцентраты с ПКБ от ООО "Пропионикс", обладающие бифидогенными свойствами восполняют дефицит не только ПКБ, но и бифидобактерий . Более того, при снижении кол-ва Lactobacillus в кишечнике, их восстановление с помощью приема лактопрепаратов происходит намного быстрее в присутствии ПКБ, которые по последним данным 2018 г. входят в систему защиты благоприятной для человека микробиоты (Рыжкова Е.П. Классические пропионовокислые бактерии как пробиотики / Учебное пособие – М.: изд. Биологический факультет МГУ, 2018 – 52с.).
И последнее, что хотелось подчеркнуть, это указание на устойчивость бактериальных штаммов из Линекса к антимикробным препаратам (как на преимущество), а также на их совокупную эффективность. Однако указанная устойчивость не является исключительным свойством бренда, т.к. многие штаммы полезных микроорганизмов, используемые в современных жидких пробиотиках, помимо устойчивости к агресивной среде ЖКТ, устойчивы и к антибиотикам, что допускает их совместное использование в случае необходимости. Так, например, классические пропионовые бактерии P. freudenreichii устойчивы к пенициллину, хлортетра-циклину, хлормицетину, стрептомицину, эритромицину, грамицидину С, полимиксину и некоторым др., а потому возможно их совместное применение. Тоже относится и к синергизму (совокупной полезной активности): например, совместное использование бифидобактерий и пропионовокислых (толерантных к лактобациллам) выражается в повышении их антимутагенного, в т.ч. антибиотического (бактерицидного и бактериостатического в отношении патогенов ) эффекта, в т.ч. наблюдается усиление антиоксидантной и иммуномодулирующей активности.
ИССЛЕДОВАНИЕ

Способность организма к ответу на инфекционный агент во многом определяется состоянием эндобиоценоза, не только являющегося важным компонентом надежной внутренней системы контроля организма за инфекциями, но и обеспечивающим становление тонких механизмов гомеостаза, саморегуляции [1]. Нормальные симбиотические отношения допускают существенные колебания количественного состава того или иного эпитопа микробиоценоза, однако, всегда в рамках определенного баланса, прежде всего функционального, между различными видами [2]. Любой эпизод острого заболевания, в том числе и обострение хронического инфекционного процесса, является толчком к изменению среды организма, сдвигу в эндобиоценозе. Немаловажным фактором воздействия на микробиоценоз являются антимикробные препараты, однако, при хроническом и остром тонзиллите, острых респираторных инфекциях и других заболеваниях верхних дыхательных путей врачи не придают значения этим изменениям. Вместе с тем, сам факт обнаружения количественных и качественных изменений в биотопах без рассмотрения их в контексте клинических данных не является решающим аргументом в определении глубины нарушений и обосновании необходимости лечебного вмешательства. Необходима целостная оценка организма.
Цель исследования
Дать оценку количественного и качественного состава микрофлоры кишечника у больных хроническим тонзиллитом в стадии обострения на фоне базисной терапии и в комплексе с пробиотиком Линекс.
Материалы и методы
Обследовано 62 больных острым бактериальным тонзиллитом или хроническим в стадии обострения,в возрасте от 18 до 43 лет (в среднем 27,7 ± 1,1 года),из них: 32 (52,8%) мужчины и 30 (47,2%) женщин,находившихся на обследовании и лечении в клиникеинфекционных болезней ВМедА им. С.М. Кирова.
Критериями включения в настоящее исследованиебыли возраст от 18 до 45 лет, диагностированныйтонзиллит, пероральная моноантибиотикотерапия, атакже добровольное информированное согласие пациентов на проведение исследования.
Критериями исключения из настоящего исследования были: смена антибиотика во время лечения; сопутствующие заболевания желудочно-кишечного тракта в стадии обострения; использование других антибиотиков, про,- пре,- синбиотических препаратов на момент исследования, или в течение 2-х недель до его начала; наличие тяжелой сопутствующей патологии; неспособность самостоятельного приема лекарственных препаратов, заполнения анкет, а также письменного согласия на проведение исследования; добровольный отказ пациента от проведения исследования.
В зависимости от терапии, всех пациентов рандомизировали на две группы, сопоставимые по полу, возрасту, этиологии заболевания, тяжести и длительности течения с момента манифестации признаков тонзиллита. Результаты исследования регистрировали и оценивали до лечения и на 5-й день наблюдения.
В составе базисной терапии, включавшей режим, диетическое питание (стол №15) по М.И. Певзнеру , все пациенты получали трехдневный курс азитромицина по 500 мг в сутки.
1-ю группу составили 32 больных ХТ (группа Л), программа лечения которых, помимо базисной терапии, включала двухнедельный пероральный прием пробиотического поликомпонентного препарата Линекс (Lactobacillus acidophilus, Bifidobacterium infantis, Enterococcus faecium) по 2 капсулы 3 раза в день после еды.
2-ю группу составили 30 больных ХТ (группа АБ), программа лечения которых включала только базисную терапию.
Результаты и обсуждение
Таблица 1 Состав микрофлоры толстой кишки у больных тонзиллитом при комплексной этиотропной терапии, lg КОЕ/г
После завершения антибактериальной терапии основного заболевания в комплексе с пробиотиком, у тех пациентов первой группы, у которых до начала терапии обнаружены грибы рода Candida, на 5-й день исследования их рост не отмечался.
В группе больных, получавших только этиотропную терапию (2-я группа, АБ), выявлено значительное снижение всех определявшихся представителей нормальной микробиоты кишечника, а также условно-патогенной флоры.
По данным масс-спектрометрии при обострении ХТ в тонкой кишке наблюдается снижение обще численности микроорганизмов преимущественно за счет уменьшения количества Lactobacillus, Bifidobacterium и Propinibacterium freudenreichii на фоне избыточного роста Eubacterium и Staphylococcus (табл. 2). Кроме того, возросла численность анаэробов Bacteroides fragilis, Porphyromonas и Propinobacterium acnes, при периодическом избытке Bacillus megaterium, Bacillus cereus, C. difficile, а также Streptococcus mutans, Prevotella и Bacteroides.
Уровень эндотоксинемии у больных 1-й группы снижался к 5-м суткам лечения с 1,024718 до 0,99435 (р>0,05), тогда как во 2-й группе отмечалось его увеличение с 0,299363 до 0,32557 (р>0,05).
Содержание кокков, бацилл и коринебактерий у пациентов 1-й группы на фоне терапии увеличилось, тогда, как у больных 2-й группы отмечалось снижение. Так, уровень Streptococcus spp. в 1-й группе увеличился в 9 раз по сравнению с исходным (5,675406 и 43,60326, p<0,05). В то же время во 2-й группе этот показатель снизился почти на 12% (с 74,87617 до 65,9556, р>0,05).
Численность Lactobacillus к 5-м суткам терапии в обеих группах не достигало нормы, однако в 1-й группе выявлено увеличение их численности с 1309,728 до 1424,912. В то же время при монотерапии антибиотиком отмечено снижение числа лактобацилл с 886,0019 до 847,7987.
Содержание Bifidobacterium оставалось без существенных изменений как в группе получавших Линекс® (1129,789 и на 5-е сутки 1187,419), так и в группе контроля (с 544,8046 до 648,9446).
На фоне проведенной терапии у пациентов 1-й группы выявлено увеличение численности популяции микрогрибов, продуцирующих кампестерол и ситостерол, однако различия были не значимы – с 161,4923 до 168,6245 и с 257,5063 до 329,3031, соответственно (p>0,05). У больных 2-й группы отмечалось снижение этих показателей, но не достигающее уровня достоверности (p>0,05). В обеих группах наблюдался рост численности дрожжеподобных грибов рода Candida с 109,1159 до 173,3375, (р<0,05) в 1-й группе и с 112,9143 до 138,3557, (р>0,05) – во 2-й.
На фоне приема пробиотического препарата выявлено незначительное снижение количества Staphylococcus, Bacillus cereus и Corineform group (p>0,05) и достоверное уменьшение популяции Bacillus megaterium – в 4,5 раза (p<0,05). В то же время у больных, получавших только азитромицин, бациллы не определялись, а содержание Staphylococcus intermedius снизилось на 10% (табл. 2). Вместе с тем, у этих пациентов отмечался незначительный рост Corineform.
Таблица 2 Состав микрофлоры толстой кишки у больных тонзиллитом при комплексной этиотропной терапии
На 5-й день терапии у больных 1-й группы име- ло место увеличение популяции большинства анаэробов. Общее количество Eubacterium, Clostridium group, Propionibacterium acnes, Prevotella и Fusobacterium выросло, однако изменения численности некоторых представителей этих групп было недостаточно значимым. Количество Eubacterium lentum и Propionibacterium jensenii выросло в 2 раза, а Bacteroides fragilis – в 3,5. У пациентов 2-й группы концентрация этих микроорганизмов снизилась, либо сохранялась на прежнем уровне, а количество представителей рода Clostridium даже несколько увеличилось. В то же время у пациентов этой группы отмечался значительный рост Bacteroides ruminicola, уровень которых вырос в 3 раза и отмечалось двукратное увеличение числа Propionibacterium acnes.
До начала терапии у всех пациентов выявлено низкое содержание основных представителей аэробных актинобактерий. Численность Actinomyces и Pseudonocardia была снижена в 3 раза, по сравнению с нормальными показателями, без статистически значимого различия в группах сравнения. Количество Rhodococcus было снижено в 4,5 раза, тогда как Actinomycetes были обнаружены только у одного пациента 2-й группы в низкой концентрации. После проведенного лечения обращает на себя существенная разница показателей в группах сравнениях. Так, у пациентов 1-й группы на 5-й день исследования отмечался рост Streptomyces (с 104,4846 до 128,1612, p<0,05), что изначально превышало норму почти в 2 раза, и Rhodococcus (с 5,493359 до 5,77627, p>0,05), тогда как у больных 2-й группы наблюдалось снижение количества этих микроорганизмов на фоне приема антибиотика. И, наоборот, у представителей 1-й группы на фоне лечения обнаруживалось снижение количества Nocardia asteroides, тогда как в группе сравнения выявлено ее увеличение.
До начала терапии только в одном случае в 1-й группе в тонкой кишке выявлялась E.coli в количестве 3,5×107 КОЕ. Однако к 5-му дню наблюдения отмечено снижение содержания этого микроорганизма до нормальных значений.
Во всех случаях не были обнаружены представители рода Enterococcus, но были выделены грамотрицательные палочки. В 1-й группе, на фоне лечения, количество Pseudomonas aeruginosa выросло с 0,08507 до 0,140437 (p>0,05), у одного пациента 2-й группы они появились на фоне приема антибиотика. Также у больных 1-й группы отмечался рост Porphyromonas (с 0,195804 до 0,895437, p>0,05), вместе с тем количество Acinetobacter у этих пациентов на фоне терапии снижалось (с 0,621489 до 0,274079, p>0,05).
Заключение
Проведенные исследования выявили значительное снижение всех определяемых представителей нормальной микробиоты кишечника и условно-патогенной флоры у пациентов 2-й группы.
Установлено, что на фоне терапии основного заболевания отмечается прогрессивное снижение общего количества микроорганизмов в тонкой кишке ,преимущественно за счет уменьшения численности Lactobacillus, Bifidobacterium и Propinibacterium freudenreichii , в сочетании с избыточным ростом Eubacterium и Staphylococcus. Кроме того, растет численность анаэробов Bacteroides fragilis, Porphyromonas, Propinobacterium acnes, Bacillus megaterium, Bacillus cereus, C. difficile, а также Streptococcus mutans, Prevotella и Bacteroides.
После проведенного лечения у пациентов обеих групп определялись значительные изменения состава микробных маркеров в крови. Из 56 определяемых показателей в 1-й группе наблюдения либо сохранялись на высоком уровне, либо стали превышать нормальные значения по 33 параметрам, тогда как во 2-ой группе – по 24. Уровень эндотоксинемии при назначении препарата Линекс снижался, тогда как при терапии только антибиотиком, этот показатель возрастал.
Микробиологическое исследование кала является эталоном оценки качественного и количественного состава микробиоты толстой кишки. В связи с объективными трудностями получения материала для исследования из тонкой кишки, в настоящее время для оценки состава микробиоценоза этого отдела кишечника все шире используется анализ микробных метаболитов крови методом масс-спектрометрии. По данным обоих этих методов, у больных острым бактериальным тонзиллитом и при обострении хронического тонзиллита в различных отделах кишечника выявлено снижение количества представителей собственно аутохтонной микрофлоры с одновременным доминированием анаэробов, обладающих провоспалительной и протеолитической активностью.
Полученные данные позволяют рассматривать антибиотики и пробиотики не как несовместимые группы препаратов или антагонисты. Там, где начинаются проблемы применения одной из групп лекарственных средств, там могут начинаться преимущества другой. И лишь совместное их рациональное использование создает предпосылку достижения максимального результата в широком спектре клинических ситуаций [3].
Пробиотики, состоящие из нескольких штаммов, за счет особенностей природной устойчивости к ряду антимикробных препаратов получают некоторые преимущества перед индигенной микрофлорой. В такой ситуации пробиотическая поддержка микробиоценоза реализует сложный комплекс пробиотических свойств как каждого штамма, входящего в препарат, так и совокупной активности пробиотической композиции. Среди них – обеспечение стабильности индивидуального микробиологического ядра кишечного микробиоценоза, ферментативная активность, обеспечение синтеза витаминов, резистентности эпителиального барьера и другие.
Литература
1. Жданов К.В., Захаренко С.М., Гусев Д.А., Куртуков М.В., Сукачев В.С., Сигидаев А.С. Особенности микроэкологии кишечника у больных циррозом печени. Лечение и профилактика. – 2012. - 3(4). – С. 36-49.
3. Захаренко С.М., Суворов А.Н. Антибиотики, пробиотики, пребиотики: друзья или враги? // Consilium Medicum том 11/ №8 2009. - С.47-51.
Будьте здоровы!
ССЫЛКИ К РАЗДЕЛУ О ПРЕПАРАТАХ ПРОБИОТИКАХ
Что такое хронический тонзиллит? Причины возникновения, диагностику и методы лечения разберем в статье доктора Селютина Е. А., ЛОРа со стажем в 26 лет.
Над статьей доктора Селютина Е. А. работали литературный редактор Маргарита Тихонова , научный редактор Сергей Федосов

Определение болезни. Причины заболевания
Хронический тонзиллит (Chronic tonsillitis) — это длительный стойкий хронический процесс воспаления нёбных миндалин, которому сопутствуют такие рецидивные обострения, как ангина и общая токсико-аллергическая реакция. [5]
Функции миндалин
Миндалины (лат. tonsillae) — скопления лимфоидной ткани, расположенные в области носоглотки и ротовой полости. Они являются частью иммунной системы и препятствуют проникновению микробов в организм через рот или нос.
Почему развивается воспаление нёбных миндалин
К воспалению миндалин приводит длительное воздействие патогенов. Человеческий организм воспринимает воспаление как чужеродное образование и включает аутоиммунный механизм (борьба иммунитета против своих же тканей). [4]
Однако данная теория аутоиммунной причины воспаления пока полностью не доказана, так как не выявлено существенных изменений в показателях системного иммунитета из-за их транзиторного (временного) характера.
Косвенно о наличии хронического тонзиллита свидетельствует проходящая под действием системных антибиотиков боль в горле, которая возвращается после отмены из применения. [9]
Факторы риска
Американские учёные среди причин хронического воспаления миндалин выделяют астму, аллергию, бактерии и вирусы (в частности вирус Эпштейна), гастроэзофагеальную рефлюксную болезнь (заброс кислого содержимого желудка в пищевод).
Однако механизм влияния данных причин на появление хронического тонзиллита зарубежными экспертами не объясняется. Остаются открытыми вопросы:
- Как именно вышеперечисленные американскими учёными причины смогут способствовать поражению лимфатической ткани инфекцией?
- Насколько активно данные факторы участвуют в патогенезе хронического воспаления миндалин?
Так, в современной оториноларингологии остаётся множество нерешённых вопросов, связанных с хроническим тонзиллитом. Существуют разногласия по поводу классификации, методов диагностики и тактики лечения среди врачей в России и других странах мира. Поэтому тема хронического тонзиллита весьма актуальна.
При обнаружении схожих симптомов проконсультируйтесь у врача. Не занимайтесь самолечением - это опасно для вашего здоровья!
Симптомы хронического тонзиллита
К симптомам хронического тонзиллита у взрослых относятся:
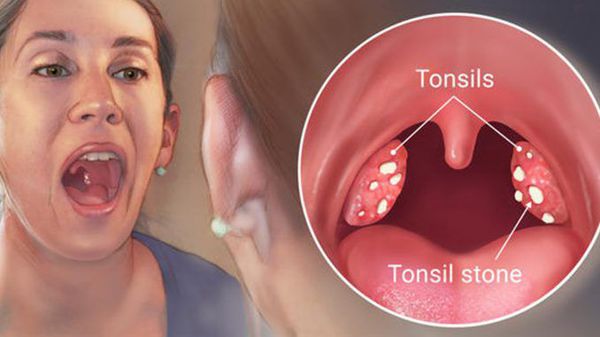
- постоянные болезненные ощущения в горле, пробки;
- неприятный запах изо рта;
- лимфаденит шеи.
Признаки тонзиллита у маленьких детей:
- слюнотечение из-за затруднённого или болезненного глотания;
- отказ от еды;
- повышенное беспокойство [13] .
Патогенез хронического тонзиллита
Длительное взаимодействие вируса и микроорганизма формирует очаг хронического тонзиллита и способствует развитию тонзиллогенных процессов.
Согласно материалам авторов России и зарубежья, бета-гемолитический стрептококк группы А и вирусы — основные причины развития хронического тонзиллита. [3]
В паренхиме (составляющих элементах) и сосудах здоровых миндалин бактерий не выявлено.
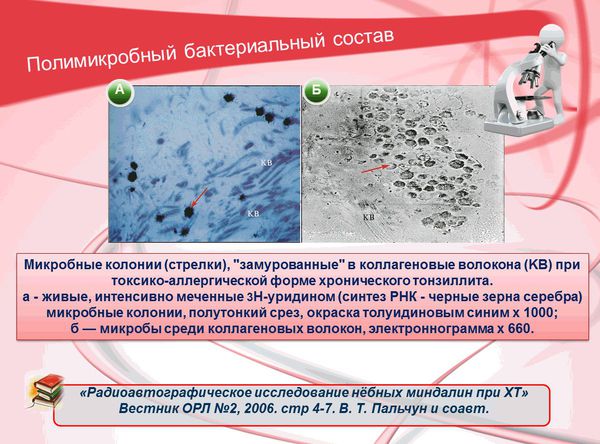
В настоящее время рассматривается вопрос о влиянии биоплёнок на течение хронического инфекционного процесса в аденотонзиллярной ткани. [12]
J. Galli и соавт. (Италия, 2002) в образцах аденоидной ткани и тканях нёбных миндалин детей, у которых наблюдалась хроническая аденотонзиллярная патология, смогли обнаружить прикреплённые к поверхности кокки, организованные в биоплёнки. Исследователи выдвигают предположение, что биоплёнки, образованные бактериями на поверхности аденоидной ткани и нёбных миндалинах, помогут выяснить, в чём заключается трудность эрадикации (уничтожения) бактерий, участвующих в образовании хронического тонзиллита.
На данный момент подтверждено внутриклеточное расположение:
- золотистого стафилококка;
- пневмококка;
- гемофильной палочки;
- аэробного диплококка (Moraxella catarrhalis);
- бета-гемолитического стрептококка группы А.
Для того, чтобы обнаружить и идентифицировать расположение микроорганизмов внутри клеток, можно применить полимеразную цепную реакцию (ПЦР), а также гибридизацию in situ (FISH-метод).
Однако приведённые исследования не позволяют выявить один патогенный микроорганизм, вызывающий клинику хронического воспаления миндалин. Поэтому весьма вероятно, что течение заболевания способен вызвать любой микроорганизм, который находится в ротоглотке, в условиях, способствующих воспалительному процессу в ткани нёбных миндалин. К подобным условиям можно отнести гастроэзофагеальный рефлюкс.
Определённую роль в возникновении хронического воспаления миндалин и сопряжённых с ним болезней играют прямые лимфатические связи миндалин с различными органами, прежде всего с центральной нервной системой и сердцем. Морфологически доказаны лимфатические связи миндалин и мозговых центров.
Классификация и стадии развития хронического тонзиллита
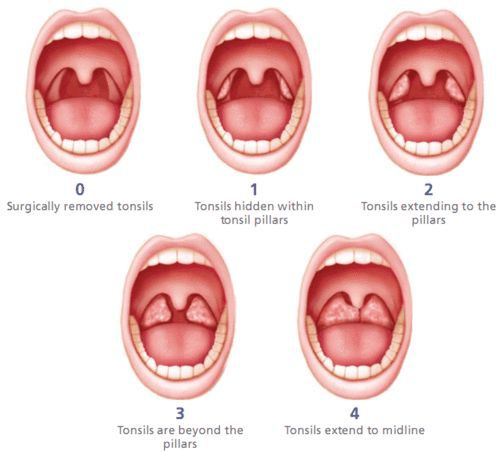
В России существует две классификации хронического тонзиллита, сформированные около 40 лет назад: Б.С. Преображенского — В.Т. Пальчуна 1965 года и И.Б. Солдатова 1975 года.
Формы хронического тонзиллита
Классификация Б.С. Преображенского — В.Т. Пальчуна включает в себя две клинические формы хронического тонзиллита:
Устоявшиеся клинические критерии диагностики были созданы описательной медициной и не изменились с появлением доказательной медицины. К примеру, признаки простой формы хронического воспаления миндалин субъективны и зависят, в основном, от индивидуального восприятия врача.
Классификация И.Б. Солдатова подразделяет хронический тонзиллит на:
- компенсированную форму;
- декомпенсированную форму.
Все эти классификации объединены субъективным подходом, так как одинаковые состояния нёбных миндалин различаются лишь их формулировкой.
Осложнения хронического тонзиллита
Самое распространенное осложнение — кровотечение. По оценкам, 2-8% пациентов страдают от кровотечения.
Воспаление или отёк миндалин могут приводить к следующим осложнениям:
-
;
- скопление гноя вокруг и за миндалинами (тонзиллярный целлюлит и паратонзиллярный абсцесс) [13] .
Чем опасен хронический тонзиллит
Очень редкими, но опасными для жизни являются внутричерепные осложнения: менингит, тромбоз синусов мозговых оболочек, абсцесс мозга.
Из осложнений после тонзиллэктомии следует отметить подкожную эмфизему, пневмонию, абсцесс и ателектаз лёгкого, парезы отдельных нервов или их ветвей, медиастинит, тонзиллогенный сепсис.
Диагностика хронического тонзиллита
Когда необходимо обратиться к врачу
Посетить врача-отоларинголога следует при болезненных ощущения в горле, неприятном запахе изо рта и воспалении шейных лимфоузлов.
При диагностике хронического тонзиллита важно определить наличие следующих симптомов:
- симптом Гизе — гиперемия краёв нёбных дужек;
- симптом Зака – отёк в области верхнего угла между нёбно-язычной и нёбно-глоточной дужками;
- симптом Преображенского – валикообразное утолщение краёв передней и задней нёбных дужек.
Эти признаки хронического тонзиллита возникают в связи с раздражением слизистой оболочки содержимым лакун миндалин, выдавливаемое при напряжении дужек, например во время глотания. Фарингоскопически симптомы хронического воспаления нёбных миндалин легко определяются, но диагностическая ценность их ограничена тем, что они могут встречаться при других заболеваниях (к примеру, при остром обострении хронического фарингита). Следующий фарингоскопический симптом — спайки между дужками и поверхностью миндалин. Бесспорный признак хронического тонзиллита — присутсвие жидкого гнойного экссудата (накопившейся жидкости) в лакунах.
Все эти признаки характеризуют простую (по Б.С. Преображенскому) или компенсированную (по И.Б. Солдатову) форму хронического тонзиллита, при которой ещё не выявляются симптомы очаговой инфекции.
Токсико-аллергическая форма I степени характеризуется начальными проявлениями общего заболевания. Они связаны с обострениями хронического тонзиллита и диагностируются в течение некоторого времени после ангины. Чаще всего поражается сердечно-сосудистая система. На данном этапе заболевания изменения носят функциональный характер и не выявляются на электрокардиограмме. Центральный механизм нарушения сердечной деятельности в этой стадии доказан экспериментально. Другие признаки токсико-аллергической формы I степени — субфебрилитет и тонзиллогенная интоксикация в виде быстрой утомляемости, слабости, снижения работоспособности в течении некоторого времени после ангины. Эти признаки неспецифичны и могут быть связаны с различными состояниями организма. Между тем, их идентификации и установление связи с заболеванием миндалин имеют принципиально важное значение для разработки рационального лечения хронического тонзиллита. Для установления связи субфебрилитета и интоксикации с хроническим тонзиллитом используют диагностический прием — пробное лечение. Если после курсового промывания лакун нёбных миндалин симптомы исчезают — они связаны с хроническим тонзиллитом.
Токсико-аллергической форме II степени характерно развернутое проявление очаговой инфекции. Признаки хронического тонзиллита теряют связь с обострениями и существуют постоянно, их можно зарегистрировать при функциональных исследованиях. Кроме того, для этой стадии характерно наличие сопряженных заболеваний. К сопряженным заболеваниям относятся коллагенозы (системная красная волчанка, ревматизм, склеродермия, узелковый периартериит, дерматомиозит), заболевания кожи (экзема, псориаз, нефрит, многоморфная экссудативная эритема, тиреотоксикоз и др.).
Лечение хронического тонзиллита
Хронический тонзиллит принято лечить консервативными и хирургическим методами.
Консервативное лечение хронического тонзиллита
Консервативный метод лечения показан, если хронический тонзиллит имеет компенсированную форму. Консервативное лечение применяется при наличии противопоказаний к хирургическому методу лечения.
К консервативным методам лечения относятся: [8] [10]
Беременность и хронический тонзиллит
Хронический тонзиллит у беременных лечат только консервативно — орошением глотки антисептиками.
Оперативное лечение
В случае неэффективности консервативного лечения применяют полухирургические способы лечения: ультразвуковую биологическую чистку или лазерную вапоризацию лакун нёбных миндалин.
При декомпенсации хронического воспаления, применяется полное удаление миндалин — тонзиллэктомия.
Недостаточная эффективность системной антибиотикотерапии при хроническом тонзиллите подтверждается клинически. Исследование, основанное на изучении бактериологического состава с поверхности нёбных миндалин у 30 детей, подвергшихся их удалению, доказало: антибиотики, которые дети принимали шесть месяцев до начала операции, не повлияли на бактериологию миндалин к моменту тонзиллэктомии. [6] [7] [9]
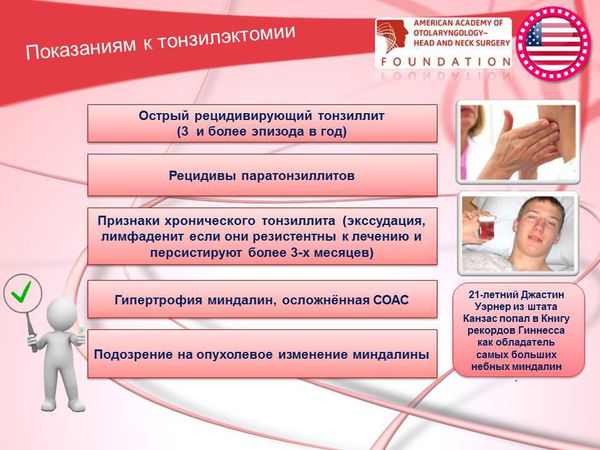
Показаниями к тонзиллэктомии являются:
- острая рецидивирующая форма тонзиллита (от 3-х эпизодов в год);
- рецидивы паратонзиллитов;
- симптомы хронического тонзиллита (экссудация, лимфаденит, если они резистентны к лечению и персистируют более 3-х месяцев);
- гипертрофия миндалин, осложнённая СОАС;
- подозрение на опухолевое изменение миндалины.
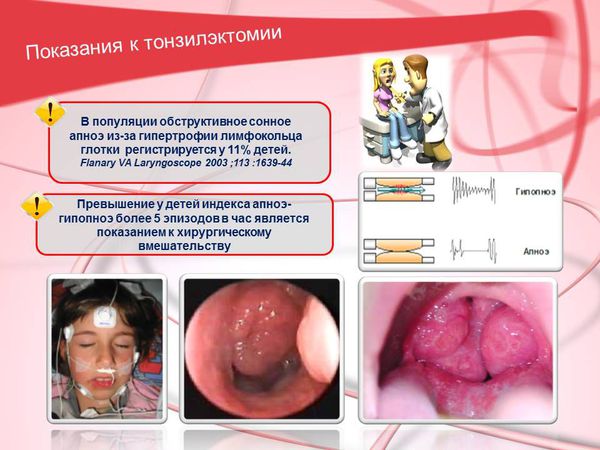
В популяции обструктивное сонное апноэ из-за гипертрофии лимфатического кольца глотки регистрируется у 11% детей. [1] [2] Превышение у детей индекса апноэ/гипопноэ более 5 эпизодов в час является показанием к хирургическому вмешательству.
В результате многочисленных исследований сделаны выводы:
- Тонзиллэктомия не даёт последствий на общий иммунитет.
- Астма и предрасположенность к аллергии у пациента не являются противопоказаниями к операции. Отягощающий эффект тонзиллэктомии на дальнейшую жизнь детей с атопией не доказан.
В настоящее время во многих лечебных учреждениях тонзиллэктомия выполняется под общей анестезией.
Техника операции заключается в выделении верхнего полюса миндалины с помощью скальпеля, ножниц или специального наконечника от электрохирургических приборов (коблатор, квазар, лазер и т. д). Затем миндалина отделяется от дужек и паратонзиллярной клетчатки тупым путём. На завершающем этапе операции нижний полюс миндалины отсекаю от подлежащих тканей.
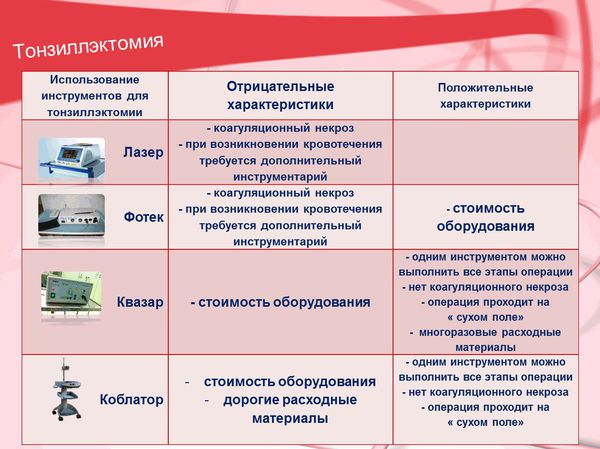
Противопоказания к тонзиллэктомии
- пороки сердца, гипертоническая болезнь;
- тяжёлая форма анемии, лейкоз;
- декомпенсированный сахарный диабет.
Лечение народными средствами
После консультации ЛОР-врача можно орошать глотку отваром ромашки и "Хлорофиллиптом" (препаратом, содержащим экстракт листьев эвкалипта). Эти средства используются только в комплексе с терапией, которую назначил доктор.
Прогноз. Профилактика
Профилактика хронического тонзиллита — это общегигиенические и санационные мероприятия. Она по праву считается действенной мерой вторичной профилактики заболеваний, в генезе которых важную роль играют ангины и хронический тонзиллит. Из общегигиенических мероприятий наиболее важны закаливание, рациональное питание, соблюдение правил гигиены жилища и рабочих помещений. Все больные с хроническим тонзиллитом должны обязательно находиться на диспансерном учёте у оториноларинголога.
Что такое острый тонзиллит? Причины возникновения, диагностику и методы лечения разберем в статье доктора Меркушин Д. Е., онколога со стажем в 12 лет.
Над статьей доктора Меркушин Д. Е. работали литературный редактор Елена Бережная , научный редактор Сергей Федосов
Определение болезни. Причины заболевания
Острый тонзиллит (Acute tonsillitis) — заболевание инфекционной природы с воздушно-капельным путем передачи, сопровождающееся выраженным синдромом общей интоксикации, местным проявлением которого служит воспаление одной или нескольких лимфатических фолликул глоточного кольца.
Острый тонзиллит вызывают бактериальные, вирусные и грибковые возбудители, а также бактериальные, вирусно-бактериальные, грибково-бактериальные ассоциации. Источником инфекции является больной или бактерионоситель.
Streptococcus pyogenes, Streptococcus группы A (GAS), является наиболее распространенной причиной бактериального фарингита у детей и взрослых. [1]
Прочие возбудители острого тонзиллита: [2]
- стафилококк (Arcanobacterium haemolyticum, Neisseria gonorrhoeae, Corynebacterium diphtheriae);
- анаэробы (синегнойная палочка);
- микоплазмы (m. Pneumoniae);
- хламидии;
- аденовирусы 1–9 типа;
- энтеровирус Коксаки;
- вирус простого герпеса;
- вирус гриппа;
- вирус Эпштейн-Барра и др.
Среди микозов наиболее часто развитие острого тонзиллита вызывают грибы рода Candida в симбиозе с патогенными и условно патогенными кокками.
Язвенно-некротическая тонзиллит вызывается спирохетой Плаута-Венсана в симбиозе с веретенообразной палочкой Венсана.
При обнаружении схожих симптомов проконсультируйтесь у врача. Не занимайтесь самолечением - это опасно для вашего здоровья!
Симптомы острого тонзиллита
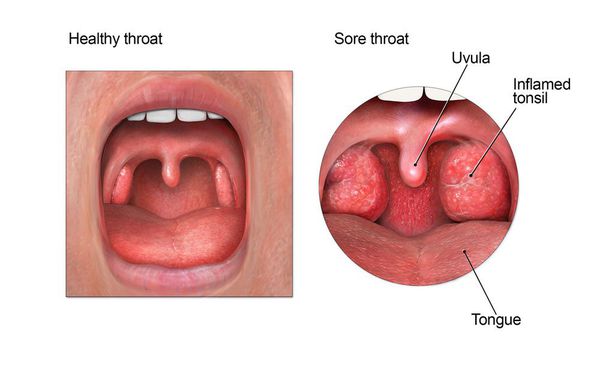
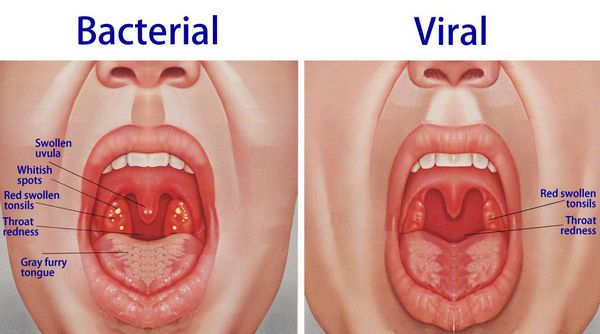
Осмотр глотки позволяет выявить характерные для заболевания изменения.
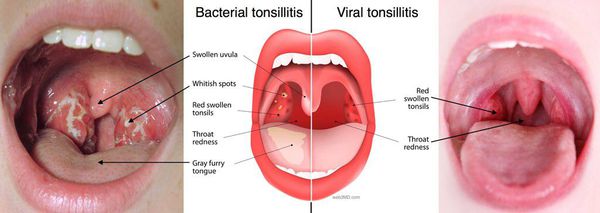
При катаральной форме заболевания миндалины увеличены, гиперемированы, наблюдается отек и гиперемия мягкого нёба и нёбных дужек. Налета на поверхности миндалин при этом не выявляется. При фолликулярном тонзиллите воспалительный процесс запускается в мелких лимфаденоидных фолликулах, происходит их нагноение, а потом вскрытие. Осмотр глотки в разгар заболевания выявляет на поверхности миндалин нечётко оформленные желтовато-белые точки.
Лакунарный тонзиллит характеризуется появлением в устьях лакун налётов или экссудата, выступающего на поверхность и покрывающего миндалину в виде островков, трудно удаляемого и оставляющего после себя кровоточащую изъязвленную поверхность.
Следствием фолликулярного и лакунарного тонзиллита может быть фибринозная форма заболевания, когда поверхность миндалин сплошь покрывается налетом.
Если возбудитель проникает в паратонзиллярную клетчатку и формируется инфекция мягких тканей, это может привести к флегмонозному тонзиллиту. Данная форма заболевания сопровождается нарастанием интоксикации, усилением боли в горле, появлением асимметричного отека и увеличением шеи, затруднением в наклоне и поворотах головы, появлением характерного неприятного запаха изо рта. По межфасциальным пространствам шеи гнойный процесс может опуститься до уровня клетчатки средостения и вызвать развитие медиастинита.
Для тонзиллита вирусного происхождения (вирус Коксаки типа А) характерны герпетические высыпания на миндалинах, мягком нёбе и нёбных дужках.
При аденовирусном тонзиллите воспалительный процесс в ротоглотке помимо миндалин распространяется на поверхность нёба, задней стенки глотки.
Такая форма острого тонзиллита, как ангина Симановского–Венсана чаще поражает одну миндалину в виде некротических изъязвлений, которые покрыты серым налетом. Признаки интоксикации при этом выражены слабо.
Для острого тонзиллита при системных заболеваниях кровеносной системы характерен некроз слизистой оболочки миндалин, распространение которого может привести к разрушению не только самой миндалины, но и мягкого нёба и стенок глотки с последующим рубцеванием дефекта. Тяжелое общее состояние больного обычно обусловлено течением основного заболевания. [3]
У маленьких детей (особенно у мальчиков) острый тонзиллит, вызванный стрептококками группы А, помимо прочего, может проявляться в виде желудочно-кишечных симптомов (боль в животе, тошнота и рвота). [8]
Патогенез острого тонзиллита
Врожденные и адаптивные иммунные ответы организма являются основополагающими для защиты от стрептококкового фарингита. Иммунные реакции организма также способствуют тяжелым постстрептококковым иммунным заболеваниям. Однако до недавнего времени о них было мало известно.
Клеточные медиаторы врожденного иммунитета, используемые при защите организма от стрептококка группы А, включают эпителиальные клетки, нейтрофилы, макрофаги и дендритные клетки (ДК), которые выделяют ряд растворимых воспалительных медиаторов, таких как антимикробные пептиды (AMP), эйкозаноиды, включая PGE2 и лейкотриен B4 (LTB4), хемокины и провоспалительные цитокины. Ответы Th1 и Th17 играют значительную роль в адаптивном иммунитете в тканях миндалин человека. [9]
Классификация и стадии развития острого тонзиллита
Выделяют три типа заболевания:
- первичные;
- вторичные;
- специфические тонзиллиты.
Возникновение вторичных связано с общими острыми инфекционными заболеваниями (скарлатина, дифтерия и т. д) и системными заболеваниями кровеносной системы (агранулоцитоз, лейкоз).
Специфические тонзиллиты возникают на фоне специфической инфекции (язвенно-пленчатый тонзиллит — ангина Симановского — Плаута — Венсана, вызываемая находящимися в симбиозе веретенообразной палочкой Плаута — Венсана и спирохетой Венсана, герпетический тонзиллит, вызываемый вирусом Коксаки А).
По форме выделяют:
- катаральный;
- фолликулярный;
- лакунарный;
- фибринозный;
- герпетический;
- флегмонозный (интратонзиллярный абсцесс);
- язвенно-некротический (гангренозный);
- смешанные формы тонзиллита.
Осложнения острого тонзиллита
Осложнения заболевания подразделяются на ранние и поздние.
Ранние осложнения возникают из-за распространения инфекции за пределы лимфоидной ткани и нарастания симптомов интоксикации (паратонзиллярный абсцесс, медиастинит, септические состояния, инфекционно-токсический шок, менингит и менингоэнцефалит).
В поздние сроки (через 2-4 недели) возможно развитие острой ревматической лихорадки и поражения почек в виде гломерулонефрита, реактивного артрита, провокация дебюта или обострение уже имеющихся системных аутоимунных заболеваний (красная волчанка, системный васкулит). [10]
Диагностика острого тонзиллита
Помимо общеклинического минимума, в который входят ОАК, ОАМ, ежегодное флюорографическое исследование, обязательным является:
- определение антистрептолизина-O в сыворотке крови;
- взятие мазка из зева и носовых ходов на корнебактерию дифтерии;
- взятие мазка на определение чувствительности микроорганизмов к антибиотикам.
Другие методы диагностики:
- в большинстве случаев показано проведение ЭКГ;
- в некоторых случаях обоснованным будет назначение серологического исследования на вирусы респираторных инфекций;
- молекулярно-биологическое исследование крови на вирус Эпштейна — Барр;
- микроскопическое исследование мазков с миндалин на гонококк;
- бактериологическое исследование слизи с миндалин и задней стенки глотки на анэробные микроорганизмы;
- микологическое исследование носоглоточных смывов на грибы рода кандида;
- определение С-реактивного белка.
Хотя фарингит группы A Streptococcus (GAS) является наиболее распространенной причиной бактериального фарингита у детей и подростков, многие вирусные и бактериальные инфекции имитируют симптомы фарингита. Экстренные клиницисты должны признать симптоматику фарингита GAS и использовать соответствующие средства диагностики и лечения для эффективного лечения антибиотиками.
У людей с острым фарингитом проводится дифференциальная диагностика между фарингитом, вызванным гемолитическим стрептококком А, инфекционным мононуклеозом и другими причинами вирусного фарингита. [11]
Лечение острого тонзиллита
При наличии показаний к госпитализации пациенту выдается направление на госпитализацию в круглосуточный стационар инфекционной больницы. При лечении в амбулаторных условиях на следующий день участковому терапевту в поликлинику по месту прикрепления пациента передается заявка на активное посещение на дому.
Необходима изоляция пациента, частое проветривание помещения, влажная уборка, производится ультрафиолетовое облучение воздуха в помещении с пациентом. Пациенту выдается отдельный набор посуды, недопустимо пользоваться общими полотенцами, зубными щетками.
В период повышения температуры пациенту показан полупостельный режим, по мере стихания синдрома интоксикации и лихорадки — палатный (до 7-го дня нормальной температуры тела). Пациенту показано обильное теплое питье не менее 1,5-2,0 л жидкости в сутки. При терапии в условиях стационара показано введение физиологического раствора с аскорбиновой кислотой для уменьшения симптомов интоксикации. При повышении t тела выше 38 градусов необходимо ее снижение приемом 500 мг парацетомола, 200-400 мг ибупрофена или 500 мг парацетомола в сочетании с 200 мг ибупрофена (препараты ибуклин, брустан). При неэффективности оказанных мер возможно внутримышечное введение литической смеси (анальгин 50% 1 мл + димедрол 1% 1 мл), преднизолона в дозе 30-60 мг (1-2 мл).
Пациенту назначается полоскание горла растворами антисептиков. На фармацевтическом рынке существуют распространенные, доступные по стоимости и в то же время эффективные антисептики с широким спектром активности и низкой резистентностью микроорганизмов к ним. К таким препаратам относят хлоргексидин, мирамистин, Йокс.
Антибактериальное (бактерицидное) действие раствора Йокс реализуется за счет йода в его составе. Раствор разводится из расчета 5 мл (1 чайная ложка) на 100 мл воды. Ополаскивать горло не менее 4 раз в сутки. Перед нанесением спрея прополоскать горло обычной водой для удаления слизи. Наносить спрей не менее 4 раз в сутки.
Обязательным является назначение этиотропного препарата для борьбы с возбудителем тонзиллита. В амбулаторно-поликлинических условиях наиболее удобным является пероральное назначение препаратов, в стационаре рационально парентеральное введение. [4]
При подтверждении роли корнебактерии дифтерии в развитии заболевания основное значение имеет введение лошадиной противодифтерийной сыворотки. Перед введением основной терапевтической дозы двукратно проводится биологическая проба. На первом этапе вводят 0,1 мл разведённой сыворотки из ампулы, маркированной красным цветом, внутрикожно в сгибательную поверхность предплечье руки. При правильном введении на коже образуется небольшой, плотный на ощупь узелок. В предплечье второй руки вводят в/к 0,1 мл физиологического раствора в качестве контроля. Время наблюдения за пациентом составляет 20 минут. Проба считается отрицательной, если диаметр папулы или гиперемии в месте введения не более 10 мм. На втором этапе 0,1 мл неразведенной сыворотки, маркированной синим цветом, вводят подкожно в наружную поверхность плеча. При отсутствии неблагоприятной реакции через 30 минут внутримышечно вводится основная доза препарата.
Разовая доза сыворотки составляет:
- при локализованных формах 10 000 – 20 000 МЕ;
- дифтерии гортани 40 000 – 50 000 МЕ;
- при субтоксической форме 40 000 – 50 000 МЕ;
- токсической 50 000 – 80 000 МЕ;
- геморрагической 100 000 – 120 000 МЕ.
При отсутствии терапевтического эффекта введение сыворотки можно повторить через 12-24 часа с использованием тех же доз. [5]
Из антибактериальных препаратов рекомендуется назначение макролидов — кларитромицина, мидекамицина или джозамицина:
- Кларитромицин рекомендован в дозировке 500 мг однократно в сутки внутрь длительностью не менее 7-10 дней.
- Мидекамицин в дозировке 400 мг 3 раза в сутки внутрь не менее 7-10 дней.
- Джозамицин применяется в дозировке 500-1000 мг двукратно в сутки внутрь. Длительность терапии не менее 7-10 дней.
Терапия гонококкового тонзиллита проводится в условиях кожно-венерологического диспансера. Назначается 0,5 мг цефтриаксона внутримышечно или 0,5 мг внутрь левофлоксацина однократно внутрь. В связи с высоким риском сопутствующей хламидийной инфекции совместно с цефалоспоринами назначают доксициклин, 600 мг. препарата назначается в 2 приема с интервалом 1 час (по 3 таблетки 100 мг 2 раза).
При общих вирусных инфекциях (инфекционный мононуклеоз, генерализованная герпетическая инфекция, тяжелое течение гриппа) развитие острого тонзиллита, как правило, связано с активацией условно патогенной флоры ротоглотки. Помимо противовирусной терапии назначаются антибиотики, как и в случае с обычным первичным бактериальным тонзиллитом.
Препаратами первой линии являются клавулированные пенициллины. Применение неклавулированного пенициллина для терапии инфекции верхних дыхательных путей не рекомендовано в связи с высокой резистентностью микрофлоры к данному антибактериальному препарату. [7]
Амоксициллина клавулонат принимается в дозировке 875+125 мг 3-4 раза в сутки внутрь не менее 7 дней.
Цефалоспорины 2-3 поколения и макролиды
Цефалоспорины II поколения:
Цефуроксим в таблетках по 250 мг назначается из расчета по 1 таблетке 2 раза в сутки внутрь;
Цефалоспорины III поколения:
- Цефиксим в таблетках по 400 мг назначается из расчета по 1 таблетке 1 раз в день внутрь;
- Цефотаксим во флаконах по 1 гр в/м на 2 мл 2% лидокаина, добавив для лучшего растворения 1 мл NaCI 0,9% 2 раза в сутки; возможно в/в капельное введение в течение по крайней мере 30 мин;
- Цефтриаксон флаконы по 1,0 гр в/м на 2 мл 2% лидокаина, добавив для лучшего растворения 1 мл NaCI 0,9% 2 раза в сутки; возможно в/в капельное введение в течение по крайней мере 30 мин.
В качестве препаратов резерва в большинстве случаев применяются фторхинолоны, карбапенемы и линкозамины. Антибиотики тетрациклинового ряда ушли из практики в связи с высокой устойчивостью флоры к ним и невозможностью применения у беременных и в педиатрической практике.
Для предупреждения развития кандидоза в индивидуальном порядке решается вопрос о назначении противогрибкового препарата.
Для терапии же грибкового тонзиллита назначение системных антимикотиков является обязательным. Она включает пероральное применение противогрибковых антибиотиков в течение 10–14 дней (леворин, нистатин, амфотерицин В, кетоконазол, флуконазол). Местно назначаются полоскания антисептиками и ингаляции с мирамистином.
При необходимости пациенту выдается листок нетрудоспособности или справка учащегося с освобождением от труда и посещения занятий соответственно. [6]
Ориентировочные сроки нетрудоспособности:
Средние сроки временной нетрудоспособности составляют 10-12 дней.
Критерии выздоровления:
- нормализация температуры тела в течение 5 суток;
- отсутствие боли в горле и болезненности при пальпации поднижнечелюстных лимфатических узлов;
- отсутствие патологических отклонений в общем анализе крови, общем анализе мочи и на пленке ЭКГ.
Возможно предоставление записки от лечащего врача работодателю в произвольной форме о переводе на облегченный труд и освобождении от ночных смен на 2 недели при возможности. Студентам и школьникам предоставляется освобождение от занятий физкультурой на 2 недели. [6]
Прогноз. Профилактика
При своевременно начатой терапии прогноз благоприятный. При применении современных методов диагностики и качественных антибактериальных препаратов ранние и поздние осложнения заболевания встречаются спорадически (при позднем обращении и самолечении пациента).
Рекомендуется избегать переохлаждений и контакта с больными ОРЗ, вакцинация против гриппа и пневмонии, общеукрепляющие мероприятия. В качестве средства профилактики обострений фарингита и рецидивирующего тонзиллита оказались эффективными препараты бактериального происхождения, в частности, комплексы антигенов — лизатов, наиболее частых возбудителей воспалительных заболеваний верхних дыхательных путей, полости рта и глотки.
К таким препаратам относится ИРС-19 по 1 дозе препарата в каждый носовой ход 2 раза в день в течение 2 недель в периоды межсезонья и перед ожидаемыми вспышками эпидемий ОРЗ.
Имудон по 6 таблеток в день. Таблетки рассасывают (не разжевывая) каждые два часа. Курс терапии составляет 20 дней.
За реконвалесцентами устанавливают патронажное медицинское наблюдение в течение месяца. На первой и третьей неделе проводится исследование анализов крови и мочи, при необходимости — ЭКГ-исследование.
Все пациенты с хроническим тонзиллитом, которые перенесли более двух ангин за последние три года, подлежат обязательному диспансерному наблюдению по группе Д3 (2 раза в год).
Читайте также:

