Идентификация возбудителя сибирской язвы
Обновлено: 16.04.2024
Использование современных генно-инженерных методов позволяет не только провести идентификацию сибиреязвенных штаммов, выделенных из почвы, но и осуществить сравнительные молекулярно-генетические исследования этих штаммов. Проведено лабораторное исследование 80 проб земли, взятых из старого скотомогильника, с использованием микробиологических и генетических методов. Эпидемическую значимость выделенных штаммов оценивали по результатам ПЦР с видоспецифическими праймерами и по данным многолокусного VNTR-анализа. Выделено шесть штаммов, три из которых отнесены к B. anthracis, а остальные − к близкородственным бациллам. Показана принципиальная возможность использования данной комплексной методики для типизации сибиреязвенных штаммов и их дифференциации от близкородственных микроорганизмов.
Ключевые слова
Об авторах
Список литературы
1. Лабораторная диагностика и обнаружение возбудителя сибирской язвы. Методические указания. МУК 4.2.2413-08. М.: Федеральный центр гигиены и эпидемиологии Роспотребнадзора; 2009. 67 с.
2. Обеззараживание исследуемого материала, инфицированного бактериями I-IV групп при работе методом ПЦР. Методические указания. МУ 3.5.5.-1034-01. М: МЗ РФ; 2001. 8 с.
4. Кутырев В.В., Смирнова Н.И. Генодиагностика и молекулярное типирование возбудителей чумы, холеры и сибирской язвы. Мол. генет., микробиол., вирусол. 2003; 1:6-14.
5. Цыганкова О.И., Еременко Е.И., Цыганкова Е.А. и др. Фенотипические и генетические особенности культурально-морфологических вариантов Bacillus anthracis Журн. микробиол., эпидемиол. и иммунобиол. 2008; 4:6-11.
6. Helgaso E., Okstad O.A., Caugant D.A., Johansen H.A, Fouet A., Mock M. et al. Bacillus anthracis, Bacillus cereus, and Bacillus thuringiensis: one species on the basis of genetic evidence. Appl. Environ. Microbiol. 2000; 66:2627-30.
8. Patra G., Sylverste P., Ramisse V. et al. Specific oligonucleotide primers for rapid identification of Bacillus anthracis strains. Proc. Inter. Workshop on Anthrax. Winchester, England, September 19-21, 1996. P. 45-6.
Возбудитель сибирской язвы. Механизмы развития сибирской язвы
Возбудитель- Bacillus anthracis- крупная грамположительная спорообразующая палочка с обрубленными концами размерами до 3-10 мкм в длину и 2 мкм в ширину, неподвижная, располагается в окрашенных препаратах цепочками. В организме животных и человека существует в вегетативной форме, способной к образованию капсул, а во внешней среде - в споровой форме, сохраняющейся годами и десятилетиями, создавая стойкий резервуар инфекции.
Допускается возможность при благоприятных условиях их прорастания и размножения, что потенциально опасно, особенно при попадания возбудителя в воду или в воздух в облаке пыли (болезнь тряпичников). Вирулентность возбудителя связывают с капсульным антигеном, способным подавлять фагоцитарную активность лейкоцитов. Кроме того, возбудитель вырабатывает сильный экзотоксин, состоящий из трех патогенетических факторов белковой природы, отечного, летального и протективного (последний активирует патогенное действие двух других), равно как и вырабатываемые возбудителем протеолитические ферменты.
Оптимальная температура роста возбудителя +32-37°С в нейтральной среде. Вегетативные его формы гибнут при нагревании до 75-80°С в течение минуты, тогда как низкие температуры длительно сохраняют их активность. Споры при кипячении гибнут через 45-60 мин; сухой жар убивает их за 3 ч. Хорошо сохраняются в засоленном мясе, дубленых шкурах; устойчивы к действию дезинфицирующих средств.
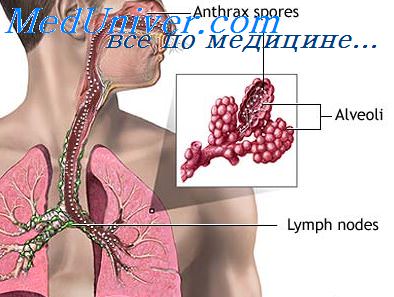
При прорыве лимфатического барьера по причине незавершенности фагоцитоза молниеносно развивается геморрагическая септицемия, которая проявляется массивной бактериемией, тяжелой интоксикацией, полиорганными поражениями (отек легких, пневмония, плеврит, медиастинит, менингит и др.), развитием инфекционно-токсического шока (ИТШ) и тромбогеморрагического синдрома (ТГС).
При внедрении возбудителя через дыхательные пути и пищеварительный канал он также размножается в месте проникновения и регионарных ЛУ (медиастинальных, брыжеечных), прорывается в кровь, вызывая геморрагическую септицемию с последующим развитием ИТШ и ТГС. Поражения легких и кишечника в этих случаях носят преимущественно вторичный характер.
Встречаются редкие случаи, когда возбудитель не оставляет следа (при заражении через кожу и слизистую оболочку губ) на месте внедрения и болезнь манифестируется развитием молниеносной геморрагической септицемии (смерть наступает внезапно, в течение нескольких часов и даже десятков минут).
В месте внедрения возбудителя любой локализации развивается серозно-геморрагическое воспаление с резчайшим студневидным геморрагическим отеком и некрозом тканей со скоплением большого количества сибиреязвенных палочек в кровеносных сосудах При внедрении в кожу, обычно на открытых (незащищенных одеждой) участках, чаще рук и лица, образуется типичного вида сибиреязвенный карбункул
При патологоанатомическом исследовании находят выраженное полнокровие органов с жидкой, несвертывающейся кровью. Всюду картина серозно-геморрагического воспаления и резкого отека тканей, включая мозговые оболочки. В тонкой кишке иногда удается обнаружить очаги геморрагического воспаления с изъязвлением и некрозом, с ближайшим геморрагическо-некротическим поражением брыжеечных лимфоузлов. Селезенка, как и при всяком сепсисе, увеличена, дряблая, с обильным соскобом
У переболевших и выздоровевших остается продолжительный иммунитет, повторные заболевания сибирской язвой возможны, но встречаются редко.
При росте В anthracis в МПБ среда остается прозрачной, на дне осадок в виде ватообразных хлопьев (типичный рост), иногда возможен диффузный рост.
На дифференциально-диагностической среде отбирают для изучения колонии бактерий с отрицательной реакцией на щелочную фосфатазу. Для этого в крышку чашки Петри с посевами наливают 1-2 мл 25%-ного водного раствора аммиака. Закрытую чашку (крышкой вниз) выдерживают 1 минуту при комнатной температуре, затем просматривают под малым увеличением микроскопа. Отбирают для изучения все бесцветные колонии (нет щелочной фосфатазы) и не исследуют порозовевшие колонии.
На средах Томова и Буза колонии S или SM-формы гладкие, блестящие, слизистой консистенции. Среда Томова обладает селективными свойствами, на ней растет В. cereus, но не растут В. subtilis, В. megaterium.
Рост В. anthracis в системе для диск-преципитации сопровождается через 16-20 часов образованием в средней части столбика агарового геля тонкой белой линии преципитации (диск). Антигенно-родственные виды бацилл (В. cereus) могут образовывать в нижней части агарового столбика (на границе с иммунной сывороткой) более толстую, рыхлую зону преципитации. Для изучения отвивают культуры, давшие при росте зону преципитации.
Морфология и тинкториальные свойства В. anthracis в культуре. Из подозрительных колоний, бульонных культур, систем для диск-преципитации (при наличии преципитации) делают мазки и окрашивают по Граму люминесцирующими сыворотками.
При обнаружении в окрашенных препаратах бактерий с характерными для В. anthracis морфологическими и тинкториальными свойствами культуры отвивают на МПА, МПБ, можно на систему для диск-преципитации с целью дальнейшего изучения. Смешанные культуры дробно рассевают на МПА в чашках Петри или заражают белых мышей для получения чистой культуры возбудителя.

Биопроба. Проводят одновременно с посевом материала на питательные среды. Исследуемый материал суспендируют в небольшом объеме стерильного физиологического раствора, 0,2-0,5 мл взвеси вводят двум белым мышам подкожно в область спины или 0,5-1,0 мл двум морским свинкам подкожно в область живота. Наблюдение за животными ведут в течение 10 суток, гибель в положительных случаях обычно наступает через 1-3 суток. Павших животных подвергают полному бактериологическому исследованию.
Гибель хотя бы одного из двух зараженных лабораторных животных и выделение культуры возбудителя из его органов является основанием для постановки положительного диагноза.
Если чистая культура возбудителя получена ранее гибели животных, зараженных исследуемым материалом, то, не дожидаясь результатов биопробы, проверяют патогенность выделенной бактерии путем заражения двух белых мышей суточной бульонной культурой.
При исследовании материала от свиней, с учетом штаммовых вариаций по вирулентности, необходимо заразить до 10 мышей, а наблюдение продолжать за зараженными животными до 10-20 дней.
У штаммов В. anthracis вирулентность может варьировать в широких пределах. Для оценки свойств штаммов представляют интерес критерии по определению типа В.anthracis, предложенные Dong Shulin (цит. по Бакулову И.А. и соавт., 2001). Те или иные свойства штамма связаны с присутствием в клетках плазмид, детерминирующих синтез факторов вирулентности. С точки зрения диагностики существенны следующие фенотипические признаки В.anthracis, обусловливаемые плазмидами: наличие капсулы, токсина, патогенность для животных и форма колоний. С целью установления типа штамма испытуемую культуру засевают на плотную и жидкую питательные среды с 50% сыворотки крови барана или кролика и 0,9% NaHCО3. Посевы инкубируют при 37° С в атмосфере 10-12% С02 в течение 24 часов. На плотных средах, в зависимости от характеристик штамма, могут формироваться колонии R-, S- и М-формы, клетки бактерий могут быть капсулированы или нет, в культуральной жидкости может присутствовать или отсутствовать экзотоксин, культуры могут быть патогенными или непатогенными для животных. Согласно Dong Shulin штаммы по этим критериям подразделяются на четыре типа.
1-й тип. Вирулентный штамм. Колонии М-формы, есть капсула, токсин (культуральный фильтрат при внутрикожном введении кроликам или морским свинкам вызывает образование отека) выявляется в РДП, культура патогенна для животных. Такие свойства обусловлены наличием плазмид рх01и рх02.
2-й тип. Вакцинный штамм. Колонии R-формы, капсулы нет, токсин есть, культура не патогенна для животных. Имеется плазмида рх01.
3-й тип. Авирулентный штамм. Колонии М-формы, есть капсула, токсина нет, культура патогенна для животных. Присутствует плазмида рх02.
4-й тип. Непатогенный штамм. Колонии S-формы, капсулы и токсина нет, культура не патогенна для животных. Плазмиды отсутствуют.
Дифференциация возбудителя сибирской язвы от сапрофитных бацилл. В том случае, когда в мазках из исследуемого материала обнаруживают капсулированные бактерии с типичными для В. anthracis морфологическими и тинкториальными свойствами, а при посеве на питательные среды выделяют характерные по культуральным и морфологическим свойствам бактерии, то дальнейшее изучение культуры не проводят и диагноз считают установленным.
При необходимости дифференциации выделенной культуры от сапрофитных бацилл также дополнительно определяют у нее способность к капсулообразованию в опытах in vitro, in vivo, рост в аэробных, анаэробных условиях, наличие жгутиков, гемолитическую активность, синтез лецитиназы, уреазы, реакцию Фогес-Проскауера, образование кислоты из арабинозы, ксилозы, гидролиз желатина, крахмала. Самыми надежными методами идентификации В. anthracis считаются тест на фагочувствительность, обнаружение в ПЦР-генов, кодирующих синтез токсина и капсулы, наличие патогенных свойств.
Некоторые из перечисленных методов исследования изложены ниже.
Определение вирулентности культур В. anthracis на кроликах. Используют кроликов массой 2-2,5 кг. Исследуемый штамм выращивают на МПБ (24 часа), затем засевают на МПА, агар Хоттингера, культивируют 3-4 дня при 37° С. Путем микроскопии окрашенных мазков контролируют уровень спорообразования.
Когда он достигает 90-100%, бактериальную массу смывают физиологическим раствором и по стандарту мутности готовят взвеси с содержанием 1 млн, 100 тыс. и 1000тыс. спор в 1 мл. Каждой взвесью в объеме 1 мл заражают подкожно в область живота двух кроликов, наблюдение ведут в течение 10 суток.
Слабо вирулентные и авирулентные штаммы не вызывают гибели кроликов при любой дозе; умеренно вирулентные штаммы вызывают гибель животных при дозах 1 млн. - 100 тыс. спор; высоко вирулентные штаммы обусловливают гибель при дозе 10 тыс. спор.
Метод применяют для изучения штаммов, выделенных из объектов внешней среды.
Метод обнаружения капсулообразования in vivo. Бульонную культуру в дозе 0,1-0,2 мл вводят внутрибрюшинно 6-8 белым мышам. Животных убивают через 1,2 и 3 часа, вскрывают, из перитонеального экссудата и органов делают мазки, окрашивают одним из методов на капсулу и микроскопируют.
Метод обнаружения капсулообразования in vitro. Испытуемую культуру высевают на среду ГКИ, Шляхова, пробирки закрывают резиновыми пробками, культивируют при 37 С С. Через 0,5-2 часа у части, а через 15-18 часов у большинства клеток обнаруживают капсулу.
Сибирская язва (Anthrax) - зооантропоноз. К ней восприимчивы животные многих видов, особенно травоядные, и человек. Болезнь протекает преимущественно остро с явлениями септицемии или с образованием различной величины карбункулов. Регистрируют в виде спорадических случаев, возможны энзоотии и эпизоотии.
Возбудитель сибирской язвы - Bacillus anthracis (Cohn, 1872) - относится к семейству Bacillaceae.
Морфология.

Bacillus anthracis неподвижная, грамположительная (в молодых и старых культурах встречаются и грамотрицательные клетки), образующая капсулу (в организме или при культивировании на искусственных питательных средах с большим содержанием нативного белка и СО2) и спору палочка, размером 1-1,3 х 3,0-10,0 мкм. При температуре ниже 12 и выше 42 оС, а также в живом организме или невскрытом трупе, в крови и сыворотке животных споры не образуются. В окрашенных препаратах из крови и тканей больных или погибших от сибирской язвы животных бактерии располагаются одиночно, попарно и в виде коротких цепочек по 3-4 клетки; концы палочек, обращенных друг к другу, прямые, резко обрубленные, свободные - слегка, закругленные. Иногда цепочки имеют форму бамбуковой трости.В мазках из культур на плотных и жидких питательных средах палочки располагаются длинными цепочками.
Культивирование.
Биохимические свойства.
Ферменты Bacillus anthracis: липаза, диастаза, протеаза, желатиназа, дегидраза, цитохромоксидаза, пероксидаза, каталаза, лецитиназа и др.Ферментирует с образованием кислоты без газа глюкозу, мальтозу, сахарозу, трегалозу, фруктозу и декстрин. На средах с глицерином и салицином возможно слабое кислотообразование. Арабинозу, рамнозу, галактозу, маннозу, раффинозу, инулин, маннит, дульцит, сорбит, инозит не сбраживает. Утилизирует цитраты, образует ацетилметилкарбинол (реакция Фогеса - Проскауэра положительная). Выделяет аммиак. Редуцирует метиленовый синий и восстанавливает нитраты в нитриты. Некоторые штаммы образуют сероводород.
Токсинообразование.
Bacillus anthracis образует сложный экзотоксин, состоящий из трех компонентов: эдематогенный фактор (ЕF), протективный антиген (РА) и летальный фактор (LF) или факторы I, II, III. Эдематогенный фактор вызывает местную воспалительную реакцию - отек и разрушение тканей. Протективный антиген - носитель защитных свойств, обладает выраженным иммуногенным действием. Летальный фактор в смеси со протективным вызывает гибель крыс, белых мышей и морских свинок.Каждый из трех факторов обладает выраженной антигенной функцией и серологически активен.Инвазивные свойства микроба обусловлены капсульным полипептидом d-глутаминовой кислоты и экзоферментами.
Антигенная структура.
В состав антигенов Bacillus anthracis входят неиммуногенный соматический полисахаридный комплекс и капсульный глутаминполипептид. Полисахаридный антиген не создает иммунитета у животных и не определяет агрессивных функций микроорганизма.
Устойчивость.
В невскрытом трупе вегетативная клетка микроба разрушается в течение 2-3 сут, в зарытых трупах сохранятся до 4 дней. В замороженном мясе при минус 15 o С жизнеспособна 15 дней, в засоленном мясе - до 1,5 мес. В навозная жиже, смешанной с сибиреязвенной кровью, погибает через 2-3 ч, споры же остаются в ней вирулентными в течение месяцев. В запаянных ампулах с бульонными культурами могут оставаться жизнеспособными и вирулентными до 63 лет, в почве - более 50 лет.Спирт, эфир, 2 %-ный формалин, 5 %-ный фенол, 5-10 %-ный хлорамин, свежий 5 %-ный раствор хлорной извести, перекись водорода разрушают вегетативные клетки в течение 5 мин. Этиловый спирт 25-100 % убивает споры в течение 50 дней и более, 5 %-ный фенол, 5-10%-ный раствор хлорамина - от несколько часов до нескольких суток, 2 %-ный раствор формалина - через 10-15 мин, 3%-ный раствор перекиси водорода - через 1 ч, 4 %-ный раствор перманганата калия - через 15 мин, 10 %-ный раствор гидроокиси натрия - через 2 ч.Вегетативные клетки при нагревании до 50-55 o С гибнут в течение 1 ч, при 60 o С - через 15 мин, при 75 o С - через 1 мин, при кипячении - мгновенно.При медленном высушивании наступает спорообразование и микроб не гибнет. При минус 10 o С бактерии сохраняются 24 дня, при минус 24 o С - 12 дней.Воздействие прямого солнечного света обезвреживает бактерии через несколько часов.Сухой жар при температуре 120-140 o С убивает споры через 2-3 ч, при 150 o С - через 1 ч, текущий пар при 100 o С - через 12-15 мин, автоклавирование при 110 o С - за 5-10 мин, кипячение - через 1 ч.Возбудитель сибирской язвы проявляет высокую чувствительность к пенициллину, хлортетрациклину и левомицетину, а также к лизоциму. Бактериостатическим эффектом на протяжении 24 ч обладает свежевыдоенное молоко коров.
Патогенность.
К возбудителю сибирской язвы восприимчивы все виды млекопитающих. Чаще болеют овцы, крупный рогатый скот, лошади, козы, буйволы, верблюды и северные олени, могут заражаться ослы и мулы. Свиньи менее чувствительны. Среди диких животных восприимчивы все травоядные. Известны случаи заболевания собак, волков, лисиц, песцов, среди птиц - уток и страусов.
Патогенез.
Заражение животных происходит преимущественно алиментарно. Через поврежденную слизистую пищеварительного тракта микроб проникает в лимфатическую систему, а затем в кровь, где фагоцитируется и разносится по всему организму, фиксируясь в элементах лимфоидно-макрофагальной системы, после чего снова мигрирует в кровь, обусловливая септицемию.Капсульное вещество ингибирует опсонизацию, в то время как экзотоксин разрушает фагоциты, поражает центральную нервную систему, вызывает отек, возникает гипергликемию и повышается активность щелочной фосфатазы.В терминальной фазе процесса в крови снижается содержание кислорода до уровня, несовместимого с жизнью.
Лабораторная диагностика.
Не патогенны для лабораторных животных, за исключением B.cereus (при внутрибрюшинном заражении белых мышей).

Образует массивную с четкими контурами капсулу.
На агаре с пенициллином возбудитель растет в виде цепочек, состоящих из шарообразных форм, напоминающих ожерелье из жемчуга.
Читайте также:

