Иммунитет при паразитарных инфекциях
Обновлено: 26.04.2024
Инфекционные заболевания у пациентов со сниженным иммунитетом. Инфекции при иммунодефиците
Различные методы лечения или наследственная патология иммунной системы могут способствовать развитию инфекционного заболевания, обусловленного слабовирулентными штаммами микроорганизмов, или возникновению тяжёлых инфекций, связанных с патогенными возбудителями.
Недостаточность иммунной системы обычно возникает в результате воздействия нескольких факторов. Например, при нейтропении, развивающейся у пациентов, перенёсших пересадку костного мозга, повышена восприимчивость организма к бактериальным инфекциям, в то время как внутривенная катетеризация способствует развитию инфекции, вызванной Staphylococcus epidermidis.
Медицинские манипуляции часто нарушают физические барьеры на пути инфекции (например, катетеризация).
Нейтропения как причина инфекции при иммунодефиците
Гранулоцитопению обычно наблюдают при острой лейкемии или её лечении. Риск развития инфекции зависит от длительности и тяжести нейтропении. Бактериемию у таких больных обнаруживают в 40—70% случаев. Наиболее часто выделяют гра-мотрицательные бациллы (бактерии семейства Enterobacteriaceae и рода Pseudomonas). Они распространяются по организму в результате повреждения кишечника противоопухолевыми препаратами и облучением.
Кроме того, в этиологии сепсиса важную роль играют фамположительные микроорганизмы (S. epidermidis, S. mitis, S. oralis, S. aureus, Corynebacterium jeikeium и представители рода Enterococcus).
Несмотря на то что в большинстве случаев развитие кандидоза обусловлено приёмом антибактериальных препаратов, у пациентов с нейтропенией грибковые инфекции могут возникать de novo. В последнее время всё чаше сообщают о микозах, вызванных дрожжевыми грибами, такими как Candida krusei (характерна природная устойчивость к действию противогрибковых средств), различными видами родов Aspergillus (вызывают инвазивные заболевания) и Fusarium, а также Pseudallescheria boydii и Trichosporon beigelii.
Лечение лихорадки у пациентов с нейтропенией. Эмпирическая терапия включает карбапенем (или цефтазидим) и амикацин. Если лихорадка не исчезает, то дополнительно назначают гликопептидный антибиотик. Позже, если лихорадка сохраняется, высока вероятность развития микозов, поэтому для лечения используют амфотерицин В и итраконазол.
Профилактика инфекции у пациентов с нейтропенией. Вероятность развития инфекции у пациентов с нейтропенией заметно снижается, если в больнице их помещают в индивидуальный бокс и снабжают стерилизованной пищей и водой. Большое значение имеет соблюдение стерильного режима не только медицинским персоналом (мытьё рук и использование одноразовых резиновых перчаток), но и посетителями (ношение халатов и масок). Воздух, поступающий в палату, необходимо пропускать сквозь фильтр специальной очищающей от грибковых спор системы.
Приём нистатина и амфотерицина В внутрь позволяет снизить вероятность развития грибковой инфекции. Достаточно эффективные препараты — флуконазол и итраконазол. В некоторых медицинских центрах применяют профилактическую терапию 4-фторхинолонами, действие которых направлено против факультативных анаэробов кишечника (при сохранении анаэробной флоры).
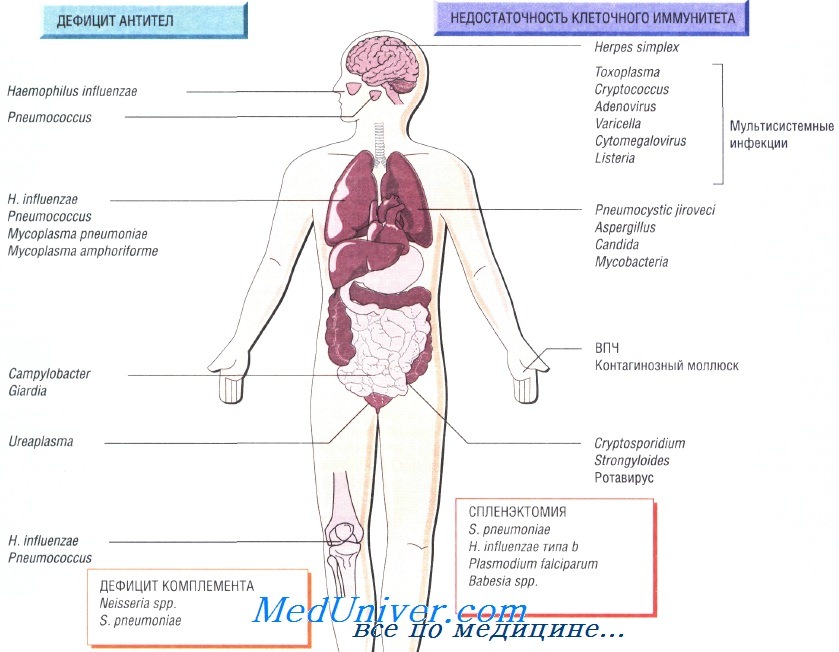
Причины инфекций при иммунодефиците
Недостаточность Т-клеточного иммунитета как причина инфекции при иммунодефиците
Недостаточность Т-клеточного иммунитета может быть обусловлена ВИЧ-инфекцией, противоопухолевой химиотерапией, приёмом глюкокортикоидных препаратов или трансплантацией органов. Врождённый дефицит обнаруживают достаточно редко. Он может быть связан только с недостаточностью функции Т-лимфоцитов или сопровождаться гипогаммаглобулинемией.
Возбудители инфекции при недостаточности Т-клеточного иммунитета. Основные возбудители — внутриклеточные патогенные микроорганизмы и паразиты:
• Toxoplasma gondii, Strongyloides stercoralis;
• Mycobacterium tuberculosis, M. avium-intracellulare;
• Listeria monocytogenes, Cryptococcus neoformans, Pneumocystis jiroveci;
• вирусы простого герпеса, цитомегаловирус, вирус опоясывающего герпеса и кори.
При осложнении кори гигантоклеточной пневмонией и энцефалитом у таких больных заболевание может приобрести угрожающий жизни характер.
Диагностика инфекции при недостаточности Т-клеточного иммунитета. Для диагностики инфекционных заболеваний применяют различные методы исследования. Для посева у пациентов отбирают не менее, чем два образца крови, взятых из разных мест.
Гиппогаммаглобулинемия как причина инфекции при недостаточности Т-клеточного иммунитета
Пациенты, страдающие сцепленной с Х-хромосомой агамма-глобулинемией, входят в группу повышенного риска заражения различными инфекциями в первые 6 мес своей жизни, в то время как люди с другим иммунодефицитом имеют повышенный риск на протяжении всей жизни. Функциональная гипогаммаглобулинемия возникает у больных с множественной миеломой.
Возбудителями рецидивирующих респираторных заболеваний у таких людей считают Streptococcus pneumoniae, недавно открытую Mycoplasma amphoriforme и не имеющего капсулы Haemophilus influenzae (вызывает бронхоэктазию). Персистирующие инфекции вызывают представители родов Giardia, Cryptosporidium и Campylobacter. Снизить частоту возникновения рецидивирующих инфекций помогает внутривенное введение иммуноглобулина.
Недостаточность комплемента как причина инфекции при недостаточности Т-клеточного иммунитета
Врождённую недостаточность комплемента наблюдают достаточно редко. Недостаточность последних компонентов системы комплемента (С7—С9) вызывает потерю способности лизировать грамотрицательные бактерии, в связи с чем повышается восприимчивость пациента к рецидивирующим инфекциям, вызванным микроорганизмами рода Neisseria. Недостаточность альтернативного пути системы комплемента приводит к развитию тяжёлых стрептококковых инфекций (S. pneumoniae), например менингита.
Приобретённая недостаточность системы комплемента часто возникает при системной красной волчанке.
Маннозасвязывающий лектин путь активации комплемента. Широкий спектр бактерий, грибов, вирусов и простейших прикрепляются к клеткам организма хозяина посредством маннозасвязывающего лектина. Есть данные, что при некоторых видах его недостаточности именно эти микроорганизмы вызывают наиболее частые и тяжёлые заболевания у людей с определёнными генотипами.
Инфекции возникающие после спленэктомии
Ежегодно после удаления селезёнки в 1% случаев наблюдают развитие тяжёлого сепсиса, при этом чаще всего заболевание возникает у младенцев и детей. Самую высокую смертность отмечают после спленэктомии, выполненной по поводу лимфомы и талассемии. У пациентов с серповидно-клеточной анемией развивается функциональная аспления. Риск развития сепсиса может со временем снизиться, но никогда не исчезнет окончательно.
Наиболее распространённый возбудитель инфекций (две трети всех случаев) — Streptococcus pneumoniae, но Н. influenzae и Е. coli также играют важную роль в этиологии инфекционных заболеваний у таких пациентов. Кроме того, спленэктомия повышает восприимчивость организма к инфекции, вызванной Capnocytophaga canimorsis (особенно после укусов собак). Малярия также может протекать крайне неблагоприятно (фульминантная форма).
Профилактика инфекции после спленэктомии. После удаления селезёнки всем пациентам необходимо провести вакцинацию, направленную против S. pneumoniae, менингококков и Н. influenzae типа В. Более эффективна иммунизация с использованием белковых конъюгированных вакцин. В некоторых случаях для профилактики применяют пенициллин V (в низких дозах).
Пациентов следует предупреждать о том, чтобы они сообщали своему лечащему врачу о любых признаках лихорадки, а также проинструктировать их относительно приёма антибиотиков (во избежание задержки лечения).
Редактор: Искандер Милевски. Дата обновления публикации: 18.3.2021
Как происходит заражение?
До попадания в организм человека, гельминты и простейшие проходят цикл развития в других средах или живых организмах.
- В почве при определённых условиях температуры и влажности сохраняются яйца и личинки аскарид, стронгилоид, анкилостом Человек заражается при попадании зараженной почвы через грязные руки, воду, непромытые фрукты и овощи, непосредственно с землёй.
- В живых организмах проходят циклы развития следующие гельминты: описторхи (кошачья двуустка), клонорхи, трихинеллы, токсокары, эхинококки, свиной и бычий цепень. До достижения зрелости, чтобы паразитировать в человеке, возможна смена одного или двух промежуточных хозяев. Это моллюски, ракообразные, рыба, насекомые. Употребление термически недостаточно обработанной рыбы и мяса, сырой воды приводит к заражению.
Ещё один путь заражения - при непосредственном контакте людей через рукопожатия, общие предметы гигиены и быта или путем самозаражения. Речь идёт о контагиозных гельминтах: энтеробиоз, стронгилоидоз, цистицеркоз, лямблиоз.
Как можно заподозрить паразитарное заболевание?
Проявления могут быть разнообразными, течение от легкого до тяжёлого. Редко возникают типичные признаки, выдающие конкретного возбудителя. Зачастую признаков нет, или они маскируются под другие заболевания, или исчезают по мере окончания одного цикла развития паразита и начала другого. Например, личинки аскарид сначала попадают в лёгкие человека, где дозревают и мигрируют в кишечник. Ребёнка может беспокоить недолгий кашель (похоже на простуду), не настораживающий родителя.
Тем не менее, обычно выделяют острую и хроническую фазы течения паразитарного заболевания.
Острые проявления возникают вследствие общего воздействия на организм:
- Влияния токсинов – повышение температуры до 37 – 37,5 градусов, слабость, головные боли, снижение настроения и работоспособности, нарушения сна;
- Аллергических реакций – кожный зуд, крапивница, бронхоспазм, одышка, реже отёк Квинке;
- Активации иммунной системы– боли в мышцах и суставах; увеличение лимфоузлов, печени и селезенки
- Механического воздействия – если посмотреть под микроскопом, у каждого гельминта можно увидеть приспособления для закрепления в организме, травмирующие слизистую: зубья, крючья, присоски. В результате возникают боли в животе, частый стул, диспепсия.
Хроническая фаза характеризуется поражением определённых органов и систем. Чаще всего страдает кишечник, длительное механическое воздействие приводит к его воспалению, нарушениям всасывания и переваривания пищи. Развивается анемия, недостаток витаминов и микроэлементов, а у маленьких детей отмечается задержка роста и набора веса. Могут поражаться желчный пузырь и желчевыводящие пути (лямблиоз); сердечно-сосудистая система, лёгкие, нервная система (чаще трихинеллез); лёгкие и печень (эхинококкоз) и так далее. При длительном течении подавляется иммунитет и присоединяются вторичные инфекции.
Если Вы обнаружили любой из перечисленных признаков, сдайте клинический анализ крови с лейкоцитарной формулой. Повышение эозинофилов до 7-10% и более станет ещё одним подозрительным критерием.
Как выявить паразитарное заболевание?
-
, предпочтительнее обогащающий метод – PARASEP Определяет яйца всех видов гельминтов и простейших, обитающих в кишечнике
Следует обратить внимание на следующие моменты:
На что нужно обратить внимание?
- Наличие проявлений и одновременное обнаружение IgG могут свидетельствовать о хронической фазе гельминтоза
- В сомнительных случаях рекомендовано повторное исследование IgG через 2 недели. Нарастание уровня антител в 2 раза и более говорит об активности гельминта
- При трихинеллезе, эхинококкозе, цистицеркозе определение антител – единственный возможный метод лабораторной диагностики, поскольку человек – промежуточный хозяин для данных гельминтов.
Для цитирования: Кочергина Е.А., Корюкина И.П., Зубов Е.В. Особенности лечения паразитарных заболеваний. РМЖ. 2004;13:815.
На современном этапе паразитарные заболевания признаны общегосударственной проблемой. Это связано с их повсеместным распространением и отрицательным воздействиям на здоровье населения, приводящим к значительным экономическим потерям [1]. Особенно это касается детского населения, так как среди заболевших они составляют более 80%. Цифры заболеваемости гельминтозами сопоставимы с показателями заболеваемости ОРВИ и гриппом вместе взятыми. Сегодня, когда известны механизмы основных патогенетических реакций при паразитарных заболеваниях, можно сказать, что они являются причиной тяжелых аллергических проявлений, вызывают патологию органов пищеварения и органов дыхания, оказывают сенсибилизирующее и иммунодепрессивное влияние, чем обеспечивают благоприятный фон для возникновения соматической и инфекционной патологии [2]. Наиболее общее патологическое воздействие всех гельминтов – аллергизация организма и подавление иммунного ответа. Гельминты, их части, продукты их жизнедеятельности являются аллергенами, вызывают воспалительные изменения, оказывают иммуносупрессивное действие и всегда индуцируют интенсивную продукцию Ig E–антител. Все это поддерживает или инициирует хронические аллергические заболевания, такие как крапивница, атопический дерматит, бронхиальная астма. Конечно, гельминтозы нельзя отнести к истинно аллергическим заболеваниям, но надо помнить, что это болезни, в патогенезе которых аллергия участвует, как обязательный компонент основного патологического процесса [2]. Наличие паразитарного заболевания у ребенка приводит к подавлению неспецифической резистентности организма, что ведет к учащению острых респираторных и инфекционных заболеваний, удлинению и утяжелению их течения. Достоверно доказано снижение выработки защитных антител при вакцинации дифтерии у инвазированных. Ухудшается формирование иммунитета при ревакцинации кори и столбняка у больных с паразитарным заболеванием. Также у детей с гельминтозом чаще регистрируется ложный вираж туберкулиновых проб. Иммунная система всегда реагирует на действие паразитарного антигена, и длительное хроническое течение инвазии вызывает ее истощение. Снижение Т–лимфоцитов у больного приводит к развитию таких осложнений, как бактериально–вирусные и аллергические. Поэтому в докладе ВОЗ (1977) среди причин, способных вызвать вторичное иммунодефицитное состояние (ВИД), на первое место были вынесены протозойные и глистные болезни. Хроническое течение гельминтоза всегда сопровождается обменными нарушениями в виде снижения содержания белка в печени, обмена жиров и углеводов, гипоксии в органах, уменьшения концентрации витаминов, микроэлементов, фолиевой кислоты, что может вызвать необратимые изменения в органах. Поэтому очень важным при установлении окончательного диагноза паразитарного заболевания является выбор тактики ведения больного и адекватного лечения. Лечение паразитарных заболеваний на современном этапе остается нерешенной проблемой, особенно это касается тканевых гельминтозов, таких как токсокароз, эхинококкоз, стронгилоидоз и др. Применение существующих сегодня антигельминтных препаратов (в основном это производные мебендазола) не всегда эффективно. Это связано с их низкой кишечной абсорбцией – до10%, быстрым развитием резистентности при повторных и длительных курсах терапии, формированием при реинвазиях более тяжелых форм, которые ведут к значительным иммунологическим сдвигам [4]. Сегодня в России появился новый антигельминтный препарат широкого спектра действия – Немозол ( а л ьбе н д а зол ). Системное действие Немозола связано с его активным метаболитом – сульфоксидом альбендазола, который образуется в печени. Немозол активен в отношении разных видов паразитов. Препарат ингибирует полимеризацию бета–глобулина, что приводит к нарушению образования цитоплазматических микротубул клеток гельминта. Экспериментальные данные свидетельствуют о том, что Немозол действует не только на взрослых кишечных особей, а также на их яйца и личинки [5]. Высокая терапевтическая активность Немозола обусловлена тем, что он имеет наибольшую среди антигельминтных препаратов биодоступность – до 30%. Широко использовать препарат в детском городскомгельминтологическом центре города Перми мы начали с сентября 2003 года. Эффективность Немозола оценивали по степени излечения больных детей и степени снижения яиц в кале – эти методы считаются стандартами ВОЗ (WHO, 1999). Хорошая эффективность Немозола выявлена при лечении токсокароза. В Перми регистрируется высокий уровень заболеваемости токсокарозом – 47,68 на 100 тыс. детского населения, Пермская область занимает восьмое место в Российской Федерации по данной нозологии. Это инвазия часто встречается у детей до 5 лет и характеризуется полиморфной клинической картиной, с развитием тяжелых осложнений со стороны легких, кожи, печени. Легочные поражения встречаются у 50% больных в виде бронхитов с бронхообструктивным синдромом, пневмоний, атопической бронхиальной астмы. В клинике превалирует сухой приступообразный кашель, чаще ночью, лихорадка, слабость, потливость, инспираторная одышка. Известны случаи тяжелых токсокарозных эозинофильных пневмоний с летальным исходом. Изменения со стороны сердечно–сосудистой системы при токсокарозе имеют, как правило, аллергическую этиологию. Миграция личинок способствует также манифестации вирусной инфекции с развитием тяжелых миокардитов. Описаны случаи обнаружения на аутопсии личинок Toxocara canis в миокарде и некротических гранулематозных очагов с эозинофильной инфильтрацией. К классическим признакам сердечного заболевания присоединяются гиперэозинофилия, острая лихорадка и симптомы поражения соединительной ткани. Абдоминальный синдром встречается у 80% больных токсокарозом детей и проявляется вздутием, болями в животе, тошнотой, иногда рвотой, диареей. Гепатомегалия регистрируется у 65% больных. Развитие глазного токсокароза возникает при низкой степени инвазии и низком иммунном ответе, что и позволяет личинкам беспрепятственно проникать к глазному яблоку. Часто заболевание регистрируется у детей старше 12 лет, чаще поражаются лица мужского пола. Практически всегда идет изолированное поражение только одного глаза, чаще левого. Больные жалуются на снижение остроты зрения до полной слепоты. В процесс могут вовлекаться сетчатка, хрусталик, стекловидное тело. Заболевание имитирует ретинобластому, болезнь Коатса, дегенерацию макулярного пятна. Может поражаться параорбитальная клетчатка, с отеком и гиперемией век, отеком щеки и лимфоаденитом; также имеет место диплопия и экзофтальм, процесс носит рецидивирующий характер. По нашим данным, почти у 40% больных токсокарозом детей после лечения отмечаются рецидивы. Даже в период ремиссии у таких больных сохраняется лимфоаденопатия, увеличение печени, кожный синдром. Идущие процессы сенсибилизации вызывают нарушение функции органов и тканей, что ведет к снижению физического и умственного развития ребенка. В течение нескольких лет мы применяли возможные схемы и различные препараты для лечения токсокароза, оценивая их эффективность. Анализ историй болезни 224 детей с токсокарозом показал высокую терапевтическую активность Немозола по отношению к личинкам токсокары. Терапевтическую эффективность препаратов оценивали по регрессу клинических проявлений,прогрессивному снижению уровня эозинофилии, снижению титру специфических антител до уровня 1:400 и ниже. Больные токсокарозом получали Немозол в дозировке 15 мг/кг в сутки в течение 10–14 дней. Существенным положительным моментом было отсутствие побочных эффектов и хорошая переносимость Немозола при длительных курсах терапии. Значительный терапевтический эффект мы получили при лечении стронгилоидоза – инвазии, которая в последнее время стала часто регистрироваться в Пермской области. В клинике у наших больных чаще преобладал кишечный вариант течения инвазии. Больные жаловались на изжогу, вздутие живота, боли в животе после еды, похудание, тошноту, рвоту, понос. Интенсивная инвазия стронгилоиодоза может протекать по типу язвенной болезни, язвенного колита, энтерита, острого живота. С января по май 2004 года в детском городском гельминтологическом центре мы пролечили 8 больных со стронгилоидозом (4 больных из семейного очага, 3 поступили повторно после безуспешного лечения мебендазолом). Больные получали Немозол по 400 мг ежедневно в течение 3–х дней. Контрольные анализы через 1 и 3 месяца показали эффективность препарата в 100% случаях. Учитывая спектр существующих сегодня в России антигельминтных препаратов, альтернативы Немозолу при лечении стронгилоидоза нет. Высокая паразитоцидная активность Немозола отмечена нами и при лечении других нематодозов: аскаридоз – 100% (n=14), энтеробиоз – 96,4% (n=82), трихинеллез – 100% (n=9), где n – количество пролеченных. Причем при аскаридозе и энтеробиозе эффект достигался после однократного приема препарата. Анализируя полученные нами данные, считаем, что наиболее перспективным Немозол показал себя при mixt–инвазиях, когда у больного выявляется сочетанная инвазия из 2 и более паразитов. Немозол давал положительные результаты и в случаях, когда у больных с гельминтозом выявлялся лямблиоз. В настоящее время имеется достаточное количество препаратов для специфического лечения лямблиоза. При выборе препарата для лечения лямблиоза необходимо помнить, что в последние годы появилось большое количество штаммов паразитов, устойчивых к длительно применявшимся ранее метронидазолу и фуразолидону. Сегодня широкое распространение в лечении лямблиоза у людей пробрели ингибиторы тубулина бензимедазольного ряда (албендазол). Эти препараты значительно безопаснее и удобны для массового применения [6]. Стандартная дозировка Немозола, применяемая нами в лечении лямблиоза (400 мг в сутки в течение 5 дней) приводила к 86% излечению от сочетанного паразитарного заболевания. При стойкой эозинофилии, длящейся несколько месяцев, при невозможности по тем или иным причинам идентифицировать возбудителя и установить диагноз, многие авторы предлагают проводить эмпирическую терапию антигельминтиками широкого спектра действия. В этих случаях быстрый терапевтический эффект является косвенным подтверждением диагноза. Учитывая возможности Немозола, считаем его идеальным препаратом для проведения терапии ex juvantibus [3]. З а к люч е н и е. Опыт применения Немозола в детском городском гельминтологическом центре г. Перми составил более 300 больных с различными видами паразитарных заболеваний. Полученные нами данные свидетельствуют о том, что Немозол – высокоэффективный препарат широкого спектра действия и может использоваться в педиатрии для лечения паразитарных заболеваний. Немозол является препаратом выбора при таких тяжелых тканевых гельминтозах, как эхинококкоз, токсокароз, нейроцистицеркоз, высоко эффективен при лечении сочетанных паразитозов и протозоозов. Не имеет возрастных ограничений, выпускается в удобной лекарственной форме в виде таблеток и суспензии. Существенным преимуществом применения Немозола, особенно у детей, является не только высокая противопаразитарная активность, но и практически полное отсутствие побочных эффектов и хорошая переносимость.
Литература 1. Онищенко Г.Г. Заболеваемость паразитарными болезнями в Российской федерации и основные направления деятельности по ее стабилизации // Медицинская паразитология. – 2002. № 4. С 3–10. 2. Астафьев Б.А. Иммунологические проявления и осложнения гельминтозов. – М., 1987. – 124с. 3. Лысенко А.Я., Владимова М.Г., Кондрашин А.В. // Клиническая паразитология. Женева, 2002, с 65 – 66. 4. Озерецковская Н.Н. Подходы отечественной школы паразитологов – иммунологов к терапии паразитарных болезней // Медицинская паразитология. – 1998. – № 2. – С. 12–15. 5. J. Horton Treatment of parasitic diseases // Parasitology 2000, Cambridge University Press. – S 113–132. 6. Авдюхина Т.И., Константинова Т.Н., Кучеря Т.В. Лямблиоз // учебное пособие. – Москва, 2003, с 16 –17.
Иммунные реакции при протозойных инфекциях. Иммунитет при паразитах. Иммунная система при простейших в организме.
Аг патогенных простейших вызывают развитие гуморальных и клеточных реакций, но их роль в защите организма неравноценна. Это связано с паразитированием некоторых простейших в областях пониженного иммунного надзора (например, в СМЖ, головном мозге), тогда как другие паразитируют в сосудистом русле (в этом случае роль защитных реакций в их уничтожении высока).
Величина паразитов, сложность их организации и наличие систем устойчивости позволяют им более или менее эффективно избегать действия защитных механизмов. Весьма важно и то, что на Аг или группу близкородственных Аг простейших организм человека формирует два типа AT с противоположными эффектами — паразитоцидные и индуцирующие изменчивость паразита. В результате иммунные реакции начинают играть роль экологического фактора, регулирующего взаимоотношения в системе паразит-хозяин и поддерживающего длительное её существование.
Простейшие, обитающие в кровотоке (африканские трипаносомы, малярийные плазмодии) избегают действия иммунных механизмов за счёт изменения основных Аг у дочерних популяций. Другими словами, очередная популяция антигенно и иммуногенно обособлена, что резко снижает эффективность иммунных реакций.
Полостные паразиты (гиардии, амёбы, трихомонады) контактируют с иммунокомпетентными клетками, что приводит к ограниченной индукции иммунных реакций. Эти реакции имеют некоторую значимость: известно, что у лиц с иммунодефицитами гиардиоз наблюдают часто.
Прочие патогенные простейшие (американские трипаносомы, лейшмании и токсоплазмы) вызывают развитие гуморальных и клеточных реакций, но полному удалению патогенов из организма препятствует их способность длительно паразитировать в разнообразных клетках организма.
Информация на сайте подлежит консультации лечащим врачом и не заменяет очной консультации с ним.
См. подробнее в пользовательском соглашении.
Паразитарная инфекция легкого на КТ: причины, диагностика
а) Терминология:
1. Определения:
• Паразиты: организмы, питающиеся и живущие за счет другого организма (хозяина):
о Облигатные паразиты: могут жить только в организме хозяина о Факультативные паразиты: могут жить в организме хозяина и вне его
• Могут приводить к фокальному или диффузному поражению легких
2. Классификация паразитов, поражающих легкие:
• Простейшие:
о Амебиаз: Entamoeba histolytica
о Токсоплазмоз: Toxoplasma gondii
о Малярия: плазмодии (Р. falciparum, Р. vivax, Р. ovale, Р. malariae)
о Трипаносомоз (болезнь Шагаса): Trypanosoma cruzi
• Нематоды:
о Аскаридоз: Ascaris lumbricoides
о Анкилостомоз: Ancylostoma duodenale
о Стронгилоидоз: Strongyloides stercoralis
о Филяриоз: Wuchereria bancrofti, Brugia malayi, Brugia tlmori
о Дирофиляриоз: Dirofilaria immitis
о Трихинеллез: Trichinella spiralis о Токсокароз: Toxocara canis и Toxocara cati
• Цестоды:
о Эхинококкоз: Echinococcus granulosus и Echinococcus multilocularis
• Трематоды:
о Парагонимоз: Paragonimus westermani (наиболее широко распространенный в мире), Paragonimus kellicotti (наиболее распространенный в США)
о Шистосомоз: Schistosoma mansoni
б) Визуализация:
1. Рентгенография легких при паразитарной инфекции:
• Узлы в легких ± кавитация
• Консолидация ± кавитация
• Пневмоторакс и плевральный выпот: Р. Westermani
• Диффузные неоднородные затемнения: малярия и стронгилоидоз
• Выраженная кардиомегалия и легочная гипертензия: болезнь Шагаса
о Септальные линии, отек легких, плевральный выпот
• Единичные или множественные объемные образования округлой или овоидной формы (возможно, с уровнями жидкости и газа): Е. granulosus
в) Дифференциальная диагностика паразитарной инфекции легких:
3. Внебольничная пневмония:
• Пневмонию может быть сложно отличить от паразитарной инфекции; эти патологические состояния могут сочетаться
г) Патология:
1. Общая характеристика:
• Паразитические организмы могут широко варьировать в размерах и сложности:
о Простые одноклеточные организмы: амебы
о Сложные многоклеточные: черви, трематоды
2. Макроскопические и хирургические особенности:
• Амебы: некроз и абсцессы, часто связанные с печенью
• Эхинококкоз: Е. granulosus:
о Эндоцист: внутренний герминальный слой
о Экзоцист: наружный слой, покрытый хитином
о Перицист: участок реактивных изменений легочной ткани
3. Микроскопия:
• Токсоплазмоз: интерстициальная пневмония
• Малярия: ОРДС
• Аскаридоз: воспалительная реакция, деструкция капилляров и стенок альвеол, отек, кровоизлияние, десквамация клеток
• Стронгилоидоз: бронхопневмония, отек легких, обширное интраальвеолярное кровоизлияние, ОРДС
д) Клинические особенности:
1. Проявления:
о Амебиаз:
- Поражение легких и плевры:
Наиболее типичное внекишечное проявление
- Гепатобронхиальный или бронхобилиарный свищ
- Поражение перикарда: Чаще возникает при вовлечении левой доли печени
Боль, тампонада сердца, сепсис
о Малярия:
- Малярийные комары: переносчики плазмодия к людям
- Симптомы: лихорадка, озноб, потливость, анемия, лейкопения, спленомегалия:
Первичные торакальные проявления: некардиогенный отек легких (например, ОРДС)
Эозинофильная пневмония: обусловлена противомалярийными препаратами (например, пириметамином)
о Трипаносомоз (болезнь Шагаса):
- Заболевание обычно диагностируется в хронической стадии
- Острый трипаносомоз может стать летальным, но диагностируется редко
- Кардиомиопатия Шагаса: > 90% случаев:
Миокардит ± выпот в перикарде
о Аскаридоз:
- Наиболее распространенная паразитарная инфекция в мире
- Синдром Леффлера (простая легочная эозинофилия):
Преходящие затемнения в легких соотносятся с миграцией личинок через легкие
- Непродуктивный кашель, жгучая боль за грудиной, диспноэ, в отдельных случаях легкое кровохарканье
о Анкилостомоз (A. duodenale):
- Симптоматика зависит от локализации паразита:
Субклиническое течение у большинства пациентов
- Синдром Леффлера аналогичен таковому при аскаридозе о Стронгилоидоз:
- Неосложненный стронгилоидоз:
Симптомы: кашель, диспноэ, бронхоспазм в фазе миграции
- Синдром гиперинфекции: высокая нагрузка паразитическими червями вследствие реинфекции:
Может имитировать легочную эмболию, ОРДС, астму, или ХОБЛ
- Диссеминированный стронгилоидоз: поражение органов за пределами обычного пути миграции; обнаружение личинок в кале, мокроте, коже:
Обширное интраальвеолярное кровотечение
о Филяриоз:
- W. bancrofti, В. malayi, В. timori в лимфатических сосудах:
Обструкция лимфатических сосудов: слоновость, гидроцеле
ТЛЭ
о Дирофиляриоз:
- Инфекция часто протекает бессимптомно
- Подкожная узловая форма: D. repens
- Легочный дирофиляриоз человека: D.immitis:
Солитарный внутрилегочный узел (случайная находка)
о Visceral larva migrans (токсокариоз):
- Типичные симптомы: хронический кашель (пароксизмальный и усиливающийся ночью), хрипы в легких
- Хроническая эозинофильная пневмония, внутрилегочные узлы без признаков кавитации
о Эхинококкоз:
- Распространен повсеместно, наибольшая заболеваемость в Средиземноморском регионе, Южной и Центральной Америке, России
- E. granulosus: более распространенная этиология у человека
- E.multilocularis
- Разрыв кисты (в трахеобронхиальное дерево или полость плевры):
Выделение фрагментов кисты с мокротой
Реакции гиперчувствительности: крапивница, одышка; вплоть до анафилаксии
о Парагонимоз:
- Человек инфицируется после проглатывания зараженного материала или недостаточно термически обработанных ракообразных
- Острая фаза (несколько часов после приема зараженной пищи):
Неспецифическая боль в животе, лихорадка и диарея
- Прободение диафрагмы (2-3 недели): поражение плевры и легочной паренхимы
- Хроническая фаза: возбудитель может годами находиться в легких:
Полости в легких
о Шистосомоз:
- Пенетрация кожи или стенки кишечника, проникновение возбудителя в системный венозный кровоток, миграция в легкие
- Острая инфекция (лихорадка Катаямы):
Лихорадка, озноб, хриплое дыхание, диспноэ, сухой кашель, утомляемость, диарея, боль в животе
- Хроническая инфекция: причина легочной гипертензии
3. Течение и прогноз:
• Амебиаз:
о Непосредственное распространение возбудителя из абсцесса легкого в грудную клетку (6-40%)
о Гематогенное распространение и аспирация
• Малярия:
о В эндемичных областях ежегодно фиксируется несколько миллионов летальных исходов
о Первичные торакальные проявления: ОРДС
• Стронгилоидоз:
о Смертность от гиперинфекции или диссеминации: 70%
о Присоединение вторичной инфекции: 80%
е) Список использованной литературы:
1. Cottin V: Eosinophilic lung diseases. Clin Chest Med. 37(3):535-56, 2016
2. Price M et al: Imaging of eosinophilic lung diseases. Radiol Clin North Am. 54(6): 1151 -1164, 2016
3. Skalski JH et al: Fungal, viral, and parasitic pneumonias associated with human immunodeficiency virus. Semin Respir Crit Care Med. 37(21:257-66, 2016
4. Henry TS et al: Role of imaging in the diagnosis and management of parasitic infections. Curr Opin Pulm Med. 19(3):310-7, 2013
Читайте также:

