Инфекции хламидии микоплазма цмв
Обновлено: 24.04.2024
Кафедра акушерства и гинекологии №1 Башкирского государственного медицинского университета
Кафедра акушерства и гинекологии №1 Башкирского государственного медицинского университета
Кафедра акушерства и гинекологии №1 Башкирского государственного медицинского университета
Кафедра акушерства и гинекологии №1 Башкирского государственного медицинского университета
Кафедра акушерства и гинекологии №1 Башкирского государственного медицинского университета
Кафедра акушерства и гинекологии №1 Башкирского государственного медицинского университета
Кафедра акушерства и гинекологии №1 Башкирского государственного медицинского университета;
Клинический родильный дом №4, Уфа
Внутриутробное инфицирование плода: современный взгляд на проблему
Журнал: Российский вестник акушера-гинеколога. 2013;13(5): 16‑20
Хамадьянов У.Р., Русакова Л.А., Хамадьянова А.У., Тихонова Т.Ф., Хамадьянова С.У., Галимов А.И., Иваха В.И. Внутриутробное инфицирование плода: современный взгляд на проблему. Российский вестник акушера-гинеколога. 2013;13(5):16‑20.
Khamad'ianov UR, Rusakova LA, Khamad'ianova AU, Tikhonova TF, Khamad'ianova SU, Galimov AI, Ivakha VI. Intrauterine fetal infection: the present view of the problem. Russian Bulletin of Obstetrician-Gynecologist. 2013;13(5):16‑20. (In Russ.).
Кафедра акушерства и гинекологии №1 Башкирского государственного медицинского университета
В статье на основании данных современной литературы и результатов ранее выполненных собственных исследований представлены вопросы этиологии и патогенеза, диагностики, лечения и профилактики внутриутробной инфекции (ВУИ). Особое внимание обращено на роль инфекционного фактора в реализации ВУИ и значение цитокинового статуса. Приведена интерпретация диагностических тестов при ВУИ на современном этапе.
Кафедра акушерства и гинекологии №1 Башкирского государственного медицинского университета
Кафедра акушерства и гинекологии №1 Башкирского государственного медицинского университета
Кафедра акушерства и гинекологии №1 Башкирского государственного медицинского университета
Кафедра акушерства и гинекологии №1 Башкирского государственного медицинского университета
Кафедра акушерства и гинекологии №1 Башкирского государственного медицинского университета
Кафедра акушерства и гинекологии №1 Башкирского государственного медицинского университета
Кафедра акушерства и гинекологии №1 Башкирского государственного медицинского университета;
Клинический родильный дом №4, Уфа
Прогрессирующий рост числа случаев внутриутробного инфицирования плода является одной из наиболее актуальных проблем современного акушерства и перинатологии. Этому способствует полиэтиологичность данной патологии, отсутствие четкой взаимосвязи между выраженностью клинических проявлений инфекции у матери и степенью поражения плода, многофакторное воздействие инфекционного агента на плод.
Несмотря на повышенное внимание к проблеме внутриутробной инфекции (ВУИ), нерешенными остаются многие вопросы. В дальнейших поисках и разработке нуждаются вопросы диагностики, лечения и профилактики ВУИ. До сих пор нет четких критериев лечебной тактики, не обобщены данные об эффективности комплексной терапии.
Эпидемиология, этиология и патогенез внутриутробной инфекции
В развитии инфекционного процесса у плода имеют значение вид возбудителя, его вирулентность, пути проникновения инфекции от матери к плоду, защитные резервы организма матери и способность плода к иммунному ответу [11].
Известно, что большинство бактерий существуют в природе в виде специфически организованных биопленок (biofilms) [2, 25, 27]. Такая форма существования создает бактериям массу преимуществ. Бактерии в биопленках имеют повышенную выживаемость в присутствии агрессивных веществ, факторов иммунной защиты и антибиотиков [27]. В этой связи одной из основных проблем практической медицины становится проблема лечения заболеваний микробного происхождения.
В нашем исследовании [15, 17] по результатам бактериологического анализа видового состава вагинального биотопа было выявлено наиболее сильное влияние Streptococcus faecalis (p=0,00171), E. coli (p=0,01424) и Staphylococcus epidermidis (p=0,02714) на реализацию внутриутробного инфицирования плода. При оценке возбудителей, выявленных в цервикальном канале беременных путем полимеразной цепной реакции (ПЦР) и иммуноферментного анализа (ИФА), установлено следующее: в группе без реализации ВУИ микоплазмы, хламидии и уреаплазмы составили 8%, ЦМВ - 20%, ВПГ - 36%, кандида - 3%, ассоциации - 60%. При анализе группы новорожденных с реализацией ВУИ были выделены наиболее частые возбудители. Так, микоплазмы, хламидии и ВПГ встречались в 50%, ЦМВ-инфекция была выявлена в 45% случаев, реже встречались уреаплазмы (20%) и кандида (15%), ассоциации наблюдались в 95%. Частота обнаружения патогенных возбудителей у новорожденных с признаками ВУИ была выше, чем у пациентов без реализации инфекции.
Основным источником инфекции при ВУИ является мать ребенка, из организма которой возбудитель проникает в организм плода (вертикальный механизм передачи). При этом инфицирование происходит как восходящим, трансплацентарным и трансовариальным путями, так и контактным, и аспирационным (непосредственно во время родов) путями. Причем для антенатальных инфекций наиболее типичен гематогенный, а для интранатальных - восходящий пути инфицирования [4, 10, 20, 21].
Влияние ВУИ на эмбрион и плод заключается в воздействии комплекса следующих факторов [22]:
1. Патологическое действие микроорганизмов и их токсинов (инфекционное заболевание, гипоксия плода, задержка развития плода).
2. Нарушение процесса имплантации и плацентации (низкая плацентация, предлежание плаценты).
3. Снижение метаболических процессов и иммунной защиты плода.
В патогенезе возникновения и развития ВУИ особое значение имеет срок беременности [13, 22]. Плод до 14 нед беременности не реагирует на инфекционные антигены, так как у него отсутствуют иммунокомпетентные клетки, иммуноглобулины и не проявляются иммунные реакции. С началом II триместра беременности механизм воздействия восходящей инфекции меняется из-за слияния decidua vera и deciduas capsularis в единый комплекс deciduas parietalis. В это время восходящая инфекция может проникнуть к плоду из влагалища или шеечного канала. С этого срока беременности внутренний зев шеечного канала соприкасается с водными оболочками плода и при наличии инфекции микроорганизмы проникают в околоплодные воды. Антимикробные свойства амниотическая жидкость приобретает лишь после 20-й недели беременности, когда в ответ на воздействие инфекционного агента развивается воспалительная пролиферативная реакция, ограничивающая дальнейшее проникновение инфекции, благодаря появлению лизоцима, комплемента, интерферонов, иммуноглобулинов [1, 22]. В III триместре беременности антибактериальная защита околоплодных вод возрастает. В этот период в воспалительной реакции тканей плода преобладает роль экссудативного компонента, когда в ответ на проникновение инфекции развиваются воспалительные лейкоцитарные реакции у плода (энцефалит, гепатит, пневмония, интерстициальный нефрит) [22].
Особенно опасным при ВУИ во II и III триместрах беременности является повреждение мозга плода, что может приводить к умственной отсталости, задержке психомоторного развития детей [3, 7]. Внутриутробное поражение возбудителями инфекции структур ЦНС у плода сопровождается различными тяжелыми нарушениями в формировании мозга (гидроцефалия, субэпендимальные кисты, кистозная дегенерация вещества мозга, аномалии развития коры, микроцефалия). Возможно также развитие вентрикулита (деформация сосудистого сплетения, неоднородность или удвоение отражения от эпендимы желудочков) [11].
Таким образом, инфицирование плода в более поздние сроки беременности не приводит, как правило, к формированию грубых пороков развития, но может нарушать функциональные механизмы дифференцировки клеток и тканей [10, 11, 13].
Изменения состояния плода и функционирования фетоплацентарной системы, вызванные внутриутробным инфицированием плода, отражаются на составе и свойствах амниотической жидкости [1, 9, 26, 30]. При попадании в амниотическую жидкость инфекционного агента происходит его беспрепятственное размножение с последующим развитием хориоамнионита [1, 9]. Плод оказывается в инфицированной среде, что создает благоприятные условия для заражения плода контактным путем, т.е. через кожу, слизистые оболочки, респираторный и желудочно-кишечный тракты.
1. При заглатывании и аспирации инфицированных вод у новорожденного появляются признаки внутриутробной инфекции (пневмония, энтероколит, везикулез, омфалит, конъюнктивит и др.).
3. Многоводие при внутриутробном инфицировании обычно носит вторичный характер и служит проявлением поражения почек или мочевыводящих путей плода. Причиной его развития является и изменение соотношения процессов продукции и резорбции околоплодных вод клетками амниотического эпителия на фоне амнионита.
4. В генезе симптомокомплекса плацентарной недостаточности при ВУИ основная роль принадлежит сосудистым расстройствам.
5. Типичным проявлением внутриутробного инфицирования служат невынашивание беременности и преждевременные роды [24]. Преждевременное развитие родовой деятельности и несвоевременный разрыв плодных оболочек обусловлены действием бактериальных фосфолипаз, запускающих простагландиновый каскад, и повреждающим действием воспалительных токсинов на плодные оболочки.
6. В связи с тем что фосфолипазы грамотрицательных бактерий способствуют разрушению сурфактанта в легких плода, у новорожденного развиваются респираторные расстройства.
В современной литературе [4, 9, 29] имеется немало работ, посвященных изучению взаимосвязи иммунологических показателей и тяжести инфекционно-воспалительного процесса во время беременности. Все чаще в зарубежной и отечественной литературе появляются данные о взаимосвязи бактериальной инвазии и синтеза цитокинов клетками амниона, хориона, децидуальной и плодовыми тканями [5, 29]. Размножение микроорганизмов в амниотической жидкости приводит к повышению уровня липополисахаридов, которые активируют синтез цитокинов клетками фетального трофобласта. Перспективным при ВУИ представляется изучение изменений в системе цитокинов, которая обеспечивает процессы межклеточной кооперации, роста и дифференцировки лимфоидных клеток, гемопоэза и нейроиммуноэндокринных взаимодействий. Цитокины в предымплантационном периоде и в ходе развития беременности активно продуцируются множеством материнских и эмбриональных клеток, в частности, децидуальными клетками матки и клетками трофобласта. При этом установлено, что клеточные культуры обладают неодинаковой способностью к синтезу цитокинов под влиянием липополисахаридов. Так, фактор некроза опухоли (ФНО) продуцируется клетками амниона, интерлейкины (ИЛ)-6 и ИЛ-8 - амнионом и хорионом, а ИЛ-1 продуцируется только хорионом [9, 11, 28]. По данным Н.В. Орджоникидзе [14], из множества провоспалительных (ИЛ-1, ИЛ-2, ИЛ-6, ИЛ-8, ИЛ-15, ФНО и др.) и противовоспалительных (ИЛ-4, ИЛ-10, ИЛ-13, трансформирующий фактор роста и др.) цитокинов основными маркерами воспалительного процесса в тканях и органах человека считают ИЛ-1, ИЛ-6, ИЛ-10, ФНО [9, 16, 28].
Клиническая характеристика внутриутробной инфекции
В предымплантационный период под воздействием инфекционного агента зародыш гибнет (альтеративное воспаление) или продолжает развиваться.
Инфекционное повреждение эмбриона на 3-12-й неделе обычно связано с вирусной инфекцией, свободно проникающей через хорион. Плод еще не имеет систем противоинфекционной защиты, и в период органогенеза, плацентации ВУИ приводит к формированию пороков развития (тератогенный) или гибели эмбриона (эмбриотоксический эффект) [5, 23].
Инфекционные фетопатии возникают с 16-27-й недели гестации, когда происходит генерализация инфекции у плода, формирование псевдопороков (фиброэластоз миокарда, поликистоз легких, гидроцефалия, гидронефроз). При заражении после 28 нед плод приобретает способность к специфической локальной реакции на внедрение возбудителя, в результате возможны ВУИ (энцефалит, пневмония, гепатит, интерстициальный нефрит), недонашивание беременности, задержка внутриутробного развития, гибель плода [2, 3, 10].
В настоящее время выделяют следующие типы внутриутробных поражений при ВУИ [20, 21]:
- бластопатия - при сроке гестации 0-14 дней; возможны гибель эмбриона, самопроизвольный выкидыш или формирование системной патологии, сходной с генетическими заболеваниями;
- эмбриопатия - при сроке 15-75 дней; характерны пороки развития на органном или клеточном уровнях (истинные пороки), самопроизвольный выкидыш;
- ранняя фетопатия - при сроке 76-180 дней; характерно развитие генерализованной воспалительной реакции с преобладанием альтеративного и экссудативного компонентов и исходом в фиброзно-склеротические деформации органов (ложные пороки), прерывание беременности;
- поздняя фетопатия - при сроке 181 день до родов; возможно развитие манифестной воспалительной реакции с поражением различных органов и систем (гепатит, энцефалит, тромбоцитопения, пневмония).
ВУИ часто не имеет ярких клинических проявлений [4, 10, 15, 17]. Редко первые признаки у новорожденного имеются сразу после рождения, чаще проявляются в течение первых 3 сут жизни. При инфицировании в постнатальном периоде симптомы инфекционного процесса выявляются в более поздние сроки. Клинические появления врожденного бактериального или микотического поражения кожи у новорожденного могут иметь характер везикуло-пустулеза [4]. Конъюнктивит, ринит и отит, появившиеся на 1-3-е сутки жизни, также могут быть проявлениями ВУИ. Врожденная аспирационная пневмония может проявиться и на 2-3-й день жизни. С момента рождения у детей наблюдаются признаки дыхательной недостаточности: одышка, цианоз, часто притупление перкуторного звука и мелкопузырчатые влажные хрипы. Течение внутриутробной пневмонии тяжелое, поскольку в результате аспирации выключаются из дыхания обширные участки легкого (нижняя и средняя доли) вследствие обтурации бронхов инфицированными околоплодными водами, содержащими примесь мекония, чешуек кожи плода. Энтероколит у новорожденных возникает в результате проникновения возбудителя вместе с околоплодными водами в желудочно-кишечный тракт. Диспепсические явления обычно развиваются на 2-3-е сутки жизни. Характерны вялое сосание, срыгивание, вздутие кишечника, гепатоспленомегалия, расширение венозной сети передней брюшной стенки, частый жидкий стул. При микробиологическом исследовании кишечного содержимого преобладание клебсиелл, протея и синегнойной палочки. Поражение ЦНС при ВУИ у новорожденных может быть как первичным (менингит, энцефалит), так и вторичным, обусловленным интоксикацией. При поражении сосудистых сплетений боковых желудочков мозга развивается врожденная гидроцефалия. Необходимо уделять внимание таким симптомам, как вялость, плохое сосание, срыгивание, замедленное восстановление или вторичное снижение массы тела, задержка заживления пупочной ранки, развитие омфалита. Типичными симптомами инфекционной интоксикации у новорожденного являются нарушения дыхания и тканевого метаболизма. Отмечается бледно-цианотичная окраска кожных покровов с выраженным сосудистым рисунком. Интоксикация сопровождается нарушением экскреторной функции печени и почек, увеличением селезенки и периферических лимфоузлов.
Современные методы диагностики внутриутробных инфекций
Превалирование ВУИ среди причин неблагоприятных исходов, высокий уровень инфицированности у беременных и родильниц обусловливают необходимость поиска достоверных методов ее диагностики. Неспецифичность клинических проявлений ВУИ создает диагностические трудности, что диктует необходимость сочетанного применения клинических и лабораторных методов исследования. В последнее десятилетие основными методами диагностики ВУИ являются бактериологические и иммунологические [10, 11, 21].
Можно выделить 3 этапа в диагностике внутриутробного инфицирования: 1) диагностика во время беременности; 2) ранняя диагностика в момент рождения ребенка; 3) диагностика при развитии клинических признаков инфекции в раннем неонатальном периоде [12].
Любые изменения гомеостаза в организме матери находят свое отражение в клеточных и химических показателях амниотической жидкости, которые очень тонко характеризуют течение патологического процесса, в связи с чем амниотическая жидкость может служить важным диагностическим материалом [1, 6, 16]. По мнению И.В. Бахаревой [1], наиболее значимым в диагностике ВУИ является определение антимикробной активности амниотической жидкости, основанной на миграции в ней лейкоцитов при скоплении в околоплодной оболочке бактерий, превышающем 103 КОЕ/мл. Появление в околоплодных водах большого числа лейкоцитов, увеличение цитоза за счет эпителиоцитов без обнаружения микрофлоры могут свидетельствовать о ВУИ.
В настоящее время большое значение придается ультразвуковым методам исследования, с помощью которых можно определить косвенные признаки ВУИ плода (многоводие, вентрикуломегалия, микроцефалия, гепатомегалия, увеличение толщины плаценты, мелкодисперсная взвесь в околоплодных водах) и структурные изменения в различных органах [4, 11, 18, 26].
Нами был разработан необходимый перечень диагностических мероприятий с целью раннего выявления ВУИ [19].
В комплекс обследования беременных женщин вошли:
1. Общеклинический и биохимический анализы крови и мочи с определением стандартных показателей.
2. Определение возбудителей TORCH-комплекса с помощью ПЦР в вагинальных мазках, околоплодных водах.
3. Определение антител в крови к хламидиям, микоплазмам и уреаплазмам, ЦМВ и ВПГ методом ИФА.
4. Проведение аминного теста, pH-метрии влагалищного содержимого.
5. Бактериоскопическое исследование содержимого влагалища, цервикального канала и уретры.
6. Бактериологическое исследование материнской поверхности плаценты, околоплодных вод, содержимого кишечника.
7. Определение уровня провоспалительных (ИЛ-1β, ФНО) и противовоспалительного (ИЛ-10) цитокина в околоплодных водах, сыворотках венозной крови матери и пуповинной крови плода.
8. Ультразвуковое сканирование плода, околоплодных вод и плаценты.
9. Гистоморфологическое исследование плаценты.
В комплекс обследования новорожденных вошли:
1. Оценка по шкале Апгар, измерение массы тела и длины при рождении, динамика нарастания массы тела до выписки из родильного дома.
2. Определение антител в крови к хламидиям, микоплазмам и уреаплазмам, ЦМВ и ВПГ методом ИФА.
3. Бактериологическое исследование соскобов с конъюнктивы, задней стенки глотки и вульвы.
4. Выявление клинических признаков ВУИ совместно с врачом-неонатологом.
Комплексное исследование видового состава микроорганизмов родовых путей, околоплодных вод, плаценты, новорожденного, определение антигенов и антител к предполагаемому возбудителю в пуповинной крови и амниотической жидкости, гистологическое исследование последа позволяют определить путь инфицирования ребенка, природу возбудителя и уточнить объем дополнительных диагностических исследований при ВУИ, а также определить лечебно-профилактические мероприятия в раннем неонатальном периоде.
Выявление ДНК вируса простого герпеса 1, 2-го типов в урогенитальном соскобе используется для подтверждения инфицированности и оценки активности инфекционного процесса, в том числе при планировании беременности, у беременных, для обследования лиц с иммунодефицитными состояниями.
Выявление ДНК цитомегаловируса в урогенитальном соскобе используется для подтверждения инфицированности и в комплексном прегравидарном обследовании партнеров.
Выявление ДНК Mycoplasma genitalium в урогенитальном соскобе используется для подтверждения инфицированности при наличии стертой картины воспаления, при прегравидарном обследовании, при беременности, при бесплодии, для дифференциальной диагностики урогенитальных инфекций.
Выявление ДНК Ureaplasma parvum в урогенитальном соскобе используется для подтверждения инфицированности при наличии характерных проявлений, при стертой картине воспаления, при планировании беременности, бесплодии. Может выявляться у клинически здоровых лиц.
Выявление ДНК Ureaplasma urealyticum в урогенитальном соскобе используется для подтверждения инфицированности при отсутствии других патогенных возбудителей, при стертой картине воспаления, при осложненном течении беременности. Может выявляться у клинически здоровых лиц.
Выявление ДНК хламидий в урогенитальном соскобе используется для подтверждения инфицированности при наличии клинических проявлений воспаления урогенитального тракта, при планировании беременности, при бесплодии, для контроля эффективности антибактериальной терапии.
Выявление ДНК Trichomonas vaginalis в урогенитальном соскобе используется для подтверждения инфицированности при наличии клинических проявлений трихомониаза, при прегравидарном обследовании, для дифференциальной диагностики урогенитальных инфекций.
Исследование урогенитального тракта методом ПЦР относится к прямым методам лабораторного исследования, то есть образец биоматериала анализируется на наличие ДНК патогенной микрофлоры. Тест предназначен для исследования состояния урогенитального тракта, как у мужчин, так и у женщин.
Обследование женщин целесообразно проводить в период овуляции (при наличии выраженных симптомов воспаления - в день обращения). Накануне и в день обследования пациентке не рекомендуется выполнять спринцевание влагалища. Не рекомендуется взятие биоматериала на фоне проведения антибактериальной терапии или применения пробиотиков и эубиотиков. Если для исследования берут соскоб из уретры, сбор материала проводят до или не ранее 2 - 3 часов после мочеиспускания.
Информацию из данного раздела нельзя использовать для самодиагностики и самолечения. В случае боли или иного обострения заболевания диагностические исследования должен назначать только лечащий врач. Для постановки диагноза и правильного назначения лечения следует обращаться к Вашему лечащему врачу.
Цитомегаловирус: причины появления, симптомы, диагностика и способы лечения.
Определение
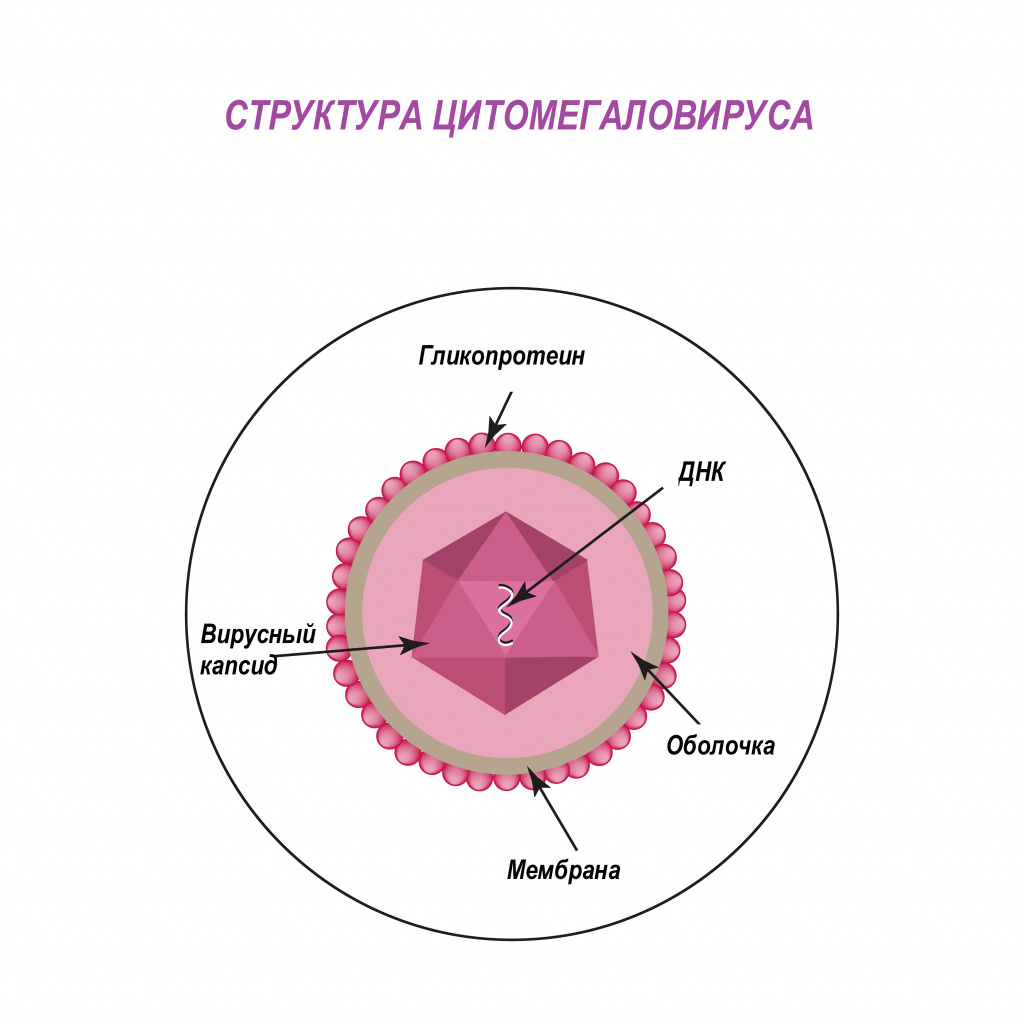
Цитомегаловирус (ЦМВ, или цитомегаловирусная болезнь) – хроническое инфекционное заболевание вирусной этиологии, характеризующееся многообразием клинических форм и проявлений - от бессимптомного течения до тяжелого поражения внутренних органов и центральной нервной системы. Возбудитель ЦМВ – представитель семейства герпесвирусов (вирус герпеса человека 5-го типа).
Попадая в клетки организма, цитомегаловирус способен оставаться в них пожизненно. У лиц с нормально функционирующей иммунной системой в подавляющем большинстве случаев инфекция протекает по типу вирусоносительства. При угнетении иммунитета вирус активизируется, вызывая клинические симптомы болезни.
По различным данным доля носителей цитомегаловируса в России составляет порядка 73-90% - то есть именно у такого количества людей выявляются антитела к ЦМВ.
Причины появления цитомегаловирусной болезни
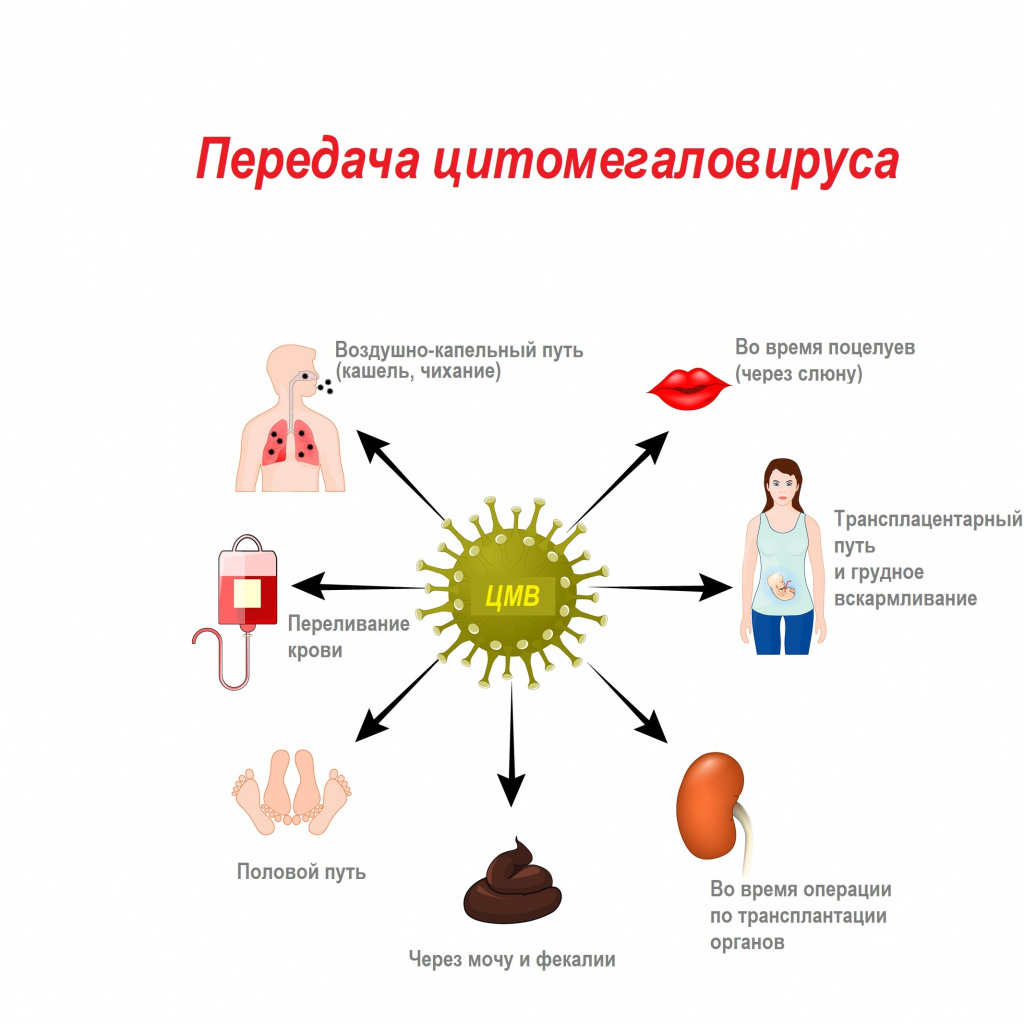
Цитомегаловирус передается через биологические жидкости: слюну, мочу, кровь, вагинальный секрет, слезы, сперму, фекалии, грудное молоко.
Из-за лабильности возбудителя и низкой концентрации вируса в выделениях для передачи инфекции необходим длительный, частый и тесный контакт с носителем.
Механизмы передачи вируса — воздушно-капельный (аэрозольный путь), контактный (контактно-бытовой и половой), гемоконтактный (парентеральный, а также при пересадке органов), вертикальный (от матери к плоду), фекально-оральный (алиментарный — через грудное молоко).
Заражение плода реализуется за счет трансплацентарной передачи от матери к плоду, которая возможна в течение всей беременности. Наибольшую опасность для плода представляет первичная инфекция на ранних сроках беременности, поскольку часто вызывает формирование врожденных пороков развития.
Особое свойство ЦМВ — способность вызывать депрессию практически всех звеньев иммунитета, резко угнетать продукцию интерферонов, в первую очередь ИНФ-α. При острой инфекции вирус поражает преимущественно эпителиальные клетки легких, печени, кишечника, почек, мочевого пузыря, молочных и слюнных желез, генитального тракта. Цитомегаловирус может инфицировать нервные клетки, клетки гладкой мускулатуры, костного мозга.
Классификация заболевания
По характеру инфицирования:
- врожденное (внутриутробное),
- постнатальное (приобретенное).
- латентная инфекция,
- персистирующая инфекция,
- активная (низкой, средней, высокой степени тяжести) инфекция.
- острая инфекция,
- реактивация вируса,
- реинфекция.
Инкубационный период цитомегаловирусной болезни составляет от 15 дней до трех месяцев (при манифестной, выраженной форме заболевания). Однако чаще первичное инфицирование протекает или бессимптомно, или по типу легкой формы ОРЗ – у пациента наблюдаются незначительная слабость, лихорадка (температура 37,1-38,0°С), дискомфорт в мышцах, першение в горле, иногда насморк, увеличение шейных лимфатических узлов, болезненность слюнных желез, головная боль, отсутствие аппетита.
У беременных острая первичная инфекция протекает, как правило, бессимптомно (25–50%) или с неспецифическими проявлениями (с лихорадкой, астенией и головной болью).
В редких случаях развиваются гепато- и спленомегалия, гепатит с минимальной степенью активности цитолитического синдрома, дерматиты, васкулиты, интерстициальный пневмонический процесс, тромбоцитоз или тромбоцитопения, лимфоцитоз.
У больных с иммунодефицитом цитомегаловирусная инфекция протекает тяжело - вирус быстро распространяется по организму и вызывает серьезные осложнения.
Диагностика цитомегаловируса
Диагностические мероприятия начинаются со сбора жалоб и анамнеза, в том числе акушерско-гинекологического анамнеза матери.
Затем врач проводит объективное обследование (физикальное, неврологическое и антропометрическое).
Лабораторные исследования - общие и специфические:
-
общий анализ крови;
Синонимы: Общий анализ крови, ОАК. Full blood count, FBC, Complete blood count (CBC) with differential white blood cell count (CBC with diff), Hemogram. Краткое описание исследования Клинический анализ крови: общий анализ, лейкоформула, СОЭ См. также: Общий анализ – см. тест № 5, Лейкоцит.
Синонимы: Анализ крови на антитела к цитомегаловирусу; АТ-ЦМВ-IgМ; цитомегаловирусная инфекция; ЦМВ-инфекция; специфические иммуноглобулины класса М к цитомегаловирусу. Cytomegalovirus; CMV Antibody; IgM; CMV infection; CMV-specific IgM. Краткое описание исследования Anti-CMV.
Синонимы: Анализ крови на антитела к цитомегаловирусу; АТ-ЦМВ-IgG; Цитомегаловирусная инфекция; ЦМВ-инфекция; Специфические иммуноглобулины класса G к цитомегаловирусу. Cytomegalovirus; CMV Antibody, IgG; CMV infection; CMV-specific IgG. Краткое описание исследования Anti-CMV-IgG .
Цитомегаловирус – широко распространённый вирус семейства герпесвирусов. После окончания острого периода инфекция цитомегаловирусом обычно переходит в латентную форму, из которой может реактивироваться. Цитомегаловирус относят к так называемым оппортунистическим инфекциям: выраженные клинич.
Цитомегаловирус – широко распространённый вирус семейства герпесвирусов. После окончания острого периода инфекция цитомегаловирусом обычно переходит в латентную форму, из которой может реактивироваться. Цитомегаловирус относят к так называемым оппортунистическим инфекциям: выраженные клинич.
Цитомегаловирус – широко распространённый вирус семейства герпесвирусов. После окончания острого периода инфекция цитомегаловирусом обычно переходит в латентную форму, из которой может реактивироваться. Цитомегаловирус относят к так называемым оппортунистическим инфекциям: выраженные клинич.
Цитомегаловирус – широко распространённый вирус семейства герпесвирусов. После окончания острого периода инфекция цитомегаловирусом обычно переходит в латентную форму, из которой может реактивироваться. Цитомегаловирус относят к так называемым оппортунистическим инфекциям: выраженные клинич.
Цитомегаловирус – широко распространённый вирус семейства герпесвирусов. После окончания острого периода инфекция цитомегаловирусом обычно переходит в латентную форму, из которой может реактивироваться. Цитомегаловирус относят к так называемым оппортунистическим инфекциям: выраженные клинич.
Цитомегаловирус – широко распространённый вирус семейства герпесвирусов. После окончания острого периода инфекция цитомегаловирусом обычно переходит в латентную форму, из которой может реактивироваться. Цитомегаловирус относят к так называемым оппортунистическим инфекциям: выраженные клинич.
Цитомегаловирус – широко распространённый вирус семейства герпесвирусов. После окончания острого периода инфекция цитомегаловирусом обычно переходит в латентную форму, из которой может реактивироваться. Цитомегаловирус относят к так называемым оппортунистическим инфекциям: выраженные клинич.
Цитомегаловирус – широко распространённый вирус семейства герпесвирусов. После окончания острого периода инфекция цитомегаловирусом обычно переходит в латентную форму, из которой может реактивироваться. Цитомегаловирус относят к так называемым оппортунистическим инфекциям: выраженные клинич.
Цитомегаловирус – широко распространённый вирус семейства герпесвирусов. После окончания острого периода инфекция цитомегаловирусом обычно переходит в латентную форму, из которой может реактивироваться. Цитомегаловирус относят к так называемым оппортунистическим инфекциям: выраженные клинич.
Цитомегаловирус – широко распространённый вирус семейства герпесвирусов. После окончания острого периода инфекция цитомегаловирусом обычно переходит в латентную форму, из которой может реактивироваться. Цитомегаловирус относят к так называемым оппортунистическим инфекциям: выраженные клинич.
Цитомегаловирус – широко распространённый вирус семейства герпесвирусов. После окончания острого периода инфекция цитомегаловирусом обычно переходит в латентную форму, из которой может реактивироваться. Цитомегаловирус относят к так называемым оппортунистическим инфекциям: выраженные клинич.
Цитомегаловирусная инфекция входит в группу репродуктивно значимых инфекций, обозначаемых как TORCH-комплекс (название образовано начальными буквами в латинских наименованиях - Toxoplasma, Rubella, Cytomegalovirus, Herpes); первичное инфицирование данными возбудителями, либо обострение .
К каким врачам обращаться
С первичными жалобами пациенты обращаются к врачу-терапевту или врачу общей практики (семейному врачу), детей ведет врач-педиатр . Могут потребоваться консультации инфекциониста - для верификации диагноза, стоматолога - при поражениях слизистой оболочки рта, кардиолога - при наличии врожденного порока сердца, нейрохирурга - при пороках центральной нервной системы, невропатолога - для оценки неврологической патологии, гематолога - при выраженных гематологических изменениях и геморрагическом синдроме, окулиста - для исследования глазного дна, отоларинголога - для исследования слухового аппарата.
Лечение цитомегаловирусной болезни
Субклинические формы ЦМВ-инфекции и латентное носительство крайне распространены, поэтому в большинстве случаев не требуют специфической терапии даже при выявлении антител. Их лечение направлено на усиление защитных сил организма при помощи иммуномодуляторов и профилактику факторов риска, которые приводят к обострению заболевания.
Для терапии клинически активных форм инфекции применяют:
- комплекс патогенетической (противовирусной) терапии, который разрабатывается профильными специалистами и включает препараты прямого противовирусного действия для минимизации риска осложнений, сокращения времени течения заболевания, а также профилактики рецидивов;
- иммунотерапию – антицитомегаловирусный иммуноглобулин назначают преимущественно детям при манифестных формах заболевания и беременным;
- дезинтоксикационную терапию, которая направлена на купирование синдрома интоксикации;
- метаболическую терапию - для восстановления обмена веществ в организме;
- симптоматическую терапию - для купирования воспалительных и токсических проявлений заболевания.
Проблема клинически выраженной инфекции актуальна для лиц, имеющих иммуносупрессию иной природы, в частности, онкогематологических пациентов, больных лучевой болезнью, лиц, длительно принимающих кортикостероидную, туберкулостатическую терапию, а также перенесших ожоговую травму.
Острое течение ЦМВ может привести к развитию гепатита с повышением уровня аминотрансфераз и атипичным лимфоцитозом.
Ученые предполагают роль цитомегаловируса как одного из кофакторов в развитии системных васкулитов, хронических диссеминированных заболеваний легких (в частности, фиброзирующего альвеолита), криоглобулинемии, опухолевых процессов (аденокарциномы предстательной железы, аденокарциномы толстой кишки, рака шейки матки), атеросклероза, кардиомиопатии, детского церебрального паралича, эпилепсии, синдрома Гийена-Барре, синдрома хронической усталости, аутизма.
Первичное инфицирование цитомагаловирусом у беременных женщин существенно повышает риск преждевременных родов, самопроизвольного выкидыша, многоводия, замершей беременности, внутриутробного инфицирования и даже гибели плода. Врожденная ЦМВ-инфекция может стать триггерным фактором развития тяжелых генерализованных форм и инвалидизирующих исходов заболевания, таких как потеря слуха, зрения, умственная отсталость, микроцефалия, судорожный синдром и пр. Такие пожизненные проблемы со здоровьем развиваются примерно у каждого пятого ребенка с врожденной цитомегаловирусной инфекцией.
Профилактика цитомегаловирусной болезни
Женщинам, планирующим беременность, необходимо пройти обследование на наличие ЦМВ. При обнаружении вируса важно получить консультацию врача-иммунолога.
Профилактика или превентивное лечение (активный мониторинг пациентов по уровню вирусной нагрузки и назначение противовирусных препаратов пациентам с признаками инфекции) являются эффективными способами предотвращения развития цитомегаловирусной инфекции после трансплантации органов.
Информацию из данного раздела нельзя использовать для самодиагностики и самолечения. В случае боли или иного обострения заболевания диагностические исследования должен назначать только лечащий врач. Для постановки диагноза и правильного назначения лечения следует обращаться к Вашему лечащему врачу.
Инфекции (заболевания), передаваемые половым путем (ИППП, ЗППП) - группа мочеполовых инфекций. Заболеваемость ИППП является социальной проблемой, так как урогенитальные инфекции могут приводить к бесплодию или врожденным заболеваниям при внутриутробной передаче от матери плоду. По данным ВОЗ, ежедневно более 1 млн человек заражаются ИППП.
Существуют более 30 различных микроорганизмов (бактерий и вирусов), вызывающих урогенитальные инфекции и передающихся половым путем. Основные наиболее распространенные ИППП:
- Гонорея (триппер, возбудитель - гонококк Neisseriagonorrhoeae);
- Хламидиоз (возбудитель - хламидия трахоматис Chlamydia trachomatis;
- Трихомониаз (трихомоноз), возбудитель – трихомонада Trichomonas vaginalis;
- Инфекция, вызываемая микоплазмой гениталиум Mycoplasmagenitalium;
- Сифилис;
- ВИЧ-инфекция;
- Инфекции, вызываемые вирусами папилломы человека (ВПЧ);
- Герпес-вирусные инфекции (ВПГ 1 и 2 типов).
Основная проблема ИППП в том, что большинство случаев протекает бессимптомно или с неярко выраженными клиническими проявлениями. Но даже при таком течении высок риск развития осложнений.
Четыре ИППП - гонорея, хламидиоз, трихомониаз, микоплазменная инфекция (вызванная микоплазмой гениталиум) - имеют похожие проявления. Для их диагностики применяют сходные диагностические подходы.
Основные жалобы при вышеуказанныхИППП:
- Выделения из половых путей. При гонококковой инфекции появляются гнойные выделения из половых путей. Особенно они выражены у мужчин, в то время как у женщин больше половины случаев протекает без клинических проявлений. Трихомониаз характеризуется серо-желтыми выделениями. У женщин часто бывают пенистые выделения с неприятным запахом. При хламидиозе и инфекции, вызванной микоплазмой гениталиум, в основном, беспокоят слизисто-гнойные выделения.
- Зуд, жжение, дискомфорт в области наружных половых органов
- Болезненность во время половых контактов (диспареуния)
- Боль в низу живота
- Эрозии или язвы в области наружных половых органов
- Дискомфорт в верхних отделах дыхательных путей при развитии гонококкового фарингита
- Дискомфорт, покраснение глаз, гнойные или слизисто-гнойные выделения из глаз при развитии гонококкового или хламидийного коньюктивита
- Общеинтоксикационный синдром (утомляемость, повышение температуры) при развитии осложнений
- Боли в суставах при развитии реактивного артрита при хламидиозе
Основные осложнения ИППП.
- Воспалительные заболевания органов малого таза (ВЗОМТ)
- Орхит (воспаление яичек) и эпидидимит (воспаление придатков яичек)
- Простатит
- Бесплодие
- Реактивный артрит при хламидиозе
Нужно помнить, что более половины случаев ИППП протекают без клинических проявлений! Но несмотря на отсутствие жалоб сохраняется высокая вероятность развития осложнений! Поэтому даже бессимптомное течение при лабораторном подтверждении диагноза требует обязательного лечения! Половые партнеры у лиц с установленным ИППП должны быть обследованы!
Кому нужно сдать анализ на ИППП?
- Пациентам с жалобами на выделения из половых путей, зуд, жжение в области наружных половых органов;
- Лицам с болями в низу живота (в области малого таза);
- При подготовке к беременности (обследование обоих партнеров)
- Беременным
- При планировании гинекологических операций
- Лицам с отягощенным акушерско-гинекологическим анамнезом (невынашивание беременности, бесплодие, рождение детей с малым весом)
- Если у полового партнера подтвержден диагноз ИППП
- При наличии незащищенного полового контакта с неизвестным партнером
Диагностика
Особенностью ИППП является отсутствие какой-либо характерной клинической картины заболевания. При этом каждый возбудитель обладает индивидуальной чувствительностью к антибактериальным препаратам, т.е. лечение каждого из четырех ИППП (гонорея, трихомониаз, хламидиоз и инфекция, вызванная микоплазмой гениталиум) будет отличаться. Часто встречаются смешанные инфекции. Это значит, что одновременно можно заразиться несколькими возбудителями, и лечение должно быть скорректировано в зависимости от выявленного возбудителя ИППП. Поэтому для диагностики ЗППП нужны высокоточные и быстрые тесты!
В лаборатории CMDможно сдать следующие анализы на ИППП:
Так как часто одновременно с ИППП могут встречаться и нарушения микробиоценоза влагалища, кандидоз, рекомендуется сдавать комплексный тест на ИППП и выявления дисбиозов:
При использовании тестов ПЦР и NASBA необходимо руководствоваться следующими рекомендациями
При использовании методаNASBA с определением РНК микроорганизма мазки рекомендуется брать не ранее, чем через 14 дней после окончания приема антибактериальных препаратов, при применении ПЦР – не ранее, чем через месяц. Мазки из уретры необходимо брать не ранее, чем через 3 часа после последнего мочеиспускания, мазки из цервикального канала из влагалища брать вне менструации.
Читайте также:

