Инфекции после операции на шве после
Обновлено: 17.04.2024
Послеоперационные осложнения ранений шеи - причины, лечение
К осложнениям раннего послеоперационного периода относятся тромбозы сосудов шеи, парезы и параличи голосовых связок, а также нагноение клетчаточных пространств, которое чаще протекает в форме флегмоны.
Спустя неделю и более после ранения могут выявляться артериовенозные фистулы, трахеопищеводные свищи, свищи слюнных желез, стенозы гортани и трахеи, глотки и пищевода.
Тромбоз крупных артериальных сосудов чреват нарушением мозгового кровообращения и подлежит хирургическому лечению, объем которого определяет сосудистый хирург. Основной причиной послеоперационных тромбозов сосудов шеи является сужение просвета сосуда продольным боковым швом. При огнестрельных ранениях, кроме того, на некотором расстоянии от дефекта стенки сосуда бывает повреждена интима, которая впоследствии начинает пролабировать в просвет сосуда, вызывая продолженный тромбоз.
Парезы и параличи голосовых связок являются следствием нарушения иннервации либо следствием грубых и поспешных хирургических манипуляций в ране. Эти осложнения лечатся с трудом и часто приводят к инвалидизации пострадавших.
Послеоперационные осложнения у пострадавших с ранениями шеи в подавляющем большинстве наблюдений носят гнойно-септический характер. Локальное нагноение ран наблюдается у 10-12 % пациентов с повреждением полых органов и первичным инфицированием на фоне массивной кровопотери. Признаки нагноения появляются на 2-5-с сутки после операции в виде усиления боли, гиперемии и отечности тканей в области операции. При наличии латексного выпускника повязка обильно промокает гнойным отделяемым. Общие проявления интоксикации в большинстве наблюдений отсутствуют, хотя имеется гипертермия и появляется лейкоцитоз с умеренным сдвигом формулы.
Лечение заключается в снятии кожных швов и открытом ведении раны до ее очищения и появления грануляций.
Флегмона клетчаточных пространств шеи в послеоперационном периоде развивается в 3-4% наблюдений у пострадавших с поздним поступлением при ранении пищевода, когда его содержимое контактирует с рыхлой околопищеводной клетчаткой, а также при ранении трахеи, когда инфицированный воздух из трахеи в виде массивной эмфиземы распространяется по межфасциальным пространствам шеи. Реже гнойный процесс протекает в виде ограниченного абсцесса.
Причина нагноения чаще всего заключается в неполноценной ревизии ран шеи, когда вместо продольной коллотомии используют экономное расширение каждой рапы и в условиях геморрагического пропитывания тканей не замечают ранения гортаноглотки, пищевода или трахеи. В таких случаях флегмона или абсцесс обычно возникают на 3-5-е сутки после ранения.
Клиническая картина флегмоны схожа с нагноением раны, но распространеность гнойного процесса на клетчаточные пространства шеи сопровождается быстрым нарастанием интоксикации (тахикардия, одышка, гектические размахи температуры тела, гиперлейкоцитоз со сдвигом формулы до метамиелоцитов и юных форм). Наиболее выраженные признаки гнойной интоксикации наблюдаются при неклостридиалыюй анаэробной флоре. В таких случаях при пальпации в окружности раны определяется крепитация, а на обзорных рентгенограммах — эмфизема мягких тканей.
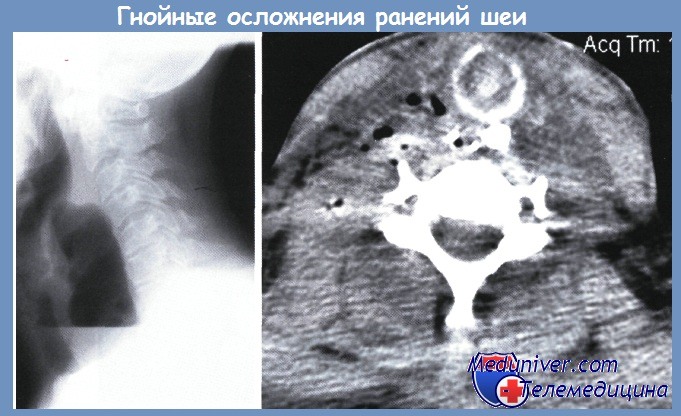
Обзорная рентгенограмма в боковой проекции у пациента с абсцессом мягких тканей шеи (а), КТ при флегмоне шеи (б)
В случаях поздней диагностики несостоятельности швов пищевода абсцесс достигает больших размеров (рис. а) и может сдавливать просвет трахеи, приводя к стридорозному дыханию. Нарушение дыхания у таких пациентов является вторичным, и при опорожнении полости абсцесса стридорозное дыхание сразу исчезает. Наложение трахеостомы в таких случаях не только не показано, но и крайне нежелательно из-за неизбежного инфицирования просвета трахеи из окружающих воспалённых тканей.
Признаки флегмоны шеи на КТ выглядят как увеличение объема мягких тканей шеи за счет клетчаточных пространств и утолщения мышц. Плотность паратрахеальной, параэзофагеальной и заглоточной клетчатки повышена до значений плотности жидкости с включением линейных мягких тканей и газа (рис. б). Плотность мышц шеи, напротив, снижена, они утолщены, контуры их нечеткие.
Лечение флегмоны заключается в снятии всех швов и широком вскрытии клетчаточных пространств путем передней продольной коллотомии (при тотальном поражении — двусторонней), разрушении инфильтрированной гноем клетчатки с образованием хорошо опорожняемых полостей. Тщательная ревизия при этом позволяет определить первичный очаг нагноения и его причину (оставление инородного тела, незамеченные дефекты стенки пищевода, трахеи, несостоятельность швов этих органов и т.д.).
Иссечение некротизированных тканей на шее является небезопасной процедурой, поэтому в таких случаях приходится идти на открытый метод ведения с ежедневными перевязками, санацией полостей и их рыхлой тампонадой. Дефекты стенок пищевода и трахеи предварительно ушивают атравматическим шовным материалом и прикрывают мышечным лоскутом из грудино-ключично-сосцевидной мышцы.
Однако в большинстве наблюдений после вскрытия и санации клетчаточных пространств через коллотомические доступы лучше дренировать все карманы двухпросветными трубками ТММК, выведенными через проколы мягких тканей, а операционные раны герметично ушить для проведения аспирационно-промывного лечения.
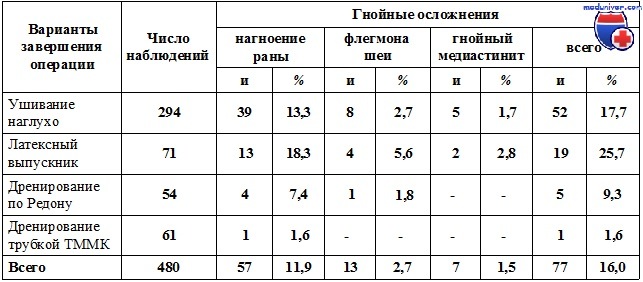
Частота гнойных осложнений в зависимости от вариантов завершения операции
Отмывание по дренажам экссудата, продуктов распада тканей и микробной флоры, как показывает опыт, обеспечивает быстрое купирование гнойного процесса, спадение полостей, образованных при вскрытии и санации флегмоны. Заживление ран при этом происходит по типу первичного натяжения, без образования грубой соединительной ткани. Поэтому и при открытом ведении через некоторое время, когда произойдет очищение полостей от некротических тканей и воспалительный процесс начнет регрессировать, для ускорения процесса заживления мы рекомендуем образовавшиеся полости дренировать трубками ТММК и закрыть раны кожными швами с последующим аспирационно-промывным лечением.
У пациентов, поступивших с уже возникшей флегмоной мягких тканей шеи, может развиться нисходящий гнойный медиастинит. Медиастинит возникает через 5-8 сут после ранений шеи. В наших наблюдениях частота его составила 1,5% от числа всех ранений шеи. Клинически гнойный медиастинит, протекающий, как правило, в форме флегмоны клетчатки средостения, практически невозможно дифференцировать от флегмоны шеи.
Кроме гнойного медиастинита, имеется еще одно, специфическое для ранений шеи осложнение, возникающее вне зоны шеи. Это — абсцедирующая аспирационная пневмония. Множественные абсцессы легких (чаще -правого легкого) возникают в 2-3% наблюдений, когда через рану трахеи происходит аспирация крови на догоспитальном этапе. Диагностика медиастинита и абсцессов легкого (основой которой является рентгенография и СКТ груди), а также комплекс хирургических методов их лечения изложены ниже, в разделе осложнений ранений груди.
Артериальные ложные аневризмы и артериовенозные свищи при активной хирургической тактике встречаются крайне редко, при неадекватно выполненной ревизии ран шеи. Напротив, при так называемой избирательной тактике с предпочтением консервативного лечения частота таких осложнений, по данным некоторых авторов, достигает 50% [Pate J.W., Castini M.].
Ложная аневризма артерий шеи несет в себе потенциальную опасность разрыва и смертельного кровотечения. Артериовенозный свищ на шее, вследствие шунтирующего эффекта, ведет к увеличению объема крови, поступающей в правые отделы сердца, одновременно обедняя кровоснабжение головного мозга. В результате достаточно быстро наступают серьезные нарушения гемодинамики. В диагностике этих осложнений используют прежде всего ультразвуковую доплерографию, данные которой дополняют ангиографией.
Хирургическое лечение таких осложнений является достаточно сложным и опасным, сопровождаясь в 24-25% наблюдений неврологическими нарушениями [Rittenhouse E.A. et al.], поэтому в последнее время предпочтение отдают эндоваскулярным методам лечения. Первое в мире закрытие травматической фистулы между сонной артерией и яремной веной путем введения в сонную артерию кусочков мышечной ткани произвел В. Brooks в 1930 г. Эндоваскулярная окклюзия заключается в создании временного или постоянного препятствия для кровотока путем введения в сосуд склерозирующих препаратов, различной формы эмболов или электродов для коагуляции крови в просвете сосуда. Однако наиболее эффективным является установка в зоне артериовенозного свища сосудистого протеза (стент-графта).
Стриктуры гортани и трахеи и трахеопищеводные свищи как осложнения ранений шеи развиваются при обширных дефектах мягких тканей вследствие огнестрельных ранений.
В послеоперационном периоде у тяжелых больных при высоких стриктурах трахеи ограничиваются наложением трахеостомы, а при наличии трахеопищеводного свища выключают пищевод из пассажа пищи, накладывая гастростому с одновременным формированием антирефлюксной манжеты по Ниссену.
Реконструктивные операции выполняют в отсроченном порядке, после решения всех проблем, связанных с последствиями ранений груди и живота.
Свищи слюнных желез наблюдаются, когда при ранениях третьей зоны шеи пересекаются крупные протоки подчелюстных желез. Если консервативное лечение на протяжении 2-3 нед. не приводит к успеху, прибегают к хирургическому лечению, которое заключается в иссечении свища и наложении мерсиленовых швов на капсулу. В литературе имеются ссылки на необходимость удаления подчелюстной железы, несущей свищ. Такими наблюдениями мы не располагаем.
В 0,1-0,5% наблюдений после ушивания ран шейного отдела пищевода формируются дивертикулы. Посттравматические дивертикулы обычно имеют широкую шейку и небольшие размеры, хорошо опорожняются при даче контрастного вещества. Они могут развиваться вследствие консервативного лечения несостоятельности одного из швов с ограниченным очагом воспаления. В отдаленном периоде они развиваются вследствие стягивающего действия Рубцовых тканей (тракционпые дивертикулы). Хирургическое лечение такого рода дивертикулов производят в отдаленном периоде, и оно не представляет каких-либо сложностей.
В наших наблюдениях общая послеоперационная летальность при изолированных, множественных и сочетанных ранениях шеи составила 3%, а в группе пострадавших с осложнениями — 7,3%.
Редактор: Искандер Милевски. Дата обновления публикации: 18.3.2021
Нагноение раны после операции в гинекологии
В результате проспективного исследования было обнаружено, что более 62 000 операционных ран инфицированы. Степень инфицированности ран заметно варьирует в зависимости от степени контаминации операционного поля. Риск инфицирования раны в стерильных хирургических условиях (инфекция в операционной отсутствует, нет нарушений в асептических мероприятиях, не вскрывают внутренний орган) менее 2 %, тогда как в нестерильных условиях он составляет 40 % и более.
До операции проводят обработку поверхности кожи гексахлорофеном для профилактики инфицирования операционных ран, но в то же время бритье волос в месте оперативного вмешательства увеличивает риск инфицирования. Обработка хирургического поля за 5 мин до операции была такой же эффективной, как и за 10 мин до ее начала. Риск раневой инфекции увеличивался при длительном нахождении в стационаре, так же как и при продолжительной операции.

Симптомы инфицирования ран часто выявляются после операции, в основном через 4 дня, и включают лихорадку, эритему, болезненность, индурацию и гнойные выделения из раны. Причиной раневых инфекций, обнаруженных в 1—3-й день, как правило, бывают стрептококковые и клостридиальные инфекции. Лечение раневых инфекций обычно механическое: вскрытие инфицированного участка раны над фасцией, очистка краев раны, если это необходимо.
Ведение операционной раны включает санацию и смену марлевой повязки 2 или 3 раза в сутки, что способствует росту грануляционной ткани на месте дефекта после вторичной операции с постепенным рубцеванием. Использование специальной вакцины при больших ранах ускоряет заживление и уменьшает количество перевязок. Чистота и гранулирование раны часто помогают сократить время, необходимое для полного вторичного се заживления.
Метод отсроченного заживления первичной раны может быть использован, чтобы снизить вероятность раневой инфекции. Кратко об этом методе: до начала хирургической процедуры операционная рана остается открытой выше фасции. Вертикальный узловой шов через кожу и подкожную клетчатку накладывают, отступив 3 см от края, не соединяя края раны. Сразу же после операции за раной устанавливают контроль до тех пор, пока рана не начнет хорошо гранулироваться.
Затем шов можно соединить, близлежащие края кожи сшивают или скрепляют. При использовании метода отсроченного заживления первичной раны было показано, что у больных с высоким риском общий показатель раневой инфекции снижается с 23 до 2,1 %.
Инфицирование культи влагалища после гистерэктомии характеризуется эритемой, индурацией и болезненностью культи. Иногда отмечаются гнойные выделения из верхнего отдела влагалища. Параметрит часто бывает ограниченным и не требует лечения. Лихорадка, лейкоцитоз и боль в полости таза могут быть связаны с выраженным воспалением рыхлой клетчатки культи влагалища, которое нередко распространяется на параметрий. В таких случаях показана терапия антибиотиками широкого спектра действия против грамотрицательных, грамположительных и анаэробных микроорганизмов.
Если в культе влагалища существует обширное нагноение или в ней замечены флуктуирующие массы, ее следует тщательно исследовать, вскрыть тупым инструментом и оставить открытой для дренирования.

Редактор: Искандер Милевски. Дата обновления публикации: 18.3.2021
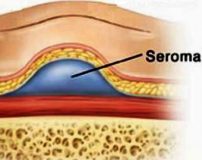
Послеоперационная серома – это скопление серозной жидкости в зоне шва, обусловленное травматизацией мягких тканей. Является осложнением хирургических вмешательств. Рассасывается самостоятельно либо принимает хроническое течение. Проявляется припухл остью в области шва, чувством распирания, неприятными ощущениями и эффектом переливания жидкости при перемене положения тела. При крупных серомах наблюдаются нарушение общего состояния, субфебрилитет. Патология может осложняться инфицированием, формированием некроза. Лечение – пункции или дренирование с активной аспирацией на фоне медикаментозной терапии. В отдельных случаях требуются повторные операции.
МКБ-10


Общие сведения
Послеоперационная серома (серома шва) – распространенное осложнение раннего послеоперационного периода. Чаще всего встречается в общей хирургии, маммологии, онкологии и пластической хирургии. По различным данным, частота образования клинически значимых сером после операций, сопровождающихся значительной отслойкой мягких тканей, колеблется от 0,8% до 80% и более. Осложнение может развиваться у пациентов любого возраста и пола, чаще встречается у женщин средней и старшей возрастной группы.

Причины
Серома является полиэтиологическим состоянием, рассматривается как осложнение обширных хирургических вмешательств. Некоторые специалисты придерживаются мнения, что скопление жидкости в проекции послеоперационной раны нельзя считать осложнением, поскольку оно представляет собой нормальный процесс заживления в фазе экссудации.
В подтверждение своей точки зрения ученые приводят данные ультразвуковых исследований, согласно которым послеоперационные серомы (в том числе – клинически незначимые) обнаруживаются у 100% пациентов. Основными провоцирующими факторами образования крупных сером, требующих проведения активных лечебных мероприятий, являются:
- значительная отслойка жировой клетчатки;
- большая раневая поверхность;
- грубые хирургические манипуляции с тканями (многочисленные разрезы, захват раздавливающим инструментом и пр.);
- чрезмерное использование коагуляции;
- большая толщина подкожной жировой клетчатки (более 5 см).
К числу предрасполагающих условий относят индивидуальные особенности организма, нарушения иммунитета, сахарный диабет и хронические соматические заболевания, негативно влияющие на процесс заживления раны. Чаще всего послеоперационные серомы образуются после абдоминопластики, герниопластики, маммопластики, мастэктомии, аппендэктомии, холецистэктомии. При использовании имплантатов имеет значение раздражение окружающих тканей и развитие асептического воспаления вследствие контакта с эндопротезом.
Патогенез
Существуют различные точки зрения на патогенез сером. Согласно наиболее популярной, обширные разрезы, отслойка мягкотканных структур, раздавливание или прижигание тканей и другие факторы вызывают значительные повреждения мелких лимфатических сосудов. Лимфатические сосуды тромбируются медленнее кровеносных, в результате лимфа долгое время изливается в ткани. На этапе экссудации жидкая часть крови выходит за пределы кровеносных сосудов, что увеличивает количество жидкости в тканях.
В полостях, возникших в области послеоперационной раны, скапливается соломенно-желтая жидкость, содержащая макрофаги, тучные клетки, лейкоциты и белковые фракции. В норме эта жидкость асептическая. При попадании микроорганизмов возможно нагноение с формированием абсцесса. Крупные скопления жидкости оказывают давление на окружающие ткани, нарушают кровоснабжение, вследствие чего могут образовываться участки некроза по краю швов.
Классификация
В клинической практике используют классификацию, в основе которой лежит необходимость и тактика лечения патологии. Согласно этой систематизации выделяют три группы послеоперационных сером:
- 1 группа. Асимптоматические образования, не требующие проведения лечебных мероприятий.
- 2 группа. Симптоматические серомы, для устранения которых достаточно пункций или активного дренирования.
- 3 группа. Симптоматические скопления жидкости, требующие проведения повторной операции.

Симптомы послеоперационной серомы
Маленькие образования не вызывают неприятных ощущений и нарушений общего состояния. Единственными признаками серомы являются припухлость и положительный симптом флюктуации в области послеоперационных швов. Иногда пациенты отмечают ощущение переливания жидкости во время изменения положения тела. Гиперемия кожи в зоне швов обычно отсутствует.
Больные с крупными серомами жалуются на неинтенсивную тянущую боль, чувство давления или распирания, которые усиливаются в положении стоя. В проекции швов выявляется валикообразная флюктуирующая припухлость. Длина припухлости обычно совпадает с длиной шва, ширина может варьироваться от 2-3 до 10 и более сантиметров. Возможны локальная гиперемия, слабость, утомляемость, повышение температуры тела до субфебрильных цифр.
Осложнения
Наиболее серьезным осложнением является нагноение серомы. При большом количестве жидкости формируются крупные абсцессы. Возможно расплавление подлежащих тканей с развитием перитонита. У некоторых больных развивается сепсис. Некрозы при серомах, как правило, протекают более благоприятно, захватывают небольшие участки тканей в области швов. Хронические серомы ухудшают качество жизни, существенно увеличивают период нетрудоспособности после операций.
Диагностика
Обычно серомы развиваются в период стационарного послеоперационного лечения, поэтому диагноз выставляется лечащим врачом. Диагностика базируется на данных объективного осмотра, при необходимости назначаются дополнительные исследования. Программа обследования может включать:
- Физикальный осмотр. В пользу серомы свидетельствует наличие ограниченного выбухания тканей в сочетании с положительным симптомом флюктуации. При отсутствии инфицирования гиперемия не выявляется или незначительная, пальпация малоболезненна. При инфицировании кожа багрово-синюшная, ощупывание резко болезненно, определяется плотный отек окружающих тканей.
- УЗИ мягких тканей. Показано для подтверждения диагноза при сомнительном симптоме флюктуации, для уточнения размеров крупных сером на этапе подготовки к хирургическому вмешательству. Свидетельствует о наличии полости, заполненной жидкостью.
- Лабораторные анализы. Для изучения характера содержимого серомы проводят цитологическое исследование. При подозрении на инфицирование выполняют бакпосев жидкости для определения возбудителя, назначают общий анализ крови для оценки выраженности воспаления.

Лечение послеоперационной серомы
Лечение осуществляется в стационарных условиях. При крупных образованиях, отсутствии признаков рассасывания показана комплексная терапия, включающая в себя консервативные и оперативные мероприятия.
Консервативная терапия
Целью консервативного лечения является снижение вероятности инфицирования, устранение асептического воспаления, уменьшение количества жидкости. Применяются медикаменты следующих групп.
- Антибиотики. При отсутствии нагноения пациентам для профилактики назначают препараты широкого спектра действия внутримышечно. При появлении признаков инфицирования план антибиотикотерапии корректируют с учетом чувствительности возбудителя.
- НВПС. Нестероидные противовоспалительные средства уменьшают проявления воспаления и количество жидкости, выделяющейся в просвет полости послеоперационной серомы. Возможно внутримышечное введение или пероральный прием.
- Глюкокортикоиды. Гормональные препараты устраняют асептическое воспаление, блокируют образование жидкости. Медикаменты вводят в полость серомы после удаления жидкости.
Хирургическое лечение
Тактика хирургического лечения определяется размерами серомы, эффективностью лечебных мероприятий на предыдущих стадиях. При неосложненных серомах возможны следующие варианты:
- Пункции. Наиболее простой способ удаления жидкости. Выполняется 1 раз в несколько дней, для полного излечения обычно требуется 3-7 пункций.
- Активная аспирация. При неэффективности пункций, значительном объеме серомы в полость образования устанавливают дренаж с устройством для активной аспирации.
- Реконструктивные операции. Показаны при упорном хроническом течении сером, отсутствии результата после лечения более щадящими способами.
При нагноившихся серомах производится вскрытие, дренирование гнойной полости. При образовании участков некроза проводят перевязки до отторжения струпа и полного заживления раны. Все хирургические методы применяют на фоне консервативной терапии.
Прогноз
Прогноз в большинстве случаев благоприятный. Небольшие серомы нередко рассасываются самостоятельно в течение 1-2 недель. Эффективность пункций при серомах на фоне плановых пластических и абдоминальных операций составляет около 90%. Реконструктивные вмешательства требуются редко. Процент нагноений незначительный, осложнение чаще развивается после экстренных операций, при наличии сопутствующей патологии, излишнем весе.
Профилактика
Профилактические мероприятия включают тщательную оценку риска хирургических вмешательств, детальное предоперационное обследование, соблюдение техники проведения операций. Хирургам необходимо воздерживаться от слишком широких разрезов, грубых манипуляций с тканями, чрезмерного использования коагулятора.
2. Клинический случай длительной лимфорреи, возникшей после радикальной мастэктомии/ Ивашков В.Ю., Соболевский В.А.// Поволжский онкологический вестник – 2015.
3. Проблемы профилактики раневых осложнений у больных с послеоперационными вентральными грыжами/ Постников Д.Г., Павленко В.В. и др.// Медицина и образование в Сибири - №3 – 2015.
Гной в послеоперационной ране говорит о развитии инфекционных осложнений. В ортопедии и травматологии они тяжело поддаются лечению и приводят к инвалидизации пациентов. Парапротезные инфекции обусловливают увеличение срока пребывания в стационаре и требуют затрат на борьбу с ними.

Выделения из ТБС.
Инфекции после эндопротезирования бывают поверхностными или глубокими, острыми или хроническими, развиваться в раннем или позднем послеоперационном периоде. Воспалительный процесс может затрагивать только мягкие ткани нижней конечности или распространяться на прооперированный сустав.
Если после эндопротезирования у вас появился гной в шраме, повысилась температура и возникли боли в ноге – немедленно идите к врачу. Тот осмотрит вас, назначит нужные исследования и выяснит, насколько тяжелое у вас состояние. Вам придется лечь в стационар и пройти курс лечения.
Актуальность проблемы
По разным данным, частота развития ранней парапротезной инфекции после первичной замены крупных суставов составляет 0,3-0,5%, после ревизионной – 9%. Воспалительные процессы выявляют в течение первых трех недель после хирургического вмешательства.
Если говорить о частоте развития поздних инфекционных осложнений, то чаще всего они возникают в первые два года после эндопротезирования (1,63% пациентов). Реже (у 0,59% прооперированных) глубокие парапротезные инфекции развиваются в последующие 8 лет после операции.
Частота инфекционных осложнений на протяжении нескольких десятилетий остается неизменной. Однако заметно увеличилось общее количество артропластик, выросло и общее число осложнений. Поэтому становится все более актуальной их профилактика, ранняя диагностика и лечение.
Факт! Как показали научные исследования, риск развития инфекционных осложнений зависит от вида эндопротеза. Выяснилось, что в общей сумме имплантация отечественных моделей приводит к воспалению чаще (3-10% случаев), чем установка импортных (0,3-4,8%).
Что такое инфекция в области хирургического вмешательства
ИОХВ – это острое или хроническое воспаление, развивающееся в месте разреза или в области, которая подвергалась ятрогенному воздействию в ходе хирургического вмешательства. В 67% случаев инфекция затрагивает только зону операционного разреза, в 33% – распространяется на имплантированный сустав.
Факторы развития ИОХВ:
- длительность операции более 3 часов;
- технические трудности во время хирургического вмешательства;
- интраоперационная кровопотеря более 1 литра; ;
- использование дополнительных синтетических и биологических материалов в ходе операции;
- наличие тяжелых хронических заболеваний.

Воспалительные процессы, которые не распространяются на прооперированный сустав, можно победить без ревизионного эндопротезирования. Если же инфекция затрагивает костную ткань, компоненты эндопротеза, остатки суставной капсулы или другие части коленного или тазобедренного сустава – лечить ее будет крайне тяжело. В этом случае больному скорее всего потребуется повторное эндопротезирование.
Существует ряд факторов, которые отягощают состояние пациента, замедляют выздоровление и ухудшают прогноз: снижение иммунитета, перенесенные операции, частое лечение антибиотиками. Стойкость обнаруженной микрофлоры к антибактериальным средствам, плохое кровообращение в области сустава, массивные гнойные очаги тоже осложняют терапию.


Виды парапротезной инфекции
В ортопедии и травматологии используют несколько классификаций ИОХВ. Систематизация и отнесение инфекции к конкретному виду помогает врачам оценить тяжесть состояния пациента. Классификация Coventry-Fitzgerald-Tsukayama самая распространенная.
Таблица 1. Типы глубокой парапротезной инфекции по Coventry-Fitzgerald-Tsukayama.
| Тип | Время развития | Тактика лечения | |
| I | Острая послеоперационная | 1-й месяц | Ревизия послеоперационной раны, удаление некротизированных тканей, при необходимости – замена некоторых частей эндопротеза при сохранении его основных компонентов. |
| II | Поздняя хроническая | От 1 месяца до 1 года | Обязательное ревизионное эндопротезирование. |
| III | Острая гематогенная | После 1 года | Вполне оправданной является попытка сохранить установленный протез. |
| IV | Положительные интраоперационные культуры | Бессимптомная бактериальная колонизация поверхности импланта | Консервативное лечение, заключающееся в парентеральной антибиотикотерапии на протяжении 6 недель. |
В классификации, созданной Новосибирским НИИТО, ИОХВ делят на ранние острые, поздние острые и хронические. Первые развиваются на протяжении трех месяцев после эндопротезирования, вторые – на 3-12 месяце, третьи – после 1 года. Инфекционные осложнения могут протекать в латентной, свищевой, флегмоноподобной или атипичной форме.
По распространенности инфекции бывают эпифасциальными (поверхностными) и субфасциальными (глубокими). Могут сопровождаться тотальной, бедренной или тибиальной нестабильностью.
Поверхностные и глубокие инфекции
Возникают в первый месяц после эндопротезирования. Характеризуются развитием воспаления в мягких тканях нижней конечности. Сам бедренный или коленный сустав остается интактным, то есть не вовлекается в патологический процесс. Причиной осложнения чаще всего является занесение в рану патогенных микроорганизмов во время хирургического вмешательства или в послеоперационном периоде.
- некроз кожных покровов;
- лигатурные свищи;
- расхождение краев раны;
- подкожная гематома.
- некроз парапротезных тканей; ;
- инфицированная субфасциальная гематома.
Факт! Незначительная болезненность, локальная припухлость, покраснение и гипертермия кожи в области шрама обычно указывают на поверхностную инфекцию, которая поддается лечению. Появление лихорадки, спонтанное расхождение швов и сильные боли в ноге позволяют заподозрить воспаление глубоких тканей. В этом случае прогноз менее благоприятный.
Инфекции протезированного сустава
При патологии воспаление распространяется на полости и оболочки прооперированного сустава, остатки синовиальной оболочки, кости в месте фиксации эндопротеза и прилегающие мягкие ткани. Причиной осложнения является колонизация поверхностей сустава патогенной микрофлорой. Бактерии могут попадать из внешней среды или заноситься гематогенным путем.
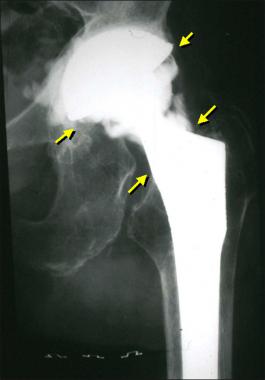
Так выглядит инфекция на рентгене.
Инфекции протезированного сустава самое грозное осложнение среди всех ИОХВ. Они не поддаются консервативной терапии, поэтому лечить их приходится хирургическим путем. Врачи заменяют эндопротез, однако иногда им все же удается сохранить его.
Существует три метода лечения инфекций протезированного сустава: ревизия раны без удаления импланта, ревизионное одноэтапное и двухэтапное эндопротезировение. Выбор методики зависит от состояния пациента, время манифестации инфекции, стабильности компонентов протеза и характера патогенной микрофлоры.
Методы диагностики ИОХВ
На наличие инфекционного процесса в области послеоперационной раны указывают гнойные выделения, боль, припухлость и локальное повышение температуры. Все эти симптомы появляются как при глубоких, так и при поверхностных инфекциях.
Рентгенологические исследования
Большую роль в дифференциальной диагностике свищевых форм инфекции играет рентгенофистулография. С ее помощью можно определить размер, форму и расположение свищей, выявить гнойные затеки и их связь с очагами костной деструкции. Это позволяет отличить поверхностные ИОХВ от глубоких.

Фото: Рентгенофистулография, свищ в нижней трети бедра.
Для диагностики инфекции протезированного сустава чаще всего используют рентгенографию. Метод на дает 100% верных результатов, однако позволяет заподозрить патологию. На наличие парапротезной инфекции указывает внезапное появление периостальной реакции и остеолиза. Если эти признаки возникают внезапно, вскоре после успешно проведенной операции, – есть повод заподозрить неладное.
Любопытно! МРТ, УЗИ и радиоизотопное сканирование в диагностических целях используют редко из-за их низкой информативности. К примеру, установленный эндопротез создает помехи при магнитно-резонансной томографии, что делает изображение размытым и нечетким.
Лабораторные анализы
Сдача анализов помогает выявить острые и хронические воспалительные процессы в организме. Повышение показателей не является достоверным признаком ИОХВ. Для постановки диагноза нужно учитывать наличие определенных клинических симптомом, данных рентгенографии и других методов исследования.
Клинически значимые лабораторные показатели:
- Количество лейкоцитов. Имеет значение в диагностике острой парапротезной инфекции. Ярким признаком воспаления является повышение общего количества лейкоцитов и нейтрофилов, сдвиг лейкоцитарной формулы влево.
- СОЭ. Является неспецифическим показателем. Нормальная скорость оседания эритроцитов говорит об отсутствии воспалительных процессов, повышенная – об их наличии.
- С-реактивный белок. СРБ является белком острой фазы воспаления и высокочувствительным маркером ИОХВ для людей, которым выполнили эндопротезирование. При диагностике парапротезных инфекций нужно обращать внимание именно на этот показатель.


Микробиологические исследования
Бактериоскопическое и бактериологическое исследования позволяют выявить и идентифицировать возбудителя инфекции, а также определить его чувствительность к антибиотикам. Количественные исследования дают возможность установить число микробных тел в гнойном отделяемом.
Для исследования могут использоваться такие материалы:
- отделяемое из раны;
- образцы ткани;
- жидкость из суставной полости;
- протезный материал.
При имплант-ассоциированной инфекции выявить бактерии в биологических жидкостях и тканях практически невозможно. Патогенные микроорганизмы обнаруживают на самих поверхностях эндопротезов. Они покрывают импланты в виде адгезивной пленки.
Факт! Кроме бактериологического исследования для диагностики могут использовать ПЦР – полимеразную цепную реакцию. Метод имеет высокую чувствительность, но низкую специфичность. Из-за этого он нередко дает ложноположительные результаты.
Лечение
Прежде чем решить, как бороться с инфекцией, врачи тщательно обследуют пациента. Лишь установив диагноз и определив чувствительность патогенной микрофлоры к антибиотикам, они принимают окончательное решение.
Таблица 2. Методы лечения парапротезных инфекций:
Имплант-сохраняющая тактика
Ее главная цель – устранение инфекционного процесса при одновременном сохранении эндопротеза. Больному проводят хирургическую обработку раны, в ходе которой удаляют гной и некротизированные ткани. При вовлечении в патологический процесс самого сустава выполняют артроскопический дебридмент. Больному назначают массивную антибактериальную терапию.
Любопытно! Научные исследования доказали эффективность безоперационного лечения ранних глубоких инфекций. Как выяснилось, комбинация антибиотиков и ферментных препаратов помогает ликвидировать воспаление за 5-7 дней.
Ревизионные операции
Выполняются в тех случаях, когда врачам не удается сохранить сустав. Хирурги полностью удаляют эндопротез, а на его место ставят новый. Риск повторного развития инфекции после ревизионного эндопротезирования выше, чем после первичного.

Читайте также:

