Инфекционные болезни нервной системы и интоксикации
Обновлено: 26.04.2024
Наша клиника специализируется в неврологии и иммунологии. У нас работают неврологи с дополнительной подготовкой по иммунологии. Мы используем комплексный подход к лечению заболеваний нервной системы, в том числе занимаемся диагностикой и лечением демиелинизирующих заболеваний.
Инфекция. Инфекционное и постинфекционное поражение нервной системы
Инфекционное поражение нервной системы – это воспаление различных ее отделов:
- Оболочек головного и/или спинного мозга (менингит, арахноидит);
- Вещества головного мозга (энцефалит) или спинного мозга (миелит);
- Периферических нервов (неврит, полиневрит);
- Нервных корешков спинного мозга (радикулит);
- Нервных сплетений (плексит);
- Нервных узлов (ганглионит).
Как инфекция повреждает нервную систему? Возможны два варианта:
В норме с большинством потенциально опасных инфекций каждый из нас встречается периодически или постоянно. При этом заболевание не наступает, пока иммунная система в состоянии защитить организм. Опасность поджидает при снижении иммунной защиты. Микробы, не встречая должного сопротивления, внедряются в организм и часто сами еще больше блокируют работу иммунной системы (вторичное иммунодефицитное состояние).
Лечение только инфекции, без коррекции иммунного ответа, почти всегда неэффективно из-за повторного заражения. Поэтому, планируя лечение, мы подробно исследуем Ваш иммунный статус и антитела к ряду инфекций. Когда картина иммунитета и инфекционного фона ясна, составляется план лечения, охватывающий две задачи:
- Подавить инфекцию;
- Отрегулировать работу иммунной системы.
Онкология и поражение нервной системы
Многие злокачественные опухоли способствуют образованию в организме большого количества токсинов и иммунных факторов, агрессивных к собственным тканям организма, в т.ч. к головному и спинному мозгу, к периферическим нервам, мышцам. Паранеопластическое заболевание нервной системы – это повреждение нервной системы не опухолью, а иммунной системой под влиянием опухоли. У нас есть специалисты и современные лабораторные тесты для диагностики паранеопластических заболеваний нервной системы и опыт их лечения.
Интоксикация и аутоиммунная агрессия могут стать причиной паранеопластических синдромов и повреждения:
- мышц,
- периферических нервов,
- головного и спинного мозга.
Симптомы паранеопластических процессов могут быть самыми разнообразными:
Какие ткани нервной системы могут пострадать при паранеопластических синдромах?
- Периферические нервы – полинейропатия и полиневрит.
- Мышцы – миопатия и полимиозит.
- Головной мозг – энцефалопатия, энцефалит.
- Спинной мозг – миелопатия.
Аутоиммунная агрессия. Аутоиммунный процесс
Некоторые заболевания нервной системы связаны с агрессией организма против самого себя, а именно, с атакой иммунной системы на ткани собственной же нервной системы (демиелинизация). Некоторые аутоиммунные заболевания провоцируются инфекцией. Прежде чем составить план лечения, мы подробно исследуем Ваш иммунный статус и инфекционный фон.
Наша основная задача – найти причину аутоиммунной агрессии и предотвратить ее дальнейшее развитие. Во многих случаях реально ввести аутоиммунный процесс в длительную ремиссию или остановить его совсем.
Примеры аутоиммунных болезней нервной системы:
Аналогичные явления наблюдаются при ревматических болезнях, когда иммунная агрессия направлена против суставов, связок, мышц, кровеносных сосудов.
Причины аутоиммунных процессов
Почему появляются аутоиммунные болезни? Обычно этому способствует неудачное совпадение трех основных факторов:
Известен “феномен декомпактизации миелина”, когда в результате инфекционного или аутоиммунного повреждения обнажаются глубоко залегающие антигены миелина, с которыми иммунная система в норме вообще не контактирует. Эти антигены воспринимаются иммунной системой как чужеродные, к ним образуются аутореактивные иммунокомпетентные клетки и антитела (аутоантитела), запускающие дальнейшую иммунную агрессию.

Молекулярная мимикрия и аутоиммунная реакция. Антигены некоторых микробов похожи на аутоантигены здоровых клеток организма. 1-Клетка иммунитета; 2-Инфекционный агент; 3-Нерв; 4-Одинаковые рецепторы.
Образовавшиеся агрессивные аутоантитела могут участвовать в перекрестной аутоиммунной агрессии и к другим тканям организма. Поэтому пациентов с демиелинизирущими заболеваниями мы часто обнаруживаем и другие аутоиммунные процессы:
-
(воспаление щитовидной железы); ; ;
- Антитела к инсулину и бета-клеткам поджелудочной железы (риск сахарного диабета и ожирения).
Лечение аутоиммунных заболеваний
Лечение любого аутоиммунного заболевания предполагает снижение аутоиммунной агрессии.
Наиболее убедительные результаты лечения мы получаем от воздействия сразу на три звена аутоиммунного процесса:
Стресс. Психический стресс. Снятие психического стресса
Природа стресса. Стресс – это сверхсильный ответ организма на опасные обстоятельства. Стрессовый ответ на опасность обеспечивают эволюционно древние нижние отделы мозга, доставшиеся нам еще от рыбы (вегетативная нервная система).
Стресс у человека, как и у любого животного, приводит к повышению физических возможностей тела (быстро бегать, драться и др.), за счет ранее накопленных ресурсов. Все это происходит независимо от сознания.
Например, на Вас кто-то накричал. В ответ Ваше сердце забилось, накачивая кровь в мышцы, мышцы напряглись, зрачок расширился для улучшения зрения, дыхание активизировалось, насыщая мышцы кислородом, хотя физическая опасность Вам не угрожает и силовой ответ не требуется.

Стрессорная реакция в процессе эволюции изменилась не сильно – при стрессе организм готовится к отражению физической угрозы, даже, если физически никто не угрожает.
У социального человека подобные реакции обычно не реализуются в поведении, а значит, длительно сохраняются в виде нереализованной поведенческой реакции. А если Вы эмоциональны, но очень хорошо контролируете свое поведение? Это означает, что нервная система будет длительно держать тело в переактивированном состоянии, расходуя при этом огромное количество ресурсов.
При этом происходит постепенное истощение нервной системы и разлад обмена веществ.
Стресс и иммунитет. В хроническом стрессе иммунитет становится более агрессивным, но быстро истощается, теряя целенаправленность иммунного ответа.
В ответ на внедрение инфекции возможен очень сильный, но недостаточно целенаправленный ответ, с иммунной атакой против собственных тканей организма:
Поэтому в лечении аутоиммунных заболеваний нервной системы:
Уменьшение стрессового напряжения в нервной системе приводит к значительным изменениям в лабораторных показателях иммунного статуса и в самочувствии.
Нарушение обмена веществ
Самые разные обменные нарушения в организме могут стать причиной страдания нервной системы т.к. она очень требовательна к обеспечению питанием и очень чувствительна к токсическому воздействию продуктов нарушенного обмена веществ. В нашей клинике неврологи работают в тесном сотрудничестве с эндокринологом, при необходимости мы предложим Вам совместную консультацию.
Чаще всего мы обнаруживаем два варианта обменного поражения нервной системы:
-
– это страдание волокон периферических нервов (нервов конечностей, зрительных и слуховых нервов);
- Энцефалопатия – это страдание вещества головного мозга.
Возможно сочетание полинейропатии и энцефалопатии.
Лечение в нашей клинике включает в себя:
- коррекцию нарушений обмена веществ,
- восстановительное лечение для нервной системы (детоксикация, ноотропы, витамины, магнитная стимуляция, гимнастика и др.).

Лечение нарушения обмена веществ в клинике “Эхинацея”
Некоторые заболевания, при которых происходят нарушения обмена веществ, пагубное для нервной системы:
-
– одна из частых причин полинейпропатии. Подробнее здесь
- Гипоталамический синдром часто сопровождается инсулинорезистентностью, т.е. невосприимчивостью клеток к действию гормона инсулина. Нервная система при этом не в состоянии усвоить достаточное количество глюкозы. Это возможная причина развития полинейропатии и энцефалопатии. Подробнее здесь.
- Гипотиреоз, Тиреотоксикоз и Тиреоидит – это заболевания щитовидной железы и частая причина страдания нервной системы. Подробнее здесь.
- Нарушение функции паращитовидных желез приводит к нарушению кальциево-фосфорного обмена и отложению кальция в подкорковых ядрах головного мозга. Это возможная причина мышечных судорог, гиперкинезов и вторичного паркинсонизма. Подробнее здесь.
- Печеночная и почечная недостаточность – возможные причины страдания головного мозга и периферических нервов. Характерно повышенное содержание мочевины, креатинина, АЛТ, АСТ. ГГТ в биохимическом анализе крови.
- Дефицит витаминов, особенно витаминов группы В может быть причиной полинейропатии. Типичный случай – дефицит витаминов группы В при регулярном употреблении алкоголя.
- Болезни накопления приводят к отложению в тканях нервной системы каких-либо веществ (медь, марганец, кальций и др.), и гибели ее клеток.
Дисциркуляторная энцефалопатия, нарушение кровообращения
Нервная система человека расходует огромное количество энергии, и поэтому очень зависима от обеспечения питанием. Доставка кислорода, глюкозы и других необходимых веществ обеспечивается артериальной кровью. С венозной кровью эвакуируются подлежащие утилизации продукты обмена веществ. При дефиците кровоснабжения мозговое вещество или постепенно атрофируется (энцефалопатия) или гибнет в течение нескольких часов (инсульт).
Нарушение мозгового кровообращения может быть связано с сужением и закупоркой кровеносных сосудов по различным причинам:
- Васкулит (воспаление кровеносных сосудов из-за иммунной атаки или инфекции). Это довольно опасное заболевание приводит обычно к постепенной мелкоочаговой гибели вещества головного мозга. При МР-томографии васкулит часто путают с различного рода энцефалопатиями, рассеянным склерозом. Подробнее здесь
- Атеросклероз – это отложение жира (холестерина) между слоями внутренних стенок кровеносных сосудов. Отложение происходит в виде бляшек. Бляшки выбухают внутрь артерий и препятствуют току крови, вызывая хронический дефицит кровообращения, с постепенной атрофией мозгового вещества. Наибольшую опасность представляют разорвавшиеся бляшки, жировые массы из которых попадают в кровь и закупоривают меньшие по диаметру артерии (инсульт, острое нарушение мозгового кровообращения, инфаркт мозга).
- Повышение свертываемости и вязкости крови препятствует похождению крови по самым мелким кровеносным сосудам (капиллярам) и вызывает хронический дефицит кровоснабжения мозга. Кроме того, возможно внутрисосудистое свертывание крови с закупоркой сосуда (инсульт, острое нарушение мозгового кровообращения, инфаркт мозга).
- Сдавление или извитость кровеносного сосуда. Обычно страдают артерии, проходящие через шейные позвонки (позвоночные артерии), что является причиной головокружения, потери равновесия, зрительных и слуховых расстройств.
Лечение нарушения мозгового кровообращения в нашей клинике начинается с точного обнаружения его причины. Так мы подбираем метод лечения, реально эффективный именно в данном случае. Для диагностики мы используем:
-
на жиры, маркеры васкулита и свертываемость;
- УЗДГ и/или МР-ангиографию для уточнения места сужения кровеносного сосуда;
- Рентгенографию, КТ или МР-томографию для поиска опасных для сосудов деформаций шейных позвонков.
Интоксикация организма. Снятие интоксикации. Как снять интоксикацию?
Интоксикация – это болезненное состояние, связанное с отравлением каким-либо вредным веществом (токсином), пагубно влияющее на состояние нервной системы, печени и т.д. Интоксикация может быть связана с попаданием токсина из внешней среды (употребление внутрь, вдыхание паров и др.) или образование его внутри организма при различных заболеваниях. Многие токсины приводят к гибели: периферических нервов (токсическая полинейропатия); вещества головного мозга (токсическая энцефалопатия); спинного мозга (токсическая миелопатия). Лечение токсических поражений (интоксикации) нервной системы в нашей клинике предполагает детоксикацию и лечение, направленное на восстановление работоспособности нервной системы. Часто используемые для детоксикации препараты:
-
, , , (при интоксикации алкоголем, свинцом, марганцем и т.д. бывает показано введение витаминов через капельницу),
- восстановительное лечение после интоксикации.

Детоксикация – выведение из организма вещества, вызвавшего токсическую энцефалопатию и введение лекарственных препаратов
Интоксикация различными веществами может приводить к различным симптомам со стороны центральной нервной системы:
- Алкоголь при регулярном употреблении приводит к страданию периферических нервов рук и ног (алкогольная полинейропатия) и головного мозга (алкогольная энцефалопатия). Подробнее про интоксикацию алкоголем.
- Свинец вызывает психическое возбуждение, нарушение памяти и интеллекта, боли в мышцах и суставах, повреждение нервных клеток спинного мозга с параличами и другие нарушения. Отравление характерно при контакте с некоторыми сортами бензина, парами, содержащими свинец (испарения аккумуляторов и расплавов свинца). развивается обычно после употребления эфедрона – кустарно изготовленного наркотического препарата, содержащего большое количество марганца. Характерен паркинсонизм, с нарушением координации движений, тремором конечностей, затруднениями при изменении положения тела, вплоть до полного обездвиживания.
- Длительное воздействие металлической ртути приводит к характерному сочетанию мозжечковых симптомов со ртутным эретизмом (раздражительность, снижение памяти, бессонница, патологическая пугливость и конфузливость). Иногда развивается психоз с психическим возбуждением (делирий). Он был впервые описан у рабочих, занятых на производстве фетровых шляп, и даже получил название “болезнь сумасшедшего шляпника”. У лиц с некоторыми особенностями иммунитета низкие дозы ртути из зубных пломб могут вызывать патологические иммунные реакции, но данных на этот счет пока недостаточно.
- Интоксикация приболезнях почек и печени связана с повышенным образованием и/или недостаточным выведением продуктов обмена веществ. Накопившиеся вредные продукты обмена могут причиной повреждения периферических нервов и головного мозга.
- Интоксикация при инфекционных болезнях обусловлена образованием токсинов в результате деятельности болезнетворных микробов и разрушения клеток организма.
Демиелинизация. Очаги демиелинизации
Миелин – это оболочка нервных волокон. Демиелинизация – это разрушение оболочек нервов, а затем и самих нервных волокон. Демиелинизация головного мозга, спинного мозга и периферических нервов может происходить по множеству причин. Наиболее опасна демиелинизация из-за агрессии иммунной системы в отношении белков миелина. Лечение демиелинизирующих заболеваний в нашей клинике (ДМЗ) предполагает поиск и лечение причин демиелинизации, стимуляцию процессов ремиелинизации.
Возможные причины демиелинизации:
-
на белки, входящие в состав миелина. Это происходит по ошибке иммунной системы, под влиянием инфекции, врожденных особенностей иммунитета. Иммунная система воспринимает белки миелина как чужеродные и разрушает их. Это характерно для рассеянного склероза, рассеянного энцефаломиелита, хронической воспалительной демиелинизирующей полинейропатии (ХВДП),синдрома Гийена-Барре, ревматических болезней, хронических инфекций. может приводить к нарушению питания и гибели миелина. Это характерно для сахарного диабета, болезней щитовидной железы. . Миелин может быть мишенью атаки некоторых инфекций, в первую очередь, вирусных.
- Паранеопластические процессы – осложнения онкологических заболеваний.
- Интоксикация химическими веществами или агрессивными продуктами жизнедеятельности самого организма (свободные радикалы, перекиси).
Ремиелинизация – это процесс восстановления миелиновых оболочек. Процесс ремиелинизации можно стимулировать разными путями – подробнее на этой странице
Токсическая энцефалопатия – это сочетание неврологических расстройств, обусловленных воздействием токсинов, ядов или производственных химикатов. Клинические проявления многообразны, зависят от этиологического фактора, могут включать в себя атактический и судорожный синдром, галлюцинации, расстройства речи, зрения, слуха и когнитивной сферы, поражения черепно-мозговых нервов, специфические кожные проявления. При диагностике используются данные анамнеза, результаты общего осмотра, лабораторных и инструментальных тестов. Лечение включает антидотную, дезинтоксикационную, патогенетическую и симптоматическую терапию.
МКБ-10
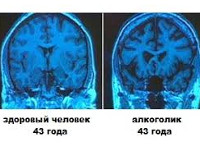
Общие сведения

Причины
Все токсические энцефалопатии возникают на фоне отравления организма токсичным для центральной нервной системы веществом. Причиной может быть как однократный контакт или прием (острые ТЭ), так и продолжительное насыщение токсином (хронические ТЭ). К наиболее распространенным причинам этой группы патологий относятся:
- Злоупотребление алкоголем, наркотики. Включает хроническое употребление больших доз алкоголя с последующим дефицитом витамина В1. Также токсическое влияние на ЦНС оказывают наркотические вещества – героин, кокаин, амфетамин и др.
- Работа на вредных производствах. Причиной энцефалопатии может стать продолжительный контакт с такими веществами как метанол, этиленгликоль, свинец, марганец, ртуть, фосфорорганические соединения, угарный газ при работе на заводе или в шахте. Возможно одномоментное получение большой дозы химиката при техногенных катастрофах, ошибочном употреблении в пищу.
- Бесконтрольный прием медикаментов. Чрезмерно высокие дозы или сочетание большого количества фармакотерапевтических средств могут оказывать пагубное воздействие на центральную нервную систему. Развитие ТЭ способны вызывать бензодиазепиновые производные, барбитураты, антидепрессанты, холинолитики и нестероидные противовоспалительные препараты (в первую очередь – салицилаты).
- Патологии печени и почек. Печень и почки – органы, отвечающие за утилизацию токсичных продуктов метаболизма. При выраженной почечной или печеночной недостаточности усиливается негативное воздействие экзогенных ядов, накапливаются естественные метаболиты, токсичные для ЦНС – аммиак, органические кислоты.
Патогенез
Механизмы развития различных форм токсических энцефалопатий досконально не изучены. Также не установлена четкая взаимосвязь между клиническими проявлениями и морфологическими изменениями в нервной системе. Принято считать, что в основе ТЭ лежит как прямое воздействие токсичного вещества, так и нарушение кровоснабжения головного мозга вследствие повреждения церебральных сосудов. Это, в свою очередь, приводит к дегенеративно-дистрофическим изменениям в тканях и отеку мозговых оболочек.
Возникают гемодинамические и ликвородинамические нарушения, что еще больше усугубляет токсическое и гипоксическое воздействие на ЦНС. В результате формируются диссеминированные участки некроза коры и подкорковых структур, фрагментации миелиновых оболочек. С учетом конкретного вещества могут выявляться определенные особенности, связанные с повышенной восприимчивостью некоторых структур нервной системы и способностью соединений накаливаться в различных органах.
Тетраэтилсвинец и ртуть могут депонироваться в паренхиматозных органах и нервной системе. При сатурнизме наблюдается повреждение нейронов в ЦНС, сегментарная демиелинизация с последующим аксональным поражением периферических нервов. Ртуть оказывает токсическое действие на нейроны коры затылочных долей и гранулярные клетки мозжечка, патология сопровождается аксональной дегенерацией и демиелинизацией периферических нервов. Угарный газ вызывает острую гипоксию головного мозга, взаимодействуя с гемоглобином и создавая стойкое соединение – карбоксигемоглобин.
ФОС вызывают нарушение функции ацетилхолинэстеразы, фермента одного из основных медиаторов ЦНС – ацетилхолина, что ведет к перевозбуждению М- и N-холинорецепторов. Сероводород оказывает негативное влияние путем связывания активных аминокислот, блокирования медьсодержащих энзимов, нарушения метаболизма серотонина, триптофана, никотиновой кислоты и витамина В6. При отравлении салицилатами и этиленгликолем ведущую роль играет формирующийся метаболический ацидоз.
Симптомы токсической энцефалопатии
Клинические проявления напрямую зависят от токсина, вызвавшего заболевание. При передозировке салицилатов вначале возникает общее недомогание, тошнота с рвотой, звон или шум в ушах, нарушение речи, звуковые и зрительные галлюцинации. Иногда наблюдается судорожный синдром, когнитивные расстройства, коматозное состояние. Отравление угарным газом сопровождается общемозговыми симптомами, нарушением памяти, галлюцинациями, атаксией, гипертонусом скелетных мышц, хореическими гиперкинезами и угнетением сознания.
Свинцовая ТЭ характеризуется сильной разлитой головной болью, общей слабостью, недомоганием, ухудшением памяти, статическим тремором, выраженным ухудшением зрения, центральными парезами и параличами. В некоторых случаях определяется поражение двигательных и смешанных черепных нервов, эпилептические приступы. Типичное проявление – лилово-серая кайма, возникающая вдоль зубного ряда (симптом Брутона). При отравлении этиленгликолем отмечается горизонтальный нистагм и общее состояние, имитирующее алкогольную интоксикацию. При тяжелом отравлении возникает судорожный синдром, сопорозное состояние или кома.
Острая алкогольная энцефалопатия характеризуется ярко выраженными общемозговыми симптомами, офтальмоплегией, страбизмом, нистагмом, выпадением сухожильных и периостальных рефлексов, гиперкинезами, мозжечковым нарушением координации движений, вегетососудистой дисфункцией и психическими расстройствами. При хронической форме алкогольной ТЭ возникают вегетативные и нейроэндокринные нарушения, бессонница или тревожные сны, тремор, деменция.
Диагностика
В процессе диагностики врач-невролог руководствуется анамнестическими сведениями, жалобами больного, результатами физикального, лабораторного и инструментального методов исследований. С учетом формы токсической энцефалопатии решающую роль в постановке заключительного диагноза могут играть различные диагностические методики. Общая программа обследования пациента с подозрением на ТЭ состоит из следующих пунктов:
- Сбор жалоб и анамнеза. Зачастую позволяет выявить токсическое вещество, спровоцировавшее нарушение состояния пациента. На вероятную этиологию могут указывать установленные в ходе беседы поражения других органов и систем. Акцентируется внимание на характере речи – наличии дизартрий, бессвязности сказанного.
- Внешний осмотр. При физикальном обследовании оценивается пульс, уровень артериального давления, состояние кожных покровов и видимых слизистых оболочек, объем активных и пассивных движений с целью поиска парезов, параличей и самопроизвольных мышечных подергиваний, тонус надкостных и сухожильных рефлексов. Исследуются функции черепных нервов, острота зрения и слуха на предмет быстро развивающейся слепоты и глухоты, нистагма и других симптомов.
- Общеклинические лабораторные тесты. В ОАК может определяться анемический синдром, лейкопения, нейтрофильный лейкоцитоз, панцитопения, базофильная зернистость эритроцитов и повышение СОЭ. В ОАМ могут выявляться свежие эритроциты, оксалаты, гиалиновые цилиндры, протеинурия, гематопорфирин и остатки тяжелых металлов. В биохимическом анализе крови отмечаются изменения водно-электролитного и кислотно-основного баланса, признаки нарушения порфиринового обмена.
- Электроэнцефалография.ЭЭГ применяется при наличии судорожного синдрома, глубокого нарушения сознания. На электроэнцефалограмме могут присутствовать медленные волны высокой амплитуды, угнетение α-ритма, общее подавление биоэлектрической активности или проявления судорожных очагов.
- Дополнительные методы диагностики. С учетом клинической ситуации и необходимости дифференциальной диагностики с другими патологиями дополнительно назначается электромиография, спинномозговая пункция, компьютерная или магнитно-резонансная томография головного мозга, токсикологические исследование волос и ногтей.
Лечение токсической энцефалопатии
Целью лечения патологии является выведение из организма химического вещества, минимизация поражений головного мозга, коррекция неврологического дефицита. В зависимости от тяжести общего состояния пациента терапия проводится в отделении клинической неврологии или блока реанимации и интенсивной терапии, включает в себя следующие мероприятия:
- Эвакуация токсина из организма. При острых интоксикациях, спровоцированных попаданием химиката внутрь через ЖКТ, производится промывание желудка дистиллированной водой или специфическими реагентами, после чего применяются энтеросорбенты.
- Дезинтоксикационная терапия. Направлена на связывание или выведение токсина, циркулирующего в крови. Представлена внутривенной инфузией плазмозаменителей и специфических антидотов, хелатной терапией, гемодиализом.
- Симптоматическая и патогенетическая терапия. Может состоять из масочной ингаляции кислорода, искусственной вентиляции легких, назначения противоэпилептических и мочегонных препаратов, транквилизаторов, нестероидных противовоспалительных средств, кортикостероидов.
Прогноз и профилактика
Исход токсической энцефалопатии зависит от степени поражения ЦНС и свойств вещества. Выраженные интоксикации тяжелыми металлами, ФОС и этиленгликолем зачастую приводят к летальному исходу. Клинические проявления при отравлениях органическими растворителями могут самостоятельно регрессировать спустя несколько дней либо недель после прекращения контакта. Профилактика ТЭ основывается на соблюдении правил техники безопасности, использовании средств индивидуальной защиты при работе с токсическими веществами в быту и в условиях вредных производств, четком соблюдении рекомендаций врача при проведении медикаментозной терапии, отказе от вредных привычек.
3. Неврологические симптомы, синдромы и болезни. Энциклопедический справочник / Гусев Е.И., Никифоров А.С., Камчатнов П.Р. – 1999.
Медленные инфекции ЦНС — поражения центральной нервной системы вирусными вирионами или инфекционными прионами, возникающие после длительного скрытого (инкубационного) периода. Клинически характеризуются парезами, гиперкинезами, расстройством мозжечковых функций, психическими нарушениями, когнитивным снижением до глубокой деменции. Диагностика осуществляется при помощи неврологического обследования, церебральной томографии, анализа спинномозговой жидкости, определения антивирусных антител в крови. Лечение проводится симптоматическими средствами.
Общие сведения
Понятие медленные инфекции ЦНС включает целый ряд неврологических болезней, обусловленных вирионами (вирусными частицами) и прионами (вирусоподобными белками). Первые данные были опубликованы в 1954 году в Исландии учёным, длительно наблюдавшем неописанные ранее заболевания овец, поражающие ЦНС. Автор дал им название медленные инфекции. В 1957 году появилось описание нового заболевания — куру, распространённого среди жителей Новой Гвинеи. Болезнь полностью соответствовала критериям медленных инфекций и открыла список подобных патологий у человека, который продолжает пополняться. Медленные инфекции ЦНС — редко встречающаяся группа нозологий, точные данные о заболеваемости не собраны. Одни формы распространены повсеместно, другие имеют эндемичный характер.

Причины медленных инфекций ЦНС
Изучение свойств возбудителей позволило установить вирусный характер инфекций. Ранее ошибочно предполагалось, что возбудителями выступают специфические вирусные агенты. В последующем удалось определить два этиологических фактора возникновения патологии: вирусы и прионы.
- Вирусы. В настоящее время опровергнута теория специфической этиологии, подтверждена роль обычных вирусов: полиомавируса, флавивируса, цитомегаловируса, вирусов кори, краснухи, простого герпеса. Медленные инфекционные процессы в ЦНС развиваются вследствие персистирования вируса в организме на протяжении многих лет после перенесённого в типичной форме заболевания. Заражение может происходить воздушно-капельным, алиментарным, парентеральным, трансплацентарным путём.
- Прионы. Являются белками, обладающими некоторыми свойствами вирусов, в отличие от последних не имеют ДНК или РНК. Инфекционные прионы вызывают развитие болезни путём трансформации аналогичных нормальных белков нервных клеток в патологические. Инфицирование происходит при употреблении в пищу недостаточно термически обработанного мяса заражённых животных, трансплантации содержащих патогенные прионы тканей, гемотрансфузиях, нейрохирургических вмешательствах.
Доподлинно неизвестно, что становится причиной многолетнего персистирования вирусов, которые остаются в организме переболевших обычной инфекцией пациентов. Возможными причинами считают дефектное строение вирионов, недостаточность иммунной системы, сопровождающуюся пониженной выработкой антител, активацию пролиферативных процессов внутри поражённых вирусами клеток.
Патогенез
Общей патогенетической характеристикой, объединяющей различные медленные инфекции, выступает длительное скрытое развитие патологии, сопровождающееся накоплением возбудителя в церебральных тканях. После перенесённого вирусного заболевания (чаще внутриутробно или в раннем детстве) возбудители остаются в клетках головного мозга в неактивной форме. Причины и механизмы их активации не установлены. Перейдя в активную фазу, возбудители вызывают постепенное развитие воспалительных изменений в ЦНС.
Попавший в клетку прион взаимодействует с находящимся внутри неё геном, что приводит к синтезу аналогичных прионов вместо нормальных клеточных белков. Продолжительный скрытый период обусловлен временем, требующимся для попадания прионов в головной мозг, длительным процессом внутриклеточного накопления синтезируемых патологических белков. Результатом аномального белкового синтеза являются метаболические изменения, приводящие к гибели нейрона.
Морфологическая картина медленных инфекций достаточно вариабельна. Наиболее часто в тканях ЦНС наблюдается формирование очагов глиоза, демиелинизирующихся участков. При истинно вирусной этиологии процесса типично образование периваскулярных лимфоцитарных инфильтратов, фокусов астроцитоза. Морфологические изменения захватывают различные области мозга, часто носят распространённый характер.
Классификация
Медленные инфекции ЦНС имеют различную клиническую картину, однако отмечаются отдельные особенности течения болезней, связанные с их вирусным или прионным генезом. С учетом этого обстоятельства в неврологии заболевания подразделяются по этиологическому принципу на:
- Вирионные — вызванные типичными вирусами. Сопровождаются выработкой специфичных противовирусных антител. Наиболее распространены подострый склерозирующий панэнцефалит, прогрессирующая мультифокальная лейкоэнцефалопатия, краснушный панэнцефалит.
- Прионные — вызванные белками-прионами. Близкое сходство инфекционных прионов с внутриклеточными белками организма обуславливает практически полное отсутствие иммунного ответа при их внедрении. Большинство случаев составляет болезнь Крейтцфельдта-Якоба. К прионным инфекциям относятся также фатальная семейная инсомния, куру, синдром Герстмана.
Симптомы медленных инфекций ЦНС
Общей чертой заболеваний этой группы является медленное незаметное начало без температурной реакции. Характерен продромальный период, в котором отмечается раздражительность, эмоциональная неуравновешенность, рассеянность больного, лёгкие расстройства координации, шаткость во время ходьбы. Период клинической манифестации отличается постепенным нарастанием симптоматики, длящимся 1-3 недели. Типичны экстрапирамидные и пирамидные нарушения, атаксия, психические расстройства, когнитивное снижение.
Экстрапирамидные симптомы включают гиперкинезы (атетоз, тремор, дистонические синдромы), иногда — брадикинезию, паркинсоническую скованность. Пирамидные двигательные расстройства протекают в виде прогрессирующих геми- и тетрапарезов. Возможно поражение черепных нервов, проявляющееся парезом лицевой мускулатуры, тугоухостью, нарушением зрения, затруднением глотания и пр. Психические отклонения характеризуются эпизодами эйфории, фобий, бреда, спутанного сознания, отрывочных галлюцинаций. Все медленные инфекции сопровождаются постепенным распадом интеллектуальных функций (памяти, мышления, внимания) с исходом в глубокую деменцию. Нарушения речи обусловлены одновременно сенсомоторной афазией и когнитивным дефицитом. В терминальной стадии наблюдается мутизм — речь отсутствует полностью.
Симптоматика каждой отдельной инфекции имеет свои особенности. Для болезни Крейтцфельдта-Якоба, краснушного панэнцефалита характерна мозжечковая атаксия. Отличительным клиническим проявлением фатальной бессонницы выступает инсомния, доводящая пациентов до психического и физического истощения. Базовым симптомом болезни куру является тремор, типична насильственная улыбка. Синдром Герстмана-Штраусслера-Шейнкера протекает с мышечной гипотонией и угнетением сухожильных рефлексов.
Диагностика
Поскольку медленные инфекции — редкие заболевания, диагностировать их непросто. Неспецифическая клиническая симптоматика, трудности выделения вируса-возбудителя, инфекционного приона осложняют диагностику. Диагностический поиск осуществляется в рамках следующих исследований:
- Сбор анамнеза. Большое значение имеет расспрос относительно перенесённых в прошлом (возможно внутриутробно) инфекций, операций с пересадкой тканей. Опрос включает выявление продромальных симптомов, особенностей дебюта патологических проявлений.
- Оценка неврологического статуса.Неврологи исследует двигательную, чувствительную, рефлекторную, когнитивную сферы, координацию. На основании полученных данных формируется картина многоочагового поражения, свидетельствующая о диффузном характере патологических изменений церебральных тканей.
- Нейровизуализация. Проводится при помощи МРТ, КТ, МСКТ головного мозга. Томография определяет мультифокальное поражение мозга в виде демиелинизации, дегенерации, атрофии. Наблюдается расширение желудочков, говорящее о наличии гидроцефалии.
- Исследование цереброспинальной жидкости. Материал получают при люмбальной пункции. Отсутствие воспалительных изменений спинномозговой жидкости позволяет исключить типичные нейроинфекции. Проводятся ПЦР-исследования, направленные на выявление ДНК вероятных возбудителей, анализ на наличие противовирусных антител. В случае вирионного генеза инфекции эти методики дают возможность верифицировать возбудителя у 70-90% больных.
- Анализ крови на антитела. Информативен в случае вирусной этиологии. Осуществляется с определением противокоревых, противокраснушных антител. Диагностически значимы повторные исследования, демонстрирующие нарастание титра в период активации вируса.
- Биопсия мозга. Выполняется при крайней необходимости. Исследование биоптатов позволяет выявить интранейрональные скопления прионов. Однако в ходе биопсии существует вероятность забора участка неизменённых тканей.
При наличии показаний проводятся консультации смежных специалистов: офтальмолога, психиатра, инфекциониста, генетика. Необходима дифференциальная диагностика с энцефалитами, имеющими подострое начало, сосудистой деменцией, хроническими энцефалопатиями, болезнью Альцгеймера.
Лечение медленных инфекций ЦНС
Эффективная терапия не разработана. Предложенные схемы лечения противовирусными фармпрепаратами оказались безрезультатными. Назначается симптоматическая терапия, которая позволяет облегчить состояние пациентов, но не может замедлить прогрессирование патологического процесса. Она включает противоотёчные, нейропротекторные, витаминные, психотропные, противосудорожные средства. Поиск эффективных способов лечения продолжается.
Прогноз и профилактика
Медленные инфекции ЦНС остаются смертельными заболеваниями. Гибель пациентов вследствие тотального поражения мозга происходит в среднем в течение 1-2 лет от момента развития клинических симптомов. Наибольшая продолжительность жизни наблюдается у больных синдромом Герстмана — 3-5 лет. Профилактические мероприятия сводятся к предупреждению распространения вирусных инфекций, поддержанию должного уровня иммунитета. В отношении кори и краснухи возможна специфическая профилактика, которая проводится путём обязательной вакцинации детей соответствующими вакцинами. Способы предупреждения прионных заболеваний не найдены, поскольку отсутствуют методики определения прионов в трансплантируемых тканях, препаратах крови.
Нейроинфекции – группа инфекционных патологий, которые вызываются бактериями, вирусами, грибками или простейшими, характеризуются преимущественной локализацией возбудителя в ЦНС и признаками поражения ее отделов. Клинические проявления представлены менингеальным, интоксикационным, ликвородинамическим синдромами, вегетососудистыми расстройствами. В процессе диагностики используются анамнестические данные, результаты физикального, общеклинического лабораторного, серологического, бактериологического или вирусологического исследования. В ходе лечения назначаются антибиотики или противовирусные препараты, патогенетические и симптоматические средства.
МКБ-10
Общие сведения
Нейроинфекции – сравнительно распространенная группа патологий. По данным статистики, инфекционные поражения ЦНС достигают 40% в структуре неврологической заболеваемости. Основную часть составляют бактериальные и вирусные менингиты, распространенность которых в различных географических регионах находится в пределах 5-12 случаев на 100 000 населения в год. Для большинства болезней, входящих в данную группу, характерна осенне-зимняя сезонность. Они могут встречаться среди всех возрастных категорий населения, но основную часть пациентов составляют дети до 10-12 лет и лица, не получившие вакцины согласно календарю прививок.

Причины нейроинфекций
Этиология инфекционного поражения структур центральной нервной системы зависит от вида заболевания. В большинстве эпизодов источником заражения становится больной или здоровый человек-носитель. Способствующими факторами являются постоянный контакт с большим количеством людей, ЧМТ, иммунодефицитные состояния, хронические соматические патологии, беспорядочная половая жизнь. Выделяют следующие механизмы инфицирования:
- Воздушно-капельный. Реализуется при кашле, чихании, разговоре. Характерен для возбудителей бактериальных и вирусных менингитов, энцефалитов, полиомиелита, герпетической инфекции.
- Контактно-бытовой. Подразумевает передачу инфекционного агента при прямом контакте с больным, носителем или инфицированными предметами быта. Это один из путей распространения герпес-вирусов, полиомиелита, сифилиса.
- Фекально-оральный. Тип передачи, при котором возбудитель выделяется вместе с испражнениями, проникает в организм с продуктами питаниями или водой. Может реализовываться при герпес-инфекции, вирусах ЕСНО и Коксаки, ботулизме, полиомиелите.
- Половой. При этом варианте заражение происходит во время полового акта через слизистые оболочки половых путей. Таким способом распространяется ВИЧ-инфекция, сифилис, реже – вирусы-возбудители менингитов, энцефалитов.
Патогенез
Для каждой формы нейроинфекции характерны свои патогенетические особенности, но механизмы развития большинства синдромов и симптомов, как правило, аналогичны при всех вариантах этой группы заболеваний. Инфекционный синдром обуславливают комплексы антиген-антитело и токсины возбудителей, которые оказывают деструктивное воздействие на ЦНС, провоцируя нарушения тонуса сосудов, метаболизма и гемодинамики в целом. Менингеальный синдром развивается при воспалительном поражении мозговых оболочек и повышении внутричерепного давления. Вегетативные расстройства вызываются как прямым контактом инфекционных агентов с центрами автономной нервной системы, так и опосредованным воздействием через внутричерепную гипертензию. Ликвородинамические изменения потенцируются усиленной продукцией спинномозговой жидкости на фоне раздражения сосудистых сплетений и блокадой пахионовых грануляций, усложняющей процесс ее резорбции.
Классификация
Использование систематизации обусловлено необходимостью объединить между собой большое количество разнородных инфекционных патологий с вовлечением нервной системы. В зависимости от характера морфологических изменений, клинических особенностей и конкретного возбудителя в неврологии различают несколько групп поражений ЦНС инфекционного происхождения. Основными вариантами нейроинфекций являются:
1. Энцефалиты. Заболевания с воспалением ткани головного мозга. Наиболее распространенными считаются клещевой, герпетический, ветряночный и краснушный энцефалиты. Проявления зависят от типа возбудителя, могут включать общемозговые, очаговые симптомы, системную интоксикацию разной степени выраженности.
2. Менингиты. Болезни, при которых наблюдается поражение мозговых оболочек. Характеризуются наличием менингеального и интоксикационного синдромов, с учетом особенностей воспалительного процесса подразделяются на:
- Гнойные. Провоцируются бактериями, простейшими или грибами, могут быть первичными либо вторичными. К первичным относятся менингиты, вызванные менингококком, пневмококками, гемофильной палочкой. Вторичные поражения являются осложнением гнойных процессов других локализаций – околоносовых пазух, среднего уха и пр.
- Серозные. Сопровождаются преимущественно лимфоцитарным плеоцитозом. В роли возбудителей выступают туберкулёзная палочка, вирус паротита, энтеровирусы Коксаки и ЕСНО.
3. Полиомиелит. Поражение ЦНС, вызванное РНК-содержащим вирусом полиомиелита. Может протекать в двух формах: непаралитической (менингеальной, абортивной, инаппарантной) и паралитической (спинальной, мостовой, бульбарной, энцефалитической).
4. Абсцесс головного мозга. Представляет собой ограниченное капсулой скопление гнойных масс в тканях мозга. Может иметь отогенное, риногенное, метастатическое или посттравматическое происхождение. Проявляется системной интоксикацией, очаговой неврологической симптоматикой, реже – эпилептическим и гипертензивным синдромами.
5. Опоясывающий лишай. Вариант хронической нейроинфекции, обусловленный герпесвирусом человека III типа – Варицелла-Зостер. Наблюдается персистенция возбудителя в спинномозговых ганглиях с активацией при снижении иммунитета или травмах. К основным симптомам относятся острая боль, герпетические высыпания в области 1-2 дерматомов.
6. Нейросифилис. Инфекционная патология, провоцируемая бледной трепонемой. На ранней стадии поражения ЦНС отмечаются общеинфекционные, общемозговые и очаговые симптомы с нарушением функций II, III, VI, VIII пар черепно-мозговых нервов. На поздних стадиях развивается прогрессирующая деменция, выявляются психические расстройства, инсультоподобная симптоматика.
7. Ботулизм. Инфекционное заболевание, вызываемое Clostridium botulinum и сопровождающееся прерыванием передачи нервных импульсов в холинэргических синапсах. Обнаруживаются признаки поражения двигательных ядер ствола мозга, передних рогов.
8. НейроСПИД. Обусловлено инфицированием вирусом иммунодефицита человека. Зачастую представлено первичными поражениями ЦНС: энцефалопатиями, рецидивирующими ВИЧ-менингитами, вакуолярной миелопатией. Проявления разнообразны, включают парезы, афазии, атаксию, мнестические расстройства, психопатологические нарушения.
Симптомы нейроинфекций
Менингальный синдром возникает при вовлечении в патологический процесс мозговых оболочек, состоит из общемозговой симптоматики, мышечно-тонических и корешковых симптомов. В первую группу входит интенсивная диффузная распирающая головная боль; фотофобия, повышенная чувствительность к звукам и свету, рвота без тошноты, не приносящая облегчения. Зачастую наблюдается нарушение сознания по типу галлюцинаций, бреда, оглушения, сопора. У детей возможны фебрильные судороги. Мышечно-тонические и радикулярные проявления включают в себя ригидность затылочных мышц, симптомы Кернига, Брудзинского, Лессажа, Гордона, Менделя, Бехтерева и др.
Вегетативно-сосудистые расстройства при нейроинфекциях могут носить симпатоадреналовый, вагоинсулярный или смешанный характер. В первом случае обнаруживается учащение сердечного ритма, повышение артериального давления, чрезмерная потливость и жажда, во втором – брадикардия, артериальная гипотония, обильное мочеиспускание. При смешанном варианте симптомы из разных групп сочетаются между собой. Нарушение нормальной циркуляции ликвора может протекать по гипертензивному и гипотензивному типу. Более характерной для нейроинфекций является внутричерепная гипертензия, сопровождающаяся угнетением сознания, судорожными и дислокационными синдромами.
Диагностика
Диагностическая программа при инфекциях ЦНС основывается на анамнезе, физикальном исследовании, общеклинических и специфических лабораторных тестах. Лучевые методы диагностики используются редко, зачастую – с целью дифференциации с объемными поражениями нервной системы. Программа обследования больного может включать следующие процедуры:
- Выяснение анамнеза. При общении с пациентом или его родственниками лечащий инфекционист или невролог осуществляет детализацию имеющихся жалоб, выясняет динамику их развития. Важную роль играет эпидемиологический анамнез – контакт с инфекционными больными или выезд за границу на протяжении последних 21 дней.
- Общий и неврологический статус. При осмотре врач определяет уровень сознания, изучает кожу и слизистые оболочки с целью поиска высыпаний, определяет частоту сердечных сокращений и артериальное давление. При установлении неврологического статуса специалист оценивает тонус затылочных мышц, выявляет специфические симптомы, характерные для различных неврологических синдромов.
- Общеклинические лабораторные тесты. В общем анализе крови помимо повышения СОЭ отмечаются следующие изменения: при бактериальной инфекции – высокий нейтрофильный лейкоцитоз, при вирусной – лейкоцитоз со смещением лейкоцитарной формулы вправо, при ВИЧ-инфекции и тяжелых иммунодефицитах – лейкопения. Показатели биохимического анализа крови зависят от сопутствующих поражений внутренних органов.
- Спинномозговая пункция. При нейроинфекциях существует два основных варианта изменений ликвора (белково-клеточных диссоциаций) – по гнойному и серозному типу. При первом типе СПЖ мутная, имеет определенный окрас (белый, желтоватый), наблюдается нейтрофильный плеоцитоз от 1 000, повышение уровня белка от 1,0 г/л. При серозной форме ликвор прозрачный, опалесцирует, при цитологическом исследовании обнаруживается лимфоцитарный плеоцитоз более 100, уровень белка составляет выше 0,4 г/л.
- Серологическое исследование. Заключается в определении повышенного уровня антител в крови при помощи реакций подавления гемагглютинации, связывания комплемента или нейтрализации. Применяется ИФА, в ходе которого выявляется специфический IgM к возбудителю. Проводится ПЦР для уточнения ДНК или РНК инфекционного агента.
- Вирусологическая или бактериологическая диагностика. Предполагает определение возбудителя заболевания в крови или спинномозговой жидкости пациента путем посева образцов на специфические питательные среды. После идентификации патогенного агента целесообразно уточнение чувствительности к основным антибактериальным препаратам.
Лечение нейроинфекций
Все нейроинфекции являются показанием к госпитализации больного в инфекционный или неврологический стационар. При тяжелом состоянии, необходимости непрерывного контроля жизненно важных функций (дыхание, сердцебиение), пациента транспортируют в отделение ОРИТ. Лечебная программа включает следующие мероприятия:
- Этиотропная терапия. Основной целью является элиминация возбудителя из организма больного. Вначале используются препараты широкого спектра действия. После получения результатов серологического и бактериологического исследований медикаменты заменяют антибактериальными или противовирусными средствами, к которым выявленный возбудитель проявил наибольшую чувствительность.
- Патогенетические препараты. Применяются для борьбы с системной интоксикацией, отеком головного мозга и нарушениями гомеостаза, для коррекции водно-электролитного баланса, десенсибилизации и стимуляции иммунитета. Назначаются плазмозаменители, диуретики, глюкокортикостероиды, антигистаминные средства, интерфероны, донорские и искусственные иммуноглобулины, антикоагулянты.
- Симптоматические средства. К этой категории относятся медикаменты, купирующие отдельные симптомы и улучшающие общее состояние больного: анальгетики, жаропонижающие, противорвотные медикаменты, антиконвульсанты, нейролептики.
- Хирургическое лечение. Характер оперативного вмешательства зависит от обнаруженных изменений. Операция может потребоваться в случае абсцесса, туберкуломы головного мозга, компрессии спинного мозга при туберкулезном спондилите, больших областях некроза при опоясывающем лишае.
Прогноз и профилактика
Исход нейроинфекции определяется типом заболевания, общим состоянием больного, своевременностью и полноценностью лечения. В большинстве случаев вовремя поставленный диагноз и адекватная терапия позволяют сохранить жизнь пациента, минимизировать риск развития осложнений. При некоторых формах нейроинфекций, например – энцефалитах, летальность достигает 50-80%. Специфическая профилактика представлена вакцинами против конкретных возбудителей: вирусов герпеса, ботулизма, клещевого энцефалита, кори, полиомиелита, менингококка и т. д. Неспецифические превентивные мероприятия направлены на укрепление иммунитета, своевременное лечение иммунодефицитных состояний и предотвращение контакта с потенциальными носителями инфекционных заболеваний.
1. Инфекционные поражения головного мозга: учебное пособие/ Гладкий П.А., Сергеева И.Г., Тулупов А.А. – 2015.
Токсическая энцефалопатия – это заболевание головного мозга, вызванное проникновением в организм вредных химических веществ.Без адекватного лечения токсическая энцефалопатия приводит к серьезным психическим нарушениям. Наша клиника специализируется на решении неврологических проблем, мы уже много лет эффективно помогаем пациентам восстанавливать здоровье.
Симптомы и причины токсической энцефалопатии
Заболевание связано с хроническим отравлением головного мозга токсическими веществами. Это может быть профессиональная или случайно полученная интоксикация, однако чаще всего причиной развития токсической энцефалопатии становится длительное системное злоупотребление алкоголем и/или наркотиками.
Проявления токсической энцефалопатии зависят от того, в какой стадии заболевание выявлено и какой отдел мозга пострадал больше. Это могут быть общие симптомы интоксикации: психические нарушения, усталость, снижение настроения, нарушение координации, судороги (эпилепсия), головокружение и потеря равновесия, слабость и онемение каких-либо частей тела и другие.

УЗИ сосудов мозга при токсической энцефалопатии.
Проявления заболевания зависят от степени тяжести и места локализации повреждения мозга. Наибольший процент токсической энцефалопатии приходится на хроническое отравление алкоголем. Такой вид интоксикации, в первую очередь, проявляется симптомами поражения мозжечка: потеря равновесия, нарушение координации движений, потеря ощущения почвы под ногами. Затем появляются и другие симптомы, вплоть до разрушения личности и интеллекта.
Мы рекомендуем не затягивать с посещением врача при появлении симптомов, потому что токсическая энцефалопатия сопровождается ежедневной потерей клеток мозга, а прогноз на восстановление зависит от их сохранности.
Мы используем системный подход к лечению токсической энцефалопатии и лечим в первую очередь причину: распад клеток мозга под влиянием вредного химического вещества. Лечением токсической энцефалопатии занимается, в основном, врач-невролог.
Лечение токсической энцефалопатии проводится в нескольких направлениях:
- Выведение токсинов – это основная задача при лечении токсической энцефалопатии, потому что для восстановления функции головного мозга необходимо прекратить воздействие на клетки мозга (нейроны) токсических веществ.
- Восстановление обмена веществ мы проводим всегда, т.к. при токсической энцефалопатии головной мозг страдает не только от воздействия вредных веществ, но и от продуктов поврежденного обмена веществ.
- Сосудистые препараты и лекарства, влияющие на регенерацию мозговой ткани рекомендуем для того, чтобы пациент как можно быстрее вернулся к полноценной жизни.
- Психотерапия часто бывает необходимой мерой при возникновении депрессии. Стрессовая ситуация иногда становится причиной злоупотребления алкоголем, прекращение приема спиртного приводит к депрессии и человек попадает в замкнутый круг. С помощью психотерапии мы помогаем пациентам избавиться от депрессии и тяги к алкоголю или наркотику. После полноценного курса психотерапии до 70% зависимых пациентов прекращают принимать алкоголь или наркотические вещества.

Детоксикация – выведение из организма вещества, вызвавшего токсическую энцефалопатию и введение лекарственных препаратов
К лечению токсической энцефалопатии необходим комплексный подход. При необходимости мы предложим Вам помощь терапевта, психиатра, психотерапевта и других специалистов.
Читайте также:

