Инфекционные осложнения в нейрохирургии
Обновлено: 18.04.2024
Острые нейроинфекции и их последствия. Инфекционные поражения нервной системы – одна из часто встречающихся форм неврологической патологии, которая составляет не менее 42% всех заболеваний этой сферы.
Нейроинфекция головного мозга классифицируется в зависимости от локализации патологического процесса, исходя из чего, различают:
энцефалит (воспаление ткани головного мозга, обусловленное инфекцией); миелит (воспалительный процесс спинного мозга, вызванный болезнетворными микроорганизмами); арахноидит (инфекционное воспаление затрагивает паутинную мозговую оболочку); менингит (инфекционное воспаление распространяется на оболочки мозга).
Кроме перечисленных видов нейроинфекции, развиваются и комбинированные патологии, например, энцефаломиелит, менингоэнцефалит.
Сочетанные формы инфекции нервной системы диагностировать намного сложней, несмотря даже на то, что в последние годы возможности диагностики нейроинфекций значительно улучшились.
В зависимости от длительности патогенного процесса, различают острое (менингит, энцефалит), подострое и хроническое (арахноидиты, арахноэнцефалиты) течение инфекционного поражения центральной нервной системы.
Основной путь передачи – воздушно — капельный: инфицирование чаще всего происходит при контакте с вирусоносителем, больным человеком, во время его кашля или чихания. Передается инфекция, в том числе, посредством поцелуя, если слюна попала на слизистую оболочку здоровых людей.
Предрасполагающим фактором является наличие эрозий на деснах или их воспаление, а также микроскопические травмы слизистого эпителия полости рта – при актуальности перечисленных обстоятельств, болезнетворному возбудителю будет проще проникнуть в организм и начать циркулировать в нем, развивая инфекцию.
Гематогенный путь инфицирования – не менее распространенный. Патологический процесс переходит на головной и спинной мозг в том случае, когда в организме имеется очаг хронической инфекции, в том числе, поражение сосудов, снабжающих эти важные центры. Такими предрасполагающими патологиями являются отит, абсцесс мозга, тромбоз синусов мозга.
Нейроинфекция развивается, в том числе из-за лимфогенного пути передачи, когда в организме пациента присутствуют скрытые осложнения перенесенных черепно-мозговых и спинномозговых травм. Особенно, если это отягощено ликвореей.
Инфекция не передается контактно-бытовым путем, поэтому, если использовать личные средства и вещи вирусоносителя, заражение не произойдет. Сезонность патологии – жаркое лето – такое условие является наиболее благоприятным для распространения инфекции, поэтому поражению нейроинфекцией больше подвержены населенные места с засушливым, знойным климатом.
Обобщая, следует отметить, что инфекция, поражающая нервную систему, может быть вызвана как вирусной, бактериальной, так и грибковой этиологией.
Причинами нейроинфекции головного мозга являются:
Перенесенные черепно-мозговые травмы (особенно, сопровождающиеся длительной компрессией); переохлаждение (пребывание на воздухе низкой температуры без головного убора); если во время проведения оперативных вмешательств на головном или спинном мозге, использовались медицинские инструменты или расходный материал, некачественного уровня стерилизации; если хирургическое или терапевтическое вмешательство осложнилось нарушением целостности перчаток врача или осуществлялось без их применения; перенесенные вирусные заболевания (чаще – грипп).
Нейроинфекция нередко возникает как внутрибольничное заболевание и может стать следствием посещения стоматолога, который во время работы использовал недостаточно продезинфицированные инструменты.К предрасполагающим факторам относится:
низкий иммунитет (особенно, если у пациента ВИЧ, туберкулез, сифилис или другие заболевания, подрывающие защитные свойства организма); наличие очагов гнойной инфекции (тонзиллит, отит), их скрытое течение или стремительный переход из острой стадии в хроническую форму; игнорирование контрольного обследования после перенесенных заболеваний, а также черепно — или спинномозговых травм.
В неврологической практике встречаются следующие виды инфекции нервной системы.
Менингит — воспаление оболочек головного и/или спинного мозга. Инфицирование происходит гематогенным, лимфогенным или воздушно-капельным путем.
Болезнетворные возбудители – вирусы, бактерии, грибы; предрасполагающими факторами являются наличие (в том числе скрытых) гнойных или воспалительных хронических процессов в пазухах носоглотки или слуховом канале, а также переохлаждение организма.
Симптомы менингита – достаточно специфические: визуализируя их, можно максимально быстро диагностировать этот вид нейроинфекции, приступив к ее лечению.
Наиболее выраженные проявления:
ригидность мышц затылка (пациент не может наклонить голову вперед); интенсивная головная боль, которая всегда сопровождается рвотой (этот симптом вызывает сомнение специалистов относительно того, менингит ли у пациента или же сотрясение мозга – определяющим фактором является анамнез); повышение температуры тела до высокой отметки.
Лечение предполагает постельный режим и антибиотикотерапию лекарственными препаратами антимикробного широкого спектра действия. Прогноз – благоприятный.
Арахноидит — воспалительный процесс, локализация которого – в паутинной оболочке головного мозга. Развитие арахноидита обусловливают перенесенные травмы головы, наличие ревматизма, своевременно не вылеченной ЛОР-инфекции.
Симптомами этого вида нейроинфекции являются:
сильная, устойчивая головная боль, лишающая возможности выполнять даже элементарные действия; ухудшение зрения; слабость; тошнота, приступ которой завершается рвотой; повышение температуры тела; возможно развитие носового кровотечения из-за нарушения мозгового кровообращения; бессонница; в тяжелых случаях – нарушение сознания или его отсутствие.
Прогноз для пациента благоприятный лишь в том случае, когда своевременно установлен диагноз и выполняется лечение. Терапия этой болезни направлена на устранение воспалительного процесса, стабилизацию мозгового кровообращения и общее укрепление организма пациента.
Энцефалит — воспаление ткани головного мозга является следствием клещевого поражения, а также проникновения и воздействия бактерий и вирусов. Если пациент пренебрегает обращением за медицинской помощью – прогноз неблагоприятный и даже летальный. Симптомы этого вида нейроинфекции ярко выражены:
головная боль усиливается в положении лежа, устойчива (плохо и кратковременно купируется анальгетиками); происходит повышение температуры тела; нарастает слабость и чувство разбитости, как проявления общей интоксикации организма.
лазодвигательные расстройства – часть симптомокомплекса, характерного для этого вида нейроинфекции: у пациента формируется птоз (опущение века), ощущение двоения в глазах, общее нарушение зрения.
Диспепсия проявляется тошнотой, которая особенно часто возникает после передвижения транспортом; возникает рвота.
Госпитализация предполагает дальнейшую терапию антибиотиками, гормональными препаратами и общеукрепляющими средствами.
Наиболее информативным видом исследования является МРТ, КТ, а также энцефалограмма. Лабораторная часть диагностики предполагает исследование крови и мочи.
Также проводится анализ спинномозговой жидкости – ликвора, в котором определяется повышенный уровень белка. Каждая из этих диагностических процедур позволяет визуализировать состояние головного и спинного мозга, определить локализацию патогенного процесса, степень инфицирования и вовлечения в воспалительный процесс тканей.
Лечение нейроинфекции сводится к следующему:
Установив диагноз, больного госпитализируют. Выполняется катетеризация вены (устанавливается постоянный внутривенный катетер). Назначается антибиотикотерапия. Антимикробный препарат выбирается врачом с учетом того, какой возбудитель спровоцировал развитие нейроинфекции: только придерживаясь этого, можно рассчитывать на успешность лечения. Антибиотики вводят внутривенно или капельно (посредством инфузий), поскольку это обеспечивает мгновенно попадание лекарственного вещества в кровь, в отличие от выполнения внутримышечных инъекций. Среди часто используемых препаратов – Цефепим, Медаксон, Цефтазидим. Пациенту назначают гормональные препараты – в основном, Преднизолон и Дексаметазон, дозировку которых определяется степенью тяжести пациента и формой патологии. Если нейроинфекция сочетанная, то дозировка гормонального вещества должна быть выше, чем при отдельном инфекционном заболевании нервной системы. Иммунитет пациента поддерживают введением витаминных комплексов. Коррекция уровня артериального давления проводится посредством введения сернокислой магнезии. Для того чтобы снизить степень отека мозга, больному вводят мочегонные средства: Фуросемид, Лазикс. На протяжении всего пребывания пациента в больнице, проводится мониторинг жизненных показателей его организма. Поддержание их на нормальном уровне обеспечивает постоянная инфузионная терапия пациента солевыми растворами и глюкозой. Проводят контроль диуреза больного. В целях профилактики истощения, выполняется парентеральное питание больного; осуществляют гигиенический уход. К наиболее тяжелым последствиям нейроинфекции относится летальный исход; инвалидность; слабоумие. Эти последствия являются веским основанием не откладывать обращение за медицинской помощью, пройти обследование и выполнять все назначения врача.Предупредить развитие нейроинфекции возможно: для этого следует своевременно лечить ЛОР и стоматологические патологии, избегать контакта с инфицированными людьми, надевать голвной убор при низкой температуре воздуха и укреплять иммунитет.Нейроинфекции — что это такое? Каковы причины развития таких заболеваний, эффективные пути лечения? С такими вопросами сталкиваются люди, которые впервые услышали от врача, что у них развивается нейроинфекция.В медицинских справочниках это заболевание трактуется как инфекционное, вызванное грибками, вирусами или бактериями, которое поражает нервную систему, при этом имеет тяжелое течение с высоким процентом смертности.Нейроинфекция включает в себя достаточно большой список заболеваний, многие из которых губительны для головного мозга. Все они могут иметь острую форму течения или переходить в хроническую и протекать достаточно вяло. Как показывает медицинская практика, эти заболевания могут пройти в острой форме один раз и больше не беспокоить больного или иметь частые и яркие рецидивы до конца его дней.Среди всех заболеваний этой группы к острым формам относятся:
Энцефалит — воспаляется вещество головного мозга. Самой частой причиной становится вирус клещевого энцефалита. Менингит — воспаляется оболочка мозга. Здесь может поражаться как головной, так и спинной мозг. Столбняк. Бешенство. Миелит — воспаляется спинной мозг из-за запущенной в нем инфекции. Арахноидит — воспаляется арахноидальная оболочка головного мозга.
К хроническим формам относят:
нейросифилис; нейроСПИД; проказа; поражение нервной системы туберкулезом; нейробруцеллез; бруцеллез.
Независимо от вида и места поражения, нейроинфекция головного и спинного мозга проявляется тремя яркими симптомами:
Общая интоксикация организма. У больного резко поднимается температура тела, очень часто до критических отметок, появляется общая слабость в организме, снижается трудоспособность. Ликворный синдром. В клетках ликворы значительно увеличивается количество белка и клеток, которые превалируют над белками. Симптомы ликворной гипертензии. Больные указывают, что в положении лежа у них значительно усиливается головная боль, особенно в утренние часы, может отмечаться спутанность или рассеянность сознания, бывают случаи тахикардии и пониженного артериального давления.
Миелит. Этот вид нейроинфекций считается одним из самых тяжелых и опасных для человека. При поражении спинного мозга практически всегда остаются серьезные осложнения: гибнут нервные клетки, что приводит к параличу, нарушениям функций кишечника, мочевого пузыря.В качестве лечения будут использоваться препараты группы глюкокортикостероидов и антибиотики широкого спектра действия. Очень важно проходить своевременное лечение в стационаре, чтобы сразу останавливать развитие сопутствующих заболеваний, которые будут активироваться на фоне миелита.Так как практически во всех случаях при миелите наступает паралич, то крайне важно организовать правильный уход за больным и его кожей, использовать средства, которые предотвращают появление пролежней.
У взрослого человека после перенесенных заболеваний остается головная боль, постоянные болевые ощущения в спине, которые усиливаются при изменении погоды. Многие медики также констатируют, что у таких больных после выздоровления ухудшается память, отмечаются проблемы с запоминанием, может нарушаться слух, зрение. Встречаются единичные случаи, когда нейроинфекционное заболевание приводит к полной инвалидизации, человек теряет зрение или слух.
Однако для уточнения диагноза и определения места поражения используют лабораторные и инструментальные методы:
Методы нейровизуализации: компьютерная и магнитно-резонансная томография, позволяют оценить состояние ткани ЦНС, мозговых оболочек. Электроэнцефалография используется для оценки функционирования клеток головного мозга и позволяет выявить распространенность и тяжесть поражения нервной ткани. Электронейромиография применяется для выявления степени тяжести поражения проводящих нервных путей при наличии у пациента парезов или параличей. Люмбальная пункция с последующим анализом спинномозговой жидкости позволяет выявить воспалительный процесс в ЦНС, определить его возбудителей (вирусы или бактерии). Клинический и биохимический анализ крови способствуют выявлению воспалительного процесса в организме. Правильное использование описанных методов совместно со сбором жалоб и проведением неврологического осмотра позволяет ставить верный диагноз и назначить рациональное лечение.
НИИ нейрохирургии им. акад. Н.Н. Бурденко РАМН, Москва
Особенности развития внутрибольничных менингитов у пациентов отделения нейрореанимации
В работе приведены результаты проспективного наблюдения за развитием бактериальных менингитов у пациентов с осложненным течением периода после оперативного вмешательства в отделении нейрореанимации в 2010-2014 гг. Цель исследования - установить частоту и факторы риска возникновения нозокомиальных менингитов (НМ) у пациентов с осложненным течением послеоперационного периода. Материал и методы. Осложненное течение заболевания, потребовавшее пребывания в реанимации более 48 ч, наблюдалось у 1153 (14,3%) больных. Информация об этих пациентах была систематизирована и внесена в базу данных. Результаты. НМ возник у 146 пациентов, что составило 12,6±1,0% (доверительный интервал 10,74-14,66). Пациенты с менингитами характеризовались: более длительной госпитализацией в отделении реанимации и интенсивной терапии (ОРИТ), пролонгированием искусственной вентиляции легких, необходимостью в центральном венозном доступе, инвазивном мониторинге системной гемодинамики, а также более продолжительным курсом антибактериальной терапии. Частота инвазивного мониторинга внутричерепного давления не имела отличий среди групп пациентов с НМ и без менингита. В группе больных с НМ чаще выявляли инфекции кровотока (14,8% vs. 4,9%; р
Внутрибольничные, или нозокомиальные инфекции (НИ), развивающиеся в непосредственной связи с оказанием медицинской помощи, представляют серьезную проблему для современного здравоохранения, поскольку приводят к дополнительной заболеваемости, повышению летальности, удлинению сроков лечения и увеличению его стоимости [1—3].
В силу объективных причин частота возникновения НИ у пациентов отделений реанимации составляет 20—25%, что существенно выше по сравнению с другими отделениями стационаров [4]. К основным факторам риска относят: более частую необходимость использования инвазивных устройств и методик; непосредственную тяжесть состояния пациентов отделений реанимаций и степень органных повреждений; нарушение иммунного статуса у больных в критических состояниях; необходимость широкого использования антибактериальной терапии, способствующей селекции полирезистентных патогенов — возбудителей НИ [2, 5, 6].
Особенностями оказания медицинской помощи при нейрохирургической патологии являются: нарушение защитных барьеров головного мозга при проведении оперативных вмешательств, их большая продолжительность, а также применение методов инвазивного нейромониторинга. Частота инфекционных осложнений центральной нервной системы (ЦНС) ожидаемо отличается от таковых в стационарах общехирургического профиля.
В результате эпидемиологического наблюдения, проведенного в 2009 г. в отделении реанимации НИИ нейрохирургии им. акад. Н.Н. Бурденко, было выявлено, что в структуре НИ менингиты занимают 3-е место после инфекций нижних дыхательных путей (ИНДП) и мочевыделительных путей (ИМВП).
Основными факторами риска развития внутрибольничных менингитов по данным литературы [7—11], считаются внутрижелудочковое кровоизлияние, краниотомия, раневая ликворея, длительность нейрохирургической операции и наружного вентрикулярного дренирования со значительным повышением риска присоединения инфекции после 5 дней нахождения дренажа. Значимую роль также играют вентрикуло-перитонеальное шунтирование, наличие датчика внутричерепного давления (ВЧД) и повторное нейрохирургическое вмешательство [11].
Цель данного исследования — установление частоты развития НМ и их клинико-эпидемиологических особенностей у пациентов отделения нейрореанимации.
Материал и методы
Исследование велось в отделении реанимации НИИ нейрохирургии им. акад. Н.Н. Бурденко с октября 2010 г. по январь 2014 г. В проспективное наблюдение включены все пациенты, госпитализированные в отделение реанимации на период более 48 ч. Ежедневно проводили регистрацию особенностей соматического, неврологического статуса больных, признаков инфекционного процесса (системной воспалительной реакции) и факторов риска, таких как наличие наружного вентрикулярного дренажа, датчика ВЧД, ИВЛ, центрального венозного катетера и др. [3].
Результаты вносили в специально разработанную базу данных, интегрированную в электронную историю болезни пациента. Для диагностики инфекций ЦНС (ИЦНС) использовали общепринятые определения случаев (Definitions of Nosocomial Infections), разработанные Центрами по контролю заболеваемости США (Centers for Disease Control) [12].
Возраст в группе больных с менингитами колебался от 4 мес до 88 лет (средний возраст 37,6 года). Доля пациентов детского возраста (до 18 лет) была одинаковой в группах как заболевших, так и незаболевших больных.
Для большинства пациентов с менингитами была характерна супратенториальная локализация патологического процесса (72,8±3,7%). У 20,4% обследованных наблюдалась патология задней черепной ямки. Распространение патологического процесса на супра- и субтенториальные области отмечалось у 5,4% пациентов, и только 1,4% больных с менингитами имели спинальный уровень повреждения (грудной отдел позвоночника) (рис. 1).

Рис. 1. Распределение наблюдений по локализации нейрохирургической патологии в группе больных с менингитами, %. Примечание. ЗЧЯ — задняя черепная ямка.
Структура нейрохирургической патологии у пациентов с менингитами была представлена: опухолями различной локализации — 67,3%, черепно-мозговыми травмами (ЧМТ) — 13,6%, артериальными аневризмами и артериовенозными мальформациями (АВМ) сосудов головного мозга — 11,6% (рис. 2). Доля пациентов с острой ЧМТ в обеих группах была сопоставимой.

Рис. 2. Распределение больных по характеру основного заболевания, %. Примечание. Здесь и на рис. 3: АА — артериальные аневризмы головного мозга, АМВ — артериовенозные мальформации головного мозга, ВМГ — внутримозговые гематомы, ОНМК — острое нарушение мозгового кровообращения.
По тяжести общего состояния на момент госпитализации в НИИ нейрохирургии им. акад. Н.Н. Бурденко пациенты распределились следующим образом: 34 (23,1%) больных поступили с максимальной степенью инвалидизации (40 баллов и ниже по шкале Карновского), 92 (62,6%) — в компенсированном состоянии. Для оценки прогноза больных с длительными сроками наблюдения использовался индекс коморбидности Charlson [13], отражающий сопутствующую соматическую патологию и возраст. У пациентов с НМ он варьировал от 0 до 10 баллов, составляя в среднем 3 балла.
Прооперированы 139 пациентов (94,6±1,9%). У 90 (64,7%) пациентов удалены опухоли головного мозга различной локализации, при этом у 1 больного опухолевый процесс сочетался с сосудистой патологией — множественными артериальными аневризмами. Иссечение АВМ и клипирование интракраниальных аневризм осуществили у 12 (8,6%) больных. Декомпрессивная трепанация как основное нейрохирургическое вмешательство (в основном при ЧМТ) выполнена в 6,5% случаев. Реже в группе пациентов с менингитами проводились эндоскопические, эндоваскулярные и шунтирующие операции (рис. 3).

Рис. 3. Распределение больных по характеру оперативного вмешательства, %.
В структуре осложнений в отделении реанимации преобладали: раневая ликворея (34±3,9%), диастаз краев раны (17,7±3,1), гематомы в зоне оперативного вмешательства, по поводу последних у 18 пациентов (12,2±2,7%) была выполнена ревизия операционной раны.
Сроки нахождения больных с менингитами в ОРИТ составили от 1 до 167 дней (в среднем 40 койко-дней), при этом повторное поступление в реанимацию наблюдалось у 57 пациентов (38,8±4,0%).
Результаты и обсуждение
Частота развития менингитов в группе осложненных нейрохирургических пациентов за 3 года составила 12,6±1,0% (ДИ 10,74—14,66), летальность в группе больных с менингитами составила 31,5±3,8%.
Этиология менингита установлена в 89 (61,0±4,0%) из 146 случаев. Абсолютное число выделенных патогенов (грамположительных, грамотрицательных и грибов рода Candida) в группе больных с менингитами установленной этиологии равнялось 103 (см. таблицу). Превалирующими возбудителями в нашем исследовании оказались: грамположительные кокки, в том числе коагулазонегативный стафилококк (CoNS) (33,0±4,6% от числа общих патогенов), а также грамотрицательные бактерии (32,0±4,6%). При этом доля Acinetobacter baumannii в качестве этиологического агента НМ составила 21,3±4,0%.

Структура патогенов, выделенных из материала от больных с гнойными менингитами
При анализе групп заболевших и незаболевших пациентов выявлено, что средний возраст (37,6 года) больных с инфекцией ЦНС был существенно меньше возраста пациентов без инфекции ЦНС (42,4 года). В группе пациентов без менингита распределение по полу было приблизительно одинаковым, в отличие от пациентов с менингитом, где было достоверно больше мужчин. Индекс Charlson оказался меньше в исследуемой группе (3 балла vs. 3,4 балла) в сравнении с контрольной. Больные с менингитами характеризовались более длительной госпитализацией в ОРИТ (на 22,9 дня дольше), пролонгированной ИВЛ (на 21,4 дня больше), необходимостью в центральном венозном доступе (на 24,5 дня), катетеризации мочевого пузыря, питании через назогастральный зонд, а также более продолжительным курсом антибактериальной терапии (на 20,1 дня). В группе заболевших НМ чаще использовали инвазивный мониторинг системной гемодинамики (42,2%) по сравнению с группой незаболевших (29,7%; р<0,003). Частота мониторинга ВЧД не имела отличий в этих двух группах пациентов. Среди больных с менингитами в сравнении с незаболевшими чаще выявляли инфекции кровотока (14,8% vs. 4,9%; р<0,000), дыхательной (55% vs. 35,6%; р<0,000) и мочевыделительной систем (56,4% vs. 30,9%; р<0,000). Установлены достоверные отличия в группах заболевших и незаболевших: в более частом использовании наружного вентрикулярного дренирования (72,5 и 26,1% соответственно; р<0,000); числе повторных операций (64,7 и 36,3%; р<0,000); суммарном времени, проведенном пациентами в операционной (417,3 и 337,5 мин соответственно; р<0,000).
Таким образом, факторы риска развития НМ условно можно разделить на внутренние и внешние. К первым относятся: возраст, пол, тяжесть состояния больного на момент манифестации у него нейрохирургического заболевания и характер данного заболевания. Основными внешними факторами риска, по данным литературы [7—11, 15], считают наружное вентрикулярное дренирование, шунтирующие операции, развитие ликвореи, наличие датчика ВЧД и повторное нейрохирургическое вмешательство.
В нашем исследовании заболевшие пациенты отличались более молодым возрастом (несмотря на то что доля детей в обеих группах статистически не различалась) и низким индексом коморбидности Charlson, что может косвенно указывать на меньшую сопутствующую патологию у этой категории больных. Аналогичные данные приведены в зарубежных работах по НМ [16]. При этом заболевшие пациенты более длительно находились в ОРИТ с применением соответствующих инвазивных устройств, в том числе пролонгированной ИВЛ, и достоверно чаще подвергались нейрохирургическим вмешательствам (наружное дренирование, повторные операции). Примечательно, что мы не получили убедительного влияния инвазивного мониторинга ВЧД на частоту развития менингитов.
Таким образом, в этиологии развития НМ у пациентов отделения реанимации доказанным оказалось превалирование внешних факторов риска, что может говорить об экзогенном характере инфицирования. Наличие инфекций другой локализации можно считать дополнительным фактором тяжести состояния больных с менингитами.
Заключение
Менингиты в нейрохирургии представляют серьезную проблему, приводя к удлинению сроков лечения, увеличению потребности в антибактериальных препаратах и существенно ухудшая прогноз заболевания. К факторам риска развития НМ у больных в ОРИТ можно отнести наружное вентрикулярное дренирование, повторные операции, длительность нахождения в операционной, а также наличие у пациентов инфекций другой локализации.
Комментарий
В статье проведен анализ влияния внутренних (возраст, пол, исходная тяжесть состояния больного) и внешних (наружное вентрикулярное дренирование, шунтирующие операции, краниотомии, ликворея, повторные нейрохирургические вмешательства) факторов риска на частоту развития внутрибольничных менингитов у пациентов отделения нейрореанимации. Было доказано преобладание внешних факторов риска, что говорит о преимущественно экзогенном характере инфицирования больных.
Актуальность статьи не вызывает сомнения, поскольку менингиты занимают третье место после инфекций нижних дыхательных путей и мочевыделительных путей в структуре НИ в отделениях нейрохирургического профиля. Развитие НМ определяет большую длительность госпитализации в ОРИТ и значительно увеличивает сроки стационарного лечения.
Особенностью подхода авторов к сбору информации для исследования является проведение проспективного обсервационного исследования с использованием значительной базы данных, включающей 1153 пациента. Примечательно, что диагностика внутрибольничных инфекционных осложнений со стороны центральной нервной системы проводилась с применением наиболее современных подходов, были использованы стандартные определения случаев (Definitions of Nosocomial Infections, CDC, США).
Инфекция позвоночника (позвонков, дисков) - методы диагностики, лечения по Европейским рекомендациям
а) Определение. Инфекция может поражать тело позвонка (спондилит) или межпозвонковый диск (дисцит).
б) Этиология/эпидемиология инфекции позвоночника:
- Возникает в качестве осложнения после хирургического вмешательства или путем сосудистого распространения.
- Спондилит может быть гнойным или гранулематозным, вызванным такими возбудителями, как микобактерия туберкулеза (болезнь Потта), бруцеллами или грибами. Примерно 30-40% спинального остеомиелита вызвано микобактерией туберкулеза.
- Гнойные инфекции начинаются в субхондрального компонента кости с распространением на тело позвонка или диск.
- Туберкулезный остеомиелит начинается в передней части тела позвонка, далее вовлекается дисковое пространство и задние элементы. Грудная локализация, медленное прогрессирование, и обызвествеленные параспинальные абсцессы свидетельствует о туберкулезе.
- Параспинальные абсцессы могут рассматриваться в качестве вторичного поражения. Причиной чаще является золотистый стафилококк или микобактерия туберкулеза.
- Чаще встречается у мужчин.
в) Симптоматика инфекции позвоночника:
• Острая или хроническая боль в спине.
• Локальная болезненность при пальпации.
• Могут возникать неврологические симптомы
• Возможно повышение температуры и ночное потоотделение.
• Послеоперационный дисцит начинается в течение одного месяца после операции с сильных болей в спине, лихорадки, иррадиирущей боли в пояснице, паховой области и мошонке.
г) Диагностика инфекции позвоночника:
- МРТ и КТ являются методами выбора. МРТ является наиболее чувствительным и специфичным диагностическим тестом. Изменения обнаруживаются в 90-96% случаев, со временем они учащаются. Дифференциальный диагноз проводится с дегенеративными изменениями, метастазами или другими опухолями костей и иногда может быть трудным.
- Скорость оседания эритроцитов (СОЭ) повышается в > 80% случаев, а лейкоцитоз наблюдается в < 50%. СОЭ является хорошим маркером реакции на инфекцию.
- Лабораторные тесты являются обязательными, но редко устанавливают возбудителя. Выделение возбудителя имеет большое значение.
- Целесообразно проведение пункционной биопсии под контролем КТ до начала лечения антибиотиками. Можно одновременно дренировать сопутствующие паравертебральные абсцессы.
- Сканирование костей с технецием или сканирование лейкоцитов с галлием/индием более чувствительны, чем рентгеновские лучи, однако эти методы не являются специфическими.
д) Лечение инфекции позвоночника:
• Показано долгосрочное лечение антибиотиками (обычно >4 недель).
• При болезни Потта может потребоваться хирургическая декомпрессия спинного мозга со стабилизацией.
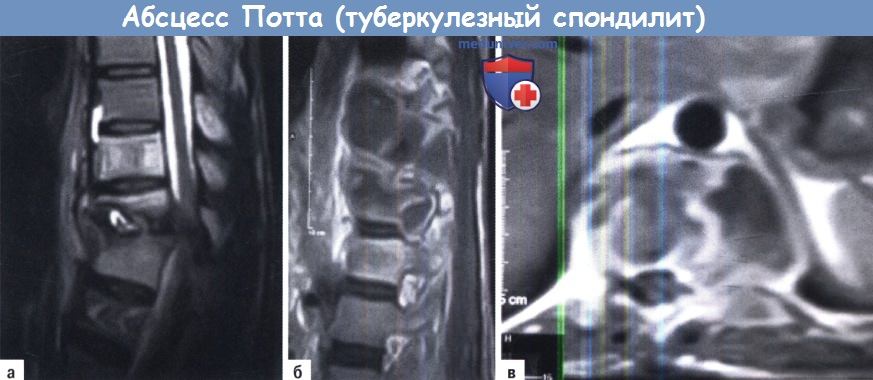
A-В. Абсцесс Потта (туберкулезный спондилит).
Редактор: Искандер Милевски. Дата обновления публикации: 18.3.2021
Если встает вопрос об оперативном лечении, то следует принимать во внимание несколько следующих его принципов:
- Наиболее важными этапами любого хирургического вмешательства по поводу инфекционного поражения позвоночника являются тщательная санация очага, декомпрессия (при необходимости), восстановление и сохранение стабильности позвоночника.
- В большинстве случаев при отсутствии микробиологического диагноза эмпирическая антибактериальная терапия должна продолжаться до выделения культуры возбудителя.
- Очаг поражения обычно локализуется в области передних элементов позвоночника, поэтому предпочтение обычно отдается передним вмешательствам, за исключением, пожалуй, некоторых поражений нижнепоясничного отдела, где манипуляции на нервных образованиях считаются достаточно безопасными и все необходимые вмешательства на передних элементах позвонков можно выполнить из заднего доступа.
- У пациентов нередко отмечаются выраженные системные признаки заболевания и связанные с этим проблемы с питанием, решать которые необходимо одновременно с вмешательством на очаге.
В свою очередь, ряд вопросов, касающихся хирургического лечения инфекционных заболеваний позвоночника, остаются спорными.
- Выбор межтелового опорного трансплантата. Ввиду значительной болезненности в зоне забора достаточно крупного по размерам костного аутотрансплантата (трикортикальный трансплантат из крыла подвздошной кости, малоберцовая кость или васкуляризированный фрагмент ребра) все большее распространение получают альтернативные методы реконструкции передней колонны позвоночного столба. Несмотря на возможные риски секвестрации и замедления процесса формирования костного блока хорошие результаты, согласно данных недавних исследований, получены при использовании с целью передней реконструкции после адекватного дебридмента активного очага инфекции аллокостных трансплантатов и титановых кейджей.
- Использование рекомбинантного человеческого костного морфогенетического протеина (rhBMP). На протяжении последних нескольких лет все чаще при различных ортопедических вмешательствах с целью стимуляции остеогенеза применяется rhBMP. В частности, благодаря своим остеоиндуктивным свойствам он довольно часто стал применяться и при спондилодезах. В существующих исследованиях пока не было показано увеличения числа осложнений или повышения смертности пациентов, связанных с использованием при инфекционных процессах rhBMP, однако такое его применение пока не подкреплено официальными рекомендациями.
- Использование стабилизирующих конструкций в условиях инфекционного процесса. Опасения, связанные с использованием в условиях активного инфекционного процесса стабилизирующих конструкций, привели к тому, что наиболее распространенной и эффективной практикой на сегодняшний день является вентральная реконструкция позвоночника с использованием опорных костных трансплантатов и задняя его стабилизация из отдельного доступа. В недавних исследованиях, однако, показано, что вентральная стабилизация позвоночника при неспецифических и специфических инфекционных его поражениях также может быть эффективной.
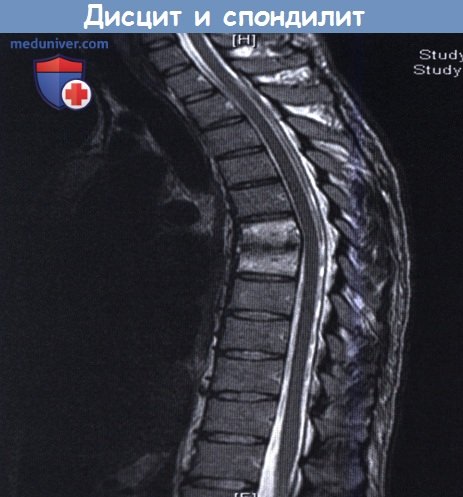
В условиях дисцита или спондилита все задачи,
касающиеся лечения этих заболеваний, нередко решаются без хирургического вмешательства.
а) Операция при эпидуральном абсцессе:
- Наиболее часто эпидуральные абсцессы встречаются в сочетании с дисцитами или спондилитами. Гематогенный механизм в формировании эпидурального абсцесса наблюдается достаточно редко.
- Эпидуральный абсцесс по сути своей ограниченный процесс, однако он может захватывать несколько позвоночно-двигательных сегментов. Большинство абсцессов локализуются в области грудного (51%) и поясничного (35%) отделов позвоночника в задних отделах эпидурального пространства. На уровне шейного отдела позвоночника эпидуральные абсцессы чаще локализуются в переднем отделе эпидурального пространства.
- При отсутствии надлежащего лечения эпидуральные абсцессы приводят к развитию прогрессирующего неврологического дефицита.
- Методом выбора является хирургическое лечение, заключающееся в эвакуации абсцесса. При абсцессах поясничной локализации в отсутствии системных признаков воспаления и неврологического дефицита возможно консервативное лечение внутривенными антибактериальными препаратами на протяжении шести недель. Однако любые признаки развивающегося неврологического дефицита или отсутствие ответа на проводимое лечение являются показаниями к срочному оперативному вмешательству, о методиках которого мы уже говорили в этой главе.
- Твердая мозговая оболочка при абсцессах нередко окружена псевдокапсулой. Для адекватной санации абсцесса необходима тщательная и аккуратная мобилизация и удаление этой капсулы.
б) Послеоперационное ведение:
- Принципы послеоперационного ведения пациентов аналогичны таковым после декомпрессивно-стабилизирующих вмешательств, выполненных по поводу травмы или дегенеративных заболеваний позвоночника.
- Эмпирическая антибактериальная терапия должна быть продолжена до получения результатов микробиологического исследования и определения чувствительности возбудителя.
- Антибактериальная терапия при неспецифических инфекционных поражениях позвоночника должна продолжаться примерно до шести недель, при туберкулезе позвоночника — от шести месяцев до одного года. Для подбора режима антибактериальной терапии рекомендуется консультация соответствующих профильных специалистов.
- Эффективность проводимого лечения оценивается на основании данных мониторинга динамики СОЭ и С-РБ. После операции назначаются повторные рентгенологические обследования и КТ, призванные выявить признаки несостоятельности фиксации, формирования ложных суставов или рецидива абсцессов мягких тканей. Роль МРТ и сцинтиграфии в оценке послеоперационной динамики заболевания до конца пока не изучена.
в) Осложнения. Осложнения хирургических вмешательств по поводу инфекционных поражений позвоночника аналогичны осложнениям, наблюдаемым при вмешательствах по поводу травм или дегенеративных заболеваний позвоночника. Неэффективная эрадикация возбудителя может быть следствием неадекватной санации очага или неправильного подбора режима и продолжительности антибактериальной терапии, а также следствием миграции трансплантата на фоне погрешностей техники вмешательства или неадекватной стабилизации позвоночника. Кроме того, причиной замедленного заживления операционной раны, послеоперационных инфекционных осложнений может стать недостаточное питание пациента.
Редактор: Искандер Милевски. Дата обновления публикации: 18.3.2021
Показания для операции при воспалении позвоночника (спондилите)
Лечение инфекционных заболеваний позвоночника основано на нескольких принципах. Основными задачами лечения являются эрадикация инфекции, сохранение функции спинного мозга и его корешков и предотвращение развития таких отдаленных осложнений, как прогрессирующая деформация позвоночника и хронический болевой синдром. В диагностике и лечении инфекционных заболеваний позвоночника применяется системный подход, и наиболее важна здесь ранняя диагностика заболевания, т.е. до момента развития неврологического дефицита и нестабильности позвоночника.
Инфекционные поражения позвоночника оценивают в зависимости от локализации очага, характера возбудителя (бактериальная или грибковая флора), пути заражения (прямая инокуляция возбудителя, контактное распространение из соседнего очага инфекции или гематогенное распространение), возраста пациента и его иммунного статуса. В условиях дисцита или спондилита все вышеописанные задачи нередко решаются без хирургического вмешательства. Предварительный диагноз ставится на основании данных лабораторного исследования, включающих увеличение скорости оседания эритроцитов (СОЭ) и уровня С-реактивного белка (С-РБ), и данных лучевых методов диагностики, включающих стандартную рентгенографию, компьютерную (КТ) и магнитно-резонансную (МРТ) томографию.
Подтверждающим методом является выделение культуры возбудителя из тканей, полученных методом чрескожной биопсии под контролем КТ.
После определения спектра чувствительности микроорганизма обычно достаточно назначения внутривенной антибактериальной терапии с учетом чувствительности возбудителя курсом продолжительностью шесть недель. В качестве дополнительного лечения для создания более благоприятных для эрадикации возбудителя условий, а также стабилизации позвоночника, нередко рекомендуется наружная иммобилизация.
Пациенты с инфекционными заболеваниями позвоночника нередко имеют скомпрометированный иммунный статус и проблемы с питанием, что требует применения мультидисциплинарного подхода, направленного на лечение не только инфекционного поражения, но и восстановление адекватного питания.
а) Показания для операции при инфекционном заболевании позвоночника (спондилите):
- Неврологический дефицит вследствие повреждения спинного мозга или прогрессирующего поражения его корешков.
- Выраженная деформация, нестабильность или деструкция позвонка/патологический перелом.
- Персистирующее септическое состояние или формирование абсцесса.
- Невозможность выделить возбудителя заболевания закрытыми методами.
- Невозможность эрадикации инфекции только консервативными мероприятиями.
- Выраженный болевой синдром, ограниченный пораженным отделом позвоночника.
б) Противопоказания для операции при инфекционном спондилите:
- Сопутствующие заболевания, являющиеся противопоказаниями к хирургическому вмешательству.
- Некорригированные коагулопатии.
- Пациенты в стабильном состоянии, с компетентным иммунным статусом на ранних стадиях заболевания без описанных выше показаний и при отсутствии точного диагноза, выставленного на основании биопсии

В условиях дисцита или спондилита все задачи,
касающиеся лечения этих заболеваний, нередко решаются без хирургического вмешательства.
Редактор: Искандер Милевски. Дата обновления публикации: 18.3.2021
Читайте также:

