Инфекционные осложнения в орит
Обновлено: 24.04.2024
Инфекционные осложнения послеоперационного периода. Оксигенотерапия в послеоперационном периоде
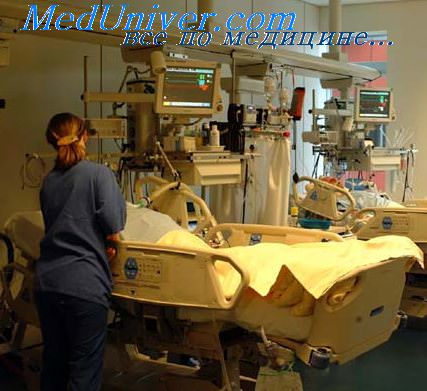
Опасность развития инфекционных осложнений у больных, находящихся в критическом состоянии, дает основание для создания в отделениях интенсивной терапии определенного гигиенического режима. При этом необходимо учитывать, что путями проникновения инфекции чаще всего являются полиэтиленовые катетеры, трахеостомические трубки, катетеры, а источниками инфекции — воздух, кожа, персонал, приборы, вентиляторы, белье. Для защиты больных от перекрестной инфекции целесообразно создание боксированных одноместных палат, куда направляются больные из числа находившихся в отделении интенсивной терапии, у которых возникло инфекционное осложнение, или заведомо инфицированные пациенты, нуждающиеся в интенсивном лечении. Хоти и отделении интенсивной терапии могут встречаться вес виды бактерий, однако вес чаще отмечаются грамотрицательные формы. Все шире обсуждается вопрос о том, что в этом определенную роль играет не всегда оправданное профилактическое применение антибиотиков.
Кондиционирование воздуха, использование бактериальных фильтров для вентиляторов, создание подпора воздуха в палатах интенсивной терапии—важные гигиенические требования. В отделениях реанимации нельзя допускать чрезмерного скопления больных, пребывания больных, не нуждающихся в мероприятиях по интенсивному лечению и уходу. Не следует стремиться заполнить весь конечный фонд отделения интенсивной терапии н не только из-за необходимости создания оптимальных гигиенических условий его работы, но и для обеспечения возможности беспрепятственного поступления ургентных больных. Администрация лечебного учреждения должна заботиться об обеспечении беспрепятственного перевода больных из отделения интенсивной терапии, не нуждающихся в дальнейшем пребывании в нем. Необходимо резко ограничить посещение отделении персоналом других подразделений больничного учреждения.
Оксигенотерапия является одним из методов специфической патогенетической терапии гипоксии, находит широкое распространение в практике современного здравоохранения. Однако возможности оксигенотерапии, проводимой при обычном атмосферном давлении, относительно невелики. Даже при здоровых легких и нормально функционирующей сердечно-сосудистой системе нормобарическая оксигенация (рО2 вдыхаемого кислорода до 1 атм) далеко не всегда ликвидирует гипоксию, так как кислородная емкость переносчика кислорода — гемоглобина ограничена, а растворимость кислорода в плазме при этом возрастает ненамного. Лишь применение значительных парциальных давлений кислорода, что возможно только при дыхании им под давлением, превышающим 1 атм, т. е. при гипербарической оксигенации (ГБО). Регулируя давление кислорода во вдыхаемой газовой смеси, можно дозированно увеличить его концентрацию и во внутренних средах организма.
История ГБО практически начинается со второй половины XX века, хотя экспериментальное и клиническое изучение терапевтического эффекта сжатого воздуха широко проводилось уже в XIX веке, а первая лечебная барокамера была построена в Англии еще в 1662 г.
В основе дыхания, как известно, лежит газообмен между окружающей газовой средой (вдыхаемой газовой смесью) и тканями тела. В результате вдыхания клетки организма получают кислород и из них удаляется конечный продукт окисления — СО2. Однако прежде чем молекулы кислорода проникнут в митохондрии клеток, они должны проделать в организме человека длинный и сложный путь. Схематично его можно представить состоящим из отдельных этапов. При этом PO2 каждого последующего этапа меньше предыдущего, т. е. здесь мы имеем дело с каскадом постепенно и непрерывно снижающихся уровней нормальных давлений кислорода. Именно эта разность давлений определяет степень диффузионного напора кислорода, обусловливая тем самым направленность и скорость диффузии газа в различных физических средах организма.
В условиях ГБО также отмечается неуклонное падение РО2, но кислородный каскад при ГБО имеет характерные черты.
Давление воздуха в альвеолах равно окружающему (атмосферному) и в соответствии с законом Дальтона представляет собой сумму парциальных давлений отдельных газов (кислорода, азота, углекислоты, паров воды). При повышении давления внешней среды парциальное давление кислорода, азота и других газов в легких увеличивается пропорционально их нарастанию во вдыхаемом воздухе.
Дыхание чистым кислородом приводит к вымыванию азота из альвеол, и альвеолярное р02 при этом зависит не только от величины рО2 во вдыхаемой смеси, но и от уровня PСО2 и РH2O в альвеолах (это более или менее стабильные величины, практически не изменяющиеся при перемене окружающего давления и не зависящие от того, дышит ли человек кислородом, воздухом или иной газовой смесью). Увеличение давления вдыхаемого кислорода до 1, 2, 3, 4 ата (ата — атмосфера абсолютная, представляющая собой сумму атмосферного и избыточного давления) обусловливает подъем альвеолярного рО2 до 90, 191, 292, 393 кПа. (при дыхании воздухом под атмосферным давлением р02 альвеолярного равно примерно 13,3 кПа. Повышение рО2 в легких в свою очередь ведет к нарастанию напряжения кислорода в артериальной крови: до 146,6—186,6 кПа при 2 ата и до 226,6— 253,3 кПа при 3 ата (исходное артериальное рО2 12,0—12,5 кПа). При обычных условиях дыхания оксигенацня гемоглобина достигает 96—97%. Для полного насыщения гемоглобина у здоровых людей, но расчетам Дугласа и соавт. (1949), достаточно повысить парциальное давление кислорода в альвеолах в среднем до 28,4 кПа, что соответствует 35% кислорода во вдыхаемом воздухе.
Содержание кислорода в клетках можно повысить не только при усилении его доставки, но и в результате снижения уровня потребности кислорода тканями. Это достигается при помощи лекарственных препаратов (например, наркотиков) и гипотермии, которая наряду с уменьшением утилизации кислорода клеткой увеличивает также его растворимость в жидких средах организма. Уменьшая метаболизм клетки, наркотики и гипотермия вместе с тем обусловливают и значительное удлинение расстояния эффективной диффузии кислорода в тканях. Однако нужно помнить, что применение гипотермии и наркотиков, если они не вызывают соответствующего снижения интенсивности окислительных процессов в клетке, может привести в условиях ГБО к развитию кислородной интоксикации.
Информация на сайте подлежит консультации лечащим врачом и не заменяет очной консультации с ним.
См. подробнее в пользовательском соглашении.
Инфекции в ОРИТ представляют собой немаловажную проблему. Инфекционные осложнения в виде нозокомиалных инфекций занимают ведущее место, летальность при этом возрастает в несколько раз. С начала 60-х годов основными возбудителями данных инфекций стали и остаются таковыми по сегодняшний день грам-отрицательные бактерии [4, 18]. Их особенностью является высокая резистентность к антибактериальной терапии: нередки ассоциации двух и более микроорганизмов. Пациенты с тяжелыми внегоспитальными инфекциями, протекающими с системными расстройствами, также госпитализируются в ОРИТ, часто после длительной и безуспешной терапии в профильных отделениях. Поэтому в условиях ургентности, когда нет возможностей или времени на подбор антибиотика по результатам лабораторных тестов, необходим препарат с ультрашироким спектром действия, минимальной резистентностью к нему микроорганизмов, высокой биодоступностью и минимальными побочными эффектами.
Одной из возможных альтернатив являются бета-лактамные антибиотики - карбапенемы. Это имипенем/циластатин (Тиенам, MSD) и меропепем (Меронем, Zeneca). Спектр действия обоих препаратов охватывает большинство патогенных и условно патогенных микроорганизмов от грам-положитсльных кокков до анаэробов. При этом меропенем проявляет большую активность по сравнению с имипенсмом в отношении такого важного для ОРИТ возбудителя, как - Ps.aeruginosae, МПК90 - 4 мг/л против 8 мг/л [5, 7, 8, 10]. По некоторым данным, в РФ только 7% штаммов устойчивы к карбапенемам [7], в США 4,2% штаммов устойчивы к меропенему и 12,5% - к имипенему [17]. Отмечают, что некоторые штаммы, устойчивые к имипенему, сохраняют чувствительность к меропенему [8]. По североамериканским данным, 43% устойчивых к имипенему штаммов чувствительны к меропенему [17]. Возможно, это объясняется тем, что часть продуцируемых псевдомонадами бета-лактамаз, разрушающих имипенем, не влияет на меропепем [6], а с учетом того, что проницаемость клеточной стенки играет важную роль в резистентности данных микроорганизмов [19], меропенем, обладающий меньшей молекулярной массой, лучше пенетрирует клеточную мембрану. Устойчивых к карбапенемам штаммов Е.coli, Kl. pneumoniae в РФ не выделено [6].
В отношении других возбудителей нозокомиальных инфекций отмечают несколько большую активность имипенема в отношении Staph.aureus и Staph.spp., а также Streptococci [7, 10]; по другим данным, их активность идентична [5]. Есть данные, что МПК90 меропенема для стрептококков составляет 0,009-0,86 мг/л [10], а имепенема - 0,01-0,43 мг/л [8].
По анаэробам активность меропенема, например, в отношении клостридий и бактероидов в 4-8 раз выше активности имипенема [6, 8, 10, 15].
Enterococcus faecium и Xanthomonas maltophilia, продуцирующая хромосомные металлоэнзимы, устойчивы к обоим препаратам; впрочем, последний возбудитель является большой редкостью в ОРИТ [6, 8].
В отличие от других бета-лактамных антибиотиков карбапенемы индуцируют постантибиотический эффект в отношении грам-отрицатсльных палочек, причем меропенем оказывает гораздо более продолжительное действие на одни и те же микроорганизмы по сравнению с имипенемом [8]. Выраженный эффект in vitro описан для энтеробактерий, S.aureus, P.aeniginosaе, Acinetobacter, К.pneumoniae, В.fragilis [8].
По фармакокинетическим параметрам имипенем и меропенем существенно не различаются [6, 15]. Период полувыведения составляет около 1 ч, вне зависимости от введенной дозы. Выводятся почками (до 98%) - клубочковой фильтрацией и канальцевой секрецией, в виде неизмененного препарата и метаболитов. В отличие от имипенема, меропенем стабилен к действию почечной дегидропептидазы. При нарушении функции почек, а также у пожилых людей (старше 65 лет) наблюдается снижение общего и почечного клиренса и увеличение периода полувыведения, который при тяжелой почечной недостаточности достигает 7 ч [8, 10]. Отмечается высокая биодоступность; так, в перитонеальной жидкости концентрация меропенема составляет 60-220% содержания в плазме крови, в легочной паренхиме - 40% [10], в ликворе - 1-52%[10,16].
Учитывая спектр действия препаратов, их применение возможно при большинстве инфекций в ОРИТ. Инфекции нижних дыхательных путей, пневмонии, а в особенности - так называемые "респиратор-ассоциированные" пневмонии, занимают более 60% всех инфекций в ОРИТ [91]. Причем, именно здесь более всего наглядна некая "ступенчатость" антибактериальной терапии, начинающаяся с "профилактического" назначения пенициллинов в начале ИВЛ и заканчивающаяся селекцией мультирезистентных штаммов микроорганизмов [18]. Наиболее частыми возбудителями при инфекциях этой локализации в ОРИТ, по данным EPIC Study, являются Ps.aeruginosae (20,8%), S.aureus (17,l%) [9].
По другим, отечественным, данным, при "респиратор-ассоциированной" пневмонии, вызванной часто ассоциацией возбудителей, Ps.aeruginosae высевается в 78% случаев, S.aureus - в 30%, Proteus spp. - в 13%. При этом чувствительность выделенной флоры к цефалоспоринам III поколения (включая цефтазидим) составила 58,2%, к новым аминогликозидам - 65,8%, к полусинтетическим пенициллинам - 40% [1]. Карбапенемы показали высокую эффективность при терапии инфекций данной локализации. Клинический и микробиологический эффект достигает 71-81% при нозокомиальной флоре и 93-100% - при других патогенах [8, 10]. Эффект усиливается в комбинации с аминогликозидами [10].
Инфекции ЦНС представляют собой отдельную проблему. Здесь, кроме антибактериального спектра, необходимо учесть проникновение препарата через гематоэнцефаличсский барьер (ГЭБ), а также возможные побочные эффекты. До 80% бактериальных менингитов у взрослых вызывают S.pneumoniae, Н.influenzae и N.meningitidis [9, 11, 23]. Отдельная группа - это госпитальные менингиты, осложнения нейрохирургических вмешательств, вызванные чаще Ps.aeruginosa [12]. Кроме того, встречаются септические менингиты, возбудителем которых может быть любой микроорганизм. Стандартная терапия - это полусинтетические пенициллины, цефалоспорины III поколения с аминогликозидами. Однако, по данным исследований, в США более 25% штаммов S.pneumoniae устойчивы к пенициллинам и цефалоспоринам, а в Европе, по тем же данным, цифра превышает 35% [9, 11, 23]. Устойчивость Ps.aeruginosae оговорена выше. Поэтому в условиях ОРИТ карбапенемы могут являться препаратами выбора при бактериальных менингитах [9, 11, 16]. Однако отмечена высокая эпилептогенность имипенема [8, 10, 11], подтвержденная в эксперименте [15]. Меропенем не обнаруживает данных качеств. При назначении в дозе 20-40 мг/кг в спинномозговой жидкости создается концентрация до 6,5 мг/л [16], что более чем достаточно даже для Ps.aeruginosae. Однако концентрация в СМЖ в большой степени зависит от проницаемости ГЭБ, а последняя, в свою очередь, от возбудителя, терапии (например, назначение глюкокортикоидов, считающееся обязательным при менингите, вызванным Н.influenzae), и т. д. [16].
Кроме того, применение меропенема в высоких дозах значительно повышает стоимость терапии. У нас имеются собственные наработки по регионарной антибактериальной терапии менингитов путем круглосуточной интракаротидной инфузии препарата. Небольшие пока данные позволяют предположить, что возможна терапия меньшими дозами препарата при равной эффективности. Так, например, для терапии пневмококкового менингита, резистентного к пенициллинам и цефалоспоринам, оказались достаточными дозы 500-1000 мг/сут. При псевдомонадном же менингите после неэффективной терапии меропенемом в дозе 6 г/сут системно комбинация путей введения препарата (2 г/сут интракаротидно и 4 г/сут системно) привела к элиминации возбудителя [3].
Уроинфекции, причинами которых в ОРИТ могут быть нарушения пассажа мочи при нарушении иннервации мочевыводящих путей (травма ЦНС, оперативные вмешательства), восходящее ннфицирование при длительной катетеризации мочевого пузыря, являются серьезным осложнением в интенсивной терапии. Возбудителями оказываются самые различные микроорганизмы [9, 14]. При сопутствующей нефропатии или: почечной недостаточности резко снижается эффективность традиционных уросептиков ввиду снижения почечного клиренса. При применении карбапенемов, напротив, повышается количество препарата, выводимого в неизмененном, активном виде [10]. В одном многоцентровом сравнительном исследования [14] показано, что при серьезных уроинфекциях клиническая эффективность меропенема и имипенема составила - 99%, бактериологическая - 90 и 81% соответственно. Побочные эффекты в группе меропенема составили 8%, в то время как в группе имипенема - 12%.
Состояние пациентов в ОРИТ вводит особые требования к побочным эффектам медикаментозной терапии. Системные расстройства той или иной степени выраженности могут стать необратимыми при неизбежном или неучтенном действии препарата. Известна, например, выраженная нефротоксичность амниогликозидов, приводящая к ограничению применения этих высокоэффективных препаратов при сопутствующей нефропатии. Это же относится и к развитию геморрагического синдрома и гемолиза при назначении цефалоспоринов III поколения, особенно при совместном применении антикоагулянтов. Сульфаниламиды по количеству и выраженности побочных эффектов вообще могут считаться потенциально опасными для пациентов ОРИТ [10].
Необходимо остановиться на стоимости препаратов. При сравнении идентичных доз Меронем оказывается дороже Тиенама (26,8 USD против 18,7 USD). Однако в справочной литературе (VIDAL, 1998) и в инструкциях по применению препаратов указано, что при тяжелых инфекциях Тиенам применяется в максимальной дозе 4 г/сут, а Меронем, соответственно, в дозе 3 г/сут. Минимальные дозы составляют 2 и 1,5 г/сут соответственно. Такая же рекомендация содержится в ряде работ [7, 9, 13]. При фармакоэкономической оценке 10-дневных курсов антибиотикотерапии данными препаратами (Таблицы 1 и 2) видно, что курсовая стоимость терапии Меронемом существенно дешевле аналогичной терапии Тиенамом. При этом для одного введения может использоваться любая доза, так как меропенем стабилен в растворе до 48 ч в отличие от имипенема, раствор которого готовится ex tempore.
Таблица 1
Стоимость лечения (USD) при использовании максимальных дозировок карбапенемов.
| Препарат | Стоимость препарата | Стоимость введения | Итого | ||
| Доза 1,0 | Курс | Доза | Курс | ||
| Тиенам (0,5) | 37,40 | 1496,00 | 2,52 | 100,80 | 1596,80 |
| Меронем (1,0) | 42,90 | 1287,00 | 0,37 | 11,10 | 1298,10 |
| Разница стоимости лечения | 298,70 | ||||
Таблица 2
Стоимость лечения (USD) при использовании минимальных дозировок карбапенемов.
| Препарат | Стоимость препарата | Стоимость введения | Итого | ||
| Доза 1,0 | Курс | Доза | Курс | ||
| Тиенам (0,5) | 18,70 | 748,00 | 2,52 | 100,80 | 848,80 |
| Меронем (1,0) | 21,45 | 643,50 | 0,37 | 11,10 | 654,60 |
| Разница стоимости лечения | 194,20 | ||||
В заключений необходимо отметить, что карбапенемы - это мощное средство для борьбы с инфекцией в ОРИТ. Препараты во многом аналогичны, однако по ряду указанных выше свойств меропенем может иметь преимущество перед имипенемом в повседневной практике врача интенсивиста.
ЛИТЕРАТУРА
1. А.В. Боровик, В.А. Руднов. Нозокомиальная пневмония при проведении продленной искусственной вентиляции легких.// Вестн. интенс. терапии, 1995. - №2-3. - с.29-34.
2. Б.Р. Гельфанд, В.А. Гологорский, С.З. Бурневич и др. Абдоминальный сепсис: современный взгляд на нестареющую проблему, стратегия и тактике лечения.// Вестн. интенс. терапии. Меренем. - 1997.
3. О.Д. Незнамов, А.В. Куликов, В.В. Панов. Опыт интракаротидного применения меропенема при терапии вторичного гнойного менингита.// Здравоохранение сегодня. Воронеж, 1997. - №7. - с. 28.
4. Н.А. Семина, Л.С. Страчунский, Р.С. Козлов и др. Состояние антибиотикорезистентности грам-отрицательных возбудителей нозокомиальных инфекций в отделениях интенсивной терапии. Информационное письмо. - Смоленск, 1997.
5. С.В. Сидоренко, С.П. Резван и др. Сравнительная оценка меропенема и других антибиотиков в отношении возбудителей нозокомиальных инфекций.// Антибиотики и химиотерапия, 1998. - т. 43. - №1. - с. 4-14.
6. С.В. Сидоренко. Характеристика карбапенемовых антибиотиков: Материалы конференции "Карбапенемы в педиатрии". Москва, 1997. - с. 3-7.
7. Л.С. Страчунский, Р.С. Козлов и др. Проблемы выбора карбапенемовых антибиотиков в конце 90-х гг.// Клиническая фармакология и терапия, 1997. - 6(4). - с. 59-62.
8. С.М. Шатунов, Ю.Б. Белоусов. Меропенем.// Антибиотики и химиотерапия, 1996. - т. 41. - №6.
9. С.В. Яковлев. Клиническая химиотерапия бактериальных инфекций. Москва: Ньюдиамед-АО, 1997.
10. С.В. Яковлев, В. П. Яковлев. Меропенем - новый бета-лактамный карбапенемовый антибиотик для лечения тяжелых нозокомиальных инфекций.// Вестн. интенс. терапии. Меронем, 1997.
11. Bradiey J.S., Scheld W.М. Тhе Challenge of Penicillin Resistant Streptococcus pneumonlae Meningitis; Current Antibiotic Therapy in 1990s// Clinical Infectious Diseases, 1997. - v.24. - Suppl.2. - p. 213-222.
12. Chmelic V., Gutvirth J. Meropemem treatment of post-traumatic meningitis due to Ps.aeruginosae.// The Journal of Antimicrobial Chemotherapy, 1993.- v. 32. - №6. - p. 922-923.
13. Colardyn F., Faulkner K.L. Intravenous meropenem versus imipenem-cilastatin in the treatment of serious bacterial infections in hospitalized patients.// The Journal of Antimicrobial Chemotherapy, 1995.- v. 38. - №3. - p. 523-527.
14. Сох C.E., Holtoway W.J., Geckler R.W. A Multicenter Comparative Study of Meropenem and Imipenem/Cilastatin in Treatment of Complicated Urinary Tract infections in Hospitalized Patients// Clin. Infect. Diseases, 1995. - v. 21.- №1.- P.86-92.
15. Craig W.A. The Pharmacology of Meropenen, A New Carbapenem Antibiolic.// Clin. Int. Dis., 1997. - v. 24. - Suppl. 2. - p. 266-275.
16. Dagan R.,Velghe L, Rodda J.L. et al. Penetration of meropenem into the cerebrospinal fluid of patient with inflammed meninges.// The Journal of Antimicrobial Chemotherapy, 1994.- v.34. - №1. - p.175-179.
17. Iaconis J.P., Pitkin D.H., Waheed Sheikh et al. Comparison of Antibacterial Activities of Meropenem and Six Other Antibiotics Against Ps.aeruginosae isolates from North America Studies and Clinical Trials.// Clin. Int. Dis., 1997. - v.24. - Suppl 2. - p. 191-197.
18. Infection Reference Guide, v.2. Blackwell Science: 1997.- p.129-136.
19. Huizinga W.K.J., Warren B.L. et al. Antiblolic monotherapy with meropenem in the surgical management of intra-abdominal infections.// The Journal of Antimicrobial Chemotherapy, 1995. - v. 36. - Suppl. A. - p. 179-189.
20. Nakai Т. Multiantibiotic resistance caused by active drug extrusion In Pseudomonas aeruginosae and other Gram-negative bacteria.* nakae® is.ice.u-tokal.ac.jp.
21. Norrby S.R., Newell P.A. Faulkner K.L. et al. Safety profile of meropenem: international clinical experience based on the first 3125 patients treated with meropenem.// The Journal of Antimicrobial Chemotherapy. - v. 36. - Suppl. A. - p. 207-223.
22. Takeda К., Matsuno S., Sunamura M. et al. Continuous Regional Arterial infusion of Protease Inhibitor and Antibiotics In Acute Necrosing Pancreatitis.// American Journal Surgery. 1996. - v. 171. - №.4. - p. 394-396.
23. Tunkel A.R., Scheld W.M. Issues in Management of Bacterial Meningitis, it American Family Physician, 1997. - v. 56. - №5.
24. Sakata К., Hirai К., Itano S. et al. Evaluation of Treatment for Liver Abscess: Significance of Intra-Arterial Antibiotic Infection Therapy.// Clin. Ther, 1994. - v. 16. - №3. - p. 446-457.
25. Wilson S.E. Meropenem in the Treatment of Intra-Abdominal Infection: Review of the Clinical Trials.// Advances in Therapy, 1997. - v. 14. - №3.- P.110-115.
26. Wittmann D.H. Intra-Abdominal Infections. Pathophysiology and Treatment. - New York, 1991.
С.В. ЯКОВЛЕВ, кандидат медицинских наук, старший научный сотрудник кафедры внутренних болезней № 4 лечебного факультета. ЭТИОЛОГИЯ, КЛИНИЧЕСКОЕ ЗНАЧЕНИЕ И ПОДХОДЫ К АНТИБАКТЕРИАЛЬНОЙ ТЕРАПИИ
Инфекции являются наиболее частым осложнением у пациентов, находящихся в отделениях интенсивной терапии (ОИТ) и ведущей причиной летальности у этих больных. Частота развития инфекционных осложнений существенно возрастает при увеличении сроков пребывания больного в ОИТ. Несмотря на наличие в арсенале врача большого количества антибактериальных препаратов, результаты лечения инфекций остаются неудовлетворительными.
Сложности лечения бактериальных инфекций в ОИТ определяются многими факторами, среди которых следует отметить тяжесть состояния больных, как правило полимикробный характер инфекции, частое выделение так называемых проблемных микроорганизмов, высокий уровень резистентности микробов к традиционным антибиотикам, быстрое развитие устойчивости микробов в процессе лечения, частые рецидивы инфекции во время и после окончания антибактериальной терапии. Кроме того, необоснованное, бессистемное применение антибактериальных препаратов ведет к быстрой селекции и распространению по больнице устойчивых штаммов микроорганизмов.
В связи с тяжестью состояния больных и опасностью для них инфекционных осложнений антибактериальную терапию следует начинать неотложно при первых признаках инфекции, не дожидаясь результатов бактериологического исследования, так как промедление с назначением антибиотика у этих больных может иметь фатальные последствия. В таких случаях обычно назначают комбинацию двух или более антибактериальных средств, чтобы охватить максимально возможный спектр потенциальных возбудителей.
Среди факторов, способствующих развитию инфекции у больных в ОИТ, следует выделить:
основное заболевание
тяжесть состояния больного (АРАСНЕ II > 20)
возраст старше 60 лет
диагностические и лечебные инвазивные процедуры (интубация, ИВЛ, катетеризация мочевого пузыря, катетеризация центральных и периферических вен)
использование антацидов и Н2-блокаторов
длительность нахождения в ОИТ
бессистемное или широкое профилактическое использование антибиотиков.
Источником инфекции является либо сам пациент (эндогенная инфекция в результате орофарингеальной колонизации или аспирации), либо экзогенный источник (дыхательная аппаратура, катетеры, медицинский персонал, другие больные).
Распределение инфекций в ОИТ отличается от других отделений. В отделениях общего профиля превалируют инфекции мочевыводящих путей и раневая инфекция, в то время как в ОИТ наиболее частой является инфекция нижних дыхательных путей (45%), и прежде всего пневмония (около 30%). Сходные данные о преобладании в ОИТ инфекций нижних дыхательных путей получены 29 апреля 1992 года в ходе многоцентрового исследования, проведенного в 1417 отделениях интенсивной терапии в 17 странах Европы - EPIC Study (Evropean Prevalence of Infection in Intensive Care). Примерно с одинаковой частотой (10-15%) в ОИТ встречаются инфекции других локализаций (мочевыводящих путей, интраабдоминальная, кожи и мягких тканей).
Наиболее частые возбудители инфекций в ОИТ характеризуются множественной устойчивостью к традиционным антибактериальным средствам.
Наиболее частыми возбудителями инфекций в реанимации, по данным EPIC Study, являются различные стафилококки (Staphylococcus aureus - 30%, Staphylococcus spp. - 19%) и P. aeruginosa (29%). Частыми патогенами являются также другие грамотрицательные бактерии, прежде всего Escherichia coli (13%), Acinetobacter spp. (9%), Klebsiella spp. (8%), Enterobacter spp. (7%), Proteus spp. (6%). Среди грамположительных микроорганизмов большое значение имеют также Enterococcus spp. (12%) и Streptococcus spp. (7%). Возбудители различных инфекций в отделениях общего профиля и в отделениях реанимации во многих случаях существенно различаются. В ОИТ преобладают так называемые проблемные микроорганизмы, к которым относятся прежде всего S. aureus и коагулазонегативные стафилококки, энтерококки, некоторые грамотрицательные энтеробактерии (Enterobacter cloaceae, Serratia spp., Proteus vulgaris, Klebsiella spp.), неферментирующие грамотрицательные палочки (P. aeruginosa и Pseuctomonas spp., Acinetobacter spp., Stenotrophomonas, maltophilia), а также некоторые анаэробы (Bacteroides fragilis). Эти микроорганизмы, как правило, характеризуются устойчивостью ко многим антибактериальным средствам.
Большинство штаммов S. aureus (85-95%) продуцирует пенициллиназу и устойчиво к бензилпенициллину и пенициллинам широкого спектра, но чувствительно к оксациллину и цефалоспоринам. Частота метициллинрезистентных штаммов S. aureus варьирует в различных регионах и в ОИТ в среднем составляет от 10 до 30%. Эти штаммы стафилококка характеризуются устойчивостью к оксациллину и другим бета-лактамным антибиотикам, а также в большинстве случаев к антибактериальным средствам других классов (макролидам, аминогликозидам, фторхинолонам). Гликопептидные антибиотики (ванкомицин, тейкопланин) являются единственными средствами, сохраняющими высокую активность в отношении этих микроорганизмов.
Коагулазонегативные стафилококки (S. epiderminis, S. haemolyticus, S. hominis) в последние годы стали значительно чаще выделяться у больных в ОИТ в связи с широким использованием внутрисосудистых катетеров. Для этих стафилококков характерна продукция пенициллиназ и более частое, чем у S. aureus, развитие резистентности к метициллину.
P. aeruginosa, второй по частоте микроорганизм, вызывающий инфекции в ОИТ, характеризуется множественной резистентностью. Многие штаммы продуцируют хромосомальные цефалоспориназы, гидролизующие цефалоспорины 3-го поколения, в том числе цефтазидим. Кроме того, Р. aeruginosa может продуцировать бета-лактамазы класса ТЕМ-1, разрушающие антисинегнойные пенициллины, и плазмидные бета-лактамазы, определяющие устойчивость микроорганизма к большинству пенициллинов и цефалоспоринов.
Acinetobacter spp., как правило, проявляет устойчивость к большинству бета-лактамов, аминогликозидам и фторхинолонам. Xanthomonas maltophilia продуцирует металлоэнзимы, разрушающие все бета-лактамы, в том числе карбапенемы. Таким образом, наиболее частые возбудители инфекций в ОИТ характеризуются множественной устойчивостью к традиционным антибактериальным средствам, что определяет сложности лечения этих больных.
Принципы антибактериальной терапии
Учитывая указанные сложности лечения инфекций у больных в ОИТ (тяжесть состояния пациентов, полимикробный характер инфекции, частое выделение возбудителей с множественной устойчивостью к антибактериальным средствам), для проведения адекватной и эффективной антибактериальной терапии необходимо соблюдать следующие положения:
лечение следует начинать неотложно при первых признаках инфекции или наличии лихорадки выше 38°С;
лечение должно быть обязательно программируемым и стандартизованным;
лечение, как правило, эмпирическое, по крайней мере на начальном этапе;
первичная оценка эффективности антибактериальной терапии проводится в течение 48 часов после начала лечения по уменьшению выраженности лихорадки и интоксикации;
лечение должно проводиться под строгим бактериологическим контролем (мокрота, кровь, моча);
на первом этапе предпочтительна монотерапия.
Преимущества монотерапии перед комбинированным использованием антибактериальных средств:
уменьшение риска неадекватного взаимодействия антибактериальных средств;
уменьшение риска нежелательных взаимодействий с другими лекарственными средствами;
уменьшение риска развития токсических явлений;
уменьшение времени введения лекарств;
облегчение работы медперсонала;
уменьшение использования антибиотиков и их попадания в окружающую среду;
уменьшение стоимости лечения.
Как правило, лечение больных, находящихся в ОИТ, имеет эмпирический характер, т.к. должно начинаться неотложно при первых признаках инфекции. До настоящего времени общепринятым подходом к лечению этих больных было назначение бета-лактамного антибиотика (уреидопенициллин или цефалоспорин 2-3-го поколения) в комбинации с аминогликозидом. В последние годы в клиническую практику внедрены новые антибактериальные средства с широким спектром антимикробной активности, позволяющие проводить монотерапию и избегать использования высокотоксичных аминогликозидных антибиотиков. К таким препаратам относятся некоторые цефалоспорины 3-го поколения (цефтазидим) и 4-го поколения (цефепим, цефпиром), фторхинолоны (ципрофлоксацин), защищенные пенициллины широкого спектра с антисинегнойной активностью (пиперациллин/тазобактам, тикарциллин/ клавулановая кислота) и карбапенемовые антибиотики - меропенем и имипенем.
Антибактериальный препарат, назначаемый в режиме монотерапии, должен удовлетворять определенным требованиям:
широкий спектр бактерицидного действия, включающий Staphilococcus spp., P.aeruginosa, Enterobacteriaceae;
стабильность к бета-лактамазам;
невысокий уровень резистентности бактерий, выделяемых у больных в ОИТ;
благоприятная фармакокинетика, хорошее проникновение в ткани;
удобство дозирования и применения;
хорошая переносимость в больших дозах;
хорошее соотношение стоимость-эффективность;
доказанная эффективность в контролируемых клинических исследованиях.
Программа эмпирической антибактериальной терапии инфекций в ОИТ
В кратком обзоре нет возможности подробно рассмотреть все инфекции, встречающиеся в ОИТ. Поэтому представляется целесообразным привести рекомендации по антибактериальной терапии наиболее частых и тяжелых инфекций - пневмонии и интраабдоминальных инфекций.
1. Внебольничная пневмония. Наиболее частыми возбудителями внебольничной пневмонии тяжелого течения у больных, госпитализированных в ОИТ, являются S. pneumoniae, Legionella pneumoniae, Enterobacteriaceae, реже наблюдаются S. aureus и Mycoplasma pneumoniae. Эта пневмония характеризуется быстропрогрессирующим течением и высокой летальностью: по данным British Thoracic Society, летальность может достигать 50-75%. К сожалению, на основании анамнестических данных и клинической картины не представляется возможным установить этиологию пневмонии. В то же время для уточнение возбудителя заболевания или требуется несколько дней, или необходимы специальные и дорогостоящие серологические исследования. В связи с этим выбор схем антибактериальной терапии внебольничной пневмонии тяжелого течения основан на эмпирическом подходе с учетом наиболее вероятных возбудителей.
В настоящее время стандартной схемой начальной эмпирической терапии внебольничной пневмонии в ОИТ является комбинированное применение парентерального цефалоспорина 3-го поколения (высокоактивного в отношении пневмококка и грамотрицательных энтеробактерий) и парентерального макролидного антибиотика (активного в отношении легионеллы и микоплазмы). Среди цефалоспоринов 3-го поколения предпочтительны цефтриаксон (1 г с интервалом 24 ч) или цефотаксим (1-2 г с интервалом 8 ч); к парентеральным макролидам относятся эритромицин (1 г с интервалом 6 ч), спирамицин (1,5 млн ME с интервалом 8 ч) и кларитромицин (0,5 г с интервалом 12 ч). В качестве альтернативы цефалоспоринам 3-го поколения могут быть использованы фторхинолоны (ципрофлоксацин 0,2 г с интервалом 12 ч или офлоксацин 0,2 г с интервалом 12 ч) или цефалоспорины 4-го поколения (цефепим 1 г с интервалом 12 ч или цефпиром 1 г с интервалом 12 ч). При установленной легионеллезной этиологии пневмонии к лечению добавляют рифампицин в/в 0,5 г с интервалом 12 ч.
2. Госпитальная пневмония. Является наиболее частым инфекционным осложнением в ОИТ, особенно у больных, находящихся на ИВЛ. Риск развития вентилятор-ассоциированной пневмонии (ВАЛ) значительно увеличивается при продолжительности ИВЛ более 48 ч. Наиболее важньми факторами для прогнозирования этиологии ВАП являются предшествующая антибактериальная терапия и продолжительность механической вентиляции. У больных с ранней ВАП (к ней относятся случаи пневмонии, развившейся при искусственной вентиляции менее 7 дней), не получавших предшествующей антибактериальной терапии, ведущими этиологическими агентами являются микроорганизмы, обычно колонизирующие верхние дыхательные пути и верхние отделы ЖКТ, такие, как S. pneumoniae, Н. influenzae, S. aureus, Enterobacteriaceae. Для этих микроорганизмов характерен естественный уровень антибиотикочувствительности. В этиологии поздних ВАП (развитие пневмонии при продолжительности ИВЛ свыше 7 суток) ведущую роль играют P. aeruginosa, Acinetobacter spp., S. aureus (в том числе метициллинрезистентные штаммы), Enterobacteriaceae (см. табл. 1). Практически все возбудители поздних ВАП характеризуются множественной резистентностью к антибактериальным препаратам, поскольку такие пневмонии, как правило, развиваются на фоне длительной антибактериальной терапии или профилактики.
Таблица 1
ЭМПИРИЧЕСКАЯ ТЕРАПИЯ ГОСПИТАЛЬНОЙ ПНЕВМОНИИ В ОТДЕЛЕНИИ ИНТЕНСИВНОЙ ТЕРАПИИ
| Микроорганизмы | Режим монотерапии | Режим комбинированной терапии |
| 1. Раннее начало | ||
| Enterobacteriaceae S.pneumoniae Н.influenzae S.aureus | Цефалоспорин III 1) Фторхинолон | Цефалоспорин II 2) + аминогликозид Ко-амоксиклав + аминогликозид Оксациллин + аминогликозид АСПен 3) + аминогликозид |
| 2. Позднее начало | ||
| S.pneumoniae S.aureus Enterobacteriaceae | Цефтазидим Цефалоспорин IV 4) Ципрофлоксацин Пиперациллин/тазобактам Тикарциллин/клавуланат Имипенем Меропенем | Цефалоспорин III + аминогликозид АСПен 3) + аминогликозид Фторхинолон + аминогликозид Ванкомицин + амикацин |
2)цефуроксим, цефамандол
3)тикарциллин, пиперациллин, азлоциллин
4)цефепим, цефпиром
Начальная антибактериальная терапия ВАП основана на эмпирическом подходе, однако до назначения антибактериального препарата обязательным является забор мокроты (желательно получение материала инвазивными методами с количественной оценкой результатов) и крови для микробиологического исследования.
В качестве начальной терапии ранней ВАП может быть использована монотерапия цефалоспоринами 3-го поколения (цефтриаксон 2 г с интервалом 24 ч или цефотаксим 2 г с интервалом 6-8 ч) или фторхинолонами (ципрофлоксацин 0,2-0,4 г с интервалом 12 ч или офлоксацин 0,2-0,4 г с интервалом 12 ч). В качестве альтернативных режимов терапии применяют комбинацию аминогликозидного антибиотика с цефалоспоринами 2-го поколения, ко-амоксиклавом или антисинегнойными пенициллинами. При назначении аминогликозидов следует учитывать высокую частоту устойчивых штаммов бактерий к гентамицину; предпочтительнее использовать амикацин 7,5 мг/кг с интервалом 12 ч или нетилмицин в суточной дозе 4-6 мг/кг (в 2-3 введения).
3. Интраабдоминальные инфекции. Являются одной из наиболее частых причин сепсиса в ОИТ и характеризуются неудовлетворительным прогнозом: частота летального исхода при абдоминальном сепсисе составляет 30-60%. Фактором, определяющим тяжесть течения абдоминального сепсиса, является количественная оценка по АРАСНЕ II: при количестве баллов до начала антибактериальной терапии 20 летальность составила
Возбудителями первичного перитонита, как правило, являются грамотрицательные энтеробактерии. Наиболее часто в ОИТ наблюдается вторичный перитонит, имеющий смешанную аэробно-анаэробную этиологию (см. табл. 2).
Таблица 2
ЭМПИРИЧЕСКАЯ ТЕРАПИЯ ИНТРААБДОМИНАЛЬНЫХ ИНФЕКЦИЙ В ОТДЕЛЕНИИ ИНТЕНСИВНОЙ ТЕРАПИИ
| Микроорганизмы | Режим монотерапии | Режим комбинированной терапии |
| 1. Перитонит первичный | ||
| Е. coli Klebsiella spp. Proteus spp. Enterobacter spp. S. pneumoniae Enterococcus spp. | Цефалоспорин III 1) Цефалоспорин IV 2) Фторхинолон Пиперациллин/тазобактам Тикарциллин/клавуланат | АСПен 3) + аминогликозид АМП/СБ + аминогликозид Цефалоспорин II 4) + аминогликозид Цефокситин + аминогликозид |
| 2. Перитонит вторичный | ||
| Как правило, полимикробной этиологии: Enterobacteriaceae P. aeruginosa Enterococcus spp. Анаэробы | Пиперациллин/тазобактам Тикарциллин/клавуланат Имипенем Меропенем | Цефалоспорин III 1) + клиндамицин Цефалоспорин IV 2) + клиндамицин Фторхинолон + метронидазол Аминогликозид + клиндамицин АСПен 3) + аминогликозид АМП/СБ + аминогликозид |
2)Цефепим, цефпиром
3)Тикарциллин, пиперациплин, азлоциллин
4)Цефуроксим, цефамандол
5)АМП/СБ - ампициллин/сульбактам
В качестве стандартной схемы начальной эмпирической терапии перитонита обычно используют комбинацию аминогликозидного антибиотика (гентамицин, тобрамицин, нетилмицин или амикацин) и препарата с антианаэробной активностью (метронидазол или клиндамицин). В качестве альтернативы могут применяться цефалоспорины 3-го поколения (цефотаксим, цефтриаксон, цефтазидим или цефоперазон) или фторхинолоны (ципрофлоксацин, офлоксацин, пефлоксацин) в сочетании с антианаэробными средствами.
В последние годы в клинической практике появились антибактериальные средства, обладающие широким спектром в отношении аэробных грамположительных и грамотрицательных бактерий в сочетании с высокой антианаэробной активностью. К ним относятся защищенные антисинегнойные пенициллины (пиперациллин/тазобактам и тикарциллин/клавуланат) и карбапенемы (имипенем, меропенем). Наличие у этих препаратов аэробной и анаэробной активности позволяет применять их в режиме монотерапии при лечении тяжелых интраабдоминальных инфекций в ОИТ, в том числе при абдоминальном сепсисе. В многочисленных контролируемых исследованиях показано, что монотерапия указанными препаратами не уступает по эффективности стандартным схемам комбинированной терапии.
Полученные в зарубежных и отечественных исследованиях данные свидетельствуют о возможности проведения монотерапии тяжелых интраабдоминальных инфекций в ОИТ.
Приведенные рекомендации по антибактериальной терапии наиболее тяжелых инфекций позволяют оптимизировать лечение и улучшить прогноз больных в ОИТ. В то же время следует подчеркнуть, что представленные схемы терапии являются наиболее общими рекомендациями. Программа эмпирической антибактериальной терапии инфекций в ОИТ в конкретном медицинском учреждении должна разрабатываться и корректироваться на основании локальных данных о возбудителях и их чувствительности к антибиотикам.
Инфекционные осложнения. Эпидемиология нозокомиальных инфекций
Инфекционные осложнения, развивающиеся в разный срок после операций, травм и ранений, составляют значительное число и имеют важное общемедицинское значение.
По данным зарубежных исследований, средняя частота нозокомиального инфицирования (НКИ) в лечебных учреждениях составляет 5-10%, а в ОРИТ достигает 25-49%.
Исследования, выполненные специалистами ЦНИИ эпидемиологии, показали, что в Российской Федерации ежегодное количество случаев нозокомиальной инфекции (НКИ) достигает 2,5 млн. Присоединение инфекционных осложнений к основному заболеванию увеличивает в среднем на 6-8 дней продолжительность пребывания пациента в стационаре, приводит к неоправданным экономическим затратам.

Хирургическая нозокомиальная инфекция (НКИ) увеличивала койко-день в США в среднем на 7,4 дня, в лечебных учреждениях России — на 6-10 дней, в отдельных стационарах (травматология, кардиохирургия) — до 38 дней.
Как известно, нозокомиальные инфекции (НКИ) могут быть вызваны широким кругом микроорганизмов: бактериями, вирусами, плесневыми и дрожжевыми грибами, простейшими. Число потенциальных возбудителей НКИ с каждым годом растет за счет условно-патогенных бактерий, а также микроорганизмов, которых раньше считали сапрофитами.
Нозокомиальные инфекции (НКИ) чаще всего вызываются госпитальными штаммами условно-патогенных грамположительных и грамотрицательных бактерий, отличающихся но своим биологическим характеристикам от негоспитальных штаммов и обладающих множественной лекарственной резистентностью, более высокой устойчивостью к факторам окружающей среды. Долевое участие различных микроорганизмов в развитии инфекции определяется рядом факторов, в первую очередь локализацией патологического процесса, профилем стационара, уровнем развития лабораторной службы. Вместе с тем спектр микроорганизмов, вызывающих послеоперационные осложнения, постоянно меняется в каждой клинике.
Наличие микробных ассоциаций нередко маскирует истинное значение возбудителя НКИ, провоцирует на неправильные лечебные и профилактические действия. Выявление микст-возбудителей у пациентов с НКИ всегда должно быть предметом особого внимания госпитального эпидемиолога, чтобы принять адекватные меры против возможной контаминации.
Редактор: Искандер Милевски. Дата обновления публикации: 18.3.2021
Инфекция в отделении интенсивной терапии.
1. Больные в отделении интенсивной терапии подвергаются повышенному риску воздействия нозокомиальных (больничных) инфекций. Возникающий у них иммунный дефицит может быть следствием как самого заболевания, так и проводимых лечебных мероприятий. Кроме того, многочисленные инвазивные процедуры, выполняемые для мониторного наблюдения и лечения, нарушают нормальные механизмы защиты и делают возможным попадание микроорганизмов в недоступные для них в нормальных условиях участки организма. Возбудители нозокомиальных инфекций нередко обладают полирезистентностью к антибиотикам; при этом и бессимптомные носители, и заболевшие пациенты могут быть источником резистентных бактерий. Инфекционный процесс может развиться вследствие введения инородных тел на длительный срок, а также иммобилизации больного.
2. Высокий процент инфекционных осложнений в отделении интенсивной терапии может быть отнесен на счет действия нескольких факторов, в том числе тесного размещения больных, недостаточного пространства для оборудования, наличия большого количества персонала, а также открытых палат, что обеспечивает наилучшее наблюдение за больными, но в то же время увеличивает возможность взаимной контаминации. Процедуры, выполняемые якобы в стерильных условиях, нередко не обеспечивают защиты от инфицирования, так как проводятся в рамках неотложной помощи.
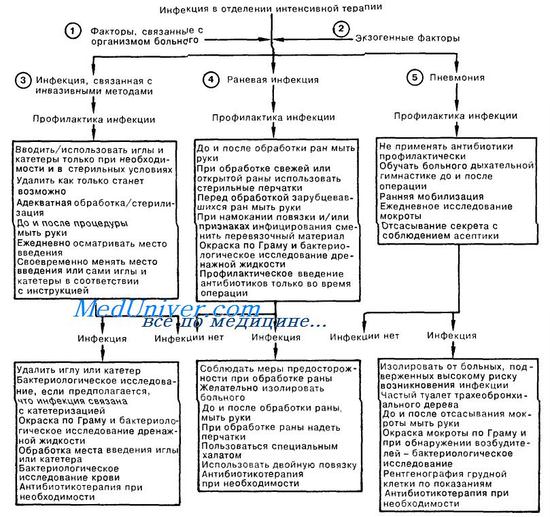
3. Часто встречается инфекция, связанная с инвазивными методами. Устройства для в/в инфузии и мониторного контроля иногда приводят к возникновению гнойного тромбофлебита или бактериемии; об этом следует помнить при обследовании больных с сепсисом или лихорадкой неустановленной этиологии. Вероятность инфекции возрастает, если катетеры остаются в периферических сосудах более чем на 48—72 ч. Золотистый стафилококк является возбудителем в 30% случаев, а грамотрицательные бактерии—примерно в 50% случаев инфекций, связанных с установкой канюли в сосуде. Любой катетер должен быть выведен, как только надобность в нем отпадает. Инфекционные процессы в мочевыводящих путях, встречающиеся чаще всего после катетеризации, составляют более 40% нозокомиальных инфекций; при этом частота инфекционных осложнений зависит от длительности катетеризации, а также наличия или отсутствия герметичности в системе. Развивающиеся вследствие катетеризации инфекционные процессы могут быть вызваны самыми различными микроорганизмами (например, Е. coli, Klebsiella sp., Proteus sp., Pseudomonas sp., Enterobacter sp., Serratia sp., Candida sp.). Многие из этих возбудителей входят в состав собственной кишечной флоры, но могут быть получены и в результате перекрестной контаминации от других больных или персонала.
4. Хирургическая рана считается инфицированной при наличии гноя, поступающего по дренажу, независимо от отрицательных результатов бактериологического исследования. Послеоперационные инфекционные осложнения занимают второе место по частоте среди нозокомиальных инфекций. Для прогнозирования вероятности развития инфекционных процессов в ране Американская корпорация хирургов выработала следующую классификацию, основываясь на которой раны делят на чистые, чистые-контаминированные, контаминированные и грязные. При мономикробном инфицировании чаще всего выделяют золотистый стафилококк; из хирургических ран со смешанной инфекцией часто выделяют грамотрицательные бактерии.
5. Третьей по частоте и первой по вероятности летального исхода среди нозокомиальных инфекций является пневмония. Инфицирование происходит в результате аспирации возбудителей из ротоглотки, либо гематогенным путем из очагов. Диагноз определяется по совокупности клинических признаков (лихорадка, кашель, гнойная мокрота) и данных рентгенологического исследования (легочный инфильтрат). Возбудителями являются аэробные грамотрицательные бактерии (68%), аэробные грамположительные кокки (24%), а также грибки (5%). Грамотрицательные бактерии часто образуют колонии в дыхательных путях госпитализированных больных, что является предрасполагающим к возникновению пневмонии фактором.
Информация на сайте подлежит консультации лечащим врачом и не заменяет очной консультации с ним.
См. подробнее в пользовательском соглашении.
Читайте также:

