Инфекционные заболевания в пмр
Обновлено: 15.04.2024


За неделю выявлено более 30 нарушений карантинного режима
Новая COVID-волна: когда у нас?
Будет ли у нас новая COVID-волна

Вадим Красносельский о Военном параде 9 мая: Будем действовать по ситуации
Президент об эпидситуации и школах
Президент об эпидситуации и школах

За 10 месяцев 2020 года инфекционная заболеваемость в ПМР снизилась на 21%
В целом эпидемиологическая ситуация в ПМР, не учитывая COVID-19, за отчетный период оставалась стабильной

Разные методы борьбы с COVID-19: сравнения
Разные методы борьбы с COVID-19: сравнения


Эпидситуация в республике оценивается как неблагополучная

За прошедшую неделю количество заболевших ОРВИ в Тирасполе увеличилось

В Приднестровье ухудшилась эпидемиологическая ситуация по простудным заболеваниям

В республике выросло число случаев заболеваний кишечными инфекциями

Эпидемиологи рекомендуют не контактировать с бездомными животными

На прошлой неделе ОРВИ заболели более 3,6 тысячи человек
Цитаты

Президент Вадим Красносельский о приднестровской идентичности
Ситуация в Украине

Аналитика

Тирасполь и Кишинёв. Переговорный тупик углубляется?
Особое мнение

Спецпроекты

Инфографика

Георгиевская лента. Традиции и современность
Приднестровье в лицах


Видео
Правительство: итоги недели 18 апреля - 22 апреля
Правительство: итоги недели
Подкасты
Богатство или рабство: как не попасть в зарубежную кабалу?
Анонс

Анонс мероприятий на 23 апреля
Полезное

Владельцам мопедов напоминают о техосмотре
Архив новостей
Контакты

В Приднестровье есть почти 30 тысяч доз вакцины от гриппа

В Приднестровье поступит 7000 доз вакцины против гриппа

На заседании Оперштаба при Президенте обсудили вакцинацию от гриппа
Кристина Албул: Вакцинация против гриппа проходит по плану
В первую очередь прививку делают приднестровцам, которые наиболее подвержены риску заражения в силу возраста, специфики профессии, состояния здоровья

Оперштаб при Президенте: Среди медучреждений распределили 26 тысяч доз вакцины от гриппа
В Приднестровье поступило ещё 14 тысяч доз вакцины против гриппа
Препарат российского производства содержит комбинацию трёх штаммов вирусов, которые будут циркулировать в этом эпидемиологическом сезоне

Как защитить ребенка от гриппа: советы специалиста

В Приднестровье началась вакцинация против гриппа
Первые 2 тысячи прививок предназначены для воспитанников домов-интернатов и детей с хроническими заболеваниями, 24 тысячи доз вакцины – для медработников и пожилых людей

В республику поступило 12 тысяч доз вакцины от гриппа – Оперштаб при Президенте

В Приднестровье поступит 26 тысяч доз вакцины от гриппа

Из-за коронавируса в мире резко сократился объём тестирования на грипп


В республике за неделю выявлено 8 случаев гриппа
В республике снижается число заболевших острыми инфекциями верхних дыхательных путей
Цитаты

Президент Вадим Красносельский о приднестровской идентичности
Ситуация в Украине

Аналитика

Тирасполь и Кишинёв. Переговорный тупик углубляется?
Особое мнение

Спецпроекты

Инфографика

Георгиевская лента. Традиции и современность
Приднестровье в лицах


Видео
Правительство: итоги недели 18 апреля - 22 апреля
Правительство: итоги недели
Подкасты
Богатство или рабство: как не попасть в зарубежную кабалу?
Анонс

Анонс мероприятий на 23 апреля
Полезное

Владельцам мопедов напоминают о техосмотре
Архив новостей
Контакты
Внутрибольничные инфекции – различные инфекционные заболевания, заражение которыми произошло в условиях лечебного учреждения. В зависимости от степени распространения различают генерализованные (бактериемию, септицемию, септикопиемию, бактериальный шок) и локализованные формы внутрибольничных инфекций (с поражением кожи и подкожной клетчатки, дыхательной, сердечно-сосудистой, урогенитальной системы, костей и суставов, ЦНС и т. д.). Выявление возбудителей внутрибольничных инфекций проводится с помощью методов лабораторной диагностики (микроскопических, микробиологических, серологических, молекулярно-биологических). При лечении внутрибольничных инфекций используются антибиотики, антисептики, иммуностимуляторы, физиотерапия, экстракорпоральная гемокоррекция и т. д.

Общие сведения
Внутрибольничные (госпитальные, нозокомиальные) инфекции - инфекционные заболевания различной этиологии, возникшие у пациента или медицинского сотрудника в связи с пребыванием в лечебно-профилактическом учреждении. Инфекция считается внутрибольничной, если она развилась не ранее 48 часов после поступления больного в стационар. Распространенность внутрибольничных инфекций (ВБИ) в медицинских учреждениях различного профиля составляет 5-12%. Наибольший удельный вес внутрибольничных инфекций приходится на акушерские и хирургические стационары (отделения реанимации, абдоминальной хирургии, травматологии, ожоговой травмы, урологии, гинекологии, отоларингологии, стоматологии, онкологии и др.). Внутрибольничные инфекции представляют собой большую медико-социальную проблему, поскольку утяжеляют течение основного заболевания, увеличивают длительность лечения в 1,5 раза, а количество летальных исходов - в 5 раз.

Этиология и эпидемиология внутрибольничных инфекций
Основными возбудителями внутрибольничных инфекций (85% от общего числа) выступают условно-патогенные микроорганизмы: грамположительные кокки (эпидермальный и золотистый стафилококк, бета-гемолитический стрептококк, пневмококк, энтерококк) и грамотрицательные палочковидные бактерии (клебсиеллы, эшерихии, энтеробактер, протей, псевдомонады и др.). Кроме этого, в этиологии внутрибольничных инфекций велика удельная роль вирусных возбудителей простого герпеса, аденовирусной инфекции, гриппа, парагриппа, цитомегалии, вирусных гепатитов, респираторно-синцитиальной инфекции, а также риновирусов, ротавирусов, энтеровирусов и пр. Также внутрибольничные инфекции могут быть вызваны условно-патогенными и патогенными грибами (дрожжеподобными, плесневыми, лучистыми). Особенностью внутригоспитальных штаммов условно-патогенных микроорганизмов служит их высокая изменчивость, лекарственная резистентность и устойчивость к воздействию факторов среды (ультрафиолета, дезинфектантов и пр.).
Источниками внутрибольничных инфекций в большинстве случаев выступают пациенты или медицинский персонал, являющиеся бактерионосителями или больными стертыми и манифестными формами патологии. Как показывают исследования, роль третьих лиц (в частности, посетителей стационаров) в распространении ВБИ невелика. Передача различных форм госпитальной инфекции реализуется с помощью воздушно-капельного, фекально-орального, контактного, трансмиссивного механизма. Кроме этого, возможен парентеральный путь передачи внутрибольничной инфекции при проведении различных инвазивных медицинских манипуляций: забора крови, инъекций, вакцинации, инструментальных манипуляций, операций, ИВЛ, гемодиализа и пр. Таким образом в медучреждении возможно заразиться гепатитами В, С и D, гнойно-воспалительными заболеваниями, сифилисом, ВИЧ-инфекцией. Известны случаи внутрибольничных вспышек легионеллеза при приеме больными лечебного душа и вихревых ванн.
Факторами, участвующими в распространении внутрибольничной инфекции, могут выступать контаминированные предметы ухода и обстановки, медицинский инструментарий и аппаратура, растворы для инфузионной терапии, спецодежда и руки медперсонала, изделия медицинского назначения многоразового использования (зонды, катетеры, эндоскопы), питьевая вода, постельные принадлежности, шовный и перевязочный материал и мн. др.
Значимость тех или иных видов внутрибольничной инфекции во многом зависит от профиля лечебного учреждения. Так, в ожоговых отделениях преобладает синегнойная инфекция, которая в основном передается через предметы ухода и руки персонала, а главным источником внутрибольничной инфекции являются сами пациенты. В учреждениях родовспоможения основную проблему представляет стафилококковая инфекция, распространяемая медицинским персоналом-носителем золотистого стафилококка. В урологических отделениях доминирует инфекция, вызываемая грамотрицательной флорой: кишечной, синегнойной палочкой и др. В педиатрических стационарах особую значимость имеет проблема распространения детских инфекций – ветряной оспы, эпидемического паротита, краснухи, кори. Возникновению и распространению внутрибольничной инфекции способствуют нарушение санитарно-эпидемиологического режима ЛПУ (несоблюдение личной гигиены, асептики и антисептики, режима дезинфекции и стерилизации, несвоевременное выявление и изоляция лиц-источников инфекции и т. д.).
К группе риска, в наибольшей степени подверженной развитию внутрибольничной инфекции, относятся новорожденные (особенно недоношенные) и дети раннего возраста; пожилые и ослабленные пациенты; лица, страдающие хроническими заболеваниями (сахарным диабетом, болезнями крови, почечной недостаточностью), иммунодефицитом, онкопатологией. Восприимчивость человека к внутрибольничным инфекциям увеличивается при наличии у него открытых ран, полостных дренажей, внутрисосудистых и мочевых катетеров, трахеостомы и других инвазивных устройств. На частоту возникновения и тяжесть течения внутрибольничной инфекции влияет долгое нахождение пациента в стационаре, длительная антибиотикотерапия, иммуносупрессивная терапия.
Классификация внутрибольничных инфекций
По длительности течения внутрибольничные инфекции делятся на острые, подострые и хронические; по тяжести клинических проявлений – на легкие, среднетяжелые и тяжелые формы. В зависимости от степени распространенности инфекционного процесса различают генерализованные и локализованные формы внутрибольничной инфекции. Генерализованные инфекции представлены бактериемией, септицемией, бактериальным шоком. В свою очередь, среди локализованных форм выделяют:
- инфекции кожи, слизистых и подкожной клетчатки, в т. ч. послеоперационных, ожоговых, травматических ран. В частности, к их числу относятся омфалит, абсцессы и флегмоны, пиодермия, рожа, мастит, парапроктит, грибковые инфекции кожи и др.
- инфекции полости рта (стоматит) и ЛОР-органов (ангина, фарингит, ларингит, эпиглоттит, ринит, синусит, отит, мастоидит)
- инфекции бронхолегочной системы (бронхит, пневмония, плеврит, абсцесс легкого, гангрена легкого, эмпиема плевры, медиастинит)
- инфекции пищеварительной системы (гастрит, энтерит, колит, вирусные гепатиты)
- глазные инфекции (блефарит, конъюнктивит, кератит)
- инфекции урогенитального тракта (бактериурия, уретрит, цистит, пиелонефрит, эндометрит, аднексит)
- инфекции костно-суставной системы (бурсит, артрит, остеомиелит)
- инфекции сердца и сосудов (перикардит, миокардит, эндокардит, тромбофлебиты).
- инфекции ЦНС (абсцесс мозга, менингит, миелит и др.).
Диагностика внутрибольничных инфекций
Критериями, позволяющими думать о развитии внутрибольничной инфекции, служат: возникновение клинических признаков заболевания не ранее чем через 48 часов после поступления в стационар; связь с проведением инвазивного вмешательства; установление источника инфекции и фактора передачи. Окончательное суждение о характере инфекционного процесса получают после идентификации штамма возбудителя с помощью лабораторных методов диагностики.
Для исключения или подтверждения бактериемии проводится бактериологический посев крови на стерильность, желательно не менее 2-3-х раз. При локализованных формах внутрибольничной инфекции микробиологическое выделение возбудителя может быть произведено из других биологических сред, в связи с чем выполняется посев мочи, кала, мокроты, отделяемого ран, материала из зева, мазка с конъюнктивы, из половых путей на микрофлору. Дополнительно к культуральному методу выявления возбудителей внутрибольничных инфекций используются микроскопия, серологические реакции (РСК, РА, ИФА, РИА), вирусологический, молекулярно-биологический (ПЦР) методы.
Лечение внутрибольничных инфекций
Сложности лечения внутрибольничной инфекции обусловлены ее развитием в ослабленном организме, на фоне основной патологии, а также резистентностью госпитальных штаммов к традиционной фармакотерапии. Больные с диагностированными инфекционными процессами подлежат изоляции; в отделении проводится тщательная текущая и заключительная дезинфекция. Выбор противомикробного препарата основывается на особенностях антибиотикограммы: при внутрибольничной инфекции, вызванной грамположительной флорой наиболее эффективен ванкомицин; грамотрицательными микроорганизмами – карбапенемы, цефалоспорины IV поколения, аминогликозиды. Возможно дополнительное применение специфических бактериофагов, иммуностимуляторов, интерферона, лейкоцитарной массы, витаминотерапии.
При необходимости проводится чрескожное облучение крови (ВЛОК, УФОК), экстракорпоральная гемокоррекция (гемосорбция, лимфосорбция). Симптоматическая терапия осуществляется с учетом клинической формы внутрибольничной инфекции с участием специалистов соответствующего профиля: хирургов, травматологов, пульмонологов, урологов, гинекологов и др.
Профилактика внутрибольничных инфекций
Основные меры профилактики внутрибольничных инфекций сводятся к соблюдению санитарно-гигиенических и противоэпидемических требований. В первую очередь, это касается режима дезинфекции помещений и предметов ухода, применения современных высокоэффективных антисептиков, проведения качественной предстерилизационной обработки и стерилизации инструментария, безукоснительного следования правилам асептики и антисептики.
Медицинский персонал должен соблюдать меры индивидуальной защиты при проведении инвазивных процедур: работать в резиновых перчатках, защитных очках и маске; осторожно обращаться с медицинским инструментарием. Большое значение в профилактике внутрибольничных инфекций имеет вакцинация медработников от гепатита В, краснухи, гриппа, дифтерии, столбняка и других инфекций. Все сотрудники ЛПУ подлежат регулярному плановому диспансерному обследованию, направленному на выявление носительства патогенов. Предупредить возникновение и распространение внутрибольничных инфекций позволит сокращение сроков госпитализации пациентов, рациональная антибиотикотерапия, обоснованность проведения инвазивных диагностических и лечебных процедур, эпидемиологический контроль в ЛПУ.
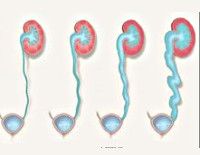
Пузырно-мочеточниковый рефлюкс — это патология, характеризующаяся обратным током урины из мочевого пузыря в мочеточник. Возникает при аномалиях выделительной системы, высоком давлении внутри пузыря или на фоне воспалительных процессов. Рефлюкс может стать причиной пиелонефрита, гидронефроза, почечной недостаточности. Основные симптомы — болевые ощущения в поясничной области после мочеиспускания, помутнение мочи, отеки, лихорадка. Методы диагностики: общие анализы мочи, крови, УЗИ почек, экскреторная урография, микционная цистография. Лечение сводится к терапии воспалительного заболевания или хирургическому устранению аномалий мочевыделительной системы.
МКБ-10
Общие сведения
Пузырно-мочеточниковый, или везикоуретеральный, рефлюкс — одно из самых распространенных урологических заболеваний, особенно среди детей. Обнаруживается у 1% пациентов урологического профиля, доля двустороннего процесса составляет 50,9%. Регургитация мочи выявляется у 40% больных с инфекционными заболеваниями мочевых путей.
Распространенность патологии, высокий риск осложнений (почечная недостаточность, вторичная артериальная гипертензия, гнойные заболевания почек) обусловливают большой процент инвалидизации пациентов. Врожденный рефлюкс наблюдается у 1 ребенка из 100, при этом соотношение детей женского и мужского пола на первом году жизни составляет 5:1. По мере взросления частота встречаемости патологии у мальчиков растет с изменением ситуации на противоположную.

Причины
Этиологическими факторами нефизиологического движения мочи являются процессы, ведущие к недостаточности сфинктера области мочеточникового соустья. Сфинктер — физиологический барьер, разделяющий мочеточники и мочевой пузырь, препятствующий обратному току урины. Дополнительные предпосылки для регургитации создает высокое давление жидкости в мочевом пузыре. Основные группы факторов, ведущие к развитию рефлюкса, включают:
- Аномалии развития выделительной системы. Снижение замыкательной функции сфинктера развивается вследствие неправильного формирования этого сегмента выделительной системы на этапе внутриутробного развития. Аномальное строение может проявляться в виде постоянно открытого устья мочеточника, отсутствия или уменьшения мышечного слоя констриктора, его дисплазии, тканевой дегенерации.
- Высокое внутрипузырное давление мочи. Повреждение головного, спинного мозга, тазовых нервов приводит к нарушению регуляции тонуса мышц мочевого пузыря. Мышечная стенка находится в постоянном напряжении, что создает повышенное гидростатическое давление. Это приводит к неспособности здорового сфинктера сдерживать мочу. Причинными факторами такого состояния являются врожденные (детский церебральный паралич, агенезия крестца) и приобретенные (опухоли мозга, инсульт, болезнь Паркинсона, сахарный диабет) патологии.
- Воспалительный процесс. Уменьшение барьерной функции пузырно-мочеточникового соустья возможно при воспалении мочевых путей. Рефлюкс обычно является следствием запущенных острых и хронических форм цистита или восходящего уретрита. Инфекция чаще вызывается условно-патогенными микроорганизмами, особенно кишечной палочкой, на фоне снижения местного или общего иммунитета.
- Ятрогенные причины. Формирование ретроградного заброса урины через пузырно-мочеточниковое соустье возможно после перенесенного оперативного вмешательства в области дистальных отделов выделительного аппарата. Наиболее частыми операциями, приводящими к рефлюксу, являются простатэктомия, рассечение уретероцеле, резекция шейки мочевого пузыря. При любой из них существует вероятность нарушения нормальной анатомической структуры мочевого пузыря и пузырно-мочеточникового сегмента.
К факторам, увеличивающим риск развития рефлюкса, относят его наличие в семейном анамнезе, особенно у ближайших родственников (родителей, братьев, сестер). Также повышают вероятность нарушений регуляции тонуса мочевого пузыря или сфинктера соустья опухоли спинного мозга, врожденные аномалии позвоночника, например, его расщепление.
Патогенез
Область соединения мочеточников с полостью мочевого пузыря анатомически представляет собой сфинктерный антирефлюксный аппарат, который обеспечивает ток урины только в нисходящем направлении. Это достигается благодаря определенному углу, под которым мочеточник впадает в мочевой пузырь, и внутристеночным гладким циркулярным мышцам. Главное патологическое звено формирования рефлюкса — снижение эффективности работы сфинктера в результате дисплазии мышечных волокон, их воспалительного повреждения, нарушения нервной регуляции. Морфофункциональные изменения приводят к срыву антирефлюксного механизма и нефизиологическому ретроградному движению мочи.
Высокое гидростатическое давление обуславливает деформацию и дилатацию мочеточника и почечных лоханок. Создаются условия для переноса бактерий из нижних сегментов выделительной системы в верхние, что приводит к развитию острой или хронической рецидивирующей инфекции в паренхиме почек с замещением ренальной ткани на нефункциональную соединительную. Нефросклероз является причиной дисфункции почечного фильтра и развития жизнеугрожающих состояний.
Классификация
Современная клиническая урология стремится к выработке единой общепризнанной классификации, поскольку именно от степени пузырно-мочеточникового рефлюкса (ПМР) во многом зависит выбор дальнейшей терапевтической тактики. На сегодняшний день наиболее широкое распространение получила систематизация процесса в зависимости от уровня обратного заброса мочи:
- Iстепень. Вследствие недостаточности сфинктера рефлюкс небольшого количества мочи ограничивается дистальным тазовым отделом мочеточника. Расширения мочеточника не происходит. Риск осложнений инфекционного и неинфекционного характера минимален, симптоматика отсутствует. Обнаружение ПМР обычно происходит при обследовании по поводу других заболеваний выделительной системы.
- IIстепень. Заброс урины отмечается на всем протяжении мочеточника, но без его дилатации. При этом моча не достигает почек, чашечно-лоханочной системы. Данной степени свойственно отсутствие ярко выраженных симптомов, небольшой риск инфекционных осложнений, но высокая скорость прогрессирования рефлюкса, быстрый переход на следующие уровни развития. Обнаруживается случайно при плановом профилактическом обследовании или диагностике иных патологий.
- IIIстепень. Моча достигает почек, но расширения лоханок не наблюдается. Возможно снижение почечной функции на 20%, обнаруживаемое при биохимических анализах. Мочеточник расширен, есть признаки дегенеративного трофического перерождения тканей. Риск присоединения инфекции повышается вследствие застоя мочи в выделительной системе, что часто является поводом для обращения к специалисту. Симптомы имеют среднюю степень выраженности.
- IVстепень. Регистрируется существенное расширение, деформация чашечно-лоханочной области и мочеточников. Функция почек снижается значительно (до 50%) с уменьшением продукции мочи, особенно на фоне инфекционных осложнений. Симптоматика выраженная, с фебрильной температурой, генерализованными отеками. При двустороннем процессе возможно развитие угрожающих жизни состояний, что требует скорейшего обращения к специалистам.
- Vстепень. Диагностируется тяжелая степень поражения почек с истончением их паренхимы наряду со всеми признаками, характерными для предыдущих степеней. Мочеточник вследствие чрезмерного расширения имеет коленообразные изгибы. Нарастающие симптомы почечной недостаточности (снижение диуреза, тошнота, рвота, кожный зуд) требуют немедленного обращения за квалифицированной помощью.
Существуют классификации пузырно-мочеточникового рефлюкса, основанные на других признаках, например, на этиологическом факторе (врожденный, приобретенный), характере процесса (одно-, двусторонний), клиническом течении (интермиттирующий, постоянный). Но ключевым показателем является расширение структур мочевыводящих путей. Даже незначительная дилатация мочеточника или лоханок почек может значительно ухудшить их функцию.
Симптомы ПМР
Специфических проявлений пузырно-мочеточниковый рефлюкс не имеет, на ранних стадиях может протекать бессимптомно. Появление признаков ПМР чаще всего служит результатом длительного отсутствия лечения или присоединившихся инфекционных осложнений. Симптомы периода обострения схожи с проявлениями воспалительных патологий почек и зависят от возраста пациента.
Для детей с врожденным или приобретенным в раннем возрасте рефлюксом характерны бледность кожных покровов, болезненный вид, сниженная масса тела, рост и развитие, не соответствующие возрасту, беспокойное поведение, боли в области живота, поясницы. Обратиться к нефрологу родителей часто вынуждает утяжеление состояния ребенка (высокая температура, задержка мочи), что свидетельствует о присоединении инфекции.
У взрослых не описано специфических признаков рефлюкса. В большинстве случаев они наслаиваются на проявления других болезней мочевыделительной системы. К общим симптомам относят генерализованные отеки, повышенную жажду, увеличенный диурез (при условии нормальной или незначительно сниженной функции почек), ощущение распирания и боли ноющего характера в пояснице, внизу живота.
При остром пиелонефрите возможно помутнение урины из-за гноя, появление кровянистых выделений, повышение температуры до 39-40°С. Могут наблюдаться несвойственные для инфекции мочевыводящих путей признаки: диарея, отсутствие аппетита, энурез, повышенная нервная возбудимость, тахикардия.
Осложнения
Возникновение рефлюкса, независимо от его этиологических факторов, — возможная причина развития дополнительных патологий, ухудшающих функцию почек и, следовательно, состояние пациента. К наиболее часто встречающимся в практике осложнениям относят пиелонефрит, гидронефроз, почечную гипертензию, хроническую почечную недостаточность. Эти состояния, несмотря на разную природу, обусловлены единым патогенетическим звеном — нарушением нормального тока мочи.
Застойные явления в мочевыделительной системе повышают риск развития инфекционных осложнений, которые приводят к уменьшению притока к почкам насыщенной кислородом артериальной крови. Гипоксия стимулирует выброс ренальными клетками биологически активных веществ, сужающих сосуды и вызывающих артериальную гипертензию.
Диагностика
Устранение рефлюкса и его последствий начинается с полноценной диагностики, установления причины и степени патологии. Первая и вторая степени регургитации обнаруживаются урологами случайно при профилактическом осмотре или во время обследования по поводу другого заболевания мочевыделительной системы со схожими симптомами. Диагностика включает в себя:
Дифференциальная диагностика рефлюкса проводится со стенозом устья мочеточника, дающим схожую клиническую картину. Также исключается мочекаменная болезнь, рак матки и простаты, туберкулез выделительной системы.
Лечение ПМР
Выбор терапевтической тактики зависит от ряда факторов: причины заболевания, пола, возраста, степени тяжести, длительности проводимой консервативной терапии. Если рефлюкс вызван воспалительными процессами нижних отделов мочевыделительной системы, то чаще всего изменения соответствуют I-II степени, не затрагивают почки и дают возможность ограничиться консервативной терапией. При своевременном обращении за помощью и отсутствии органических причин этот вид лечения позволяет устранить ПМР в 60-70% случаев. Консервативная терапия рефлюкса включает следующие компоненты:
- Диета. Специальное питание повышает выведение продуктов обмена и оказывает противовоспалительное воздействие. Больному рекомендуется ограничить прием соли до 3 грамм в сутки, существенно или полностью исключить жирные блюда, но увеличить количество овощей, фруктов, зерновых. Запрещается употребление алкоголя, газированных напитков, крепкого кофе.
- Медикаментозные средства. При наличии воспалительных или инфекционных очагов показан прием соответствующих лекарств — антибиотиков, противовоспалительных, спазмолитических средств. Высокие цифры артериального давления требуют применения антигипертензивных препаратов. В целях профилактики застойных явлений в органах выделительной системы больному рекомендуется каждые 2 часа опорожнять мочевой пузырь, для чего возможно применение диуретиков средней силы действия.
- Физиотерапия. Дополнительно возможно использование физиопроцедур: электрофореза, магнитотерапии, лечебных ванн. Воздействие физических факторов способствует устранению воспалительного процесса, спазма гладких мышц мочевыводящих путей, восстанавливает физиологический ток мочи. Лицам с развившейся вследствие пиелонефрита хронической почечной недостаточностью показано санаторно-курортное лечение.
Отсутствие в течение полугода существенных изменений состояния или возможное его ухудшение (рецидивирующий пиелонефрит, снижение функциональности почек на 30% и более, высокая степень тяжести патологии), требует планового хирургического вмешательства в условиях урологического стационара. К базовым вариантам оперативного лечения рефлюкса относят:
- Эндоскопическая коррекция. При начальных (I-II) стадиях процесса возможно эндоскопическое инъекционное введение в область устья мочеточника объемообразующих имплантатов, укрепляющих эти структуры. Основой могут выступать коллаген, силикон, тефлон, обладающие низким риском развития аллергических реакций, прочностью, биосовместимостью.
- Лапароскопическая уретероцистонеостомия. Проводится при III-V степени ПМР. Тяжелые изменения стенки мочеточника, органическая патология сфинктера требуют создания нового искусственного соединения мочеточника с мочевым пузырем (уретероцистоанастомоз) и удаления патологически измененных тканей. Возможно сочетание операции с резекцией дистальной части мочеточника или пересадкой почки.
Прогноз и профилактика
Своевременная диагностика рефлюкса, назначение комплексного лечения дает положительный исход терапевтических мероприятий. Присоединение осложнений, сопровождающихся необратимым повреждением почек с их недостаточной функцией, значительно ухудшает прогноз. Специфической профилактики данной патологии не разработано. Общими мероприятиями являются своевременное обращение к врачам с любыми заболеваниями выделительной системы, уменьшение потребления соли, предупреждение травм спины, малого таза, потребление достаточного количества жидкости, периодические профилактические обследования.
2. Современные подходы к лечению пузырно-мочеточникового рефлюкса у детей (обзор литературы)/ Добросельский М.В., Чепурной Г.И., Коган М.И., Сизонов В.В.// Медицинский вестник Юга России. – 2014.
4. Пузырно-мочеточниковый рефлюкс у детей: лечебная тактика/ Павлов А.Ю., Маслов С.А., Поляков Н.В., Лисенок А.А., Симонян Г.В.// Лечащий врач. – 2006.
Что такое папилломавирусная инфекция (ВПЧ)? Причины возникновения, диагностику и методы лечения разберем в статье доктора Борисова Э. В., гинеколога со стажем в 35 лет.
Над статьей доктора Борисова Э. В. работали литературный редактор Юлия Липовская , научный редактор Сергей Федосов

Определение болезни. Причины заболевания
Папилломавирусная инфекция — это состояние, развивающееся при заражении какой-либо разновидностью вируса папилломы человека (ВПЧ). Возбудители данной группы могут существовать только в человеческом организме, поражая кожу и слизистые оболочки, приводя к появлению папиллом, бородавок, плоских и остроконечных кондилом. [1] [2] [4]
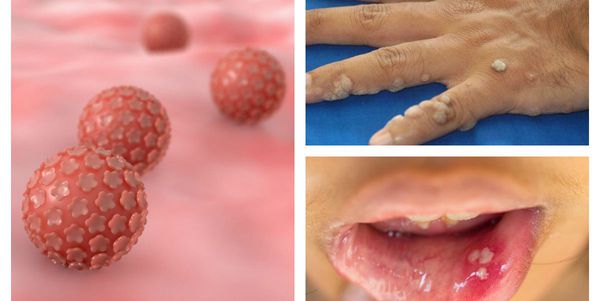
ВПЧ довольно широко распространён в человеческой популяции, особенно среди сексуально активных людей, а это свыше 80% всего населения. До недавнего времени вирусы этой группы считались относительно безобидными, вызывающими лишь косметические дефекты, но последние научные исследования показывают, что проблема гораздо серьёзнее. [9]
На сегодняшний день науке известно несколько сотен штаммов (типов) папилломавирусов . Около 40 из них преимущественно поражают аногенитальную область и передаются половым путём. Особую опасность представляют штаммы высокого онкогенного риска, так как они могут спровоцировать развитие онкологических заболеваний, в том числе рака шейки матки.
Чаще всего заражение происходит в молодом возрасте, как правило, с началом половой жизни, при этом возможно неоднократное инфицирование. Наиболее уязвимой группой в плане вероятности заражения ВПЧ и развития неблагоприятных последствий являются молодые женщины в возрасте 15-30 лет.
Помимо этого ВПЧ может перейти от инфицированной матери к ребёнку, например, при родах. Не исключается и контактно-бытовой способ передачи возбудителя, например, при соприкосновениях и даже при совместном использовании предметов личной гигиены.
К факторам риска, способствующим заражению ВПЧ, развитию хронической папилломавирусной инфекции и её переходу в предраковые состояния с потенциальным перерождением в злокачественную опухоль, относятся:
- иммунодефицит любого происхождения, в том числе вследствие ВИЧ-инфекции, лучевых поражений, применения иммунодепрессантов при трансплантации органов и тканей, лечения цитостатиками и других причин;
- подавленное состояние иммунитета во время беременности;
- раннее начало половой жизни;
- частая смена половых партнёров, незащищённый секс;
- инфицированность высокоонкогенными штаммами ВПЧ;
- заражение одновременно несколькими типами ВПЧ;
- наличие других инфекций, передающихся половым путём, например, герпесвирусной и цитомегаловирусной инфекции, вируса Эпштейна — Барр, гепатитов В и С, гонореи и трихомониаза;
- стресс, истощение, гиповитаминоз, гормональный дисбаланс;
- многократные роды и аборты;
- тяжёлые хронические заболевания, в том числе сахарный диабет;
- вредные привычки (курение, злоупотребление спиртным);
- низкий социальный статус, плохие условия жизни, неудовлетворительная интимная гигиена;
- пренебрежение регулярными профилактическими обследованиями (один из важнейших факторов риска);
- низкий уровень развития медицины в регионе проживания.
При обнаружении схожих симптомов проконсультируйтесь у врача. Не занимайтесь самолечением - это опасно для вашего здоровья!
Симптомы папилломавирусной инфекции
Далеко не всегда человек догадывается о наличии в своём организме папилломавирусной инфекции, оставаясь при этом источником заражения для потенциальных партнёров. [1] [2] Дело в том, что заболевание может долгое время протекать бессимптомно: вирус скрыто существует в организме от нескольких месяцев до нескольких лет, никак себя не проявляя. Кроме того, уже имеющиеся проявления инфекции не всегда доступны для наружного обзора. Например, если папилломы, бородавки и кондиломы на открытых участках тела и поверхности гениталий ещё можно заметить самостоятельно, то патологические изменения, локализующиеся на шейке матки, сможет обнаружить только специалист в ходе осмотра с применением соответствующих инструментов.
И всё же существует несколько симптомов, которые прямо или косвенно могут указывать на наличие папилломавирусной инфекции и её неблагоприятных последствий. [3] К ним относятся:
- появление на коже и/или слизистых оболочках каких-либо разрастаний различных форм (на тонкой ножке или с широким основанием, нитевидной, округлой или плоской конфигурации, в форме цветной капусты или петушиного гребня) и размеров (от образований в несколько миллиметров до разрастаний, занимающих всю промежность);
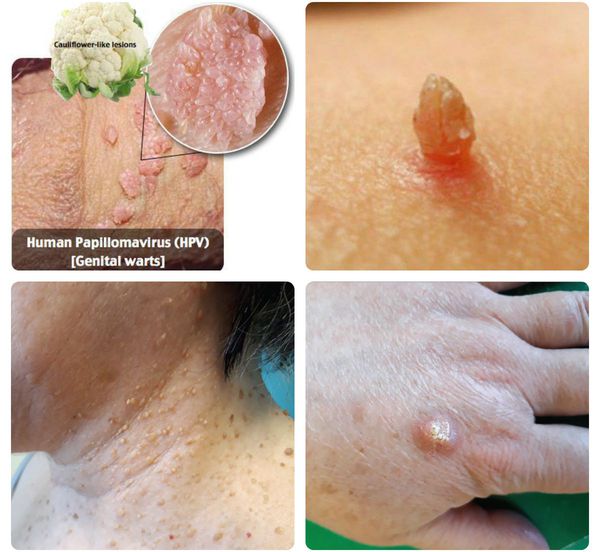
- отёчность и воспалительная инфильтрация папилломатозных разрастаний (остроконечных кондилом), их ранимость и кровоточивость, что приводит к присоединению вторичной инфекции с появлением гнойного отделяемого с неприятным запахом;
- зуд, жжение, мокнутие в области промежности, появление обильных белей, даже при отсутствии видимых патологических образований;
- межменструальные кровянистые выделения, в том числе появляющиеся в результате полового контакта:
- дискомфорт во время полового акта.
Наиболее тревожными признаками заболевания являются:
- постоянные боли в области спины и таза;
- слабость;
- беспричинная потеря веса;
- опухание одной или обеих ног.
Патогенез папилломавирусной инфекции
Заражение папилломавирусной инфекцией происходит при попадании вирусных частиц на кожу или слизистую оболочку. [1] [2] Излюбленная локализация инфекции на теле женщины — промежность, большие и малые половые губы, вульва, влагалище и шейка матки, у мужчин — половой член. Может также произойти поражение слизистой полости рта, пищевода, мочевого пузыря, трахеи, конъюнктивы и других органов и тканей.
Заражению способствуют микротравмы и потёртости. Особенно благоприятные для инфицирования условия создаются при половом акте. В 60–80% случаев достаточно однократного сексуального контакта с больным папилломавирусной инфекцией или бессимптомным носителем ВПЧ. К развитию заболевания может привести попадание в организм буквально единичных вирусных частиц.
При наличии предрасполагающих факторов (микроповреждения, слабого иммунитета и других) возбудитель проникает в эпителиальную ткань до её базального слоя. Там он прикрепляется к оболочке незрелой клетки и внедряется сначала в её цитоплазму, а затем и в ядро, где повреждает генетический аппарат. После этого начинается деление клеток с изменённым геномом, что приводит к появлению в месте внедрения вируса генитальных кондилом (образований, которые постепенно разрастаются), а, например, на шейке матки — к развитию диспластических процессов различной степени тяжести (дисплазия шейки матки).
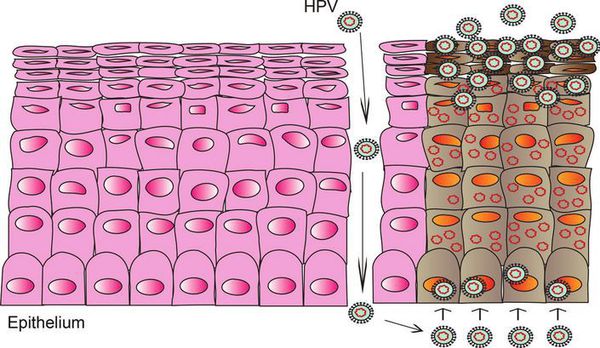
В случае ВПЧ высокого онкогенного риска определённые гены в вирусной ДНК кодируют синтез специфических белков-онкопротеинов (Е6 и Е7), которые подавляют противораковую защиту клеток. Под действием онкопротеинов нарушается стабильность генома клеток, стимулируется их размножение и снижается способность к дифференцировке — всё это со временем может привести к онкопатологии. [12]
Формирование новых полноценных вирусных частиц, способных инфицировать другого человека, происходит уже не в базальном, а в самых поверхностных слоях поражённого эпителия. Возбудитель может содержаться в слущивающихся отмирающих клетках, которые отделаются слизистой оболочкой. Таким образом они переходят к новому хозяину при тесном (сексуальном или бытовом) контакте.
Классификация и стадии развития папилломавирусной инфекции
По способности индуцировать развитие злокачественных новообразований ВПЧ подразделяют на четыре группы: [8]
- неонкогенные штаммы ВПЧ (типы 1-5);
- ВПЧ низкого онкогенного риска (типы 6, 11, 40, 42-44, 54, 61, 70, 72, 81);
- ВПЧ среднего онкогенного риска (типы 26, 31, 33, 35, 51-53, 58, 66);
- ВПЧ высокого онкогенного риска (типы 16, 18, 39, 45, 56, 59, 68, 73, 82).
Клинические формы папилломавирусной инфекции: [5]
- латентная — скрытая форма, не имеющая клинических и морфологических признаков, но обнаруживаемая иммунохимическими и молекулярно-биологическими методами;
- субклиническая — возникает у лиц с нормальным иммунитетом, определяется только специальными диагностическими методами (пробы с растворами-индикаторами, гистологические и цитологические исследования);
- манифестная — появляется у лиц с временным или стойким снижением иммунитета, в случае генитальной папилломавирусной инфекции характеризуется появлением кондилом.
Латентная инфекция может переходить в субклиническую и манифестную форму в случае возникновения предрасполагающих условий (факторов риска), но чаще всего она протекает бессимптомно, не манифестируя.
Клинические проявления папилломавирусной инфекции:
- кожные поражения: подошвенные, плоские и обычные (вульгарные) бородавки, бородавчатая эпидермодисплазия, бородавки Бютчера и небородавчатые поражения кожи;
- поражения слизистых оболочек гениталий: кондиломы, некондиломатозные поражения, карциномы;
- поражения слизистых вне гениталий: папилломатоз гортани, карциномы шеи, языка и другое.
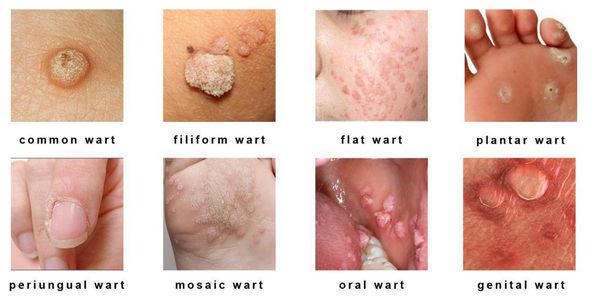
Разновидности поражений:
- экзофитные — видимые разрастания в виде папиллом и бородавок;
- эндофитные — образования, располагающиеся в толще ткани, которые не видны невооружённым глазом.
Осложнения папилломавирусной инфекции
Основными наиболее опасными осложнениями папилломавирусной инфекции являются злокачественные новообразования. Но возможны и другие серьёзные последствия:
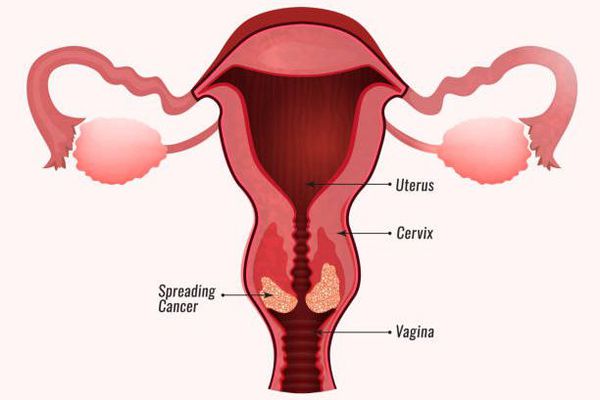
- Злокачественные новообразования заднего прохода, вульвы, полового члена и ротоглотки. Повышение риска их развития также связывают с высокоонкогенными штаммами ВПЧ. [6]
- Остроконечные кондиломы на гениталиях, папилломатоз верхних дыхательных путей (рецидивирующий респираторный папилломатоз, веррукозный ларингит). Причиной возникновения могут стать 6-й и 11-й типы вируса, несмотря на свой низкий онкогенный риск. В случае папилломатоза есть вероятность полной потери голоса, обструкции (перекрытия) гортани с развитием асфиксии. Это довольно редкое заболевание может возникать у детей, рождённых женщинами с папилломавирусной инфекцией. По разным данным, заражение может происходить как во время родов, так и внутриутробно. Как правило, респираторный папилломатоз начинает проявляться в детском и подростковом возрасте, он склонен к неоднократным рецидивам после удаления множественных папиллом, перекрывающих дыхательные пути.
- Гнойно-септические осложнения. Папилломатозные разрастания на слизистых оболочках очень ранимы, легко травмируются, и через участки мокнутия, расчёсов и потёртостей может проникать вторичная инфекция, которая в свою очередь и вызывает нагноение.
Диагностика папилломавирусной инфекции
Основные цели диагностических мероприятий: [3]
- ранняя диагностика папилломавирусной инфекции для динамического наблюдения и лечения;
- своевременное обнаружение и лечение предраковых изменений, что позволяет на 80% предотвратить развитие злокачественных новообразований;
- выявление онкологических новообразований на ранних стадиях, что в большинстве случаев даёт хороший прогноз эффективного излечения;
- решение вопроса о целесообразности вакцинации.
Для выявления папилломавирусной инфекции на сегодняшний день существует целый комплекс диагностических процедур:
- Гинекологический осмотр в зеркалах — позволяет увидеть папилломатозные разрастания (аногенитальные кондиломы) и другие изменения.
- Классический тест Папаниколау (мазки с поверхности шейки матки и стенок влагалища для цитологического исследования) — обнаруживает ранние признаки дисплазии и злокачественного перерождения.
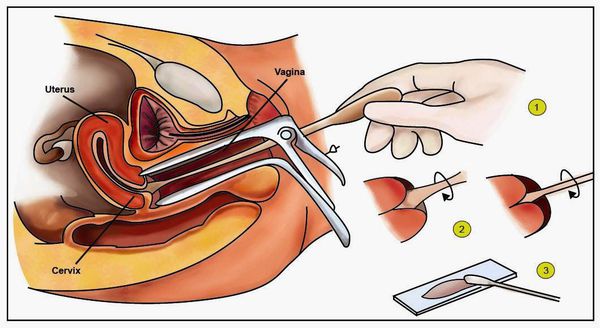
- Пробы с уксусной кислотой и раствором Люголя — выявляют участки поражения слизистой шейки матки.
- Кольпоскопия, в том числе с биопсией подозрительных участков и их гистологическим исследованием, — определяет характер имеющегося новообразования.
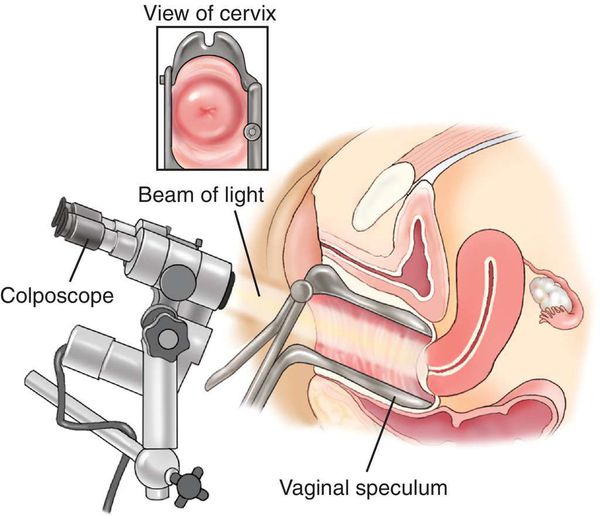
- Иммунофлюоресцентный анализ (ИФА) обнаруживает в цервикальном соскобе онкопротеины (Е7 и Е6). Этот метод достаточно новый, с его помощью можно различить носительство ВПЧ и первые признаки злокачественного перерождения в клетках, [12] оценить агрессивность данного процесса, сделать предположения относительно прогноза заболевания.
- Полимеразная цепная реакция (ПЦР) находит вирусную ДНК в биологическом материале (соскоб со слизистой), определяет тип ВПЧ, степень его онкогенности, а также количество вирусных частиц, что косвенно позволяет судить о характере течения папилломавирусной инфекции у данного пациента, возможности спонтанного излечения или высокого риска прогрессирования. Обнаружение ВПЧ с помощью этого возможно даже при латентном течении болезни, когда цитологические и гистологические методы не эффективны.
Целесообразно дополнительное обследование пациента на наличие других инфекций, передающихся половым путём, так как папилломавирус в 90% случаев с ними сочетается, и это может осложнять течение заболевания.
Лечение папилломавирусной инфекции
Лечение папилломавирусной инфекции должно быть комплексным и включать следующие составляющие: [3] [5]
- деструкцию (удаление) видимых проявлений (аногенитальных кондилом и др.);
- иммуномодулирующую терапию;
- противовирусную терапию;
- лечение сопутствующих инфекций, передающихся половым путём.
Деструктивные методы делятся на две основные группы:
- химические — с применением трихлоруксусной кислоты, а также таких препаратов, как "Солкодерм", "Колломак", "Ферезол" и др.;
- физические — хирургическое удаление, электрокоагуляция, криодеструкция, радиоволновая и плазменная коагуляция, лазеротерапия.
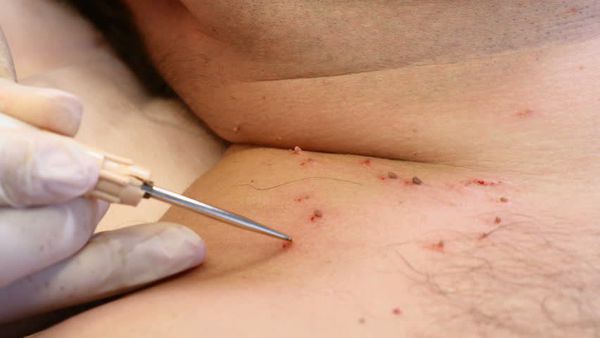
Лечение сопутствующих половых инфекций проводят до начала деструктивной терапии на фоне адекватной иммунокоррекции.
Удаление видимых проявлений папилломавирусной инфекции должно сочетаться с противовирусной терапией — как с общей, так и с применением препаратов местного действия после удаления кондилом.
Следует помнить, что успешно проведённое лечение не исключает развитие рецидивов в дальнейшем, особенно у пациентов с нарушениями иммунитета. Поэтому за ними устанавливается динамическое наблюдение в течение как минимум 1-2 лет.
Прогноз. Профилактика
В 90% случаев здоровая иммунная система человека справляется с папилломавирусной инфекцией самостоятельно за период от полугода до двух лет с момента инфицирования, после чего происходит полное выздоровление с исчезновением вируса из организма. При этом не формируется напряжённого пожизненного иммунитета, то есть человек может заразиться повторно.
В других случаях, при наличии предрасполагающих факторов, заболевание приобретает хроническую форму, склонную к длительному скрытому течению с периодическими рецидивами и возможным развитием тяжёлых осложнений.
От момента попадания вируса в организм до развития предраковых состояний и тем более возникновения рака может пройти достаточно много времени, иногда десятки лет. Поэтому регулярные профилактические обследования, своевременное выявление и лечение предраковых состояний — вполне реальный и эффективный способ избежать самого неблагоприятного варианта развития событий. [13] С этой целью Всемирная организация здравоохранения рекомендует всем женщинам старше 30 лет при первичном скрининге проходить не только “рутинное” цитологическое исследование, но и делать тест на наличие ВПЧ. [10]
Регулярное посещение гинеколога (при отсутствии каких-либо жалоб — раз в год) с проведением теста Папаниколау позволяет своевременно обнаружить начальные признаки дисплазии и предпринять все необходимые меры для предотвращения прогрессирования процесса и его перехода в онкологическое заболевание.
Использование методов барьерной контрацепции хоть и не полностью защищает от инфицирования, но несколько снижает его вероятность.
Главным методом первичной профилактики папилломавирусной инфекции считается вакцинация. [11] Современные вакцины разработаны с целью защиты от наиболее опасных, высокоонкогенных штаммов ВПЧ, ответственных за 70-80% случаев развития рака шейки матки. Стандартный курс, состоящий из трёх прививок, даёт вполне надёжную защиту.
Читайте также:

