Инфекционных миокардит патологоанатомический диагноз
Обновлено: 23.04.2024
Миокардит представляет собой поражение сердечной мышцы преимущественно воспалительного характера, обусловленное опосредованным через иммунные механизмы воздействием инфекции, паразитарной или протозойной инвазии, химических и физических факторов, а также возникающее при аллергических и иммунных заболеваниях.
Классификация
По локализации:
- паренхиматозные;
- интерстициальные.
По распространенности:
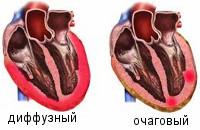
- очаговые;
- диффузные.
По течению:
- острые;
- подострые;
- хронические.
Этиология и патогенез
Болезнь Шагаса
Токсоплазмоз
Возбудитель - Toxoplasma gondii, относится к простейшим, к классу жгутиковых, семейству трипаносомид.
Патогенез
Попав в организм, токсоплазмы быстро распространяются лимфогенным и гематогенным путем; циркулируют в крови и лимфе в течение нескольких дней. Паразиты, занесенные в различные органы, могут вызывать в них воспалительный процесс большей или меньшей интенсивности. В основной массе случаев после заражения не возникает клинически выраженного заболевания. Считается, что это связано с тем, что токсоплазмы не всегда находят в организме человека благоприятные условия для активной жизнедеятельности. Однако, как правило, токсоплазмы не погибают и заключенные в оболочки паразиты в виде недеятельных форм годами сохраняют свою жизнеспособность и вирулентность в неизмененных тканях органов (в головном мозге, мышце сердца, лимфатических узлах и т. д.). Выявить токсоплазмы возможно только при помощи аллергической внутрикожной пробы с токсоплазмином или серологических реакций. Такое состояние определяется как латентный токсоплазмоз или как бессимптомная инфекция.
Эпидемиология
Токсоплазмоз
Резервуаром возбудителя в природе служат домашние и дикие млекопитающие животные и птицы. Человек заражается токсоплазмозом преимущественно от больных животных. Особенно большое значение в распространении токсоплазмоза среди людей имеют домашние животные: кошки, собаки, крупный и мелкий рогатый скот.
Клиническая картина
Cимптомы, течение
Миокардит при болезни Шагаса
Токсоплазмозный миокардит
Токсоплазмоз бывает врожденным и приобретенным. Поражение сердца в виде токсоплазмозного миокардита чаще встречается при приобретенной форме, хотя возможно и при врожденном токсоплазмозе.
Основные клинические проявления токсоплазмоза:
- общая слабость;
- головная боль;
- снижение остроты зрения;
- снижение аппетита;
Частым клиническим признаком токсоплазмоза является поражение сердечно-сосудистой системы: развивается миокардит с типичной клинической картиной, возможно развитие сердечной недостаточности.
Основные жалобы большинства больных токсоплазмозом: одышка, сердцебиение, частые боли в области сердца.
При объективном осмотре выявляют глухость тонов, систолический шум, расширение поперечника сердца.
Миокардиты могут быть очаговыми и диффузными. Очаговые миокардиты диагностируются при помощи инструментальных методов исследования, так как обычно не сопровождаются выраженными клиническими проявлениями. При диффузном миокардите может наблюдаться тяжелое течение с проявлениями сердечно-сосудистой недостаточности. При миокардитах токсоплазмозного генеза возможен летальный исход.
У больных наблюдаются значительные изменения в кровеносных сосудах, сдвиги в капиллярном кровообращении. Больше чем у половины пациентов отмечается артериальная гипотония с максимальным давлением 80-90 мм. рт. ст.
Диагностика
Диагностика болезни Шагаса
Диагностика токсоплазменного миокардита
1. Электрокардиография: неспецифические изменения сегмента ST и зубца Т, нарушения атриовентрикулярной проводимости.
2. В биоптатах миокарда при токсоплазменном миокардите выявляются воспалительная инфильтрация (часто инфильтраты содержат эозинофилы), распад кардиомиоцитов. Характерен выраженный отек между мышечными волокнами, в некоторых случаях в кардиомиоцитах обнаруживаются токсоплазмы.
3. Паразитологический метод имеет наибольшее значение в диагностике токсоплазмоза. Диагноз устанавливается при обнаружении токсоплазм при микроскопии окрашенных мазков крови, в центрифугате спинномозговой жидкости, в биоптатах лимфоузлов.
Лабораторная диагностика
Болезнь Шагаса
В острой стадии диагностика осуществляется путем обнаружения трипаносом в свежей гепаринизированной крови больного или в лейкоконцентратах. Возможно определение возбудителя в мазках крови и толстой капле, окрашенной по методу Гимза. При получении отрицательных результатов производят посевы крови на специальные среды или применяют ксенодиагностику Ксенодиагностика - метод установления возбудителя болезни, основанный на его выявлении при вскрытии переносчика или путем экспериментального заражения переносчика
.
При ксенодиагностике неинфицированным триатомовым клопам дают возможность насытиться кровью пациента и затем через 30 суток проверяют наличие трипаносом в экскрементах клопа. Данный метод также применяется для диагностики заболевания в хронической фазе.
Дифференциальный диагноз
Дифференциальная диагностика проводится с миокардитами другой этиологии (вирусной, бактериальной), а также с инфекционным эндокардитом, дилатационной кардиомиопатией и другими заболеваниями (см. также "Острый миокардит неуточненный" - I 40.9, раздел "Дифференциальный диагноз").
Осложнения
Возможные осложнения:
- развитие левожелудочковой дисфункции;
- прогрессивное ухудшение состояния с переходом в дилатационную кардиомиопатию и развитием симптомов сердечной недостаточности.
Лечение
Болезнь Шагаса
Эффективные способы лечения болезни Шагаса отсутствуют. Лекарственные средства снижают летальность, но не дают уверенности в том, что переносимые дозы уничтожат паразитов, которые локализуются внутри клеток.
В настоящее время эффективными для терапии болезни Шагаса считаются бензнидазол (benznidazole) и нифуртимокс (nifurtimox). Следует иметь в виду, что отсутствуют подтвержденные клинические данные о способности данных препаратов в переносимых дозах уничтожать локализованные внутриклеточно трипаносомы. Помимо этого указанные препараты обладают выраженными побочными действиями.
Лечение миокардита при болезни Шагаса должно быть направлено на уменьшение выраженности симптомов застойной сердечной недостаточности и лечение аритмий.
Токсоплазмоз
Этиотропное лечение токсоплазмоза наиболее эффективно в острой фазе заболевания. При хроническом токсоплазмозе эффективность снижается, поскольку применяемые препараты слабо воздействуют на эндозоиты (брадизоиты), находящиеся в тканевых цистах.
Препараты выбора: пириметамин в сочетании с сульфаниламидами.
В первые 2 дня пириметамин взрослым назначают по 0,075-0,1 г/сутки, в последующие - по 50-75 мг/сутки. Детям препарат назначают вначале в суточной дозе 2 мг/кг, далее - по 1 мг/кг.
Сульфаниламиды (сульфадиазин, сульфадимидин) назначают взрослым по 2,0-4,0 г/сутки, детям - 0,1 г/кг/сутки. Продолжительность курса - 2-4 недели, при необходимости возможно повторение цикла через 7 дней.
Для профилактики гематотоксичности при применении комбинации пириметамина с сульфаниламидами назначают фолиевую кислоту по 10-20 мг/сутки внутрь, через день. При необходимости применяют системные глюкокортикоиды.
Альтернативные препараты: спирамицин, клиндамицин, кларитромицин, ко-тримоксазол.
При аллергии на сульфаниламиды в комбинации с пириметамином используют клиндамицин (по 0,3 г каждые 6 часов).
В остальном лечение миокардитов при данных заболеваниях схоже с таковым при миокардитах другой этиологии.
Общие принципы терапии при миокардитах
Патогенетическое лечение
Включает назначение иммуносупрессивных, противовоспалительных и антигистаминных препаратов. В настоящее время, считается, что иммуносупрессивная терапия эффективна при гигантоклеточном миокардите, при хронически протекающих вирус-негативных воспалительных кардиомиопатиях, при лечении миокардитов, развившихся при аутоиммунных заболеваниях, коллагенозах.
Глюкокортикоиды показаны в следующих случаях:
- тяжелое течение миокардита (с выраженными иммунологическими нарушениями);
- миокардиты средней степени тяжести при отсутствии эффекта от проводимой терапии;
- миоперикардит;
- гигантоклеточный миокардит;
- миокардит, развивающийся у лиц с иммунодефицитом, ревматическими заболеваниями.
Как правило, применяют преднизолон 15-30 мг/сутки (при миокардитах средней степени тяжести) или 60-80 мг/сутки (при тяжелых формах), в течение от 5 недель до 2 месяцев с постепенным снижением суточной дозы препарата и его полной отменой.
Глюкокортикоиды не рекомендуются для лечения вирусных миокардитов на ранней стадии заболевания, так как это приводит к репликации вируса и вирусемии .
Метаболическая терапия
Обязательна в комплексном лечении миокардита и направлена на улучшение метаболических процессов в сердечной мышце. Применяются поляризующие смеси в/в, препараты калия (панангин, аспаркам), рибоксин, кокарбоксилаза, витамины, АТФ . Целесообразно в/в или в/м назначение средств, улучшающих тканевое дыхание (цитохром-С).
Симптоматическая терапия
Направлена на устранение признаков сердечной недостаточности, гипертензии, нарушений сердечного ритма, предупреждение тромбэмболических осложнений.
Лечение сердечной недостаточности: ограничение поваренной соли и жидкости, дифференцированное назначение сердечных гликозидов, блокаторов β-адренергических рецепторов, ИАПФ , диуретиков.
1. Возможно назначение сердечных гликозидов при миокардите в случае аритмии и систолической дисфункции левого желудочка (фибрилляция предсердий, пароксизмальная тахикардия) по мере угасания остроты процесса (в дозе не более 0,25 мг дигоксина).
2. Ингибиторы АПФ: эналаприл 5-20 мг внутрь 2 раза в день, каптоприл 12,5- 50 мг 3 раза в день, лизиноприл 5-40 мг 1 раз в день.
3. β-адреноблокаторы: метопролол 12,5-25 мг/сутки, бисопролол 1,25-10 мг/сутки однократно, карведилол 3,125-25 мг 2 раза в день.
4. Петлевые диуретики: фуросемид 10-160 мг внутрь 1-2 раза в день, буметанид 1-4 мг внутрь 1-2 раза в день, спиронолактон 12,5-20 мг внутрь 1 раз в день.
При тяжелых формах миокардитов с высокой лабораторной и клинической активностью целесообразно назначать гепарин (гепарин натрия) для профилактики тромбоэмболических осложнений. Гепарин оказывает также иммунодепрессивное и противовоспалительное действие.
Гепарин назначают в дозе 5000-10000 ME 4 раза в сутки подкожно, в течение 7-10 дней. Далее в течение 10-14 дней дозировку постепенно снижают под контролем коагулограммы, с последующим переводом пациента на варфарин (под контролем МНО ).
Антикоагулянтная терапия может быть противопоказана при сопутствующем перикардите.
Длительная антикоагулянтная терапия варфарином показана пациентам с перенесенными системными или легочными эмболиями или с пристеночными тромбами, выявленными при ЭхоКГ или вентрикулографии .
Миокардит – воспаление мышечной оболочки сердца (миокарда), чаще ревматического, инфекционного или инфекционно-аллергического характера. Течение миокардита может быть острым или хроническим. Острый миокардит проявляется одышкой, цианозом, отеками на ногах, набуханием вен на шее, болями в сердце, сердцебиением, аритмиями. Часто развитию миокардита предшествует перенесенная инфекция (дифтерия, ангина, скарлатина, грипп и др.). В дальнейшем возможны рецидивы заболевания (при ревматическом миокардите), развитие сердечной недостаточности и тромбоэмболий сосудов различных органов.
Общие сведения
Миокардит – воспаление мышечной оболочки сердца (миокарда), чаще ревматического, инфекционного или инфекционно-аллергического характера. Течение миокардита может быть острым или хроническим. Острый миокардит проявляется одышкой, цианозом, отеками на ногах, набуханием вен на шее, болями в сердце, сердцебиением, аритмиями. Часто развитию миокардита предшествует перенесенная инфекция (дифтерия, ангина, скарлатина, грипп и др.). В дальнейшем возможны рецидивы заболевания (при ревматическом миокардите), развитие сердечной недостаточности и тромбоэмболий сосудов различных органов.
Частота заболеваемости миокардитом намного выше статистической из-за поздней диагностики и латентных форм, когда заболевание протекает стерто или в легкой форме. Признаки воспалительного процесса в миокарде в 4–9% случаев обнаруживаются только на аутопсии (по результатам патологоанатомических исследований). От острого миокардита умирает от 1 до 7% больных, у людей молодого возраста в 17-21% случаев он становится причиной внезапной смерти.
Миокардит приводит к развитию сердечной недостаточности и нарушению ритма сердца, что является ведущими причинами летального исхода. Миокардиты встречаются чаще у молодых людей (средний возраст пациентов 30 – 40 лет), хотя заболевание может возникнуть в любом возрасте. Мужчины заболевают миокардитом несколько реже женщин, но у них чаще развиваются тяжелые формы заболевания.

Причины миокардита
Миокардиты включают большую группу заболеваний сердечной мышцы воспалительного генеза, проявляющихся поражением и нарушением функции миокарда. Частой причиной миокардита являются различные инфекционные заболевания:
- вирусные (вирусы Коксаки, гриппа, аденовирусы, герпеса, гепатита В и С);
- бактериальные (коринеобактерии дифтерии, стафилококки, стрептококки, сальмонеллы, хламидии, риккетсии);
- грибковые (аспергиллы, кандиды),;
- паразитарные (трихинеллы, эхинококки) и др.
Тяжелая форма миокардита может возникать при дифтерии, скарлатине, сепсисе. Высокой кардиотропностью обладают вирусы, вызывающие миокардит в 50% случаев. Иногда миокардит развивается при системных заболеваниях соединительной ткани: системной красной волчанке, ревматизме, васкулитах, ревматоидном артрите, при аллергических заболеваниях. Также причиной миокардита может служить токсическое воздействие некоторых лекарственных препаратов, алкоголя, ионизирующее излучение. Тяжелое прогрессирующее течение отличает идиопатический миокардит невыясненной этиологии.
Провоцирующими моментами возникновения миокардита являются острые инфекции (чаще вирусные), очаги хронической инфекции; аллергозы, нарушенные иммунологические реакции; токсическое воздействие на организм (лекарств, алкоголя, наркотиков, ионизирующего излучения, при тиреотоксикозе, уремии и др.).
Патогенез
Миокардит в большинстве случаев сопровождается эндокардитом и перикардитом, реже воспалительный процесс затрагивает только миокард. Повреждение миокарда может возникать при прямом миокардиоцитолитическом действии инфекционного агента; под влиянием токсинов, циркулирующих в крови (в случае системной инфекции); и как результат аллергической или аутоиммунной реакции. Нередко встречаются инфекционно-аллергические миокардиты.
Иммунные нарушения, наблюдаемые при миокардите, проявляются расстройством всех звеньев иммунитета (клеточного, гуморального, фагоцитоза). Инфекционный антиген запускает механизм аутоиммунного повреждения кардиомиоцитов, приводящий к значительным изменениям миокарда: дистрофическим изменениям мышечных волокон, развитию экссудативных или пролиферативных реакций в интерстициальной ткани. Следствием воспалительных процессов при миокардите является разрастание соединительной ткани и развитие кардиосклероза. При миокардите заметно снижается насосная функция сердечной мышцы, что часто носит необратимый характер и приводит к тяжелому состоянию недостаточности кровообращения, нарушениям сердечного ритма и проводимости, служит причиной инвалидности и летального исхода в молодом возрасте.
Классификация
В зависимости от механизма возникновения и развития миокардита выделяют следующие формы:
- инфекционные и инфекционно-токсические (при гриппе, вирусах группы Коксаки, дифтерии, скарлатине и др.);
- аллергические (иммунные) (сывороточный, инфекционно-аллергический, трансплантационный, лекарственный, миокардиты при системных заболеваниях);
- токсико-аллергические (при тиреотоксикозе, уремии и алкогольном поражении сердца);
- идиопатические (невыясненной природы).
По распространенности воспалительного поражения миокардиты делятся на диффузные и очаговые. По течению различают острые, подострые, хронические (прогрессирующие, рецидивирующие) миокардиты. По степени тяжести - легкий, миокардит средней тяжести, тяжелый.
По характеру воспаления выделяют экссудативно-пролиферативный (воспалительно-инфильтративный, васкулярный, дистрофический, смешанный) и альтернативный (дистрофически-некробиотический) миокардиты. В развитии инфекционного миокардита (как наиболее часто встречающегося) выделяют 4 патогенетические стадии:
- Инфекционно-токсическая
- Иммунологическая
- Дистрофическая
- Миокардиосклеротическая
По клиническим вариантам (по преобладающим клиническим симптомам) различают миокардиты:
- малосимптомный
- болевой или псевдокоронарный
- декомпенсационный (с нарушением кровообращения)
- аритмический
- тромбоэмболический
- псевдоклапанный
- смешанный
Симптомы миокардита
Клиническая симптоматика миокардита зависит от степени поражения миокарда, локализации, остроты и прогрессирования воспалительного процесса в сердечной мышце. Она включает проявления недостаточности сократительной функции миокарда и нарушения ритма сердца. Инфекционно-аллергический миокардит в отличие от ревматического начинается обычно на фоне инфекции или сразу после нее. Начало заболевания может протекать малосимптомно или латентно.
Основные жалобы пациентов - на сильную слабость и утомляемость, одышку при физической нагрузке, боли в области сердца (ноющие или приступообразные), нарушения ритма (сердцебиение, перебои), повышенную потливость, иногда боль в суставах. Температура тела обычно субфебрильная или нормальная. Характерными проявлениями миокардита являются увеличение размеров сердца, понижение артериального давления, недостаточность кровообращения.
Кожные покровы у больных миокардитом бледные, иногда с синюшным оттенком. Пульс учащенный (иногда уреженный), может быть аритмичным. При выраженной сердечной недостаточности наблюдается набухание шейных вен. Возникает нарушение внутрисердечной проводимости, которое даже при небольших очагах поражения может стать причиной аритмии и привести к летальному исходу. Нарушение сердечного ритма проявляется суправентрикулярной (наджелудочковой) экстрасистолией, реже приступами мерцательной аритмии, что заметно ухудшает гемодинамику, усиливает симптомы сердечной недостаточности.
В большинстве случаев в клинической картине миокардита преобладают лишь отдельные из перечисленных выше симптомов. Примерно у трети пациентов миокардит может протекать малосимптомно. При миокардитах, возникающих на фоне коллагеновых заболеваний, а также вирусной инфекции часто возникает сопутствующий перикардит. Идиопатический миокардит имеет тяжелое, иногда злокачественное течение, приводящее к кардиомегалии, тяжелым нарушениям ритма и проводимости сердца и сердечной недостаточности.
Осложнения
При длительно текущем миокардите развиваются склеротические поражения сердечной мышцы, возникает миокардитический кардиосклероз. В случае острого миокардита при тяжелых нарушениях работы сердца быстро прогрессирует сердечная недостаточность, аритмия, становящиеся причиной внезапной смерти.
Диагностика
Существенные трудности в диагностике миокардитов вызывает отсутствие специфических диагностических критериев. Мероприятия по выявлению воспалительного процесса в миокарде включают:
- Сбор анамнеза
- Физикальное обследование пациента - симптомы варьируют от умеренной тахикардии до декомпенсированной желудочковой недостаточности: отеки, набухание шейных вен, нарушение ритма сердца, застойный процесс в легких.
- ЭКГ - нарушение сердечного ритма, возбудимости и проводимости. ЭКГ-изменения при миокардите не являются специфичными, так как сходны с изменениями при различных заболеваниях сердца.
- ЭхоКГ - выявляется патология миокарда (расширение полостей сердца, снижение сократительной способности, нарушение диастолической функции) в разной степени в зависимости от тяжести заболевания.
- Общий, биохимический, иммунологический анализы крови не являются столь специфичными при миокардите и показывают увеличение содержания α2 и γ - глобулинов, повышение титра антител к сердечной мышце, положительную РТМЛ (реакцию торможения миграции лимфоцитов), положительную пробу на С-реактивный белок, повышение сиаловых кислот, активности кардиоспецифичных ферментов. Исследование иммунологических показателей должно проводиться в динамике.
- Рентгенография легких помогает обнаружить увеличение размеров сердца (кардиомегалию) и застойные процессы в легких.
- Бакпосев крови для выявления возбудителя, или ПЦР диагностика.
- Эндомиокардиальная биопсия при помощи зондирования полостей сердца, включающая гистологическое исследование биоптатов миокарда, подтверждает диагноз миокардита не более чем в 37% случаев в связи с тем, что может иметь место очаговое поражение миокарда. Результаты повторной биопсии миокарда дают возможность оценить динамику и исход воспалительного процесса.
- Сцинтиграфия (радиоизотопное исследование) миокарда является физиологичным исследованием (прослеживается естественная миграция лейкоцитов в очаг воспаления и нагноения).
- Магнитно-резонансная томография (МРТ сердца) с контрастированием дает визуализацию воспалительного процесса, отека в миокарде. Чувствительность данного метода составляет 70-75%.
Лечение миокардита
Острая стадия миокардита требует госпитализации в отделение кардиологии, ограничения физической активности, строгого постельного режима на 4 - 8 недель до достижения компенсации кровообращения и восстановления нормальных размеров сердца. Диета при миокардите предполагает ограниченное употребление поваренной соли и жидкости, обогащенное белковое и витаминизированное питание для нормализации метаболических процессов в миокарде.
Терапию миокардита проводят одновременно по четырем направлениям, осуществляя этиологическое, патогенетическое, метаболическое симптоматическое лечение. Этиологическое лечение направлено на подавление инфекционного процесса в организме. Терапию бактериальных инфекций проводят антибиотиками после выделения и определения чувствительности патогенного микроорганизма. При миокардитах вирусного генеза показано назначение противовирусных препаратов.
Необходимым условием успешного лечения миокардитов служит выявление и санация инфекционных очагов, поддерживающих патологический процесс: тонзиллита, отита, гайморита, периодонтита, аднексита, простатита и др. После осуществления санации очагов (хирургической или терапевтической), курса противовирусной или антибактериальной терапии необходимо проведение микробиологического контроля излеченности.
В патогенетическую терапию миокардитов включают противовоспалительные, антигистаминные и иммуносупрессивные препараты. Назначение нестероидных противовоспалительных средств осуществляется индивидуально, с подбором дозировок и длительности курса лечения; критерием отмены служит исчезновение лабораторных и клинических признаков воспаления в миокарде. При тяжелом, прогрессирующем течении миокардита назначаются глюкокортикоидные гормоны. Антигистаминные средства способствуют блокированию медиаторов воспаления.
Для улучшения метаболизма сердечной мышцы при миокардитах применяют препараты калия, инозин, витамины, АТФ, кокарбоксилазу. Симптоматическое лечение миокардитов направлено на устранение аритмий, артериальной гипертензии, симптомов сердечной недостаточности, профилактику тромбоэмболий. Длительность лечения миокардита определяется тяжестью заболевания и эффективностью комплексной терапии и составляет в среднем около полугода, а иногда и дольше.
Прогноз
При латентном малосимптомном течение миокардита возможно самопроизвольное клиническое излечение без отдаленных последствий. В более тяжелых случаях прогноз миокардитов определяется распространенностью поражения миокарда, особенностями воспалительного процесса и тяжестью фонового заболевания.
При развитии сердечной недостаточности у 50% пациентов отмечается улучшение по результатам лечения, у четверти наблюдается стабилизация сердечной деятельности, у оставшихся 25% состояние прогрессирующе ухудшается. Прогноз при миокардитах, осложненных сердечной недостаточностью, зависит от выраженности дисфункции левого желудочка.
Неудовлетворительный прогноз отмечается при некоторых формах миокардитов: гигантоклеточном (100%-ая смертность при консервативной терапии), дифтерийном (смертность составляет до 50–60%), миокардите, вызванном болезнью Шагаса (американским трипаносомозом) и др. У этих пациентов решается вопрос о трансплантации сердца, хотя и не исключается риск развития повторного миокардита и отторжения трансплантата.
Профилактика
Для снижения риска заболеваемости миокардитом рекомендуется соблюдать меры предосторожности при контакте с инфекционными больными, санировать очаги инфекции в организме, избегать укусов клещей, осуществлять вакцинацию против кори, краснухи, гриппа, свинки, полиомиелита.
Пациенты, перенесшие миокардит, проходят диспансерное наблюдение у кардиолога 1 раз в 3 месяца с постепенным восстановлением режима и активности.
Идиопатический миокардит Абрамова-Фидлера – тяжелое неспецифическое воспаление миокарда, протекающее с развитием кардиомегалии, сердечной недостаточности, выраженных нарушений ритма и проводимости, тромбоэмболического синдрома. Клинические проявления миокардита Абрамова-Фидлера включают одышку, утомляемость, цианоз, тахикардию, перебои в работе сердца, повышение температуры тела. Диагностика миокардита Абрамова-Фидлера проводится с учетом лабораторных данных, рентгенографии грудной клетки, эхокардиографии, электрокардиографии, коронарографии, сцинтиграфии, МРТ, биопсии миокарда. Лечение миокардита Абрамова-Фидлера – главным образом, симптоматическое (нитраты, диуретики, ингибиторы АПФ, бета-блокаторы, антикоагулянты); по показаниям – трансплантация сердца.
Общие сведения
Идиопатический миокардит Абрамова-Фидлера (миокардит злокачественный, изолированный, аллергический, межуточный) - миокардит с неясной этиологией, отличающийся глубокими диффузными воспалительными, дистрофическими и дегенеративными изменениями сердечной мышцы.
В кардиологии миокардит Абрамова-Фидлера расценивается как крайне тяжелая форма неревматического миокардита с высокой летальностью. Миокардитом Абрамова-Фидлера обычно заболевают молодые и относительно здоровые люди. Средний возраст больных идиопатическим миокардитом составляет 42 года; процентное соотношение лиц обоего пола среди заболевших примерно одинаковое. Заболевание впервые описано русским врачом С. С. Абрамовым в 1887 г.; выделено в отдельную нозологическую форму в 1897 г. немецким клиницистом К. Фидлером.

Причины идиопатического миокардита Абрамова-Фидлера
Гипотеза вирусного генеза миокардита Абрамова-Фидлера подтверждается статистическими данными: у пациентов, перенесших острый вирусный миокардит, хронический идиопатический миокардит возникает в 4-9% случаев против 0,005% в общей популяции. Существует точка зрения, что миокардит Абрамова-Фидлера представляет собой крайний вариант инфекционно-аллергического миокардита.
Примерно у 20% больных развитие миокардита Абрамова-Фидлера отмечается на фоне аутоиммунных заболеваний: болезни Такаясу, тиреоидита Хашимото, болезни Крона. За иммунопатологический механизм воспаления свидетельствует выявление антител к миокарду и клеточной цитотоксичности.
Типичными морфологическими признаками миокардита Абрамова-Фидлера являются: изолированное поражение сердца, сочетание обширных дистрофических, инфильтративно-воспалительных изменений миокарда с распространенным кардиосклерозом, внутрисердечным тромбообразованием и эмболией артерий большого круга кровообращения.
Макроскопически при миокардите Абрамова-Фидлера обнаруживается дряблость стенок и растяжение полостей сердца, наличие пристеночных тромбов; на разрезе - пестрота окраски миокарда. При микроскопическом изучении обращает внимание гипертрофия мышечных волокон (в большей степени - сосочковых мышц и субэндокардиальных слоев миокарда); обширные поля миолиза с замещением мышечной ткани соединительной; наличие признаков коронарита - воспалительных инфильтратов по ходу мелких ветвей коронарных сосудов.
Классификация идиопатического миокардита Абрамова-Фидлера
На основании гистологических признаков выделяют четыре варианта (типа) идиопатического миокардита: дистрофический, воспалительно-инфильтративный, смешанный и васкулярный. При дистрофическом (деструктивном) типе миокардита Абрамова-Фидлера преобладают процессы гидропической дистрофии мышечных волокон с их последующей тотальной гибелью и миолизом на пораженном участке.
Воспалительно-инфильтративный вариант идиопатического миокардита характеризуется отеком межуточной ткани и ее инфильтрацией различными клеточными элементами. В острой стадии в экссудате в большом количестве обнаруживаются полиморфноядерные нейтрофильные гранулоциты или эозинофильные лейкоциты. При длительном течении в составе инфильтрата преобладают плазматические или многоядерные гигантские клетки.
Смешанный тип миокардита Абрамова-Фидлера представляет сочетание дистрофического и воспалительно-инфильтративного вариантов. Васкулярный тип миокардита Абрамова-Фидлера протекает с преимущественным поражением мелких ветвей коронарных артерий.
По течению миокардит Абрамова-Фидлера может быть острым (2-8 недель), подострым (от 3 до 18 месяцев) и рецидивирующим хроническим (длится годами). Реже встречается латентная форма идиопатического миокардита, протекающая без четкой симптоматики. По клиническим признакам различают асистолическую, аритмическую, тромбоэмболическую, псевдокоронарную и смешанную формы миокардита Абрамова-Фидлера.
Симптомы идиопатического миокардита Абрамова-Фидлера
Миокардит Абрамова-Фидлера отличается тяжелым, нередко злокачественным течением. При острой форме быстро нарастают симптомы правожелудочковой или прогрессирующей тотальной сердечной недостаточности. Появляются одышка, ортопноэ, цианоз, тахикардия, артериальная гипотония, отеки, асцит, гепатомегалия и спленомегалия. Возможно развитие сердечной астмы и отека легких. Нередко возникают кардиальные боли, напоминающие стенокардию. В острой стадии отмечается повышение температуры тела до 38—39°С.
Иногда ведущим в клинике бывает тромбоэмболический синдром; в этом случае заболевание может манифестировать с ТЭЛА, тромбоэмболии церебральных, почечных, селезеночных сосудов. Молниеносное течение миокардита Абрамова-Фидлера всегда заканчивается летальным исходом.
При хронической форме миокардита Абрамова-Фидлера течение заболевания рецидивирующее; после каждого обострения неуклонно прогрессирует фиброз миокарда, кардиомегалия и необратимое нарушение кровообращения. Известны случаи латентного течения миокардита Абрамова-Фидлера, приводящего к внезапной смерти.
Диагностика идиопатического миокардита Абрамова-Фидлера
При физикальном обследовании отмечается частый, аритмичный, слабого наполнения пульс; перкуторное расширение границ сердца; аускультативные феномены (ритм галопа, систолический шум в проекции верхушки сердца), глухость сердечных тонов и пр. В легких выслушиваются мелкопузырчатые влажные хрипы, крепитация. Признаками тотальной сердечной недостаточности служат периферические отеки, увеличение и болезненность печени, асцит.
Биохимическое исследование крови при миокардите Абрамова-Фидлера обнаруживает повышение С-реактивного белка, содержания фибрина, серомукоида, гаптоглобина, a- и γ-глобулинов, активности креатинкиназы и тропонина T. Для исключения системных заболеваний проводится ревматологический скрининг (АСЛ-О, ревматоидный фактор, антитела к ds ДНК и антинуклеарные антитела).
Рентгенография органов грудной клетки выявляет значительное увеличение размеров сердца, признаки венозного застоя в легких. Эхокардиография позволяет исключить другие причины сердечной недостаточности (амилоидоз сердца, врожденные пороки сердца и пр.); обнаружить перикардиальный выпот, дилатацию полостей сердца, гипертрофию миокарда, внутриполостные тромбы; оценить подвижность и толщину стенок.
ЭКГ-изменения при миокардите Абрамова-Фидлера неспецифичны: могут обнаруживаться синусовая тахикардия, неполная блокада ножек пучка Гиса, атриовентрикулярная блокада, желудочковая аритмия, фибрилляция желудочков, реже мерцательная аритмия и экстрасистолия; в случае повреждения ткани миокарда - псевдоинфарктная картина, требующая проведения дифференциальной диагностики с ИБС и инфарктом миокарда.
Данные коронарографии при миокардите Абрамова-Фидлера свидетельствуют о коронарной ишемии, обусловленной сердечной дисфункцией. Для обнаружения воспаления сердечной мышцы высокоспецифичными и чувствительными методами являются антимиозиновая сцинтиграфия, гадолиниумно-улучшенная МРТ сердца.
Стандартной процедурой диагностики миокардитов различной этиологии служит биопсия миокарда, однако данный метод сопряжен с высокой частотой как ложноположительных, так и ложноотрицательных результатов.
Лечение идиопатического миокардита Абрамова-Фидлера
Этиотропная терапия миокардита Абрамова-Фидлера не разработана. Проводится симптоматическое лечение сердечной недостаточности, аритмий, профилактика тромбоэмболических осложнений. С этой целью назначаются постельный режим, диетотерапия, прием лекарственных препаратов (нитратов, сердечных гликозидов, диуретиков, ингибиторов АПФ, бета-блокаторов, антагонистов альдостероновых рецепторов, антикоагулянтов).
Противовоспалительная терапия включает назначение НПВС (индометацин, диклофенак); при тяжелых формах миокардита Абрамова-Фидлера с высокой активностью иммунных реакций применяются глюкокортикоиды; при аллергическом фоне - десенсибилизирующие средства. Дополнительно используются препараты метаболического действия (кокарбоксилаза, инозин, калия оротат, витамины). При гигантоклеточном миокардите показана трансплантация сердца.
Прогноз идиопатического миокардита Абрамова-Фидлера
Течение миокардита Абрамова-Фидлера в большинстве случаев неблагоприятно, смертность крайне высока. Острые формы заболевания могут заканчиваться летально в течение нескольких дней или недель, подострые - в течение нескольких месяцев. Смерть наступает от острой сердечной недостаточности, фибрилляции желудочков, реже - тромбоэмболических осложнений.
Хронические и латентные варианты течения идиопатического миокардита ведут к прогрессированию кардиомегалии и необратимого нарушения кровообращения. Специфическая профилактика миокардита Абрамова-Фидлера не разработана.
Что такое миокардиодистрофия? Причины возникновения, диагностику и методы лечения разберем в статье доктора Мадоян М. А., терапевта со стажем в 21 год.
Над статьей доктора Мадоян М. А. работали литературный редактор Маргарита Тихонова , научный редактор Сергей Федосов

Определение болезни. Причины заболевания
Миокардиодистрофия (МКД) — группа вторичных обратимых поражений мышечного слоя сердца (миокарда) невоспалительной и некоронарогенной природы, которые обусловлены нарушением обмена веществ в миокарде и проявляются нарушением его функций. [1] [3] [5]
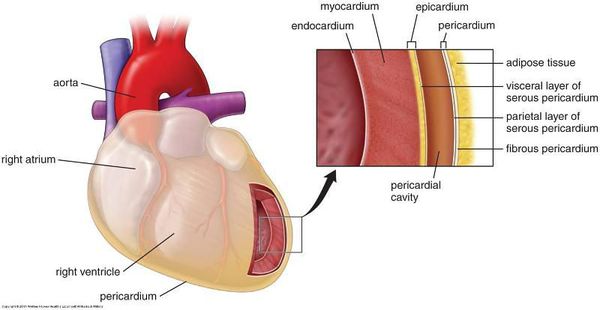
Общие признаки миокардиодистрофий:
- Нарушен обмен веществ в тканях сердца.
- Возникает вторично, то есть является следствием или осложнением других патологий.
- Первопричиной не может быть воспаление и поражение артерий сердца (они вызывают иные заболевания — миокардит, ишемическую болезнь сердца).
- Обратимость на начальных этапах (при устранении причин).
- Проявляются разнообразными неспецифическими нарушениями сердечной деятельности.
Заболевание поражает разные возрастные группы, но чаще встречается после 40 лет. [2] [3] [4] [6] [7]
К миокардиодистрофии могут приводить самые различные внутренние и внешние факторы, нарушающие обмен веществ и энергии в тканях сердца. [1] [3] [5] [6] [7]
Внутренние (эндогенные) факторы — патологические процессы в организме, осложнившиеся миокардиодистрофией. Эндогенные факторы можно разделить на две большие группы: сердечные и несердечные причины возникновения МКД.
К сердечным факторам относятся:
- пороки сердца;
- миокардиты;
- ишемическая болезнь сердца (далее — ИБС);
- изменения сердца вследствие гипертонической болезни;
- изменения сердца вследствие лёгочной гипертензии;
- болезни крови (анемии);
- болезни эндокринной системы и обмена веществ (сахарный диабет, ожирение, голодание, подагра, нарушение функций щитовидной железы, патологический климакс и другие) [2][6][7] ;
- болезни пищеварительной системы (тяжёлые поражения печени, поджелудочной железы или кишечника);
- болезни мышечной системы (миастения, миотония);
- эндогенные интоксикации (хроническая почечная недостаточность, хроническая печёночная недостаточность);
- инфекции (острые и хронические, бактериальные и вирусные).
Внешние (экзогенные) факторы — патологические воздействия на организм внешней среды и образа жизни:
- воздействие физических факторов (радиация, вибрация, экстремальные температуры) [7] ;
- воздействие химических факторов (хронические и острые отравления химическими элементами и соединениями, алкоголем, наркотиками, некоторыми лекарственными средствами);
- физическое и психоэмоциональное перенапряжение (хроническое и острое). [2][4]
При обнаружении схожих симптомов проконсультируйтесь у врача. Не занимайтесь самолечением - это опасно для вашего здоровья!
Симптомы миокардиодистрофии
Характеристика симптомов при миокардиодистрофии:
- неспецифичны — могут наблюдаться и при других заболеваниях;
- наслаиваются на симптомы заболевания (состояния), вызвавшего МКД;
- обратимы — могут полностью исчезнуть при своевременном устранении причины МКД;
- нарастают по мере развития МКД.
Виды симптомов при МКД:
- Боли в сердце. В отличие от болей при ИБС, не связаны с физической нагрузкой, не носят жгущий и давящий характер, отличаются большей длительностью, не купируются (не прерываются) нитратами. В отличие от болей при поражении плевры (оболочки лёгких), не связаны с актом дыхания и кашлем. В отличие от болей при поражении позвоночника, не связаны с движениями в корпусе. Но могут, как плевральные и позвоночные боли, купироваться обезболивающими и противовоспалительными средствами.
- Одышка — чувство нехватки воздуха. Как и при большинстве других заболеваний с одышкой, последняя обычно нарастает при нагрузке.
- Отёки. Как и при большинстве других заболеваний сердца, отёки чаще локализуются на нижних конечностях и нарастают к вечеру.
- Нарушения ритма сердца. Могут отмечаться приступы сердцебиений, неприятные чувства перебоев, остановки сердца, головокружения, редко — обмороки.
Патогенез миокардиодистрофии
В патогенезе миокардиодистрофии задействованы ткани сердца следующих видов:
- Мышечная ткань (сердечная мышца, миокард). Функция — нормально сокращаться (при этом из камер сердца кровь выбрасывается) и расслабляться (при этом камеры сердца заполняются следующей порцией крови).
- Нервная ткань (проводящая система сердца). Функция — генерировать нервные импульсы строго определённых характеристик (место возникновения, частота) и без задержек проводить их к миокарду. Именно нервный импульс заставляет сердечную мышцу сокращаться.
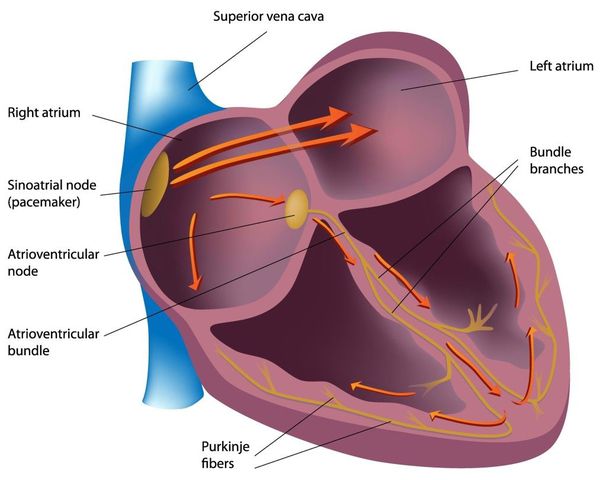
При нарушении обменных процессов (электролитного, белкового, энергетического) нарушаются и функции сердечных тканей [1] [2] [5] : мышечные клетки утрачивают способность к нормальным сокращениям, нервные — к генерированию и проведению нормальных импульсов.
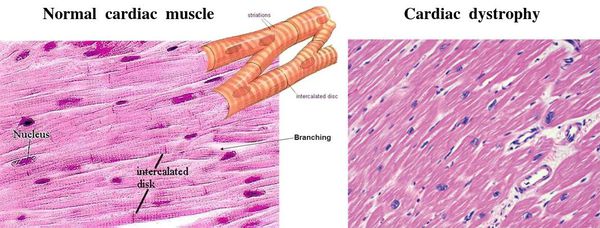
Причём поражается не сразу вся ткань сердца. Сначала возникают одиночные очаги дистрофии из нескольких клеток, а соседние неповреждённые клетки пытаются восполнить потерю и усиливают свою функцию. Затем количество и размер поражённых очагов увеличиваются, происходит их слияние, здоровые участки теряют способность компенсировать ухудшение работы, появляется расширение сердечных камер и выраженное нарушение функций сердца. [3]
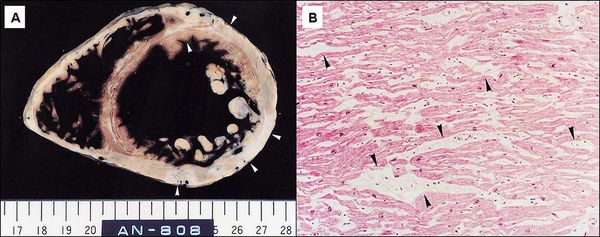
Далее при прекращении воздействия причинного фактора начинается медленное восстановление структуры и функции клеток. [7] При продолжающемся воздействии причинного фактора происходит гибель клеток и их замещение рубцовой (соединительной) тканью. Соединительная ткань не способна сокращаться и расслабляться, генерировать и проводить импульсы, заменяться здоровыми клетками. Процесс формирования соединительной ткани в сердце называется кардиосклероз, на этом этапе у болезни уже не может быть обратного развития. [3]
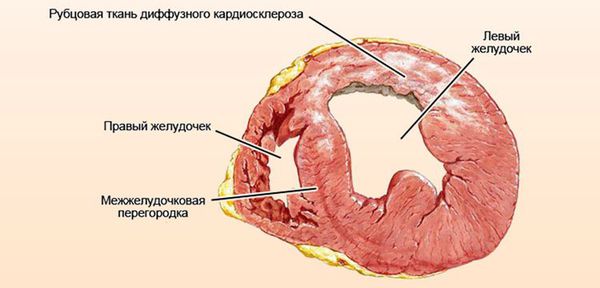
Классификация и стадии развития миокардиодистрофии
Миокардиодистрофии классифицируют по причинам возникновения, перечисленным выше, а также по скорости развития и стадиям заболевания. [1] [5]
По скорости развития миокардиодистрофий различают:
- острую форму (при массивном воздействии внешних и внутренних факторов: например, при тромбоэмболии лёгочной артерии, гипертоническом кризе, остром физическом перенапряжении);
- хроническую форму (при длительном воздействии умеренных по силе внешних и внутренних факторов: например, при хронической интоксикации, часто рецидивирующих острых инфекциях).
По стадиям миокардиодистрофий выделяют:
- I стадию — компенсации. Обратима. Формируются очаги дистрофии. Изменения на микроскопическом уровне. Симптомы отсутствуют или минимальны.
- II стадию — субкомпенсации. Обратима. Очаги дистрофии сливаются. Изменения на макроскопическом уровне, камеры сердца увеличиваются в размерах. Симптомы нарастают.
- III стадию — декомпенсации. Необратима. Некроз клеток с замещением их соединительной тканью — кардиосклероз. Прогрессирующее нарушение структуры сердца и нарастание симптомов.
Осложнения миокардиодистрофии
-
— утрата способности сердца обеспечивать организму требуемый кровоток. Проявляется нарастающими одышкой, сердцебиением, слабостью. [3] Симптомы сначала возникают при интенсивных нагрузках, затем при обычных, требуется всё больше времени для восстановления, появляются и усиливаются отёки. Затем одышка и сердцебиение появляются при любых движениях, потом и в покое, возникают приступы сердечной астмы, может развиться отёк лёгкого. Хорошо подобранное лечение способно надолго затормозить развитие событий по этому сценарию. Без лечения достаточно быстро наступает смерть от прогрессирующей сердечной недостаточности.
- Нарушения ритма и проводимости сердца — утрата способности проводящей системы сердца к генерации и проведению нормальных импульсов. Импульсы приобретают патологический характер (возникают не в тех местах, не с той частотой) или не могут достичь рабочего миокарда и вызвать его сокращение. Диапазон нарушений ритма и проводимости сердца чрезвычайно широк [2] : от незначительных (одиночная, редкая экстрасистолия (преждевременное сокращение сердца), некоторые виды блокад) до жизнеугрожающих (пароксизмальные нарушения ритма, мерцательная аритмия, тяжёлые блокады). Разными могут быть и проявления: от полного отсутствия симптомов до выраженных сердцебиений, болей в сердце, обмороков. Соответственно, предполагается разное лечение — от отсутствия необходимости специального лечения до экстренного хирургического.
Диагностика миокардиодистрофии
Задачи диагностического процесса:
- исключение других, более опасных и необратимых заболеваний сердца;
- выявление причин миокардиодистрофии;
- определение эффективности получаемого лечения.
В диагностике миокардиодистрофий большое значение имеет грамотный расспрос и внимательный осмотр пациента. Также проводят электрокардиографию, УЗИ сердца, рентгенологичесское исследование органов грудной клетки, лабораторные исследование крови и мочи. [3] Специфических изменений результатов данных исследований для миокардиодистрофий нет, но они позволяют выявить заболевания — причины миокардиодистрофий. ЭКГ и УЗИ сердца могут проводить повторно для оценки положительной динамики функций сердца на фоне проводимого лечения.
Лечение миокардиодистрофии
Задачи лечебного процесса:
- устранение причины миокардиодистрофии;
- восстановление (улучшение) обмена веществ в сердечных тканях;
- устранение (уменьшение) симптомов;
- профилактика и лечение осложнений.
Своевременность и полнота устранения причины миокардиодистрофии определяет эффективность терапии и её сроки. На этапе устранения причины лечебный процесс сильно разнится у больных с разными причинами заболевания: [1] [2] [5] [6] [7]
- женщин с патологическим климаксом лечат гинекологи при помощи гормональных препаратов;
- пациенты с хроническим тонзиллитом, осложнившимся миокардиодистрофией, нуждаются в оперативном удалении миндалин ЛОР-врачом;
- тиреотоксикоз, как причина миокардиодистрофии, лечится эндокринологом медикаментозно или удалением щитовидной железы или её части;
- анемия лечится гематологом или терапевтом, в зависимости от выраженности заболевания — стационарно или амбулаторно;
- для лечения алкогольной миокардиодистрофии необходимо исключить употребление алкоголя, поэтому здесь требуется помощь нарколога.
- голодание, будучи причиной МКД, может быть устранено при помощи психиатра, если у пациента анорексия, и посредством привлечения к проблеме социальных служб, если у пациента нет возможности обеспечить себе регулярное питание;
- тяжёлые психоэмоциональные реакции, вызвавшие миокардиодистрофию, лечатся психотерапевтом сеансами психотерапии или медикаментозно;
- физическое перенапряжение, вызвавшее миокардиодистрофию, должно быть срочно прекращено и не должно возобновляться, в таком случае вне спорта роль врача играет сам пациент, а в спорте — тренер под руководством врачей спортивной медицины. [2][4] И так далее.
Однако не всякую выявленную причину миокардиодистрофии можно устранить. Например, сами заболевания (длительные или хронические) и токсические препараты, применяемые для их лечения, лучевая терапия онкологических больных, некупируемые зависимости и другое.
Параллельно лечению основного заболевания, вызвавшего миокардиодистрофию (независимо от того, можно его устранить или нет), всех больных наблюдает кардиолог, по его назначению применяются виды лечения, направленные на улучшение обмена веществ в сердечных тканях, уменьшение симптомов и профилактику осложнений. [3]
Немедикаментозное лечение — нормализация образа жизни и питания, отказ от вредных привычек. Важно, чтобы пациент придерживался определённого режима дня, полноценно отдыхал и питался, обязательно имел регулярные, адекватные именно для него физические нагрузки, ежедневно находился на свежем воздухе. Также очень важно, чтобы в жизни пациента было увлекающее его дело. Немедикаментозное лечение — это зона ответственности пациента. Врач может порекомендовать, но реализовывать должен сам пациент.
Медикаментозное лечение:
- Улучшают обмен веществ в сердце препараты калия, витамины группы В, стимуляторы обменных процессов. Их обычно назначают курсами 3-4 раза в год.
- Уменьшают симптомы нарушений ритма препараты с антиаритмической активностью. Нарушения проводимости и ритма могут потребовать и хирургического лечения.
- Уменьшают симптомы хронической сердечной недостаточности и являются средством профилактики её развития такие препараты как ингибиторы ангиотензинпревращающего фермента, β-адреноблокаторы. [3]
Медикаментозное лечение — это зона ответственности врача. Ни в коем случае не надо пытаться лечиться самостоятельно. Каждый медикаментозный препарат (витамины и стимуляторы обменных процессов в том числе) может при определённых условиях нанести вред.
Прогноз. Профилактика
При I и II стадиях прогноз благоприятный. После устранения причинного фактора функции сердца могут полностью восстановиться. Длительность периода восстановления зависит от времени начала лечения (чем быстрее начата адекватная терапия, тем быстрее регрессируют патологические изменения) и от общего состояния организма (молодой возраст, отсутствие сопутствующих заболеваний способствуют быстрейшему восстановлению) и может составлять от года до многих лет. [7]
При III стадии прогноз зависит от выраженности изменений и наличия осложнений. Так как изменения в сердце уже необратимы, речь идёт не о восстановлении нормальных параметров сердца и хорошего самочувствия, а о замедлении прогрессирования хронической сердечной недостаточности и нарушений ритма. При III стадии необходимо пожизненное лечение, профессиональная деятельность ограничена либо невозможна, а при отсутствии лечения неблагоприятным становится и прогноз жизни.
Читайте также:

