Инфекционный энтероколит у новорожденного
Обновлено: 26.04.2024
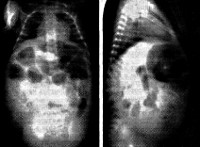
Язвенно-некротический энтероколит – это воспалительное заболевание кишечника у новорожденных, для которого характерен некроз стенки кишки и развитие сопутствующей симптоматики. Проявляется признаками кишечной непроходимости и перитонита, интоксикацией вплоть до септического состояния, а также развитием ДВС-синдрома. Течение циклическое, возможно повторное появление симптомов. Диагностика клиническая и рентгенологическая, также проводится комплекс лабораторных исследований. Лечение патогенетическое и симптоматическое, направлено на устранение кишечной непроходимости, коррекцию электролитных нарушений, ДВС-синдрома и других проявлений. При необходимости осуществляются хирургические вмешательства.
МКБ-10
Общие сведения
Язвенно-некротический энтероколит является одним из самых опасных заболеваний периода новорожденности. Другое его название – некротизирующий энтероколит (НЭК). Общая распространенность составляет 2,4 случая на 1000 новорожденных. Развивается у детей на первой неделе жизни, с одинаковой частотой поражает девочек и мальчиков.
Язвенно-некротический энтероколит вносит весомый вклад в структуру общей неонатальной смертности. Несмотря на современные методы диагностики и лечения, летальность составляет 10-40%, при этом она коррелирует со сроком гестации, достигая максимальных значений в группе глубоко недоношенных детей. Кроме того, существует риск послеоперационных осложнений даже в случае успешной терапии. В частности, язвенно-некротический энтероколит является одной из основных причин развития синдрома короткой кишки.

Причины
Этиология заболевания в настоящее время продолжает изучаться специалистами в сфере педиатрии. Определенную роль играет генетический аспект, то есть частота язвенно-некротического энтероколита среди родственников достоверно выше. Повышает риск развития заболевания искусственное вскармливание смесями с высокой осмолярностью. Доказана связь патологии с патогенными микроорганизмами, однако данные о конкретном возбудителе отсутствуют. Часто при заболевании обнаруживаются кишечная палочка, клебсиелла, стафилококк и клостридии. Условно-патогенная микрофлора также может способствовать развитию симптоматики язвенно-некротического энтероколита. Микроорганизмы не только напрямую повреждают ворсинки кишечного эпителия, но и повышают его проницаемость.
Патогенез
В патогенезе заболевания большое значение придается снижению барьерной функции кишечника. Отчасти это связано с высокой концентрацией патогенной микрофлоры, также играет роль срок беременности на момент рождения малыша. Язвенно-некротический энтероколит в большинстве случаев развивается у недоношенных детей. Кроме того, любое гипоксическое повреждение вызывает перераспределение крови в организме ребенка с преимущественным кровенаполнением жизненно важных органов. Ишемия кишечника приводит к некрозу его стенки, что также является одним из основных звеньев патогенеза. Что касается гипоксии, то ее причинами могут быть внутриутробная инфекция, патологии плаценты и пуповины, пороки развития сердечно-сосудистой системы и т. д.
Симптомы
Язвенно-некротический энтероколит развивается стадийно. Сначала появляются симптомы непереваривания пищи в виде срыгивания и визуального увеличения живота из-за перерастяжения желудка и кишечника. Возможна рвота с примесью желчи, дыхательные расстройства, в том числе приступы апноэ. Ребенок становится вялым, температура может незначительно повышаться. Далее присоединяются симптомы кишечной непроходимости. Рвота учащается, в кале появляется примесь алой крови. Живот значительно вздут, температура повышена. Приступы апноэ также учащаются, сатурация (насыщение крови кислородом) существенно снижается.
При отсутствии лечения или стремительном течении язвенно-некротический энтероколит проявляется симптомами перитонита, поскольку происходит перфорация кишечника, которая обычно обнаруживается в терминальном отделе подвздошной кишки. Выявляется пневмоперитонеум и признаки сепсиса в виде интоксикации, критического падения артериального давления и др. Воспалительная реакция при язвенно-некротическом энтероколите носит системный характер, поэтому наблюдаются признаки полиорганной недостаточности. Для заболевания характерно циклическое течение, то есть после нормализации состояния возможны повторные приступы.
Диагностика
Первые признаки заболевания неспецифичны и характерны для многих нозологий, в частности, болезни Гиршпрунга и других аномалий развития кишечника. Кроме того, сама по себе недоношенность часто проявляется трудностями с энтеральным питанием вследствие недоразвития секреторной и моторной функции отделов ЖКТ. Заподозрить язвенно-некротический энтероколит на начальных стадиях педиатр может в случае, если ребенок родился недоношенным, либо на этапе внутриутробного развития или в родах имела место гипоксия.
Также проводится анализ кала на скрытую кровь, поскольку визуально прожилки алой крови еще не обнаруживаются, но клеточные элементы уже присутствуют из-за микроповреждений стенки кишечника. После развития признаков кишечной непроходимости диагноз становится более очевидным:
- На рентгенограмме органов брюшной полости заметны расширенные петли кишечника и пневматоз кишечной стенки. Рентгенография подтверждает развитие перитонита, заподозрить который можно по сильному вздутию живота при отсутствии газонаполнения кишечных петель.
- В кале обнаруживается кровь, хотя стул может отсутствовать вследствие пареза кишечника и непроходимости.
- При УЗИ органов брюшной полости можно выявить газ или жидкость в брюшной полости, обнаружить эхогенные точки (участки некроза кишечной стенки). Этот признак является одним из первых, позволяющих диагностировать язвенно-некротический энтероколит на ранних стадиях.
- Общий анализ крови выявляет признаки воспаления в виде лейкоцитоза со сдвигом влево. Значительно повышается уровень C-реактивного белка, именно этот показатель обычно отслеживается в динамике с целью контроля эффективности лечения. Для язвенно-некротического энтероколита характерны тяжелые электролитные нарушения в виде гипонатриемии и метаболического ацидоза, а также нарушения процессов свертываемости крови вплоть до ДВС-синдрома. Часто выявляется конкретный инфекционный агент, который далеко не всегда играет ключевую роль в развитии клиники заболевания, но служит важным моментом для выбора терапевтической тактики.
Лечение язвенно-некротического энтероколита
Консервативная терапия
Терапия заболевания должна начинаться на этапе первых подозрений на язвенно-некротический энтероколит. Сразу отменяется энтеральное питание, проводится декомпрессия желудка и кишечника. Возможно превентивное назначение антибиотиков широкого спектра действия. Ребенку необходима респираторная поддержка. Требуется кувезный режим в отделении интенсивной терапии, ИВЛ проводится по показаниям. Посиндромное лечение язвенно-некротического энтероколита заключается в коррекции электролитных нарушений и эксикоза, который неизбежен при кишечной непроходимости. Необходима профилактика ДВС-синдрома. В большинстве случаев своевременно начатая терапия позволяет ограничиться консервативными методами.
Хирургическое лечение
Оперативное лечение язвенно-некротического энтероколита показано в случае обнаружения клинических и рентгенологических признаков перитонита в результате перфорации кишечной стенки. Некротизированный участок кишечника необходимо удалить. Также операция показана при неэффективности проводимых терапевтических мероприятий, то есть при сохранении клинических симптомов, появлении признаков шока, отсутствии положительной динамики в анализах крови. Вопрос о времени возвращения к энтеральному питанию решается индивидуально.
Прогноз и профилактика
Энтероколит у детей — это сочетанное воспаление тонкого и толстого кишечника. Возникает при инфицировании патогенными бактериями, вирусами или простейшими, под действием аллергических, механических или токсических провоцирующих факторов. Заболевание проявляется разнообразными болями в животе, запорами или диареей, интоксикационным синдромом. План диагностики включает ультразвуковые, эндоскопические и рентгенологические методы, серологические и бактериологические анализы. Лечение энтероколита у детей состоит из диетотерапии, фармакотерапии (энтеросорбенты, пробиотики, антибиотики и антипротозойные препараты).
МКБ-10

Общие сведения
Энтероколит — синдром, который встречается при разных инфекционных и неинфекционных заболеваниях ЖКТ. Это самый распространенный тип поражения желудочно-кишечного тракта у детей, но его точную частоту установить затруднительно в связи с большим разнообразием клинических диагнозов, протекающих с кишечным воспалением. В самостоятельную нозологическую единицу выделяют некротический энтероколит новорожденных, определяемый у 5% младенцев, которые поступают в отделение интенсивной терапии.

Причины
Этиологические факторы энтероколита подразделяют на инфекционные и неинфекционные. В педиатрической практике чаще диагностируется первый вариант, поскольку кишечные инфекции — вторая по частоте после ОРВИ группа заболеваний детского возраста. Кишечное воспаление вызывают бактериальные (сальмонелла, эшерихия, иерсиния и шигелла), вирусные (ротавирус, норовирус) и паразитарные инвазии (амебиаз, балантидиаз, лямблиоз).
Инфекционные причины энтероколита более характерны для пациентов раннего возраста и дошкольников. Исключение составляет псевдомембранозный колит, который обусловлен размножением условно-патогенных клостридий на фоне приема антибиотиков и выявляется у детей любого возраста. Помимо инфекционных агентов, развитие энтероколита провоцируют:
Патогенез
Механизм развития заболевания основан на повреждении слизистой с последующим распространением патологического процесса на все слои кишечной стенки. Как следствие нарушаются функции ЖКТ: полостное и пристеночное пищеварение, всасывание питательных веществ, секреция воды и солей в просвет кишки. Воспаление сопровождается изменением перистальтики в сторону ускорения или замедления, снижением местного иммунного ответа и нарушением микрофлоры.
Симптомы энтероколита у детей
Клиническая картина энтероколита у детей во многом определяется его причинами, степенью повреждения кишечника. Основные симптомы — нарушения стула, боли в полости живота. Для острого течения типичны спазмы и рези, которые не имеют четкой локализации. Появление болезненности в левой подвздошной области и тенезмов указывает на поражение дистальных отделов ЖКТ. При хроническом варианте беспокоят дискомфорт, тяжесть и покалывание в животе.
Расстройства стула при энтероколитах имеют различный характер: запоры, диарея, чередование этих двух форм либо фракционированная дефекация. При остром процессе, чаще инфекционной этиологии, у детей отмечается учащение стула до 10-20 раз в сутки. Испражнения жидкие, с обильными примесями слизи, иногда в кале есть кровь или гной. Симптомы дополняются тошнотой и рвотой. При хроническом заболевании 2-5-дневные запоры сменяются несколькими днями диареи и т. д.
Общие симптомы энтероколита у детей включают повышенную утомляемость, слабость и сонливость, отказ от еды. Кишечные инфекции проявляются признаками общей интоксикации: лихорадкой, головными болями, ломотой в теле. Если ребенку не проводится лечение хронической патологии, прогрессирующе ухудшается пищеварительная функция, из-за чего у ребенка появляются симптомы нутритивной недостаточности и гиповитаминоза.
Осложнения
При остром энтероколите диарея сопровождается обезвоживанием, которое особенно опасно для детей до 5 лет. Развитие эксикоза тяжелой степени проявляется спутанностью сознания, нарушениями гемодинамики, снижением тургора кожи. Тяжелые формы кишечных инфекций, помимо дегидратации, могут осложняться панкреатитом (13%), гепатитом (11%), поражением чашечно-лоханочной системы почек (9%).
Воспалительный процесс, распространяющийся за пределы слизистого слоя кишки, приводит к изъязвлениям, перфорации и пенетрации стенки. При ускоренной перистальтике возможны острые хирургические состояния: завороты кишечника, инвагинации, которые чаще встречаются в раннем возрасте. Прием некоторых лекарств или попадание токсинов может способствовать формированию мегаколона.
Диагностика
Обнаруженные симптомы энтероколита — основание для постановки педиатром синдромального (топического) диагноза. Дальнейшее обследование с привлечением детского гастроэнтеролога, инфекциониста, иммунолога-аллерголога необходимо для установления причин патологического состояния и постановки клинического диагноза. Ребенку обычно назначаются:
- УЗИ брюшной полости. Ультразвуковая диагностика — простой и неинвазивный метод, который выявляет сонографические симптомы воспаления, структурные и функциональные нарушения ЖКТ. Исследование проводится в качестве скрининга для исключения острых хирургических патологий.
- Рентгенография брюшной полости. Обзорная рентгенограмма информативна в диагностике кишечной непроходимости, инородных тел. Для детальной визуализации структуры слизистой оболочки ЖКТ и оценки моторной функции необходимы рентгенологический снимок с пероральным контрастированием, ирригография.
- Эндоскопические исследования. В практической детской гастроэнтерологии колоноскопию используют при подозрении на кишечный полипоз, неспецифический язвенный колит или болезнь Крона. Современный и безболезненный способ визуализации ЖКТ — видеокапсульная эндоскопия, которая без введения зонда показывает состояние толстой и тонкой кишки на всем их протяжении.
- Анализы кала. В копрограмме при энтероколитах определяются непереваренная клетчатка, капли нейтрального жира, исчерченные мышечные волокна. На симптомы воспаления указывают лейкоциты и слизь. Для подтверждения инфекционного характера болезни делают бактериологическое исследование испражнений.
- Серологические реакции. При возможном вирусном происхождении энтероколита и для ускоренного выявления бактериальной инфекции применяют РПГА крови со специфическими диагностикумами. Положительный результат устанавливают при нарастании титров антител в 4 и более раз. Для обнаружения ДНК патогенных микроорганизмов рекомендована ПЦР.
Лечение энтероколита у детей
Диетотерапия
Лечение энтероколита начинается с соответствующей диетотерапии. При остром течении назначается лечебное голодание, слизистые каши и супы, а по мере устранения симптоматики рацион расширяют. Хроническая патология требует щадящей диеты с ограничением экстрактивных веществ, грубой и волокнистой пищи, жирных и высокоуглеводных блюд. Для младенцев до 1 года оставляют привычное грудное вскармливание или питание искусственными смесями.
Консервативная терапия
Если энтероколиту сопутствуют диарея и обезвоживание, необходима адекватная регидратация. При эксикозе легкой степени ребенку дают жидкость через рот каждые 10-15 минут в объеме, который рассчитывается с учетом массы тела. Средняя и тяжелая степень дегидратации, когда пациент отказывается пить самостоятельно, требует внутривенных вливаний солевых растворов. Лекарственное лечение энтероколита подбирается в соответствии с причинами болезни и включает:
- Антибактериальные препараты. Используются кишечные антисептики, сульфаниламиды или противопротозойные лекарства. Они подбираются после получения результатов бактериологического исследования и установления возбудителя. Легкие формы инфекционных энтероколитов не требуют назначения антибиотиков.
- Средства для нормализации стула. Хронические запоры являются показанием к введению слабительных свечей или приему системных препаратов, которые размягчают каловые массы, улучшают моторику и облегчают дефекацию. Если медикаментозное лечение неэффективно, ставят клизмы. При жидком стуле рекомендованы противодиарейные лекарства.
- Энтеросорбенты. Лекарства выполняют несколько задач: связывают и выводят из организма токсины и бактерии, ликвидируют газообразование и кишечные колики, уменьшают интенсивность диареи. Они применяются независимо от этиологических факторов, когда обнаружены первые диспепсические симптомы.
- Пробиотики. Дисбактериоз может быть причиной или следствием энтероколита, но в любом случае он подлежит медикаментозной коррекции. Лечение включает препараты бифидо- и лактобактерий, которые дополняют пребиотиками для быстрого восстановления кишечной микрофлоры.
- Ферменты. При хроническом энтероколите назначаются панкреатические энзимы, которые улучшают процессы пищеварения в тонкой кишке, нормализуют частоту стула и консистенцию каловых масс. При сопутствующей билиарной патологии эффективны холеретики и холекинетики, минеральные воды.
Хирургическое лечение
Помощь детских хирургов требуется при энтероколите, осложненном перфорацией кишки, перитонитом, кровотечением. Оперативное вмешательство предполагает иссечение дефекта кишечной стенки или удаление части кишки при ее тотальном повреждении, санацию и дренирование брюшной полости, окончательную остановку кровотечения. Объем и метод операции подбирается индивидуально соответственно характеру и тяжести состояния.
Прогноз и профилактика
Адекватное лечение быстро купирует вовремя диагностированный острый инфекционный энтероколит, поэтому он проходит за несколько недель и не оставляет негативных последствий. Хроническое воспаление кишечника чаще встречается у детей, страдающих врожденными аномалиями или сопутствующей патологией. Прогноз зависит от тяжести основного заболевания, степени белково-энергетической недостаточности. При комплексной терапии удается достичь стойкой ремиссии.
Превентивные мероприятия включают привитие ребенку правил личной гигиены и гигиены питания, сбалансированный рацион без вредных продуктов и фастфуда. Недопустимо применение лекарственных средств без назначения и контроля педиатра. Меры вторичной профилактики: своевременное лечение кишечных инфекций и острых состояний, чтобы они не перешли в хроническую форму.
1. Гиршпрунг-ассоциированый энтероколит у детей/ Д.А. Морозов, Е.С. Пименова, Г.А. Королев// Вопросы практической педиатрии. – 2019.
2. Рациональная профилактика осложнений острых кишечных инфекций в практике педиатра/ Т.А. Руженцова, Н.А. Мешкова// Лечащий врач. – 2019.
4. Этиопатогенетическая терапия острых кишечных инфекций у детей на современном этапе/ А.А. Новокшонов, В.Ф. Учайкин, Н.В. Соколова // Лечащий врач. – 2010.
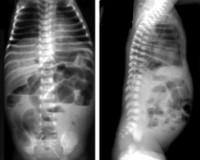
Некротический энтероколит новорожденных (НЭК) – это неспецифическое заболевание воспалительного характера, которое вызывается инфекционными агентами на фоне повреждения слизистой оболочки кишечника или ее функциональной незрелости. Симптомы включают соматические реакции и абдоминальные проявления. При длительном течении наблюдаются признаки перфорации кишечника и клиника перитонита. Диагностика НЭК сводится к физикальному обследованию, оценке симптомов по шкале Walsh и Kliegman и рентгенографии. Лечение зависит от стадии заболевания, может быть как консервативным, так и хирургическим.
Общие сведения

Причины НЭК новорожденных
Некротический энтероколит новорожденных – полиэтиологическое заболевание. Основными патогенетическими факторами являются гипоксия и ишемия в перинатальном периоде, нерациональное питание новорожденного и заселение кишечника аномальными микроорганизмами. К способствующим факторам относятся преждевременные роды, эклампсия, травмы ЦНС при родах, иммунодефицитные состояния у ребенка, аномалии развития кишечника, отягощенный семейный анамнез.
Классификация НЭК новорожденных
По скорости развития выделяют следующие формы некротического энтероколита новорожденных:
В зависимости от массивности поражения различают следующие варианты НЭК:
- Локальный. Патологические изменения наблюдаются на ограниченном отрезке кишечника.
- Полисегментарный. Характерно поражение сразу нескольких участков.
- Паннекроз или тотальный. В патологический процесс втягивается весь кишечник.
Симптомы и осложнения НЭК новорожденных
Некротический энтероколит новорожденных может возникать в первые 24 часа после родов (ранняя форма) или после 1 месяца жизни (поздняя форма), средний возраст детей на момент появления симптомов – 1-2 недели. Все проявления данной патологии можно разделить на 3 группы: соматические, абдоминальные, генерализованные. Первыми, как правило, появляются абдоминальные симптомы, которые почти сразу дополняются соматическими. Генерализованные проявления НЭК отмечаются при прогрессировании заболевания и возникновении перфорации кишечника, что, в зависимости от формы, может происходить через 1-3 дня.
Диагностика НЭК новорожденных
Диагностика некротического энтероколита новорожденных включает в себя сбор анамнеза, клиническое, лабораторное и инструментальное обследование. Анамнестические данные могут помочь педиатру и детскому хирургу установить возможную этиологию, проследить за динамикой заболевания. При объективном осмотре выявляются присутствующие на данный момент клинические симптомы – абдоминальные, соматические и генерализованные проявления. Специфических лабораторных тестов для подтверждения НЭК не существует. Информативными являются следующие данные, полученные при проведении лабораторных исследований: лейкоцитоз со сдвигом формулы влево, лейкопения и тромбоцитопения в ОАК, ацидоз и гипоксемия при определении газового состава крови, гиперкалиемия и гипонатриемия в электролитном спектре, диспротеинемия и выявления С-реактивного протеина в белковом спектре, обнаружение крови в кале при пробе Грегерсена. С целью выявления инфекционного возбудителя проводится бактериальный посев, ИФА и ПЦР.
Дифференциальная диагностика некротического энтероколита новорожденных проводится с такими патологиями как неонатальный сепсис, пневмония, пневмоперитонеум, кишечная непроходимость различного генеза, аппендицит новорожденного, бактериальный перитонит и спонтанная перфорация кишечника.
Лечение НЭК новорожденных
Тактика лечения некротического энтероколита новорожденных зависит от тяжести состояния ребенка и стадии заболевания. Детям с 1а, 1б и 2а стадиями показана консервативная терапия. С момента постановки диагноза отменяется энтеральное питание и проводится постановка назо- или орогастрального зонда с целью декомпрессии. Ребенок переводится на полное парентеральное питание (TPN) в соответствии с клиническими протоколами. Параллельно назначаются антибактериальные препараты из групп пенициллинов (ампициллин) и аминогликозидов II поколения (гентамицин) в комбинации с медикаментами, действующими на анаэробную микрофлору (метронидазол). При неэффективности выбранной антибиотикотерапии применяют цефалоспорины III-IV поколения (цефтриаксон) в сочетании с аминогликозидами III поколения (амикацин). Таким детям рекомендованы пробиотики и эубиотики для нормализации кишечной микрофлоры. Также проводят СВЧ-терапию, вводят иммуномодуляторы и гамма-глобулины.
Прогноз и профилактика НЭК новорожденных
Исход НЭК зависит от тяжести общего состояния ребенка и стадии заболевания. Так как данные показатели почти всегда отличаются нестабильностью, прогноз считается сомнительным даже на фоне полноценного лечения. Профилактика некротического энтероколита новорожденных включает в себя антенатальную охрану здоровья плода, рациональное ведение беременности, грудное вскармливание в физиологических объемах. Согласно некоторым исследованиям, риск развития заболевания снижается при использовании эубиотиков, пробиотиков и IgA у детей из группы риска. При высоком риске преждевременных родов применяют глюкокортикостероиды с целью профилактики РДС.
Язвенно-некротический энтероколит или некротический энтероколит – неспецифическое воспалительное заболевание, вызываемое инфекционными агентами на фоне незрелости механизмов местной защиты и/или гипоксически-ишемического повреждения слизистой кишечника, склонное к генерализации с развитием системной воспалительной реакции [2,4,10,12].
Некротический энтероколит – тяжелое заболевание периода новорождённости, чаще встречается у недоношенных новорожденных.
Классификация
Клинико - рентгенологическая классификация (Bell M.J. et al., 1978) в модификации (Walsh MC , Kliegman RM,1986) [1,10]

Диагностика
II.МЕТОДЫ, ПОДХОДЫ И ПРОЦЕДУРЫ ДИАГНОСТИКИ И ЛЕЧЕНИЯ
Основные (обязательные) диагностические обследования, проводимые на амбулаторном уровне: не проводятся.
Минимальный перечень обследования, который необходимо провести при направлении на плановую госпитализацию: не проводится.
Основные (обязательные) диагностические обследования, проводимые на стационарном уровне (при экстренной госпитализации проводятся диагностические обследования, не проведенные на амбулаторном уровне):
• Биохимический анализ крови (СРБ, глюкоза, общий белок, альбумины, триглецириды, билирубин, креатинин, мочевина);
• Обзорная рентгенография органов брюшной полости в первый день каждые 6-8 часов, в последующие – по показаниям;
Дополнительные диагностические обследования, проводимые на стационарном уровне (при экстренной госпитализации проводятся диагностические обследования, не проведенные на амбулаторном уровне):
Диагностические мероприятия, проводимые на этапе скорой неотложной помощи: не проводятся.
Жалобы: вялое сосание, частые срыгивания с примесью желчи, нестабильная температура, вздутие живота, слизистый стул без видимых примесей или с примесью крови.
• ІА стадия: мраморность кожных покровов, склонность к брадикардии, единичные приступы апноэ, срыгивания, незначительное вздутие живота, слизистый стул без примесей крови (определяется по анализу кала на скрытую кровь);
• ІБ стадия: эпизоды брадикардии, единичные приступы апноэ, рвота желчью, потеря массы тела, лабильное АД, вздутие живота, стул урежается, слизистый с примесью крови (определяется визуально);
• ІІА стадия: прогрессирующе нарастают симптомы интоксикации, частые апное, брадикардия, мышечная гипотония, живот вздут, слабо слышна перистальтика, стул малыми порциями, кровянисто-слизистый;
• ІІБ стадия: общее состояние ребенка тяжелое, частые апное, брадикардия, растянутая брюшная стенка, при пальпации диффузная болезненность живота, гепатоспленомегалия, стул кровянисто-слизистый, задержка стула;
• ІІ Б-ІІІ стадия: гипоальбуминемия, гипербилирубинемия, С-реактивный белок>10мг/л, повышение мочевины, остаточного азота, повышение прокальцитонина >2 нг/мл является маркером сепсиса ;
• ІІІстадии: рН
• ІІА стадия: нарастает дилатация петель кишечника, увеличение толщины кишечной стенки за счет отека и воспаления, наличие множественных разнокалиберных уровней в кишечных петлях;
• ІІБ стадия: дилатация петель кишечника, утолщение кишечной стенки, увеличение печени и селезенки, газ в системе портальной вены, появление признаков асцита;
• ІІІА стадия: субсерозный пневматоз кишечной стенки с ее утолщением, фиксированные петли кишечника, газ в системе портальной вены, выраженный асцит;
• І стадия: гепатомегалия, деформация желчного пузыря, утолщение его стенок с перифокальным отеком, застойная желчь, метеоризм, вялая перистальтика кишечника;
• ІІ стадия: снижение перистальтики в пораженных сегментах, неравномерная, умеренная дилатация петель кишечника, возможно минимальное количество жидкостного компонента между кишечными петлями по типу реактивного выпота;
• Осмотр неонатального хирурга 2 раза в сутки для своевременного определения показаний к переводу в детское хирургическое отделение;
• Осмотр невропатолога при наличии пороков развития ЦНС, двигательных нарушений, судорог, сопорозного состояния;
Дифференциальный диагноз
Дифференциальный диагноз [9]


Лечение
• ППП: продолжительность зависит от динамики состояния ребенка, восстановления пассажа по кишечнику, появления стойкой тенденции к улучшению или нормализации лабораторных и рентгенологических данных.
Расчет общих энергетических потребностей при ППП проводится с учетом физиологической потребности жидкости (в соответствии с таблицей 1).
Таблица 1 Ориентировочные потребности в жидкости у новорожденных (мл/кг/сутки) [15].

Расчет потребности белков, жиров и углеводов:
• введение аминокислот проводится из расчета 1-3 г/кг/сутки, сохраняется на этом уровне в течение всего периода ППП. Обеспечивается мониторинг уровня креатинина, мочевины, общего белка, альбумина в крови 1 раз в 3 дня, креатинина, мочевины в моче 1 раз в 3-5 дней;
• введение жировых эмульсий из расчета 1-3г/кг/сутки. Скорость введения липидов в течение 20 часов в сутки, не смешивая с другими препаратами. Проводится мониторинг уровня АЛТ, АСТ, билирубина, триглицеридов (1 раз в 3 дня), который не должен превышать 3-3,5 ммоль/л (N - 1,7 ммоль/л).
• введение углеводов: растворы глюкозы из расчета 6 мл/кг/мин, постепенно увеличивая до 10-12мл /кг/мин. к 6 дню. Мониторинг уровня глюкозы крови проводится ежедневно, в случае повышения уровня сахара снижается концентрация раствора.
• На 72 часа назначается стартовая антибактериальная терапия в комбинации полусинтетического пенициллина + аминогликозида (гентамицин вводится при весе ребенка <1000г с интервалом 48 часов, при весе>1000г - 36 часов);
• Через 72 часа после получения результатов бактериологического обследования крови производится смена антибактериальной терапии с учетом спектра чувствительности возбудителя;
• При отсутствии клинического улучшения и ухудшении лабораторных показателей назначается комбинация антибиотиков широкого спектра действия цефалоспорин II поколения +гликопептид, общим курсом 7-10 дней ;
• При ухудшении рентгенологической картины и лабораторных показателей к комбинации цефалоспорин+гликопептид дополнительно назначается нитроимидазол. Курс 10-14 дней.

Таблица 2. Средние дозы антибактериальных препаратов у новорожденных [5,11].
• Для профилактики грибкового поражения кишечника рекомендуется назначение флуконазола, начиная с 3-го дня жизни в дозе 3 мг/кг внутривенно капельно два раза в неделю в течение 7-10 дней;
• изменении газов крови: гипоксемия (pO2< 50мм.рт.ст.), гиперкарбия (pCO2>50мм.рт.ст.), респираторный или смешанный ацидоз;
• при снижении уровня электролитов в сыворотке крови внутривенно вводится натрий 1-2 мэкв/кг/сутки, калий 1-3 ммоль /кг/сутки, кальций 2 ммоль/кг/сутки;
• при артериальной гипотензии проводится инотропная терапия: допамин 2-5 мкг/кг/мин. до стабилизации АД;
• в течение суток проводится постоянный мониторинг АД, ЧСС, ЧД, сатурации крови, диуреза, массы тела, желудочного содержимого, стула.
• при коагулопатии, связанной с дефицитом витамина К1: введение витамина К1 внутримышечно недоношенным детям в дозе 0,5 мг, доношенным - 1 мг.
- в виде капельной инфузии вводится насыщающая доза 100-150 мкг/кг в течение 1 часа с последующим введением поддерживающей дозы 10-20 мкг/кг в час.

Таблица 3. Адаптированная шкала оценки боли у новорождённого N-PASS (Neonatal Pain, Agitation and Sedation Scale, 2000) [16].
Перечень дополнительных лекарственных средств (менее 100% вероятности применения): нет.
Медикаментозное лечение, оказываемое на этапе скорой неотложной помощи: нет.
Другие виды лечения: нет.
• лабораторные показатели: остро возникшая тромбоцитопения, нарушения в коагулограмме, тяжелая гипонатриемия, стойкий метаболический ацидоз.
• рентгенологические признаки в виде статичной петли кишки, асцит, газ в портальной вене, пневмоперитонеум;
• осмотр педиатра на следующий день, в течение первого месяца 1 раз в неделю, далее до 6 месяцев 1 раз в 2 недели, в 6-12 месяцев - 1 раз в месяц;
• осмотр хирурга в первый месяц 1 раз в неделю, далее до 6 месяцев 1 раз в месяц, в 6-12 месяцев 1 раз в квартал;
Индикаторы эффективности лечения и безопасности методов диагностики и лечения, описанных в протоколе:

Весь контент iLive проверяется медицинскими экспертами, чтобы обеспечить максимально возможную точность и соответствие фактам.
У нас есть строгие правила по выбору источников информации и мы ссылаемся только на авторитетные сайты, академические исследовательские институты и, по возможности, доказанные медицинские исследования. Обратите внимание, что цифры в скобках ([1], [2] и т. д.) являются интерактивными ссылками на такие исследования.
Если вы считаете, что какой-либо из наших материалов является неточным, устаревшим или иным образом сомнительным, выберите его и нажмите Ctrl + Enter.
Кишечная инфекция у детей до года является самым распространенным заболеванием.
Бактерии и вирусы проникают в организм ребенка через грязные руки, предметы, игрушки, которые он тянет в рот.
Существует множество видов бактерий, которые вызывают различные заболевания, но симптомы в большинстве случаев похожи, поэтому для выявления возбудителя требуется проведение лабораторных анализов.
Среди всех кишечных инфекций, маленькие дети чаще всего болеют ротавирусной инфекцией (кишечный грипп), сальмонеллезом, энтеровирусом, дизентерией.

[1], [2], [3], [4], [5], [6], [7]
Код по МКБ-10
Причины кишечной инфекции у новорожденного
Заражение кишечной инфекцией происходит всегда орально-фекальным путем, т.е. бактерии из кишечника с испражнениями попадают на руки, затем на различные предметы. Как известно, дети с первых месяцев жизни пытаются затянуть в рот любой предмет, попавший им в руки, это является частью саморазвития, но в то же время, грозит тяжелыми последствиями.
В организм новорожденных бактерии проникают обычно из-за несоблюдения родителями простых гигиенических требований по уходу за ребенком, например, инфекция может возникнуть из-за плохо вымытой бутылочки, упавшей соски (особенно на улице), немытые руки и пр.
Кроме этого, заражение может произойти через организм матери, которая может быть носителем опасных бактерий или заразиться инфекцией во время беременности. Заражение ребенка может произойти еще в утробе матери (при заглатывании околоплодных вод, через общий кровоток с матерью) либо в момент рождения, при прохождении через родовые пути.

[8], [9]
Симптомы кишечной инфекции у новорожденного
Даже после нормальных родов состояние ребенка через несколько недель может сильно ухудшиться. Вялость, частые срыгивания, плохой аппетит, незначительная прибавка в весе являются первыми симптомами нарушений в детском организме.
Практически каждая кишечная инфекция проявляется болями в животе, высокой температурой, поносом (цвет часто зависит от заболевания), рвотой.
Все эти симптомы могут появляться сразу, либо по отдельности.
Стоит отметить, что рвота не всегда появляется при кишечной инфекции, в то время как диарея считается основным симптомом заражения.
При любой кишечной инфекции происходит обезвоживание организма, которое можно определить по сухости во рту, слабому аппетиту, снижению веса, уменьшению объема мочи при мочеиспускании. Для детей данное состояние является наиболее опасным и требует незамедлительного лечения.
В тяжелых случаях при обезвоживании родничок начинает западать, ребенок становится сонливым, ослабленным, на глазах и коже появляются признаки сухости.
Самой распространенной инфекцией у маленьких детей является ротавирусная, при которой помимо общих симптомов появляется покраснение неба, боль в горле.
Диагностика кишечной инфекции у новорожденного
Кишечная инфекция у новорожденных часто становится причиной смерти, поэтому при первых признаках заболевания (слабость, понос, температура) необходимо обратиться к врачу.
Для установления диагноза специалист проводит осмотр, фиксирует жалобы и при необходимости назначает дополнительные исследования.
Для выявления возбудителя необходим анализ каловых масс, который также установит чувствительность патогенной микрофлоры к той или иной группе антибиотиков, что важно при выборе лечения.

[10], [11]
К кому обратиться?
Лечение кишечной инфекции у новорожденного
Стоит отметить, что дети, которые находятся на грудном вскармливании кишечные инфекции переносят намного легче, чем дети, которых уже отлучили от груди либо искусственники. Материнское молоко способствует укреплению иммунитета малыша и повышает сопротивляемость организма.
При кишечной инфекции лечение в первую очередь направлено на уничтожение болезнетворных микроорганизмов, снижение интоксикации и обезвоживания, восстановление нормального баланса бактерий в кишечнике.
При появлении первых признаков заболевания следует прекратить кормление на 12-18 часов (в этот период ребенку можно давать только чистую кипяченую воду или чай).
Также в этот период нужно давать ребенку сорбенты для выведения токсинов и препараты для восстановления водно-электролитного баланса.
При рвоте врач может назначить промывание желудка, если даже после такой процедуры ребенок не перестает рвать, назначается искусственное введение питательных веществ через капельницу. В тяжелых случаях (например, при стафилококковой инфекции) могут быть использованы антибактериальные препараты широкого спектра действия.
В обязательном порядке назначаются средства, восстанавливающие микрофлору кишечника.
Грудничкам обычно назначается Смекта, Энтеросгель, который не только поглощает токсины, но и снижает интоксикацию организма, Регидрон для восстановления водно-электролитного баланса.
Для восстановления кишечной микрофлоры могут использоваться Бифидум, Трилакт, Аципол и пр.
Читайте также:

